Другие названия и синонимы
Levocetirizine.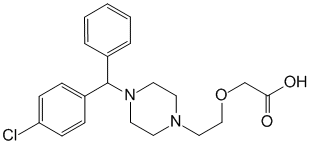
Фармакологическая группа
|
|
Латинское название
Levocetirizinum ( Levocetirizini).
Химическое название
2-(2-(4-[(R)-(4-Хлорфенил)(фенил)метил]пиперазин-1-ил)этокси)уксусная кислота.
Используется в лечении
Код CAS
130018-77-8.
Фармакологическое действие
H1-антигистаминное, противоаллергическое.
Характеристика вещества
Пероральный антагонист H1-рецепторов. Левоцетиризина дигидрохлорид - R-энантиомер цетиризина гидрохлорида, рацемического соединения с антигистаминными свойствами. Белый кристаллический порошок, растворим в воде. Молекулярная масса 461,82.
Фармакодинамика
Механизм действия.
Левоцетиризин - активный энантиомер цетиризина, является антигистаминным ЛС, его основные эффекты опосредованы селективным ингибированием H1-рецепторов. Антигистаминная активность левоцетиризина была документально подтверждена на различных моделях животных и у человека. Исследования связывания in vitro >in vitro показали, что сродство левоцетиризина к H1-рецепторам человека в 2 раза выше, чем у цетиризина (Ki=3 нмоль/л vs 6 нмоль/л соответственно). Клиническая значимость этих данных неизвестна.
Фармакодинамика.
Исследования у взрослых здоровых людей показали, что левоцетиризин в дозах 2,5 и 5 мг подавлял вызванные в/к инъекцией гистамина волдыри и гиперемию кожи. Напротив, декстроцетиризин не показал явных изменений в подавлении реакции в виде волдырей и гиперемии. Левоцетиризин в дозе 5 мг подавлял вызванные в/к инъекцией гистамина волдыри и гиперемию кожи у 14 педиатрических пациентов (от 6 до 11 лет), и активность сохранялась не менее 24 Клиническая значимость гистаминового теста на кожные волдыри неизвестна.
Исследование интервала QT/QTc с использованием однократной дозы 30 мг левоцетиризина не продемонстрировало влияния на интервал QTc. Хотя однократная доза левоцетиризина не оказала влияния, эффекты левоцетиризина могут не достигать равновесного состояния после однократной дозы. Влияние левоцетиризина на интервал QTc после приема многократных доз неизвестно. Не ожидается, что левоцетиризин будет иметь влияние на интервал QT/QTc, поскольку в результатах исследований QTc с цетиризином и при длительном постмаркетинговом применении цетиризина не было сообщений об удлинении интервала QT.
Левоцетиризин - активный энантиомер цетиризина, является антигистаминным ЛС, его основные эффекты опосредованы селективным ингибированием H1-рецепторов. Антигистаминная активность левоцетиризина была документально подтверждена на различных моделях животных и у человека. Исследования связывания in vitro >in vitro показали, что сродство левоцетиризина к H1-рецепторам человека в 2 раза выше, чем у цетиризина (Ki=3 нмоль/л vs 6 нмоль/л соответственно). Клиническая значимость этих данных неизвестна.
Фармакодинамика.
Исследования у взрослых здоровых людей показали, что левоцетиризин в дозах 2,5 и 5 мг подавлял вызванные в/к инъекцией гистамина волдыри и гиперемию кожи. Напротив, декстроцетиризин не показал явных изменений в подавлении реакции в виде волдырей и гиперемии. Левоцетиризин в дозе 5 мг подавлял вызванные в/к инъекцией гистамина волдыри и гиперемию кожи у 14 педиатрических пациентов (от 6 до 11 лет), и активность сохранялась не менее 24 Клиническая значимость гистаминового теста на кожные волдыри неизвестна.
Исследование интервала QT/QTc с использованием однократной дозы 30 мг левоцетиризина не продемонстрировало влияния на интервал QTc. Хотя однократная доза левоцетиризина не оказала влияния, эффекты левоцетиризина могут не достигать равновесного состояния после однократной дозы. Влияние левоцетиризина на интервал QTc после приема многократных доз неизвестно. Не ожидается, что левоцетиризин будет иметь влияние на интервал QT/QTc, поскольку в результатах исследований QTc с цетиризином и при длительном постмаркетинговом применении цетиризина не было сообщений об удлинении интервала QT.
Фармакокинетика
Левоцетиризин имеет линейную фармакокинетику в диапазоне терапевтических доз у здоровых взрослых.
Абсорбция. Левоцетиризин быстро и экстенсивно всасывается после приема внутрь. У взрослых Сmax в плазме достигается через 0,9 ч после перорального приема в виде таблеток. Коэффициент кумуляции при ежедневном пероральном приеме составляет 1,12 с достижением равновесного состояния через 2 дня. Сmax обычно составляют 270 и 308 нг/мл соответственно после однократного и повторных приемов в дозе 5 мг 1 раз в сутки. Прием пищи не влияет на степень экспозиции (AUC) левоцетиризина в виде таблеток, но замедляет maxTmax примерно на 1,25 а maxCmax снижается примерно на 36% после приема с пищей с высоким содержанием жиров, поэтому левоцетиризин можно принимать с пищей или без нее.
Доза 5 мг (10 мл) перорального раствора левоцетиризина биоэквивалентна дозе 5 мг таблетки левоцетиризина. После перорального приема левоцетиризина в дозе 5 мг в виде перорального раствора здоровыми взрослыми людьми средние maxCmax в плазме достигались примерно через 0,5 ч после приема.
Распределение. Среднее связывание левоцетиризина с белками плазмы in vitro >in vitro колеблется от 91 до 92%, независимо от концентрации в диапазоне 90-5000 нг/мл, что включает наблюдаемые терапевтические уровни в плазме. После перорального приема средний кажущийся dVd составляет приблизительно 0,4 л/кг, что отображает распределение в общей жидкости организма.
Метаболизм. Степень метаболизма левоцетиризина у человека составляет менее 14% от дозы, и поэтому ожидается, что различия, возникающие в результате генетического полиморфизма или одновременного применения ингибиторов ферментов, метаболизирующих ЛС в печени, будут незначительными. Метаболические пути включают ароматическое окисление, N- и O-деалкилирование и конъюгацию таурина. Пути деалкилирования в основном опосредуются изоферментом сYP3A4, в то время как ароматическое окисление включает множественные и/или неидентифицированные изоформы сYP.
Выведение. 1/2T1/2 из плазмы у здоровых взрослых составлял от 8 до 9 ч после перорального приема в виде таблеток и в виде раствора, а средний пероральный общий клиренс левоцетиризина составлял приблизительно 0,63 мл/кг/мин. Основной путь выведения левоцетиризина и его метаболитов - с мочой, что составляет в среднем 85,4% дозы. Выведение с фекалиями составляет всего 12,9% дозы. Левоцетиризин выводится как за счет КФ, так и за счет активной канальцевой секреции. Почечный клиренс левоцетиризина коррелирует с клиренсом креатинина. У пациентов с почечной недостаточностью клиренс левоцетиризина уменьшается.
Особые группы пациентов.
Педиатрические пациенты. Данные педиатрического фармакокинетического исследования при пероральном приеме однократной дозы 5 мг левоцетиризина у 14 детей от 6 до 11 лет с массой тела от 20 до 40 кг показали, что значения maxCmax и AUC примерно в 2 раза больше, чем у здоровых взрослых людей при сравнении в перекрестном исследовании. Среднее значение maxCmax составляло 450 нг/мл, Тmax в среднем - 1,2 общий клиренс с учетом массы тела был на 30% выше, а 1/2T1/2 на 24% короче у этой педиатрической популяции, чем соответствующие показатели у взрослых.
Специальные фармакокинетические исследования у детей младше 6 лет не проводились. Ретроспективный популяционный фармакокинетический анализ был проведен у 323 пациентов (181 ребенок от 1 до 5 лет, 18 детей от 6 до 11 лет и 124 взрослых от 18 до 55 лет), получавших однократную или многократную дозу левоцетиризина в диапазоне от 1,25 до 30 мг. Данные, полученные в результате этого анализа, показали, что прием в дозе 1,25 мг 1 раз в день у детей от 6 мес до 5 лет приводит к концентрациям в плазме, соответствующим таковым у взрослых при приеме 5 мг 1 раз в день.
Гериатрические пациенты. Данные по фармакокинетике у пожилых пациентов ограничены. При повторном пероральном приеме 30 мг левоцетиризина 1 раз в день в течение 6 дней у 9 пожилых пациентов (65-74 года) общий клиренс был примерно на 33% ниже, чем таковой у более молодых взрослых. Было показано, что распределение рацемата цетиризина больше зависит от функции почек, а не от возраста. Это утверждение также может быть применимо к левоцетиризину, поскольку левоцетиризин и цетиризин выводятся преимущественно с мочой. Поэтому у пожилых пациентов доза левоцетиризина должна быть скорректирована в зависимости от функции почек.
Пол. Фармакокинетические результаты для 77 пациентов (40 мужчин, 37 женщин) были оценены на предмет потенциального влияния пола на фармакокинетику левоцетиризина. 1/2T1/2 был немного короче у женщин (7,08±1,72) чем у мужчин (8,62±1,84) однако пероральный клиренс с поправкой на массу тела у женщин (0,67±0,16) мл/мин/кг является сопоставимым с таковым у мужчин (0,59±0,12) мл/мин/кг. Одинаковые суточные дозы и интервалы дозирования применимы для мужчин и женщин с нормальной функцией почек.
Раса. Влияние расы на левоцетиризин не изучалось. Поскольку левоцетиризин в основном выводится почками и нет серьезных расовых различий в клиренсе креатинина, не ожидается, что фармакокинетические характеристики левоцетиризина будут различаться у разных рас. Каких-либо расовых различий в фармакокинетике рацемата цетиризина не наблюдалось.
Нарушение функции почек. Экспозиция левоцетиризина (AUC) показала увеличение в 1,8; 3,2; 4,3 и 5,7 раза у пациентов с нарушением функции почек легкой, средней, тяжелой степени и терминальной стадией почечной недостаточности соответственно по сравнению со здоровыми людьми. Соответствующее увеличение оценочного периода полураспада - в 1,4; 2; 2,9 и 4 раза соответственно.
Общий клиренс левоцетиризина после перорального приема коррелировал с клиренсом креатинина и постепенно снижался в зависимости от тяжести почечной недостаточности. Поэтому рекомендуется корректировать дозу и интервалы дозирования левоцетиризина в зависимости от клиренса креатинина у пациентов с нарушением функции почек легкой, средней или тяжелой степени. Пациентам с терминальной стадией почечной недостаточности (Cl креатинина <10 мл/мин) левоцетиризин противопоказан. Менее 10% левоцетиризина удаляется в ходе стандартной 4-часовой процедуры гемодиализа.
Дозу левоцетиризина следует уменьшать у пациентов с нарушением функции почек легкой степени. И доза, и частота приема должны быть уменьшены у пациентов с нарушением функции почек умеренной или тяжелой степени.
Нарушение функции печени. Левоцетиризин не изучали у пациентов с нарушением функции печени. Было обнаружено, что внепочечный клиренс (показывающий степень участия печени) составляет около 28% от общего клиренса у здоровых взрослых людей после перорального приема.
Поскольку левоцетиризин в основном выводится в неизмененном виде почками, маловероятно, что клиренс левоцетиризина значительно снижается у пациентов с нарушением функции только печени.
Доклиническая токсикология.
Канцерогенность, мутагенность, влияние на фертильность.
Исследования канцерогенности левоцетиризина не проводили. Однако оценка исследований канцерогенности цетиризина важна для определения канцерогенного потенциала левоцетиризина. В двухгодичном исследовании канцерогенности у крыс цетиризин не проявлял канцерогенного действия при применении с пищей в дозах до 20 мг/кг (примерно 40, 40, 25 и 10 МРДЧ у взрослых, детей от 6 до 11 лет, детей 2-5 лет и детей от 6 мес до 2 лет соответственно из расчета в мг/м2). В двухгодичном исследовании канцерогенности у мышей цетиризин вызывал повышение частоты возникновения доброкачественных опухолей печени у самцов при дозе 16 мг/кг (примерно 15, 15, 9 и 5 МРДЧ у взрослых, детей от 6 до 11 лет, детей 2-5 лет и детей от 6 мес до 2 лет соответственно из расчета в мг/м2). Не наблюдалось увеличения частоты возникновения доброкачественных опухолей при дозе 4 мг/кг (примерно 4, 4, 2 и 1 МРДЧ у взрослых, детей от 6 до 11 лет, детей 2-5 лет и детей от 6 мес до 2 лет соответственно из расчета в мг/м2). Клиническая значимость этих результатов при длительном применении левоцетиризина неизвестна.
Левоцетиризин не проявлял мутагенности в тесте Эймса и кластогенности в тесте на лимфоцитах человека, тесте на лимфоме у мышей и in vivo >in vivo в микроядерном тесте у мышей.
Цетиризин не влиял на фертильность и репродуктивную способность у самцов и самок мышей и крыс, которые получали цетиризин в пероральных дозах до 64 и 200 мг/кг/сут соответственно (примерно в 60 и 390 раз больше МРДЧ у взрослых из расчета в мг/м2).
Клинические исследования.
Круглогодичный аллергический ринит.
Взрослые и подростки от 12 лет и старше.
Эффективность левоцетиризина оценивали в четырех рандомизированных плацебо-контролируемых двойных слепых клинических испытаниях у взрослых и подростков 12 лет и старше с симптомами круглогодичного аллергического ринита. Четыре клинических испытания включают два испытания с диапазоном доз продолжительностью 4 нед и два испытания эффективности (одно 6-недельное и одно 6-месячное) у пациентов с круглогодичным аллергическим ринитом.
Эти испытания включали в общей сложности 1729 пациентов (752 мужского пола и 977 женского пола), из которых 227 были подростками от 12 до 17 лет. Эффективность оценивали с использованием общей шкалы симптомов из записи пациентом 4 симптомов (чихание, ринорея, зуд в носу и зуд в глазах) в трех исследованиях и 5 симптомов (чихание, ринорея, зуд в носу, зуд в глазах и заложенность носа) в одном исследовании. Пациенты регистрировали симптомы с использованием категориальной шкалы степени тяжести 0-3 (0 = отсутствие симптомов, 1 = легкая, 2 = умеренная, 3 = тяжелая) 1 раз в сутки вечером, что отражало 24-часовой период лечения. Первичной конечной точкой было значение общего балла симптомов по шкале, усредненного за первую неделю и за 4 недели в испытаниях круглогодичного аллергического ринита.
Два испытания с диапазоном доз были проведены для оценки эффективности левоцетиризина в дозах 2,5; 5 и 10 мг 1 раз в сутки вечером. Эти испытания длились 4 нед и включали пациентов с круглогодичным аллергическим ринитом. В этих испытаниях каждая из трех доз левоцетиризина продемонстрировала большее снижение ретроспективной общей оценки симптомов, чем плацебо, и разница была статистически значимой для всех трех доз в двух исследованиях. Результаты одного из этих испытаний показаны в таблице 1.
Таблица 1.
Среднее значение ретроспективной общей оценки симптомов1 в испытаниях аллергического ринита с диапазоном доз.
1 Общая оценка симптомов представляет собой сумму отдельных симптомов (чихание, ринорея, зуд в носу и зуд в глазах), оцененных пациентами по шкале тяжести от 0 до 3.
В одном клиническом исследовании оценивали эффективность левоцетиризина в дозе 5 мг 1 раз в день вечером по сравнению с плацебо у пациентов с круглогодичным аллергическим ринитом в течение 6-недельного периода лечения. В другом испытании в течение 6-месячного периода лечения, оценивалась эффективность через 4 нед. Левоцетиризин в дозе 5 мг продемонстрировал большее снижение по сравнению с исходным уровнем ретроспективной общей оценки симптомов, чем плацебо, и разница с плацебо была статистически значимой. Результаты показаны в таблице 2.
Таблица 2.
Среднее значение ретроспективной общей оценки симптомов1 в испытаниях аллергического ринита.
1 Общая оценка симптомов представляет собой сумму отдельных симптомов (чихание, ринорея, зуд в носу и зуд в глазах), оцененных пациентами по шкале тяжести от 0 до 3.
Начало действия оценивали в двух исследованиях при воздействии окружающей среды у пациентов с аллергическим ринитом при однократной дозе левоцетиризина 2,5 или 5 мг. Было обнаружено, что действие левоцетиризина в дозе 5 мг наступает через 1 ч после перорального приема. Начало действия также оценивалось по ежедневной записи симптомов вечером перед приемом левоцетиризина в исследованиях аллергического ринита. В этих испытаниях начало эффекта отмечалось через 1 день после приема левоцетиризина.
Педиатрические пациенты до 12 лет.
Нет каких-либо клинических испытаний эффективности левоцетиризина в дозе 2,5 мг 1 раз в день у педиатрических пациентов до 12 лет, а также клинических испытаний эффективности левоцетиризина в дозе 1,25 мг 1 раз в день у педиатрических пациентов от 6 мес до 5 лет. Клиническая эффективность левоцетиризина у педиатрических пациентов до 12 лет была экстраполирована из исследований клинической эффективности у взрослых на основе фармакокинетических сравнений ( см «Меры предосторожности»).
Хроническая идиопатическая крапивница.
Взрослые пациенты 18 лет и старше.
Эффективность левоцетиризина для лечения неосложненных кожных проявлений хронической идиопатической крапивницы была оценена в двух многоцентровых рандомизированных плацебо-контролируемых двойных слепых клинических испытаниях продолжительностью 4 нед у взрослых пациентов от 18 до 85 лет с хронической идиопатической крапивницей. Эти два испытания включали одно 4-недельное испытание с диапазоном доз и одно 4-недельное испытание эффективности однократной дозы. В эти испытания были включены 423 пациента (139 мужчин и 284 женщины). Большинство пациентов (>90%) принадлежали к европеоидной расе, средний возраст составлял 41 год. 146 из этих пациентов получали левоцетиризин в дозе 5 мг 1 раз в день вечером. Эффективность оценивали на основании записи пациентом тяжести зуда по шкале тяжести от 0 до 3 (0 = нет, 3 = тяжелая). Первичной конечной точкой эффективности было значение выраженности зуда по шкале тяжести в течение первой недели и всего периода лечения. Дополнительными переменными эффективности были немедленная оценка тяжести зуда, количество и размер волдырей и продолжительность зуда.
Испытание с диапазоном доз было проведено для оценки эффективности левоцетиризина в дозах 2,5; 5 и 10 мг 1 раз в день вечером. В этом испытании каждая из трех доз левоцетиризина продемонстрировала большее снижение ретроспективной оценки степени тяжести зуда по шкале, чем плацебо, и разница была статистически значимой для всех трех доз ( см таблицу 3).
В испытании уровня однократной дозы оценивали эффективность левоцетиризина в дозе 5 мг 1 раз в день вечером по сравнению с плацебо у пациентов с хронической идиопатической крапивницей в течение 4-недельного периода лечения.
Левоцетиризин в дозе 5 мг продемонстрировал большее снижение по сравнению с исходным уровнем ретроспективной оценки степени тяжести зуда по шкале, чем плацебо, и разница с плацебо была статистически значимой.
Продолжительность зуда, количество и размер волдырей и немедленная оценка тяжести зуда также показали значительное улучшение по сравнению с плацебо. Значительное улучшение немедленной оценки степени тяжести зуда по сравнению с плацебо подтвердило эффективность в конце интервала дозирования ( см таблицу 3).
Таблица 3.
Среднее значение ретроспективной оценки степени тяжести зуда по шкале в испытаниях хронической идиопатической крапивницы.
Педиатрические пациенты.
Клинических испытаний эффективности у педиатрических больных с хронической идиопатической крапивницей ( см «Меры предосторожности») не проводилось.
Абсорбция. Левоцетиризин быстро и экстенсивно всасывается после приема внутрь. У взрослых Сmax в плазме достигается через 0,9 ч после перорального приема в виде таблеток. Коэффициент кумуляции при ежедневном пероральном приеме составляет 1,12 с достижением равновесного состояния через 2 дня. Сmax обычно составляют 270 и 308 нг/мл соответственно после однократного и повторных приемов в дозе 5 мг 1 раз в сутки. Прием пищи не влияет на степень экспозиции (AUC) левоцетиризина в виде таблеток, но замедляет maxTmax примерно на 1,25 а maxCmax снижается примерно на 36% после приема с пищей с высоким содержанием жиров, поэтому левоцетиризин можно принимать с пищей или без нее.
Доза 5 мг (10 мл) перорального раствора левоцетиризина биоэквивалентна дозе 5 мг таблетки левоцетиризина. После перорального приема левоцетиризина в дозе 5 мг в виде перорального раствора здоровыми взрослыми людьми средние maxCmax в плазме достигались примерно через 0,5 ч после приема.
Распределение. Среднее связывание левоцетиризина с белками плазмы in vitro >in vitro колеблется от 91 до 92%, независимо от концентрации в диапазоне 90-5000 нг/мл, что включает наблюдаемые терапевтические уровни в плазме. После перорального приема средний кажущийся dVd составляет приблизительно 0,4 л/кг, что отображает распределение в общей жидкости организма.
Метаболизм. Степень метаболизма левоцетиризина у человека составляет менее 14% от дозы, и поэтому ожидается, что различия, возникающие в результате генетического полиморфизма или одновременного применения ингибиторов ферментов, метаболизирующих ЛС в печени, будут незначительными. Метаболические пути включают ароматическое окисление, N- и O-деалкилирование и конъюгацию таурина. Пути деалкилирования в основном опосредуются изоферментом сYP3A4, в то время как ароматическое окисление включает множественные и/или неидентифицированные изоформы сYP.
Выведение. 1/2T1/2 из плазмы у здоровых взрослых составлял от 8 до 9 ч после перорального приема в виде таблеток и в виде раствора, а средний пероральный общий клиренс левоцетиризина составлял приблизительно 0,63 мл/кг/мин. Основной путь выведения левоцетиризина и его метаболитов - с мочой, что составляет в среднем 85,4% дозы. Выведение с фекалиями составляет всего 12,9% дозы. Левоцетиризин выводится как за счет КФ, так и за счет активной канальцевой секреции. Почечный клиренс левоцетиризина коррелирует с клиренсом креатинина. У пациентов с почечной недостаточностью клиренс левоцетиризина уменьшается.
Особые группы пациентов.
Педиатрические пациенты. Данные педиатрического фармакокинетического исследования при пероральном приеме однократной дозы 5 мг левоцетиризина у 14 детей от 6 до 11 лет с массой тела от 20 до 40 кг показали, что значения maxCmax и AUC примерно в 2 раза больше, чем у здоровых взрослых людей при сравнении в перекрестном исследовании. Среднее значение maxCmax составляло 450 нг/мл, Тmax в среднем - 1,2 общий клиренс с учетом массы тела был на 30% выше, а 1/2T1/2 на 24% короче у этой педиатрической популяции, чем соответствующие показатели у взрослых.
Специальные фармакокинетические исследования у детей младше 6 лет не проводились. Ретроспективный популяционный фармакокинетический анализ был проведен у 323 пациентов (181 ребенок от 1 до 5 лет, 18 детей от 6 до 11 лет и 124 взрослых от 18 до 55 лет), получавших однократную или многократную дозу левоцетиризина в диапазоне от 1,25 до 30 мг. Данные, полученные в результате этого анализа, показали, что прием в дозе 1,25 мг 1 раз в день у детей от 6 мес до 5 лет приводит к концентрациям в плазме, соответствующим таковым у взрослых при приеме 5 мг 1 раз в день.
Гериатрические пациенты. Данные по фармакокинетике у пожилых пациентов ограничены. При повторном пероральном приеме 30 мг левоцетиризина 1 раз в день в течение 6 дней у 9 пожилых пациентов (65-74 года) общий клиренс был примерно на 33% ниже, чем таковой у более молодых взрослых. Было показано, что распределение рацемата цетиризина больше зависит от функции почек, а не от возраста. Это утверждение также может быть применимо к левоцетиризину, поскольку левоцетиризин и цетиризин выводятся преимущественно с мочой. Поэтому у пожилых пациентов доза левоцетиризина должна быть скорректирована в зависимости от функции почек.
Пол. Фармакокинетические результаты для 77 пациентов (40 мужчин, 37 женщин) были оценены на предмет потенциального влияния пола на фармакокинетику левоцетиризина. 1/2T1/2 был немного короче у женщин (7,08±1,72) чем у мужчин (8,62±1,84) однако пероральный клиренс с поправкой на массу тела у женщин (0,67±0,16) мл/мин/кг является сопоставимым с таковым у мужчин (0,59±0,12) мл/мин/кг. Одинаковые суточные дозы и интервалы дозирования применимы для мужчин и женщин с нормальной функцией почек.
Раса. Влияние расы на левоцетиризин не изучалось. Поскольку левоцетиризин в основном выводится почками и нет серьезных расовых различий в клиренсе креатинина, не ожидается, что фармакокинетические характеристики левоцетиризина будут различаться у разных рас. Каких-либо расовых различий в фармакокинетике рацемата цетиризина не наблюдалось.
Нарушение функции почек. Экспозиция левоцетиризина (AUC) показала увеличение в 1,8; 3,2; 4,3 и 5,7 раза у пациентов с нарушением функции почек легкой, средней, тяжелой степени и терминальной стадией почечной недостаточности соответственно по сравнению со здоровыми людьми. Соответствующее увеличение оценочного периода полураспада - в 1,4; 2; 2,9 и 4 раза соответственно.
Общий клиренс левоцетиризина после перорального приема коррелировал с клиренсом креатинина и постепенно снижался в зависимости от тяжести почечной недостаточности. Поэтому рекомендуется корректировать дозу и интервалы дозирования левоцетиризина в зависимости от клиренса креатинина у пациентов с нарушением функции почек легкой, средней или тяжелой степени. Пациентам с терминальной стадией почечной недостаточности (Cl креатинина <10 мл/мин) левоцетиризин противопоказан. Менее 10% левоцетиризина удаляется в ходе стандартной 4-часовой процедуры гемодиализа.
Дозу левоцетиризина следует уменьшать у пациентов с нарушением функции почек легкой степени. И доза, и частота приема должны быть уменьшены у пациентов с нарушением функции почек умеренной или тяжелой степени.
Нарушение функции печени. Левоцетиризин не изучали у пациентов с нарушением функции печени. Было обнаружено, что внепочечный клиренс (показывающий степень участия печени) составляет около 28% от общего клиренса у здоровых взрослых людей после перорального приема.
Поскольку левоцетиризин в основном выводится в неизмененном виде почками, маловероятно, что клиренс левоцетиризина значительно снижается у пациентов с нарушением функции только печени.
Доклиническая токсикология.
Канцерогенность, мутагенность, влияние на фертильность.
Исследования канцерогенности левоцетиризина не проводили. Однако оценка исследований канцерогенности цетиризина важна для определения канцерогенного потенциала левоцетиризина. В двухгодичном исследовании канцерогенности у крыс цетиризин не проявлял канцерогенного действия при применении с пищей в дозах до 20 мг/кг (примерно 40, 40, 25 и 10 МРДЧ у взрослых, детей от 6 до 11 лет, детей 2-5 лет и детей от 6 мес до 2 лет соответственно из расчета в мг/м2). В двухгодичном исследовании канцерогенности у мышей цетиризин вызывал повышение частоты возникновения доброкачественных опухолей печени у самцов при дозе 16 мг/кг (примерно 15, 15, 9 и 5 МРДЧ у взрослых, детей от 6 до 11 лет, детей 2-5 лет и детей от 6 мес до 2 лет соответственно из расчета в мг/м2). Не наблюдалось увеличения частоты возникновения доброкачественных опухолей при дозе 4 мг/кг (примерно 4, 4, 2 и 1 МРДЧ у взрослых, детей от 6 до 11 лет, детей 2-5 лет и детей от 6 мес до 2 лет соответственно из расчета в мг/м2). Клиническая значимость этих результатов при длительном применении левоцетиризина неизвестна.
Левоцетиризин не проявлял мутагенности в тесте Эймса и кластогенности в тесте на лимфоцитах человека, тесте на лимфоме у мышей и in vivo >in vivo в микроядерном тесте у мышей.
Цетиризин не влиял на фертильность и репродуктивную способность у самцов и самок мышей и крыс, которые получали цетиризин в пероральных дозах до 64 и 200 мг/кг/сут соответственно (примерно в 60 и 390 раз больше МРДЧ у взрослых из расчета в мг/м2).
Клинические исследования.
Круглогодичный аллергический ринит.
Взрослые и подростки от 12 лет и старше.
Эффективность левоцетиризина оценивали в четырех рандомизированных плацебо-контролируемых двойных слепых клинических испытаниях у взрослых и подростков 12 лет и старше с симптомами круглогодичного аллергического ринита. Четыре клинических испытания включают два испытания с диапазоном доз продолжительностью 4 нед и два испытания эффективности (одно 6-недельное и одно 6-месячное) у пациентов с круглогодичным аллергическим ринитом.
Эти испытания включали в общей сложности 1729 пациентов (752 мужского пола и 977 женского пола), из которых 227 были подростками от 12 до 17 лет. Эффективность оценивали с использованием общей шкалы симптомов из записи пациентом 4 симптомов (чихание, ринорея, зуд в носу и зуд в глазах) в трех исследованиях и 5 симптомов (чихание, ринорея, зуд в носу, зуд в глазах и заложенность носа) в одном исследовании. Пациенты регистрировали симптомы с использованием категориальной шкалы степени тяжести 0-3 (0 = отсутствие симптомов, 1 = легкая, 2 = умеренная, 3 = тяжелая) 1 раз в сутки вечером, что отражало 24-часовой период лечения. Первичной конечной точкой было значение общего балла симптомов по шкале, усредненного за первую неделю и за 4 недели в испытаниях круглогодичного аллергического ринита.
Два испытания с диапазоном доз были проведены для оценки эффективности левоцетиризина в дозах 2,5; 5 и 10 мг 1 раз в сутки вечером. Эти испытания длились 4 нед и включали пациентов с круглогодичным аллергическим ринитом. В этих испытаниях каждая из трех доз левоцетиризина продемонстрировала большее снижение ретроспективной общей оценки симптомов, чем плацебо, и разница была статистически значимой для всех трех доз в двух исследованиях. Результаты одного из этих испытаний показаны в таблице 1.
Таблица 1.
Среднее значение ретроспективной общей оценки симптомов1 в испытаниях аллергического ринита с диапазоном доз.
| Лечение | N | Исходный уровень | Среднее значение, скорректированное при лечении | Разница с плацебо | ||
| Оценка | 95% ДИ | р-значение | ||||
| Испытания круглогодичного аллергического ринита - ретроспективная общая оценка симптомов | ||||||
| Левоцетиризин, 2,5 мг | 133 | 7,14 | 4,12 | 1,17 | (0,71; 1,63) | <0,001 |
| Левоцетиризин, 5 мг | 127 | 7,18 | 4,07 | 1,22 | (0,76; 1,69) | <0,001 |
| Левоцетиризин, 10 мг | 129 | 7,58 | 4,19 | 1,1 | (0,64; 1,57) | <0,001 |
| Плацебо | 128 | 7,22 | 5,29 | |||
1 Общая оценка симптомов представляет собой сумму отдельных симптомов (чихание, ринорея, зуд в носу и зуд в глазах), оцененных пациентами по шкале тяжести от 0 до 3.
В одном клиническом исследовании оценивали эффективность левоцетиризина в дозе 5 мг 1 раз в день вечером по сравнению с плацебо у пациентов с круглогодичным аллергическим ринитом в течение 6-недельного периода лечения. В другом испытании в течение 6-месячного периода лечения, оценивалась эффективность через 4 нед. Левоцетиризин в дозе 5 мг продемонстрировал большее снижение по сравнению с исходным уровнем ретроспективной общей оценки симптомов, чем плацебо, и разница с плацебо была статистически значимой. Результаты показаны в таблице 2.
Таблица 2.
Среднее значение ретроспективной общей оценки симптомов1 в испытаниях аллергического ринита.
| Лечение | N | Исходный уровень | Среднее значение, скорректированное при лечении | Разница с плацебо | ||
| Оценка | 95% ДИ | р-значение | ||||
| Испытания круглогодичного аллергического ринита - ретроспективная общая оценка симптомов | ||||||
| Левоцетиризин, 5 мг | 150 | 7,69 | 3,93 | 1,17 | (0,7; 1,64) | <0,001 |
| Плацебо | 142 | 7,44 | 5,1 | |||
1 Общая оценка симптомов представляет собой сумму отдельных симптомов (чихание, ринорея, зуд в носу и зуд в глазах), оцененных пациентами по шкале тяжести от 0 до 3.
Начало действия оценивали в двух исследованиях при воздействии окружающей среды у пациентов с аллергическим ринитом при однократной дозе левоцетиризина 2,5 или 5 мг. Было обнаружено, что действие левоцетиризина в дозе 5 мг наступает через 1 ч после перорального приема. Начало действия также оценивалось по ежедневной записи симптомов вечером перед приемом левоцетиризина в исследованиях аллергического ринита. В этих испытаниях начало эффекта отмечалось через 1 день после приема левоцетиризина.
Педиатрические пациенты до 12 лет.
Нет каких-либо клинических испытаний эффективности левоцетиризина в дозе 2,5 мг 1 раз в день у педиатрических пациентов до 12 лет, а также клинических испытаний эффективности левоцетиризина в дозе 1,25 мг 1 раз в день у педиатрических пациентов от 6 мес до 5 лет. Клиническая эффективность левоцетиризина у педиатрических пациентов до 12 лет была экстраполирована из исследований клинической эффективности у взрослых на основе фармакокинетических сравнений ( см «Меры предосторожности»).
Хроническая идиопатическая крапивница.
Взрослые пациенты 18 лет и старше.
Эффективность левоцетиризина для лечения неосложненных кожных проявлений хронической идиопатической крапивницы была оценена в двух многоцентровых рандомизированных плацебо-контролируемых двойных слепых клинических испытаниях продолжительностью 4 нед у взрослых пациентов от 18 до 85 лет с хронической идиопатической крапивницей. Эти два испытания включали одно 4-недельное испытание с диапазоном доз и одно 4-недельное испытание эффективности однократной дозы. В эти испытания были включены 423 пациента (139 мужчин и 284 женщины). Большинство пациентов (>90%) принадлежали к европеоидной расе, средний возраст составлял 41 год. 146 из этих пациентов получали левоцетиризин в дозе 5 мг 1 раз в день вечером. Эффективность оценивали на основании записи пациентом тяжести зуда по шкале тяжести от 0 до 3 (0 = нет, 3 = тяжелая). Первичной конечной точкой эффективности было значение выраженности зуда по шкале тяжести в течение первой недели и всего периода лечения. Дополнительными переменными эффективности были немедленная оценка тяжести зуда, количество и размер волдырей и продолжительность зуда.
Испытание с диапазоном доз было проведено для оценки эффективности левоцетиризина в дозах 2,5; 5 и 10 мг 1 раз в день вечером. В этом испытании каждая из трех доз левоцетиризина продемонстрировала большее снижение ретроспективной оценки степени тяжести зуда по шкале, чем плацебо, и разница была статистически значимой для всех трех доз ( см таблицу 3).
В испытании уровня однократной дозы оценивали эффективность левоцетиризина в дозе 5 мг 1 раз в день вечером по сравнению с плацебо у пациентов с хронической идиопатической крапивницей в течение 4-недельного периода лечения.
Левоцетиризин в дозе 5 мг продемонстрировал большее снижение по сравнению с исходным уровнем ретроспективной оценки степени тяжести зуда по шкале, чем плацебо, и разница с плацебо была статистически значимой.
Продолжительность зуда, количество и размер волдырей и немедленная оценка тяжести зуда также показали значительное улучшение по сравнению с плацебо. Значительное улучшение немедленной оценки степени тяжести зуда по сравнению с плацебо подтвердило эффективность в конце интервала дозирования ( см таблицу 3).
Таблица 3.
Среднее значение ретроспективной оценки степени тяжести зуда по шкале в испытаниях хронической идиопатической крапивницы.
| Лечение | N | Исходный уровень | Среднее значение, скорректированное при лечении | Разница с плацебо | ||
| Оценка | 95% ДИ | р-значение | ||||
| Испытание с диапазоном доз - ретроспективная оценка степени тяжести зуда по шкале | ||||||
| Левоцетиризин, 2,5 мг | 69 | 2,08 | 1,02 | 0,82 | (0,58; 1,06) | <0,001 |
| Левоцетиризин, 5 мг | 62 | 2,07 | 0,92 | 0,91 | (0,66; 1,16) | <0,001 |
| Левоцетиризин, 10 мг | 55 | 2,04 | 0,73 | 1,11 | (0,85; 1,37) | <0,001 |
| Плацебо | 60 | 2,25 | 1,84 | |||
| Испытание при терапии хронической идиопатической крапивницы - ретроспективная оценка степени тяжести зуда по шкале | ||||||
| Левоцетиризин, 5 мг | 80 | 2,07 | 0,94 | 0,62 | (0,38; 0,86) | <0,001 |
| Плацебо | 82 | 2,06 | 1,56 | |||
Педиатрические пациенты.
Клинических испытаний эффективности у педиатрических больных с хронической идиопатической крапивницей ( см «Меры предосторожности») не проводилось.
|
|
Показания к применению
Круглогодичный аллергический ринит.
Левоцетиризин показан для облегчения симптомов, связанных с круглогодичным аллергическим ринитом, у детей от 6 мес до 2 лет.
Хроническая идиопатическая крапивница.
Левоцетиризин показан для лечения неосложненных кожных проявлений хронической идиопатической крапивницы у взрослых и детей от 6 мес.
Левоцетиризин показан для облегчения симптомов, связанных с круглогодичным аллергическим ринитом, у детей от 6 мес до 2 лет.
Хроническая идиопатическая крапивница.
Левоцетиризин показан для лечения неосложненных кожных проявлений хронической идиопатической крапивницы у взрослых и детей от 6 мес.
Противопоказания
Пациенты с известной гиперчувствительностью к левоцетиризину или цетиризину. Наблюдавшиеся реакции варьируют от крапивницы до анафилаксии ( см «Побочные действия»).
Пациенты с терминальной стадией почечной недостаточности (Cl креатинина<10 мл/мин) и пациенты, находящиеся на гемодиализе.
Дети от 6 мес до 11 лет с нарушением функции почек.
Пациенты с терминальной стадией почечной недостаточности (Cl креатинина<10 мл/мин) и пациенты, находящиеся на гемодиализе.
Дети от 6 мес до 11 лет с нарушением функции почек.
При беременности и кормлении грудью
Беременность.
Резюме рисков. Доступных данных в опубликованной литературе и постмаркетингового опыта применения левоцетиризина у беременных женщин недостаточно для выявления каких-либо лекарственноассоциированных рисков развития выкидыша, врожденных дефектов или неблагоприятных исходов для матери или плода. В исследованиях репродукции у животных не было получено доказательств вреда для плода при пероральном применении левоцетиризина у беременных крыс и крольчих в период органогенеза в дозах, превышающих МРДЧ для взрослых до 390 и 470 раз соответственно. У крыс при применении на поздних сроках беременности и в период лактации цетиризин не влиял на развитие детенышей при пероральных дозах, примерно в 60 раз превышающих МРДЧ для взрослых. У мышей при применении на поздних сроках беременности и в период лактации цетиризин при пероральном использовании не оказывал влияния на развитие детенышей в дозе, которая примерно в 25 раз превышала МРДЧ для взрослых; однако более низкая прибавка массы тела детенышей во время лактации наблюдалась при дозе, которая в 95 раз превышала МРДЧ для взрослых ( см Данные у животных).
Предполагаемый фоновый риск развития серьезных врожденных дефектов и выкидыша для указанной популяции неизвестен. При любой беременности существует фоновый риск развития врожденного порока, потери или других неблагоприятных исходов. В общей популяции в США оцениваемые фоновые риски развития серьезных врожденных пороков развития и выкидыша при клинически установленной беременности составляют от 2 до 4% и от 15 до 20% соответственно.
Данные у животных. В исследованиях эмбриофетального развития беременные крысы получали ежедневные дозы левоцетиризина до 200 мг/кг/сут с 6-го по 15-й дни беременности, а беременные крольчихи - до 120 мг/кг/сут с 6-го по 18-й дни беременности. Левоцетиризин не проявлял признаков неблагоприятного влияния на плод у крыс и крольчих при дозах, в 390 и 470 раз соответственно превышающих МРДЧ (из расчета в мг/м2 при пероральных дозах для самок 200 и 120 мг/кг/сут у крыс и крольчих соответственно).
Исследования пренатального и постнатального развития у животных с левоцетиризином не проводили. В исследовании пренатального и постнатального развития, проведенном у мышей, цетиризин применяли перорально в дозах до 96 мг/кг/сут с 15-го дня беременности до 21-го дня лактации. Цетиризин снижал прирост массы тела детенышей во время лактации при пероральной дозе у самок, которая была примерно в 95 раз выше МРДЧ (из расчета в мг/м2 при пероральной дозе для самок 96 мг/кг/сут), однако не влиял на прибавку массы тела детенышей при пероральной дозе у самок, которая примерно в 25 раз превышала МРДЧ (из расчета в мг/м2 при пероральной дозе для самок 24 мг/кг/сут). В исследовании пренатального и постнатального развития, проведенном у крыс, цетиризин применяли перорально в дозах до 180 мг/кг/сут с 17-го дня беременности до 22-го дня лактации. Цетиризин не оказывал каких-либо побочных эффектов на самок крыс или на развитие потомства в дозах, примерно до 60 раз превышающих МРДЧ (из расчета в мг/м2 при пероральной дозе для самок 30 мг/кг/сут). Цетиризин вызывал чрезмерную токсичность для самок при пероральной дозе, которая примерно в 350 раз превышала МРДЧ (из расчета в мг/м2 при пероральной дозе для самок 180 мг/кг/сут).
Грудное вскармливание.
Резюме рисков. Нет данных о присутствии левоцетиризина в материнском молоке, о влиянии на грудного ребенка или о влиянии на выработку молока. Однако сообщалось, что цетиризин присутствует в грудном молоке женщин. Исследования показали, что цетиризин экскретируется в молоко у мышей и собак породы бигль ( см Данные у животных). Если ЛС присутствует в молоке животных, скорее всего, оно будет присутствовать в материнском молоке. Преимущества грудного вскармливания для развития и здоровья следует учитывать наряду с клинической потребностью матери в левоцетиризине и любыми потенциальными неблагоприятными последствиями для ребенка, находящегося на грудном вскармливании, вследствие применения левоцетиризина или под влиянием основного состояния матери.
Данные у животных. Цетиризин был обнаружен в молоке мышей. При пероральном применении у самок в период лактации цетиризина в дозе, которая примерно в 25 раз превышала МРДЧ для взрослых, не наблюдалось неблагоприятных эффектов развития у детенышей ( см Беременность). Исследования у собак породы бигль показали, что примерно 3% дозы цетиризина экскретируется в молоко. Концентрация ЛС в молоке животных не обязательно прогнозирует концентрацию ЛС в материнском молоке.
Резюме рисков. Доступных данных в опубликованной литературе и постмаркетингового опыта применения левоцетиризина у беременных женщин недостаточно для выявления каких-либо лекарственноассоциированных рисков развития выкидыша, врожденных дефектов или неблагоприятных исходов для матери или плода. В исследованиях репродукции у животных не было получено доказательств вреда для плода при пероральном применении левоцетиризина у беременных крыс и крольчих в период органогенеза в дозах, превышающих МРДЧ для взрослых до 390 и 470 раз соответственно. У крыс при применении на поздних сроках беременности и в период лактации цетиризин не влиял на развитие детенышей при пероральных дозах, примерно в 60 раз превышающих МРДЧ для взрослых. У мышей при применении на поздних сроках беременности и в период лактации цетиризин при пероральном использовании не оказывал влияния на развитие детенышей в дозе, которая примерно в 25 раз превышала МРДЧ для взрослых; однако более низкая прибавка массы тела детенышей во время лактации наблюдалась при дозе, которая в 95 раз превышала МРДЧ для взрослых ( см Данные у животных).
Предполагаемый фоновый риск развития серьезных врожденных дефектов и выкидыша для указанной популяции неизвестен. При любой беременности существует фоновый риск развития врожденного порока, потери или других неблагоприятных исходов. В общей популяции в США оцениваемые фоновые риски развития серьезных врожденных пороков развития и выкидыша при клинически установленной беременности составляют от 2 до 4% и от 15 до 20% соответственно.
Данные у животных. В исследованиях эмбриофетального развития беременные крысы получали ежедневные дозы левоцетиризина до 200 мг/кг/сут с 6-го по 15-й дни беременности, а беременные крольчихи - до 120 мг/кг/сут с 6-го по 18-й дни беременности. Левоцетиризин не проявлял признаков неблагоприятного влияния на плод у крыс и крольчих при дозах, в 390 и 470 раз соответственно превышающих МРДЧ (из расчета в мг/м2 при пероральных дозах для самок 200 и 120 мг/кг/сут у крыс и крольчих соответственно).
Исследования пренатального и постнатального развития у животных с левоцетиризином не проводили. В исследовании пренатального и постнатального развития, проведенном у мышей, цетиризин применяли перорально в дозах до 96 мг/кг/сут с 15-го дня беременности до 21-го дня лактации. Цетиризин снижал прирост массы тела детенышей во время лактации при пероральной дозе у самок, которая была примерно в 95 раз выше МРДЧ (из расчета в мг/м2 при пероральной дозе для самок 96 мг/кг/сут), однако не влиял на прибавку массы тела детенышей при пероральной дозе у самок, которая примерно в 25 раз превышала МРДЧ (из расчета в мг/м2 при пероральной дозе для самок 24 мг/кг/сут). В исследовании пренатального и постнатального развития, проведенном у крыс, цетиризин применяли перорально в дозах до 180 мг/кг/сут с 17-го дня беременности до 22-го дня лактации. Цетиризин не оказывал каких-либо побочных эффектов на самок крыс или на развитие потомства в дозах, примерно до 60 раз превышающих МРДЧ (из расчета в мг/м2 при пероральной дозе для самок 30 мг/кг/сут). Цетиризин вызывал чрезмерную токсичность для самок при пероральной дозе, которая примерно в 350 раз превышала МРДЧ (из расчета в мг/м2 при пероральной дозе для самок 180 мг/кг/сут).
Грудное вскармливание.
Резюме рисков. Нет данных о присутствии левоцетиризина в материнском молоке, о влиянии на грудного ребенка или о влиянии на выработку молока. Однако сообщалось, что цетиризин присутствует в грудном молоке женщин. Исследования показали, что цетиризин экскретируется в молоко у мышей и собак породы бигль ( см Данные у животных). Если ЛС присутствует в молоке животных, скорее всего, оно будет присутствовать в материнском молоке. Преимущества грудного вскармливания для развития и здоровья следует учитывать наряду с клинической потребностью матери в левоцетиризине и любыми потенциальными неблагоприятными последствиями для ребенка, находящегося на грудном вскармливании, вследствие применения левоцетиризина или под влиянием основного состояния матери.
Данные у животных. Цетиризин был обнаружен в молоке мышей. При пероральном применении у самок в период лактации цетиризина в дозе, которая примерно в 25 раз превышала МРДЧ для взрослых, не наблюдалось неблагоприятных эффектов развития у детенышей ( см Беременность). Исследования у собак породы бигль показали, что примерно 3% дозы цетиризина экскретируется в молоко. Концентрация ЛС в молоке животных не обязательно прогнозирует концентрацию ЛС в материнском молоке.
Побочные эффекты
Применение левоцетиризина было ассоциировано с сонливостью, утомляемостью, астенией и задержкой мочи ( см «Меры предосторожности»).
Опыт клинических испытаний.
Приведенные ниже данные по безопасности отражают экспозицию левоцетиризина у 2708 пациентов с аллергическим ринитом или хронической идиопатической крапивницей в 14 контролируемых клинических испытаниях продолжительностью от 1 нед до 6 мес.
Краткосрочные (экспозиция до 6 нед) данные по безопасности у взрослых и подростков основаны на 8 клинических испытаниях. в которых 1896 пациентов (825 лиц мужского пола и 1071 - женского от 12 лет и старше) получали левоцетиризин в дозах 2,5. 5 или 10 мг 1 раз в день вечером.
Краткосрочные данные по безопасности у педиатрических пациентов основаны на двух клинических испытаниях. в которых 243 ребенка с аллергическим ринитом (162 мальчика и 81 девочка от 6 до 12 лет) получали левоцетиризин в дозе 5 мг 1 раз в день в течение 4-6 нед. одном клиническом испытании. в котором 114 детей (65 мальчиков и 49 девочек от 1 года до 5 лет) с аллергическим ринитом или хронической идиопатической крапивницей получали левоцетиризин в дозе 1,25 мг 2 раза в день в течение 2 нед. и одном клиническом испытании. в котором 45 детей (28 мальчиков и 17 девочек от 6 до 11 мес) с симптомами аллергического ринита или хронической крапивницы получали левоцетиризин в дозе 1,25 мг 1 раз в день в течение 2 нед.
Долгосрочные (экспозиция 4 или 6 мес) данные по безопасности у взрослых и подростков основаны на двух клинических испытаниях. в которых 428 пациентов (190 лиц мужского пола и 238 - женского) с аллергическим ринитом получали левоцетиризин в дозе 5 мг 1 раз в день. Данные по долгосрочной безопасности также доступны из 18-месячного испытания с участием 255 пациентов 12-24 мес, получавших левоцетиризин.
Поскольку клинические испытания проводятся в самых разных условиях. частота побочных реакций. наблюдаемых в этих клинических испытаниях. не может быть непосредственно сравнена с частотой неблагоприятных эффектов в других клинических испытаниях и может не отражать частоту встречаемости этих неблагоприятных эффектов. наблюдаемую в клинической практике.
Взрослые и подростки от 12 лет и старше.
В исследованиях продолжительностью до 6 нед средний возраст взрослых и подростков составлял 32 года. 44% пациентов были мужского пола. 56% - женского. и подавляющее большинство (более 90%) составляли представители европеоидной расы.
В этих испытаниях 43 и 42% пациентов в группах, получавших левоцетиризин в дозах 2,5 и 5 мг соответственно, имели по крайней мере одно нежелательное явление по сравнению с 43% в группе плацебо.
В плацебо-контролируемых исследованиях продолжительностью 1-6 нед наиболее частыми побочными реакциями были сонливость. ринофарингит. утомляемость. сухость во рту и фарингит. и большинство из них были легкими или умеренными по интенсивности. Сонливость при приеме левоцетиризина имела дозозависимый характер и при тестируемых дозах 2,5; 5 и 10 мг была наиболее частой побочной реакцией, приводящей к прекращению приема (0,5%).
В таблице 4 перечислены побочные реакции. которые были зарегистрированы у ≥2% пациентов от 12 лет и старше. подвергавшихся экспозиции левоцетиризина в дозах 2,5 или 5 мг в восьми плацебо-контролируемых клинических испытаниях. и наблюдались чаще при приеме левоцетиризина. чем при приеме плацебо.
Таблица 4.
Побочные реакции. зарегистрированные у ≥2%1 пациентов от 12 лет и старше. подвергавшихся экспозиции левоцетиризина в дозах 2,5 или 5 мг 1 раз в день в плацебо-контролируемых клинических испытаниях продолжительностью 1-6 нед.
1 Округлено до ближайшего процентного соотношения.
Дополнительные побочные реакции. имеющие клиническое значение. которые наблюдались чаще. чем в группе плацебо. у взрослых и подростков от 12 лет и старше. подвергавшихся экспозиции левоцетиризина. включают обморок (0,2%) и увеличение массы тела (0,5%).
Педиатрические пациенты от 6 до 12 лет.
243 педиатрических пациента от 6 до 12 лет получали левоцетиризин в дозе 5 мг 1 раз в день в двух краткосрочных плацебо-контролируемых двойных слепых испытаниях. Средний возраст пациентов составлял 9,8 года, 79 (32%) были в возрасте от 6 до 8 лет, 50% принадлежали к европеоидной расе. В таблице 5 перечислены побочные реакции. которые регистрировались у ≥2% пациентов от 6 до 12 лет. подвергавшихся экспозиции левоцетиризина в дозе 5 мг в плацебо-контролируемых клинических испытаниях. и наблюдались чаще при приеме левоцетиризина. чем при приеме плацебо.
Таблица 5.
Побочные реакции, зарегистрированные у ≥2%1 пациентов 6-12 лет, подвергавшихся экспозиции левоцетиризина в дозе 5 мг 1 раз в день в плацебо-контролируемых клинических испытаниях продолжительностью 4 и 6 нед.
1 Округлено до ближайшего процентного соотношения.
Педиатрические пациенты от 1 года до 5 лет.
114 педиатрических пациентов от 1 года до 5 лет получали левоцетиризин в дозе 1,25 мг 2 раза в день в ходе двухнедельного плацебо-контролируемого двойного слепого исследования безопасности. Средний возраст пациентов составлял 3,8 года, 32% были в возрасте от 1 до 2 лет, 71% принадлежали к европеоидной расе и 18% - к негроидной. В таблице 6 перечислены побочные реакции. которые были зарегистрированы у ≥2% пациентов от 1 года до 5 лет. подвергавшихся экспозиции левоцетиризина в дозе 1,25 мг 2 раза в день в плацебо-контролируемом исследовании безопасности. и наблюдались чаще при приеме левоцетиризина. чем при приеме плацебо.
Таблица 6.
Побочные реакции, зарегистрированные у ≥2%1 пациентов 1-5 лет, подвергавшихся экспозиции левоцетиризина в дозе 1,25 мг 2 раза в день в 2-недельном плацебо-контролируемом клиническом исследовании.
1 Округлено до ближайшего процентного соотношения.
Педиатрические пациенты от 6 до 11 мес.
45 педиатрических пациентов от 6 до 11 мес получали левоцетиризин в дозе 1,25 мг 1 раз в день в ходе двухнедельного плацебо-контролируемого двойного слепого исследования безопасности. Средний возраст пациентов составлял 9 мес, 51% принадлежали к европеоидной расе и 31% - к негроидной. Побочные реакции. которые регистрировались более чем у 1 пациента ( ≥3%) от 6 до 11 мес. подвергавшихся экспозиции левоцетиризина в дозе 1,25 мг 1 раз в день в плацебо-контролируемом исследовании безопасности. и наблюдались чаще при приеме левоцетиризина. чем при приеме плацебо. включали диарею и запор. которые наблюдались у 6 (13%) и 1 (4%). 3 (7%) и 1 (4%) ребенка в группах. получавших левоцетиризин и плацебо соответственно.
Опыт долгосрочных клинических испытаний.
В двух контролируемых клинических испытаниях 428 пациентов (190 лиц мужского пола и 238 - женского) от 12 лет и старше получали левоцетиризин в дозе 5 мг 1 раз в день в течение 4 или 6 мес. Характеристики пациентов и профиль безопасности были аналогичны тем, которые наблюдались в краткосрочных исследованиях. Десять (2,3%) пациентов. принимавших левоцетиризин. прекратили лечение из-за появления побочных эффектов - сонливости. утомляемости или астении. по сравнению с 2 пациентами. у которых наблюдались те же побочные явления. (<1%) в группе плацебо.
Долгосрочные клинические исследования у детей младше 12 лет с аллергическим ринитом или хронической идиопатической крапивницей отсутствуют.
Отклонения лабораторных тестов.
Повышение уровня билирубина и трансаминаз в крови было зарегистрировано у <1% пациентов в клинических испытаниях. Повышения были преходящими и не привели к отмене лечения ни у одного пациента.
Постмаркетинговый опыт.
В дополнение к побочным реакциям, о которых сообщалось во время клинических испытаний и перечисленным выше, в постмаркетинговый период применения левоцетиризина были также выявлены следующие побочные реакции. Поскольку об этих реакциях сообщалось добровольно от популяции неопределенного размера, не всегда возможно надежно оценить их частоту или установить причинную связь с экспозицией ЛС.
Со стороны ССС. Пальпитация, тахикардия.
Со стороны органа слуха и лабиринтные расстройства. Вертиго.
Со стороны органа зрения. Нечеткость зрительного восприятия, нарушение зрения.
Со стороны ЖКТ. Тошнота, рвота.
Общие расстройства и реакции в месте введения. Отек.
Со стороны печени и желчевыводящих путей. Гепатит.
Со стороны иммунной системы. Реакции гиперчувствительности, включая анафилаксию.
Со стороны метаболизма и расстройства питания. Повышение аппетита.
Со стороны скелетно-мышечной системы и соединительной ткани. Артралгия, миалгия.
Со стороны нервной системы. Головокружение. дисгевзия. фебрильные судороги. двигательные расстройства (включая дистонию и окулогирный криз). парестезия. судороги (сообщалось у субъектов с известным судорожным расстройством и без него). тремор.
Нарушение психики. Агрессия и ажитация. депрессия. галлюцинации. инсомния. ночные кошмары. суицидальные мысли.
Со стороны почек и мочевыводящих путей. Дизурия, задержка мочи.
Со стороны респираторной системы, органов грудной клетки и средостения. Одышка.
Со стороны кожи и подкожной клетчатки. Ангионевротический отек, стойкая лекарственная эритема, зуд, сыпь и крапивница.
Помимо реакций, которые регистрировались при лечении левоцетиризином, в постмаркетинговый период применения цетиризина сообщалось о других потенциально серьезных нежелательных явлениях. Поскольку левоцетиризин является основным фармакологически активным компонентом цетиризина. следует принимать во внимание тот факт. что следующие побочные эффекты также потенциально могут возникать при лечении левоцетиризином.
Со стороны ССС. Тяжелая гипотензия.
Со стороны ЖКТ. Холестаз.
Со стороны нервной системы. Экстрапирамидные симптомы, миоклонус, орофациальная дискинезия, тик.
Беременность, послеродовый период и перинатальные состояния. Мертворождение.
Со стороны почек и мочевыводящих путей. Гломерулонефрит.
Со стороны кожи и подкожной клетчатки. Острый генерализованный экзантематозный пустулез. рикошетный зуд - зуд в течение нескольких дней после отмены цетиризина. обычно после его длительного применения (например. от месяцев до нескольких лет).
Опыт клинических испытаний.
Приведенные ниже данные по безопасности отражают экспозицию левоцетиризина у 2708 пациентов с аллергическим ринитом или хронической идиопатической крапивницей в 14 контролируемых клинических испытаниях продолжительностью от 1 нед до 6 мес.
Краткосрочные (экспозиция до 6 нед) данные по безопасности у взрослых и подростков основаны на 8 клинических испытаниях. в которых 1896 пациентов (825 лиц мужского пола и 1071 - женского от 12 лет и старше) получали левоцетиризин в дозах 2,5. 5 или 10 мг 1 раз в день вечером.
Краткосрочные данные по безопасности у педиатрических пациентов основаны на двух клинических испытаниях. в которых 243 ребенка с аллергическим ринитом (162 мальчика и 81 девочка от 6 до 12 лет) получали левоцетиризин в дозе 5 мг 1 раз в день в течение 4-6 нед. одном клиническом испытании. в котором 114 детей (65 мальчиков и 49 девочек от 1 года до 5 лет) с аллергическим ринитом или хронической идиопатической крапивницей получали левоцетиризин в дозе 1,25 мг 2 раза в день в течение 2 нед. и одном клиническом испытании. в котором 45 детей (28 мальчиков и 17 девочек от 6 до 11 мес) с симптомами аллергического ринита или хронической крапивницы получали левоцетиризин в дозе 1,25 мг 1 раз в день в течение 2 нед.
Долгосрочные (экспозиция 4 или 6 мес) данные по безопасности у взрослых и подростков основаны на двух клинических испытаниях. в которых 428 пациентов (190 лиц мужского пола и 238 - женского) с аллергическим ринитом получали левоцетиризин в дозе 5 мг 1 раз в день. Данные по долгосрочной безопасности также доступны из 18-месячного испытания с участием 255 пациентов 12-24 мес, получавших левоцетиризин.
Поскольку клинические испытания проводятся в самых разных условиях. частота побочных реакций. наблюдаемых в этих клинических испытаниях. не может быть непосредственно сравнена с частотой неблагоприятных эффектов в других клинических испытаниях и может не отражать частоту встречаемости этих неблагоприятных эффектов. наблюдаемую в клинической практике.
Взрослые и подростки от 12 лет и старше.
В исследованиях продолжительностью до 6 нед средний возраст взрослых и подростков составлял 32 года. 44% пациентов были мужского пола. 56% - женского. и подавляющее большинство (более 90%) составляли представители европеоидной расы.
В этих испытаниях 43 и 42% пациентов в группах, получавших левоцетиризин в дозах 2,5 и 5 мг соответственно, имели по крайней мере одно нежелательное явление по сравнению с 43% в группе плацебо.
В плацебо-контролируемых исследованиях продолжительностью 1-6 нед наиболее частыми побочными реакциями были сонливость. ринофарингит. утомляемость. сухость во рту и фарингит. и большинство из них были легкими или умеренными по интенсивности. Сонливость при приеме левоцетиризина имела дозозависимый характер и при тестируемых дозах 2,5; 5 и 10 мг была наиболее частой побочной реакцией, приводящей к прекращению приема (0,5%).
В таблице 4 перечислены побочные реакции. которые были зарегистрированы у ≥2% пациентов от 12 лет и старше. подвергавшихся экспозиции левоцетиризина в дозах 2,5 или 5 мг в восьми плацебо-контролируемых клинических испытаниях. и наблюдались чаще при приеме левоцетиризина. чем при приеме плацебо.
Таблица 4.
Побочные реакции. зарегистрированные у ≥2%1 пациентов от 12 лет и старше. подвергавшихся экспозиции левоцетиризина в дозах 2,5 или 5 мг 1 раз в день в плацебо-контролируемых клинических испытаниях продолжительностью 1-6 нед.
| Побочные реакции | Левоцетиризин, 2,5 мг (n=421) | Левоцетиризин, 5 мг (n=1070) | Плацебо (n=912) |
| Сонливость | 22 (5%) | 61 (6%) | 16 (2%) |
| Назофарингит | 25 (6%) | 40 (4%) | 28 (3%) |
| Утомляемость | 5 (1%) | 46 (4%) | 20 (2%) |
| Сухость во рту | 12 (3%) | 26 (2%) | 11 (1%) |
| Фарингит | 10 (2%) | 12 (1%) | 9 (1%) |
1 Округлено до ближайшего процентного соотношения.
Дополнительные побочные реакции. имеющие клиническое значение. которые наблюдались чаще. чем в группе плацебо. у взрослых и подростков от 12 лет и старше. подвергавшихся экспозиции левоцетиризина. включают обморок (0,2%) и увеличение массы тела (0,5%).
Педиатрические пациенты от 6 до 12 лет.
243 педиатрических пациента от 6 до 12 лет получали левоцетиризин в дозе 5 мг 1 раз в день в двух краткосрочных плацебо-контролируемых двойных слепых испытаниях. Средний возраст пациентов составлял 9,8 года, 79 (32%) были в возрасте от 6 до 8 лет, 50% принадлежали к европеоидной расе. В таблице 5 перечислены побочные реакции. которые регистрировались у ≥2% пациентов от 6 до 12 лет. подвергавшихся экспозиции левоцетиризина в дозе 5 мг в плацебо-контролируемых клинических испытаниях. и наблюдались чаще при приеме левоцетиризина. чем при приеме плацебо.
Таблица 5.
Побочные реакции, зарегистрированные у ≥2%1 пациентов 6-12 лет, подвергавшихся экспозиции левоцетиризина в дозе 5 мг 1 раз в день в плацебо-контролируемых клинических испытаниях продолжительностью 4 и 6 нед.
| Побочные реакции | Левоцетиризин, 5 мг (n=243) | Плацебо (n=240) |
| Лихорадка | 10 (4%) | 5 (2%) |
| Кашель | 8 (3%) | 2 (<1%) |
| Сонливость | 7 (3%) | 1 (<1%) |
| Носовое кровотечение | 6 (2%) | 1 (<1%) |
1 Округлено до ближайшего процентного соотношения.
Педиатрические пациенты от 1 года до 5 лет.
114 педиатрических пациентов от 1 года до 5 лет получали левоцетиризин в дозе 1,25 мг 2 раза в день в ходе двухнедельного плацебо-контролируемого двойного слепого исследования безопасности. Средний возраст пациентов составлял 3,8 года, 32% были в возрасте от 1 до 2 лет, 71% принадлежали к европеоидной расе и 18% - к негроидной. В таблице 6 перечислены побочные реакции. которые были зарегистрированы у ≥2% пациентов от 1 года до 5 лет. подвергавшихся экспозиции левоцетиризина в дозе 1,25 мг 2 раза в день в плацебо-контролируемом исследовании безопасности. и наблюдались чаще при приеме левоцетиризина. чем при приеме плацебо.
Таблица 6.
Побочные реакции, зарегистрированные у ≥2%1 пациентов 1-5 лет, подвергавшихся экспозиции левоцетиризина в дозе 1,25 мг 2 раза в день в 2-недельном плацебо-контролируемом клиническом исследовании.
| Побочные реакции | Левоцетиризин, 1,25 мг 2 раза в день (n=114) | Плацебо (n=59) |
| Лихорадка | 5 (4%) | 1 (2%) |
| Диарея | 4 (4%) | 2 (3%) |
| Рвота | 4 (4%) | 2 (3%) |
| Средний отит | 3 (3%) | 0 (0%) |
1 Округлено до ближайшего процентного соотношения.
Педиатрические пациенты от 6 до 11 мес.
45 педиатрических пациентов от 6 до 11 мес получали левоцетиризин в дозе 1,25 мг 1 раз в день в ходе двухнедельного плацебо-контролируемого двойного слепого исследования безопасности. Средний возраст пациентов составлял 9 мес, 51% принадлежали к европеоидной расе и 31% - к негроидной. Побочные реакции. которые регистрировались более чем у 1 пациента ( ≥3%) от 6 до 11 мес. подвергавшихся экспозиции левоцетиризина в дозе 1,25 мг 1 раз в день в плацебо-контролируемом исследовании безопасности. и наблюдались чаще при приеме левоцетиризина. чем при приеме плацебо. включали диарею и запор. которые наблюдались у 6 (13%) и 1 (4%). 3 (7%) и 1 (4%) ребенка в группах. получавших левоцетиризин и плацебо соответственно.
Опыт долгосрочных клинических испытаний.
В двух контролируемых клинических испытаниях 428 пациентов (190 лиц мужского пола и 238 - женского) от 12 лет и старше получали левоцетиризин в дозе 5 мг 1 раз в день в течение 4 или 6 мес. Характеристики пациентов и профиль безопасности были аналогичны тем, которые наблюдались в краткосрочных исследованиях. Десять (2,3%) пациентов. принимавших левоцетиризин. прекратили лечение из-за появления побочных эффектов - сонливости. утомляемости или астении. по сравнению с 2 пациентами. у которых наблюдались те же побочные явления. (<1%) в группе плацебо.
Долгосрочные клинические исследования у детей младше 12 лет с аллергическим ринитом или хронической идиопатической крапивницей отсутствуют.
Отклонения лабораторных тестов.
Повышение уровня билирубина и трансаминаз в крови было зарегистрировано у <1% пациентов в клинических испытаниях. Повышения были преходящими и не привели к отмене лечения ни у одного пациента.
Постмаркетинговый опыт.
В дополнение к побочным реакциям, о которых сообщалось во время клинических испытаний и перечисленным выше, в постмаркетинговый период применения левоцетиризина были также выявлены следующие побочные реакции. Поскольку об этих реакциях сообщалось добровольно от популяции неопределенного размера, не всегда возможно надежно оценить их частоту или установить причинную связь с экспозицией ЛС.
Со стороны ССС. Пальпитация, тахикардия.
Со стороны органа слуха и лабиринтные расстройства. Вертиго.
Со стороны органа зрения. Нечеткость зрительного восприятия, нарушение зрения.
Со стороны ЖКТ. Тошнота, рвота.
Общие расстройства и реакции в месте введения. Отек.
Со стороны печени и желчевыводящих путей. Гепатит.
Со стороны иммунной системы. Реакции гиперчувствительности, включая анафилаксию.
Со стороны метаболизма и расстройства питания. Повышение аппетита.
Со стороны скелетно-мышечной системы и соединительной ткани. Артралгия, миалгия.
Со стороны нервной системы. Головокружение. дисгевзия. фебрильные судороги. двигательные расстройства (включая дистонию и окулогирный криз). парестезия. судороги (сообщалось у субъектов с известным судорожным расстройством и без него). тремор.
Нарушение психики. Агрессия и ажитация. депрессия. галлюцинации. инсомния. ночные кошмары. суицидальные мысли.
Со стороны почек и мочевыводящих путей. Дизурия, задержка мочи.
Со стороны респираторной системы, органов грудной клетки и средостения. Одышка.
Со стороны кожи и подкожной клетчатки. Ангионевротический отек, стойкая лекарственная эритема, зуд, сыпь и крапивница.
Помимо реакций, которые регистрировались при лечении левоцетиризином, в постмаркетинговый период применения цетиризина сообщалось о других потенциально серьезных нежелательных явлениях. Поскольку левоцетиризин является основным фармакологически активным компонентом цетиризина. следует принимать во внимание тот факт. что следующие побочные эффекты также потенциально могут возникать при лечении левоцетиризином.
Со стороны ССС. Тяжелая гипотензия.
Со стороны ЖКТ. Холестаз.
Со стороны нервной системы. Экстрапирамидные симптомы, миоклонус, орофациальная дискинезия, тик.
Беременность, послеродовый период и перинатальные состояния. Мертворождение.
Со стороны почек и мочевыводящих путей. Гломерулонефрит.
Со стороны кожи и подкожной клетчатки. Острый генерализованный экзантематозный пустулез. рикошетный зуд - зуд в течение нескольких дней после отмены цетиризина. обычно после его длительного применения (например. от месяцев до нескольких лет).
|
|
Взаимодействие
По данным in vitro >in vitro, ФКВ левоцетиризина с другими ЛС путем ингибирования или индукции ферментов, метаболизирующих ЛС в печени, маловероятно.
Данные in vitro >in vitro о метаболическом взаимодействии показывают, что вряд ли левоцетиризин вызывает или будет подвергаться метаболическим взаимодействиям. Левоцетиризин в концентрациях, значительно превышающих уровень maxCmax, достигаемый в диапазонах терапевтических доз, не является ингибитором изоферментов сYP1A2, сYP2C9, сYP2C19, сYP2A1, сYP2D6, сYP2E1 и сYP3A4, а также не является индуктором изоферментов UGT1A или сYP1A2, сYP2C9 и сYP3A4.
Исследования взаимодействия in vivo >in vivo с левоцетиризином не проводили. Были проведены исследования взаимодействия с рацематом цетиризина.
Феназон, азитромицин, циметидин, эритромицин, кетоконазол, теофиллин и псевдоэфедрин.
Исследования ФКВ, проведенные с рацематом цетиризина, показали, что цетиризин не взаимодействует с феназоном, псевдоэфедрином, эритромицином, азитромицином, кетоконазолом и циметидином. Наблюдалось небольшое снижение (≈16%) клиренса цетиризина, вызванное теофиллином в дозе 400 мг. Возможно, что более высокие дозы теофиллина могут иметь больший эффект.
Ритонавир.
Ритонавир увеличивал AUC цетиризина в плазме примерно на 42%, что сопровождалось увеличением 1/2T1/2 (53%) и снижением клиренса (29%) цетиризина. Распределение ритонавира не изменялось при одновременном применении цетиризина.
Данные in vitro >in vitro о метаболическом взаимодействии показывают, что вряд ли левоцетиризин вызывает или будет подвергаться метаболическим взаимодействиям. Левоцетиризин в концентрациях, значительно превышающих уровень maxCmax, достигаемый в диапазонах терапевтических доз, не является ингибитором изоферментов сYP1A2, сYP2C9, сYP2C19, сYP2A1, сYP2D6, сYP2E1 и сYP3A4, а также не является индуктором изоферментов UGT1A или сYP1A2, сYP2C9 и сYP3A4.
Исследования взаимодействия in vivo >in vivo с левоцетиризином не проводили. Были проведены исследования взаимодействия с рацематом цетиризина.
Феназон, азитромицин, циметидин, эритромицин, кетоконазол, теофиллин и псевдоэфедрин.
Исследования ФКВ, проведенные с рацематом цетиризина, показали, что цетиризин не взаимодействует с феназоном, псевдоэфедрином, эритромицином, азитромицином, кетоконазолом и циметидином. Наблюдалось небольшое снижение (≈16%) клиренса цетиризина, вызванное теофиллином в дозе 400 мг. Возможно, что более высокие дозы теофиллина могут иметь больший эффект.
Ритонавир.
Ритонавир увеличивал AUC цетиризина в плазме примерно на 42%, что сопровождалось увеличением 1/2T1/2 (53%) и снижением клиренса (29%) цетиризина. Распределение ритонавира не изменялось при одновременном применении цетиризина.
Передозировка
Сообщалось о передозировке левоцетиризина.
Симптомы передозировки могут включать сонливость у взрослых. У детей вначале могут возникать ажитация и беспокойство, за которыми следует сонливость.
Лечение. Известного специфического антидота левоцетиризина нет. В случае передозировки рекомендуется симптоматическое или поддерживающее лечение. Левоцетиризин не удаляется эффективно с помощью диализа.
Острая максимальная нелетальная пероральная доза левоцетиризина для мышей составила 240 мг/кг (примерно в 190 раз больше максимальной рекомендованной суточной пероральной дозы для взрослых. примерно в 230 раз больше максимальной рекомендованной суточной пероральной дозы для детей от 6 до 11 лет и примерно в 180 раз больше максимальной рекомендованной суточной пероральной дозы для детей от 6 мес до 5 лет из расчета на мг/м2). У крыс максимальная нелетальная пероральная доза составляла 240 мг/кг (примерно в 390 раз больше максимальной рекомендованной суточной пероральной дозы для взрослых. примерно в 460 раз больше максимальной рекомендованной суточной пероральной дозы для детей от 6 до 11 лет и примерно в 370 раз больше максимальной рекомендуемой суточной пероральной дозы для детей от 6 мес до 5 лет из расчета на мг/м2).
Симптомы передозировки могут включать сонливость у взрослых. У детей вначале могут возникать ажитация и беспокойство, за которыми следует сонливость.
Лечение. Известного специфического антидота левоцетиризина нет. В случае передозировки рекомендуется симптоматическое или поддерживающее лечение. Левоцетиризин не удаляется эффективно с помощью диализа.
Острая максимальная нелетальная пероральная доза левоцетиризина для мышей составила 240 мг/кг (примерно в 190 раз больше максимальной рекомендованной суточной пероральной дозы для взрослых. примерно в 230 раз больше максимальной рекомендованной суточной пероральной дозы для детей от 6 до 11 лет и примерно в 180 раз больше максимальной рекомендованной суточной пероральной дозы для детей от 6 мес до 5 лет из расчета на мг/м2). У крыс максимальная нелетальная пероральная доза составляла 240 мг/кг (примерно в 390 раз больше максимальной рекомендованной суточной пероральной дозы для взрослых. примерно в 460 раз больше максимальной рекомендованной суточной пероральной дозы для детей от 6 до 11 лет и примерно в 370 раз больше максимальной рекомендуемой суточной пероральной дозы для детей от 6 мес до 5 лет из расчета на мг/м2).
Способ применения и дозы
Внутрь. Режим дозирования индивидуальный, в зависимости от показаний, возраста, функции почек.
Меры предосторожности применения
Сонливость.
В клинических испытаниях у некоторых пациентов, принимавших левоцетиризин, сообщалось о возникновении сонливости, утомляемости и астении. Пациентам следует воздерживаться от занятий потенциально опасными видами деятельности, требующими повышенной концентрации внимания и координации движений, таких как управление механизмами или вождение автомобиля, после приема левоцетиризина. Следует избегать одновременного применения левоцетиризина с алкоголем или ЛС, угнетающими ЦНС, поскольку возможно их аддитивное действие и снижение активности и дополнительное нарушение работы ЦНС.
Задержка мочи.
В постмаркетинговый период применения левоцетиризина сообщалось о задержке мочи. Левоцетиризин следует применять с осторожностью у пациентов с предрасполагающими к задержке мочи факторами (например, повреждение спинного мозга, гиперплазия предстательной железы), поскольку левоцетиризин может увеличивать риск задержки мочи. При возникновении задержки мочи прием левоцетиризина следует прекратить.
Применение в педиатрии.
Рекомендуемая доза левоцетиризина для лечения неосложненных кожных проявлений хронической идиопатической крапивницы у пациентов от 6 мес до 17 лет основана на экстраполяции эффективности у взрослых 18 лет и старше ( см Клинические исследования).
Рекомендуемая доза левоцетиризина для пациентов от 6 мес до 2 лет для лечения симптомов круглогодичного аллергического ринита и от 6 мес до 11 лет с хронической идиопатической крапивницей основана на сравнениях перекрестных исследований системной экспозиции левоцетиризина у взрослых и педиатрических пациентов, а также на профиле безопасности левоцетиризина как у взрослых, так и у педиатрических пациентов при дозах, равных или превышающих рекомендуемую дозу для пациентов от 6 мес до 11 лет.
Безопасность левоцетиризина в дозе 5 мг 1 раз в день оценивали у 243 педиатрических пациентов от 6 до 12 лет в двух плацебо-контролируемых клинических испытаниях продолжительностью 4 и 6 нед. Безопасность левоцетиризина в дозе 1,25 мг 2 раза в день оценивали в одном 2-недельном клиническом испытании с участием 114 педиатрических пациентов от 1 года до 5 лет, а безопасность левоцетиризина в дозе 1,25 мг 1 раз в день оценивали в одном 2-недельном клиническом исследовании с участием 45 педиатрических пациентов от 6 до 11 мес ( см «Побочные действия»).
Эффективность левоцетиризина в дозе 1,25 мг 1 раз в день (пациенты от 6 мес до 5 лет) и 2,5 мг 1 раз в день (пациенты от 6 до 11 лет) для лечения симптомов круглогодичного аллергического ринита и хронической идиопатической крапивницы была подтверждена экстраполяцией продемонстрированной эффективности левоцетиризина в дозе 5 мг 1 раз в сутки у пациентов от 12 лет и старше, на основе фармакокинетического сравнения у взрослых и детей.
Сравнения перекрестных исследований показывают, что применение левоцетиризина в дозе 5 мг у педиатрических пациентов от 6 до 12 лет приводило примерно к двукратному увеличению AUC, наблюдаемому при применении левоцетиризина в дозе 5 мг у здоровых взрослых. Поэтому у детей от 6 до 11 лет не следует превышать рекомендуемую дозу 2,5 мг 1 раз в сутки. В популяционном фармакокинетическом исследовании применение дозы 1,25 мг 1 раз в день у детей от 6 мес до 5 лет приводило к системному воздействию, сравнимому с воздействием при применении дозы 5 мг 1 раз в день у взрослых ( см «Фармакология», Фармакокинетика, Клинические исследования).
Применение в гериатрии.
Клинические исследования левоцетиризина для каждого утвержденного показания не включали достаточное количество пациентов от 65 лет и старше, чтобы определить, реагируют ли они иначе, чем пациенты более молодого возраста. Другой зарегистрированный клинический опыт не выявил различий в ответах пожилых и молодых пациентов. В целом подбор дозы для пожилого пациента следует проводить с осторожностью, обычно начиная с нижнего предела диапазона дозирования, в связи с более высокой частотой снижения функции печени, почек или сердца и сопутствующего заболевания или другой лекарственной терапии.
Нарушение функции почек.
Известно, что левоцетиризин в значительной степени выводится почками и риск развития побочных реакций на это ЛС может быть выше у пациентов с нарушением функции почек. Поскольку у пожилых пациентов более вероятно снижение функции почек, следует соблюдать осторожность при выборе дозы, и может быть полезен мониторинг функции почек ( см «Фармакология», Фармакокинетика).
Нарушение функции печени.
Поскольку левоцетиризин в основном выводится в неизмененном виде почками, маловероятно, что клиренс левоцетиризина значительно снижается у пациентов с нарушением функции только печени ( см «Фармакология», Фармакокинетика).
В клинических испытаниях у некоторых пациентов, принимавших левоцетиризин, сообщалось о возникновении сонливости, утомляемости и астении. Пациентам следует воздерживаться от занятий потенциально опасными видами деятельности, требующими повышенной концентрации внимания и координации движений, таких как управление механизмами или вождение автомобиля, после приема левоцетиризина. Следует избегать одновременного применения левоцетиризина с алкоголем или ЛС, угнетающими ЦНС, поскольку возможно их аддитивное действие и снижение активности и дополнительное нарушение работы ЦНС.
Задержка мочи.
В постмаркетинговый период применения левоцетиризина сообщалось о задержке мочи. Левоцетиризин следует применять с осторожностью у пациентов с предрасполагающими к задержке мочи факторами (например, повреждение спинного мозга, гиперплазия предстательной железы), поскольку левоцетиризин может увеличивать риск задержки мочи. При возникновении задержки мочи прием левоцетиризина следует прекратить.
Применение в педиатрии.
Рекомендуемая доза левоцетиризина для лечения неосложненных кожных проявлений хронической идиопатической крапивницы у пациентов от 6 мес до 17 лет основана на экстраполяции эффективности у взрослых 18 лет и старше ( см Клинические исследования).
Рекомендуемая доза левоцетиризина для пациентов от 6 мес до 2 лет для лечения симптомов круглогодичного аллергического ринита и от 6 мес до 11 лет с хронической идиопатической крапивницей основана на сравнениях перекрестных исследований системной экспозиции левоцетиризина у взрослых и педиатрических пациентов, а также на профиле безопасности левоцетиризина как у взрослых, так и у педиатрических пациентов при дозах, равных или превышающих рекомендуемую дозу для пациентов от 6 мес до 11 лет.
Безопасность левоцетиризина в дозе 5 мг 1 раз в день оценивали у 243 педиатрических пациентов от 6 до 12 лет в двух плацебо-контролируемых клинических испытаниях продолжительностью 4 и 6 нед. Безопасность левоцетиризина в дозе 1,25 мг 2 раза в день оценивали в одном 2-недельном клиническом испытании с участием 114 педиатрических пациентов от 1 года до 5 лет, а безопасность левоцетиризина в дозе 1,25 мг 1 раз в день оценивали в одном 2-недельном клиническом исследовании с участием 45 педиатрических пациентов от 6 до 11 мес ( см «Побочные действия»).
Эффективность левоцетиризина в дозе 1,25 мг 1 раз в день (пациенты от 6 мес до 5 лет) и 2,5 мг 1 раз в день (пациенты от 6 до 11 лет) для лечения симптомов круглогодичного аллергического ринита и хронической идиопатической крапивницы была подтверждена экстраполяцией продемонстрированной эффективности левоцетиризина в дозе 5 мг 1 раз в сутки у пациентов от 12 лет и старше, на основе фармакокинетического сравнения у взрослых и детей.
Сравнения перекрестных исследований показывают, что применение левоцетиризина в дозе 5 мг у педиатрических пациентов от 6 до 12 лет приводило примерно к двукратному увеличению AUC, наблюдаемому при применении левоцетиризина в дозе 5 мг у здоровых взрослых. Поэтому у детей от 6 до 11 лет не следует превышать рекомендуемую дозу 2,5 мг 1 раз в сутки. В популяционном фармакокинетическом исследовании применение дозы 1,25 мг 1 раз в день у детей от 6 мес до 5 лет приводило к системному воздействию, сравнимому с воздействием при применении дозы 5 мг 1 раз в день у взрослых ( см «Фармакология», Фармакокинетика, Клинические исследования).
Применение в гериатрии.
Клинические исследования левоцетиризина для каждого утвержденного показания не включали достаточное количество пациентов от 65 лет и старше, чтобы определить, реагируют ли они иначе, чем пациенты более молодого возраста. Другой зарегистрированный клинический опыт не выявил различий в ответах пожилых и молодых пациентов. В целом подбор дозы для пожилого пациента следует проводить с осторожностью, обычно начиная с нижнего предела диапазона дозирования, в связи с более высокой частотой снижения функции печени, почек или сердца и сопутствующего заболевания или другой лекарственной терапии.
Нарушение функции почек.
Известно, что левоцетиризин в значительной степени выводится почками и риск развития побочных реакций на это ЛС может быть выше у пациентов с нарушением функции почек. Поскольку у пожилых пациентов более вероятно снижение функции почек, следует соблюдать осторожность при выборе дозы, и может быть полезен мониторинг функции почек ( см «Фармакология», Фармакокинетика).
Нарушение функции печени.
Поскольку левоцетиризин в основном выводится в неизмененном виде почками, маловероятно, что клиренс левоцетиризина значительно снижается у пациентов с нарушением функции только печени ( см «Фармакология», Фармакокинетика).
|
|
Список литературы
RxList.com, 2021.
Входит в состав
- 140₽ Фри-ал
- 162₽ Левоцетиризин
- 192₽ Левоцетиризин-Тева
- 206₽ Квисил дропс (Треугольник ООО )
- 128-296₽ Эльцет
- 214-356₽ Левоцетиризин-ВЕРТЕКС
- 317₽ Аллервэй Экспресс (Атена Драг Деливери Солюшнз Пвт.Лтд )
- 347₽ Алерсэт-Л (Micro Labs )
- 218-500₽ Супрастинекс (Фармацевтический завод ЭГИС)
- 219-504₽ Аллервэй
- 275-503₽ Квисил табс
- 342-540₽ Ксизал (3 фирмы)
- 341-797₽ Гленцет (Glenmark Pharmaceuticals Ltd (Nasik) )
- 372-1084₽ Зодак Экспресс (2 фирмы)
- 351-1229₽ Монтрал МЛ (Micro Labs )
- 515-1329₽ Монтлезир ( офис 9509)
- — Аллергофри (2 фирмы)
- — Зенаро
- — Левоцетиризин Реневал
- — Левоцетиризин Сандоз
- — Левоцетиризина дигидрохлорид (3 фирмы)
- — СТРЕГА табс (Synthon Hispania S.L. )
- — Тивовин
- — Цетрин Л