Pharmacological Group
Latin name
Bortezomibum ( вortezomibi).
Chemical name
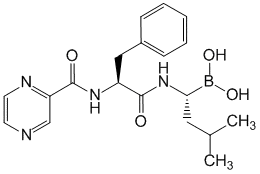
[(1R)-3-Метил-1-[[(2S)-1-оксо-3-фенил-2-[(пиразинилкарбонил)амино]пропил]амино]бутил]бороновая кислота.
Used in the treatment
CAS Code
179324-69-7.
Pharmacological action
Противоопухолевое.
Characteristics of the substance
Противоопухолевое средство, протеасомный ингибитор. Бортезомиб представляет собой модифицированную борную кислоту. Растворимость в воде 3,3-3,8 мг/мл в диапазоне pH 2-6,5. Молекулярная масса 384,24.
Pharmacodynamics
Обратимо ингибирует химотрипсиноподобную активность протеасомы 26S. Протеасома 26S - крупный белковый комплекс, который катализирует расщепление основных белков и регулирует их внутриклеточные концентрации. Так называемый «убиквитин-протеасомный путь» играет важную роль в регуляции уровня специфических белков, поддерживая таким образом гомеостаз внутри клеток млекопитающих. Ингибируя химотрипсиноподобное действие протеасомы 26S, бортезомиб вызывает торможение протеолиза, приводящего к сложному сигнальному каскаду внутри клетки, нарушение нормального клеточного гомеостаза и, возможно, апоптоз. Эксперименты продемонстрировали, что бортезомиб цитотоксичен для большого числа типов опухолевых клеток in vitro. Он также вызывает задержку роста опухоли in vivo >in vivo в неклинических моделях опухолей, включая множественную миелому.
Канцерогенность, мутагенность, влияние на фертильность.
Исследований канцерогенности бортезомиба не проводили.
Бортезомиб проявлял кластогенную активность (структурные хромосомные аберрации) в тесте in vitro >in vitro на клетках яичника китайского хомячка. Не проявлял генотоксических свойств в тестах in vitro >in vitro (тест Эймса) и in vivo >in vivo (микроядерный тест у мышей).
Изучение влияния бортезомиба на фертильность не выполнено, но оценка состояния репродуктивных тканей проведена в исследованиях общей токсичности. В 6-месячном токсикологическом исследовании у крыс наблюдались дегенеративные процессы в яичниках при дозах ≥0,3 мг/м2 (1/4 рекомендуемой клинической дозы) и дегенеративные изменения в яичках при дозе 1,2 мг/м2. Таким образом, бортезомиб может оказывать эффект на фертильность представителей обоих полов.
Токсичность у животных.
Сердечно-сосудистая токсичность. В исследованиях на обезьянах и собаках показано, что в/в введение бортезомиба в дозах, примерно в 2-3 раза превышающих рекомендуемую клиническую дозу (в мг/м2 основания), приводило к увеличению ЧСС, снижению сократимости миокарда, глубокой прогрессирующей гипотензии, брадикардии и смерти. У обезьян дозы ≥3,0 мг/м2 (примерно в 2 раза выше рекомендованной клинической дозы) вели к прогрессирующей гипотензии через 1 ч после введения и летальному исходу спустя 12-14 Дозы ≥1,2 мг/м2 вызывали дозозависимое изменение сердечных параметров. Бортезомиб распределяется по большей части тканей организма, включая миокард. При повторных введениях при изучении токсичности у обезьян наблюдались кровоизлияние в миокард, воспаление и некроз.
Хроническое введение. В исследованиях на животных при дозе и режиме дозирования, сходных с рекомендованными для человека (дважды в неделю в течение 2 нед после 1 нед перерыва), наблюдавшиеся проявления токсичности включали выраженные анемию и тромбоцитопению, токсичность в отношении ЖКТ, лимфоидной системы, неврологические проявления. Нейротоксические эффекты бортезомиба в исследованиях на животных включали набухание аксонов и дегенерацию периферических нервов, дорзальных спинальных путей и трактов спинного мозга. Кроме того, отмечались многоочаговые кровоизлияния и некроз в мозге, глазах и сердце.
Канцерогенность, мутагенность, влияние на фертильность.
Исследований канцерогенности бортезомиба не проводили.
Бортезомиб проявлял кластогенную активность (структурные хромосомные аберрации) в тесте in vitro >in vitro на клетках яичника китайского хомячка. Не проявлял генотоксических свойств в тестах in vitro >in vitro (тест Эймса) и in vivo >in vivo (микроядерный тест у мышей).
Изучение влияния бортезомиба на фертильность не выполнено, но оценка состояния репродуктивных тканей проведена в исследованиях общей токсичности. В 6-месячном токсикологическом исследовании у крыс наблюдались дегенеративные процессы в яичниках при дозах ≥0,3 мг/м2 (1/4 рекомендуемой клинической дозы) и дегенеративные изменения в яичках при дозе 1,2 мг/м2. Таким образом, бортезомиб может оказывать эффект на фертильность представителей обоих полов.
Токсичность у животных.
Сердечно-сосудистая токсичность. В исследованиях на обезьянах и собаках показано, что в/в введение бортезомиба в дозах, примерно в 2-3 раза превышающих рекомендуемую клиническую дозу (в мг/м2 основания), приводило к увеличению ЧСС, снижению сократимости миокарда, глубокой прогрессирующей гипотензии, брадикардии и смерти. У обезьян дозы ≥3,0 мг/м2 (примерно в 2 раза выше рекомендованной клинической дозы) вели к прогрессирующей гипотензии через 1 ч после введения и летальному исходу спустя 12-14 Дозы ≥1,2 мг/м2 вызывали дозозависимое изменение сердечных параметров. Бортезомиб распределяется по большей части тканей организма, включая миокард. При повторных введениях при изучении токсичности у обезьян наблюдались кровоизлияние в миокард, воспаление и некроз.
Хроническое введение. В исследованиях на животных при дозе и режиме дозирования, сходных с рекомендованными для человека (дважды в неделю в течение 2 нед после 1 нед перерыва), наблюдавшиеся проявления токсичности включали выраженные анемию и тромбоцитопению, токсичность в отношении ЖКТ, лимфоидной системы, неврологические проявления. Нейротоксические эффекты бортезомиба в исследованиях на животных включали набухание аксонов и дегенерацию периферических нервов, дорзальных спинальных путей и трактов спинного мозга. Кроме того, отмечались многоочаговые кровоизлияния и некроз в мозге, глазах и сердце.
Pharmacokinetics
После в/в введения дозы 1,3 мг/м2 значение медианы maxCmax бортезомиба составляло 509 нг/мл (в диапазоне 109-1300 нг/мл) у 8 пациентов с множественной миеломой и клиренсом креатинина в диапазоне 31-169 мл/мин. Значение Т1/2 бортезомиба после первой дозы варьировало в диапазоне от 9 до 15 ч при дозах от 1,45 до 2,0 мг/м2 у пациентов с запущенными злокачественными опухолями. Фармакокинетика бортезомиба при использовании в рекомендуемой дозе у пациентов с множественной миеломой не полностью охарактеризована, в частности не оценен dVd. Связывание с белками плазмы составляет в среднем 83% в диапазоне концентраций от 100 до 1000 нг/мл. В in vitro >in vitro исследованиях с использованием микросом печени человека показано, что бортезомиб метаболизируется главным образом путем микросомального окисления с участием изоферментов сYP3A4, сYP2D6, сYP2C19, сYP2C9 и сYP1А2 цитохрома Р450. Образующиеся метаболиты неактивны в отношении протеасомы 26S. В объединенной пробе плазмы, полученной от 8 пациентов через 10 и 30 мин после введения, уровень метаболитов был низким по сравнению с уровнем самого вещества. Путь элиминации бортезомиба у человека пока не охарактеризован.
Зависимость параметров фармакокинетики от некоторых факторов.
Влияние возраста, пола, расы на фармакокинетику бортезомиба не оценивали.
Фармакокинетических исследований у пациентов с нарушением функции печени и/или почек не проводили. В клинические исследования были включены пациенты с клиренсом креатинина от 13,8 до 220 мл/мин.
Среди пациентов, участвовавших в Фазе 2 клинических испытаний (n=202), 35% были в возрасте 65 лет и старше. В этой возрастной группе у 19% пациентов была отмечена реакция на бортезомиб, в сравнении с 32% у пациентов до 65 лет. Среди 256 пациентов, у которых оценивали безопасность бортезомиба, частота побочных реакций 3 и 4 степени тяжести составляла 74, 80 и 85% у пациентов младше 50, 51-65 и старше 65 лет соответственно.
Клинические исследования.
Оценку безопасности и эффективности бортезомиба (клинические испытания Фазы 2) проводили в открытом нерандомизированном мультицентровом исследовании, в котором участвовало 202 пациента с рецидивирующей и резистентной множественной миеломой, которые ранее прошли, как минимум, 2 курса лечения и у которых заболевание продолжало прогрессировать после последнего курса. Пациенты получали бортезомиб в виде болюса в дозе 1,3 мг/м2 дважды в неделю в течение 2 нед, затем - 10-дневный перерыв; максимально проводилось 8 циклов.
Зависимость параметров фармакокинетики от некоторых факторов.
Влияние возраста, пола, расы на фармакокинетику бортезомиба не оценивали.
Фармакокинетических исследований у пациентов с нарушением функции печени и/или почек не проводили. В клинические исследования были включены пациенты с клиренсом креатинина от 13,8 до 220 мл/мин.
Среди пациентов, участвовавших в Фазе 2 клинических испытаний (n=202), 35% были в возрасте 65 лет и старше. В этой возрастной группе у 19% пациентов была отмечена реакция на бортезомиб, в сравнении с 32% у пациентов до 65 лет. Среди 256 пациентов, у которых оценивали безопасность бортезомиба, частота побочных реакций 3 и 4 степени тяжести составляла 74, 80 и 85% у пациентов младше 50, 51-65 и старше 65 лет соответственно.
Клинические исследования.
Оценку безопасности и эффективности бортезомиба (клинические испытания Фазы 2) проводили в открытом нерандомизированном мультицентровом исследовании, в котором участвовало 202 пациента с рецидивирующей и резистентной множественной миеломой, которые ранее прошли, как минимум, 2 курса лечения и у которых заболевание продолжало прогрессировать после последнего курса. Пациенты получали бортезомиб в виде болюса в дозе 1,3 мг/м2 дважды в неделю в течение 2 нед, затем - 10-дневный перерыв; максимально проводилось 8 циклов.
Indications for use
Множественная миелома у пациентов, прошедших, как минимум, 2 курса лечения, у которых наблюдается прогрессирование болезни после последнего курса.
Contraindications
Гиперчувствительность, в тч к бору.
Restrictions on use
Детский возраст (безопасность и эффективность применения у детей не установлены).
Use during pregnancy and lactation
Назначать беременным женщинам можно лишь в том случае, если преимущества терапии превышают потенциальный риск для плода (адекватных и строго контролируемых исследований у беременных женщин не проведено). Неизвестно, проходит ли бортезомиб через плаценту. В случае применения при беременности или в период планируемой беременности необходимо предупредить пациентку о потенциальном риске для плода. Женщинам детородного возраста во время терапии необходимо использовать эффективные методы контрацепции.
Категория действия на плод по FDA. D.
Бортезомиб не проявлял тератогенных свойств в доклинических исследованиях токсичности у крыс и кроликов при наивысшей тестируемой дозе (0,075 мг/кг; 0,5 мг/м2 у крыс и 0,05 мг/кг; 0,6 мг/м2 у кроликов) при введении в период органогенеза. Эти дозы примерно эквивалентны 1/2 клинической дозы 1,3 мг/м2 в пересчете на площадь поверхности тела.
У беременных крольчих, получавших бортезомиб в период органогенеза в дозе 0,05 мг/кг (0,6 мг/м2), наблюдались значительные постимплантационные потери и снижение числа жизнеспособных детенышей при рождении. Детеныши из этих приплодов при рождении имели также сниженную массу тела.
Неизвестно, проникает ли бортезомиб в грудное молоко женщин. Поскольку многие ЛС экскретируются в грудное молоко и могут оказывать серьезное неблагоприятное воздействие на детей, находящихся на грудном вскармливании, на время терапии бортезомибом необходимо прекратить кормление грудью.
Категория действия на плод по FDA. D.
Бортезомиб не проявлял тератогенных свойств в доклинических исследованиях токсичности у крыс и кроликов при наивысшей тестируемой дозе (0,075 мг/кг; 0,5 мг/м2 у крыс и 0,05 мг/кг; 0,6 мг/м2 у кроликов) при введении в период органогенеза. Эти дозы примерно эквивалентны 1/2 клинической дозы 1,3 мг/м2 в пересчете на площадь поверхности тела.
У беременных крольчих, получавших бортезомиб в период органогенеза в дозе 0,05 мг/кг (0,6 мг/м2), наблюдались значительные постимплантационные потери и снижение числа жизнеспособных детенышей при рождении. Детеныши из этих приплодов при рождении имели также сниженную массу тела.
Неизвестно, проникает ли бортезомиб в грудное молоко женщин. Поскольку многие ЛС экскретируются в грудное молоко и могут оказывать серьезное неблагоприятное воздействие на детей, находящихся на грудном вскармливании, на время терапии бортезомибом необходимо прекратить кормление грудью.
Side effects
Представлены результаты двух исследований с участием 228 пациентов с множественной миеломой. получавших бортезомиб в дозе 1,3 мг/м2 дважды в неделю в течение 2 нед с 10-дневным перерывом (продолжительность цикла лечения - 21 день) максимально в течение не более 8 циклов.
Наиболее частыми побочными эффектами были астенические состояния (включая повышенную утомляемость. общую слабость. недомогание) (65%). тошнота (64%). диарея (51%). снижение аппетита (включая анорексию) (43%). запор (43%). тромбоцитопения (43%). периферическая нейропатия (включая периферическую сенсорную и обострение периферической нейропатии) (37%). лихорадка (36%). рвота (36%). анемия (32%). По крайней мере у 14% пациентов наблюдался как минимум один эпизод 4 степени токсичности, наиболее общими среди них были тромбоцитопения (3%) и нейтропения (3%).
В таблице представлены наиболее общие побочные эффекты, отмеченные в клинических испытаниях у пациентов, получавших бортезомиб. Все включенные в таблицу эффекты наблюдались у ?10% пациентов. В нерандомизированном исследовании часто невозможно разграничить нежелательные явления, связанные с приемом лекарства и эффекты, обусловленные заболеванием.
Таблица.
Побочные эффекты, наблюдавшиеся в клинических испытаниях у пациентов при лечении бортезомибом (N=228).
Серьезные побочные эффекты. Серьезные побочные эффекты определяли как какой-либо случай. безотносительно причины. который имел результатом летальный исход. был угрожающим жизни. требовал госпитализации или продлевал текущую госпитализацию. приводя к значительной беспомощности или считающийся важным медицинским случаем.
Во время исследования серьезные побочные эффекты наблюдались у 113 (50%) из 228 пациентов. Наиболее общими серьезными побочными эффектами были лихорадка (7%). пневмония (7%). диарея (6%). рвота (5%). дегидратация (5%). тошнота (4%).
Побочные эффекты, отмеченные исследователями как обусловленные приемом лекарства и вызвавшие прекращение лечения, были отмечены у 18% пациентов. Поводом к прекращению приема лекарства послужили периферическая нейропатия (5%), тромбоцитопения (4%), диарея (2%), повышенная утомляемость (2%).
Были зафиксированы два летальных исхода. которые рассматривались исследователями как предположительно связанные с исследованием лекарства: один случай остановки сердца вследствие сердечно-легочной недостаточности и один случай - из-за дыхательной недостаточности.
Астенические состояния (повышенная утомляемость, общая слабость, недомогание). Астения была отмечена у 65% пациентов и в основном имела 1 и 2 степень выраженности. Первоначально повышенная утомляемость отмечалась наиболее часто в течение 1-го и 2-го циклов терапии. Астения 3 степени выраженности была отмечена у 18% пациентов. Прекратили лечение из-за возникновения повышенной утомляемости 2% пациентов.
Желудочно-кишечные эффекты, наблюдавшиеся у большинства пациентов. Тошнота, диарея, запор, рвота. Эффекты 3 и 4 степени выраженности отмечались у 21% и были определены как серьезные у 13% пациентов. Рвота и диарея были тяжелыми и имели 3 степень выраженности у 7%, 4 степень - менее чем у 1% пациентов. Прекратили лечение из-за расстройств ЖКТ 5% больных. Снижение аппетита (анорексия) была отмечена как побочный эффект у 43% пациентов (3 степени выраженности - 3%).
Тромбоцитопения при лечении бортезомибом наблюдалась у 43% пациентов. она характеризовалась дозозависимым снижением числа тромбоцитов в период применения бортезомиба (с 1 по 11 день) и возвращалась к исходному уровню в период перерыва (дни с 12 по 21) в каждом цикле. Число тромбоцитов снижалось на 40% по сравнению с исходным. Значения числа тромбоцитов составляли менее 50 тыс. клеток/мкл и менее 10 тыс. клеток/мкл у 27 и 3% пациентов соответственно. Прекратили лечение из-за тромбоцитопении вне зависимости от степени ее выраженности 4% больных.
Периферическая сенсорная нейропатия. Нейропатия, включая сенсорную и обострение периферической нейропатии, отмечалась в 37% случаев. Периферическая нейропатия 3 степени - у 14%, не было отмечено случаев нейропатии 4 степени. Начальные проявления или обострение предшествующей нейропатии отмечалось на протяжении цикла лечения. Нейропатия явилась причиной отмены препарата в 6% случаев. Более чем у 80% пациентов, участвовавших в исследовании, имелись признаки и симптомы периферической нейропатии по сравнению с исходным состоянием. Частота нейропатии 3 степени составила 5% (2 из 41 пациента) у людей без предшествующей нейропатии. Симптомы могут улучшаться или возвращаться к исходному уровню у некоторых пациентов при отмене препарата. Полная оценка зависимости развития этого вида токсичности от времени не проведена.
Лихорадка (>38 °C) отмечалась как побочный эффект у 36% пациентов и имела 3 степень выраженности у 4% пациентов.
Нейтропения встречалась у 26% больных и имела 3 степень выраженности в 13% случаев и 4 степень - в 3%. Частота фебрильной нейтропении составила <1%.
Гипотензия (включая сообщения об ортостатической гипотензии) отмечалась у 12% пациентов, большинство случаев были 1 и 2 степени выраженности, у 4% - 3 степени, ни у кого не было гипотензии 4 степени выраженности. Пациенты, у которых отмечалась ортостатическая гипотензия, не имели таковой в начале исследования, у половины больных была предшествующая гипертензия, у 1/3 - периферическая нейропатия. Дозы антигипертензивных препаратов могут быть скорректированы у пациентов, получающих бортезомиб. У 4% пациентов с гипотензией, включая ортостатическую, отмечались одновременно обморочные состояния.
Серьезные побочные эффекты во время клинических исследований. Примерно у 580 пациентов наблюдались следующие серьезные неблагоприятные эффекты (не описаны выше). рассматриваемые как возможно связанные с лечением и отмеченные по крайней мере у одного пациента. получавшего бортезомиб в качестве монотерапии или в комбинации с другими химиотерапевтическими средствами. Эти исследования были проведены у пациентов с гематологическими злокачественными новообразованиями и сoлидными опухолями.
Заболевания крови и лимфатической системы. Диссеминированная внутрисосудистая коагуляция.
Сердечные заболевания. Приступы фибрилляции предсердий. трепетание предсердий. сердечный амилоидоз. остановка сердца. застойная сердечная недостаточность. ишемия миокарда. инфаркт миокарда. перикардиальный выпот. отек легких. желудочковая тахикардия.
Заболевания ЖКТ. Асцит. дисфагия. фекалома. геморрагический гастрит. гематемезис. паралитическая непроходимость кишечника. обструкция толстого кишечника. обструкция тонкого кишечника. прободение тостой кишки. стоматит. мелена. острый панкреатит.
Гепатобилиарная система. Гипербилирубинемия, тромбоз портальной вены.
Иммунная система. Анафилактические реакции, реакции гиперчувствительности.
Инфекции и инвазии. Бактериемия.
Повреждение, отравление, осложнения. Переломы, субдуральная гематома.
Метаболизм и обмен веществ. Гипокальциемия, гиперурикемия, гипокалиемия, гипонатриемия, синдром лизиса опухоли.
Нервная система. Атаксия. кома. головокружение. дизартрия. нарушение функций вегетативной нервной системы. паралич черепно-мозговых нервов. судорожные припадки типа grand mal. геморрагический инсульт. двигательные нарушения. компрессия спинного мозга. транзиторная ишемическая атака.
Психиатрия. Ажитация, спутанность сознания, психоз, суицидальные мысли.
Почки и мочевыводящие пути. Почечные камни. билатеральный гидронефроз. спазм мочевого пузыря. гематурия. недержание мочи. задержка мочеиспускания. почечная недостаточность (острая и хроническая). клубочковый пролиферативный нефрит.
Респираторная система. Острый респираторный дистресс-синдром. ателектаз. обострение хронической обструктивной болезни легких. дисфагия. диспноэ. одышка при физической нагрузке. носовое кровотечение. кровохарканье. гипоксия. инфильтрация легких. плевральный выпот. пневмонит. респираторный дистресс. дыхательная недостаточность.
Сосудистые. Цереброваскулярные нарушения, тромбоз глубоких вен, периферическая эмболия, легочная эмболия.
Наиболее частыми побочными эффектами были астенические состояния (включая повышенную утомляемость. общую слабость. недомогание) (65%). тошнота (64%). диарея (51%). снижение аппетита (включая анорексию) (43%). запор (43%). тромбоцитопения (43%). периферическая нейропатия (включая периферическую сенсорную и обострение периферической нейропатии) (37%). лихорадка (36%). рвота (36%). анемия (32%). По крайней мере у 14% пациентов наблюдался как минимум один эпизод 4 степени токсичности, наиболее общими среди них были тромбоцитопения (3%) и нейтропения (3%).
В таблице представлены наиболее общие побочные эффекты, отмеченные в клинических испытаниях у пациентов, получавших бортезомиб. Все включенные в таблицу эффекты наблюдались у ?10% пациентов. В нерандомизированном исследовании часто невозможно разграничить нежелательные явления, связанные с приемом лекарства и эффекты, обусловленные заболеванием.
Таблица.
Побочные эффекты, наблюдавшиеся в клинических испытаниях у пациентов при лечении бортезомибом (N=228).
| Побочный эффект | Частота нежелательных явлений, n (%) | ||
| Все случаи | 3 степень тяжести | 4 степень тяжести | |
| Астенические состояния | 149 (65) | 42 (18) | 1 (<1) |
| Тошнота | 145 (64) | 13 (6) | 0 |
| Диарея | 116 (51) | 16 (7) | 2 (<1) |
| Снижение аппетита | 99 (43) | 6 (3) | 0 |
| Запор | 97 (43) | 5 (2) | 0 |
| Тромбоцитопения | 97 (43) | 61 (27) | 7 (3) |
| Периферическая нейропатия | 84 (37) | 31 (14) | 0 |
| Лихорадка | 82 (36) | 9 (4) | 0 |
| Рвота | 82 (36) | 16 (7) | 1 (<1) |
| Анемия | 74 (32) | 21 (9) | 0 |
| Головная боль | 63 (28) | 8 (4) | 0 |
| Инсомния | 62 (27) | 3 (1) | 0 |
| Артралгия | 60 (26) | 11 (5) | 0 |
| Боль в конечностях | 59 (26) | 16 (7) | 0 |
| Отек | 58 (25) | 3 (1) | 0 |
| Нейтропения | 55 (24) | 30 (13) | 6 (3) |
| Парестезия и дизестезия | 53 (23) | 6 (3) | 0 |
| Диспноэ | 50 (22) | 7 (3) | 1 (<1) |
| Головокружение (исключая вертиго) | 48 (21) | 3 (1) | 0 |
| Сыпь | 47 (21) | 1 (<1) | 0 |
| Обезвоживание | 42 (18) | 15 (7) | 0 |
| Инфекция верхних дыхательных путей | 41 (18) | 0 | 0 |
| Кашель | 39 (17) | 1 (<1) | 0 |
| Боль в костях | 33 (14) | 5 (2) | 0 |
| Тревога | 32 (14) | 0 | 0 |
| Миалгия | 32 (14) | 5 (2) | 0 |
| Боль в спине | 31 (14) | 9 (4) | 0 |
| Спазмы мышц | 31 (14) | 1 (<1) | 0 |
| Диспепсия | 30 (13) | 0 | 0 |
| Абдоминальная боль | 29 (13) | 5 (2) | 0 |
| Извращение вкуса | 29 (13) | 1 (<1) | 0 |
| Гипотензия | 27 (12) | 8 (4) | 0 |
| Озноб | 27 (12) | 1 (<1) | 0 |
| Herpes zoster | 26 (11) | 2 (<1) | 0 |
| Зуд | 26 (11) | 0 | 0 |
| Нечеткость зрения | 25 (11) | 1 (<1) | 0 |
| Пневмония | 23 (10) | 12 (5) | 0 |
Серьезные побочные эффекты. Серьезные побочные эффекты определяли как какой-либо случай. безотносительно причины. который имел результатом летальный исход. был угрожающим жизни. требовал госпитализации или продлевал текущую госпитализацию. приводя к значительной беспомощности или считающийся важным медицинским случаем.
Во время исследования серьезные побочные эффекты наблюдались у 113 (50%) из 228 пациентов. Наиболее общими серьезными побочными эффектами были лихорадка (7%). пневмония (7%). диарея (6%). рвота (5%). дегидратация (5%). тошнота (4%).
Побочные эффекты, отмеченные исследователями как обусловленные приемом лекарства и вызвавшие прекращение лечения, были отмечены у 18% пациентов. Поводом к прекращению приема лекарства послужили периферическая нейропатия (5%), тромбоцитопения (4%), диарея (2%), повышенная утомляемость (2%).
Были зафиксированы два летальных исхода. которые рассматривались исследователями как предположительно связанные с исследованием лекарства: один случай остановки сердца вследствие сердечно-легочной недостаточности и один случай - из-за дыхательной недостаточности.
Астенические состояния (повышенная утомляемость, общая слабость, недомогание). Астения была отмечена у 65% пациентов и в основном имела 1 и 2 степень выраженности. Первоначально повышенная утомляемость отмечалась наиболее часто в течение 1-го и 2-го циклов терапии. Астения 3 степени выраженности была отмечена у 18% пациентов. Прекратили лечение из-за возникновения повышенной утомляемости 2% пациентов.
Желудочно-кишечные эффекты, наблюдавшиеся у большинства пациентов. Тошнота, диарея, запор, рвота. Эффекты 3 и 4 степени выраженности отмечались у 21% и были определены как серьезные у 13% пациентов. Рвота и диарея были тяжелыми и имели 3 степень выраженности у 7%, 4 степень - менее чем у 1% пациентов. Прекратили лечение из-за расстройств ЖКТ 5% больных. Снижение аппетита (анорексия) была отмечена как побочный эффект у 43% пациентов (3 степени выраженности - 3%).
Тромбоцитопения при лечении бортезомибом наблюдалась у 43% пациентов. она характеризовалась дозозависимым снижением числа тромбоцитов в период применения бортезомиба (с 1 по 11 день) и возвращалась к исходному уровню в период перерыва (дни с 12 по 21) в каждом цикле. Число тромбоцитов снижалось на 40% по сравнению с исходным. Значения числа тромбоцитов составляли менее 50 тыс. клеток/мкл и менее 10 тыс. клеток/мкл у 27 и 3% пациентов соответственно. Прекратили лечение из-за тромбоцитопении вне зависимости от степени ее выраженности 4% больных.
Периферическая сенсорная нейропатия. Нейропатия, включая сенсорную и обострение периферической нейропатии, отмечалась в 37% случаев. Периферическая нейропатия 3 степени - у 14%, не было отмечено случаев нейропатии 4 степени. Начальные проявления или обострение предшествующей нейропатии отмечалось на протяжении цикла лечения. Нейропатия явилась причиной отмены препарата в 6% случаев. Более чем у 80% пациентов, участвовавших в исследовании, имелись признаки и симптомы периферической нейропатии по сравнению с исходным состоянием. Частота нейропатии 3 степени составила 5% (2 из 41 пациента) у людей без предшествующей нейропатии. Симптомы могут улучшаться или возвращаться к исходному уровню у некоторых пациентов при отмене препарата. Полная оценка зависимости развития этого вида токсичности от времени не проведена.
Лихорадка (>38 °C) отмечалась как побочный эффект у 36% пациентов и имела 3 степень выраженности у 4% пациентов.
Нейтропения встречалась у 26% больных и имела 3 степень выраженности в 13% случаев и 4 степень - в 3%. Частота фебрильной нейтропении составила <1%.
Гипотензия (включая сообщения об ортостатической гипотензии) отмечалась у 12% пациентов, большинство случаев были 1 и 2 степени выраженности, у 4% - 3 степени, ни у кого не было гипотензии 4 степени выраженности. Пациенты, у которых отмечалась ортостатическая гипотензия, не имели таковой в начале исследования, у половины больных была предшествующая гипертензия, у 1/3 - периферическая нейропатия. Дозы антигипертензивных препаратов могут быть скорректированы у пациентов, получающих бортезомиб. У 4% пациентов с гипотензией, включая ортостатическую, отмечались одновременно обморочные состояния.
Серьезные побочные эффекты во время клинических исследований. Примерно у 580 пациентов наблюдались следующие серьезные неблагоприятные эффекты (не описаны выше). рассматриваемые как возможно связанные с лечением и отмеченные по крайней мере у одного пациента. получавшего бортезомиб в качестве монотерапии или в комбинации с другими химиотерапевтическими средствами. Эти исследования были проведены у пациентов с гематологическими злокачественными новообразованиями и сoлидными опухолями.
Заболевания крови и лимфатической системы. Диссеминированная внутрисосудистая коагуляция.
Сердечные заболевания. Приступы фибрилляции предсердий. трепетание предсердий. сердечный амилоидоз. остановка сердца. застойная сердечная недостаточность. ишемия миокарда. инфаркт миокарда. перикардиальный выпот. отек легких. желудочковая тахикардия.
Заболевания ЖКТ. Асцит. дисфагия. фекалома. геморрагический гастрит. гематемезис. паралитическая непроходимость кишечника. обструкция толстого кишечника. обструкция тонкого кишечника. прободение тостой кишки. стоматит. мелена. острый панкреатит.
Гепатобилиарная система. Гипербилирубинемия, тромбоз портальной вены.
Иммунная система. Анафилактические реакции, реакции гиперчувствительности.
Инфекции и инвазии. Бактериемия.
Повреждение, отравление, осложнения. Переломы, субдуральная гематома.
Метаболизм и обмен веществ. Гипокальциемия, гиперурикемия, гипокалиемия, гипонатриемия, синдром лизиса опухоли.
Нервная система. Атаксия. кома. головокружение. дизартрия. нарушение функций вегетативной нервной системы. паралич черепно-мозговых нервов. судорожные припадки типа grand mal. геморрагический инсульт. двигательные нарушения. компрессия спинного мозга. транзиторная ишемическая атака.
Психиатрия. Ажитация, спутанность сознания, психоз, суицидальные мысли.
Почки и мочевыводящие пути. Почечные камни. билатеральный гидронефроз. спазм мочевого пузыря. гематурия. недержание мочи. задержка мочеиспускания. почечная недостаточность (острая и хроническая). клубочковый пролиферативный нефрит.
Респираторная система. Острый респираторный дистресс-синдром. ателектаз. обострение хронической обструктивной болезни легких. дисфагия. диспноэ. одышка при физической нагрузке. носовое кровотечение. кровохарканье. гипоксия. инфильтрация легких. плевральный выпот. пневмонит. респираторный дистресс. дыхательная недостаточность.
Сосудистые. Цереброваскулярные нарушения, тромбоз глубоких вен, периферическая эмболия, легочная эмболия.
Interaction
В in vitro >in vitro исследованиях на микросомах печени человека показано, что бортезомиб является субстратом для изоферментов цитохрома Р450 сYP3A4, сYP2D6, сYP2C19, сYP2C9, сYP1A2. За состоянием пациентов, получающих одновременно бортезомиб и ЛС, являющиеся ингибиторами или индукторами сYP3A4, следует тщательно наблюдать ввиду возможности токсического действия или снижения эффективности терапии. Во время клинических испытаний сообщалось о гипогликемии и гипергликемии у пациентов с сахарным диабетом, принимавших пероральные гипогликемические средства. У пациентов, принимающих одновременно бортезомиб и пероральные гипогликемические ЛС, может потребоваться мониторинг уровня глюкозы в крови и корректировка дозы гипогликемического средства.
Бортезомиб является слабым ингибитором микросомальных печеночных изоферментов цитохрома Р450 - сYP1A2, сYP2C9, сYP2D6, сYP3А4 с 50IC5030 μM (>11,5 мкг/мл). Бортезомиб может ингибировать активность сYP2C19 (IC50=18 μM; 6,9 мкг/мл) и увеличивать экспозицию веществ, которые являются субстратом для этого фермента. Бортезомиб не индуцирует активность сYP3A4 и сYP1А2 в первичной культуре человеческих гепатоцитов.
Бортезомиб является слабым ингибитором микросомальных печеночных изоферментов цитохрома Р450 - сYP1A2, сYP2C9, сYP2D6, сYP3А4 с 50IC5030 μM (>11,5 мкг/мл). Бортезомиб может ингибировать активность сYP2C19 (IC50=18 μM; 6,9 мкг/мл) и увеличивать экспозицию веществ, которые являются субстратом для этого фермента. Бортезомиб не индуцирует активность сYP3A4 и сYP1А2 в первичной культуре человеческих гепатоцитов.
Overdose
Описан один случай передозировки бортезомиба (превышение рекомендуемой дозы более чем в 2 раза) у больного с сепсисом, закончившийся летальным исходом.
Симптомы: острое развитие симптоматической гипотензии и тромбоцитопении.
Лечение. Контроль показателей гемодинамики, поддержание жизненно важных функций, симптоматическая терапия (в тч инфузионная терапия). Специфический антидот неизвестен.
Симптомы: острое развитие симптоматической гипотензии и тромбоцитопении.
Лечение. Контроль показателей гемодинамики, поддержание жизненно важных функций, симптоматическая терапия (в тч инфузионная терапия). Специфический антидот неизвестен.
Method of drug use and dosage
В/в. Рекомендуемая доза 1,3 мг/м2 в виде болюса в течение 3-5 с дважды в неделю в течение 2 нед (в 1, 4, 8 и 11 день) после 10-дневного перерыва (дни 12-21). Для длительной терапии более 8 циклов можно вводить препарат по стандартной схеме или в поддерживающем режиме - 1 раз в неделю в течение 4 нед (дни 1, 8, 15 и 22) после 13-дневного перерыва (дни 23-35). Между введением последовательных доз бортезомиба должно пройти не менее 72.
Application precautions
Бортезомиб может назначаться только врачом, имеющим опыт проведения противоопухолевой химиотерапии.
Периферическая нейропатия. При возникновении нейропатии ( см «Побочные действия»), преимущественно сенсорной (хотя отмечались и другие случаи, в тч смешанной сенсорно-моторной нейропатии), проводят поддерживающую терапию. У пациентов с предшествующими симптомами (нечувствительность, боль или жжение в руках или ногах) и/или признаками периферической нейропатии возможно обострение заболевания. Следует проводить наблюдение за пациентами для своевременного выявления таких симптомов, как ощущение жжения, гиперестезия, гипестезия, парестезия, дискомфорт или нейропатическая боль. При появлении новых или усилении имеющихся симптомов нейропатии может потребоваться снижение дозы и изменение режима дозирования.
Гипотензия. Поскольку терапия бортезомибом сопровождается развитием ортостатической гипотензии ( см «Побочные действия»), которая может наблюдаться в ходе терапии, то следует соблюдать осторожность при лечении больных, имевших в анамнезе эпизоды потери сознания, получающих гипотензивные ЛС, а также у больных с обезвоживанием на фоне диареи или рвоты.
При применении бортезомиба описано развитие или усиление имеющейся застойной сердечной недостаточности, к которой может предрасполагать задержка жидкости.
До начала и во время каждого цикла терапии необходимо проводить анализ крови с подсчетом лейкоцитарной формулы и числа тромбоцитов.
Тромбоцитопения обычно максимально выражена на 11-й день цикла, уровень тромбоцитов восстанавливается до исходного значения к следующему циклу ( см «Побочные действия»). При снижении числа тромбоцитов менее 25 тыс./мкл терапию следует приостановить, при восстановлении числа тромбоцитов - продолжить в уменьшенных дозах при тщательном сопоставлении возможной пользы и риска лечения. Имеются сообщения о гастроинтестинальных и интрацеребральных геморрагиях, ассоциированных с вызываемой бортезомибом тромбоцитопенией. Для лечения гематологической токсичности можно применять колониестимулирующие факторы, переливание тромбоцитарной и эритроцитарной массы.
Для профилактики тошноты и рвоты применяют противорвотные препараты, при возникновении диареи - противодиарейные ЛС, для профилактики или лечения обезвоживания - регидратационную терапию и поддержание водно-электролитного баланса. В связи с возможным развитием непроходимости кишечника следует проводить динамическое наблюдение за больными с запорами.
В связи с возможным развитием гиперурикемии, связанной с синдромом лизиса опухоли, во время терапии рекомендуется определять концентрацию мочевой кислоты и креатинина в сыворотке крови. Для профилактики гиперурикемии - обильное питье, при необходимости - аллопуринол и подщелачивание мочи. При терапии больных с амилоидозом следует проявлять осторожность, неизвестно влияние угнетения активности протеасомы при заболеваниях, сопровождающихся увеличением содержания белка.
При работе с препаратом следует соблюдать общепринятые правила обращения с цитотоксическими препаратами.
Некоторые побочные эффекты (повышенная утомляемость, головокружение, ортостатическая гипотензия, нарушение зрения), могут сказаться на способности управлять автомобилем и выполнять деятельность, требующую повышенной концентрации внимания и быстроты психомоторных реакций, поэтому следует соблюдать особую осторожность.
Периферическая нейропатия. При возникновении нейропатии ( см «Побочные действия»), преимущественно сенсорной (хотя отмечались и другие случаи, в тч смешанной сенсорно-моторной нейропатии), проводят поддерживающую терапию. У пациентов с предшествующими симптомами (нечувствительность, боль или жжение в руках или ногах) и/или признаками периферической нейропатии возможно обострение заболевания. Следует проводить наблюдение за пациентами для своевременного выявления таких симптомов, как ощущение жжения, гиперестезия, гипестезия, парестезия, дискомфорт или нейропатическая боль. При появлении новых или усилении имеющихся симптомов нейропатии может потребоваться снижение дозы и изменение режима дозирования.
Гипотензия. Поскольку терапия бортезомибом сопровождается развитием ортостатической гипотензии ( см «Побочные действия»), которая может наблюдаться в ходе терапии, то следует соблюдать осторожность при лечении больных, имевших в анамнезе эпизоды потери сознания, получающих гипотензивные ЛС, а также у больных с обезвоживанием на фоне диареи или рвоты.
При применении бортезомиба описано развитие или усиление имеющейся застойной сердечной недостаточности, к которой может предрасполагать задержка жидкости.
До начала и во время каждого цикла терапии необходимо проводить анализ крови с подсчетом лейкоцитарной формулы и числа тромбоцитов.
Тромбоцитопения обычно максимально выражена на 11-й день цикла, уровень тромбоцитов восстанавливается до исходного значения к следующему циклу ( см «Побочные действия»). При снижении числа тромбоцитов менее 25 тыс./мкл терапию следует приостановить, при восстановлении числа тромбоцитов - продолжить в уменьшенных дозах при тщательном сопоставлении возможной пользы и риска лечения. Имеются сообщения о гастроинтестинальных и интрацеребральных геморрагиях, ассоциированных с вызываемой бортезомибом тромбоцитопенией. Для лечения гематологической токсичности можно применять колониестимулирующие факторы, переливание тромбоцитарной и эритроцитарной массы.
Для профилактики тошноты и рвоты применяют противорвотные препараты, при возникновении диареи - противодиарейные ЛС, для профилактики или лечения обезвоживания - регидратационную терапию и поддержание водно-электролитного баланса. В связи с возможным развитием непроходимости кишечника следует проводить динамическое наблюдение за больными с запорами.
В связи с возможным развитием гиперурикемии, связанной с синдромом лизиса опухоли, во время терапии рекомендуется определять концентрацию мочевой кислоты и креатинина в сыворотке крови. Для профилактики гиперурикемии - обильное питье, при необходимости - аллопуринол и подщелачивание мочи. При терапии больных с амилоидозом следует проявлять осторожность, неизвестно влияние угнетения активности протеасомы при заболеваниях, сопровождающихся увеличением содержания белка.
При работе с препаратом следует соблюдать общепринятые правила обращения с цитотоксическими препаратами.
Некоторые побочные эффекты (повышенная утомляемость, головокружение, ортостатическая гипотензия, нарушение зрения), могут сказаться на способности управлять автомобилем и выполнять деятельность, требующую повышенной концентрации внимания и быстроты психомоторных реакций, поэтому следует соблюдать особую осторожность.
Included in the composition
- 91.7€ Boramilan (2 firms)
- 104.5€ Велмиб3.5 (2 firms)
- 136.3€ Бартизар (3 firms)
- 140-149.4€ Velcade (7 firms)
- 35-453.9€ BoramilanFS
- — Bortezol
- — Bortezomib (8 firms)
- — Verozomib (Верофарм ООО )
- — БОРАТЕРИН (Laboratorio Tuteur S.A.C.I.F.I.A. )
- — Бортезомиб (форма-II) (Hetero Labs Limited )
- — Бортезомиб Канон
- — Бортезомиб-Тева (2 firms)
- — Бортезомиб-промомед
- — Майборте
- — Милатиб (3 firms)