МКБ-10 коды
- МКБ-10
- C48.0 Злокачественное новообразование забрюшинного пространства
- C38.1 Злокачественное новообразование переднего средостения
- C49.5 Злокачественное новообразование соединительной и мягких тканей таза
- C49.9 Злокачественное новообразование соединительной и мягких тканей неуточненной локализации
- C62 Злокачественное новообразование яичка
- C62.1 Злокачественное новообразование опущенного яичка
- C49.0 Злокачественное новообразование соединительной и мягких тканей головы, лица и шеи
- C62.9 Злокачественное новообразование яичка неуточненное
|
|
Вступление
Кодирование по Международной статистической классификации болезней и проблем, связанных со здоровьем: с38.1, с48.0, с49.0, с49.5, с49.9, с62, с62.0, с62.1, с62.9.
Год утверждения (частота пересмотра): 2020.
Возрастная категория: Дети.
Пересмотр не позднее: 2022.
ID: 69.
Разработчик клинической рекомендации.
• Национальное общество детских гематологов, онкологов.
Одобрено Научно-практическим Советом Минздрава РФ.
Год утверждения (частота пересмотра): 2020.
Возрастная категория: Дети.
Пересмотр не позднее: 2022.
ID: 69.
Разработчик клинической рекомендации.
• Национальное общество детских гематологов, онкологов.
Одобрено Научно-практическим Советом Минздрава РФ.
|
|
 Список сокращений
Список сокращений
АЛТ - аланинаминотрансфераза.
АСТ - аспартатаминотрансфераза.
АФП - альфа-фетопротеин.
β-ХГЧ - β-хорионического гонадотропина человека.
БАК - биохимический анализ крови.
ВОЗ - Всемирная организация здравоохранения.
ГКО - герминогенно-клеточные опухоли.
ДНК - дезоксирибонуклеиновая кислота.
ИФА - иммуноферментный анализ.
КТ - компьютерная томография.
ЛДГ - лактатдегидрогеназа.
МРТ - магнитно-резонансная томография.
МСКТ - мультиспиральная компьютерная томография.
МТС - метастатическое поражение.
ПХТ - полихимиотерапия.
ПЭТ - позитронно-эмиссионная томография.
СРП - С-реактивный протеин.
УЗИ - ультразвуковое исследование.
ФСГ - фолликулостимулирующий гормон.
ЭКГ - электрокардиограмма.
PEI - cisplatin, etoposide, ifosfamide (цисплатин, этопозид, ифосфамид).
BEP - bleomycin, etoposide, cisplatin (блеомицин, этопозид, цисплатин).
EC - эмбриональная карцинома.
ChCa - хориокарцинома.
GI - GIII - степень злокачественности незрелой тератомы.
SIOP - Международное общество детских онкологов.
TNM - Международная классификация по стадированию злокачественных опухолей.
YST - опухоль желточного мешка.
АСТ - аспартатаминотрансфераза.
АФП - альфа-фетопротеин.
β-ХГЧ - β-хорионического гонадотропина человека.
БАК - биохимический анализ крови.
ВОЗ - Всемирная организация здравоохранения.
ГКО - герминогенно-клеточные опухоли.
ДНК - дезоксирибонуклеиновая кислота.
ИФА - иммуноферментный анализ.
КТ - компьютерная томография.
ЛДГ - лактатдегидрогеназа.
МРТ - магнитно-резонансная томография.
МСКТ - мультиспиральная компьютерная томография.
МТС - метастатическое поражение.
ПХТ - полихимиотерапия.
ПЭТ - позитронно-эмиссионная томография.
СРП - С-реактивный протеин.
УЗИ - ультразвуковое исследование.
ФСГ - фолликулостимулирующий гормон.
ЭКГ - электрокардиограмма.
PEI - cisplatin, etoposide, ifosfamide (цисплатин, этопозид, ифосфамид).
BEP - bleomycin, etoposide, cisplatin (блеомицин, этопозид, цисплатин).
EC - эмбриональная карцинома.
ChCa - хориокарцинома.
GI - GIII - степень злокачественности незрелой тератомы.
SIOP - Международное общество детских онкологов.
TNM - Международная классификация по стадированию злокачественных опухолей.
YST - опухоль желточного мешка.

Термины и определения
Безрецидивная выживаемость (БРВ). От момента наступления ремиссии до момента возникновения рецидива.
Общая выживаемость (ОВ). От начала лечения до окончания исследования или смерти пациента.
Полихимиотерапия. Схема введения нескольких химиопрепаратов, в которой учитывается доза, кратность, дни и способ введения лекарственного препарата.
Общая выживаемость (ОВ). От начала лечения до окончания исследования или смерти пациента.
Полихимиотерапия. Схема введения нескольких химиопрепаратов, в которой учитывается доза, кратность, дни и способ введения лекарственного препарата.
Описание
Герминогенно-клеточные опухоли (ГКО) происходят из плюрипотентных зародышевых клеток и представляют собой гетерогенную группу новообразований с различной гистологической картиной, локализацией, клиническим течением и прогнозом [1]. Нарушения дифференцировки этих клеток приводят к возникновению эмбриональной карциномы и тератомы (эмбриональная линия дифференцировки) или хориокарциномы и опухоли желточного мешка (экстраэмбриональный путь дифференцировки). Нарушение развития унипотентных примитивных зародышевых клеток приводит к развитию герминомы. ГКО могут возникать как в половых органах, так и вне их. Внегонадные ГКО локализуются по срединной линии тела, вдоль пути миграции примордиальных зародышевых клеток.
Микроскопически тотальная (R0):
• полная резекция опухоли единым блоком с органом происхождения, полностью с копчиковой костью или всего яичка, или всего яичника с фаллопиевой трубой;
• нет предыдущей биопсии;
• опухолевая киста не подвергалась пункции и не было разрыва во время операции с излитием содержимого;
• при гистологической оценке - капсула или псевдокапсула опухоли свободны от опухолевых клеток (отсутствие опухолевых клеток в крае резекции);
• нет опухолевых клеток в асцитической или лаважной абдоминальной жидкости.
Макроскопически тотальная, микроскопически резидуальная (R1):
• удаление всей опухоли несколькими частями, удаление опухоли при повторной операции;
• резекция копчиковой кости, яичника или яичка отдельными частями;
• трансcкротальная хирургия тестикулярных опухолей;
• нарушение целостности опухолевой капсулы, например при разрыве опухоли, пункции опухолевой кисты, или интраоперационная биопсия для гистологического исследования;
• опухолевые клетки в асцитическом или плевральном экссудате;
• опухолевые клетки на поверхности органа или в крае резекции.
Макроскопически остаточная (R2):
• энуклеация опухоли из органа с оставлением органа: всей копчиковой кости, яичника или яичка;
• остатки видимой опухоли или инфильтрация тканей;
• метастатические остатки в пределах хирургического поля, например перитонеальные импланты (исключая глиоматоз) или метастатическое поражение региональных лимфатических узлов. Исключены отдаленные метастазы в легкие, печень или другие участки;
• жидкая консистенция опухоли.
Образование псевдокапсулы возникает вследствие компрессии опухоли соседними структурами. Только достаточное и безопасное расстояние гарантирует возможность полного удаления опухоли.
Если ткань опухоли ограничена нечетко, обязательно отдельное исследование срезов за пределами подозрительной области для гистологического уточнения, независимо от того, замечена инвазия опухоли или нет хирургом.
Необходимо удаление и маркировка всех лимфоузлов для последующей гистологической верификации.
Определение понятий полной или неполной резекции опухоли.
Под полной резекцией понимают удаление всего объема опухолевой ткани:
• при опухолях, локализованных в области копчика, проводится резекция опухоли, капсулы и копчика в одном блоке;
• при опухолях яичника должны быть резицированы яичник, придаток яичника и фаллопиева труба;
• также для правильного стадирования, если необходимо, удаляются регионарные лимфатические узлы.
Под неполной резекцией понимают, такую резекцию, если:
• во время или после операции произошел разрыв капсулы;
• обнаружена инфильтрация опухоли в окружающие ткани или наблюдается прилегание (срастание) опухоли к (с) окружающей ткани, в результате которой, полная резекция опухоли невозможна.
При инфильтрации опухоли в окружающую ткань необходимо выполнение гистологического исследования ткани в краях резекции.
Опухолевая псевдокапсула появляется в результате сдавления опухолью прилегающих структур. Только достаточная и безопасная дистанция гарантирует возможность полного удаления опухоли. Если возможна полная резекция опухоли, и точно диагностирована 1а стадия заболевания, на этом этапе лечение может быть завершено, в случае поражения яичника или другой экстракраниальной локализации, за исключением крестцово-копчиковой локализации. Однако такие пациенты должны тщательно наблюдаться в строго установленные сроки.
Опухоли с локализацией в крестцово-копчиковой области часто презентируют в виде огромной массы. Наиболее удобен дорзальный доступ. Инфильтрированные участки кожи должны быть удалены единым блоком вместе с опухолью, так как последующее закрытие кожей операционного поля не проблематично. Отделение опухоли от прямой кишки возможно при пальцевом контроле. После операции функции кишки и мочевого пузыря обычно восстанавливаются. Резекция копчика вместе с опухолью является абсолютно обязательной при копчиковых локализациях. Копчиковая кость должна быть удалена в едином блоке с опухолью для избежания разрыва опухоли.
При IV типе ККО по Альтаману (огромная опухолевая часть находится в малом тазу, включая копчиковую область) - необходимо обсудить проведение предоперационной химиотерапии до оперативного вмешательства в случае секретирующей ГКО. В этом случае для достижения радикального удаления опухоли единым блоком полезным является дополнительный вентральный доступ.
Таким образом при локализации в крестцово-копчиковой области опухоль должна быть удалена единым блоком с копчиковой костью, что предотвращает развитие рецидива в большинстве случаев. При зрелой тератоме и в некоторых случаях злокачественной ГКО достаточно проведения радикальной операции и обеспечения последующего тщательного диспансерного наблюдения.
Опухоли яичников.
При опухолях яичников лучший интраоперационный обзор дает абдоминальный доступ через срединную линию, чем традиционный доступ. Абсолютно важно при опухолях яичников первоначально лигировать яичниковые вены и артерии, чтобы избежать диссеминации опухолевых клеток. Придатки инфильтрированного участка должны быть удалены тотально в блоке с опухолью.
Для интраоперационного стадирования важным являются точный размер опухоли, точная идентификация и цитология интраперитонеальной жидкости, а также обследование контралатерального участка. Необходимо провести биопсию всех подозрительных участков и отдаленных лимфатических узлов.
Пациенты с герминомой яичника с кариотипом XY должны быть обсуждены в дальнейшем в отношении удаления контралатерального яичника.
Опухоли яичек.
ВНИМАНИЕ. При выявлении новообразования яичка противопоказано применение трансскротального доступа. Целесообразно использование пахового доступа с лигированием семенного канатика.
Другие локализации.
Хирургический доступ к другим местам первичных локализаций, таких, как средостение, забрюшинное пространство, должен быть запланирован в соответствии с выявленной ситуацией.
Изолированные ретроперитонеальные опухоли лучше всего лечить аналогично опухолям копчика.
Большинство опухолей средостения типично располагаются в переднем средостении, вызывая клинические симптомы вследствие смещения соседних структур. Оперативным доступом в основном является правосторонняя торакотомия, иногда - стернотомия.
В некоторых случаях отделение опухоли от крупных сосудов или ворот легких является проблематичным. Поэтому весьма важна анатомическая информация, полученная с помощью визуализирующих методов, таких как КТ- или МРТ-сканирование.
Если при КТ- или МРТ-сканировании выявлена инфильтрация в окружающую ткань или метастазы в лимфоузлы или печень, легкие , первым терапевтическим шагом будет первичная химиотерапия после клинической диагностики с помощью опухолевых маркеров.
При инфильтрирующем росте «не секретирующей» ( уровень АФП и β-ХГЧ не повышен) опухоли для подтверждения гистологического диагноза необходимо выполнить биопсию.
Биопсия.
Биопсия опухоли сопровождается риском диссеминации опухолевых клеток. Поэтому биопсия показана только тогда, когда диагностируется массивный предоперационный инфильтрат при отсутствии возможности полного удаления, а опухоль не показывает никаких опухолевых маркеров. Тогда вид опухоли может быть диагностирован только гистологически. В этом случае важно избежать осложнений во время биопсии. Это означает безопасную обработку окружающей ткани, а также определение границы, затронутой опухолевым поражением.
ЗРЕЛАЯ (G 0) и не зрелая тератома (G 1-2), злокачественная тератома (G 3).
(классификация «Grad» по Гонзалес-Крузи).
Примечание. Тератома яичника с глиоматозом брюшины - FIGO 1с - только операция с последующим ежемесячным наблюдением.
• YST яичка IA стадии после R0 у детей в возрасте до 2 лет жизни.
• Опухоли яичника I cтадии после радикально выполненной операции при регулярном наблюдении (известно, что из этой группы пациентов нуждаются в дальнейшем в ХТ только 25 % по случаю рецидива. Отсроченная ХТ не приводит к ухудшению выживаемости в данной группе, в то время, как 75 % не получат токсичность, связанную с проведением ХТ) [20].
6,3,3. ТЕРАПИЯ НЕГОНАДНЫХ ЗЛОКАЧЕСТВЕННЫХ ГКО [11].
Схемы лечения - см приложение А3,1.
Увеличение количества циклов при отсутствии ответа на терапию в виде сокращения опухоли и/или нормализации опухолевых маркеров не приводит к выздоровлению или профилактики рецидива.
Эти пациенты нуждаются в проведении другой терапии вне клинических рекомендаций.
Пациенты старше 10 лет со злокачественной негонадной ГКО с поражением региональных лимфоузлов и отдаленными метастазами имеют наихудший прогноз. После проведения биопсии и 1 курса ХТ (в целях сдерживания опухоли) должны быть обсуждены с Федеральным центром в целях интенсификации терапии вне клинических рекомендаций.
6,3,4. ТЕРАПИЯ ЗЛОКАЧЕСТВЕННЫХ ГЕРМИНОГЕННО-КЛЕТОЧНЫХ ОПУХОЛЕЙ ЯИЧКА [11].
Схемы лечения - см приложение А3,1.
• пациенты с инвазией опухоли в лимфоузлы или сосуды должны лечиться по высокой группе риска (с ифосфамидом**);
• при задержке ответа на лечение - обсуждение пациента;
• объем опухоли неизменный / нарастающие опухолевые маркеры - «growing teratoma syndrom» - скорейшая операция;
• объем опухоли неизменный / нарастающие опухолевые маркеры или замедлена нормализация маркеров / прогрессия - менять группу риска;
• пациенты с R1-2 резекцией опухоли и/или «живой» опухолью после 2nd look - интенсификация терапии вне клинических рекомендаций;
• подростки с тератомой яичка обсуждаются для проведения ХТ, так как у этой группы пациентов высокий риск отдаленных отсроченных рецидивов.
6,3,5 ТЕРАПИЯ ЗЛОКАЧЕСТВЕННЫХ ГЕРМИНОГЕННО-КЛЕТОЧНЫХ ОПУХОЛЕЙ ЯИЧНИКОВ [11].
Схемы лечения - см приложение А3,1.
• при гепатоидной или эндометриоидной дифференциации YST, терапия проводится по более высокой группе риска (при стадиях III и IV - по терапии высокой группы риска негонадальных ГКО;
• пациенты с FIGO 1 и наличием опухоли в лимфоузлах, сосудах должны лечиться по более высокой группе риска - FIGO 2;
• при замедленном ответе - обсуждение пациента;
• объем опухоли неизменный / нарастающие опухолевые маркеры - «growing teratoma s yndrome» - скорейшая операция;
• объем опухоли неизменный / нарастающие опухолевые маркеры или замедлена нормализация маркеров / прогрессия - менять группу риска;
• Пациенты с R1-2 резекцией опухоли и/или «живой» опухолью после 2nd look - интенсификация терапии вне клинических рекомендаций.
• Отсутствие клинических признаков болезни;
• Отсутствие опухоли по данным визуализации с контрастным усилением.
• Нормальный уровень опухолевых онкомаркеров (АФП, β-ХГЧ).
Частичный ответ (PR).
• Уменьшение объема первичной опухоли, и очагов метастатического поражения более чем на 50 % (по максимальным размерам); в случае если единственным проявлением заболевания являлись высокие цифры онкомаркеров - снижение уровня на 90 % и более.
• Отсутствие новых очагов опухолевого роста.
• Нормальный уровень опухолевых онкомаркеров (АФП, β-ХГЧ).
Стабилизация болезни (SD).
• Уменьшение объема первичной опухоли и очагов метастатического поражения менее чем на 50 % суммы объема всех измеряемых поражений.
• Отсутствие новых очагов опухолевого роста.
• Нет динамики/либо незначительное снижение опухолевых маркеров (АФП или β-ХГЧ).
Прогрессирование болезни (PD).
• Увеличение более чем на 25 % размера любого из измеряемых поражений.
• Появление новых очагов опухолевого роста.
• Повышение уровня онкомаркеров (исключая первую неделю ХТ).
Микроскопически тотальная (R0):
• полная резекция опухоли единым блоком с органом происхождения, полностью с копчиковой костью или всего яичка, или всего яичника с фаллопиевой трубой;
• нет предыдущей биопсии;
• опухолевая киста не подвергалась пункции и не было разрыва во время операции с излитием содержимого;
• при гистологической оценке - капсула или псевдокапсула опухоли свободны от опухолевых клеток (отсутствие опухолевых клеток в крае резекции);
• нет опухолевых клеток в асцитической или лаважной абдоминальной жидкости.
Макроскопически тотальная, микроскопически резидуальная (R1):
• удаление всей опухоли несколькими частями, удаление опухоли при повторной операции;
• резекция копчиковой кости, яичника или яичка отдельными частями;
• трансcкротальная хирургия тестикулярных опухолей;
• нарушение целостности опухолевой капсулы, например при разрыве опухоли, пункции опухолевой кисты, или интраоперационная биопсия для гистологического исследования;
• опухолевые клетки в асцитическом или плевральном экссудате;
• опухолевые клетки на поверхности органа или в крае резекции.
Макроскопически остаточная (R2):
• энуклеация опухоли из органа с оставлением органа: всей копчиковой кости, яичника или яичка;
• остатки видимой опухоли или инфильтрация тканей;
• метастатические остатки в пределах хирургического поля, например перитонеальные импланты (исключая глиоматоз) или метастатическое поражение региональных лимфатических узлов. Исключены отдаленные метастазы в легкие, печень или другие участки;
• жидкая консистенция опухоли.
Образование псевдокапсулы возникает вследствие компрессии опухоли соседними структурами. Только достаточное и безопасное расстояние гарантирует возможность полного удаления опухоли.
Если ткань опухоли ограничена нечетко, обязательно отдельное исследование срезов за пределами подозрительной области для гистологического уточнения, независимо от того, замечена инвазия опухоли или нет хирургом.
Необходимо удаление и маркировка всех лимфоузлов для последующей гистологической верификации.
Определение понятий полной или неполной резекции опухоли.
Под полной резекцией понимают удаление всего объема опухолевой ткани:
• при опухолях, локализованных в области копчика, проводится резекция опухоли, капсулы и копчика в одном блоке;
• при опухолях яичника должны быть резицированы яичник, придаток яичника и фаллопиева труба;
• также для правильного стадирования, если необходимо, удаляются регионарные лимфатические узлы.
Под неполной резекцией понимают, такую резекцию, если:
• во время или после операции произошел разрыв капсулы;
• обнаружена инфильтрация опухоли в окружающие ткани или наблюдается прилегание (срастание) опухоли к (с) окружающей ткани, в результате которой, полная резекция опухоли невозможна.
При инфильтрации опухоли в окружающую ткань необходимо выполнение гистологического исследования ткани в краях резекции.
Опухолевая псевдокапсула появляется в результате сдавления опухолью прилегающих структур. Только достаточная и безопасная дистанция гарантирует возможность полного удаления опухоли. Если возможна полная резекция опухоли, и точно диагностирована 1а стадия заболевания, на этом этапе лечение может быть завершено, в случае поражения яичника или другой экстракраниальной локализации, за исключением крестцово-копчиковой локализации. Однако такие пациенты должны тщательно наблюдаться в строго установленные сроки.
6,2 Оперативные методики при ГКО.
Крестцово-копчиковая локализация.Опухоли с локализацией в крестцово-копчиковой области часто презентируют в виде огромной массы. Наиболее удобен дорзальный доступ. Инфильтрированные участки кожи должны быть удалены единым блоком вместе с опухолью, так как последующее закрытие кожей операционного поля не проблематично. Отделение опухоли от прямой кишки возможно при пальцевом контроле. После операции функции кишки и мочевого пузыря обычно восстанавливаются. Резекция копчика вместе с опухолью является абсолютно обязательной при копчиковых локализациях. Копчиковая кость должна быть удалена в едином блоке с опухолью для избежания разрыва опухоли.
При IV типе ККО по Альтаману (огромная опухолевая часть находится в малом тазу, включая копчиковую область) - необходимо обсудить проведение предоперационной химиотерапии до оперативного вмешательства в случае секретирующей ГКО. В этом случае для достижения радикального удаления опухоли единым блоком полезным является дополнительный вентральный доступ.
Таким образом при локализации в крестцово-копчиковой области опухоль должна быть удалена единым блоком с копчиковой костью, что предотвращает развитие рецидива в большинстве случаев. При зрелой тератоме и в некоторых случаях злокачественной ГКО достаточно проведения радикальной операции и обеспечения последующего тщательного диспансерного наблюдения.
Опухоли яичников.
При опухолях яичников лучший интраоперационный обзор дает абдоминальный доступ через срединную линию, чем традиционный доступ. Абсолютно важно при опухолях яичников первоначально лигировать яичниковые вены и артерии, чтобы избежать диссеминации опухолевых клеток. Придатки инфильтрированного участка должны быть удалены тотально в блоке с опухолью.
Для интраоперационного стадирования важным являются точный размер опухоли, точная идентификация и цитология интраперитонеальной жидкости, а также обследование контралатерального участка. Необходимо провести биопсию всех подозрительных участков и отдаленных лимфатических узлов.
Пациенты с герминомой яичника с кариотипом XY должны быть обсуждены в дальнейшем в отношении удаления контралатерального яичника.
Опухоли яичек.
ВНИМАНИЕ. При выявлении новообразования яичка противопоказано применение трансскротального доступа. Целесообразно использование пахового доступа с лигированием семенного канатика.
Другие локализации.
Хирургический доступ к другим местам первичных локализаций, таких, как средостение, забрюшинное пространство, должен быть запланирован в соответствии с выявленной ситуацией.
Изолированные ретроперитонеальные опухоли лучше всего лечить аналогично опухолям копчика.
Большинство опухолей средостения типично располагаются в переднем средостении, вызывая клинические симптомы вследствие смещения соседних структур. Оперативным доступом в основном является правосторонняя торакотомия, иногда - стернотомия.
В некоторых случаях отделение опухоли от крупных сосудов или ворот легких является проблематичным. Поэтому весьма важна анатомическая информация, полученная с помощью визуализирующих методов, таких как КТ- или МРТ-сканирование.
Если при КТ- или МРТ-сканировании выявлена инфильтрация в окружающую ткань или метастазы в лимфоузлы или печень, легкие , первым терапевтическим шагом будет первичная химиотерапия после клинической диагностики с помощью опухолевых маркеров.
При инфильтрирующем росте «не секретирующей» ( уровень АФП и β-ХГЧ не повышен) опухоли для подтверждения гистологического диагноза необходимо выполнить биопсию.
Биопсия.
Биопсия опухоли сопровождается риском диссеминации опухолевых клеток. Поэтому биопсия показана только тогда, когда диагностируется массивный предоперационный инфильтрат при отсутствии возможности полного удаления, а опухоль не показывает никаких опухолевых маркеров. Тогда вид опухоли может быть диагностирован только гистологически. В этом случае важно избежать осложнений во время биопсии. Это означает безопасную обработку окружающей ткани, а также определение границы, затронутой опухолевым поражением.
6,3 Терапевтические опции после оперативного лечения.
6,3,1. ЧИСТАЯ» ТЕРАТОМА И ТЕРАТОМА С МИКРОФОКУСАМИ.ЗРЕЛАЯ (G 0) и не зрелая тератома (G 1-2), злокачественная тератома (G 3).
(классификация «Grad» по Гонзалес-Крузи).
| Резекция | Злокачественные микрофокусы | Группа риска | Терапия | |
| Гонадальные и негонадальные тератомы Grad 0-3 | R0 или R1 | Нет | Благоприятная | W&W каждые три месяца |
| Есть | неопределенная | W&W ежемесячно | ||
| R2 | Нет | неопределенная | W&W ежемесячно | |
| есть | неблагоприятная | Лечение как при злокачественных ГКО |
Примечание. Тератома яичника с глиоматозом брюшины - FIGO 1с - только операция с последующим ежемесячным наблюдением.
6,3,2 ПАЦИЕНТЫ НАБЛЮДЕНИЯ.
• Тератомы (Grade 0-2) различной локализации после радикально выполненной операции при регулярном!!! контроле.• YST яичка IA стадии после R0 у детей в возрасте до 2 лет жизни.
• Опухоли яичника I cтадии после радикально выполненной операции при регулярном наблюдении (известно, что из этой группы пациентов нуждаются в дальнейшем в ХТ только 25 % по случаю рецидива. Отсроченная ХТ не приводит к ухудшению выживаемости в данной группе, в то время, как 75 % не получат токсичность, связанную с проведением ХТ) [20].
6,3,3. ТЕРАПИЯ НЕГОНАДНЫХ ЗЛОКАЧЕСТВЕННЫХ ГКО [11].
| TNM | ОПЕРАТИВНОЕ ЛЕЧЕНИЕ | ||
| T1a N0 M0 | R0 R1 R2 | w&w 3 * PEI 3 * PEI - (2nd look ) - 1 * PEI | |
| T1b N0 M0 | R0 R1 R2 | w&w 3 * PEI 3 * PEI - (2nd look ) 1 * PEI | |
| T2a / b N0 M0 | R0 R1 R2 | 4 * PEI 4 * PEI 3 * PEI - (2nd look ) 1 * PEI | |
| N1 или М1 у детей младше 10 лет | биопсия | 3 * PEI - OP - 1 * PEI | |
| N1 или М1 у детей старше 10 лет | биопсия | 1 * PEI - 3 * HD PEI - OP с поддержкой ауто-ТПСК | |
| Неполный ответ или интенсификация терапии: | 2 * сarbo-PET ауто-ТПСК | ||
Схемы лечения - см приложение А3,1.
Увеличение количества циклов при отсутствии ответа на терапию в виде сокращения опухоли и/или нормализации опухолевых маркеров не приводит к выздоровлению или профилактики рецидива.
Эти пациенты нуждаются в проведении другой терапии вне клинических рекомендаций.
Пациенты старше 10 лет со злокачественной негонадной ГКО с поражением региональных лимфоузлов и отдаленными метастазами имеют наихудший прогноз. После проведения биопсии и 1 курса ХТ (в целях сдерживания опухоли) должны быть обсуждены с Федеральным центром в целях интенсификации терапии вне клинических рекомендаций.
6,3,4. ТЕРАПИЯ ЗЛОКАЧЕСТВЕННЫХ ГЕРМИНОГЕННО-КЛЕТОЧНЫХ ОПУХОЛЕЙ ЯИЧКА [11].
| ВЫСОКАЯ ПАХОВАЯ ОРХИЭКТОМИЯ | LUGANO | I A | «чистая» YST | Watch. And - wait | |||
| I A | Другая / смешанная ГКО | 2 * PE | |||||
| I в | |||||||
| I с | |||||||
| II A | 2 * PEI | ПОВТОРНАЯ ОЦЕНКАПАЦИЕНТА | сR | STOP | |||
| PR | 2nd look | ||||||
| II в | 3 * PEI | сR | 1 * PEI | ||||
| II с | |||||||
| II D | |||||||
| IIIA | |||||||
| IIIB | PR | 2nd look + 1 * PEI | |||||
| IIIC | |||||||
| IIID | |||||||
Схемы лечения - см приложение А3,1.
• пациенты с инвазией опухоли в лимфоузлы или сосуды должны лечиться по высокой группе риска (с ифосфамидом**);
• при задержке ответа на лечение - обсуждение пациента;
• объем опухоли неизменный / нарастающие опухолевые маркеры - «growing teratoma syndrom» - скорейшая операция;
• объем опухоли неизменный / нарастающие опухолевые маркеры или замедлена нормализация маркеров / прогрессия - менять группу риска;
• пациенты с R1-2 резекцией опухоли и/или «живой» опухолью после 2nd look - интенсификация терапии вне клинических рекомендаций;
• подростки с тератомой яичка обсуждаются для проведения ХТ, так как у этой группы пациентов высокий риск отдаленных отсроченных рецидивов.
6,3,5 ТЕРАПИЯ ЗЛОКАЧЕСТВЕННЫХ ГЕРМИНОГЕННО-КЛЕТОЧНЫХ ОПУХОЛЕЙ ЯИЧНИКОВ [11].
| FIGO | Ia | удаление опухоли яичника | R0-R1 | Watch-and-wait | |||
| Ib | |||||||
| Ic | R2 | 2 * PE | 2nd look | ||||
| IIa | туморадренал эктомия | R0-R1 | 2 * PE | ||||
| Iib | |||||||
| Iic | R2 | 3 * PEI | 2nd look | 1 * PEI | |||
| IIIa | предоперационная ХТ | 3 * PEI | у даление яичника, удаление остаточной опухоли | 1 * PEI | |||
| IIIb | |||||||
| IIIc | |||||||
| IV | |||||||
Схемы лечения - см приложение А3,1.
• при гепатоидной или эндометриоидной дифференциации YST, терапия проводится по более высокой группе риска (при стадиях III и IV - по терапии высокой группы риска негонадальных ГКО;
• пациенты с FIGO 1 и наличием опухоли в лимфоузлах, сосудах должны лечиться по более высокой группе риска - FIGO 2;
• при замедленном ответе - обсуждение пациента;
• объем опухоли неизменный / нарастающие опухолевые маркеры - «growing teratoma s yndrome» - скорейшая операция;
• объем опухоли неизменный / нарастающие опухолевые маркеры или замедлена нормализация маркеров / прогрессия - менять группу риска;
• Пациенты с R1-2 резекцией опухоли и/или «живой» опухолью после 2nd look - интенсификация терапии вне клинических рекомендаций.
6,4 Критерии ответа.
Полный ответ (CR).• Отсутствие клинических признаков болезни;
• Отсутствие опухоли по данным визуализации с контрастным усилением.
• Нормальный уровень опухолевых онкомаркеров (АФП, β-ХГЧ).
Частичный ответ (PR).
• Уменьшение объема первичной опухоли, и очагов метастатического поражения более чем на 50 % (по максимальным размерам); в случае если единственным проявлением заболевания являлись высокие цифры онкомаркеров - снижение уровня на 90 % и более.
• Отсутствие новых очагов опухолевого роста.
• Нормальный уровень опухолевых онкомаркеров (АФП, β-ХГЧ).
Стабилизация болезни (SD).
• Уменьшение объема первичной опухоли и очагов метастатического поражения менее чем на 50 % суммы объема всех измеряемых поражений.
• Отсутствие новых очагов опухолевого роста.
• Нет динамики/либо незначительное снижение опухолевых маркеров (АФП или β-ХГЧ).
Прогрессирование болезни (PD).
• Увеличение более чем на 25 % размера любого из измеряемых поражений.
• Появление новых очагов опухолевого роста.
• Повышение уровня онкомаркеров (исключая первую неделю ХТ).
Причины
ГКО - это новообразования, развивающиеся из первичных половых клеток человеческого эмбриона, которые в норме формируют сперматозоиды и яйцеклетки [2].
Первичные половые клетки происходят из энтодермы желточного мешка и мигрируют вдоль задней кишки к урогенитальному гребню, где становятся частью развивающихся гонад. При нарушении процесса миграции по каким-то причинам зародышевые клетки могут задерживаться в любом месте на пути следования и вызывать опухолевый рост. Поэтому ГКО могут возникать как в половых органах, так и экстрагонадно, локализуясь по средней линии.
Наиболее часто ГКО у детей локализуются в яичках (25 %), яичниках (25 %), крестцово-копчиковой области (20 %) и головном мозге (20 %). К редким локализациям относятся средостение (в том числе - вилочковая железа), забрюшинное пространство, урогенитальный тракт, носоглотка, влагалище, мочевой пузырь, печень. При этом частота поражения различных органов зависит от возраста. Для новорожденных и детей первого года жизни характерно поражение крестцово-копчиковой области, составляющее около.
45 % всех ГКО в этом возрасте. У мальчиков до 2 лет чаще поражается яичко. ГКО половых органов нередко сочетаются с пороками развития (крипторхизм, дисгенезия гонад ).
ГКО метастазируют по сосудам в лимфатические узлы, легкие или печень.
При аномальной дифференцировке зародышевых клеток возникают различные гистологические варианты ГКО. В случае нарушения гонадной дифференцировки возникают герминомы, семиномы и дисгерминомы.
Нарушение соматической дифференцировки приводит к возникновению тератомы различной степени зрелости и эмбриональной карциномы, а экстраэмбриональной дифференцировки - к развитию опухоли желточного мешка и хориокарциномы.
Кроме так называемых «чистых вариантов» ГКО различают смешанные опухоли, состоящие из тканей более чем одного гистологического типа. Выделяют 4 степени зрелости тератомы (Т) в зависимости от содержания в тератоме незрелой эмбриональной ткани (классификации Gonzales-Crussi) [3].
Биологическая активность этих опухолей различна.
Первичные половые клетки происходят из энтодермы желточного мешка и мигрируют вдоль задней кишки к урогенитальному гребню, где становятся частью развивающихся гонад. При нарушении процесса миграции по каким-то причинам зародышевые клетки могут задерживаться в любом месте на пути следования и вызывать опухолевый рост. Поэтому ГКО могут возникать как в половых органах, так и экстрагонадно, локализуясь по средней линии.
Наиболее часто ГКО у детей локализуются в яичках (25 %), яичниках (25 %), крестцово-копчиковой области (20 %) и головном мозге (20 %). К редким локализациям относятся средостение (в том числе - вилочковая железа), забрюшинное пространство, урогенитальный тракт, носоглотка, влагалище, мочевой пузырь, печень. При этом частота поражения различных органов зависит от возраста. Для новорожденных и детей первого года жизни характерно поражение крестцово-копчиковой области, составляющее около.
45 % всех ГКО в этом возрасте. У мальчиков до 2 лет чаще поражается яичко. ГКО половых органов нередко сочетаются с пороками развития (крипторхизм, дисгенезия гонад ).
ГКО метастазируют по сосудам в лимфатические узлы, легкие или печень.
При аномальной дифференцировке зародышевых клеток возникают различные гистологические варианты ГКО. В случае нарушения гонадной дифференцировки возникают герминомы, семиномы и дисгерминомы.
Нарушение соматической дифференцировки приводит к возникновению тератомы различной степени зрелости и эмбриональной карциномы, а экстраэмбриональной дифференцировки - к развитию опухоли желточного мешка и хориокарциномы.
Кроме так называемых «чистых вариантов» ГКО различают смешанные опухоли, состоящие из тканей более чем одного гистологического типа. Выделяют 4 степени зрелости тератомы (Т) в зависимости от содержания в тератоме незрелой эмбриональной ткани (классификации Gonzales-Crussi) [3].
Биологическая активность этих опухолей различна.
|
|
Эпидемиология
ГКО составляют менее 3 % всех злокачественных новообразований у детей. При этом биологические особенности герминогенных опухолей отличаются в различных возрастных группах [4].
ГКО относятся к редким видам опухолей у детей, и составляют 3-4 % всех злокачественных новообразований у детей в возрасте до от 0-15 лет.
Достоверных эпидемиологических данных по ГКО у детей и подростков в России в настоящее время нет.
По данным немецкого детского регистра опухолей, тератомы составляют 48,2 % случаев, опухоли желточного мешка - 19,1 %, смешанные ГКО - 18 %; герминомы - 12,2 %; эмбриональные карциномы - 1,6 %; хориокарциномы - 0,9 %.
Чаще определяется зрелая тератома (54,5 %), реже - злокачественная тератома (7,8 %). Зрелая тератома имеет наилучший прогноз. Хориокарцинома является наиболее агрессивной ГКО, поэтому пациенты без лечения имеют самую короткую прогнозируемую выживаемость.
Для детей первого года жизни характерны внегонадные герминогенные опухоли, большинство из которых представлено тератомами. Тератомы содержат элементы всех трех зародышевых листков (эктодермы, эндодермы и мезодермы). Зрелая тератома состоит из хорошо дифференцированных тканей. Незрелая тератома подразделяется на три гистологических подтипа в зависимости от содержания незрелой нейроглиальной или бластемной тканей. Тератомы - как зрелая, так и незрелая - могут содержать элементы различных ГКО, а в редких случаях также элементы других опухолей (нейробластомы, ретинобластомы). Наиболее часто тератомы локализуются в крестцово-копчиковой области. У детей второго полугодия жизни начинают преобладать YST. В неонатальный период заболеваемость ГКО составляет у девочек 2,6 на 100 000; у мальчиков 0,9 на 100 000. Затем, заболеваемость ГКО уменьшается, и составляет у подростков менее 0,1 на 100 000. Тестикулярная локализация встречается в младенческом возрасте, второй пик заболеваемости отмечается у подростков. У юношей 14 % ГКО имеют тестикулярную локализацию. Уровень заболеваемости у них в этот период составляет 7-8 на 100 000.
• С48,0. Злокачественное новообразование забрюшинного пространства.
• С49,0. Злокачественное новообразование соединительной и мягких тканей головы, лица и шеи.
• С49,5. Злокачественное новообразование соединительной и мягких тканей таза.
• С49,9 - злокачественное новообразование соединительной и мягких тканей неуточненной локализации.
• С62. Злокачественное новообразование яичка.
• С62,0 - неопустившегося яичка.
• С62,1 - опущенного яичка.
• С62,9 - яичка неуточненное.
ГКО относятся к редким видам опухолей у детей, и составляют 3-4 % всех злокачественных новообразований у детей в возрасте до от 0-15 лет.
Достоверных эпидемиологических данных по ГКО у детей и подростков в России в настоящее время нет.
По данным немецкого детского регистра опухолей, тератомы составляют 48,2 % случаев, опухоли желточного мешка - 19,1 %, смешанные ГКО - 18 %; герминомы - 12,2 %; эмбриональные карциномы - 1,6 %; хориокарциномы - 0,9 %.
Чаще определяется зрелая тератома (54,5 %), реже - злокачественная тератома (7,8 %). Зрелая тератома имеет наилучший прогноз. Хориокарцинома является наиболее агрессивной ГКО, поэтому пациенты без лечения имеют самую короткую прогнозируемую выживаемость.
Для детей первого года жизни характерны внегонадные герминогенные опухоли, большинство из которых представлено тератомами. Тератомы содержат элементы всех трех зародышевых листков (эктодермы, эндодермы и мезодермы). Зрелая тератома состоит из хорошо дифференцированных тканей. Незрелая тератома подразделяется на три гистологических подтипа в зависимости от содержания незрелой нейроглиальной или бластемной тканей. Тератомы - как зрелая, так и незрелая - могут содержать элементы различных ГКО, а в редких случаях также элементы других опухолей (нейробластомы, ретинобластомы). Наиболее часто тератомы локализуются в крестцово-копчиковой области. У детей второго полугодия жизни начинают преобладать YST. В неонатальный период заболеваемость ГКО составляет у девочек 2,6 на 100 000; у мальчиков 0,9 на 100 000. Затем, заболеваемость ГКО уменьшается, и составляет у подростков менее 0,1 на 100 000. Тестикулярная локализация встречается в младенческом возрасте, второй пик заболеваемости отмечается у подростков. У юношей 14 % ГКО имеют тестикулярную локализацию. Уровень заболеваемости у них в этот период составляет 7-8 на 100 000.
1,4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем.
• С38,1- злокачественное новообразование переднего средостения.• С48,0. Злокачественное новообразование забрюшинного пространства.
• С49,0. Злокачественное новообразование соединительной и мягких тканей головы, лица и шеи.
• С49,5. Злокачественное новообразование соединительной и мягких тканей таза.
• С49,9 - злокачественное новообразование соединительной и мягких тканей неуточненной локализации.
• С62. Злокачественное новообразование яичка.
• С62,0 - неопустившегося яичка.
• С62,1 - опущенного яичка.
• С62,9 - яичка неуточненное.
Классификация
1,5 Классификация заболевания или состояния (группы заболеваний или состояний).
1,5,1 Гистологическая классификация герминогенно-клеточных опухолей ВОЗ (Mostofi, Talerman) + классификации Gonzales-Crussi для тератом [3]:
- тератома.G0 - зрелая тератома (не содержит эмбриональной ткани),.
G1 - незрелая тератома (эмбриональной ткани менее 10 %),.
G2 - незрелая тератома (эмбриональной ткани 11-49 %),.
G3 - злокачественная тератома (содержит более 50 % эмбриональной ткани);
- герминома (семинома яичка, дисгерминома яичника);
- опухоль желточного мешка (YST);
- эмбриональная карцинома (EC);
- хориокарцинома (ChCa).
Различные гистологические варианты могут проявляться как в чистой форме, так и в виде смешанных опухолей.
Встречаются гистологические варианты тератомы со злокачественным соматическим вариантом ( + карцинома, панкреатическая нервно-эндокринная опухоль, нейробластома, рабдомиосаркома, рабдомиосаркома + липосаркома, хондросаркома, нейрогенная саркома, хондросаркома + нейроэктодермальная саркома, злокачественная периферическая нервная оболочечная (sheath) опухоль), с более худшим прогнозом.
1,5,2 Стадирование ГКО.
ЭКСТРАГОНАДНЫЕ ЛОКАЛИЗАЦИИ. TNM (до лечения, после операции).
| TNM | |
| ТХ | первичная опухоль не может быть оценена |
| Т0 | нет данных о первичной опухоли |
| Т1 | опухоль ограничена органом |
| Т1а | опухоль диаметром ≤ 5 см |
| Т1 b | опухоль диаметром better 5 см |
| T2 | инфильтрация соседних органов |
| T2a | ≤ 5 см |
| T2b | > 5 см |
| N | регионарные лимфоузлы |
| NX | недостаточно данных для оценки состояния регионарных лимфоузлов |
| N0 | нет признаков поражения регионарных лимфоузлов |
| N1 | региональные лимфоузлы поражены |
| M | отдаленные метастазы: |
| М X | недостаточно данных для определения отдаленных метастазов |
| M0 | нет отдаленных метастазов |
| M1 | отдаленные метастазы |
ОПУХОЛЬ ЯИЧКА. LUGANO стадии.
| LUGANO | ||
| I | Локализованная опухоль | |
| IA | опухоль ограничена яичком | |
| IB | инфильтрация семенного канатика или опухоль в неопущенном яичке | |
| IC | инфильтрация мошонки или ранее проведена операция или опухоль была удалена или биопсирована трансскротальным доступом | |
| II | Распространение метастазов в поддиафрагмальные лимфоузлы | |
| IIA | все узлы ≤ 2 см | |
| IIB | по крайней мере один узел размерами от 2 до 5 см | |
| IIC | по крайней мере один узел размерами better 5 см | |
| IID | пальпируемая абдоминальная опухоль или неподвижные паховые лимфоузлы | |
| III | Распространение метастазов в наддиафрагмальные лимфоузлы или отдаленные метастазы | |
| IIIA | медиастинальные и/или надключичные лимфоузлы, но при отсутствии отдаленных гематогенных метастазов | |
| IIIB | отдаленные метастазы только в легкие: «minimal»: worse 5 метастазов в каждом легком, все размерами ≤ 2 см «advanced»: better 5 метастазов в каждом легком или better 2 см плеврального выпота | |
| IIIC | гематогенное распространение за пределы легких | |
| IIID | определение персистирующих опухолевых маркеров после комплексной терапии, но без очевидно обнаруживаемой опухоли | |
ЗЛОКАЧЕСТВЕННЫЕ ОПУХОЛИ ЯИЧКА.
PTNM. КЛАССИФИКАЦИЯ ЗЛОКАЧЕСТВЕННЫХ ГЕРМИНАЛЬНЫХ ОПУХОЛЕЙ ЯИЧКА [ UICC 1993] [ UICC 1997].
| pTNM | UICC 1992/93 | UICC 1997 |
| pT- первичная опухоль | ||
| pTx | Размер первичной опухоли не может быть оценен. Если радикальная орхиэктомия невозможна, выставляют Тх | |
| pT 0 | Нет данных о первичной опухоли (например, гистологические рубцы в яичках) | |
| pTis | Интратубулярная герминальная опухоли (н-р, carcinoma in situ) | |
| pT 1 | Опухоль ограничена яичком (включая оболочки) | Опухоль ограничена яичком и придатком, нет инвазии в кровеносные и лимфатические сосуды (опухоль может инфильтрировать белочную оболочку, но не влагалищную оболочку яичка) |
| pT 2 | Опухоль прорастает белочную оболочку яичка или инфильтрирует придаток яичка | Опухоль ограничена яичком и придатком, с инвазией в кровяные и лимфатические сосуды, или опухоль с распространением через белочную оболочку с поражением влагалищной оболочки яичка |
| pT 3 | Опухоль инфильтрирует семенной канатик (с или без инвазии кровеносных и лимфатических сосудов) | |
| pT 4 | Опухоль инфильтрирует мошонку (с или без инвазии кровеносных и лимфатических сосудов) | |
| pN - региональные лимфоузлы | ||
| pNx | невозможно провести экспертизу региональных лимфоузлов | |
| pN0 | Нет метастазов в региональных лимфоузлах | |
| pN1 | Метастаз в единичном лимфоузле, не более 2 см в максимальном измерении | Метастазирование в конгломерате лимфоузлов или в (единичном или в нескольких) лимфоузлах, но не превышают в размерах 2 см в максимальном измерении и 5 или менее позитивных л/узлов, не более чем 2 см в наибольшем измерении |
| pN2 | Метастаз в единичном лимфоузле, превышающий 2 но не более 5 см в максимальном измерении, или в нескольких лимфоузлах, не превышающих в размере 5 см | Метастазирование в конгломерате лимфоузлов или в нескольких лимфоузлах, превышающих в размерах 2 но не более 5 см в максимальном измерении, Или не более 5 позитивных лимфоузлов, не превышающих в максимальном размере 5 см или экстранодулярное распространение опухоли |
| pN3 | Метастаз(ы) в лимфатических узлах превышающий 5 см в максимальном измерении | Метастазирование в конгломераты лимфоузлов, превышающий в максимальном измерении 5 см |
| pM -отдаленные метастазы | ||
| pMx | Отдаленные метастазы не могут быть оценены | |
| pM0 | Нет отдаленных метастазов | |
| pM1 | Отдаленные метастазы | Отдаленные метастазы: • М1а нерегиональные лимфоузлы или метастазы в легкие; • М1b другие отдаленные метастазы |
СТАДИИ ЗЛОКАЧЕСТВЕННЫХ ГЕРМИНАЛЬНЫХ ОПУХОЛЕЙ ЯИЧКА.
| СТАДИЯ | UICC 1992/93 | UICC 1997 | |
| Stadium 0 | pTis N0 M0 | pTis N0 M0 S0/ Sx | |
| Stadium I | pT 1-4 N0 M0 | pT 1-4 N0 M0 Sx | |
| I A | p T1 S0 | ||
| I в | p T2-4 S0 | ||
| I S | любой pT/Tx S1-3 | ||
| Stadium II | любой pT N1-3 M0 | любой pT/Tx N1-3 M0 S0/S1 | |
| II A | N1 | ||
| II в | N2 | ||
| II S | N3 | ||
| Stadium III | любой pT любой N M1 | любой pT/Tx любой N M1, 1a Sx | |
| III A | любой N M1, 1a S0, 1 | ||
| III в | N1-3 M0 S2 любой N M1, 1a S2 | ||
| III с | N1-3 M0 S3 любой N M1, 1a S3 любой N M1b любой S | ||
КЛАССИФИКАЦИЯ ЗЛОКАЧЕСТВЕННЫХ ГЕРМИНОГЕННЫХ ОПУХОЛЕЙ ЯИЧКА В ЗАВИСИМОСТИ ОТ ОПУХОЛЕВЫХ МАРКЕРОВ*.
| Sx | Исследование не проводилось или не имеется в распоряжении | ||||
| S 0 | Маркеры в пределах нормы | ||||
| S1- S3 | Повышение даже одного из маркеров | ||||
| ЛДГ | Β-ХГЧ | АФП | |||
| S1 | Менее 1,5 * N** | и | Менее 5 000 mlU/ml | и | Менее 1 000 ng/ml |
| S2 | 1,5-10 * N | или | 5 000-50 000 mlU/ml | или | 1 000-10 000 ng/ml |
| S3 | Более 10 * N | или | Более 50 000 mlU/ml | или | Более 10 000 ng/ml |
Примечание. UICC, 1997 г. - верхняя граница нормального значения ЛДГ.
ОПУХОЛЬ ЯИЧНИКА. TNM - и FIGO стадии.
| TNM FIGO | ||
| ТХ | первичная опухоль не может быть оценена | |
| Т0 | нет данных о первичной опухоли | |
| Т1 | I | опухоль ограничена яичником (яичниками) |
| Т1а | I А | односторонняя опухоль, ограниченная яичником, микроскопически удалена полностью, капсула интактна |
| Т1 b | I В | двусторонняя опухоль, ограничена яичником, микроскопически удалена полностью, капсула интактна |
| T1c | I С | одно- или двусторонняя опухоль, злокачественные клетки в асцитической жидкости, интраоперационный разрыв опухоли или микроскопически неполное удаление |
| T2 | II | поражение одного или обоих яичников с распространением в малый таз |
| T2a | II А | распространение в матку и/или в трубы, отсутствие злокачественных клеток в асцитической жидкости |
| T2b | II В | распространение в другие структуры малого таза, отсутствие злокачетсвенных клеток в асцитической жидкости |
| T2c | II С | IIA или IIB и злокачетсвенные клетки в асцитической жидкости |
| T3 и/ или N1 | III | поражение одного или обоих яичников с микроскопически подтвержденными перитонеальными метастазами за пределами малого таза и/или метастатическим злокачественным поражением регионарных лимфоузлов |
| T3a | III А | микроскопически подтвержденные перитонеальные метастазы за пределами малого таза |
| T3b | III В | макроскопически подтвержденные перитонеальные метастазы за пределами малого таза ≤ 2 см в диаметре |
| T3c | III С | макроскопически подтвержденные перитонеальные метастазы за пределами малого таза better 2 см в диаметре или метастатическое поражение забрюшинных лимфоузлов |
| M1 | IV | отдаленные метастазы |
СТАДИИ ОПУХОЛЕЙ ЯИЧНИКОВ ПО TNM-КЛАССИФИКАЦИИ.
[UICC 1993] [UICC1997].
| Стадия | T | N | M |
| IA | T1a | N0 | M0 |
| IB | T1b | N0 | M0 |
| IC | T1c | N0 | M0 |
| IIA | T2a | N0 | M0 |
| IIB | T2b | N0 | M0 |
| IIC | T2c | N0 | M0 |
| IIIA | T3a | N0 | M0 |
| IIIB | T3b | N0 | M0 |
| IIIC | T3c | N0 | M0 |
| Любая T | N1 | ||
| IV | Любая T | Любая N | M1 |
|
|
Клиническая картина
Злокачественные ГКО могут секретировать опухолевые маркеры. Повышенный уровень альфа-фетопротеина (АФП) говорит за наличие тканей желточного мешка (YST), в то время как повышение уровня β-хорионического гонадотропина человека (β-ХГЧ) характерно для хориокарциномы (ChCa). Уровни АФП и β-ХГЧ пропорциональны количеству продуцирующих их опухолевых клеток.
У здоровых доношенных новорожденных концентрация АФП в сыворотке крови может колебаться в больших пределах и быть значительно повышенной, но в норме уровень маркера снижается по мере взросления ребенка. Таким образом, нарастание АФП в динамике у младенцев может служить диагностическим критерием наличия компонента YST без гистологического подтверждения.
Маркеры АФП и β-ХГЧ используются для клинической диагностики ГКО, оценки ответа на терапию и определения рецидива.
При ГКО рекомендуется проведение цитогенетического исследования и генетического консультирования для выявления возможных генетических синдромов.
У здоровых доношенных новорожденных концентрация АФП в сыворотке крови может колебаться в больших пределах и быть значительно повышенной, но в норме уровень маркера снижается по мере взросления ребенка. Таким образом, нарастание АФП в динамике у младенцев может служить диагностическим критерием наличия компонента YST без гистологического подтверждения.
Маркеры АФП и β-ХГЧ используются для клинической диагностики ГКО, оценки ответа на терапию и определения рецидива.
При ГКО рекомендуется проведение цитогенетического исследования и генетического консультирования для выявления возможных генетических синдромов.
Диагностика
Критерии установления диагноза/состояния:
1) данные анамнеза;
2) данные физикального обследования;
3) данные лабораторных исследований;
4) данные инструментального обследования;
5) данные патологоанатомического исследования биопсийного (операционного) материала.
Клинический диагноз основан на комбинации результатов:
1) физикального осмотра (визуального осмотра и пальпации), при котором выяв- ляют критерии, указывающие на возможное новообразование яичка;
2) лабораторных исследований, при которых выявляют повышенный уровень сы- вороточных онкомаркеров (АФП, ХГЧ);
3) морфологической верификации диагноза.
Уровень убедительности рекомендаций - С (уровень достоверности доказательств - 5).
Комментарии. Подробный сбор семейного анамнеза, детальное выяснение акушерского анамнеза матери, особенности беременности и развития пациента от рождения до момента обследования. Уточнение онкологического анамнеза - наличие доброкачественных, или злокачественных опухолей у членов семьи, а также наличие в семье или у пациента врождённых пороков развития.
Локализация опухоли в мягких тканях черепа.
Нарушения жевания, глотания, дыхания. Чувство помехи во рту (при соответствующей локализации опухоли). В зависимости от характера распространения: болевой синдром, в том числе «головная боль».
Локализация опухоли в ККО.
Беспокойство, боль при попытке усадить ребенка, нарушение ритма дефекации и мочеиспускания, появление «+» ткани в перианальной и крестцово-копчиковой области в далеко зашедших случаях.
Локализация опухоли в яичках.
Увеличение яичка безболезненное или болезненное в раннем возрасте и чаще болезненное у подростков.
Достаточно часто образование яичка у детей до 7 лет жизни обнаруживают при прохождении медицинского осмотра с последующим проведением УЗИ мошонки.
(в декретированные сроки осмотра осмотра врача-детского хирурга и врача- детского андролога-уролога). Дифференциальную диагностику необходимо проводить с варикоцеле, гематомой яичка.
Локализация опухоли в яичнике/яичниках.
Боли в животе, клиника острого живота, увеличение живота при относительно хорошем самочувствии, появление выделений из влагалища, нарушение пубертатного развития.
Локализация опухоли в забрюшинном пространстве.
Увеличение живота в объеме, боли в животе, пальпируемое образование, нарушение стула, дизурические расстройства.
Локализация опухоли в средостении.
Кашель, нарушение глотания, нарушение сердечного ритма. Образование может быть выявлено случайно при прохождении рентгенологических видов исследования и, или УЗИ щитовидной железы в декретированные сроки.ведение в подраздел(по желанию).
• Полное физикальное обследование.
• антропометрические измерения (вес, рост и площадь поверхности тела).
• оценка нутритивного статуса (процентили).
• оценка физического развития.
• оценка наличия пороков развития и стигм дизэмбриогенеза.
• Оценка кожных покровов и слизистых.
• выявление пятен «кофе с молоком».
• выявление пальпируемого образования, определение локализации, характеристики опухоли (отек, спаянность с тканями), степень функциональных нарушений.
• Оценка костно-мышечной системы.
• выявление наличия болевого синдрома.
• выявление нарушения функции конечностей.
• Оценка функции сердечно-сосудистой системы.
• Оценка функции легочной системы.
• Пальпация живота с оценкой наличия гепатоспленомегалии.
• Оценка размеров лимфатических узлов.
• вовлечение регионарных лимфоузлов, размеры во всех случаях должны регистрироваться.
• Характеристика функции тазовых органов.
• выявление дисфункции внутренних органовведениев подраздел (по желанию).
• Общий (клинический) анализ крови.
• Общий (клинический) анализ мочи.
• Анализ крови биохимический общетерапевтический (общий белок, альбумин, мочевина, креатинин, калий, натрий, глюкоза, общий билирубин, прямой биллирубин, АЛТ, АСТ, ЛДГ); электролиты крови (Na, K, сa, P, Mg).
• Определение основных групп по системе AB0, определение антигена D системы Резус (резус-фактор).
• Молекулярно-биологического исследования крови на вирус гепатита в (Hepatitis в virus) и на вирус гепатита с (Hepatitis с virus);
• Молекулярно-биологического исследования крови на вирус иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1);
• Коагулограмма (ориентировочное исследование системы гемостаза).
• Исследование уровня иммуноглобулинов А, M, G в крови;
• Молекулярно-биологическое исследование крови на цитомегаловирус (Cytomegalovirus) у детей первого года при необходимости проведения ПХТ;
• Скорость клубочковой фильтрации по клиренсу эндогенного креатинина или по уровню цистатина С в сыворотке крови;
• Тесты тубулярной реабсорбции по уровню реабсорбции фосфатов.
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
• Рекомендуется всем пациентам до начала лечения (до хирургического вмешательства, в том числе до биопсии), а также, в случае «секретирующих опухолей», перед каждым этапом лечения оценивать следующие опухолевые маркеры [7,10,11]:
• Исследование уровня альфа-фетопротеина (АФП) в сыворотке крови.
• Исследование уровня хорионического гонадотропина в крови (β-ХГЧ).
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии: маркеры определяют до начала лечения (до хирургического вмешательства, в том числе до проведения биопсии.
При оценке результатов анализов необходимо ориентироваться на нормы лаборатории.
У детей первого года жизни необходимо исследовать онкомаркеры в динамике с интервалом в 5-7 дней. Нарастание опухолевых маркеров в случае типичной локализации делает диагноз секретирующей ГКО несомненным.
В случае «секретирующих опухолей» исследование онкомаркеров повторять перед каждым этапом лечения.а фоне проведения ПХТ контроль онкомаркеров проводят 1 раз в 7 дней.
• ЭКГ, Эхо-КГ.
• УЗИ опухоли (определение объема опухоли) - при возможности, в зависимости от локализации.
• УЗИ органов брюшной полости, забрюшинного пространства, малого таза.
• Рентгенография грудной клетки в 2 проекциях.
• КТ органов грудной клетки, брюшной полости и малого таза с контрастным усилением включая 3 фазы контрастирования (артериальная, венозная, паренхиматозная); шаг 0,5-1,2.
• МРТ малого таза и брюшной полости с контрастным усилением при локализации опухоли и /или метастазов в малом тазу или брюшной полости, в том числе у новорожденных детей и младенцев при крестцово-копчиковой локализации опухоли.
• МРТ головного мозга с контрастным усилением при подозрении на 4-ю стадию заболевания, у подростков с первичной локализацией опухоли в яичке или в средостении, а также в случае гистологического диагноза хориокарцинома.
• Сцинтиграфия костей всего тела с Технецием99 для опухолей с отдаленными метастазами, а также при подозрении на локальное поражение костей.
• При необходимости и/или в сложных случаях возможно рассмотрение вопроса о проведении ПЭТ-КТ.
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Уровень убедительности рекомендаций - с (уровень достоверности доказа- тельств - 4).
• Рекомендуется при метастатических формах ГКО следует рассмотреть вопрос о получении цитологического препарата костного мозга путем пункции строго из 4 точек, ввиду очаговости поражения костного мозга при метастазировании солидных новообразований у детей [12,14].
Уровень убедительности рекомендаций - в (уровень достоверности доказательств - 3).
Комментарии: следует помнить, что ввиду особенностей костномозгового кроветворения у детей до 6 месяцев жизни, в качестве анатомических структур для проведения пункции следует выбирать пяточную кость и бугристости большеберцовых костей. В остальных случаях возможно рассмотрение вопроса проведение пункций из передних и задних гребней тазовых костей. Следует приготовить по 10 стекол из каждой точки.
• Рекомендуется детям первого года жизни с ГКО выполнение стандартного цитогенетического исследования (кариотип) [15,16].
Уровень убедительности рекомендаций - с (уровень достоверности доказа- тельств - 4).
1) данные анамнеза;
2) данные физикального обследования;
3) данные лабораторных исследований;
4) данные инструментального обследования;
5) данные патологоанатомического исследования биопсийного (операционного) материала.
Клинический диагноз основан на комбинации результатов:
1) физикального осмотра (визуального осмотра и пальпации), при котором выяв- ляют критерии, указывающие на возможное новообразование яичка;
2) лабораторных исследований, при которых выявляют повышенный уровень сы- вороточных онкомаркеров (АФП, ХГЧ);
3) морфологической верификации диагноза.
2,1 Жалобы и анамнез.
• Рекомендуется сбор жалоб и анамнеза у пациента с герминогенной опухолью для выявления факторов, которые могут повлиять на выбор тактики лечения, методов диагностики и вторичной профилактики [5,6].Уровень убедительности рекомендаций - С (уровень достоверности доказательств - 5).
Комментарии. Подробный сбор семейного анамнеза, детальное выяснение акушерского анамнеза матери, особенности беременности и развития пациента от рождения до момента обследования. Уточнение онкологического анамнеза - наличие доброкачественных, или злокачественных опухолей у членов семьи, а также наличие в семье или у пациента врождённых пороков развития.
Локализация опухоли в мягких тканях черепа.
Нарушения жевания, глотания, дыхания. Чувство помехи во рту (при соответствующей локализации опухоли). В зависимости от характера распространения: болевой синдром, в том числе «головная боль».
Локализация опухоли в ККО.
Беспокойство, боль при попытке усадить ребенка, нарушение ритма дефекации и мочеиспускания, появление «+» ткани в перианальной и крестцово-копчиковой области в далеко зашедших случаях.
Локализация опухоли в яичках.
Увеличение яичка безболезненное или болезненное в раннем возрасте и чаще болезненное у подростков.
Достаточно часто образование яичка у детей до 7 лет жизни обнаруживают при прохождении медицинского осмотра с последующим проведением УЗИ мошонки.
(в декретированные сроки осмотра осмотра врача-детского хирурга и врача- детского андролога-уролога). Дифференциальную диагностику необходимо проводить с варикоцеле, гематомой яичка.
Локализация опухоли в яичнике/яичниках.
Боли в животе, клиника острого живота, увеличение живота при относительно хорошем самочувствии, появление выделений из влагалища, нарушение пубертатного развития.
Локализация опухоли в забрюшинном пространстве.
Увеличение живота в объеме, боли в животе, пальпируемое образование, нарушение стула, дизурические расстройства.
Локализация опухоли в средостении.
Кашель, нарушение глотания, нарушение сердечного ритма. Образование может быть выявлено случайно при прохождении рентгенологических видов исследования и, или УЗИ щитовидной железы в декретированные сроки.ведение в подраздел(по желанию).
2,2 Физикальное обследование.
Первичный осмотр включает:• Полное физикальное обследование.
• антропометрические измерения (вес, рост и площадь поверхности тела).
• оценка нутритивного статуса (процентили).
• оценка физического развития.
• оценка наличия пороков развития и стигм дизэмбриогенеза.
• Оценка кожных покровов и слизистых.
• выявление пятен «кофе с молоком».
• выявление пальпируемого образования, определение локализации, характеристики опухоли (отек, спаянность с тканями), степень функциональных нарушений.
• Оценка костно-мышечной системы.
• выявление наличия болевого синдрома.
• выявление нарушения функции конечностей.
• Оценка функции сердечно-сосудистой системы.
• Оценка функции легочной системы.
• Пальпация живота с оценкой наличия гепатоспленомегалии.
• Оценка размеров лимфатических узлов.
• вовлечение регионарных лимфоузлов, размеры во всех случаях должны регистрироваться.
• Характеристика функции тазовых органов.
• выявление дисфункции внутренних органовведениев подраздел (по желанию).
2,3 Лабораторные диагностические исследования.
• Рекомендуется выполнять следующие общеклинические методы обследования для определения общего состояния пациента, возможности проведения хирургического вмешательства и лекарственного лечения, необходимости назначения сопуствующей и сопроводительной терапии [6-9].• Общий (клинический) анализ крови.
• Общий (клинический) анализ мочи.
• Анализ крови биохимический общетерапевтический (общий белок, альбумин, мочевина, креатинин, калий, натрий, глюкоза, общий билирубин, прямой биллирубин, АЛТ, АСТ, ЛДГ); электролиты крови (Na, K, сa, P, Mg).
• Определение основных групп по системе AB0, определение антигена D системы Резус (резус-фактор).
• Молекулярно-биологического исследования крови на вирус гепатита в (Hepatitis в virus) и на вирус гепатита с (Hepatitis с virus);
• Молекулярно-биологического исследования крови на вирус иммунодефицита человека ВИЧ-1 (Human immunodeficiency virus HIV-1);
• Коагулограмма (ориентировочное исследование системы гемостаза).
• Исследование уровня иммуноглобулинов А, M, G в крови;
• Молекулярно-биологическое исследование крови на цитомегаловирус (Cytomegalovirus) у детей первого года при необходимости проведения ПХТ;
• Скорость клубочковой фильтрации по клиренсу эндогенного креатинина или по уровню цистатина С в сыворотке крови;
• Тесты тубулярной реабсорбции по уровню реабсорбции фосфатов.
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
• Рекомендуется всем пациентам до начала лечения (до хирургического вмешательства, в том числе до биопсии), а также, в случае «секретирующих опухолей», перед каждым этапом лечения оценивать следующие опухолевые маркеры [7,10,11]:
• Исследование уровня альфа-фетопротеина (АФП) в сыворотке крови.
• Исследование уровня хорионического гонадотропина в крови (β-ХГЧ).
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии: маркеры определяют до начала лечения (до хирургического вмешательства, в том числе до проведения биопсии.
При оценке результатов анализов необходимо ориентироваться на нормы лаборатории.
У детей первого года жизни необходимо исследовать онкомаркеры в динамике с интервалом в 5-7 дней. Нарастание опухолевых маркеров в случае типичной локализации делает диагноз секретирующей ГКО несомненным.
В случае «секретирующих опухолей» исследование онкомаркеров повторять перед каждым этапом лечения.а фоне проведения ПХТ контроль онкомаркеров проводят 1 раз в 7 дней.
2,4 Инструментальные диагностические исследования.
• Рекомендуется выполнять следующие инструментальные методы диагностики для оценки распространенности заболевания, определения общего состояния пациента, возможности проведения хирургического вмешательства и лекарственного лечения, необходимости назначения сопутствующей и сопроводительной терапии [3,5,7,10,12]:• ЭКГ, Эхо-КГ.
• УЗИ опухоли (определение объема опухоли) - при возможности, в зависимости от локализации.
• УЗИ органов брюшной полости, забрюшинного пространства, малого таза.
• Рентгенография грудной клетки в 2 проекциях.
• КТ органов грудной клетки, брюшной полости и малого таза с контрастным усилением включая 3 фазы контрастирования (артериальная, венозная, паренхиматозная); шаг 0,5-1,2.
• МРТ малого таза и брюшной полости с контрастным усилением при локализации опухоли и /или метастазов в малом тазу или брюшной полости, в том числе у новорожденных детей и младенцев при крестцово-копчиковой локализации опухоли.
• МРТ головного мозга с контрастным усилением при подозрении на 4-ю стадию заболевания, у подростков с первичной локализацией опухоли в яичке или в средостении, а также в случае гистологического диагноза хориокарцинома.
• Сцинтиграфия костей всего тела с Технецием99 для опухолей с отдаленными метастазами, а также при подозрении на локальное поражение костей.
• При необходимости и/или в сложных случаях возможно рассмотрение вопроса о проведении ПЭТ-КТ.
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
2,5 Иные диагностические исследования.
• Рекомендуется для морфологической верификации диагноза выполнение у пациентов с внегонадной локализацией первичной опухоли выполнение core-биопсии под контролем УЗИ или КТ [13].Уровень убедительности рекомендаций - с (уровень достоверности доказа- тельств - 4).
• Рекомендуется при метастатических формах ГКО следует рассмотреть вопрос о получении цитологического препарата костного мозга путем пункции строго из 4 точек, ввиду очаговости поражения костного мозга при метастазировании солидных новообразований у детей [12,14].
Уровень убедительности рекомендаций - в (уровень достоверности доказательств - 3).
Комментарии: следует помнить, что ввиду особенностей костномозгового кроветворения у детей до 6 месяцев жизни, в качестве анатомических структур для проведения пункции следует выбирать пяточную кость и бугристости большеберцовых костей. В остальных случаях возможно рассмотрение вопроса проведение пункций из передних и задних гребней тазовых костей. Следует приготовить по 10 стекол из каждой точки.
• Рекомендуется детям первого года жизни с ГКО выполнение стандартного цитогенетического исследования (кариотип) [15,16].
Уровень убедительности рекомендаций - с (уровень достоверности доказа- тельств - 4).
|
|
Лечение
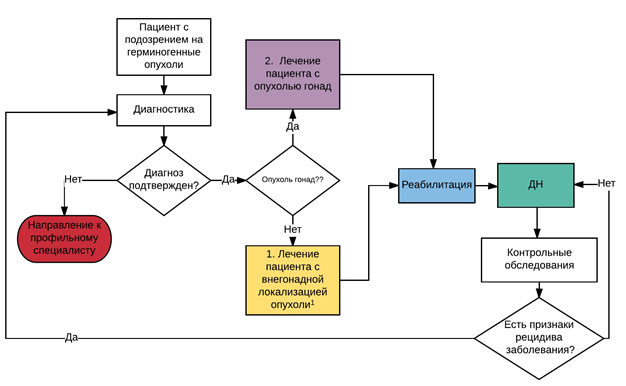
Типичная локализация опухоли и повышенная концентрация опухолевых маркеров в сыворотке крови позволяет установить диагноз ГКО без морфологического подтверждения, что особенно важно при распространенных опухолевых процессах.
Тактика лечения ГКО определяется с учетом возраста, гистологического варианта, локализации опухоли, стадии заболевания и наличия опухолевых маркеров.
Первым и важнейшим терапевтическим мероприятием при экстракраниальных ГКО является наиболее полная резекция опухоли. Микроскопически тотальная резекция опухоли (R0) - является одним из значимых прогностических факторов.
При злокачественных ГКО дополнительно необходима адъювантная химиотерапия.
При неоперабельных опухолях первично показано проведение неоадъювантной химиотерапии. (ХТ) в целях сокращения объема опухоли, выполнения радикального удаления опухоли, предотвращения калечащей операции.
Возможно клиническое установление диагноза на основании визуализирующих методов и повышенных опухолевых маркеров, что позволяет в единичных случаях отказаться от биопсии.
Наибольшую эффективность имеет комбинированная химиотерапия, включающая 3 препарата, одним из которых всегда является соединение платины.
Цисплатин** (P) относится к наиболее эффективным препаратам, который, однако, может привести к тубулярным нарушениям функции почек и тугоухости. В сравнении с этим карбоплатин** является менее токсичным и должен дозироваться в 6 раз выше.
У пациентов со злокачественными ГКО первых 4 месяцев жизни применяется комбинация 2 препаратов - цисплатина** и этопозида**.
Рекомендуется ребенку с подозрением на ГКО на первичном этапе оперативное вмешательство с гистологической верификацией образования ( см раздел 7,2) [10].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии: по жизненным показаниям возможно проведение биопсии/удаления образования до завершения клинического обследования. Однако, в стандартных ситуациях следует рассматривать вопрос об объеме первичного хирургического вмешательства только после завершения комплексного обследования. В случае четко отграниченной опухоли, отсутствии данных за инфильтрацию окружающих органов, возможно рассмотреть вопрос о проведении радикальной операции. Следует минимизировать возможные хирургические риски. В случае инфильтрации опухолью как жизненно важных структур, так и других органов и тканей, а также при наличии большого количества послеоперационных осложнений, показано проведение биопсии образования с последующим принятием решения о тактике ведения по результатам гистологического и ИГХ-исследований.
• Рекомендуется ребенку после оперативного лечения по поводу ГКО выбор послеоперационной терапии в зависимости от возраста, локализации опухоли, гистологического варианта, радикальности проведенной операции ( см раздел 7,3) [10,17].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Тактика лечения ГКО определяется с учетом возраста, гистологического варианта, локализации опухоли, стадии заболевания и наличия опухолевых маркеров.
Первым и важнейшим терапевтическим мероприятием при экстракраниальных ГКО является наиболее полная резекция опухоли. Микроскопически тотальная резекция опухоли (R0) - является одним из значимых прогностических факторов.
При злокачественных ГКО дополнительно необходима адъювантная химиотерапия.
При неоперабельных опухолях первично показано проведение неоадъювантной химиотерапии. (ХТ) в целях сокращения объема опухоли, выполнения радикального удаления опухоли, предотвращения калечащей операции.
Возможно клиническое установление диагноза на основании визуализирующих методов и повышенных опухолевых маркеров, что позволяет в единичных случаях отказаться от биопсии.
Наибольшую эффективность имеет комбинированная химиотерапия, включающая 3 препарата, одним из которых всегда является соединение платины.
Цисплатин** (P) относится к наиболее эффективным препаратам, который, однако, может привести к тубулярным нарушениям функции почек и тугоухости. В сравнении с этим карбоплатин** является менее токсичным и должен дозироваться в 6 раз выше.
У пациентов со злокачественными ГКО первых 4 месяцев жизни применяется комбинация 2 препаратов - цисплатина** и этопозида**.
Рекомендуется ребенку с подозрением на ГКО на первичном этапе оперативное вмешательство с гистологической верификацией образования ( см раздел 7,2) [10].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии: по жизненным показаниям возможно проведение биопсии/удаления образования до завершения клинического обследования. Однако, в стандартных ситуациях следует рассматривать вопрос об объеме первичного хирургического вмешательства только после завершения комплексного обследования. В случае четко отграниченной опухоли, отсутствии данных за инфильтрацию окружающих органов, возможно рассмотреть вопрос о проведении радикальной операции. Следует минимизировать возможные хирургические риски. В случае инфильтрации опухолью как жизненно важных структур, так и других органов и тканей, а также при наличии большого количества послеоперационных осложнений, показано проведение биопсии образования с последующим принятием решения о тактике ведения по результатам гистологического и ИГХ-исследований.
• Рекомендуется ребенку после оперативного лечения по поводу ГКО выбор послеоперационной терапии в зависимости от возраста, локализации опухоли, гистологического варианта, радикальности проведенной операции ( см раздел 7,3) [10,17].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Реабилитация и амбулаторное лечение
• Рекомендуется включить в план реабилитационных мероприятий на всем протяжении специального лечения оказание социально-педагогической помощи (нейропсихологическая реабилитация, врачебно-педагогическое наблюдение) ребенку, а также социально-психологическую поддержку семьи (семейное клинико-психологическое консультирование) [18].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Профилактика
• Рекомендована всем пациентам с экстракраниальными герминогенно-клеточными опухолями следующая программа наблюдения после химиотерапии [19]:
• наличие осложнений меланомы, требующих оказания специализированной медицинской помощи в экстренной и неотложной форме;
• наличие осложнений лечения (хирургическое вмешательство, лучевая терапия, лекарственная терапия ) меланомы.
Показанием для госпитализации в медицинскую организацию в плановой форме является:
• необходимость выполнения сложных интервенционных диагностических медицинских вмешательств, требующих последующего наблюдения в условиях круглосуточного или дневного стационара;
• наличие показаний к специализированному противоопухолевому лечению (хирургическое вмешательство, лучевая терапия, в том числе контактная, дистанционная и другие виды лучевой терапии, лекарственная терапия ), требующему наблюдения в условиях круглосуточного или дневного стационара.
Показанием к выписке пациента из медицинской организации является:
• завершение курса лечения или одного из этапов оказания специализированной, в том числе высокотехнологичной, медицинской помощи в условиях круглосуточного или дневного стационара при условиях отсутствия осложнений лечения, требующих медикаментозной коррекции и/или медицинских вмешательств в стационарных условиях;
• отказ пациента или его законного представителя от специализированной, в том числе высокотехнологичной, медицинской помощи в условиях круглосуточного или дневного стационара, установленной консилиумом медицинской организации, оказывающей онкологическую помощь при условии отсутствия осложнений основного заболевания и/или лечения, требующих медикаментозной коррекции и/или медицинских вмешательств в стационарных условиях;
• необходимость перевода пациента в другую медицинскую организацию по соответствующему профилю оказания медицинской помощи. Заключение о целесообразности перевода пациента в профильную медицинскую организацию осуществляется после предварительной консультации по предоставленным медицинским документам и/или данным предварительного осмотра пациента врачами специалистами медицинской организации, в которую планируется перевод.
| Показатель | 1-й год наблюдения | 2-й год наблюдения | 3-5-й годы наблюдения |
| Антропометрия | ежемесячно | каждые 4 мес. | каждые 6 мес. |
| Клиническое исследование | ежемесячно | каждые 2 мес. | каждые 3 мес. |
| УЗИ первичной локализации опухоли | ежемесячно | каждые 2 мес. | каждые 3 мес. |
| КТ/МРТ с КУ (в случае неполной резекции) | каждые 2 мес. | каждые 4 мес. | каждые 6 мес. |
| Аудиограмма | каждые 6 мес. | каждые 6 мес. | каждые 6 мес. |
| Клиренс креатинина; ОАК, ОАМ | ежемесячно | каждые 4 мес. | каждые 6 мес. |
| Онкомаркеры: АФП, ß-ХГЧ | ежемесячно | каждые 4 мес. | каждые 6 мес. |
| Определение половых гормонов | Однократно или при патологии. При нарушении пубертата - определение ФСГ, ЛГ, пролактина. У девочек (при нарушении цикла) определение эстрадиола. У юношей - измерение тестостерона | ||
| Контроль вторых опухолей | |||
| Контроль костных опухолей, ОЛЛ, МДС | |||
| Контроль метахронных опухолей между 2-м и 10-м годами постановки диагноза, особенно при локализации опухоли в яичниках | |||
| Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5) | |||
Организация оказания медицинской помощи.
Показанием для госпитализации в медицинскую организацию в экстренной или неотложной форме является:• наличие осложнений меланомы, требующих оказания специализированной медицинской помощи в экстренной и неотложной форме;
• наличие осложнений лечения (хирургическое вмешательство, лучевая терапия, лекарственная терапия ) меланомы.
Показанием для госпитализации в медицинскую организацию в плановой форме является:
• необходимость выполнения сложных интервенционных диагностических медицинских вмешательств, требующих последующего наблюдения в условиях круглосуточного или дневного стационара;
• наличие показаний к специализированному противоопухолевому лечению (хирургическое вмешательство, лучевая терапия, в том числе контактная, дистанционная и другие виды лучевой терапии, лекарственная терапия ), требующему наблюдения в условиях круглосуточного или дневного стационара.
Показанием к выписке пациента из медицинской организации является:
• завершение курса лечения или одного из этапов оказания специализированной, в том числе высокотехнологичной, медицинской помощи в условиях круглосуточного или дневного стационара при условиях отсутствия осложнений лечения, требующих медикаментозной коррекции и/или медицинских вмешательств в стационарных условиях;
• отказ пациента или его законного представителя от специализированной, в том числе высокотехнологичной, медицинской помощи в условиях круглосуточного или дневного стационара, установленной консилиумом медицинской организации, оказывающей онкологическую помощь при условии отсутствия осложнений основного заболевания и/или лечения, требующих медикаментозной коррекции и/или медицинских вмешательств в стационарных условиях;
• необходимость перевода пациента в другую медицинскую организацию по соответствующему профилю оказания медицинской помощи. Заключение о целесообразности перевода пациента в профильную медицинскую организацию осуществляется после предварительной консультации по предоставленным медицинским документам и/или данным предварительного осмотра пациента врачами специалистами медицинской организации, в которую планируется перевод.
|
|
Критерии оценки качества медицинской помощи
| № п/п | Критерии качества | Оценка выполнения |
| 1 | Выполнен осмотр врачом-детским онкологом (при установлении диагноза) | Да/нет |
| 2 | Выполнена МРТ с внутривенным контрастированием органов малого таза и брюшной полости и забрюшинного пространства (при установлении диагноза) | Да/нет |
| 3 | Выполнено УЗИ органов малого таза и брюшной полости и забрюшинного пространства и первичного опухолевого очага (при установлении диагноза) | Да/нет |
| 4 | Выполнена КТ органов грудной клетки (при установлении диагноза) | Да/нет |
| 5 | Выполнена сцинтиграфия костей всего тела (при установлении диагноза) | Да/нет |
| 6 | Выполнено исследование уровня АФП в сыворотке крови (при установлении диагноза) | Да/нет |
| 7 | Выполнено исследование уровня β-ХГЧ в крови (при установлении диагноза) | Да/нет |
| 8 | Выполнено исследование уровня ЛДГ в крови (при установлении диагноза) | Да/нет |
| 9 | Выполнено патолого-анатомическое исследование ткани первичной опухоли и/или очагов, подозрительных на метастатические (при биопсии и/или при хирургическом вмешательстве на этапе диагностики) (при установлении диагноза) | Да/нет |
| 10 | Выполнено удаление опухоли без повреждения ее капсулы (при радикальном хирургическом вмешательстве) | Да/нет |
| 11 | Проведена ПХТ не ранее 5 и не позднее 7 сут от момента хирургического вмешательства (при наличии медицинских показаний и отсутствии медицинских противопоказаний) | Да/нет |
| 12 | Выполнено УЗИ органов малого таза и брюшной полости и забрюшинного пространства и первичного опухолевого очага перед началом каждого курса ПХТ | Да/нет |
| 13 | Выполнена повторная МРТ с внутривенным контрастированием органов малого таза и брюшной полости и забрюшинного пространства (перед хирургическим вмешательством) | Да/нет |
| 14 | Выполнена КТ органов грудной клетки не реже 1 раза в 2 мес | Да/нет |
| 15 | Выполнено исследование уровня АФП в сыворотке крови перед каждым курсом ПХТ | Да/нет |
| 16 | Выполнено исследование уровня β-ХГЧ в крови перед каждым курсом ПХТ | Да/нет |
| 17 | Выполнено исследование уровня ЛДГ в крови перед каждым курсом ПХТ | Да/нет |
| 18 | Выполнен ОАК развернутый с подсчетом лейкоцитарной формулы перед каждым курсом ПХТ и не реже 1 раза в неделю при проведении лучевой терапии или ПХТ | Да/нет |
| 19 | Выполнен анализ крови биохимический общетерапевтический (мочевина, креатинин, общий белок, альбумин, общий билирубин, аланинаминотрансфераза, аспартатаминотрансфераза, натрий, калий, хлор) перед каждым курсом ПХТ и не реже 1 раза в неделю при проведении лучевой терапии или ПХТ | Да/нет |
| 20 | Выполнен ОАМ перед каждым курсом ПХТ и не реже 1 раза в неделю при проведении лучевой терапии или ПХТ | Да/нет |
Список литературы
1. Dehner L.P. Gonadal and extragonadal germ cell neoplasia of childhood // Hum. Pathol. 1983. Vol. 14, № 6. P. 493-511.
2. Miller R.W., Young J.L., Novakovic в. сhildhood cancer // сancer. John Wiley & Sons, Ltd, 1995. Vol. 75, № S1. P. 395-405.
3. сastleberry R.P., сushing в., Perlman E. Germ cell tumors // Principles and Practice of Pediatric Oncology, 3rd ed. / ed. Pizzo P.A., Poplack D.G. 1997. P. 921-945.
4. Malogolowkin M.H. et al. Germ cell tumors in infancy and childhood: A 45-year experience // Fetal Pediatr. Pathol. Informa Healthcare, 1990. Vol. 10, № 1-2. P. 231-241.
5. Фасеева Н.Д. Оптимизация тактики лечения герминогенных опухолей у детей. Диссертационная работа на соискание ученой степени кандидата медицинских наук. 2018. 146 p.
6. Детская онкология. Национальное руководство. Под ред. М.Д. Алиева, В.Г. Полякова, Г.Л. Менткевича, С.А. Маяковой. М. Издательская группа РОНЦ. Практическая медицина, 2012. 684 p.
7. сalaminus G. et al. Age-Dependent Presentation and сlinical сourse of 1465 Patients Aged 0 to Less than 18 Years with Ovarian or Testicular Germ сell Tumors; Data of the MAKEI 96 Protocol Revisited in the Light of Prenatal Germ сell вiology // сancers (Basel). 2020. Vol. 12, № 3. P. 611.
8. Герминогенноклеточные опухоли // Стандарты оказания специализированной помощи детям и подросткам с гематологическими и онкологическими заболеваниями. 2009. P. 525-538.
9. Gray A. et al. Persistence of parvovirus в19 DNA in testis of patients with testicular germ cell tumours // J. Gen. Virol. Microbiology Society, 1998. Vol. 79, № 3. P. 573-579.
10. сecchetto G. Gonadal germ cell tumors in children and adolescents // Journal of Indian Association of Pediatric Surgeons. Medknow Publications, 2014. Vol. 19, № 4. P. 189-194.
11. Göbel U. et al. Germ-cell tumors in childhood and adolescence // Annals of Oncology. 2000. Vol. 11, № 3. P. 263-271.
12. Варфоломеева С.Р. Экстракраниальные герминогенноклеточные опухоли. Стандарты обследования и терапевтические подходы. Electronic resource]. P. 27.
13. Hussain H.K. et al. Imaging-guided core biopsy for the diagnosis of malignant tumors in pediatric patients // Am. J. Roentgenol. American Roentgen Ray Society, 2001. Vol. 176, № 1. P. 43-47.
14. Penchansky L. вone marrow biopsy in the metastatic work-up of solid tumors in children. // сancer. 1984. Vol. 54, № 7. P. 1447-1448.
15. Piazza M.J., Urbanetz A.A. Germ сell Tumors in Dysgenetic Gonads // сlinics. Hospital das сlinicas da Faculdade de Medicina da Universidade de Sao Paulo, 2019. Vol. 74.
16. сunha S.C. et al. Early development of a gonadal tumor in a patient with mixed gonadal dysgenesis // Arch. Endocrinol. Metab. Sociedade вrasileira de Endocrinologia e Metabologia, 2018. Vol. 62, № 6. P. 644-647.
17. Marina N. et al. Treatment of childhood germ cell tumors: Review of the St. Jude experience from 1979 to 1988 // сancer. 1992. Vol. 70, № 10. P. 2568-2575.
18. Thorsteinsson T. et al. Study protocol: Rehabilitation including social and physical activity and education in children and teenagers with cancer (RESPECT) // вMC сancer. вioMed сentral, 2013. Vol. 13. P. 544.
19. Румянцев А.Г., Самочатова Е.В. Практическое руководство по детским болезням. Гематология/онкология детского возраста. Медпрактика-М, Москва, 2004.
20. Marina N.M. et al. сomplete surgical excision is effective treatment for children with immature teratomas with or without malignant elements: A Pediatric Oncology Group/Children’s сancer Group Intergroup Study. J. сlin. Oncol. 1999. Vol. 17, № 7. P. 2137-2143.
21. Владимирова Л.Ю. et al. Практические рекомендации по профилактике и лечению тошноты и рвоты у онкологических больных // Практические рекомендации Российского общества клинической онкологии. Лекарственное лечение злокачественных опухолей. Поддерживающая терапия в онкологии. 2018. P. 502-511.
22. Wu J.T., вook L., Sudar K. Serum alpha fetoprotein (AFP) levels in normal infants // Pediatr. Res. Nature Publishing Group, 1981. Vol. 15, № 1. P. 50-52.
2. Miller R.W., Young J.L., Novakovic в. сhildhood cancer // сancer. John Wiley & Sons, Ltd, 1995. Vol. 75, № S1. P. 395-405.
3. сastleberry R.P., сushing в., Perlman E. Germ cell tumors // Principles and Practice of Pediatric Oncology, 3rd ed. / ed. Pizzo P.A., Poplack D.G. 1997. P. 921-945.
4. Malogolowkin M.H. et al. Germ cell tumors in infancy and childhood: A 45-year experience // Fetal Pediatr. Pathol. Informa Healthcare, 1990. Vol. 10, № 1-2. P. 231-241.
5. Фасеева Н.Д. Оптимизация тактики лечения герминогенных опухолей у детей. Диссертационная работа на соискание ученой степени кандидата медицинских наук. 2018. 146 p.
6. Детская онкология. Национальное руководство. Под ред. М.Д. Алиева, В.Г. Полякова, Г.Л. Менткевича, С.А. Маяковой. М. Издательская группа РОНЦ. Практическая медицина, 2012. 684 p.
7. сalaminus G. et al. Age-Dependent Presentation and сlinical сourse of 1465 Patients Aged 0 to Less than 18 Years with Ovarian or Testicular Germ сell Tumors; Data of the MAKEI 96 Protocol Revisited in the Light of Prenatal Germ сell вiology // сancers (Basel). 2020. Vol. 12, № 3. P. 611.
8. Герминогенноклеточные опухоли // Стандарты оказания специализированной помощи детям и подросткам с гематологическими и онкологическими заболеваниями. 2009. P. 525-538.
9. Gray A. et al. Persistence of parvovirus в19 DNA in testis of patients with testicular germ cell tumours // J. Gen. Virol. Microbiology Society, 1998. Vol. 79, № 3. P. 573-579.
10. сecchetto G. Gonadal germ cell tumors in children and adolescents // Journal of Indian Association of Pediatric Surgeons. Medknow Publications, 2014. Vol. 19, № 4. P. 189-194.
11. Göbel U. et al. Germ-cell tumors in childhood and adolescence // Annals of Oncology. 2000. Vol. 11, № 3. P. 263-271.
12. Варфоломеева С.Р. Экстракраниальные герминогенноклеточные опухоли. Стандарты обследования и терапевтические подходы. Electronic resource]. P. 27.
13. Hussain H.K. et al. Imaging-guided core biopsy for the diagnosis of malignant tumors in pediatric patients // Am. J. Roentgenol. American Roentgen Ray Society, 2001. Vol. 176, № 1. P. 43-47.
14. Penchansky L. вone marrow biopsy in the metastatic work-up of solid tumors in children. // сancer. 1984. Vol. 54, № 7. P. 1447-1448.
15. Piazza M.J., Urbanetz A.A. Germ сell Tumors in Dysgenetic Gonads // сlinics. Hospital das сlinicas da Faculdade de Medicina da Universidade de Sao Paulo, 2019. Vol. 74.
16. сunha S.C. et al. Early development of a gonadal tumor in a patient with mixed gonadal dysgenesis // Arch. Endocrinol. Metab. Sociedade вrasileira de Endocrinologia e Metabologia, 2018. Vol. 62, № 6. P. 644-647.
17. Marina N. et al. Treatment of childhood germ cell tumors: Review of the St. Jude experience from 1979 to 1988 // сancer. 1992. Vol. 70, № 10. P. 2568-2575.
18. Thorsteinsson T. et al. Study protocol: Rehabilitation including social and physical activity and education in children and teenagers with cancer (RESPECT) // вMC сancer. вioMed сentral, 2013. Vol. 13. P. 544.
19. Румянцев А.Г., Самочатова Е.В. Практическое руководство по детским болезням. Гематология/онкология детского возраста. Медпрактика-М, Москва, 2004.
20. Marina N.M. et al. сomplete surgical excision is effective treatment for children with immature teratomas with or without malignant elements: A Pediatric Oncology Group/Children’s сancer Group Intergroup Study. J. сlin. Oncol. 1999. Vol. 17, № 7. P. 2137-2143.
21. Владимирова Л.Ю. et al. Практические рекомендации по профилактике и лечению тошноты и рвоты у онкологических больных // Практические рекомендации Российского общества клинической онкологии. Лекарственное лечение злокачественных опухолей. Поддерживающая терапия в онкологии. 2018. P. 502-511.
22. Wu J.T., вook L., Sudar K. Serum alpha fetoprotein (AFP) levels in normal infants // Pediatr. Res. Nature Publishing Group, 1981. Vol. 15, № 1. P. 50-52.
|
|
Приложения
Приложение А1.
Состав рабочей группы.• Варфоломеева С.Р.
• Качанов Д.Ю.
• Шевцов Д.В.
• Капкова О.А.
• Киргизов И.
• Рыскаль О.В.
• Мушинская М.В.
• Казанцев А.П.
• Керимов П.А.
• Ахаладзе Д.Г.
• Терещенко Г.В.
• Поляков В.Г.
Конфликт интересов: отсутствует.
Приложение А2.
Методология разработки клинических рекомендаций.Целевая аудитория данных клинических рекомендаций:
1. Врачи-детские окологи-гематологи.
2. Студенты медицинских ВУЗов, ординаторы, аспиранты.
Таблица 1. Шкала оценки уровней достоверности доказательств (УДД)для методов диагностики (диагностических вмешательств).
| УДД | Расшифровка |
| 1 | Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением мета-анализа |
| 2 | Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением мета-анализа |
| 3 | Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода или нерандомизированные сравнительные исследования, в том числе когортные исследования |
| 4 | Несравнительные исследования, описание клинического случая |
| 5 | Имеется лишь обоснование механизма действия или мнение экспертов |
Таблица 2. Шкала оценки уровней достоверности доказательств (УДД)для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств).
| УДД | Расшифровка |
| 1 | Систематический обзор РКИ с применением мета-анализа |
| 2 | Отдельные РКИ и систематические обзоры исследований любого дизайна, за исключением РКИ, с применением мета-анализа |
| 3 | Нерандомизированные сравнительные исследования, в тч когортные исследования |
| 4 | Несравнительные исследования, описание клинического случая или серии случаев, исследования «случай-контроль» |
| 5 | Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов |
Таблица 3. Шкала оценки уровней убедительности рекомендаций(УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств).
| УУР | Расшифровка |
| A | Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными) |
| в | Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными) |
| с | Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными) |
Порядок обновления клинических рекомендаций.
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию - не реже чем один раз в три года,а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений/замечаний к ранее утверждённым КР, но не чаще 1 раза в 6 месяцев.
Приложение А3.
Связанные документы.Приложение А3,1 Схемы химиотерапии с сопроводительной терапией.
5,3,1. Цисплатин** / этопозид** (PE) [5].| Препарат | Доза, сут | Продолжительность инфузии | Дни курса | Кумулятивная Доза за курс |
| Цисплатин** (Р) | 20 мг/м2 | 1 ч | 1,2,3,4,5 | 100 мг/м2 |
| Этопозид** (Е) | 100 мг/м2 | 1 ч (до цисплатина**) | 1,2,3 | 300 мг/м2 |
Инфузионная терапия 3 000 л/м2/24 ч (дни 1-5):
| Состав инфузионной терапии | декстроза** | 1 500 мл / м2 / 24 | |
| натрия хлорид** | 1 500 мл / м2 / 24 | ||
| калия хлорид** | 60 мл / м2 / 24 | ||
| кальция глюконат** | 20 мл / м2 / 24 | ||
| магния сульфат** | 8 мл / м2 / 24 | ||
| Противорвотные препараты согласно профильным рекомендациям [21] | |||
5,3,2. Цисплатин** / этопозид** / ифосфамид** (PEI) [5,11].
| Препарат | Доза , сут | Продолжительность инфузии | Дни курса | Кумулятивная Доза за курс |
| Цисплатин** ( Р ) | 20 мг/м2 | 1 ч | 1, 2, 3, 4, 5 | 100 мг/м2 |
| Этопозид** ( Е ) | 100 мг/м2 | 1 ч (до цисплатина**) | 1, 2, 3 | 300 мг/м2 |
| Ифосфамид** (I) | 1500 мг/м2 | 22 ч | 1, 2, 3, 4, 5 | 7 500 мг/м2 |
Инфузионная терапия 3 000 л/м2/24 ч (дни 1-7):
| Состав инфузионной терапии | декстроза** | 1 500 мл / м2 / 24 | |
| натрия хлорид** | 1 500 мл / м2 / 24 | ||
| калия хлорид** | 60 мл / м2 / 24 | ||
| кальция глюконат** | 20 мл / м2 / 24 | ||
| магния сульфат** месна** | 8 мл / м2 / 24 1 500 мл / м2 / 24 | ||
| Противорвотные препараты согласно профильным рекомендациям [21] | |||
Приложение А3,2 Рекомендации по проведению химиотерапии.
• интервал между курсами ХТ - 21 день;• детям младше 2 лет, либо меньше 10 кг доза должна быть рассчитана на кг (30 кг = 1 м2);
• при индексе Карновского менее 50 - доза ифосфамида 1000 мг/м2/день, дни 1-5;
• в возрасте менее 4 месяцев ифосфамид исключается из схемы лечения;
• условия для продолжения ХТ:
• количество лейкоцитов более 1,5 × 109/л.
• количество тромбоцитов более 50 × 109/л;
• если клиренс креатинина менее 50 мл/мин или количество сывороточного креатинина более чем 1,2 мг/дл в начале следующего курса ХТ, интервал между курсами должен быть продлен еще на одну неделю, а цисплатин долж6н быть сокращен до 3 дней (вместо 5);
• если функция почек не улучшится, цисплатин отменяется, а ифосфамид сокращается до 1 г/м2;
• аудиометрия является обязательной перед каждым курсом ХТ. Если слуховая функция снизилась более чем на 50 децибел при 2000 Герц, цисплатин не должен вводиться. В таком случае вместо него пациент должен получать карбоплатин.
600 мг/м2.
Приложение В.
Информация для пациентов.Герминогенные опухоли - достаточно редкое заболевание у детей, частота их в популяции 4-6 случаев на 1 млн детского населения. Герминогенные опухоли развиваются из предшественников половых клеток (эмбриональных соматических клеток). В зависимости от конкретной локализации к этой группе заболеваний относятся: герминогенные опухоли гонад (яички и яичники), а также внегонадные локализации (крестцово-копчиковая область, переднее средостение, забрюшинная клетчатка, влагалище, почка. Крайне редко выявляется опухоль в желудке, шее, орбите.
Подходы к лечению этих заболеваний несколько отличаются: при локализациях в гонадах - на первом этапе показано хирургическое лечение, при внегонадных локализациях - лечение начинают с химиотерапии.
Установлены два возрастных пика заболеваемости герминогенными опухолями у детей: до 3 лет (крестцово- копчиковаые, яички, влагалище, орбита, шея, забрюшинная локализации) и после 12 лет (яичники, яички и средостение ).
Основная опасность герминогенных опухолей яичников - разрыв опухоли, что может вызвать диссеминацию процесса по брюшине. При герминогенных опухолях яичка - метастазирование в регионарные и забрюшинные лимфатические узлы, что может приводить к сдавлению магистральных вен и образованию тромбозов. Герминогенные опухоли, локализованные в крестцово-копчиковой области, могут вызывать кишечную непроходимость (то есть полностью перекрывать просвет кишки и препятствовать прохождению пищи), вызывать запоры и нарушение мочеиспускания. Все герминогенные опухоли могут метастазировать ( формировать новые очаги болезни) в регионарных и отдаленных лимфатических узлах, а также в других органах (чаще всего в легких, реже печени, головном мозге и костях ). Метастатическое поражение головного мозга приводит к неврологической симптоматике. К счастью, на сегодняшний день большинство даже запущенных форм герминогенных опухолей успешно излечивается, при условии, что лечением исходно занимается квалифицированный специалист в этой области.
Большинство пациентов могут полностью выздороветь и полноценно вернуться к привычному образу жизни. Исключение составляют ситуации, когда герминогенные опухоли локализованы в средостении, а также после проведения при ГО расширенной биопсии в неспециализированных учреждениях, длительного диагностического этапа и при выявлении множественных метастазов в печени и головном мозге. Но даже в таких случаях, при невозможности полного излечения, пациентам можно значительно увеличить продолжительность жизни и облегчить симптомы заболевания.
Лечение герминогенных опухолей у детей - задача не одного специалиста. В зависимости от конкретной ситуации, требуется наличие в клиники квалифицированного хирурга, детского онколога, детского онкогинеколога, химиотерапевта, патоморфолога, анестезиолога, реаниматолога, кардиолога, невролога.
Приложение Г.
Приложение Г1 Шкалы оценки общего состояния пациента.
Приложение Г2 Таблица уровня альфа-фетопротеина у здоровых новорожденных [22].
| Возраст, дни | Медиана АФП, ng/ml | АФП 95 % интервал, ng/ml | Период полураспада в днях |
| 0 | 158 125 | 31 261-799 834 | 6 |
| 1 | 140 605 | 27 797-711 214 | |
| 2 | 125 026 | 24 717-732 412 | |
| 3 | 111 173 | 21 979-562 341 | |
| 4 | 98 855 | 19 543-500 035 | |
| 5 | 87 902 | 17 371-444 631 | |
| 6 | 77 625 | 15 346-392 645 | |
| 7 | 69 183 | 12 589-349 945 | |
| 8-14 | 43 401 | 6 039-311 889 | |
| 15-21 | 19 230 | 2 667-151 356 | 14 |
| 22-28 | 12 246 | 1 164-118 850 | |
| 29-45 | 5 129 | 389-79 433 | |
| 46-60 | 2 443 | 91-39 084 | |
| 61-90 | 1 047 | 19-21 878 | 28 |
| 91-120 | 398 | 9-18 620 | |
| 121-150 | 193 | 4-8 318 | |
| 151-180 | 108 | 3-4 365 | |
| 181-270 | 47 | 0,8-2 630 | 100 |
| 271-360 | 18 | 0,4-832 | |
| 361-720 | 4 | 0-372 |
|
|
Год актуализации информации
2020.
Связанные заболевания
Связанные клинические рекомендации
Связанные стандарты мед. помощи
- Стандарт медицинской помощи больным злокачественным новообразованием соединительной и других мягких тканей
- Стандарт медицинской помощи больным злокачественным новообразованием яичника, яичка
- Стандарт медицинской помощи больным злокачественными новообразованиями соединительной, подкожной и других мягких тканей (при оказании специализированной помощи)
- Стандарт медицинской помощи взрослым при саркомах мягких тканей
- Стандарт медицинской помощи взрослым при гастроинтестинальных стромальных опухолях
- Стандарт специализированной медицинской помощи детям при преждевременном половом созревании
- Стандарт специализированной медицинской помощи детям при нейробластоме (низкий риск)
- Стандарт медицинской помощи взрослым при опухолях средостения (диагностика и лечение)