Другие названия и синонимы
Dabigatran etexilate.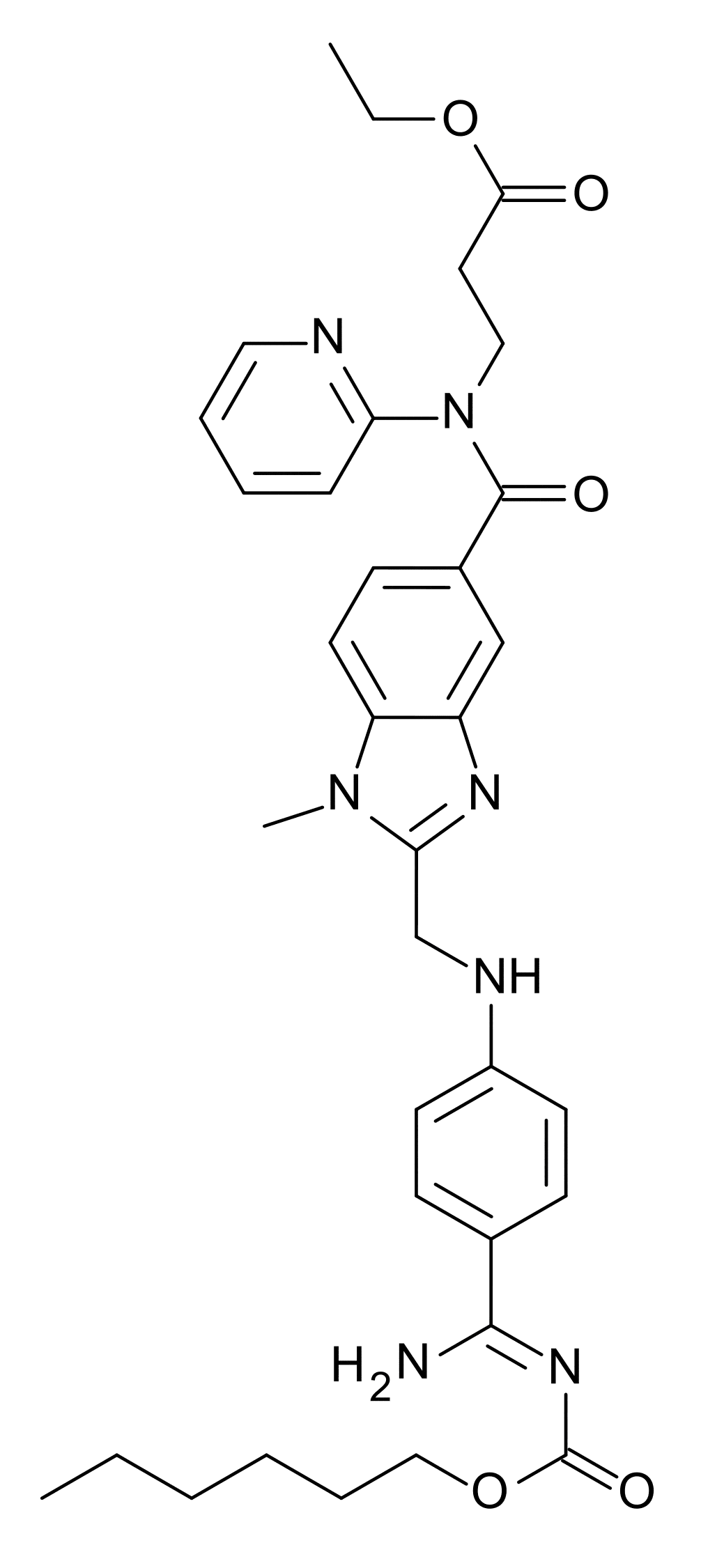
Фармакологическая группа
|
|
Латинское название
Dabigatrani etexilas ( Dabigatrani etexilatis).
Химическое название
Этил 3-([(2-([(4-(N -гексилоксикарбонил карбамидоил)фенил)амино]метил)-1-метил-1H-бензимидазол-5-ил)карбонил](пиридин-2-ил-амино)пропаноат (в виде мезилата).
Используется в лечении
Код CAS
211915-06-9.
Характеристика вещества
Прямой ингибитор тромбина.
RxList.com.
Дабигатрана этексилата мезилат - порошок от желто-белого до желтого цвета. Насыщенный раствор в воде имеет растворимость 1,8 мг/мл. Легко растворим в метаноле, слабо растворим в этаноле и плохо растворим в изопропаноле. Молекулярная масса - 723,86 (мезилат); 627,75 (основание).
RxList.com.
Дабигатрана этексилата мезилат - порошок от желто-белого до желтого цвета. Насыщенный раствор в воде имеет растворимость 1,8 мг/мл. Легко растворим в метаноле, слабо растворим в этаноле и плохо растворим в изопропаноле. Молекулярная масса - 723,86 (мезилат); 627,75 (основание).
Фармакодинамика
Фармакодинамика.
Дабигатрана этексилат является низкомолекулярным, не обладающим фармакологической активностью предшественником активной формы дабигатрана. После приема внутрь дабигатрана этексилат быстро всасывается в ЖКТ и путем гидролиза, катализируемого эстеразами, в печени и плазме крови превращается в дабигатран. Дабигатран является сильным конкурентным обратимым прямым ингибитором тромбина и основным активным веществом в плазме крови. Поскольку тромбин (сериновая протеаза) в процессе коагуляции превращает фибриноген в фибрин, угнетение активности тромбина препятствует образованию тромба. Дабигатран оказывает ингибирующее воздействие на свободный тромбин, тромбин, связанный с фибриновым сгустком, и вызванную тромбином агрегацию тромбоцитов. В экспериментальных исследованиях на различных моделях тромбоза in vivo >in vivo и ex vivo подтверждено антитромботическое действие и антикоагулянтная активность дабигатрана после в/в введения и дабигатрана этексилата - после приема внутрь. Установлена прямая корреляция между концентрацией дабигатрана в плазме крови и выраженностью антикоагулянтного эффекта. Дабигатран удлиняет АЧТВ, экариновое время свертывания (ЭВС) и тромбиновое время (ТВ).
Профилактика венозных тромбоэмболий (ВТЭ) после эндопротезирования крупных суставов.
Результаты клинических исследований у пациентов, перенесших ортопедические операции - эндопротезирование коленного и тазобедренного суставов - подтвердили сохранение параметров гемостаза и эквивалентность применения 75 или 110 мг дабигатрана этексилата через 1-4 ч после операции и последующей поддерживающей дозы 150 или 220 мг один раз в сутки в течение 6-10 дней (при операции на коленном суставе) и 28-35 дней (на тазобедренном суставе) по сравнению с эноксапарином натрия в дозе 40 мг 1 раз в сутки, который применяли накануне и после операции.
Показана эквивалентность антитромботического эффекта дабигатрана этексилата при применении 150 или 220 мг по сравнению с эноксапарином натрия в дозе 40 мг в сутки при оценке основной конечной точки, которая включает все случаи ВТЭ и смертность от любых причин.
Профилактика инсульта и системных тромбоэмболий у пациентов с фибрилляцией предсердий.
При длительном, в среднем около 20 мес, применении у пациентов с фибрилляцией предсердий и умеренным или высоким риском инсульта или системных тромбоэмболий было показано, что дабигатрана этексилат в дозе 110 мг, назначенный 2 раза в день, не уступал варфарину по эффективности предотвращения инсульта и системных тромбоэмболий у пациентов с фибрилляцией предсердий; также в группе дабигатрана было отмечено снижение риска внутричерепных кровотечений и общей частоты кровотечений. Применение более высокой дозы (150 мг 2 раза в день) достоверно снижало риск ишемического и геморрагического инсультов, сердечно-сосудистой смертности, внутричерепных кровотечений и общей частоты кровотечений по сравнению с варфарином. Меньшая доза дабигатрана характеризовалась существенно более низким риском больших кровотечений по сравнению с варфарином.
Чистый клинический эффект оценивался путем определения комбинированной конечной точки, включавшей частоту инсульта, системных тромбоэмболий, легочных тромбоэмболий, острого инфаркта миокарда, сердечно-сосудистой смертности и больших кровотечений.
Ежегодная частота перечисленных событий у пациентов, получавших дабигатрана этексилат, была ниже, чем у пациентов, получавших варфарин.
Изменения в лабораторных показателях функции печени у пациентов, получавших дабигатрана этексилат, отмечались со сравнимой или меньшей частотой по сравнению с пациентами, получавшими варфарин.
Профилактика тромбоэмболии у пациентов с протезированными клапанами сердца.
В ходе клинических исследований фазы II применения дабигатрана и варфарина у пациентов, перенесших операцию по замене клапана сердца механическим протезом (недавно проведенные операции и операции, проведенные более 3 мес назад), было выявлено повышение частоты тромбоэмболий и общего числа кровотечений (преимущественно за счет малых кровотечений) у пациентов, получавших дабигатрана этексилат. В раннем послеоперационном периоде большие кровотечения в основном характеризовались геморрагическим выпотом в перикард, особенно у пациентов, которым дабигатрана этексилат был назначен в раннем периоде (на 3-й день) после хирургической замены клапанов сердца.
RxList.com.
Тромбоэмболические осложнения и кровотечения у пациентов с протезированными клапанами сердца.
Безопасность и эффективность дабигатрана этексилата оценивали в исследовании RE-ALIGN, в котором пациенты с двустворчатыми механическими протезами клапанов сердца (недавно имплантированные или имплантированные более чем за 3 мес до включения пациентов в исследование) были рандомизированы в группы для получения варфарина или дабигатрана этексилата в дозах 150, 220 или 300 мг дважды в день. Исследование RE-ALIGN было прекращено досрочно в связи с большей частотой тромбоэмболий (тромбоз клапана, инсульт, транзиторная ишемическая атака и инфаркт миокарда) и больших кровотечений (преимущественно послеоперационный выпот в перикард, требующий вмешательства для восстановления гемодинамического равновесия) в группах лечения дабигатраном по сравнению с группой лечения варфарином. Эти кровотечения и тромбоэмболические осложнения были отмечены как у пациентов, которые начали прием дабигатрана этексилата в течение трех дней после операции по имплантации механического клапана, так и у пациентов, у которых клапаны были имплантированы более чем за 3 мес до включения в исследование. В связи с этим применение дабигатрана этексилата противопоказано пациентам с наличием механических протезов клапанов ( см «Противопоказания»).
Применение дабигатрана этексилата для профилактики тромбоэмболических осложнений у пациентов с фибрилляцией предсердий или при наличии других форм заболеваний клапанов сердца, включая наличие биопротеза сердечного клапана, не изучено и не рекомендуется.
Лечение острого тромбоза глубоких вен (ТГВ) и/или тромбоэмболии легочной артерии (ТЭЛА) и профилактика смертельных исходов, вызываемых этими заболеваниями.
Результаты клинических исследований у пациентов с наличием острого ТГВ и/или ТЭЛА, которые первоначально получали парентеральную терапию в течение как минимум 5 дней, подтвердили, что дабигатрана этексилат в дозе 150 мг, назначенный 2 раза в день, не уступал варфарину по эффективности в отношении снижения частоты рецидивирующего симптоматического ТГВ и/или ТЭЛА и случаев смерти, обусловленных этими заболеваниями, на протяжении 6-месячного периода лечения. У пациентов, получавших дабигатрана этексилат, кровотечения отмечались значительно реже, чем у пациентов, получавших варфарин.
Частота развития инфаркта миокарда во всех проводимых исследованиях при ВТЭ во всех лечебных группах была низкой.
Показатели функции печени. В исследованиях с применением активных препаратов сравнения возможные изменения показателей функции печени возникали у пациентов, получавших дабигатрана этексилат, со сравнимой или меньшей частотой, чем у пациентов, получавших варфарин. В исследовании с плацебо существенного различия в отношении изменений показателей функции печени, возможно имеющих клиническое значение, между группами с применением дабигатрана и плацебо не отмечалось.
Профилактика рецидивирующего ТГВ и/или ТЭЛА и смертельных исходов, вызываемых этими заболеваниями.
Результаты клинического исследования у пациентов с рецидивирующим ТГВ и ТЭЛА, уже получавших в течение от 3 до 12 мес антикоагулянтную терапию и нуждавшихся в ее продолжении, подтвердили, что лечение дабигатрана этексилатом в дозе 150 мг два раза в день не уступало лечебному эффекту варфарина (р=0,0135). У пациентов, получавших дабигатрана этексилат, кровотечения отмечались значительно реже, чем у пациентов, получавших варфарин.
В исследовании сравнения дабигатрана этексилата с плацебо у пациентов, уже получавших в течение от 6 до 18 мес антагонисты витамина было установлено, что дабигатран превосходил плацебо в отношении профилактики рецидивирующего симптоматического ТГВ/ТЭЛА, включая случаи смерти от неустановленной причины; снижение риска за период лечения составило 92% (р<0,0001).
Частота развития инфаркта миокарда во всех проводимых исследованиях при ВТЭ во всех лечебных группах была низкой.
Показатели функции печени. В исследованиях с применением активных препаратов сравнения возможные изменения показателей функции печени возникали у пациентов, получавших дабигатрана этексилат, со сравнимой или меньшей частотой, чем у пациентов, получавших варфарин. В исследовании с плацебо существенного различия в отношении изменений показателей функции печени, возможно имеющих клиническое значение, между группами с применением дабигатрана и плацебо не отмечалось.
Дабигатрана этексилат является низкомолекулярным, не обладающим фармакологической активностью предшественником активной формы дабигатрана. После приема внутрь дабигатрана этексилат быстро всасывается в ЖКТ и путем гидролиза, катализируемого эстеразами, в печени и плазме крови превращается в дабигатран. Дабигатран является сильным конкурентным обратимым прямым ингибитором тромбина и основным активным веществом в плазме крови. Поскольку тромбин (сериновая протеаза) в процессе коагуляции превращает фибриноген в фибрин, угнетение активности тромбина препятствует образованию тромба. Дабигатран оказывает ингибирующее воздействие на свободный тромбин, тромбин, связанный с фибриновым сгустком, и вызванную тромбином агрегацию тромбоцитов. В экспериментальных исследованиях на различных моделях тромбоза in vivo >in vivo и ex vivo подтверждено антитромботическое действие и антикоагулянтная активность дабигатрана после в/в введения и дабигатрана этексилата - после приема внутрь. Установлена прямая корреляция между концентрацией дабигатрана в плазме крови и выраженностью антикоагулянтного эффекта. Дабигатран удлиняет АЧТВ, экариновое время свертывания (ЭВС) и тромбиновое время (ТВ).
Профилактика венозных тромбоэмболий (ВТЭ) после эндопротезирования крупных суставов.
Результаты клинических исследований у пациентов, перенесших ортопедические операции - эндопротезирование коленного и тазобедренного суставов - подтвердили сохранение параметров гемостаза и эквивалентность применения 75 или 110 мг дабигатрана этексилата через 1-4 ч после операции и последующей поддерживающей дозы 150 или 220 мг один раз в сутки в течение 6-10 дней (при операции на коленном суставе) и 28-35 дней (на тазобедренном суставе) по сравнению с эноксапарином натрия в дозе 40 мг 1 раз в сутки, который применяли накануне и после операции.
Показана эквивалентность антитромботического эффекта дабигатрана этексилата при применении 150 или 220 мг по сравнению с эноксапарином натрия в дозе 40 мг в сутки при оценке основной конечной точки, которая включает все случаи ВТЭ и смертность от любых причин.
Профилактика инсульта и системных тромбоэмболий у пациентов с фибрилляцией предсердий.
При длительном, в среднем около 20 мес, применении у пациентов с фибрилляцией предсердий и умеренным или высоким риском инсульта или системных тромбоэмболий было показано, что дабигатрана этексилат в дозе 110 мг, назначенный 2 раза в день, не уступал варфарину по эффективности предотвращения инсульта и системных тромбоэмболий у пациентов с фибрилляцией предсердий; также в группе дабигатрана было отмечено снижение риска внутричерепных кровотечений и общей частоты кровотечений. Применение более высокой дозы (150 мг 2 раза в день) достоверно снижало риск ишемического и геморрагического инсультов, сердечно-сосудистой смертности, внутричерепных кровотечений и общей частоты кровотечений по сравнению с варфарином. Меньшая доза дабигатрана характеризовалась существенно более низким риском больших кровотечений по сравнению с варфарином.
Чистый клинический эффект оценивался путем определения комбинированной конечной точки, включавшей частоту инсульта, системных тромбоэмболий, легочных тромбоэмболий, острого инфаркта миокарда, сердечно-сосудистой смертности и больших кровотечений.
Ежегодная частота перечисленных событий у пациентов, получавших дабигатрана этексилат, была ниже, чем у пациентов, получавших варфарин.
Изменения в лабораторных показателях функции печени у пациентов, получавших дабигатрана этексилат, отмечались со сравнимой или меньшей частотой по сравнению с пациентами, получавшими варфарин.
Профилактика тромбоэмболии у пациентов с протезированными клапанами сердца.
В ходе клинических исследований фазы II применения дабигатрана и варфарина у пациентов, перенесших операцию по замене клапана сердца механическим протезом (недавно проведенные операции и операции, проведенные более 3 мес назад), было выявлено повышение частоты тромбоэмболий и общего числа кровотечений (преимущественно за счет малых кровотечений) у пациентов, получавших дабигатрана этексилат. В раннем послеоперационном периоде большие кровотечения в основном характеризовались геморрагическим выпотом в перикард, особенно у пациентов, которым дабигатрана этексилат был назначен в раннем периоде (на 3-й день) после хирургической замены клапанов сердца.
RxList.com.
Тромбоэмболические осложнения и кровотечения у пациентов с протезированными клапанами сердца.
Безопасность и эффективность дабигатрана этексилата оценивали в исследовании RE-ALIGN, в котором пациенты с двустворчатыми механическими протезами клапанов сердца (недавно имплантированные или имплантированные более чем за 3 мес до включения пациентов в исследование) были рандомизированы в группы для получения варфарина или дабигатрана этексилата в дозах 150, 220 или 300 мг дважды в день. Исследование RE-ALIGN было прекращено досрочно в связи с большей частотой тромбоэмболий (тромбоз клапана, инсульт, транзиторная ишемическая атака и инфаркт миокарда) и больших кровотечений (преимущественно послеоперационный выпот в перикард, требующий вмешательства для восстановления гемодинамического равновесия) в группах лечения дабигатраном по сравнению с группой лечения варфарином. Эти кровотечения и тромбоэмболические осложнения были отмечены как у пациентов, которые начали прием дабигатрана этексилата в течение трех дней после операции по имплантации механического клапана, так и у пациентов, у которых клапаны были имплантированы более чем за 3 мес до включения в исследование. В связи с этим применение дабигатрана этексилата противопоказано пациентам с наличием механических протезов клапанов ( см «Противопоказания»).
Применение дабигатрана этексилата для профилактики тромбоэмболических осложнений у пациентов с фибрилляцией предсердий или при наличии других форм заболеваний клапанов сердца, включая наличие биопротеза сердечного клапана, не изучено и не рекомендуется.
Лечение острого тромбоза глубоких вен (ТГВ) и/или тромбоэмболии легочной артерии (ТЭЛА) и профилактика смертельных исходов, вызываемых этими заболеваниями.
Результаты клинических исследований у пациентов с наличием острого ТГВ и/или ТЭЛА, которые первоначально получали парентеральную терапию в течение как минимум 5 дней, подтвердили, что дабигатрана этексилат в дозе 150 мг, назначенный 2 раза в день, не уступал варфарину по эффективности в отношении снижения частоты рецидивирующего симптоматического ТГВ и/или ТЭЛА и случаев смерти, обусловленных этими заболеваниями, на протяжении 6-месячного периода лечения. У пациентов, получавших дабигатрана этексилат, кровотечения отмечались значительно реже, чем у пациентов, получавших варфарин.
Частота развития инфаркта миокарда во всех проводимых исследованиях при ВТЭ во всех лечебных группах была низкой.
Показатели функции печени. В исследованиях с применением активных препаратов сравнения возможные изменения показателей функции печени возникали у пациентов, получавших дабигатрана этексилат, со сравнимой или меньшей частотой, чем у пациентов, получавших варфарин. В исследовании с плацебо существенного различия в отношении изменений показателей функции печени, возможно имеющих клиническое значение, между группами с применением дабигатрана и плацебо не отмечалось.
Профилактика рецидивирующего ТГВ и/или ТЭЛА и смертельных исходов, вызываемых этими заболеваниями.
Результаты клинического исследования у пациентов с рецидивирующим ТГВ и ТЭЛА, уже получавших в течение от 3 до 12 мес антикоагулянтную терапию и нуждавшихся в ее продолжении, подтвердили, что лечение дабигатрана этексилатом в дозе 150 мг два раза в день не уступало лечебному эффекту варфарина (р=0,0135). У пациентов, получавших дабигатрана этексилат, кровотечения отмечались значительно реже, чем у пациентов, получавших варфарин.
В исследовании сравнения дабигатрана этексилата с плацебо у пациентов, уже получавших в течение от 6 до 18 мес антагонисты витамина было установлено, что дабигатран превосходил плацебо в отношении профилактики рецидивирующего симптоматического ТГВ/ТЭЛА, включая случаи смерти от неустановленной причины; снижение риска за период лечения составило 92% (р<0,0001).
Частота развития инфаркта миокарда во всех проводимых исследованиях при ВТЭ во всех лечебных группах была низкой.
Показатели функции печени. В исследованиях с применением активных препаратов сравнения возможные изменения показателей функции печени возникали у пациентов, получавших дабигатрана этексилат, со сравнимой или меньшей частотой, чем у пациентов, получавших варфарин. В исследовании с плацебо существенного различия в отношении изменений показателей функции печени, возможно имеющих клиническое значение, между группами с применением дабигатрана и плацебо не отмечалось.
|
|
Фармакокинетика
После перорального применения дабигатрана этексилата отмечается быстрое дозозависимое увеличение его концентрации в плазме крови и AUC. Сmах дабигатрана этексилата достигается в течение 0,5-2.
После достижения сmах плазменные концентрации дабигатрана снижаются биэкспоненциально, конечный 1/2T1/2 в среднем составляет около 11 ч (у людей пожилого возраста). Конечный 1/2T1/2 после многократного применения дабигатрана этексилата составлял около 12-14 Т1/2 не зависит от дозы. Однако в случае нарушения функции почек Т1/2 удлиняется.
Абсолютная биодоступность дабигатрана после приема дабигатрана этексилата внутрь в капсулах, покрытых оболочкой из гипромеллозы, составляет около 6,5%. Прием пищи не влияет на биодоступность дабигатрана этексилата, однако время достижения Сmах возрастает на 2.
При использовании дабигатрана этексилата без специальной капсульной оболочки, изготовленной из гипромеллозы, биодоступность дабигатрана по сравнению с ЛФ в капсулах может увеличиваться примерно на 75% (в 1,8 раза) при однократном приеме и примерно на 37% (в 1,4 раза) в равновесном состоянии. Поэтому следует сохранять целостность капсул, изготовленных из гипромеллозы, учитывая риск повышения биодоступности дабигатрана этексилата, и не рекомендуется вскрывать капсулы и применять их содержимое в чистом виде (например добавляя в пищу или напитки). При применении дабигатрана этексилата через 1-3 ч у пациентов после оперативного лечения отмечается снижение скорости его всасывания по сравнению со здоровыми добровольцами. AUC характеризуется постепенным повышением амплитуды без появления высокого пика концентрации в плазме. Сmах в плазме крови отмечается через 6 ч после применения дабигатрана этексилата или через 7-9 ч после операции. Следует отметить, что такие факторы, как анестезия, парез ЖКТ и хирургическая операция могут иметь значение в замедлении всасывания, независимо от ЛФ препарата. Снижение скорости всасывания препарата отмечается обычно только в день операции. В последующие дни всасывание происходит быстро, с достижением Сmах через 2 ч после приема дабигатрана этексилата внутрь.
Метаболизм. После приема внутрь в процессе гидролиза под влиянием эстеразы дабигатрана этексилат быстро и полностью превращается в дабигатран, который является основным активным метаболитом в плазме крови. При конъюгации дабигатрана образуется 4 изомера фармакологически активных ацилглюкуронидов: 1-О, 2-О, 3-О, 4-О, каждый из которых составляет менее 10% от общего содержания дабигатрана в плазме крови. Следы других метаболитов обнаруживаются только при использовании высокочувствительных аналитических методов.
Распределение. dVd дабигатрана составляет 60-70 л и превосходит объем общего содержания воды в организме, что указывает на умеренное распределение дабигатрана в тканях.
Выведение. Дабигатран выводится в неизмененном виде, преимущественно почками (85%), и только 6% - через ЖКТ. Установлено, что через 168 ч после введения меченного радиоактивного препарата 88-94% его дозы выводится из организма.
Дабигатран обладает низкой способностью связывания с белками плазмы крови (34-35%), она не зависит от концентрации препарата.
Особые группы пациентов.
Пожилые пациенты. У лиц пожилого возраста значение AUC выше, чем у молодых лиц, в 1,4-1,6 раза (на 4-60%), а Сmах - более чем в 1,25 раза (на 25%).
Наблюдаемые изменения коррелировали с возрастным снижением клиренса креатинина.
У женщин пожилого возраста (старше 65 лет) величины AUCτ,ss и сmax,ss были примерно в 1,9 и в 1,6 раза выше, чем у женщин молодого возраста (18-40 лет), а у мужчин пожилого возраста - в 2,2 и 2 раза выше, чем у мужчин молодого возраста. В исследовании у пациентов с фибрилляцией предсердий подтверждено влияние возраста на экспозицию дабигатрана: исходные концентрации дабигатрана у пациентов в возрасте ≥75 лет были примерно в 1,3 раза (на 31%) выше, а у пациентов в возрасте <65 лет - примерно на 22% ниже, чем у пациентов в возрасте 65-75 лет.
Нарушение функции почек. У добровольцев с умеренным нарушением функции почек (Cl креатинина - 30-50 мл/мин) значение AUC дабигатрана после приема внутрь было приблизительно в 3 раза больше, чем у лиц с неизмененной функцией почек.
У пациентов с тяжелыми нарушениями функции почек (Cl креатинина - 10-30 мл/мин) значения AUC дабигатрана этексилата и Т1/2 возрастали соответственно в 6 и 2 раза, по сравнению с аналогичными показателями у лиц без нарушений функции почек.
У пациентов с фибрилляцией предсердий и умеренной почечной недостаточностью (Cl креатинина 30-50 мл/мин) концентрации дабигатрана до и после применения препарата были в среднем в 2,29 и 1,81 раза выше, чем у пациентов без нарушения функции почек. При лечении острого ТГВ и/или ТЭЛА и профилактики смертельных исходов, вызываемых этими заболеваниями, у пациентов с легкой и умеренной степенью почечной недостаточности (Cl креатинина 30-50 мл/мин), базальные концентрации дабигатрана в период устойчивого состояния фармакокинетики были в среднем в 1,7 и в 3,4 раза выше, чем у пациентов с сl креатинина >80 мл/мин.
При использовании гемодиализа у пациентов без фибрилляции предсердий было установлено, что количество выводившегося препарата пропорционально скорости тока крови. Длительность диализа, со скоростью тока диализата 700 мл/мин. составляла 4 а скорость тока крови - 200 мл/мин или 350-390 мл/мин. Это приводило к удалению соответственно 50 и 60% концентраций свободного и общего дабигатрана. Антикоагулянтная активность дабигатрана снижалась по мере уменьшения концентраций в плазме, взаимосвязь ФК и ФД не менялась.
Нарушение функции печени. У пациентов с умеренным нарушением функции печени (7-9 баллов по шкале Чайлд-Пью) не было выявлено изменений концентрации дабигатрана в плазме крови по сравнению с пациентами без нарушения функции печени.
Масса тела. В исследованиях базальные концентрации дабигатрана у пациентов с массой тела >100 кг были примерно на 20% ниже, чем у пациентов с массой тела 50-100 кг. Масса тела у большинства (80,8%) пациентов составляла ≥50-<100 кг, в пределах этого диапазона явных различий концентраций дабигатрана не установлено. Данные в отношении пациентов с массой тела ≤50 кг ограничены.
Пол. В основных исследованиях по профилактике развития ВТЭ установлено, что воздействие препарата у женщин было примерно в 1,4-1,5 раза (на 40-50%) выше. У пациенток с фибрилляцией предсердий базальные концентрации и концентрации после применения дабигатрана этексилата были в среднем в 1,3 (на 30%) выше. Установленные различия не имели клинического значения.
Этнические группы. В сравнительном исследовании фармакокинетики дабигатрана этексилата у европейцев и японцев после однократного и повторного приема препарата в исследуемых этнических группах не было выявлено клинически значимых различий. Фармакокинетические исследования у пациентов негроидной расы ограничены, однако имеющиеся данные указывают на отсутствие значимых различий.
После достижения сmах плазменные концентрации дабигатрана снижаются биэкспоненциально, конечный 1/2T1/2 в среднем составляет около 11 ч (у людей пожилого возраста). Конечный 1/2T1/2 после многократного применения дабигатрана этексилата составлял около 12-14 Т1/2 не зависит от дозы. Однако в случае нарушения функции почек Т1/2 удлиняется.
Абсолютная биодоступность дабигатрана после приема дабигатрана этексилата внутрь в капсулах, покрытых оболочкой из гипромеллозы, составляет около 6,5%. Прием пищи не влияет на биодоступность дабигатрана этексилата, однако время достижения Сmах возрастает на 2.
При использовании дабигатрана этексилата без специальной капсульной оболочки, изготовленной из гипромеллозы, биодоступность дабигатрана по сравнению с ЛФ в капсулах может увеличиваться примерно на 75% (в 1,8 раза) при однократном приеме и примерно на 37% (в 1,4 раза) в равновесном состоянии. Поэтому следует сохранять целостность капсул, изготовленных из гипромеллозы, учитывая риск повышения биодоступности дабигатрана этексилата, и не рекомендуется вскрывать капсулы и применять их содержимое в чистом виде (например добавляя в пищу или напитки). При применении дабигатрана этексилата через 1-3 ч у пациентов после оперативного лечения отмечается снижение скорости его всасывания по сравнению со здоровыми добровольцами. AUC характеризуется постепенным повышением амплитуды без появления высокого пика концентрации в плазме. Сmах в плазме крови отмечается через 6 ч после применения дабигатрана этексилата или через 7-9 ч после операции. Следует отметить, что такие факторы, как анестезия, парез ЖКТ и хирургическая операция могут иметь значение в замедлении всасывания, независимо от ЛФ препарата. Снижение скорости всасывания препарата отмечается обычно только в день операции. В последующие дни всасывание происходит быстро, с достижением Сmах через 2 ч после приема дабигатрана этексилата внутрь.
Метаболизм. После приема внутрь в процессе гидролиза под влиянием эстеразы дабигатрана этексилат быстро и полностью превращается в дабигатран, который является основным активным метаболитом в плазме крови. При конъюгации дабигатрана образуется 4 изомера фармакологически активных ацилглюкуронидов: 1-О, 2-О, 3-О, 4-О, каждый из которых составляет менее 10% от общего содержания дабигатрана в плазме крови. Следы других метаболитов обнаруживаются только при использовании высокочувствительных аналитических методов.
Распределение. dVd дабигатрана составляет 60-70 л и превосходит объем общего содержания воды в организме, что указывает на умеренное распределение дабигатрана в тканях.
Выведение. Дабигатран выводится в неизмененном виде, преимущественно почками (85%), и только 6% - через ЖКТ. Установлено, что через 168 ч после введения меченного радиоактивного препарата 88-94% его дозы выводится из организма.
Дабигатран обладает низкой способностью связывания с белками плазмы крови (34-35%), она не зависит от концентрации препарата.
Особые группы пациентов.
Пожилые пациенты. У лиц пожилого возраста значение AUC выше, чем у молодых лиц, в 1,4-1,6 раза (на 4-60%), а Сmах - более чем в 1,25 раза (на 25%).
Наблюдаемые изменения коррелировали с возрастным снижением клиренса креатинина.
У женщин пожилого возраста (старше 65 лет) величины AUCτ,ss и сmax,ss были примерно в 1,9 и в 1,6 раза выше, чем у женщин молодого возраста (18-40 лет), а у мужчин пожилого возраста - в 2,2 и 2 раза выше, чем у мужчин молодого возраста. В исследовании у пациентов с фибрилляцией предсердий подтверждено влияние возраста на экспозицию дабигатрана: исходные концентрации дабигатрана у пациентов в возрасте ≥75 лет были примерно в 1,3 раза (на 31%) выше, а у пациентов в возрасте <65 лет - примерно на 22% ниже, чем у пациентов в возрасте 65-75 лет.
Нарушение функции почек. У добровольцев с умеренным нарушением функции почек (Cl креатинина - 30-50 мл/мин) значение AUC дабигатрана после приема внутрь было приблизительно в 3 раза больше, чем у лиц с неизмененной функцией почек.
У пациентов с тяжелыми нарушениями функции почек (Cl креатинина - 10-30 мл/мин) значения AUC дабигатрана этексилата и Т1/2 возрастали соответственно в 6 и 2 раза, по сравнению с аналогичными показателями у лиц без нарушений функции почек.
У пациентов с фибрилляцией предсердий и умеренной почечной недостаточностью (Cl креатинина 30-50 мл/мин) концентрации дабигатрана до и после применения препарата были в среднем в 2,29 и 1,81 раза выше, чем у пациентов без нарушения функции почек. При лечении острого ТГВ и/или ТЭЛА и профилактики смертельных исходов, вызываемых этими заболеваниями, у пациентов с легкой и умеренной степенью почечной недостаточности (Cl креатинина 30-50 мл/мин), базальные концентрации дабигатрана в период устойчивого состояния фармакокинетики были в среднем в 1,7 и в 3,4 раза выше, чем у пациентов с сl креатинина >80 мл/мин.
При использовании гемодиализа у пациентов без фибрилляции предсердий было установлено, что количество выводившегося препарата пропорционально скорости тока крови. Длительность диализа, со скоростью тока диализата 700 мл/мин. составляла 4 а скорость тока крови - 200 мл/мин или 350-390 мл/мин. Это приводило к удалению соответственно 50 и 60% концентраций свободного и общего дабигатрана. Антикоагулянтная активность дабигатрана снижалась по мере уменьшения концентраций в плазме, взаимосвязь ФК и ФД не менялась.
Нарушение функции печени. У пациентов с умеренным нарушением функции печени (7-9 баллов по шкале Чайлд-Пью) не было выявлено изменений концентрации дабигатрана в плазме крови по сравнению с пациентами без нарушения функции печени.
Масса тела. В исследованиях базальные концентрации дабигатрана у пациентов с массой тела >100 кг были примерно на 20% ниже, чем у пациентов с массой тела 50-100 кг. Масса тела у большинства (80,8%) пациентов составляла ≥50-<100 кг, в пределах этого диапазона явных различий концентраций дабигатрана не установлено. Данные в отношении пациентов с массой тела ≤50 кг ограничены.
Пол. В основных исследованиях по профилактике развития ВТЭ установлено, что воздействие препарата у женщин было примерно в 1,4-1,5 раза (на 40-50%) выше. У пациенток с фибрилляцией предсердий базальные концентрации и концентрации после применения дабигатрана этексилата были в среднем в 1,3 (на 30%) выше. Установленные различия не имели клинического значения.
Этнические группы. В сравнительном исследовании фармакокинетики дабигатрана этексилата у европейцев и японцев после однократного и повторного приема препарата в исследуемых этнических группах не было выявлено клинически значимых различий. Фармакокинетические исследования у пациентов негроидной расы ограничены, однако имеющиеся данные указывают на отсутствие значимых различий.
Показания к применению
Профилактика венозных тромбоэмболий у пациентов после ортопедических операций. профилактика инсульта. системных тромбоэмболий и снижение сердечно-сосудистой смертности у пациентов с фибрилляцией предсердий. лечение острого тромбоза глубоких вен и/или тромбоэмболии легочной артерии и профилактика смертельных исходов. вызываемых этими заболеваниями. профилактика рецидивирующего тромбоза глубоких вен и/или тромбоэмболии легочной артерии и смертельных исходов. вызываемых этими заболеваниями.
|
|
Противопоказания
Известная гиперчувствительность к дабигатрану, дабигатрана этексилату.
Тяжелая степень почечной недостаточности (Cl креатинина <30 мл/мин).
Активное клинически значимое кровотечение, геморрагический диатез, спонтанное или фармакологически индуцированное нарушение гемостаза.
Поражение органов в результате клинически значимого кровотечения, включая геморрагический инсульт в течение 6 мес до начала терапии.
Существенный риск развития большого кровотечения из имеющегося или недавнего изъязвления ЖКТ. наличие злокачественных образований с высоким риском кровотечения. недавнее повреждение головного или спинного мозга. недавняя операция на головном или спинном мозге или офтальмологическая операция. недавнее внутричерепное кровоизлияние. наличие или подозрение на варикознорасширенные вены пищевода. врожденные артериовенозные дефекты. сосудистые аневризмы или большие внутрипозвоночные или внутримозговые сосудистые нарушения.
Одновременное назначение любых других антикоагулянтов. в тч нефракционированного гепарина. низкомолекулярных гепаринов (в тч эноксапарин натрия. далтепарин натрия). производных гепарина (в тч фондапаринукс натрия). пероральных антикоагулянтов (в тч варфарин. ривароксабан. апиксабан). за исключением случаев перехода лечения с или на дабигатрана этексилат или в случае применения нефракционированного гепарина в дозах. необходимых для поддержания центрального венозного или артериального катетера.
Одновременное назначение кетоконазола для системного применения, циклоспорина, итраконазола, такролимуса и дронедарона.
Нарушения функции печени и заболевания печени, которые могут повлиять на выживаемость.
Наличие протезированного клапана сердца.
Возраст до 18 лет (клинические данные отсутствуют).
Тяжелая степень почечной недостаточности (Cl креатинина <30 мл/мин).
Активное клинически значимое кровотечение, геморрагический диатез, спонтанное или фармакологически индуцированное нарушение гемостаза.
Поражение органов в результате клинически значимого кровотечения, включая геморрагический инсульт в течение 6 мес до начала терапии.
Существенный риск развития большого кровотечения из имеющегося или недавнего изъязвления ЖКТ. наличие злокачественных образований с высоким риском кровотечения. недавнее повреждение головного или спинного мозга. недавняя операция на головном или спинном мозге или офтальмологическая операция. недавнее внутричерепное кровоизлияние. наличие или подозрение на варикознорасширенные вены пищевода. врожденные артериовенозные дефекты. сосудистые аневризмы или большие внутрипозвоночные или внутримозговые сосудистые нарушения.
Одновременное назначение любых других антикоагулянтов. в тч нефракционированного гепарина. низкомолекулярных гепаринов (в тч эноксапарин натрия. далтепарин натрия). производных гепарина (в тч фондапаринукс натрия). пероральных антикоагулянтов (в тч варфарин. ривароксабан. апиксабан). за исключением случаев перехода лечения с или на дабигатрана этексилат или в случае применения нефракционированного гепарина в дозах. необходимых для поддержания центрального венозного или артериального катетера.
Одновременное назначение кетоконазола для системного применения, циклоспорина, итраконазола, такролимуса и дронедарона.
Нарушения функции печени и заболевания печени, которые могут повлиять на выживаемость.
Наличие протезированного клапана сердца.
Возраст до 18 лет (клинические данные отсутствуют).
Ограничения к использованию
С осторожностью при состояниях, повышающих риск кровотечения: возраст 75 лет и старше; умеренное снижение функции почек (Cl креатинина 30-50 мл/мин); одновременное применение ингибиторов P-gp (за исключением указанных в разделе «Противопоказания»); масса тела меньше 50 кг; одновременный прием ацетилсалициловой кислоты (АСК), НПВС, клопидогрела, СИОЗС и селективных ингибиторов обратного захвата норадреналина, а также других ЛС, применение которых может нарушать гемостаз; врожденные или приобретенные заболевания свертывающей системы крови; тромбоцитопения или функциональные дефекты тромбоцитов; недавно проведенная биопсия или перенесенная обширная травма; бактериальный эндокардит; эзофагит, гастрит или гастроэзофагеальная рефлюксная болезнь.
При беременности и кормлении грудью
Данные о применении дабигатрана этексилата во время беременности отсутствуют. Потенциальный риск у человека неизвестен.
В экспериментальных исследованиях не установлено неблагоприятное воздействие на фертильность или постнатальное развитие новорожденных.
Женщинам репродуктивного возраста следует избегать наступления беременности при лечении дабигатрана этексилатом. При наступлении беременности применение не рекомендуется, за исключением случаев, когда ожидаемая польза превышает возможный риск.
При необходимости применения в период грудного вскармливания в связи с отсутствием клинических данных грудное вскармливание рекомендуется прекратить (в качестве меры предосторожности).
RxList.com.
Категория действия на плод по FDA - с.
Адекватные и строго контролируемые испытания дабигатрана этексилата у беременных женщин не проведены.
Безопасность и эффективность дабигатрана этексилата в период родов и родоразрешения не были оценены в клинических испытаниях. Необходимо учитывать риск кровотечения при применении дабигатрана этексилата в такой ситуации.
Неизвестно, экскретируется ли дабигатран в грудное молоко женщин. Поскольку многие ЛС экскретируются в грудное молоко, из-за потенциальной возможности развития серьезных побочных реакций у детей, находящихся на грудном вскармливании, кормящим женщинам следует прекратить либо грудное вскармливание, либо применение дабигатрана этексилата (учитывая значимость лекарства для матери).
В экспериментальных исследованиях не установлено неблагоприятное воздействие на фертильность или постнатальное развитие новорожденных.
Женщинам репродуктивного возраста следует избегать наступления беременности при лечении дабигатрана этексилатом. При наступлении беременности применение не рекомендуется, за исключением случаев, когда ожидаемая польза превышает возможный риск.
При необходимости применения в период грудного вскармливания в связи с отсутствием клинических данных грудное вскармливание рекомендуется прекратить (в качестве меры предосторожности).
RxList.com.
Категория действия на плод по FDA - с.
Адекватные и строго контролируемые испытания дабигатрана этексилата у беременных женщин не проведены.
Безопасность и эффективность дабигатрана этексилата в период родов и родоразрешения не были оценены в клинических испытаниях. Необходимо учитывать риск кровотечения при применении дабигатрана этексилата в такой ситуации.
Неизвестно, экскретируется ли дабигатран в грудное молоко женщин. Поскольку многие ЛС экскретируются в грудное молоко, из-за потенциальной возможности развития серьезных побочных реакций у детей, находящихся на грудном вскармливании, кормящим женщинам следует прекратить либо грудное вскармливание, либо применение дабигатрана этексилата (учитывая значимость лекарства для матери).
Побочные эффекты
Побочные эффекты, выявленные при применении дабигатрана этексилата:
- с целью профилактики ВТЭ после ортопедических операций;
- для профилактики инсульта и системных тромбоэмболий у пациентов с фибрилляцией предсердий;
- для лечения острого ТГВ и/или ТЭЛА и профилактики смертельных исходов, вызываемых этими заболеваниями;
- для профилактики рецидивирующего ТГВ и/или ТЭЛА и смертельных исходов, вызываемых этими заболеваниями.
Классификация побочных реакций по частоте развития (количество зарегистрированных случаев/количество пациентов): очень часто - до 1/10 случаев. часто - от 1/100 до 1/10 случаев. редко - от 1/1000 до 1/100 случаев. неизвестно - побочные эффекты из опыта использования не могут быть оценены на основе имеющихся данных.
Таблица 1.
Дополнительные специфичные побочные эффекты, выявленные при профилактике ВТЭ у пациентов, которым проведены ортопедические операции.
Со стороны сосудов. Нечасто - кровотечение из операционной раны.
Общие расстройства и нарушения в месте введения. Редко - кровянистые выделения.
Повреждения. токсичность и осложнения послеоперационной обработки: часто - кровотечение после проведения обработки раны. нечасто - гематома после проведения обработки раны. выделения из раны после проведения процедур. секреция из раны. редко - анемия в послеоперационном периоде.
Хирургические и терапевтические процедуры. Редко - дренаж раны, дренаж после обработки раны.
RxList.com.
Опыт клинических исследований.
Поскольку клинические исследования проводятся с различным набором условий. частота встречаемости побочных реакций. наблюдаемых в этих исследованиях. не может непосредственно сравниваться с частотой в других клинических испытаниях и прогнозировать возникновение побочных эффектов в клинической практике.
Снижение риска инсульта и системных тромбоэмболий у пациентов с неклапанной фибрилляцией предсердий.
В исследовании RE-LY (Randomized Evaluation of Long-term Anticoagulant Therapy. Рандомизированная оценка длительной антикоагулянтной терапии) была получена информация по безопасности использования двух доз дабигатрана этексилата. а также варфарина.
Общее количество пациентов, получавших дабигатрана этексилат в дозе 110 мг дважды в день, было 5983, получавших дабигатрана этексилат в дозе 150 мг дважды в день - 6059, получавших варфарин - 5998. В этих трех группах воздействие осуществлялось >12 мес у 4936. 4939 и 5193 пациентов. >24 мес - у 2387. 2405 и 2470 пациентов. при средней экспозиции 20,5. 20,3 и 21,3 мес. всего человеко-лет 10,242. 10,261 и 10,659.
Прекращение применения ЛС в исследовании RE-LY.
Частота побочных реакций, приведших к прекращению лечения, составила 21% для принимавших дабигатрана этексилат в дозе 150 мг и 16% для получавших варфарин. Наиболее частыми побочными реакциями. приводящими к прекращению приема дабигатрана этексилата. были кровотечения и желудочно-кишечные события ( диспепсия. тошнота. боль в верхней части живота. желудочно-кишечные кровотечения. диарея).
Информация по дозировке дабигатрана этексилата 110 мг является ограниченной, поскольку эта доза не одобрена к применению по данному показанию.
Кровотечения.
Ниже приведены данные о частоте развития больших кровотечений в период лечения в исследовании RE-LY. Большое кровотечение определялось как кровотечение. сопровождающееся одним или несколькими из следующих признаков: уменьшение уровня гемоглобина на ≥2 г/дл. трансфузия ≥2 единиц эритроцитарной массы. кровотечение в жизненно-важной области или с фатальным исходом. Внутричерепное кровоизлияние включало внутримозговое (геморрагический инсульт), субарахноидальное и субдуральное кровоизлияние.
Подтвержденные случаи больших кровотечений у пациентов1 в период лечения.
Рядом с названием указано количество пациентов. у которых при приеме дабигатрана этексилата в дозе 150 мг было зафиксировано большое кровотечение. в скобках - частота данного кровотечения в процентах на 100 человеко-лет (%)2. через запятую - аналогичные данные в группе пациентов. применявших варфарин. далее - отношение рисков дабигатрана этексилат/варфарин (95% ДИ).
Дабигатрана этексилат в дозе 150 мг принимали 6059 пациентов, варфарин - 5998 пациента.
Большое кровотечение3: 350 (3,47), 374 (3,58), 0,97 (0,84; 1,12).
Внутричерепное кровоизлияние4: 23 (0,22), 82 (0,77), 0,29 (0,18; 0,46).
- Геморрагический инсульт5: 6 (0,06), 40 (0,37), 0,16 (0,07; 0,37).
- Другие типы внутричерепных кровоизлияний: 17 (0,17), 46 (0,43), 0,38 (0,22; 0,67).
Желудочно-кишечное кровотечение: 162 (1,59), 111 (1,05), 1,51 (1,19; 1,92).
Фатальное кровотечение6: 7 (0,07), 16 (0,15), 0,45 (0,19; 1,1).
- Внутричерепное кровоизлияние: 3 (0,03), 9 (0,08), 0,35 (0,09; 1,28).
- Внечерепное кровотечение7: 4 (0,04), 7 (0,07), 0,59 (0,17; 2,02).
1 Пациенты во время лечения или в течение 2 дней после прекращения исследования. Случаи больших кровотечений в пределах каждой подкатегории были подсчитаны один раз у одного пациента, но у пациентов могли быть случаи кровотечений из нескольких подкатегорий.
2 Годовая частота событий на 100 пациенто-лет = 100 × количество участников со случившимся событием/человеко-лет. Человеко-годы определялись как совокупное количество дней. прошедших с первого приема препарата до дня наступившего события. дня последнего приема препарата + 2. даты смерти (любая дата. наступившая первой) у всех леченных пациентов. поделенное на 365,25. В случае повторяющихся событий одной и той же категории, рассматривалось первое событие.
3 Определено как кровотечение. сопровождающееся одним или более из следующих признаков: уменьшение уровня гемоглобина на ≥2 г/дл. трансфузия ≥2 единиц эритроцитарной массы. кровотечение в жизненно-важной области или с фатальным исходом.
4 Внутричерепное кровоизлияние включало внутримозговое (геморрагический инсульт), субарахноидальное и субдуральное кровоизлияние.
5 По результатам анализа, проводимого во время лечения, основанного на безопасности в популяции.
6 Фатальное кровотечение: подтвержденное большое кровотечение, в соответствии с определенным выше, с констатацией исследователем фатального исхода, основной причиной которого явилось кровотечение.
7 Внечерепное фатальное кровотечение: большое кровотечение. в соответствии с определенным выше. и констатация смерти. основной причиной которой явилось кровотечение. но без симптоматики внутричерепного кровоизлияния на основе клинической оценки исследователя.
Более высокий уровень какого-либо желудочно-кишечного кровотечения отмечался у пациентов, получавших дабигатрана этексилат в дозе 150 мг, чем у пациентов, получавших варфарин (6,6 против 4,2% соответственно).
Риск больших кровотечений был сходным при приеме дабигатрана этексилата в дозе 150 мг и варфарина во всех основных подгруппах. определенных по исходным характеристикам. за исключением возраста. где наблюдалась тенденция к более высокой частоте больших кровотечений при приеме дабигатрана этексилата (отношение рисков 1,2. 95% ДИ: от 1 до 1,5) для пациентов ≥75 лет.
Желудочно-кишечные побочные реакции.
Пациенты, получавшие дабигатрана этексилат в дозе 150 мг, имели более высокую частоту желудочно-кишечных побочных реакций (35 против 24% пациентов, получавших варфарин). Обычно это были диспепсия (включая боль в верхней части живота. абдоминальную боль. дискомфорт в животе и дискомфорт в эпигастрии) и гастритоподобные симптомы (в тч ГЭРБ. эзофагит. эрозивный гастрит. желудочное кровотечение. геморрагический гастрит. геморрагический эрозивный гастрит. язва ЖКТ).
Реакции гиперчувствительности.
В исследовании RE-LY сообщалось о гиперчувствительности к ЛС (включая крапивницу, сыпь и зуд), аллергическом отеке, анафилактической реакции и анафилактическом шоке у <0,1% пациентов, получавших дабигатрана этексилат.
Лечение и профилактика рецидивирующего ТГВ и ТЭЛА.
Дабигатрана этексилат был изучен у 4387 пациентов в 4 базовых контролируемых параллельных рандомизированных двойных слепых испытаниях. Три из этих испытаний были актив-контролируемыми (варфарин) (RE-COVER, RE-COVER II и RE-MEDY) и одно исследование (RE-SONATE) было плацебо-контролируемым. Демографические характеристики были сходными между 4 контролируемыми исследованиями и между группами лечения в этих исследованиях. Приблизительно 60% пациентов были мужского пола, средний возраст - 55,1 лет. Большинство пациентов принадлежали к европеоидной расе (87,7%), 10,3% - монголоидной, 1,9% - негроидной со средним значением сl креатинина 105,6 мл/мин.
Случаи кровотечений в 4 контролируемых исследованиях были классифицированы как большие кровотечения при соответствии по крайней мере одному из следующих критериев: фатальное кровотечение. симптоматическое кровотечение в жизненноважной области или органе (внутриглазное. внутричерепное. интраспинальное или внутримышечное с синдромом сдавления. забрюшинное кровотечение. внутрисуставное кровотечение или перикардиальное кровотечение). кровотечение. вызывающее снижение уровня Hb на 2 г/дл (1,24 ммоль/л или более или ведущее к трансфузии 2 или более единиц цельной крови или эритроцитов).
В исследованиях RE-COVER и RE-COVER II было проведено сравнение дабигатрана этексилата в дозе 150 мг два раза в день с варфарином для лечения ТГВ и ТЭЛА.
Пациенты получали в течение 5-10 дней стандартную парентеральную антикоагулянтную терапию и в последующие 6 мес только пероральное лечение со средней экспозицией 164 дня.
Ниже приведены данные объединенного анализа результатов исследований RE-COVER и RE-COVER II о частоте развития кровотечений во время полного курса лечения. включая период парентерального лечения и период только перорального лечения после рандомизации.
Рядом с названием указано количество пациентов. у которых на фоне приема дабигатрана этексилата в дозе 150 мг дважды в день было зафиксировано кровотечение. в скобках - частота данного кровотечения в процентах. через запятую - аналогичные данные в группе пациентов. применявших варфарин. далее - отношение рисков (95% ДИ)3.
Дабигатрана этексилат в дозе 150 мг принимали 2553 пациента, варфарин - 2554 пациента.
Большое кровотечение1: 37 (1,4), 51 (2), 0,73 (0,48; 1,11).
- Фатальное кровотечение: 1 (0,04), 2 (0,1).
- Кровотечение в жизненноважной области или органе: 7 (0,3), 15 (0,6).
- Снижение уровня Hb ≥2 г/дл или трансфузия ≥2 единиц цельной крови или эритроцитов: 32 (1,3), 38 (1,5).
Большое кровотечение в различных областях2.
- Внутричерепное: 2 (0,1), 5 (0,2).
- Забрюшинное: 2 (0,1), 1 (0,04).
- Внутрисуставное: 2 (0,1), 4 (0,2).
- Внутримышечное: 2 (0,1), 6 (0,2).
- Желудочно-кишечное: 15 (0,6), 14 (0,5).
- Урогенитальное: 7 (0,3), 14 (0,5).
- Другое: 8 (0,3), 8 (0,3).
Клинически значимое кровотечение, не относящееся к большим: 101 (4), 170 (6,7), 0,58 (0,46; 0,75).
Любое кровотечение: 411 (16,1), 567 (22,7), 0,7 (0,61; 0,79).
Примечание: случай большого кровотечения может соответствовать более чем одному критерию.
1 Пациенты по меньшей мере с одним эпизодом большого кровотечения.
2 Область кровотечения указана по оценке исследователя. У пациентов могут быть кровотечения более чем в одном месте.
3 Доверительный интервал.
Частота любого из желудочно-кишечных кровотечений у пациентов, получавших дабигатрана этексилат в дозе 150 мг, составила 3,1% (2,4% при применении варфарина).
Исследования RE-MEDY и RE-SONATE представили информацию по безопасности использования дабигатрана этексилата для снижения риска рецидива ТГВ и ТЭЛА.
Исследование RE-MEDY - активконтролируемое исследование (варфарин). в котором 1430 пациентов. ранее в течение 3-12 мес получавших пероральную антикоагулянтную терапию. принимали дабигатрана этексилат в дозе 150 мг дважды в день. У пациентов, включенных в исследование RE-MEDY, продолжительность комбинированного лечения составила до >3 лет, средняя экспозиция - 473 дня.
Далее приведены данные исследования RE-MEDY о частоте развития кровотечений.
Рядом с названием указано количество пациентов. у которых на фоне приема дабигатрана этексилата в дозе 150 мг дважды в день было зафиксировано кровотечение. в скобках - частота данного кровотечения в процентах. через запятую - аналогичные данные в группе пациентов. применявших варфарин. далее - отношение рисков (95% ДИ)3.
Дабигатрана этексилат в дозе 150 мг принимали 1430 пациентов, варфарин - 1426 пациентов.
Большое кровотечение1: 13 (0,9), 25 (1,8), 0,54 (0,25; 1,16).
- Фатальное кровотечение: 0, 1 (0,1).
- Кровотечение в жизненноважной области или органе: 7 (0,5), 11 (0,8).
- Снижение уровня Hb ≥2 г/дл или трансфузия ≥2 единиц цельной крови или эритроцитов: 7 (0,5), 16 (1,1).
Большое кровотечение в различных областях2.
- Внутричерепное: 2 (0,1), 4 (0,3).
- Внутриглазное: 4 (0,3), 2 (0,1).
- Забрюшинное: 0, 1 (0,1).
- Внутрисуставное: 0, 2 (0,1).
- Внутримышечное: 0, 4 (0,3).
- Желудочно-кишечное: 4 (0,3), 8 (0,6).
- Урогенитальное: 1 (0,1), 1 (0,1).
- Другое: 2 (0,1), 4 (0,3).
Клинически значимое кровотечение, не относящееся к большим: 71 (5), 125 (8,8), 0,56 (0,42; 0,75).
Любое кровотечение: 278 (19,4), 373 (26,2), 0,71 (0,61; 0,83).
Примечание: случай большого кровотечения может соответствовать более чем одному критерию.
1 Пациенты по меньшей мере с одним эпизодом большого кровотечения.
2 Область кровотечения указана по оценке исследователя. У пациентов могут быть кровотечения более чем в одном месте.
3 Доверительный интервал.
В исследовании RE-MEDY частота любого желудочно-кишечного кровотечения у пациентов, получавших дабигатрана этексилат в дозе 150 мг, составила 3,1% (против 2,2% при применении варфарина).
RE-SONATE - плацебо-контролируемое исследование, в котором 684 пациента получали дабигатрана этексилат в дозе 150 мг дважды в день после 6-18 мес пероральной антикоагулянтной терапии. У пациентов, включенных в исследование RE-SONATE, продолжительность комбинированного лечения была до 9 мес, среднее значение экспозиции - 165 дней.
Далее приведены данные исследования RE-SONATE о частоте развития кровотечений.
Рядом с названием указано количество пациентов. у которых на фоне приеме дабигатрана этексилата в дозе 150 мг дважды в день было зафиксировано кровотечение. в скобках - частота данного кровотечения в процентах. через запятую - аналогичные данные в группе пациентов. применявших варфарин. далее - отношение рисков (95% ДИ)3.
Дабигатрана этексилат в дозе 150 мг принимали 684 пациента, варфарин - 659 пациентов.
Большое кровотечение1: 2 (0,3), 0.
Кровотечение в жизненноважной области или органе: 0, 0.
Желудочно-кишечное: 2 (0,3), 0.
Клинически значимое кровотечение, не относящееся к большим: 34 (5), 13 (2), 2,54 (1,34; 4,82).
Любое кровотечение: 72 (10,5), 40 (6,1), 1,77 (1,2; 2,61).
Примечание: случай большого кровотечения может соответствовать более чем одному критерию.
1 Пациенты по меньшей мере с одним эпизодом большого кровотечения.
2 Область кровотечения указана по оценке исследователя. У пациентов могут быть кровотечения более чем в одном месте.
3 Доверительный интервал.
В исследовании RE-SONATE частота любого желудочно-кишечного кровотечения у пациентов, получавших дабигатрана этексилат в дозе 150 мг, составила 0,7% (0,3% по сравнению с плацебо).
Клинические случаи развития инфаркта миокарда.
В актив-контролируемых исследованиях у пациентов с ВТЭ бóльшая частота развития клинически выраженного инфаркта миокарда была зарегистрирована у пациентов. получавших дабигатрана этексилат [20 (0,66 на 100 пациенто-лет)]. чем у пациентов. получавших варфарин [5 (0,17 на 100 пациенто-лет)]. В плацебо-контролируемом исследовании сходная частота нефатального и фатального клинически выраженного инфаркта миокарда была зарегистрирована у пациентов. получавших дабигатрана этексилат [1 (0,32 на 100 пациенто-лет)]. и у тех. кто получал плацебо [1 (0,34 на 100 пациенто-лет)].
Желудочно-кишечные побочные реакции.
В четырех базовых исследованиях у пациентов, получавших дабигатрана этексилат в дозе 150 мг, была сходная частота желудочно-кишечных побочных реакций (24,7 против 22,7% у получавших варфарин). Диспепсия (включая боль в верхней области живота. абдоминальную боль. дискомфорт в животе и дискомфорт в эпигастрии) была отмечена у 7,5% пациентов при приеме дабигатрана этексилата против 5,5% при приеме варфарина. гастритоподобные симптомы (включая гастрит. ГЭРБ. эзофагит. эрозивный гастрит и кровоизлияние) наблюдались в 3% случаев против 1,7% соответственно.
Реакции гиперчувствительности.
В 4-х базовых исследованиях гиперчувствительность к ЛС (включая крапивницу. сыпь и зуд). аллергический отек. анафилактическая реакция и анафилактический шок были отмечены у 0,1% пациентов. получавших дабигатрана этексилат.
Профилактика ТГВ и ТЭЛА после протезирования тазобедренного сустава.
В двух двойных слепых рандомизированных актив-контролируемых исследованиях дабигатрана этексилата (RE-NOVATE и RE-NOVATE II) участвовали 5476 пациентов. Демографические характеристики были схожи как между исследованиями, так и между группами лечения в этих исследованиях. Приблизительно 45,3% пациентов были мужского пола, средний возраст - 63,2 года. Большинство пациентов были европеоидной расы (96,1%), 3,6% - монголоидной и 0,3% - негроидной расы со средним значением сl креатинина 92 мл/мин.
Случаи кровотечения в исследованиях RE-NOVATE и RE-NOVATE II были классифицированы как большие кровотечения. если они удовлетворяли по крайней мере одному из следующих критериев: фатальное кровотечение. симптоматическое кровотечение в жизненно-важную область или орган (внутриглазное. внутричерепное. интраспинальное или забрюшинное кровотечение). кровотечение. вызывающее снижение уровня Hb на ≥2 г/дл (1,24 ммоль/л) или более. приводящее к трансфузии 2 или более единиц цельной крови или эритроцитарной массы. требующее прекращения лечения. являющееся причиной повторной операции.
В исследовании RE-NOVATE с целью оценки эффективности дабигатрана этексилата для профилактики ТГВ и ТЭЛА у пациентов. перенесших операцию протезирования тазобедренного сустава. сравнивали дабигатрана этексилат в дозе 75 мг внутрь через 1-4 ч после операции и затем в дозе 150 мг один раз в день. дабигатрана этексилат в дозе 110 мг внутрь через 1-4 ч после операции и затем 220 мг один раз в день и эноксапарин натрия при п/к введении 40 мг один раз в сутки. начиная с вечера перед операцией. В исследовании RE-NOVATE II для оценки эффективности дабигатрана этексилата в профилактике ТГВ и ТЭЛА у пациентов. перенесших операцию протезирования тазобедренного сустава. проведено сравнение дабигатрана этексилата в дозе 110 мг внутрь через 1-4 ч после операции и затем 220 мг один раз в день с эноксапарином натрия п/к 40 мг один раз в день. начиная с вечера перед операцией. В исследованиях RE-NOVATE и RE-NOVATE II пациенты в течение 28-35 дней получали дабигатрана этексилат или эноксапарин натрия со средней экспозицией 33 дня.
Ниже представлены данные, показывающие количество пациентов, у которых были зафиксированы кровотечения, в исследованиях RE-NOVATE и RE-NOVATE II. Рядом с названием указано количество пациентов. у которых при приеме дабигатрана этексилата было зафиксировано кровотечение. в скобках - частота данного кровотечения в процентах. через запятую - аналогичные данные в группе пациентов. применявших эноксапарин натрия.
Случаи кровотечения в исследовании RE-NOVATE.
Дабигатрана этексилат в дозе 220 мг принимали 1146 пациентов, эноксапарин натрия - 1154 пациента.
Большое кровотечение: 23 (2), 18 (1,6).
Клинически значимое небольшое кровотечение: 48 (4,2), 40 (3,5).
Любое кровотечение: 141 (12,3), 132 (11,4).
Случаи кровотечения в исследовании RE-NOVATE II.
Дабигатрана этексилат в дозе 220 мг принимали 1010 пациентов, эноксапарин натрия - 1003 пациента.
Большое кровотечение: 14 (1,4), 9 (0,9).
Клинически значимое небольшое кровотечение: 26 (2,6), 20 (2).
Любое кровотечение: 98 (9,7), 83 (8,3).
В двух исследованиях частота больших желудочно-кишечных кровотечений у пациентов. получавших дабигатрана этексилат и эноксапарин натрия. была одинаковой (0,1%). частота любых желудочно-кишечных кровотечений составила 1,4% на фоне приема дабигатрана этексилата в дозе 220 мг и 0,9% - при применении эноксапарина натрия.
Желудочно-кишечные побочные реакции.
В двух исследованиях частота желудочно-кишечных побочных реакций у пациентов, получавших дабигатрана этексилат в дозе 220 мг и эноксапарин натрия, была 39,5 и 39,5% соответственно. Диспепсия (включая боль в верхней части живота. абдоминальную боль. дискомфорт в животе и дискомфорт в эпигастрии) была зафиксирована у 4,1% пациентов. получавших дабигатрана этексилат в дозе 220 мг. и у 3,8% пациентов. получавших эноксапарин натрия. гастритоподобные симптомы (включая гастрит. ГЭРБ. эзофагит. эрозивный гастрит и желудочное кровотечение) - у 0,6 против 1% соответственно.
Реакции гиперчувствительности.
В двух исследованиях реакции гиперчувствительности к препарату (такие, как крапивница, сыпь и зуд) были отмечены у 0,3% пациентов, получавших дабигатрана этексилат в дозе 220 мг.
Клинические случаи развития инфаркта миокарда.
В двух исследованиях о развитии инфаркта миокарда сообщалось у 2 (0,1%) пациентов, получавших дабигатрана этексилат в дозе 220 мг, и у 6 (0,3%) пациентов, получавших эноксапарин натрия.
Постмаркетинговый опыт.
Дополнительные побочные реакции были выявлены в постмаркетинговый период использования дабигатрана этексилата. Поскольку сообщения об этих реакциях поступают добровольно от популяции неопределенного размера. как правило. не представляется возможным достоверно оценить их частоту или установить причинно-следственную связь с действием ЛС.
У пациентов были выявлены следующие побочные реакции: ангионевротический отек, тромбоцитопения, язва пищевода.
- с целью профилактики ВТЭ после ортопедических операций;
- для профилактики инсульта и системных тромбоэмболий у пациентов с фибрилляцией предсердий;
- для лечения острого ТГВ и/или ТЭЛА и профилактики смертельных исходов, вызываемых этими заболеваниями;
- для профилактики рецидивирующего ТГВ и/или ТЭЛА и смертельных исходов, вызываемых этими заболеваниями.
Классификация побочных реакций по частоте развития (количество зарегистрированных случаев/количество пациентов): очень часто - до 1/10 случаев. часто - от 1/100 до 1/10 случаев. редко - от 1/1000 до 1/100 случаев. неизвестно - побочные эффекты из опыта использования не могут быть оценены на основе имеющихся данных.
Таблица 1.
| Системно-органный класс/побочный эффект | Показание | |||
| Профилактика инсульта, системных тромбоэмболий и снижение сердечно-сосудистой смертности у пациентов с фибрилляцией предсердий | Профилактика ВТЭ у пациентов после ортопедических операций | Лечение острого ТГВ и/или ТЭЛА и профилактика смертельных исходов, вызываемых этими заболеваниями | Профилактика рецидивирующего ТГВ и/или ТЭЛА и смертельных исходов, вызываемых этими заболеваниями | |
| Частота возникновения | ||||
| Со стороны кроветворной и лимфатической системы: | ||||
| анемия | часто | нечасто | нечасто | редко |
| тромбоцитопения | нечасто | редко | редко | редко |
| Со стороны иммунной системы: | ||||
| реакции гиперчувствительности | нечасто | нечасто | нечасто | нечасто |
| - крапивница | редко | редко | редко | редко |
| - кожная сыпь | нечасто | редко | нечасто | нечасто |
| - кожный зуд | нечасто | редко | редко | редко |
| - бронхоспазм | неизвестно | неизвестно | неизвестно | неизвестно |
| ангионевротический отек | редко | редко | редко | редко |
| анафилактические реакции | неизвестно | неизвестно | неизвестно | неизвестно |
| Со стороны нервной системы: | ||||
| внутричерепное кровотечение | нечасто | редко | редко | редко |
| Со стороны сосудов: | ||||
| гематома | нечасто | нечасто | нечасто | нечасто |
| кровотечение | нечасто | редко | нечасто | нечасто |
| Со стороны органов дыхания, грудной клетки и средостения: | ||||
| носовое кровотечение | часто | нечасто | часто | часто |
| кровохарканье | нечасто | редко | нечасто | нечасто |
| Со стороны ЖКТ: | ||||
| желудочно-кишечные кровотечения | часто | нечасто | часто | часто |
| ректальные кровотечения | нечасто | нечасто | часто | часто |
| геморроидальные кровотечения | нечасто | нечасто | редко | нечасто |
| боль в животе | часто | редко | нечасто | нечасто |
| диарея | часто | нечасто | нечасто | нечасто |
| диспепсия | часто | редко | часто | часто |
| тошнота | часто | нечасто | нечасто | нечасто |
| изъязвление слизистой оболочки ЖКТ, в тч язва пищевода | нечасто | редко | нечасто | редко |
| гастроэзофагит | нечасто | редко | нечасто | нечасто |
| ГЭРБ | нечасто | редко | нечасто | нечасто |
| рвота | нечасто | нечасто | нечасто | нечасто |
| дисфагия | нечасто | редко | редко | редко |
| Со стороны гепатобилиарной системы: | ||||
| повышение активности печеночных трансаминаз | редко | нечасто | нечасто | нечасто |
| нарушение функции печени | нечасто | часто | нечасто | нечасто |
| гипербилирубинемия | редко | нечасто | неизвестно | неизвестно |
| Со стороны кожи и подкожных тканей: | ||||
| кожный геморрагический синдром | часто | нечасто | часто | часто |
| Скелетно-мышечные нарушения, нарушения со стороны соединительной ткани и костей: | ||||
| гемартроз | редко | нечасто | нечасто | редко |
| Со стороны почек и мочевыводящих путей: | ||||
| урогенитальные кровотечения | часто | нечасто | часто | часто |
| гематурия | часто | нечасто | часто | часто |
| Нарушения общего характера и изменения в месте проведения инъекций: | ||||
| кровотечения из места инъекции | редко | редко | редко | редко |
| кровотечения из места введения катетера | редко | редко | редко | редко |
| Повреждения, токсичность и осложнения от процедур: | ||||
| посттравматическое кровотечение | редко | нечасто | нечасто | редко |
| кровотечения из места операционного доступа | редко | редко | редко | редко |
Дополнительные специфичные побочные эффекты, выявленные при профилактике ВТЭ у пациентов, которым проведены ортопедические операции.
Со стороны сосудов. Нечасто - кровотечение из операционной раны.
Общие расстройства и нарушения в месте введения. Редко - кровянистые выделения.
Повреждения. токсичность и осложнения послеоперационной обработки: часто - кровотечение после проведения обработки раны. нечасто - гематома после проведения обработки раны. выделения из раны после проведения процедур. секреция из раны. редко - анемия в послеоперационном периоде.
Хирургические и терапевтические процедуры. Редко - дренаж раны, дренаж после обработки раны.
RxList.com.
Опыт клинических исследований.
Поскольку клинические исследования проводятся с различным набором условий. частота встречаемости побочных реакций. наблюдаемых в этих исследованиях. не может непосредственно сравниваться с частотой в других клинических испытаниях и прогнозировать возникновение побочных эффектов в клинической практике.
Снижение риска инсульта и системных тромбоэмболий у пациентов с неклапанной фибрилляцией предсердий.
В исследовании RE-LY (Randomized Evaluation of Long-term Anticoagulant Therapy. Рандомизированная оценка длительной антикоагулянтной терапии) была получена информация по безопасности использования двух доз дабигатрана этексилата. а также варфарина.
Общее количество пациентов, получавших дабигатрана этексилат в дозе 110 мг дважды в день, было 5983, получавших дабигатрана этексилат в дозе 150 мг дважды в день - 6059, получавших варфарин - 5998. В этих трех группах воздействие осуществлялось >12 мес у 4936. 4939 и 5193 пациентов. >24 мес - у 2387. 2405 и 2470 пациентов. при средней экспозиции 20,5. 20,3 и 21,3 мес. всего человеко-лет 10,242. 10,261 и 10,659.
Прекращение применения ЛС в исследовании RE-LY.
Частота побочных реакций, приведших к прекращению лечения, составила 21% для принимавших дабигатрана этексилат в дозе 150 мг и 16% для получавших варфарин. Наиболее частыми побочными реакциями. приводящими к прекращению приема дабигатрана этексилата. были кровотечения и желудочно-кишечные события ( диспепсия. тошнота. боль в верхней части живота. желудочно-кишечные кровотечения. диарея).
Информация по дозировке дабигатрана этексилата 110 мг является ограниченной, поскольку эта доза не одобрена к применению по данному показанию.
Кровотечения.
Ниже приведены данные о частоте развития больших кровотечений в период лечения в исследовании RE-LY. Большое кровотечение определялось как кровотечение. сопровождающееся одним или несколькими из следующих признаков: уменьшение уровня гемоглобина на ≥2 г/дл. трансфузия ≥2 единиц эритроцитарной массы. кровотечение в жизненно-важной области или с фатальным исходом. Внутричерепное кровоизлияние включало внутримозговое (геморрагический инсульт), субарахноидальное и субдуральное кровоизлияние.
Подтвержденные случаи больших кровотечений у пациентов1 в период лечения.
Рядом с названием указано количество пациентов. у которых при приеме дабигатрана этексилата в дозе 150 мг было зафиксировано большое кровотечение. в скобках - частота данного кровотечения в процентах на 100 человеко-лет (%)2. через запятую - аналогичные данные в группе пациентов. применявших варфарин. далее - отношение рисков дабигатрана этексилат/варфарин (95% ДИ).
Дабигатрана этексилат в дозе 150 мг принимали 6059 пациентов, варфарин - 5998 пациента.
Большое кровотечение3: 350 (3,47), 374 (3,58), 0,97 (0,84; 1,12).
Внутричерепное кровоизлияние4: 23 (0,22), 82 (0,77), 0,29 (0,18; 0,46).
- Геморрагический инсульт5: 6 (0,06), 40 (0,37), 0,16 (0,07; 0,37).
- Другие типы внутричерепных кровоизлияний: 17 (0,17), 46 (0,43), 0,38 (0,22; 0,67).
Желудочно-кишечное кровотечение: 162 (1,59), 111 (1,05), 1,51 (1,19; 1,92).
Фатальное кровотечение6: 7 (0,07), 16 (0,15), 0,45 (0,19; 1,1).
- Внутричерепное кровоизлияние: 3 (0,03), 9 (0,08), 0,35 (0,09; 1,28).
- Внечерепное кровотечение7: 4 (0,04), 7 (0,07), 0,59 (0,17; 2,02).
1 Пациенты во время лечения или в течение 2 дней после прекращения исследования. Случаи больших кровотечений в пределах каждой подкатегории были подсчитаны один раз у одного пациента, но у пациентов могли быть случаи кровотечений из нескольких подкатегорий.
2 Годовая частота событий на 100 пациенто-лет = 100 × количество участников со случившимся событием/человеко-лет. Человеко-годы определялись как совокупное количество дней. прошедших с первого приема препарата до дня наступившего события. дня последнего приема препарата + 2. даты смерти (любая дата. наступившая первой) у всех леченных пациентов. поделенное на 365,25. В случае повторяющихся событий одной и той же категории, рассматривалось первое событие.
3 Определено как кровотечение. сопровождающееся одним или более из следующих признаков: уменьшение уровня гемоглобина на ≥2 г/дл. трансфузия ≥2 единиц эритроцитарной массы. кровотечение в жизненно-важной области или с фатальным исходом.
4 Внутричерепное кровоизлияние включало внутримозговое (геморрагический инсульт), субарахноидальное и субдуральное кровоизлияние.
5 По результатам анализа, проводимого во время лечения, основанного на безопасности в популяции.
6 Фатальное кровотечение: подтвержденное большое кровотечение, в соответствии с определенным выше, с констатацией исследователем фатального исхода, основной причиной которого явилось кровотечение.
7 Внечерепное фатальное кровотечение: большое кровотечение. в соответствии с определенным выше. и констатация смерти. основной причиной которой явилось кровотечение. но без симптоматики внутричерепного кровоизлияния на основе клинической оценки исследователя.
Более высокий уровень какого-либо желудочно-кишечного кровотечения отмечался у пациентов, получавших дабигатрана этексилат в дозе 150 мг, чем у пациентов, получавших варфарин (6,6 против 4,2% соответственно).
Риск больших кровотечений был сходным при приеме дабигатрана этексилата в дозе 150 мг и варфарина во всех основных подгруппах. определенных по исходным характеристикам. за исключением возраста. где наблюдалась тенденция к более высокой частоте больших кровотечений при приеме дабигатрана этексилата (отношение рисков 1,2. 95% ДИ: от 1 до 1,5) для пациентов ≥75 лет.
Желудочно-кишечные побочные реакции.
Пациенты, получавшие дабигатрана этексилат в дозе 150 мг, имели более высокую частоту желудочно-кишечных побочных реакций (35 против 24% пациентов, получавших варфарин). Обычно это были диспепсия (включая боль в верхней части живота. абдоминальную боль. дискомфорт в животе и дискомфорт в эпигастрии) и гастритоподобные симптомы (в тч ГЭРБ. эзофагит. эрозивный гастрит. желудочное кровотечение. геморрагический гастрит. геморрагический эрозивный гастрит. язва ЖКТ).
Реакции гиперчувствительности.
В исследовании RE-LY сообщалось о гиперчувствительности к ЛС (включая крапивницу, сыпь и зуд), аллергическом отеке, анафилактической реакции и анафилактическом шоке у <0,1% пациентов, получавших дабигатрана этексилат.
Лечение и профилактика рецидивирующего ТГВ и ТЭЛА.
Дабигатрана этексилат был изучен у 4387 пациентов в 4 базовых контролируемых параллельных рандомизированных двойных слепых испытаниях. Три из этих испытаний были актив-контролируемыми (варфарин) (RE-COVER, RE-COVER II и RE-MEDY) и одно исследование (RE-SONATE) было плацебо-контролируемым. Демографические характеристики были сходными между 4 контролируемыми исследованиями и между группами лечения в этих исследованиях. Приблизительно 60% пациентов были мужского пола, средний возраст - 55,1 лет. Большинство пациентов принадлежали к европеоидной расе (87,7%), 10,3% - монголоидной, 1,9% - негроидной со средним значением сl креатинина 105,6 мл/мин.
Случаи кровотечений в 4 контролируемых исследованиях были классифицированы как большие кровотечения при соответствии по крайней мере одному из следующих критериев: фатальное кровотечение. симптоматическое кровотечение в жизненноважной области или органе (внутриглазное. внутричерепное. интраспинальное или внутримышечное с синдромом сдавления. забрюшинное кровотечение. внутрисуставное кровотечение или перикардиальное кровотечение). кровотечение. вызывающее снижение уровня Hb на 2 г/дл (1,24 ммоль/л или более или ведущее к трансфузии 2 или более единиц цельной крови или эритроцитов).
В исследованиях RE-COVER и RE-COVER II было проведено сравнение дабигатрана этексилата в дозе 150 мг два раза в день с варфарином для лечения ТГВ и ТЭЛА.
Пациенты получали в течение 5-10 дней стандартную парентеральную антикоагулянтную терапию и в последующие 6 мес только пероральное лечение со средней экспозицией 164 дня.
Ниже приведены данные объединенного анализа результатов исследований RE-COVER и RE-COVER II о частоте развития кровотечений во время полного курса лечения. включая период парентерального лечения и период только перорального лечения после рандомизации.
Рядом с названием указано количество пациентов. у которых на фоне приема дабигатрана этексилата в дозе 150 мг дважды в день было зафиксировано кровотечение. в скобках - частота данного кровотечения в процентах. через запятую - аналогичные данные в группе пациентов. применявших варфарин. далее - отношение рисков (95% ДИ)3.
Дабигатрана этексилат в дозе 150 мг принимали 2553 пациента, варфарин - 2554 пациента.
Большое кровотечение1: 37 (1,4), 51 (2), 0,73 (0,48; 1,11).
- Фатальное кровотечение: 1 (0,04), 2 (0,1).
- Кровотечение в жизненноважной области или органе: 7 (0,3), 15 (0,6).
- Снижение уровня Hb ≥2 г/дл или трансфузия ≥2 единиц цельной крови или эритроцитов: 32 (1,3), 38 (1,5).
Большое кровотечение в различных областях2.
- Внутричерепное: 2 (0,1), 5 (0,2).
- Забрюшинное: 2 (0,1), 1 (0,04).
- Внутрисуставное: 2 (0,1), 4 (0,2).
- Внутримышечное: 2 (0,1), 6 (0,2).
- Желудочно-кишечное: 15 (0,6), 14 (0,5).
- Урогенитальное: 7 (0,3), 14 (0,5).
- Другое: 8 (0,3), 8 (0,3).
Клинически значимое кровотечение, не относящееся к большим: 101 (4), 170 (6,7), 0,58 (0,46; 0,75).
Любое кровотечение: 411 (16,1), 567 (22,7), 0,7 (0,61; 0,79).
Примечание: случай большого кровотечения может соответствовать более чем одному критерию.
1 Пациенты по меньшей мере с одним эпизодом большого кровотечения.
2 Область кровотечения указана по оценке исследователя. У пациентов могут быть кровотечения более чем в одном месте.
3 Доверительный интервал.
Частота любого из желудочно-кишечных кровотечений у пациентов, получавших дабигатрана этексилат в дозе 150 мг, составила 3,1% (2,4% при применении варфарина).
Исследования RE-MEDY и RE-SONATE представили информацию по безопасности использования дабигатрана этексилата для снижения риска рецидива ТГВ и ТЭЛА.
Исследование RE-MEDY - активконтролируемое исследование (варфарин). в котором 1430 пациентов. ранее в течение 3-12 мес получавших пероральную антикоагулянтную терапию. принимали дабигатрана этексилат в дозе 150 мг дважды в день. У пациентов, включенных в исследование RE-MEDY, продолжительность комбинированного лечения составила до >3 лет, средняя экспозиция - 473 дня.
Далее приведены данные исследования RE-MEDY о частоте развития кровотечений.
Рядом с названием указано количество пациентов. у которых на фоне приема дабигатрана этексилата в дозе 150 мг дважды в день было зафиксировано кровотечение. в скобках - частота данного кровотечения в процентах. через запятую - аналогичные данные в группе пациентов. применявших варфарин. далее - отношение рисков (95% ДИ)3.
Дабигатрана этексилат в дозе 150 мг принимали 1430 пациентов, варфарин - 1426 пациентов.
Большое кровотечение1: 13 (0,9), 25 (1,8), 0,54 (0,25; 1,16).
- Фатальное кровотечение: 0, 1 (0,1).
- Кровотечение в жизненноважной области или органе: 7 (0,5), 11 (0,8).
- Снижение уровня Hb ≥2 г/дл или трансфузия ≥2 единиц цельной крови или эритроцитов: 7 (0,5), 16 (1,1).
Большое кровотечение в различных областях2.
- Внутричерепное: 2 (0,1), 4 (0,3).
- Внутриглазное: 4 (0,3), 2 (0,1).
- Забрюшинное: 0, 1 (0,1).
- Внутрисуставное: 0, 2 (0,1).
- Внутримышечное: 0, 4 (0,3).
- Желудочно-кишечное: 4 (0,3), 8 (0,6).
- Урогенитальное: 1 (0,1), 1 (0,1).
- Другое: 2 (0,1), 4 (0,3).
Клинически значимое кровотечение, не относящееся к большим: 71 (5), 125 (8,8), 0,56 (0,42; 0,75).
Любое кровотечение: 278 (19,4), 373 (26,2), 0,71 (0,61; 0,83).
Примечание: случай большого кровотечения может соответствовать более чем одному критерию.
1 Пациенты по меньшей мере с одним эпизодом большого кровотечения.
2 Область кровотечения указана по оценке исследователя. У пациентов могут быть кровотечения более чем в одном месте.
3 Доверительный интервал.
В исследовании RE-MEDY частота любого желудочно-кишечного кровотечения у пациентов, получавших дабигатрана этексилат в дозе 150 мг, составила 3,1% (против 2,2% при применении варфарина).
RE-SONATE - плацебо-контролируемое исследование, в котором 684 пациента получали дабигатрана этексилат в дозе 150 мг дважды в день после 6-18 мес пероральной антикоагулянтной терапии. У пациентов, включенных в исследование RE-SONATE, продолжительность комбинированного лечения была до 9 мес, среднее значение экспозиции - 165 дней.
Далее приведены данные исследования RE-SONATE о частоте развития кровотечений.
Рядом с названием указано количество пациентов. у которых на фоне приеме дабигатрана этексилата в дозе 150 мг дважды в день было зафиксировано кровотечение. в скобках - частота данного кровотечения в процентах. через запятую - аналогичные данные в группе пациентов. применявших варфарин. далее - отношение рисков (95% ДИ)3.
Дабигатрана этексилат в дозе 150 мг принимали 684 пациента, варфарин - 659 пациентов.
Большое кровотечение1: 2 (0,3), 0.
Кровотечение в жизненноважной области или органе: 0, 0.
Желудочно-кишечное: 2 (0,3), 0.
Клинически значимое кровотечение, не относящееся к большим: 34 (5), 13 (2), 2,54 (1,34; 4,82).
Любое кровотечение: 72 (10,5), 40 (6,1), 1,77 (1,2; 2,61).
Примечание: случай большого кровотечения может соответствовать более чем одному критерию.
1 Пациенты по меньшей мере с одним эпизодом большого кровотечения.
2 Область кровотечения указана по оценке исследователя. У пациентов могут быть кровотечения более чем в одном месте.
3 Доверительный интервал.
В исследовании RE-SONATE частота любого желудочно-кишечного кровотечения у пациентов, получавших дабигатрана этексилат в дозе 150 мг, составила 0,7% (0,3% по сравнению с плацебо).
Клинические случаи развития инфаркта миокарда.
В актив-контролируемых исследованиях у пациентов с ВТЭ бóльшая частота развития клинически выраженного инфаркта миокарда была зарегистрирована у пациентов. получавших дабигатрана этексилат [20 (0,66 на 100 пациенто-лет)]. чем у пациентов. получавших варфарин [5 (0,17 на 100 пациенто-лет)]. В плацебо-контролируемом исследовании сходная частота нефатального и фатального клинически выраженного инфаркта миокарда была зарегистрирована у пациентов. получавших дабигатрана этексилат [1 (0,32 на 100 пациенто-лет)]. и у тех. кто получал плацебо [1 (0,34 на 100 пациенто-лет)].
Желудочно-кишечные побочные реакции.
В четырех базовых исследованиях у пациентов, получавших дабигатрана этексилат в дозе 150 мг, была сходная частота желудочно-кишечных побочных реакций (24,7 против 22,7% у получавших варфарин). Диспепсия (включая боль в верхней области живота. абдоминальную боль. дискомфорт в животе и дискомфорт в эпигастрии) была отмечена у 7,5% пациентов при приеме дабигатрана этексилата против 5,5% при приеме варфарина. гастритоподобные симптомы (включая гастрит. ГЭРБ. эзофагит. эрозивный гастрит и кровоизлияние) наблюдались в 3% случаев против 1,7% соответственно.
Реакции гиперчувствительности.
В 4-х базовых исследованиях гиперчувствительность к ЛС (включая крапивницу. сыпь и зуд). аллергический отек. анафилактическая реакция и анафилактический шок были отмечены у 0,1% пациентов. получавших дабигатрана этексилат.
Профилактика ТГВ и ТЭЛА после протезирования тазобедренного сустава.
В двух двойных слепых рандомизированных актив-контролируемых исследованиях дабигатрана этексилата (RE-NOVATE и RE-NOVATE II) участвовали 5476 пациентов. Демографические характеристики были схожи как между исследованиями, так и между группами лечения в этих исследованиях. Приблизительно 45,3% пациентов были мужского пола, средний возраст - 63,2 года. Большинство пациентов были европеоидной расы (96,1%), 3,6% - монголоидной и 0,3% - негроидной расы со средним значением сl креатинина 92 мл/мин.
Случаи кровотечения в исследованиях RE-NOVATE и RE-NOVATE II были классифицированы как большие кровотечения. если они удовлетворяли по крайней мере одному из следующих критериев: фатальное кровотечение. симптоматическое кровотечение в жизненно-важную область или орган (внутриглазное. внутричерепное. интраспинальное или забрюшинное кровотечение). кровотечение. вызывающее снижение уровня Hb на ≥2 г/дл (1,24 ммоль/л) или более. приводящее к трансфузии 2 или более единиц цельной крови или эритроцитарной массы. требующее прекращения лечения. являющееся причиной повторной операции.
В исследовании RE-NOVATE с целью оценки эффективности дабигатрана этексилата для профилактики ТГВ и ТЭЛА у пациентов. перенесших операцию протезирования тазобедренного сустава. сравнивали дабигатрана этексилат в дозе 75 мг внутрь через 1-4 ч после операции и затем в дозе 150 мг один раз в день. дабигатрана этексилат в дозе 110 мг внутрь через 1-4 ч после операции и затем 220 мг один раз в день и эноксапарин натрия при п/к введении 40 мг один раз в сутки. начиная с вечера перед операцией. В исследовании RE-NOVATE II для оценки эффективности дабигатрана этексилата в профилактике ТГВ и ТЭЛА у пациентов. перенесших операцию протезирования тазобедренного сустава. проведено сравнение дабигатрана этексилата в дозе 110 мг внутрь через 1-4 ч после операции и затем 220 мг один раз в день с эноксапарином натрия п/к 40 мг один раз в день. начиная с вечера перед операцией. В исследованиях RE-NOVATE и RE-NOVATE II пациенты в течение 28-35 дней получали дабигатрана этексилат или эноксапарин натрия со средней экспозицией 33 дня.
Ниже представлены данные, показывающие количество пациентов, у которых были зафиксированы кровотечения, в исследованиях RE-NOVATE и RE-NOVATE II. Рядом с названием указано количество пациентов. у которых при приеме дабигатрана этексилата было зафиксировано кровотечение. в скобках - частота данного кровотечения в процентах. через запятую - аналогичные данные в группе пациентов. применявших эноксапарин натрия.
Случаи кровотечения в исследовании RE-NOVATE.
Дабигатрана этексилат в дозе 220 мг принимали 1146 пациентов, эноксапарин натрия - 1154 пациента.
Большое кровотечение: 23 (2), 18 (1,6).
Клинически значимое небольшое кровотечение: 48 (4,2), 40 (3,5).
Любое кровотечение: 141 (12,3), 132 (11,4).
Случаи кровотечения в исследовании RE-NOVATE II.
Дабигатрана этексилат в дозе 220 мг принимали 1010 пациентов, эноксапарин натрия - 1003 пациента.
Большое кровотечение: 14 (1,4), 9 (0,9).
Клинически значимое небольшое кровотечение: 26 (2,6), 20 (2).
Любое кровотечение: 98 (9,7), 83 (8,3).
В двух исследованиях частота больших желудочно-кишечных кровотечений у пациентов. получавших дабигатрана этексилат и эноксапарин натрия. была одинаковой (0,1%). частота любых желудочно-кишечных кровотечений составила 1,4% на фоне приема дабигатрана этексилата в дозе 220 мг и 0,9% - при применении эноксапарина натрия.
Желудочно-кишечные побочные реакции.
В двух исследованиях частота желудочно-кишечных побочных реакций у пациентов, получавших дабигатрана этексилат в дозе 220 мг и эноксапарин натрия, была 39,5 и 39,5% соответственно. Диспепсия (включая боль в верхней части живота. абдоминальную боль. дискомфорт в животе и дискомфорт в эпигастрии) была зафиксирована у 4,1% пациентов. получавших дабигатрана этексилат в дозе 220 мг. и у 3,8% пациентов. получавших эноксапарин натрия. гастритоподобные симптомы (включая гастрит. ГЭРБ. эзофагит. эрозивный гастрит и желудочное кровотечение) - у 0,6 против 1% соответственно.
Реакции гиперчувствительности.
В двух исследованиях реакции гиперчувствительности к препарату (такие, как крапивница, сыпь и зуд) были отмечены у 0,3% пациентов, получавших дабигатрана этексилат в дозе 220 мг.
Клинические случаи развития инфаркта миокарда.
В двух исследованиях о развитии инфаркта миокарда сообщалось у 2 (0,1%) пациентов, получавших дабигатрана этексилат в дозе 220 мг, и у 6 (0,3%) пациентов, получавших эноксапарин натрия.
Постмаркетинговый опыт.
Дополнительные побочные реакции были выявлены в постмаркетинговый период использования дабигатрана этексилата. Поскольку сообщения об этих реакциях поступают добровольно от популяции неопределенного размера. как правило. не представляется возможным достоверно оценить их частоту или установить причинно-следственную связь с действием ЛС.
У пациентов были выявлены следующие побочные реакции: ангионевротический отек, тромбоцитопения, язва пищевода.
|
|
Взаимодействие
Фармакокинетические взаимодействия.
Дабигатрана этексилат и дабигатран не метаболизируются ферментами микросомального окисления печени и не являются ни индукторами, ни ингибиторами активности изоферментов цитохрома Р450. Поэтому предполагается, что у дабигатрана отсутствуют клинически значимые фармакокинетические лекарственные взаимодействия с ЛС, метаболизм которых осуществляется изоферментами цитохрома Р450. В клинических исследованиях у здоровых добровольцев не выявлены какие-либо взаимодействия дабигатрана с аторвастатином (субстрат сYP3A4) и диклофенаком (субстрат сYP2C9).
Взаимодействия с ингибиторами/индукторами P-gp. Субстратом для транспортной молекулы P-gp является пролекарство дабигатрана этексилат, но не дабигатран. Поэтому проводилось изучение совместного применения с ингибиторами и индукторами транспортера P-gp. Одновременное использование ингибиторов P-gp (амиодарон, верапамил, хинидин, кетоконазол для системного применения, дронедарон, тикагрелор и кларитромицин) приводит к увеличению концентрации дабигатрана в плазме крови.
Одновременное применение с ингибиторами P-gp. Одновременное применение с такими ингибиторами P-gp, как кетоконазол для системного применения, циклоспорин, итраконазол, такролимус и дронедарон, противопоказано. Следует соблюдать осторожность при одновременном назначении с ингибиторами P-gp (например амиодарон, хинидин, верапамил и тикагрелор).
Амиодарон. При одновременном применении дабигатрана этексилата с однократной дозой амиодарона (600 мг), принимавшегося внутрь, степень и скорость всасывания амиодарона и его активного метаболита, дезэтиламиодарона, не изменялись. Значения AUC и Сmах дабигатрана увеличивались примерно в 1,6 и 1,5 раз (на 60 и 50%) соответственно.
В исследовании у пациентов с фибрилляцией предсердий концентрация дабигатрана увеличивалась не более чем на 14%, повышение риска кровотечений не было зарегистрировано. Рекомендуется наблюдение за пациентами, применяющими одновременно амиодарон и дабигатрана этексилат, в отношении риска кровотечения, в особенности при наличии почечной недостаточности (от слабой до умеренно выраженной).
Дронедарон. После одновременного применения дабигатрана этексилата и дронедарона в дозе 400 мг однократно, AUC0-∞ и Сmах дабигатрана увеличиваются в 2,1 и 1,9 раз (на 114 и 87%) соответственно, а после многократного применения дронедарона в дозе 400 мг в день - в 2,4 и 2,3 раза (на 136 и 125%) соответственно. После однократного и многократного применения дронедарона через 2 ч после приема дабигатрана этексилата AUC0-∞ возрастала в 1,3 и 1,6 раз соответственно. Дронедарон не влиял на конечный Т1/2 и почечный клиренс дабигатрана. Одновременное применение дабигатрана этексилата и дронедарона противопоказано.
Тикагрелор. После одновременного применения однократной дозы (75 мг) дабигатрана этексилата с нагрузочной дозой тикагрелора (180 мг) значения AUC0-∞ и Сmах дабигатрана увеличиваются в 1,73 и 1,95 раз (на 73 и 95%) соответственно. После многократного приема тикагрелора (90 мг два раза в день) это повышение воздействия дабигатрана (в отношении AUC0-∞ и Сmах) уменьшалось соответственно до 1,56 раза (до 56%) и до 1,46 раза (до 46%).
Концентрация дабигатрана у здоровых добровольцев повышалась в 1,26 раз (до 26%) при совместном применении с тикагрелором в стационарном состоянии или в 1,49 раз (до 49%) при применении нагрузочной дозы тикагрелора с совместным применением дабигатрана этексилата, принимавшегося в дозе 110 мг два раза в сутки. Повышение концентрации было менее выраженным, если нагрузочная доза (180 мг) тикагрелора принималась через 2 ч после приема дабигатрана (до 27%). Совместное назначение нагрузочной дозы (180 мг) тикагрелора и 110 мг дабигатрана этексилата (в стационарном состоянии) увеличивало показатели AUCτ,ss и сmax,ss дабигатрана в 1,49 и 1,65 раз (+49 и 65%) соответственно, по сравнению с приемом только дабигатрана этексилата. Если нагрузочная доза 180 мг тикагрелора давалась через 2 ч после приема 110 мг дабигатрана этексилата (в стационарном состоянии), степень повышения AUCτ,ss и сmax,ss дабигатрана уменьшалась до 1,27-кратной и 1,24-кратной (+27% и 24%) соответственно по сравнению с приемом только дабигатрана этексилата. Совместное назначение 90 мг тикагрелора 2 раза в сутки (поддерживающая доза) со 110 мг дабигатрана этексилата повышало корректированные показатели AUCτ,ss и Сmax,ss в 1,26 и 1,29 раз соответственно по сравнению с приемом только дабигатрана этексилата.
Верапамил. При одновременном применении дабигатрана этексилата с верапамилом, назначавшимся перорально, значения Сmах и AUC дабигатрана увеличивались в зависимости от времени применения и ЛФ верапамила.
Наибольшее повышение эффекта дабигатрана наблюдалось при использовании первой дозы верапамила в ЛФ с немедленным высвобождением, которая применялась за 1 ч до приема дабигатрана этексилата (Сmах повысилась на 180%, a AUC - на 150%). При использовании ЛФ верапамила с замедленным высвобождением этот эффект прогрессивно снижался (Сmах повысилась на 90%, a AUC - на 70%), также как при использовании многократных доз верапамила (Сmах повысилась на 60%, a AUC - на 50%), что может объясняться индукцией P-gp в ЖКТ при длительном применении верапамила.
При использовании верапамила через 2 ч после приема дабигатрана этексилата клинически значимых взаимодействий не наблюдалось (Сmах повышалась на 10%, a AUC - на 20%), поскольку через 2 ч дабигатран полностью всасывается.
В исследовании у пациентов с фибрилляцией предсердий концентрация дабигатрана увеличивалась не более чем на 21%, повышение риска кровотечений не было зарегистрировано.
Данные о взаимодействии дабигатрана этексилата с верапамилом, введенным парентерально, отсутствуют; клинически значимое взаимодействие не ожидается.
Кетоконазол. Кетоконазол для системного применения после однократного назначения в дозе 400 мг увеличивает AUC0-∞ и Сmах дабигатрана примерно в 2,4 раза (на 138 и 135%) соответственно, а после многократного назначения кетоконазола в дозе 400 мг в день - примерно в 2,5 раза (на 153 и 149%) соответственно. Кетоконазол не влиял на Тmах и конечный Т1/2. Одновременное применение дабигатрана этексилата и кетоконазола для системного применения противопоказано.
Кларитромицин. При одновременном применении кларитромицина в дозе 500 мг 2 раза в день с дабигатрана этексилатом клинически значимое фармакокинетическое взаимодействие не наблюдалось (Сmах повысилась на 15%, a AUC - на 19%).
Хинидин. Значения AUCτ,ss и сmax,ss дабигатрана при применении 2 раза в сутки в случае одновременного назначения с хинидином в дозе 200 мг каждые 2 ч до достижения суммарной дозы 1000 мг повышались в среднем соответственно на 53 и на 56%.
Взаимодействие с итраконазолом, такролимусом и циклоспорином не изучалось, однако из данных in vitro >in vitro можно ожидать схожего эффекта, как и от взаимодействия с кетоконазолом. Одновременное применение этих ингибиторов P-gp противопоказано.
Одновременное применение с субстратами для P-gp.
Дигоксин. В исследовании, проведенном с участием 24 здоровых испытуемых, при одновременном назначении дабигатрана этексилата с дигоксином не наблюдалось изменений концентрации дигоксина и клинически значимых изменений концентрации дабигатрана. При одновременном применении дабигатрана этексилата с дигоксином, являющимся субстратом P-gp, фармакокинетическое взаимодействие не наблюдалось. Ни дабигатран, ни пролекарство дабигатрана этексилат не являются клинически значимыми ингибиторами P-gp.
Одновременное применение с индукторами P-gp.
Следует избегать одновременного назначения дабигатрана этексилата и индукторов P-gp, поскольку совместное применение приводит к снижению воздействия дабигатрана ( см «Меры предосторожности»).
Рифампицин. Предварительное применение тест-индуктора рифампицина в дозе 600 мг в день в течение 7 дней приводило к снижению воздействия дабигатрана. После отмены рифампицина этот индуктивный эффект снижался, на 7-й день эффект дабигатрана был близок к исходному уровню. В течение последующих 7 дней дальнейшее увеличение биодоступности дабигатрана не наблюдалось.
Через 7 дней лечения рифампицином в дозе 600 мг ежедневно AUC0-∞ и Сmах общего дабигатрана были снижены на 67 и 66% соответственно.
Предполагается, что другие индукторы P-gp, такие как зверобой продырявленный или карбамазепин, могут также снижать концентрацию дабигатрана в плазме крови и должны применяться с осторожностью.
Одновременное применение с антиагрегантами.
Совместное применение дабигатрана этексилата с ЛС, влияющими на гемостаз или систему коагуляции, включая нефракционированый гепарин, низкомолекулярный гепарин, АСК, НПВС, антагонисты витамина может существенно повысить риск развития кровотечений.
Нефракционированный гепарин. Можно применять в дозах, необходимых для поддержания проходимости центрального венозного или артериального катетера.
АСК. Эффект одновременного применения дабигатрана этексилата и АСК на риск развития кровотечений был изучен у пациентов с фибрилляцией предсердий в рандомизированном исследовании II фазы совместного применения с АСК. При изучении одновременного применения дабигатрана этексилата в дозе 150 мг 2 раза в день и АСК у пациентов с фибрилляцией предсердий установлено, что риск кровотечений может повышаться с 12 до 18% (при использовании АСК в дозе 81 мг) и до 24% (при использовании АСК в дозе 325 мг).
НПВС. Применявшиеся НПВС для краткосрочной анальгезии после операций не повышали риск кровотечений при одновременном использовании с дабигатрана этексилатом. Длительное применение НПВС увеличивало риск кровотечения примерно на 50% как при совместном применении дабигатрана этексилата, так и варфарина.
Необходим тщательный контроль за признаками кровотечения в связи с риском развития при совместном применении с НПВС (T1/2 более 12 ч).
Низкомолекулярный гепарин. Специальных исследований по одновременному применению дабигатрана этексилата и низкомолекулярных гепаринов, таких как эноксапарин натрия, не проводилось.
Через 24 ч после трехдневного лечения (40 мг один раз в день) эноксапарином натрия экспозиция дабигатрана была ниже, чем после приема разовой дозы 220 мг дабигатрана этексилата.
Высокая активность анти-FXa/FII наблюдалась после применения дабигатрана этексилата с эноксапарином натрия по сравнению с лечением только дабигатрана этексилатом. Считается, что это связано с действием эноксапарина натрия и не имеет клинического значения. Другие тесты, связанные с антикоагулянтным действием дабигатрана, значительно не изменялись при предшествующем лечении эноксапарином натрия.
Клопидогрел. Установлено, что одновременное применение дабигатрана этексилата и клопидогрела не приводит к дополнительному увеличению времени капиллярного кровотечения в сравнении с монотерапией клопидогрелом. Кроме того показано, что значения AUCτ,ss и сmax,ss дабигатрана, а также параметры свертывания крови, которые контролировались для оценки эффекта дабигатрана (АЧТВ, ЭВС или ТВ (анти FIIa), а также степень ингибирования агрегации тромбоцитов (основной показатель эффекта клопидогрела) во время комбинированной терапии не изменялись по сравнению с соответствующими показателями в монотерапии. При использовании «нагрузочной» дозы клопидогрела (300 или 600 мг) значения AUCτ,ss и сmax,ss дабигатрана повышались на 30-40%.
Одновременное применение с ЛС, повышающими рН содержимого желудка.
Выявленные в ходе популяционного анализа изменения фармакокинетических параметров дабигатрана под влиянием ингибиторов протонной помпы и антацидных средств оказались клинически незначимыми, поскольку степень выраженности этих изменений была небольшой (снижение биодоступности не было значимым при назначении антацидов, а при использовании ингибиторов протонной помпы составляло 14,6%).
Установлено, что одновременное применение ингибиторов протонной помпы не сопровождается снижением концентрации дабигатрана и в среднем лишь незначительно снижает его концентрацию в плазме крови (на 11%). Поэтому одновременное применение ингибиторов протонной помпы, по-видимому, не ведет к повышению частоты инсульта или системных тромбоэмболий, особенно в сравнении с варфарином, и, следовательно, снижение биодоступности дабигатрана, вызываемое одновременным применением пантопразола, вероятно, не имеет клинической значимости.
Пантопразол. При совместном применении дабигатрана этексилата и пантопразола наблюдалось снижение AUC дабигатрана на 30%. Пантопразол и другие ингибиторы протонной помпы применялись совместно с дабигатрана этексилатом в клинических исследованиях, влияние на риск кровотечения или эффективность не наблюдалось.
Ранитидин. Ранитидин при применении одновременно с дабигатрана этексилатом, не оказывал значимое влияние на степень всасывания дабигатрана.
Дабигатрана этексилат и дабигатран не метаболизируются ферментами микросомального окисления печени и не являются ни индукторами, ни ингибиторами активности изоферментов цитохрома Р450. Поэтому предполагается, что у дабигатрана отсутствуют клинически значимые фармакокинетические лекарственные взаимодействия с ЛС, метаболизм которых осуществляется изоферментами цитохрома Р450. В клинических исследованиях у здоровых добровольцев не выявлены какие-либо взаимодействия дабигатрана с аторвастатином (субстрат сYP3A4) и диклофенаком (субстрат сYP2C9).
Взаимодействия с ингибиторами/индукторами P-gp. Субстратом для транспортной молекулы P-gp является пролекарство дабигатрана этексилат, но не дабигатран. Поэтому проводилось изучение совместного применения с ингибиторами и индукторами транспортера P-gp. Одновременное использование ингибиторов P-gp (амиодарон, верапамил, хинидин, кетоконазол для системного применения, дронедарон, тикагрелор и кларитромицин) приводит к увеличению концентрации дабигатрана в плазме крови.
Одновременное применение с ингибиторами P-gp. Одновременное применение с такими ингибиторами P-gp, как кетоконазол для системного применения, циклоспорин, итраконазол, такролимус и дронедарон, противопоказано. Следует соблюдать осторожность при одновременном назначении с ингибиторами P-gp (например амиодарон, хинидин, верапамил и тикагрелор).
Амиодарон. При одновременном применении дабигатрана этексилата с однократной дозой амиодарона (600 мг), принимавшегося внутрь, степень и скорость всасывания амиодарона и его активного метаболита, дезэтиламиодарона, не изменялись. Значения AUC и Сmах дабигатрана увеличивались примерно в 1,6 и 1,5 раз (на 60 и 50%) соответственно.
В исследовании у пациентов с фибрилляцией предсердий концентрация дабигатрана увеличивалась не более чем на 14%, повышение риска кровотечений не было зарегистрировано. Рекомендуется наблюдение за пациентами, применяющими одновременно амиодарон и дабигатрана этексилат, в отношении риска кровотечения, в особенности при наличии почечной недостаточности (от слабой до умеренно выраженной).
Дронедарон. После одновременного применения дабигатрана этексилата и дронедарона в дозе 400 мг однократно, AUC0-∞ и Сmах дабигатрана увеличиваются в 2,1 и 1,9 раз (на 114 и 87%) соответственно, а после многократного применения дронедарона в дозе 400 мг в день - в 2,4 и 2,3 раза (на 136 и 125%) соответственно. После однократного и многократного применения дронедарона через 2 ч после приема дабигатрана этексилата AUC0-∞ возрастала в 1,3 и 1,6 раз соответственно. Дронедарон не влиял на конечный Т1/2 и почечный клиренс дабигатрана. Одновременное применение дабигатрана этексилата и дронедарона противопоказано.
Тикагрелор. После одновременного применения однократной дозы (75 мг) дабигатрана этексилата с нагрузочной дозой тикагрелора (180 мг) значения AUC0-∞ и Сmах дабигатрана увеличиваются в 1,73 и 1,95 раз (на 73 и 95%) соответственно. После многократного приема тикагрелора (90 мг два раза в день) это повышение воздействия дабигатрана (в отношении AUC0-∞ и Сmах) уменьшалось соответственно до 1,56 раза (до 56%) и до 1,46 раза (до 46%).
Концентрация дабигатрана у здоровых добровольцев повышалась в 1,26 раз (до 26%) при совместном применении с тикагрелором в стационарном состоянии или в 1,49 раз (до 49%) при применении нагрузочной дозы тикагрелора с совместным применением дабигатрана этексилата, принимавшегося в дозе 110 мг два раза в сутки. Повышение концентрации было менее выраженным, если нагрузочная доза (180 мг) тикагрелора принималась через 2 ч после приема дабигатрана (до 27%). Совместное назначение нагрузочной дозы (180 мг) тикагрелора и 110 мг дабигатрана этексилата (в стационарном состоянии) увеличивало показатели AUCτ,ss и сmax,ss дабигатрана в 1,49 и 1,65 раз (+49 и 65%) соответственно, по сравнению с приемом только дабигатрана этексилата. Если нагрузочная доза 180 мг тикагрелора давалась через 2 ч после приема 110 мг дабигатрана этексилата (в стационарном состоянии), степень повышения AUCτ,ss и сmax,ss дабигатрана уменьшалась до 1,27-кратной и 1,24-кратной (+27% и 24%) соответственно по сравнению с приемом только дабигатрана этексилата. Совместное назначение 90 мг тикагрелора 2 раза в сутки (поддерживающая доза) со 110 мг дабигатрана этексилата повышало корректированные показатели AUCτ,ss и Сmax,ss в 1,26 и 1,29 раз соответственно по сравнению с приемом только дабигатрана этексилата.
Верапамил. При одновременном применении дабигатрана этексилата с верапамилом, назначавшимся перорально, значения Сmах и AUC дабигатрана увеличивались в зависимости от времени применения и ЛФ верапамила.
Наибольшее повышение эффекта дабигатрана наблюдалось при использовании первой дозы верапамила в ЛФ с немедленным высвобождением, которая применялась за 1 ч до приема дабигатрана этексилата (Сmах повысилась на 180%, a AUC - на 150%). При использовании ЛФ верапамила с замедленным высвобождением этот эффект прогрессивно снижался (Сmах повысилась на 90%, a AUC - на 70%), также как при использовании многократных доз верапамила (Сmах повысилась на 60%, a AUC - на 50%), что может объясняться индукцией P-gp в ЖКТ при длительном применении верапамила.
При использовании верапамила через 2 ч после приема дабигатрана этексилата клинически значимых взаимодействий не наблюдалось (Сmах повышалась на 10%, a AUC - на 20%), поскольку через 2 ч дабигатран полностью всасывается.
В исследовании у пациентов с фибрилляцией предсердий концентрация дабигатрана увеличивалась не более чем на 21%, повышение риска кровотечений не было зарегистрировано.
Данные о взаимодействии дабигатрана этексилата с верапамилом, введенным парентерально, отсутствуют; клинически значимое взаимодействие не ожидается.
Кетоконазол. Кетоконазол для системного применения после однократного назначения в дозе 400 мг увеличивает AUC0-∞ и Сmах дабигатрана примерно в 2,4 раза (на 138 и 135%) соответственно, а после многократного назначения кетоконазола в дозе 400 мг в день - примерно в 2,5 раза (на 153 и 149%) соответственно. Кетоконазол не влиял на Тmах и конечный Т1/2. Одновременное применение дабигатрана этексилата и кетоконазола для системного применения противопоказано.
Кларитромицин. При одновременном применении кларитромицина в дозе 500 мг 2 раза в день с дабигатрана этексилатом клинически значимое фармакокинетическое взаимодействие не наблюдалось (Сmах повысилась на 15%, a AUC - на 19%).
Хинидин. Значения AUCτ,ss и сmax,ss дабигатрана при применении 2 раза в сутки в случае одновременного назначения с хинидином в дозе 200 мг каждые 2 ч до достижения суммарной дозы 1000 мг повышались в среднем соответственно на 53 и на 56%.
Взаимодействие с итраконазолом, такролимусом и циклоспорином не изучалось, однако из данных in vitro >in vitro можно ожидать схожего эффекта, как и от взаимодействия с кетоконазолом. Одновременное применение этих ингибиторов P-gp противопоказано.
Одновременное применение с субстратами для P-gp.
Дигоксин. В исследовании, проведенном с участием 24 здоровых испытуемых, при одновременном назначении дабигатрана этексилата с дигоксином не наблюдалось изменений концентрации дигоксина и клинически значимых изменений концентрации дабигатрана. При одновременном применении дабигатрана этексилата с дигоксином, являющимся субстратом P-gp, фармакокинетическое взаимодействие не наблюдалось. Ни дабигатран, ни пролекарство дабигатрана этексилат не являются клинически значимыми ингибиторами P-gp.
Одновременное применение с индукторами P-gp.
Следует избегать одновременного назначения дабигатрана этексилата и индукторов P-gp, поскольку совместное применение приводит к снижению воздействия дабигатрана ( см «Меры предосторожности»).
Рифампицин. Предварительное применение тест-индуктора рифампицина в дозе 600 мг в день в течение 7 дней приводило к снижению воздействия дабигатрана. После отмены рифампицина этот индуктивный эффект снижался, на 7-й день эффект дабигатрана был близок к исходному уровню. В течение последующих 7 дней дальнейшее увеличение биодоступности дабигатрана не наблюдалось.
Через 7 дней лечения рифампицином в дозе 600 мг ежедневно AUC0-∞ и Сmах общего дабигатрана были снижены на 67 и 66% соответственно.
Предполагается, что другие индукторы P-gp, такие как зверобой продырявленный или карбамазепин, могут также снижать концентрацию дабигатрана в плазме крови и должны применяться с осторожностью.
Одновременное применение с антиагрегантами.
Совместное применение дабигатрана этексилата с ЛС, влияющими на гемостаз или систему коагуляции, включая нефракционированый гепарин, низкомолекулярный гепарин, АСК, НПВС, антагонисты витамина может существенно повысить риск развития кровотечений.
Нефракционированный гепарин. Можно применять в дозах, необходимых для поддержания проходимости центрального венозного или артериального катетера.
АСК. Эффект одновременного применения дабигатрана этексилата и АСК на риск развития кровотечений был изучен у пациентов с фибрилляцией предсердий в рандомизированном исследовании II фазы совместного применения с АСК. При изучении одновременного применения дабигатрана этексилата в дозе 150 мг 2 раза в день и АСК у пациентов с фибрилляцией предсердий установлено, что риск кровотечений может повышаться с 12 до 18% (при использовании АСК в дозе 81 мг) и до 24% (при использовании АСК в дозе 325 мг).
НПВС. Применявшиеся НПВС для краткосрочной анальгезии после операций не повышали риск кровотечений при одновременном использовании с дабигатрана этексилатом. Длительное применение НПВС увеличивало риск кровотечения примерно на 50% как при совместном применении дабигатрана этексилата, так и варфарина.
Необходим тщательный контроль за признаками кровотечения в связи с риском развития при совместном применении с НПВС (T1/2 более 12 ч).
Низкомолекулярный гепарин. Специальных исследований по одновременному применению дабигатрана этексилата и низкомолекулярных гепаринов, таких как эноксапарин натрия, не проводилось.
Через 24 ч после трехдневного лечения (40 мг один раз в день) эноксапарином натрия экспозиция дабигатрана была ниже, чем после приема разовой дозы 220 мг дабигатрана этексилата.
Высокая активность анти-FXa/FII наблюдалась после применения дабигатрана этексилата с эноксапарином натрия по сравнению с лечением только дабигатрана этексилатом. Считается, что это связано с действием эноксапарина натрия и не имеет клинического значения. Другие тесты, связанные с антикоагулянтным действием дабигатрана, значительно не изменялись при предшествующем лечении эноксапарином натрия.
Клопидогрел. Установлено, что одновременное применение дабигатрана этексилата и клопидогрела не приводит к дополнительному увеличению времени капиллярного кровотечения в сравнении с монотерапией клопидогрелом. Кроме того показано, что значения AUCτ,ss и сmax,ss дабигатрана, а также параметры свертывания крови, которые контролировались для оценки эффекта дабигатрана (АЧТВ, ЭВС или ТВ (анти FIIa), а также степень ингибирования агрегации тромбоцитов (основной показатель эффекта клопидогрела) во время комбинированной терапии не изменялись по сравнению с соответствующими показателями в монотерапии. При использовании «нагрузочной» дозы клопидогрела (300 или 600 мг) значения AUCτ,ss и сmax,ss дабигатрана повышались на 30-40%.
Одновременное применение с ЛС, повышающими рН содержимого желудка.
Выявленные в ходе популяционного анализа изменения фармакокинетических параметров дабигатрана под влиянием ингибиторов протонной помпы и антацидных средств оказались клинически незначимыми, поскольку степень выраженности этих изменений была небольшой (снижение биодоступности не было значимым при назначении антацидов, а при использовании ингибиторов протонной помпы составляло 14,6%).
Установлено, что одновременное применение ингибиторов протонной помпы не сопровождается снижением концентрации дабигатрана и в среднем лишь незначительно снижает его концентрацию в плазме крови (на 11%). Поэтому одновременное применение ингибиторов протонной помпы, по-видимому, не ведет к повышению частоты инсульта или системных тромбоэмболий, особенно в сравнении с варфарином, и, следовательно, снижение биодоступности дабигатрана, вызываемое одновременным применением пантопразола, вероятно, не имеет клинической значимости.
Пантопразол. При совместном применении дабигатрана этексилата и пантопразола наблюдалось снижение AUC дабигатрана на 30%. Пантопразол и другие ингибиторы протонной помпы применялись совместно с дабигатрана этексилатом в клинических исследованиях, влияние на риск кровотечения или эффективность не наблюдалось.
Ранитидин. Ранитидин при применении одновременно с дабигатрана этексилатом, не оказывал значимое влияние на степень всасывания дабигатрана.
|
|
Передозировка
Передозировка при применении дабигатрана этексилата может сопровождаться геморрагическими осложнениями, что обусловлено фармакодинамическими особенностями препарата. При возникновении кровотечения применение прекращают. Показано симптоматическое лечение. Учитывая основной путь выведения дабигатрана (почками), рекомендуется обеспечить адекватный диурез. Проводят хирургический гемостаз и восполнение ОЦК. Возможно использование свежей цельной крови или переливание свежезамороженной плазмы. Поскольку дабигатран обладает низкой способностью к связыванию с белками плазмы крови. он может выводиться при гемодиализе. однако клинический опыт по использованию диализа в этих ситуациях ограничен ( см «Фармакокинетика»).
При передозировке дабигатрана этексилата возможно использование концентратов факторов свертывания (активированных или неактивированных) или рекомбинантного фактора VIIа. Существуют экспериментальные данные, подтверждающие эффективность этих средств в устранении антикоагулянтного эффекта дабигатрана, однако специальных клинических исследований не проводилось.
В случае развития тромбоцитопении или при применении антиагрегантов длительного действия может быть рассмотрен вопрос о применении тромбоцитарной массы. Для ситуаций, когда требуется быстрое устранение активности, существует специфический антидот дабигатрана (идаруцизумаб), являющийся антагонистом по отношению к фармакодинамическому действию дабигатрана.
При передозировке дабигатрана этексилата возможно использование концентратов факторов свертывания (активированных или неактивированных) или рекомбинантного фактора VIIа. Существуют экспериментальные данные, подтверждающие эффективность этих средств в устранении антикоагулянтного эффекта дабигатрана, однако специальных клинических исследований не проводилось.
В случае развития тромбоцитопении или при применении антиагрегантов длительного действия может быть рассмотрен вопрос о применении тромбоцитарной массы. Для ситуаций, когда требуется быстрое устранение активности, существует специфический антидот дабигатрана (идаруцизумаб), являющийся антагонистом по отношению к фармакодинамическому действию дабигатрана.
Способ применения и дозы
Внутрь, 1 или 2 раза в день независимо от времени приема пищи. Доза (110-300 мг в сутки) и продолжительность лечения зависят от показаний.
Меры предосторожности применения
RxList.com.
Преждевременное прекращение приема дабигатрана этексилата повышает риск тромботических осложнений.
Преждевременное прекращение приема любого перорального антикоагулянта, включая дабигатрана этексилат, при отсутствии адекватной альтернативной антикоагулянтной терапии, увеличивает риск тромбообразования. Если прием дабигатрана этексилата прекращен по иной причине, кроме патологического кровотечения или завершения курса терапии, следует рассмотреть вопрос о применении другого антикоагулянта и возобновить прием дабигатрана этексилата как только это будет возможно с медицинской точки зрения.
Риск развития кровотечений.
Применение дабигатрана этексилата, так же как и других антикоагулянтов, рекомендуется с осторожностью при состояниях, характеризующихся повышенным риском кровотечений. Во время терапии дабигатрана этексилатом возможно развитие кровотечений различной локализации. Снижение концентрации Hb и/или гематокрита в крови, сопровождающееся снижением АД, является основанием для поиска источника кровотечения.
Лечение дабигатрана этексилатом не требует контроля антикоагулянтной активности. Тест для определения MHO применяться не должен, поскольку есть данные о ложном завышении уровня MHO.
Для выявления чрезмерной антикоагулянтной активности дабигатрана следует использовать тесты для определения ТВ или ЭВС. В случае, когда эти тесты недоступны, следует использовать тест для определения АЧТВ.
В исследовании RE-LY у пациентов с фибрилляцией предсердий превышение уровня АЧТВ в 2-3 раза выше границы нормы перед приемом очередной дозы дабигатрана этексилата было ассоциировано с повышенным риском кровотечения.
В фармакокинетических исследованиях дабигатрана этексилата показано, что у пациентов со сниженной функцией почек (в тч у пожилых пациентов) наблюдается повышение экспозиции препарата. Применение дабигатрана этексилата противопоказано в случае выраженных нарушений функции почек (Cl креатинина <30 мл/мин).
В случае развития острой почечной недостаточности дабигатрана этексилат следует отменить.
К повышению концентрации дагибатрана в плазме могут приводить следующие факторы: снижение функции почек (Cl креатинина 30-50 мл/мин), возраст ≥75 лет, одновременное применение ингибитора P-gp. Наличие одного или нескольких таких факторов может повышать риск кровотечения. Совместное применение дабигатрана этексилата с ЛС, влияющими на гемостаз или систему коагуляции, включая нефракционированый гепарин, низкомолекулярный гепарин, АСК, НПВС, антагонисты витамина может существенно повысить риск развития кровотечений.
Не изучалось, но может повышать риск кровотечений одновременное применение дабигатрана этексилата со следующими ЛС: фондапаринукс натрия, тромболитические препараты, блокаторы гликопротеиновых GP IIb/IIIa рецепторов тромбоцитов, тиклопидин, декстран, ривароксабан и ингибиторы P-gp (итраконазол, такролимус, циклоспорин, ритонавир, нелфинавир и саквинавир). Риск кровотечений может повышаться за счет фармакологического взаимодействия у пациентов, одновременно принимающих СИОЗС или селективные ингибиторы обратного захвата норадреналина. Также риск кровотечений может повышаться при одновременном применении антиагрегантов и других антикоагулянтов.
Совместное применение дронедарона и дабигатрана противопоказано ( см «Противопоказания»).
Одновременное применение тикагрелора может увеличивать воздействие дабигатрана и может приводить к фармакодинамическому взаимодействию, результатом которого может стать повышение риска кровотечений.
RxList.com.
Риск кровотечений.
Дабигатрана этексилат увеличивает риск кровотечений и может привести к значительным и иногда смертельным кровотечениям. Следует незамедлительно оценивать любые признаки или симптомы потери крови (например снижение уровня Hb и/или гематокрита или гипотензия). У пациентов с активным патологическим кровотечением прием дабигатрана этексилата необходимо прекратить.
Факторы риска развития кровотечения включают сопутствующее применение других ЛС, которые повышают риск кровотечения (например антитромбоцитарные средства, гепарин), фибринолитическую терапию, постоянное применение НПВС. Антикоагулянтная активность и 1/2T1/2 дабигатрана этексилата повышаются у пациентов с нарушением функции почек.
Инверсия антикоагулянтного эффекта.
Специфический антагонист дабигатрана - идаруцизумаб - применяется при необходимости прекращения антикоагулянтного действия дабигатрана:
- для экстренной хирургии/ургентных процедур;
- при жизнеугрожающем или неконтролируемом кровотечении.
Дабигатран может удаляться при гемодиализе, однако клинический опыт использования гемодиализа в качестве метода терапии кровотечения в данном случае ограничен ( см «Передозировка»).
Профилактика ВТЭ у пациентов после ортопедических операций.
Установлено, что применение НПВC для кратковременной анестезии при хирургических вмешательствах одновременно с дабигатрана этексилатом не сопровождается повышенным риском кровотечений. Имеются ограниченные данные о регулярном применении НПВC (имеющих Т1/2 менее 12 ч) на фоне лечения дабигатрана этексилатом, данных о повышении риска кровотечений не получено.
Профилактика инсульта, системных тромбоэмболий и снижение сердечно-сосудистой смертности у пациентов с фибрилляцией предсердий.
Одновременное применение дабигатрана этексилата, антиагрегантов (включая АСК и клопидогрел) и НПВС увеличивает риск кровотечения. В особенности одновременное применение антиагрегантов или сильных ингибиторов P-gp увеличивает риск больших кровотечений, в тч желудочно-кишечных кровотечений, у пациентов в возрасте ≥75 лет. Если возникают клинические подозрения на кровотечение, рекомендуется проведение соответствующих исследований, таких как анализ кала на скрытую кровь или определение уровня Hb (на предмет его снижения). Применение фибринолитических ЛС может рассматриваться только в случае, если показатели ТВ, ЭВС или АЧТВ у пациента не превышают ВГН.
При повышении риска кровотечений (например при недавно проведенной биопсии или перенесенной обширной травме, бактериальном эндокардите) требуется контроль состояния пациента с целью своевременного обнаружения признаков кровотечения.
Взаимодействие с индукторами P-gp.
Применение внутрь совместно с дабигатрана этексилатом индуктора P-gp рифампицина снижало концентрацию дабигатрана в плазме. Предполагается, что другие индукторы P-gp, такие как зверобой продырявленный или карбамазепин, могут также снижать концентрацию дабигатрана в плазме крови и должны применяться с осторожностью ( см «Взаимодействие»).
RxList.com.
Влияние индукторов и ингибиторов P-gp на экспозицию дабигатрана.
Сочетанное применение дабигатрана этексилата с индукторами P-gp (например рифампицин) снижает экспозицию дабигатрана и, как правило, их совместного применения следует избегать.
Применение индукторов P-gp и нарушение функции почек являются основными независимыми факторами, которые приводят к увеличению экспозиции дабигатрана. Сочетанное применение с ингибиторами P-gp у пациентов с нарушением функции почек, как ожидается, приведет к увеличению экспозиции дабигатрана по сравнению с таковой при влиянии только одного из двух факторов.
Хирургические операции и вмешательства.
У пациентов, применяющих дабигатрана этексилат при проведении хирургических операций или инвазивных процедур повышается риск кровотечений. Поэтому при проведении хирургических вмешательств следует отменить дабигатрана этексилат ( см «Фармакокинетика»).
Предоперационный период.
Перед проведением инвазивных процедур или хирургических операций дабигатрана этексилат отменяют по крайней мере за 24 ч до их проведения. У пациентов с повышенным риском кровотечений или перед проведением обширных операций, требующих полного гемостаза, следует прекратить применение дабигатрана этексилата за 2-4 дня до операции. У пациентов с почечной недостаточностью клиренс дабигатрана может удлиняться.
При отмене дабигатрана этексилата следует учитывать следующую информацию:
При сl креатинина ≥80 мл/мин, T1/2»13 ч и высоком риске кровотечения или проведении большой операции дабигатрана этексилат отменяют за 2 дня, при стандартном риске - за 24 при сl креатинина ≥50-<80 мл/мин, T1/2»15 ч - за 2-3 дня или 1-2 дня соответственно; при сl креатинина ≥30-<50 мл/мин, T1/2»18 ч - за 4 дня или за 2-3 дня (>48 ч) соответственно.
Это следует принимать во внимание перед проведением любых процедур ( см «Фармакокинетика»).
Дабигатрана этексилат противопоказан пациентам с тяжелыми нарушениями функции почек (Cl креатинина <30 мл/мин), но если препарат все же применяют, отменять его следует не менее чем за 5 дней до операции.
В случае необходимости проведения экстренного хирургического вмешательства прием дабигатрана этексилата необходимо временно прекратить. Хирургическое вмешательство, при наличии такой возможности, целесообразно выполнять не ранее чем через 12 ч после последнего приема дабигатрана этексилата. Если операция не может быть отложена, риск кровотечения может повышаться. В таком случае следует оценить соотношение риска кровотечения и необходимости экстренного проведения вмешательства.
Спиналъная анестезия/эпидуральная анестезия/люмбальная пункция.
Такие процедуры, как спинномозговая анестезия, могут потребовать полного восстановления гемостаза.
В случае травматичной или повторной спинномозговой пункции и длительного использования эпидурального катетера может повышаться риск развития спинномозгового кровотечения или эпидуральной гематомы. Первую дозу дабигатрана этексилата следует принимать не ранее, чем через 2 ч после удаления катетера. Необходим контроль состояния пациентов для исключения неврологических симптомов, которые могут быть обусловлены спинномозговым кровотечением или эпидуральной гематомой.
RxList.com.
Спиналъная/эпидуральная гематома.
Эпидуральная или спинальная гематомы могут возникнуть у пациентов, получавших дабигатрана этексилат, которым одновременно проводили нейроаксиальную анестезию или спинномозговую пункцию. Эти гематомы могут привести к длительному или постоянному параличу. Следует рассмотреть эти риски при планировании для пациентов процедур, связанных с позвоночником. Факторы, которые могут увеличивать риск развития эпидуральной или спинальной гематом у этих пациентов, включают:
- использование постоянного эпидурального катетера;
- сопутствующее применение других ЛС, влияющих на гемостаз, таких как НПВС, ингибиторы тромбоцитов, другие антикоагулянты;
- травматическая или неоднократные эпидуральная или спинальная пункции в анамнезе;
- деформация позвоночника или операции на позвоночнике в анамнезе.
Оптимальное время между приемом дабигатрана этексилата и нейроаксиальными процедурами неизвестно.
Для снижения потенциального риска кровотечения, связанного с одновременным применением дабигатрана и проведением эпидуральной или спинномозговой анестезии/анальгезии или спинномозговой пункции, следует учитывать фармакокинетический профиль дабигатрана ( см «Фармакология»). Установку или удаление эпидурального катетера или люмбальную пункцию лучше всего проводить, когда антикоагулянтный эффект дабигатрана низок; однако точное время достижения достаточно малого антикоагулянтного эффекта у каждого пациента неизвестно.
При необходимости проведения эпидуральной или спинальной анестезии/анальгезии или спинномозговой пункции на фоне лечения дабигатрана этексилатом, следует проводить частый мониторинг пациентов для выявления каких-либо признаков или симптомов неврологических нарушений, таких как боль в средней части спины, сенсорные или моторные нарушения (онемение, покалывание или слабость в нижних конечностях), дисфункция кишечника и/или мочевого пузыря. Необходимо проинструктировать пациентов о необходимости немедленно сообщать врачу, если они испытывают какие-либо из перечисленных выше признаков или симптомов. При подозрении на спинальную гематому следует провести срочную диагностику и лечение, включая рассмотрение вопроса о декомпрессии спинного мозга, даже если такое лечение может не помочь в предотвращении или обратном развитии неврологических осложнений.
Следует оценить преимущества и риски до проведения нейроаксиального вмешательства у пациентов, получающих антикоагулянты.
Период после проведения процедуры.
Применение дабигатрана этексилата можно продолжить по достижении полного гемостаза.
В случае появления желудочно-кишечных симптомов рекомендуется принимать дабигатрана этексилат с пищей и/или с ингибитором протонной помпы типа пантопразола.
Влияние на способность к управлению транспортными средствами и механизмами. Влияние дабигатрана этексилата на способность управлять транспортными средствами и заниматься другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций, не изучалось, но учитывая, что его применение может сопровождаться повышенным риском кровотечений, следует соблюдать осторожность при выполнении таких видов деятельности.
Преждевременное прекращение приема дабигатрана этексилата повышает риск тромботических осложнений.
Преждевременное прекращение приема любого перорального антикоагулянта, включая дабигатрана этексилат, при отсутствии адекватной альтернативной антикоагулянтной терапии, увеличивает риск тромбообразования. Если прием дабигатрана этексилата прекращен по иной причине, кроме патологического кровотечения или завершения курса терапии, следует рассмотреть вопрос о применении другого антикоагулянта и возобновить прием дабигатрана этексилата как только это будет возможно с медицинской точки зрения.
Риск развития кровотечений.
Применение дабигатрана этексилата, так же как и других антикоагулянтов, рекомендуется с осторожностью при состояниях, характеризующихся повышенным риском кровотечений. Во время терапии дабигатрана этексилатом возможно развитие кровотечений различной локализации. Снижение концентрации Hb и/или гематокрита в крови, сопровождающееся снижением АД, является основанием для поиска источника кровотечения.
Лечение дабигатрана этексилатом не требует контроля антикоагулянтной активности. Тест для определения MHO применяться не должен, поскольку есть данные о ложном завышении уровня MHO.
Для выявления чрезмерной антикоагулянтной активности дабигатрана следует использовать тесты для определения ТВ или ЭВС. В случае, когда эти тесты недоступны, следует использовать тест для определения АЧТВ.
В исследовании RE-LY у пациентов с фибрилляцией предсердий превышение уровня АЧТВ в 2-3 раза выше границы нормы перед приемом очередной дозы дабигатрана этексилата было ассоциировано с повышенным риском кровотечения.
В фармакокинетических исследованиях дабигатрана этексилата показано, что у пациентов со сниженной функцией почек (в тч у пожилых пациентов) наблюдается повышение экспозиции препарата. Применение дабигатрана этексилата противопоказано в случае выраженных нарушений функции почек (Cl креатинина <30 мл/мин).
В случае развития острой почечной недостаточности дабигатрана этексилат следует отменить.
К повышению концентрации дагибатрана в плазме могут приводить следующие факторы: снижение функции почек (Cl креатинина 30-50 мл/мин), возраст ≥75 лет, одновременное применение ингибитора P-gp. Наличие одного или нескольких таких факторов может повышать риск кровотечения. Совместное применение дабигатрана этексилата с ЛС, влияющими на гемостаз или систему коагуляции, включая нефракционированый гепарин, низкомолекулярный гепарин, АСК, НПВС, антагонисты витамина может существенно повысить риск развития кровотечений.
Не изучалось, но может повышать риск кровотечений одновременное применение дабигатрана этексилата со следующими ЛС: фондапаринукс натрия, тромболитические препараты, блокаторы гликопротеиновых GP IIb/IIIa рецепторов тромбоцитов, тиклопидин, декстран, ривароксабан и ингибиторы P-gp (итраконазол, такролимус, циклоспорин, ритонавир, нелфинавир и саквинавир). Риск кровотечений может повышаться за счет фармакологического взаимодействия у пациентов, одновременно принимающих СИОЗС или селективные ингибиторы обратного захвата норадреналина. Также риск кровотечений может повышаться при одновременном применении антиагрегантов и других антикоагулянтов.
Совместное применение дронедарона и дабигатрана противопоказано ( см «Противопоказания»).
Одновременное применение тикагрелора может увеличивать воздействие дабигатрана и может приводить к фармакодинамическому взаимодействию, результатом которого может стать повышение риска кровотечений.
RxList.com.
Риск кровотечений.
Дабигатрана этексилат увеличивает риск кровотечений и может привести к значительным и иногда смертельным кровотечениям. Следует незамедлительно оценивать любые признаки или симптомы потери крови (например снижение уровня Hb и/или гематокрита или гипотензия). У пациентов с активным патологическим кровотечением прием дабигатрана этексилата необходимо прекратить.
Факторы риска развития кровотечения включают сопутствующее применение других ЛС, которые повышают риск кровотечения (например антитромбоцитарные средства, гепарин), фибринолитическую терапию, постоянное применение НПВС. Антикоагулянтная активность и 1/2T1/2 дабигатрана этексилата повышаются у пациентов с нарушением функции почек.
Инверсия антикоагулянтного эффекта.
Специфический антагонист дабигатрана - идаруцизумаб - применяется при необходимости прекращения антикоагулянтного действия дабигатрана:
- для экстренной хирургии/ургентных процедур;
- при жизнеугрожающем или неконтролируемом кровотечении.
Дабигатран может удаляться при гемодиализе, однако клинический опыт использования гемодиализа в качестве метода терапии кровотечения в данном случае ограничен ( см «Передозировка»).
Профилактика ВТЭ у пациентов после ортопедических операций.
Установлено, что применение НПВC для кратковременной анестезии при хирургических вмешательствах одновременно с дабигатрана этексилатом не сопровождается повышенным риском кровотечений. Имеются ограниченные данные о регулярном применении НПВC (имеющих Т1/2 менее 12 ч) на фоне лечения дабигатрана этексилатом, данных о повышении риска кровотечений не получено.
Профилактика инсульта, системных тромбоэмболий и снижение сердечно-сосудистой смертности у пациентов с фибрилляцией предсердий.
Одновременное применение дабигатрана этексилата, антиагрегантов (включая АСК и клопидогрел) и НПВС увеличивает риск кровотечения. В особенности одновременное применение антиагрегантов или сильных ингибиторов P-gp увеличивает риск больших кровотечений, в тч желудочно-кишечных кровотечений, у пациентов в возрасте ≥75 лет. Если возникают клинические подозрения на кровотечение, рекомендуется проведение соответствующих исследований, таких как анализ кала на скрытую кровь или определение уровня Hb (на предмет его снижения). Применение фибринолитических ЛС может рассматриваться только в случае, если показатели ТВ, ЭВС или АЧТВ у пациента не превышают ВГН.
При повышении риска кровотечений (например при недавно проведенной биопсии или перенесенной обширной травме, бактериальном эндокардите) требуется контроль состояния пациента с целью своевременного обнаружения признаков кровотечения.
Взаимодействие с индукторами P-gp.
Применение внутрь совместно с дабигатрана этексилатом индуктора P-gp рифампицина снижало концентрацию дабигатрана в плазме. Предполагается, что другие индукторы P-gp, такие как зверобой продырявленный или карбамазепин, могут также снижать концентрацию дабигатрана в плазме крови и должны применяться с осторожностью ( см «Взаимодействие»).
RxList.com.
Влияние индукторов и ингибиторов P-gp на экспозицию дабигатрана.
Сочетанное применение дабигатрана этексилата с индукторами P-gp (например рифампицин) снижает экспозицию дабигатрана и, как правило, их совместного применения следует избегать.
Применение индукторов P-gp и нарушение функции почек являются основными независимыми факторами, которые приводят к увеличению экспозиции дабигатрана. Сочетанное применение с ингибиторами P-gp у пациентов с нарушением функции почек, как ожидается, приведет к увеличению экспозиции дабигатрана по сравнению с таковой при влиянии только одного из двух факторов.
Хирургические операции и вмешательства.
У пациентов, применяющих дабигатрана этексилат при проведении хирургических операций или инвазивных процедур повышается риск кровотечений. Поэтому при проведении хирургических вмешательств следует отменить дабигатрана этексилат ( см «Фармакокинетика»).
Предоперационный период.
Перед проведением инвазивных процедур или хирургических операций дабигатрана этексилат отменяют по крайней мере за 24 ч до их проведения. У пациентов с повышенным риском кровотечений или перед проведением обширных операций, требующих полного гемостаза, следует прекратить применение дабигатрана этексилата за 2-4 дня до операции. У пациентов с почечной недостаточностью клиренс дабигатрана может удлиняться.
При отмене дабигатрана этексилата следует учитывать следующую информацию:
При сl креатинина ≥80 мл/мин, T1/2»13 ч и высоком риске кровотечения или проведении большой операции дабигатрана этексилат отменяют за 2 дня, при стандартном риске - за 24 при сl креатинина ≥50-<80 мл/мин, T1/2»15 ч - за 2-3 дня или 1-2 дня соответственно; при сl креатинина ≥30-<50 мл/мин, T1/2»18 ч - за 4 дня или за 2-3 дня (>48 ч) соответственно.
Это следует принимать во внимание перед проведением любых процедур ( см «Фармакокинетика»).
Дабигатрана этексилат противопоказан пациентам с тяжелыми нарушениями функции почек (Cl креатинина <30 мл/мин), но если препарат все же применяют, отменять его следует не менее чем за 5 дней до операции.
В случае необходимости проведения экстренного хирургического вмешательства прием дабигатрана этексилата необходимо временно прекратить. Хирургическое вмешательство, при наличии такой возможности, целесообразно выполнять не ранее чем через 12 ч после последнего приема дабигатрана этексилата. Если операция не может быть отложена, риск кровотечения может повышаться. В таком случае следует оценить соотношение риска кровотечения и необходимости экстренного проведения вмешательства.
Спиналъная анестезия/эпидуральная анестезия/люмбальная пункция.
Такие процедуры, как спинномозговая анестезия, могут потребовать полного восстановления гемостаза.
В случае травматичной или повторной спинномозговой пункции и длительного использования эпидурального катетера может повышаться риск развития спинномозгового кровотечения или эпидуральной гематомы. Первую дозу дабигатрана этексилата следует принимать не ранее, чем через 2 ч после удаления катетера. Необходим контроль состояния пациентов для исключения неврологических симптомов, которые могут быть обусловлены спинномозговым кровотечением или эпидуральной гематомой.
RxList.com.
Спиналъная/эпидуральная гематома.
Эпидуральная или спинальная гематомы могут возникнуть у пациентов, получавших дабигатрана этексилат, которым одновременно проводили нейроаксиальную анестезию или спинномозговую пункцию. Эти гематомы могут привести к длительному или постоянному параличу. Следует рассмотреть эти риски при планировании для пациентов процедур, связанных с позвоночником. Факторы, которые могут увеличивать риск развития эпидуральной или спинальной гематом у этих пациентов, включают:
- использование постоянного эпидурального катетера;
- сопутствующее применение других ЛС, влияющих на гемостаз, таких как НПВС, ингибиторы тромбоцитов, другие антикоагулянты;
- травматическая или неоднократные эпидуральная или спинальная пункции в анамнезе;
- деформация позвоночника или операции на позвоночнике в анамнезе.
Оптимальное время между приемом дабигатрана этексилата и нейроаксиальными процедурами неизвестно.
Для снижения потенциального риска кровотечения, связанного с одновременным применением дабигатрана и проведением эпидуральной или спинномозговой анестезии/анальгезии или спинномозговой пункции, следует учитывать фармакокинетический профиль дабигатрана ( см «Фармакология»). Установку или удаление эпидурального катетера или люмбальную пункцию лучше всего проводить, когда антикоагулянтный эффект дабигатрана низок; однако точное время достижения достаточно малого антикоагулянтного эффекта у каждого пациента неизвестно.
При необходимости проведения эпидуральной или спинальной анестезии/анальгезии или спинномозговой пункции на фоне лечения дабигатрана этексилатом, следует проводить частый мониторинг пациентов для выявления каких-либо признаков или симптомов неврологических нарушений, таких как боль в средней части спины, сенсорные или моторные нарушения (онемение, покалывание или слабость в нижних конечностях), дисфункция кишечника и/или мочевого пузыря. Необходимо проинструктировать пациентов о необходимости немедленно сообщать врачу, если они испытывают какие-либо из перечисленных выше признаков или симптомов. При подозрении на спинальную гематому следует провести срочную диагностику и лечение, включая рассмотрение вопроса о декомпрессии спинного мозга, даже если такое лечение может не помочь в предотвращении или обратном развитии неврологических осложнений.
Следует оценить преимущества и риски до проведения нейроаксиального вмешательства у пациентов, получающих антикоагулянты.
Период после проведения процедуры.
Применение дабигатрана этексилата можно продолжить по достижении полного гемостаза.
В случае появления желудочно-кишечных симптомов рекомендуется принимать дабигатрана этексилат с пищей и/или с ингибитором протонной помпы типа пантопразола.
Влияние на способность к управлению транспортными средствами и механизмами. Влияние дабигатрана этексилата на способность управлять транспортными средствами и заниматься другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций, не изучалось, но учитывая, что его применение может сопровождаться повышенным риском кровотечений, следует соблюдать осторожность при выполнении таких видов деятельности.
|
|
Список литературы
Обобщенные материалы www.grls.rosminzdrav.ru, 2016 и www.rxlist.com, 2016.
Входит в состав
- 1252-10167₽ Прадакса (3 фирмы)
- — Аксартобан
- — Дабигатран (KRKA )
- — Дабигатрана этексилат Сандоз (MSN Laboratories Privat Limited )
- — Дабиксом (КРКА-Рус )