Другие названия и синонимы
Pemetrexed.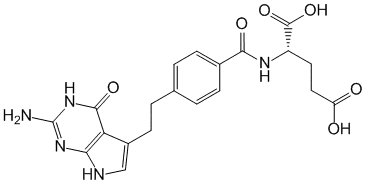
Фармакологическая группа
|
|
Латинское название
Pemetrexedum ( Pemetrexedi).
Химическое название
N-[4-[2-(2-Амино-4,7-дигидро-4-оксо-1Н-пиррол[2,3-d]пиримидин-5-ил)этил]бензоил]-L-глутаминовая кислота.
Используется в лечении
Код CAS
137281-23-3.
Фармакологическое действие
Противоопухолевое.
Характеристика вещества
Противоопухолевое средство, антиметаболит.
Пеметрексед динатрия гептагидрат - белое или почти белое вещество. Молекулярная масса 597,49.
Пеметрексед динатрия гептагидрат - белое или почти белое вещество. Молекулярная масса 597,49.
Фармакодинамика
Пеметрексед - антифолат, содержащий пирролопиримидиновое ядро, противоопухолевая активность обусловлена нарушением фолатзависимых метаболических процессов, существенных для клеточной репликации. В исследованиях in vitro >in vitro показано, что пеметрексед ингибирует тимидилатсинтетазу (ТС), дигидрофолатредуктазу (ДГФР), глицинамид-рибонуклеотид-формил-трансферазу (ГАРФТ), являющиеся ключевыми фолатзависимыми ферментами для биосинтеза de novo тимидиновых и пуриновых нуклеотидов. Пеметрексед транспортируется в клетки как с помощью переносчика восстановленных фолатов, так и посредством мембранных фолатсвязывающих белковых транспортных систем. Попав в клетку, пеметрексед превращается в полиглутаматные формы с помощью фермента фолилполиглутаматсинтетазы. Полиглутаматные формы накапливаются в клетках и являются ингибиторами ТС и ГАРФТ. Полиглутамация - процесс, зависимый от времени и концентрации, отмечается в опухолевых клетках и, в меньшей степени, в клетках нормальных тканей. У полиглутамированных метаболитов увеличивается внутриклеточное время полужизни, что приводит к пролонгации действия вещества в опухолевых клетках.
Предклинические исследования показали, что пеметрексед ингибирует in vitro >in vitro рост клеточных линий мезотелиомы (MSTO-211H, NCI-H2052). Исследования с клетками мезотелиомы линии MSTO-211H показали, что при комбинированном применении пеметрекседа и цисплатина в исследованиях in vitro >in vitro наблюдался синергизм противоопухолевого действия.
Канцерогенность, мутагенность, влияние на фертильность.
Исследований канцерогенности пеметрекседа не проведено. Пеметрексед оказывал кластогенный эффект in vivo в микроядерном тесте у мышей, но не проявлял мутагенной активности в ряде тестов (тест Эймса, тест на клетках яичника китайского хомячка). В/в введение пеметрекседа в дозах 0,1 мг/кг/сут и выше (около 1/1666 рекомендуемой в/в дозы для человека в пересчете на мг/м2) самцам мышей приводило к снижению фертильности, гипоспермии и тестикулярной атрофии.
Предклинические исследования показали, что пеметрексед ингибирует in vitro >in vitro рост клеточных линий мезотелиомы (MSTO-211H, NCI-H2052). Исследования с клетками мезотелиомы линии MSTO-211H показали, что при комбинированном применении пеметрекседа и цисплатина в исследованиях in vitro >in vitro наблюдался синергизм противоопухолевого действия.
Канцерогенность, мутагенность, влияние на фертильность.
Исследований канцерогенности пеметрекседа не проведено. Пеметрексед оказывал кластогенный эффект in vivo в микроядерном тесте у мышей, но не проявлял мутагенной активности в ряде тестов (тест Эймса, тест на клетках яичника китайского хомячка). В/в введение пеметрекседа в дозах 0,1 мг/кг/сут и выше (около 1/1666 рекомендуемой в/в дозы для человека в пересчете на мг/м2) самцам мышей приводило к снижению фертильности, гипоспермии и тестикулярной атрофии.
Фармакокинетика
Фармакокинетика пеметрекседа в виде однократной 10-минутной инфузии в диапазоне доз от 0,2 до 838 мг/м2 была оценена у 426 больных с различными сóлидными опухолями. Пеметрексед ограниченно метаболизируется в печени. Выводится преимущественно через почки, главным образом путем гломерулярной фильтрации и тубулярной секреции, 70-90% дозы - в неизмененном виде в первые 24 ч после введения. Общий системный клиренс пеметрекседа - 91,8 мл/мин, T1/2 - 3,5 ч у пациентов с нормальной функцией почек (Cl креатинина 90 мл/мин). При снижении функции почек клиренс уменьшается и экспозиция (AUC) увеличивается. Общая системная экспозиция пеметрекседа (AUC) и maxCmax увеличиваются пропорционально дозе. Фармакокинетика пеметрекседа не изменяется при проведении многократных циклов. Объем распределения в равновесном состоянии - 16,1 л. Связывание с белками плазмы - примерно 81% (не зависит от степени нарушения функции почек).
Зависимость параметров фармакокинетики от некоторых факторов.
Фармакокинетика пеметрекседа была изучена в контролируемых исследованиях примерно у 400 пациентов. Фармакокинетические параметры не зависели от пола и возраста (в диапазоне от 26 до 80 лет) пациентов.
Детский возраст. Дети не были включены в клинические испытания.
Нарушение функции печени. Исследований фармакокинетики пеметрекседа у пациентов с нарушением функции печени не проводили. Из клинических исследований были исключены пациенты с уровнем билирубина более чем в 1,5 раза превышающем верхнюю границу нормы (ВГН), пациенты с уровнем печеночных трансаминаз более чем в 3 раза превышающем ВГН при отсутствии метастазов в печени. В исследования были включены пациенты с уровнем трансаминаз, составляющем 3-5 ВГН при наличии метастазов в печени. Есть данные о том, что повышение уровня печеночных трансаминаз (АЛТ, АСТ) или общего билирубина не оказывает влияния на фармакокинетику пеметрекседа.
Нарушение функции почек. Анализ фармакокинетики пеметрекседа был проведен у 127 пациентов со сниженной функцией почек. Плазменный клиренс пеметрекседа в присутствии цисплатина уменьшался в результате снижения функции почек, тогда как системная экспозиция увеличивалась. У пациентов с сl креатинина 45, 50 и 80 мл/мин системная экспозиция (AUC) была выше на 65, 54 и 13% соответственно по сравнению с таковой у пациентов с сl креатинина 100 мл/мин.
Зависимость параметров фармакокинетики от некоторых факторов.
Фармакокинетика пеметрекседа была изучена в контролируемых исследованиях примерно у 400 пациентов. Фармакокинетические параметры не зависели от пола и возраста (в диапазоне от 26 до 80 лет) пациентов.
Детский возраст. Дети не были включены в клинические испытания.
Нарушение функции печени. Исследований фармакокинетики пеметрекседа у пациентов с нарушением функции печени не проводили. Из клинических исследований были исключены пациенты с уровнем билирубина более чем в 1,5 раза превышающем верхнюю границу нормы (ВГН), пациенты с уровнем печеночных трансаминаз более чем в 3 раза превышающем ВГН при отсутствии метастазов в печени. В исследования были включены пациенты с уровнем трансаминаз, составляющем 3-5 ВГН при наличии метастазов в печени. Есть данные о том, что повышение уровня печеночных трансаминаз (АЛТ, АСТ) или общего билирубина не оказывает влияния на фармакокинетику пеметрекседа.
Нарушение функции почек. Анализ фармакокинетики пеметрекседа был проведен у 127 пациентов со сниженной функцией почек. Плазменный клиренс пеметрекседа в присутствии цисплатина уменьшался в результате снижения функции почек, тогда как системная экспозиция увеличивалась. У пациентов с сl креатинина 45, 50 и 80 мл/мин системная экспозиция (AUC) была выше на 65, 54 и 13% соответственно по сравнению с таковой у пациентов с сl креатинина 100 мл/мин.
Показания к применению
Злокачественная мезотелиома плевры в комбинации с препаратами платины. Немелкоклеточный рак легкого (местно-распространенный или метастатический) в качестве терапии 2 линии.
Противопоказания
Гиперчувствительность.
Ограничения к использованию
Нарушение функции почек (Cl креатинина <45 мл/мин), гипербилирубинемия (уровень билирубина более чем в 1,5 раза превышающий ВГН), повышение активности печеночных трансаминаз более чем в 3 раза при отсутствии метастазов в печени или более чем в 5 раз при наличии метастазов в печени (недостаточно данных для оценки эффективности и безопасности применения), детский возраст (эффективность и безопасность применения не установлены).
При беременности и кормлении грудью
Нет исследований применения пеметрекседа у беременных женщин. В случае применения при беременности или в период планируемой беременности необходимо предупредить пациентку о потенциальном риске для плода. Пеметрексед может оказывать неблагоприятное воздействие на развитие плода при применении у беременных женщин.
Категория действия на плод по FDA. D.
Показана фетотоксичность и тератогенность пеметрекседа у мышей при в/в введении в дозах 0,2 мг/кг (0,6 мг/м2) или 5 мг/кг (15 мг/м2) в период с 6-го по 15-й день беременности. Пеметрексед вызывал уродства при развитии плода (неполная оссификация таранной кости и костей черепа) при 0,2 мг/кг (около 1/833 рекомендуемой в/в дозы для человека в пересчете на мг/м2) и волчья пасть при 5 мг/кг (около 1/33 рекомендуемой в/в дозы для человека в пересчете на мг/м2). Эмбриотоксичность характеризовалась повышением эмбриофетальных смертей и снижением величины приплода.
Неизвестно, выделяется ли пеметрексед или его метаболиты с грудным молоком женщин. Однако с учетом того, что многие ЛС экскретируются в грудное молоко и могут вызывать серьезные побочные реакции у детей, находящихся на грудном вскармливании, кормящим матерям рекомендуется прекратить вскармливание при лечении пеметрекседом.
Категория действия на плод по FDA. D.
Показана фетотоксичность и тератогенность пеметрекседа у мышей при в/в введении в дозах 0,2 мг/кг (0,6 мг/м2) или 5 мг/кг (15 мг/м2) в период с 6-го по 15-й день беременности. Пеметрексед вызывал уродства при развитии плода (неполная оссификация таранной кости и костей черепа) при 0,2 мг/кг (около 1/833 рекомендуемой в/в дозы для человека в пересчете на мг/м2) и волчья пасть при 5 мг/кг (около 1/33 рекомендуемой в/в дозы для человека в пересчете на мг/м2). Эмбриотоксичность характеризовалась повышением эмбриофетальных смертей и снижением величины приплода.
Неизвестно, выделяется ли пеметрексед или его метаболиты с грудным молоком женщин. Однако с учетом того, что многие ЛС экскретируются в грудное молоко и могут вызывать серьезные побочные реакции у детей, находящихся на грудном вскармливании, кормящим матерям рекомендуется прекратить вскармливание при лечении пеметрекседом.
|
|
Побочные эффекты
Побочные эффекты. наблюдавшиеся у пациентов со злокачественной мезотелиомой плевры при терапии пеметрекседом/цисплатином при добавлении в терапию в качестве профилактической меры препаратов фолиевой кислоты и витамина В12. представлены в таблице 1. Причинная связь с приемом ЛС не установлена. В таблице представлены побочные эффекты, которые встречались по крайней мере у 5% пациентов, а также наблюдавшиеся с меньшей частотой, но рассматриваемые как важные (почечная недостаточность, инфекция). Наиболее частыми эффектами были гематологическая токсичность, лихорадка и инфекции, стоматит/фарингит, сыпь/десквамация.
Таблица 1.
Побочные эффекты, отмеченные в клинических исследованиях пеметрекседа.
В таблице 2 представлены сравнительные данные частоты побочных эффектов (3 и 4 степени тяжести) у пациентов, получавших и не получавших фолиевую кислоту и цианокобаламин.
Таблица 2.
Сравнительная частота тяжелых побочных эффектов, наблюдавшихся при проведении клинических испытаний.
Побочными эффектами. которые в исследовании встречались чаще у пациентов. дополнительно получавших фолиевую кислоту и витамин В12. были гипертензия (11. 3%). боль в груди (8. 6%) и тромбоз/тромбоэмболия (6. 3%).
У пациентов старше 65 лет чаще наблюдались лейкопения, нейтропения, тромбоцитопения. У пациентов мужского пола чаще (24%), чем у женщин (16%) отмечалась сыпь.
Таблица 1.
Побочные эффекты, отмеченные в клинических исследованиях пеметрекседа.
| Показатели/побочные эффекты | Все отмеченные побочные эффекты (% случаев) | ||
| Пеметрексед/цисплатин (N=168) | |||
| Любая степень тяжести | 3 степень тяжести | 4 степень тяжести | |
| Лабораторные | |||
| Гематологические | |||
| Нейтропения | 58 | 19 | 5 |
| Лейкопения | 55 | 14 | 2 |
| Анемия | 33 | 5 | 1 |
| Тромбоцитопения | 27 | 4 | 1 |
| Почечные | |||
| Повышение креатинина | 16 | 1 | 0 |
| Почечная недостаточность | 2 | 0 | 1 |
| Клинические | |||
| Конституциональные | |||
| Усталость | 80 | 17 | 0 |
| Лихорадка | 17 | 0 | 0 |
| Другие общие симптомы | 11 | 2 | 1 |
| Сердечно-сосудистые | |||
| Тромбоз/эмболия | 7 | 4 | 2 |
| Желудочно-кишечные | |||
| Тошнота | 84 | 11 | 1 |
| Рвота | 58 | 10 | 1 |
| Запор | 44 | 2 | 1 |
| Анорексия | 35 | 2 | 0 |
| Стоматит/фарингит | 28 | 2 | 1 |
| Диарея в отсутствии колостомы | 26 | 4 | 0 |
| Обезвоживание | 7 | 3 | 1 |
| Дисфагия/эзофагит/боль при глотании | 6 | 1 | 0 |
| Легочные | |||
| Диспноэ | 66 | 10 | 1 |
| Боль | |||
| Боль в груди | 40 | 8 | 1 |
| Неврологические | |||
| Нейропатия/чувствительность | 17 | 0 | 0 |
| Лабильность настроения/депрессия | 14 | 1 | 0 |
| Инфекции/фебрильная нейтропения | |||
| Инфекции без нейтропении | 11 | 1 | 1 |
| Инфекции с нейтропенией 3 и 4 степени | 6 | 1 | 0 |
| Инфекции/фебрильная нейтропения | 3 | 1 | 0 |
| Фебрильная нейтропения | 1 | 1 | 0 |
| Иммунные | |||
| Аллергические реакции/гиперчувствительность | 2 | 0 | 0 |
| Дерматологические/кожа | |||
| Сыпь/десквамация | 22 | 1 | 0 |
В таблице 2 представлены сравнительные данные частоты побочных эффектов (3 и 4 степени тяжести) у пациентов, получавших и не получавших фолиевую кислоту и цианокобаламин.
Таблица 2.
Сравнительная частота тяжелых побочных эффектов, наблюдавшихся при проведении клинических испытаний.
| Побочные эффекты | Побочные эффекты 3-й и 4-й степени тяжести у пациентов, получавших пеметрексед/цисплатин на фоне фолиевой кислоты и цианокобаламина и без них (% пациентов) | |
| У пациентов на фоне фолиевой кислоты и цианокобаламина (N=168) | У пациентов, не получавших препараты для профилактики токсичности (N=32) | |
| Нейтропения | 24 | 38 |
| Тромбоцитопения | 5 | 9 |
| Тошнота | 12 | 31 |
| Рвота | 11 | 34 |
| Анорексия | 2 | 9 |
| Диарея в отсутствии колостомы | 4 | 9 |
| Обезвоживание | 4 | 9 |
| Лихорадка | 0 | 6 |
| Фебрильная нейтропения | 1 | 9 |
| Инфекция с нейтропенией 3-й и 4-й степени | 1 | 6 |
| Усталость | 17 | 25 |
Побочными эффектами. которые в исследовании встречались чаще у пациентов. дополнительно получавших фолиевую кислоту и витамин В12. были гипертензия (11. 3%). боль в груди (8. 6%) и тромбоз/тромбоэмболия (6. 3%).
У пациентов старше 65 лет чаще наблюдались лейкопения, нейтропения, тромбоцитопения. У пациентов мужского пола чаще (24%), чем у женщин (16%) отмечалась сыпь.
Взаимодействие
Нефротоксичные ЛС и/или ЛС, выводящиеся путем почечной тубулярной секреции, могут снизить клиренс пеметрекседа. Результаты исследований in vitro >in vitro показывают, что пеметрексед не вызывает клинически значимого ингибирования метаболизма ЛС, метаболизирующихся с участием изоферментов сYP3A, сYP2D6, сYP2C9, сYP1A2 цитохромома P450. При одновременном приеме внутрь фолиевой кислоты или в/м введении цианокобаламина фармакокинетика пеметрекседа не изменяется. Цисплатин не влияет на фармакокинетику пеметрекседа. Пеметрексед не изменяет общий клиренс платины. Ацетилсалициловая кислота при приеме в низких или средних дозах (325 мг каждые 6 ч) не влияет на фармакокинетику пеметрекседа. Эффект больших доз ацетилсалициловой кислоты на фармакокинетику пеметрекседа неизвестен.
Ежедневный прием ибупрофена (400 мг 4 раза в день) снижает клиренс пеметрекседа примерно на 20% (и увеличивает AUC на 20%) у пациентов с нормальной функцией почек (клиренс креатинина ≥80 мл/мин). Эффект бóльших доз ибупрофена на фармакокинетику пеметрекседа неизвестен. Следует соблюдать осторожность при одновременном применении ибупрофена и пеметрекседа при нарушении функции почек легкой или средней степени тяжести (клиренс креатинина - 45-79 мл/мин). Больным с легкой и средней степенью тяжести почечной недостаточности не следует применять НПВС с коротким 1/2T1/2 в течение 2 дней перед применением пеметрекседа, в день применения и в течение 2 дней после применения. Ввиду отсутствия данных о возможном взаимодействии между пеметрекседом и НПВС с длительным 1/2T1/2, все пациенты, принимающие НПВС, должны прервать лечение НПВС по крайней мере за 5 дней до, в день приема и в течение 2 дней после применения пеметрекседа. Если требуется совместное назначение НПВС, необходим строгий контроль за токсичностью, особенно в отношении миелосупрессии и токсичности со стороны ЖКТ.
Ежедневный прием ибупрофена (400 мг 4 раза в день) снижает клиренс пеметрекседа примерно на 20% (и увеличивает AUC на 20%) у пациентов с нормальной функцией почек (клиренс креатинина ≥80 мл/мин). Эффект бóльших доз ибупрофена на фармакокинетику пеметрекседа неизвестен. Следует соблюдать осторожность при одновременном применении ибупрофена и пеметрекседа при нарушении функции почек легкой или средней степени тяжести (клиренс креатинина - 45-79 мл/мин). Больным с легкой и средней степенью тяжести почечной недостаточности не следует применять НПВС с коротким 1/2T1/2 в течение 2 дней перед применением пеметрекседа, в день применения и в течение 2 дней после применения. Ввиду отсутствия данных о возможном взаимодействии между пеметрекседом и НПВС с длительным 1/2T1/2, все пациенты, принимающие НПВС, должны прервать лечение НПВС по крайней мере за 5 дней до, в день приема и в течение 2 дней после применения пеметрекседа. Если требуется совместное назначение НПВС, необходим строгий контроль за токсичностью, особенно в отношении миелосупрессии и токсичности со стороны ЖКТ.
Передозировка
Имеется несколько случаев передозировки пеметрекседа. Симптомы: угнетение костного мозга (нейтропения. тромбоцитопения и анемия). присоединение вторичных инфекций. диарея. воспаление слизистых оболочек. кожная сыпь.
Лечение. Симптоматическое, в тч немедленное применение кальция фолината (Лейковорина).
Лечение. Симптоматическое, в тч немедленное применение кальция фолината (Лейковорина).
Способ применения и дозы
В/в капельно, в течение 10 мин.
При злокачественной мезотелиоме плевры (комбинированное лечение с цисплатином): рекомендованная доза пеметрекседа - 500 мг/м2 в 1-й день каждого 21-дневного цикла; цисплатин - 75 мг/м2 в виде 2-часовой в/в инфузии на фоне гидратации через 30 мин после введения пеметрекседа в 1-й день каждого 21-дневного цикла.
При немелкоклеточном раке легкого (монотерапия): рекомендованная доза - 500 мг/м2 в 1-й день каждого 21-дневного цикла.
Коррекция дозы перед повторными курсами должна основываться на наиболее низком пороге гематологических показателей или на максимальной негематологической токсичности в течение предыдущего цикла лечения. Лечение может быть отсрочено с целью восстановления. По мере восстановления пациентам необходимо продолжить лечение по схеме (в монотерапии или в комбинации с цисплатином): при содержании нейтрофилов <500 клеток/мм3 и минимальном содержании тромбоцитов ≥50000/мм3 вводят 75% от предыдущей дозы (оба ЛС); при количестве тромбоцитов <50000 клеток/мм3 независимо от минимального содержания нейтрофилов назначают 50% от предыдущей дозы (оба ЛС). При развитии негематологической токсичности (исключая нейротоксичность) более 3-й степени (за исключением повышения активности печеночных трансаминаз 3-й степени) введение пеметрекседа необходимо отложить до восстановления показателей, соответствующих уровню до начала лечения. Далее терапию продолжают по схеме: любая токсичность 3-й степени (за исключением повышения активности печеночных трансаминаз 3-й степени) или 4-й степени за исключением воспаления слизистой оболочки - 75% от предыдущей дозы (оба ЛС); диарея, требующая госпитализации (независимо от степени) или диарея 3-й или 4-й степени - 75% от предыдущей дозы (оба ЛС); воспаление слизистой оболочки 3-й или 4-й степени - 50% от предыдущей дозы для пеметрекседа и 100% от предыдущей дозы для цисплатина. В случае развития нейротоксичности коррекцию дозы пеметрекседа и цисплатина проводят по схеме: 0-1-я степень токсичности - 100% от предыдущей дозы (оба ЛС); 2-я степень токсичности - 100% от предыдущей дозы для пеметрекседа и 50% от предыдущей дозы для цисплатина. Лечение отменяют, если отмечается нейротоксичность 3-й или 4-й степени, а также гематологическая и негематологическая токсичность 3-й или 4-й степени после двух снижений доз (за исключением повышения активности печеночных трансаминаз 3-й степени) и немедленно отменяют при наличии нейротоксичности 3-й или 4-й степени.
При злокачественной мезотелиоме плевры (комбинированное лечение с цисплатином): рекомендованная доза пеметрекседа - 500 мг/м2 в 1-й день каждого 21-дневного цикла; цисплатин - 75 мг/м2 в виде 2-часовой в/в инфузии на фоне гидратации через 30 мин после введения пеметрекседа в 1-й день каждого 21-дневного цикла.
При немелкоклеточном раке легкого (монотерапия): рекомендованная доза - 500 мг/м2 в 1-й день каждого 21-дневного цикла.
Коррекция дозы перед повторными курсами должна основываться на наиболее низком пороге гематологических показателей или на максимальной негематологической токсичности в течение предыдущего цикла лечения. Лечение может быть отсрочено с целью восстановления. По мере восстановления пациентам необходимо продолжить лечение по схеме (в монотерапии или в комбинации с цисплатином): при содержании нейтрофилов <500 клеток/мм3 и минимальном содержании тромбоцитов ≥50000/мм3 вводят 75% от предыдущей дозы (оба ЛС); при количестве тромбоцитов <50000 клеток/мм3 независимо от минимального содержания нейтрофилов назначают 50% от предыдущей дозы (оба ЛС). При развитии негематологической токсичности (исключая нейротоксичность) более 3-й степени (за исключением повышения активности печеночных трансаминаз 3-й степени) введение пеметрекседа необходимо отложить до восстановления показателей, соответствующих уровню до начала лечения. Далее терапию продолжают по схеме: любая токсичность 3-й степени (за исключением повышения активности печеночных трансаминаз 3-й степени) или 4-й степени за исключением воспаления слизистой оболочки - 75% от предыдущей дозы (оба ЛС); диарея, требующая госпитализации (независимо от степени) или диарея 3-й или 4-й степени - 75% от предыдущей дозы (оба ЛС); воспаление слизистой оболочки 3-й или 4-й степени - 50% от предыдущей дозы для пеметрекседа и 100% от предыдущей дозы для цисплатина. В случае развития нейротоксичности коррекцию дозы пеметрекседа и цисплатина проводят по схеме: 0-1-я степень токсичности - 100% от предыдущей дозы (оба ЛС); 2-я степень токсичности - 100% от предыдущей дозы для пеметрекседа и 50% от предыдущей дозы для цисплатина. Лечение отменяют, если отмечается нейротоксичность 3-й или 4-й степени, а также гематологическая и негематологическая токсичность 3-й или 4-й степени после двух снижений доз (за исключением повышения активности печеночных трансаминаз 3-й степени) и немедленно отменяют при наличии нейротоксичности 3-й или 4-й степени.
|
|
Меры предосторожности применения
Пеметрексед должен назначаться под наблюдением квалифицированного врача, имеющего опыт применения противоопухолевых ЛС.
Режим премедикации.
Необходимость приема фолата и цианокобаламина. Для уменьшения токсичности пеметрекседа пациент должен получать препараты фолиевой кислоты и витамин В12 - в качестве профилактической меры для снижения связанной с лечением гематологической и гастроинтестинальной токсичности. Препараты фолиевой кислоты или поливитамины, содержащие суточную дозу фолиевой кислоты (350-1000 мкг, в среднем 400 мкг), необходимо принимать как минимум 5 дней перед первым введением пеметрекседа. Прием фолиевой кислоты должен продолжаться во время всего цикла лечения и в течение 21 дня после последнего введения пеметрекседа. Также необходимо однократно ввести цианокобаламин в дозе 1000 мкг в/м в период 7 дней перед первым введением пеметрекседа и через каждые 3 цикла после начала лечения. Последующие введения цианокобаламина в той же дозе могут проводиться в день введения пеметрекседа. В клинических исследованиях сообщалось о том, что при предварительном приеме фолиевой кислоты и витамина В12 отмечалась меньшая токсичность в целом, снижение гематологической токсичности 3/4 степени и негематологической токсичности, в тч нейтропении, фебрильной нейтропении и инфекции с нейтропенией 3/4 степени.
Кортикостероиды. У пациентов, получавших лечение пеметрекседом и не применявших предварительно кортикостероиды, более часто отмечалась кожная сыпь. В клинических испытаниях показано, что назначение дексаметазона (или аналога) внутрь в дозе 4 мг 2 раза в сутки за 1 день до начала лечения пеметрекседом, в день введения и в последующий день после введения пеметрекседа снижает частоту и выраженность кожных реакций.
Нарушение функции почек. У пациентов с нарушением функции почек при клиренсе креатинина ≥45 мл/мин коррекции режима дозирования не требуется. При клиренсе креатинина <45 мл/мин применение не рекомендуется ввиду недостаточности данных по использованию пеметрекседа у этой группы пациентов.
Один пациент с тяжелой почечной недостаточностью (клиренс креатинина 19 мл/мин), который не получал фолиевую кислоту и цианокобаламин, умер из-за лекарственно-обусловленной токсичности после введения пеметрекседа.
Супрессия костного мозга. Пеметрексед может вызывать угнетение функции костного мозга, проявляющееся нейтропенией, тромбоцитопенией и анемией ( см «Побочные действия»). Миелосупрессия обычно является дозозависимой. Снижение дозы при повторных курсах следует проводить с учетом снижения абсолютного числа нейтрофилов, при подсчете числа тромбоцитов и анализе максимальной негематологической токсичности в предыдущем цикле ( см «Способ применения и дозы»).
Лабораторный мониторинг. Перед началом применения препарата абсолютное количество нейтрофилов должно составлять ≥1500 клеток/мм3, тромбоцитов - ≥100000 клеток/мм3. Перед каждым введением пеметрекседа необходимо проводить общий анализ крови с подсчетом лейкоцитарной формулы и количества тромбоцитов.
Для оценки функции почек и печени необходимо периодически проводить биохимический анализ крови.
Режим премедикации.
Необходимость приема фолата и цианокобаламина. Для уменьшения токсичности пеметрекседа пациент должен получать препараты фолиевой кислоты и витамин В12 - в качестве профилактической меры для снижения связанной с лечением гематологической и гастроинтестинальной токсичности. Препараты фолиевой кислоты или поливитамины, содержащие суточную дозу фолиевой кислоты (350-1000 мкг, в среднем 400 мкг), необходимо принимать как минимум 5 дней перед первым введением пеметрекседа. Прием фолиевой кислоты должен продолжаться во время всего цикла лечения и в течение 21 дня после последнего введения пеметрекседа. Также необходимо однократно ввести цианокобаламин в дозе 1000 мкг в/м в период 7 дней перед первым введением пеметрекседа и через каждые 3 цикла после начала лечения. Последующие введения цианокобаламина в той же дозе могут проводиться в день введения пеметрекседа. В клинических исследованиях сообщалось о том, что при предварительном приеме фолиевой кислоты и витамина В12 отмечалась меньшая токсичность в целом, снижение гематологической токсичности 3/4 степени и негематологической токсичности, в тч нейтропении, фебрильной нейтропении и инфекции с нейтропенией 3/4 степени.
Кортикостероиды. У пациентов, получавших лечение пеметрекседом и не применявших предварительно кортикостероиды, более часто отмечалась кожная сыпь. В клинических испытаниях показано, что назначение дексаметазона (или аналога) внутрь в дозе 4 мг 2 раза в сутки за 1 день до начала лечения пеметрекседом, в день введения и в последующий день после введения пеметрекседа снижает частоту и выраженность кожных реакций.
Нарушение функции почек. У пациентов с нарушением функции почек при клиренсе креатинина ≥45 мл/мин коррекции режима дозирования не требуется. При клиренсе креатинина <45 мл/мин применение не рекомендуется ввиду недостаточности данных по использованию пеметрекседа у этой группы пациентов.
Один пациент с тяжелой почечной недостаточностью (клиренс креатинина 19 мл/мин), который не получал фолиевую кислоту и цианокобаламин, умер из-за лекарственно-обусловленной токсичности после введения пеметрекседа.
Супрессия костного мозга. Пеметрексед может вызывать угнетение функции костного мозга, проявляющееся нейтропенией, тромбоцитопенией и анемией ( см «Побочные действия»). Миелосупрессия обычно является дозозависимой. Снижение дозы при повторных курсах следует проводить с учетом снижения абсолютного числа нейтрофилов, при подсчете числа тромбоцитов и анализе максимальной негематологической токсичности в предыдущем цикле ( см «Способ применения и дозы»).
Лабораторный мониторинг. Перед началом применения препарата абсолютное количество нейтрофилов должно составлять ≥1500 клеток/мм3, тромбоцитов - ≥100000 клеток/мм3. Перед каждым введением пеметрекседа необходимо проводить общий анализ крови с подсчетом лейкоцитарной формулы и количества тромбоцитов.
Для оценки функции почек и печени необходимо периодически проводить биохимический анализ крови.
Список литературы
Physicians Desk Reference. 62 th ed. Thomson PDR, 2008. P. 1779-1784.
Входит в состав
- 7619-37769₽ Пемелан
- 40769₽ Пеметрексед (7 фирм)
- 44719-48000₽ Алимта (3 фирмы)
- — Антифолат
- — Веротрексед (Верофарм ООО )
- — ИСПОЛАТ (2 фирмы)
- — Пемджем
- — Пеметрексед Дж (2 фирмы)
- — Пеметрексед Канон
- — Пеметрексед динатрия (Qilu Pharmaceutical Co. Ltd )
- — Пеметрексед-ДЕКО (ДЕКО компания )
- — Пеметрексед-Келун-Казфарм (Келун-Казфарм ТОО )
- — Пеметрексед-Рус (2 фирмы)
- — Пеметрексед-ТЛ (2 фирмы)
- — Пеметрексед-натив (2 фирмы)
- — Пеметрексед-промомед
- — Пеметрекседа динатрия гемипентагидрат (ДЕКО компания )
- — Пеметрекседа динатрия гептагидрат (5 фирм)
- — Фолитрекс (2 фирмы)