МКБ-10 коды
- МКБ-10
- C41.9 Злокачественное новообразование костей и суставных хрящей неуточненное
- C40.2 Злокачественное новообразование длинных костей нижней конечности
- C41.2 Злокачественное новообразование позвоночного столба
- C40 Злокачественное новообразование костей и суставных хрящей конечностей
- C40.3 Злокачественное новообразование коротких костей нижней конечности
- C41 Злокачественное новообразование костей и суставных хрящей других и неуточненных локализаций (остеосаркома, рак остеогенный)
- C41.1 Злокачественное новообразование нижней челюсти
- C41.3 Злокачественное новообразование ребер, грудины и ключицы
|
|
Вступление
МКБ 10: с40, с41.
Год утверждения (частота пересмотра): 2018 (пересмотр каждые 3 года).
ID: КР276/1.
Профессиональные ассоциации.
• Ассоциация онкологов России Восточно-европейская группа по изучению сарком Российское общество клинической онкологии.
Год утверждения (частота пересмотра): 2018 (пересмотр каждые 3 года).
ID: КР276/1.
Профессиональные ассоциации.
• Ассоциация онкологов России Восточно-европейская группа по изучению сарком Российское общество клинической онкологии.
Профессиональные ассоциации
• Ассоциация онкологов России Восточно-европейская группа по изучению сарком Российское общество клинической онкологии.

 Список сокращений
Список сокращений
ЖКТ - желу́дочно-кише́чный тракт.
ИГХ - Иммуногистохимия.
КТ - Компью́терная томогра́фия.
МРТ - Магни́тно-резона́нсная томогра́фия.
ПНЭТ(PNET) - примитивная нейроэктодермальная опухоль.
ПЭТ - Позитро́нно-эмиссио́нная томогра́фия.
СМТ - Саркомы мягких тканей.
УЗИ - Ультразвуковое исследование.
ЭКГ - Электрокардиогра́фия.
IMRT - Intensity-modulated radiation therapy.
ИГХ - Иммуногистохимия.
КТ - Компью́терная томогра́фия.
МРТ - Магни́тно-резона́нсная томогра́фия.
ПНЭТ(PNET) - примитивная нейроэктодермальная опухоль.
ПЭТ - Позитро́нно-эмиссио́нная томогра́фия.
СМТ - Саркомы мягких тканей.
УЗИ - Ультразвуковое исследование.
ЭКГ - Электрокардиогра́фия.
IMRT - Intensity-modulated radiation therapy.
Термины и определения
Безрецидивная выживаемость (БРВ). От момента наступления ремиссии до момента возникновения рецидива.
Бессобытийная выживаемость (БСВ). От начала лечения до момента прекращения ремиссии независимо от причины, приведшей к ней.
Общая выживаемость (ОВ). От начала лечения до окончания исследования или смерти больного.
Полная ремиссия (ПР). Отсутствие признаков опухолевого роста в течение 4 нед. после достижения полного эффекта.
Полный эффект (ПЭ). Отсутствие признаков опухоли по данным лаборатнорных и инструментальных методов обследования.
Прогрессирование. Появление нового опухолевого очага и/или рост первичного опухолевого очага, метастатических очагов чем, на 25%.
Прогрессия в виде метастазов. Метастазирование в кости, костный мозг, лимфатические узлы, головной мозг и/или другие органы.
Прогрессия локальная. Повторный рост опухоли на том же месте и/или появление новых очагов, для лечения которых возможно применение методов локальной терапии.
Стабилизация болезни. Отсутствие роста опухоли и/или активной опухоли, а также отсутствие данных за появление новых очагов.
Частичная ремиссия (ЧР). Сокращение размеров опухолевых очагов более чем, на 50%, при отсутствии новых.
Бессобытийная выживаемость (БСВ). От начала лечения до момента прекращения ремиссии независимо от причины, приведшей к ней.
Общая выживаемость (ОВ). От начала лечения до окончания исследования или смерти больного.
Полная ремиссия (ПР). Отсутствие признаков опухолевого роста в течение 4 нед. после достижения полного эффекта.
Полный эффект (ПЭ). Отсутствие признаков опухоли по данным лаборатнорных и инструментальных методов обследования.
Прогрессирование. Появление нового опухолевого очага и/или рост первичного опухолевого очага, метастатических очагов чем, на 25%.
Прогрессия в виде метастазов. Метастазирование в кости, костный мозг, лимфатические узлы, головной мозг и/или другие органы.
Прогрессия локальная. Повторный рост опухоли на том же месте и/или появление новых очагов, для лечения которых возможно применение методов локальной терапии.
Стабилизация болезни. Отсутствие роста опухоли и/или активной опухоли, а также отсутствие данных за появление новых очагов.
Частичная ремиссия (ЧР). Сокращение размеров опухолевых очагов более чем, на 50%, при отсутствии новых.
Описание
Саркома кости. Редкая злокачественная опухоль, развивающаяся в костной системе.
Причины
К факторам риска развития сарком костей можно отнести предшествующую лучевую терапию, состояние иммунодефицита, болезнь Педжета, болезнь Олье, доброкачественные опухолевые поражения кости так же могут приводить к злокачественной трансформации. Однако, у большинства пациентов специфических этиологических факторов не выявляется [2,6,7].
Эпидемиология
Первичные злокачественные опухоли костей составляют 0,001% от всех впервые выявленных злокачественных новообразований. В России заболеваемость первичными злокачественными опухолями костей составляет 1,03 случая на 100 тыс. населения, что соответствует данным по заболеваемости в других странах [1].
Классификация
1,5 Классификация,.
Международная классификация болезней. Онкология (ВОЗ 2017).| 8810/3 | Фибросаркома, БДУ |
| 8811/3 | Фибромиксосаркома |
| 8812/3 | Периостальная фибросаркома (С40._, С41._) Периостальная саркома, БДУ (С40._, С41._) |
| 8813/3 | Фасциальная фибросаркома |
| 8814/3 | Инфантильная фибросаркома Врожденная фибросаркома |
| 8812/3 | Периостальная фибросаркома (С40._, С41._) Периостальная саркома, БДУ (С40._, С41._) |
| 8890/3 | Лейомиосаркома, БДУ |
| 8830/3 | Злокачественная фиброзная гистиоцитома Фиброксантома, злокачественная |
| 8850/3 | Липосаркома, БДУ Фибролипосаркома |
| 8851/3 | Липосаркома, высокодифференци. Рованная Липомоподобная липосаркома Липосаркома, дифференцированная Воспалительная липосаркома Склерозирующая липосаркома |
| 8852/3 | Миксоидная липосаркома Миксолипосаркома |
| 8853/3 | Круглоклеточная липосаркома |
| 8855/3 | Смешанная липосаркома |
| 8857/3 | Фибробластическая липосаркома |
| 8858/3 | Дедифференцированная липосаркома |
| 8890/3 | Лейомиосаркома, БДУ |
| 8891/3 | Эпителиоидная лейомиосаркома |
| 9120/3 | Гемангиосаркома Ангиосаркома |
| 9133/3 | Эпителиоидная гемангио эндотелиома, злокачественная |
| 9180/3 | Остеосаркома, БДУ (С40._, С41._) Остеогенная саркома, БДУ (С40._, С41._) Остеобластическая саркома (С40._, С41._) Остеохондросаркома (С40._, С41._) |
| 9181/3 | Хондробластическая остеосаркома (С40._, С41._) |
| 9182/3 | Фибробластическая остеосаркома (С40._, С41._) Остеофибросаркома (С40._, С41._) |
| 9183/3 | Телеангиэктатическая остеосаркома (С40._, С41._) |
| 9184/3 | Остеосаркома при болезни Педжета костей (С40._, С41._) |
| 9185/3 | Мелкоклеточная остеосаркома (С40._, С41._) Круглоклеточная остеосаркома (С40._, С41._) |
| 9186/3 | Центральная остеосаркома (С40._, С41._) Обычная центральная остеосаркома (С40._, С41._) Медуллярная остеосаркома (С40._, С41._) |
| 9187/3 | Внутрикостная высокодифференцированная остеосаркома (С40._, С41._) Внутрикостная остеосаркома низкой степени злокачественности (С40._, С41._) |
| 9192/3 | Паростальная остеосаркома (С40._, С41._) Юкстакортикальная остеосаркома (С40._, С41._) |
| 9193/3 | Периостальная остеосаркома (С40._, С41._) |
| 9194/3 | Поверхностная остеосаркома высокой степени злокачественности (С40._, С41._) |
| 9195/3 | Интракортикальная остеосаркома (С40._, С41._) |
| 9220/3 | Хондросаркома, БДУ (С40._, С41._) Фиброхондросаркома (С40._, С41._) |
| 9221/3 | Юкстакортикальная хондросаркома (С40._, С41._) Периостальная хондросаркома (С40._, С41._) |
| 9230/3 | Хондробластома, злокачественная (С40._, С41._) |
| 9231/3 | Миксоидная хондросаркома |
| 9240/3 | Мезенхимальная хондросаркома |
| 9242/3 | Светлоклеточная хондросаркома (С40._, С41._) |
| 9243/3 | Дедифференцированная хондросаркома (С40._, С41._) |
| 9250/3 | Гигантоклеточная опухоль костей, злокачественная (С40._, С41._) Гигантоклеточная саркома костей (С40._, С41._) Остеобластокластома, злокачествен- ная (С40._, С41._) |
| 9260/3 | Саркома Юинга Опухоль Юинга |
| 9261/3 | Адамантинома длинных костей (С40._) Адамантинома большеберцовой кости (С40,2) |
| 9364/3 | Периферическая нейроэктодермаль. Ная опухоль Нейроэктодермальная опухоль, БДУ Периферическая примитивная нейроэк- тодермальная опухоль, БДУ ППНЭО (PPNET, Peripheral Primitive NeuroEctodermal Tumor) |
| 9270/3 | Одонтогенная опухоль, злокачественная Одонтогенная саркома |
| 9290/3 | Амелобластическая одонтосаркома Амелобластическая фиброодонтосаркома Амелобластическая фибродентиносаркома |
| 9310/3 | Амелобластома, злокачественная Адамантинома, злокачественная (за исключением длинных костей М-9261/3) |
| 9330/3 | Амелобластическая фибросаркома Амелобластическая саркома Одонтогенная фибросаркома |
| 9370/3 | Хордома, БДУ |
| 9371/3 | Хондроидная хордома |
| 9372/3 | Дедифференцированная хордома |
1,6 Стадирование первичных злокачественных опухолей кости по системе TNM.
Система стадирования первичных злокачественных опухолей кости по TNM №7 положена в основу алгоритма выбора тактики лечения, вида операции, оценке прогноза выживаемости пациента. Стадирование сарком кости включает определение степени злокачественности опухоли, объём местного распространения опухоли, наличия отдаленных метастазов.Стадия (AJCC, 7th, 2010).
• G-степень злокачественности (G1-2 - низкая степень злокачественности; G3-4 - высокая степень злокачественности);
• Т - местная распространённость (T1 - опухоль ограничена кортикальным слоем; T2 - опухоль распространяется за кортикальный слой);
• М - отдалённые метастазы (М0-без метастазов; М1 - отдалённые метастазы).
Т - местная распространенность:
Тх - Недостаточно данных для оценки первичной опухоли;
Т0 - Первичная опухоль не определяется;
Т1 - Опухоль <8 см в наибольшем измерении;
Т2 - Опухоль >8 см в наибольшем измерении;
T3 - опухоль без границ в поражённой кости.
N - регионарные лимфатические узлы:
Nх - Недостаточно данных для определения регионарных лимфатических узлов;
N0 - Нет признаков метастатического поражения регионарных лимфатических узлов;
N1 - Регионарные лимфатические узлы поражены метастазами.
M - отдаленные метастазы:
Мх - Недостаточно данных для определения отдаленных метастазов;
М0 - Нет признаков отдаленных метастазов;
М1 - Имеются отдаленные метастазы:
M1a - лёгкое;
M1b - в другие отдалённые органы.
G - степень дифференцировки опухоли (определяется на основании гистологического строения опухоли, степени дифференцировки, количества митозов и спонтанных некрозов):
Gх - Степень дифференцировки не может быть установлена;
G1 - Высокая степень дифференцировки;
G2 - Средняя степень дифференцировки;
G3 - Низкая степень дифференцировки;
G4 - Недифференцированные опухоли.
Группировка опухолей костей по стадиям приведена в табл. 1.
Таблица 1. Группировка опухолей костей по стадиям TNM.
| Стадия IA | G 1,2 | T1 | N0 | M0 |
| Стадия IB | G 1,2 | T2 | N0 | M0 |
| Стадия IIA | G 3,4 | T1 | N0 | M0 |
| Стадия IIB | G 3,4 | T2 | N0 | M0 |
| Стадия III | G 1-4 | T3 | N0 | M0 |
| Стадия IVA | любое G | любое T | N0 | M1a |
| Стадия IVB | любое G | любое T | N1 | Любая M |
| любое G | любое T | любое N | M1b |
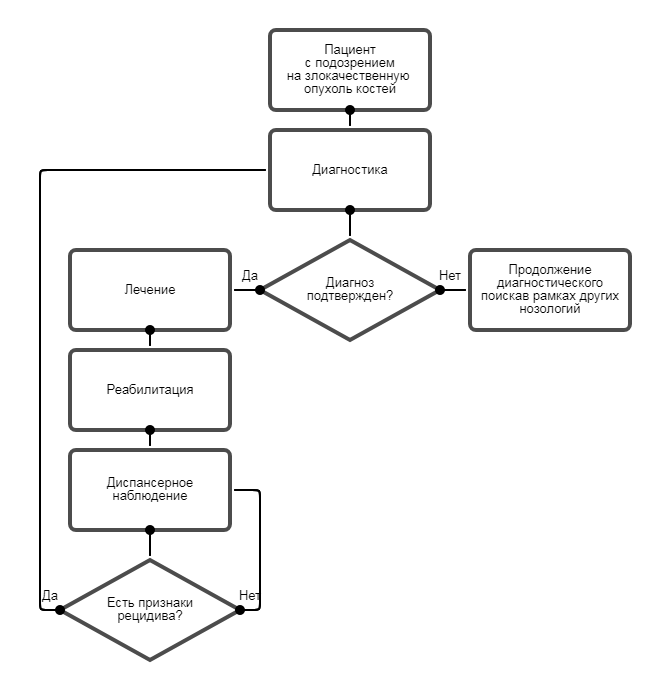
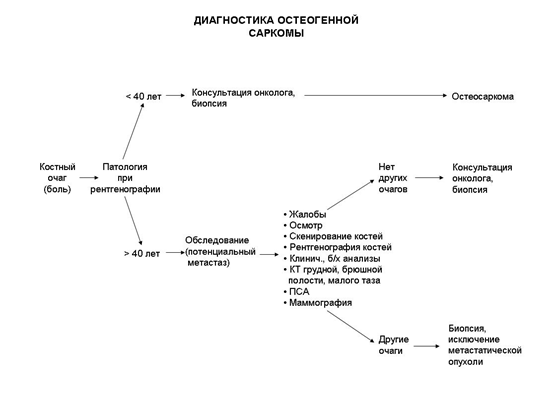
Диагностика
2,1 Жалобы и анамнез.
• Рекомендуется тщательный сбор анамнеза у пациента, родителей. У пациентов старше 40 лет необходимо исключить метастатическое поражение скелета [2,5,6].Уровень убедительности рекомендаций В (уровень достоверности доказательств. IIb).
Комментарии. Уточняют начало развития заболевания, наличие болевого синдрома, изменения функции, оценивают влияние клинических проявлений на качество жизни больного.
2,2 Физикальное обследование.
• Рекомендуется в случае подозрений на развитие саркомы кости, направить пациента в специализированное лечебное учреждение (онкологического профиля) [1].Уровень убедительности рекомендаций. в (уровень достоверности доказательств - IV).
• Рекомендуется оценить состояние области пораженной кости, проверить функцию работы сустава, исключить риск развития патологического перелома, оценить периферические лимфоузлы [3].
Уровень убедительности рекомендаций С (уровень достоверности доказательств. IV).
2,3 Лабораторная диагностика.
• Рекомендуется провести гистологическое исследование биопсийного материала [2,6].Уровень убедительности рекомендаций. в (уровень достоверности доказательств - IIb).
Комментарии. Является основополагающим исследованием при лечении сарком костей, на основании которого определяется тактика лечения и прогноз.
• Рекомендуется гистологическое исследование удаленной кости или иных удаленных органов и тканей [2,6,10,11].
Уровень убедительности рекомендаций. А (уровень достоверности доказательств - Ib).
Комментарии. Обязательное морфологическое исследование после плановой операции позволяет оценить края резекции, лечебный патоморфоз в случаях, когда проводилась неоадъювантная химиотерапия, что необходимо для определения дальнейшей тактики лечения и прогноза.
• Рекомендуется неспецифическая лабораторная диагностика.
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - IV).
Комментарии. Включает в себя общий анализ мочи, общий анализ крови, биохимический анализ крови (с определением содержания белка, билирубина, мочевины, креатинина, аспартатаминотрансфераза (АСT), аланинаминотрансфераза (AЛТ), лактатдегидрогеназа (ЛДГ), щелочная фосфотаза (ЩФ), Na +, K +, Са +, сl-), а также расширенную коагулограмму.
2,4 Инструментальная диагностика.
• Рекомендуется рентгенография пораженной области и близлежащего сустава в двух проекциях с линейкой.Уровень убедительности рекомендаций С (уровень достоверности доказательств. IV).
Комментарии. Позволяет провести первичную диагностику и спрогнозировать при необходимости органосохраняющий вид реконструкции.
• Рекомендуется ультразвуковое исследование (УЗИ) пораженной области.
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - IV).
Комментарии. Позволяет оценить наличие и объем мягкотканого компонента опухоли и оценить связь опухоли с магистральными сосудами.
• Рекомендуется сцинтиграфия костей с 99Tc.
Уровень убедительности рекомендаций в (уровень достоверности доказательств. III).
Комментарий. Позволяет исключить множественное поражение скелета и оценить степень накопления радиофармпрепарата в очаге поражения.
• Рекомендуется магнитно-резонансная томография (МРТ) пораженного отдела скелета.
Уровень убедительности рекомендаций С (уровень достоверности доказательств. IV).
Комментарий. Позволяет оценить наличие мягкотканого компонента опухоли, поражение мышц, вовлечение сосудов и нервов в опухолевый процесс, оценить распространенность по костномозговому каналу.
• Рекомендуется компьютерная томография (КТ) органов грудной клетки с целью исключения патологии органов грудной клетки, в том числе метастазов.
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - IV).
• Рекомендуется УЗИ органов брюшной полости, забрюшинного пространства, периферических лимфатических узлов для исключения метастазов и патологии.
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - IV).
• Рекомендуется при подозрении на диссеминированную форму саркомы кости проводить расширенное обследование.
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - IV).
Комментарии. Расширенное обследование включает:
• Рентгенографию костей с очагами патологического накопления 99Tc;
• Пункцию костного мозга не менее, чем из 2-х точек с последующим цитологическим исследованием (по 3 образца из каждой точки).
• Рекомендуется первым этапом лечения больного с подозрением на саркому кости выполнять биопсию опухоли [2,6,17].
Уровень убедительности рекомендаций. А (уровень достоверности доказательств - Ib).
Комментарии. Правильное проведение биопсии опухоли позволяет в короткие сроки верифицировать диагноз и начать лечение. Вне зависимости от способа проведения биопсии (трепанобиопсия или хирургический) выполнение забора материала должно производиться наименее травматично для пациента. При выборе места забора материала необходимо учитывать предполагаемый доступ последующего хирургического лечения, что позволит в дальнейшем удалить биопсийный рубец, без изменения стандартного хирургического доступа. Учитывая, что нарушение целостности кости может спровоцировать патологический перелом, биопсию внутрикостного фрагмента опухоли необходимо проводить только в случаях, когда внекостный компонент опухоли отсутствует или слабо выражен.
Стандарты выполнения биопсии опухоли:
• Биопсия должна выполняться под контролем сертифицированного онкоортопеда или радиолога;
• Морфологическая верификация полученного биопсийного материала должна проводиться в крупных учреждениях онкологического профиля, при наличии морфолога соответствующей подготовки;
• Предпочтительным способом получения опухолевой ткани для патоморфологического исследования является толстоигольная биопсия;
• Проведение биопсии опухоли открытым доступом возможно: 1) при анатомически трудной локализации очага опухоли; 2) как второй этап, при отрицательном результате после проведённой трепанобиопсии, скудности и малой информативности полученного с помощью трепанобиопсии материала;
• При выполнении биопсии опухоли открытым доступом основополагающим топографическим критерием её проведения является стандартный оперативный доступ предстоящего оперативного лечения, с учётом локализации опухоли;
• Определение тактики дальнейшего лечения должно проводиться совместно с участием хирурга онкоортопеда, химиотерапевта и при необходимости лучевого терапевта;
• Неправильный выбор места биопсии или нарушения техники её выполнения, ставит под угрозу адекватный локальный контроль, ограничивает выбор способа мышечной пластики, значительно повышает риск рецидива после выполнения последующей органосохранной операции.
• Рекомендуется консультация кардиолога и невролога.
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - IV).
Комментарии. Показана перед методами инструментальной диагностики, требующими проведения наркоза и при подготовке к любым видам оперативного вмешательства.
• Рекомендуется консультация стоматолога, оториноларинголога.
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - IV).
Комментарии. Для исключения очагов инфекции с целью их санации перед высокодозной химиотерапией и по показаниям.
• Рекомендуется проводить дифференциальную диагностику с доброкачественными и метастатическими опухолями костей, остеомиелитом, артритом и другими дегенеративно-дистрофическими изменениями суставов [6].
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - IV).
Комментарии. Как правило, ошибочный диагноз остеомиелита, артрита и другими дегенеративно-дистрофических изменений суставов приводит к неправильной диагностике на начальном этапе, неправильному лечению и как следствие приводит к прогрессированию болезни и зачастую невозможности выполнения органосохраняющего лечения.
|
|
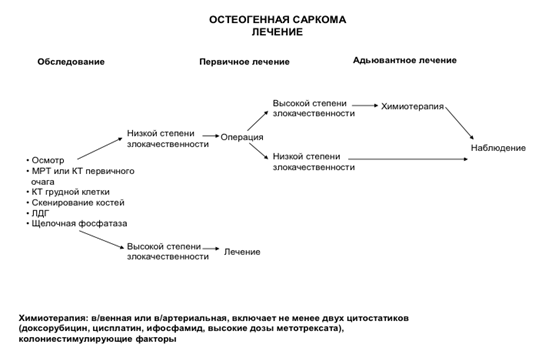
Лечение
• Рекомендуется выбор тактики лечения в зависимости от возраста пациента, стадии заболевания, размера и локализации опухоли, степени дифференцировки опухоли [2,3,6].
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - IV).
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - IV).
Комментарии. В первую очередь следует рассматривать возможность выполнения органосохранных операций. Размер первичного очага опухоли, степень распространения внекостного компонента не могут использоваться как самостоятельные независимые критерии в решении вопроса о проведении калечащей операции. Костные резекции при наличии минимального необходимого отступа от предполагаемого края опухоли не менее 3-5 см (при условии отсутствия распространения опухоли в костномозговом канале оставшейся части кости).
При невозможности выполнения органосохранных операций необходимо выполнение калечащих операций в радикальном объеме. Ампутация или экзартикуляция конечности выполняются в следующих случаях:
• обширное первично-множественное распространение опухоли;
• вовлечение в опухолевый процесс магистрального сосудисто-нервного пучка, технически исключающий проведение реконструктивно-пластического этапа операции;
• прогрессирование на фоне предоперационной химиотерапии;
• отказ пациента от органосохранной операции;
• жизненные показания к экстренной хирургии - распад опухоли, кровотечения.
В специализированных центрах операции с сохранением конечности удается выполнить у 80 % больных. Широкое отступление от опухоли важно для профилактики местных рецидивов вне зависимости от опухолевого ответа.
• Рекомендуются следующие тактики лечения в зависимости от формы остеосаркомы:
• Паростальная (юкстакортикальная) остеосаркома - только радикальное хирургическое лечение (вне зависимости от степени распространения опухоли);
• Периостальная остеосаркома - радикальное хирургическое лечение. В зависимости от размера первичного очага и степени распространения опухоли на консилиуме в составе хирурга-онкоортопеда и химиотерапевта принимается решение о целесообразности консервативного лечения. Применяемая химиотерапия в ряде случаев может уменьшить размеры первичного очага и метастазов опухоли, способствовать ее отграничению псевдокапсулой и перевести в резектабельное состояние;
• Остеосаркома высокой степени злокачественности - проведение комбинированного лечения: блока неоадъювантной химиотерапии, радикальное хирургическое лечение, блок адъювантной химиотерапии [2,6].
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - IV).
• Рекомендуется использование модульных систем эндопротезирования, что признано наиболее актуальным и современным, отвечающим основным требованиям реконструкции костных дефектов при саркомах костей [3].
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - IV).
Комментарии. Выделяют следующие виды реконструктивных операций в объеме эндопротезирования:
• Стандартные первичные операции у взрослых;
• Стандартные первичные операции у детей и подростков;
• Эндопротезирование редких анатомических зон;
• Ревизионное эндопротезиование.
Требования, предъявляемые к конструкции эндопротеза при первичном эндопротезировании у взрослых:
• Модульность конструкции эндопротеза;
• Максимальная надежность и ремонтопригодность эндопротеза;
• Универсальность компонентов эндопротеза;
• Максимальный срок службы;
• Стабильная фиксация эндопротеза;
• Хороший функциональный результат;
• Короткий срок изготовления эндопротеза.
Особенности эндопротеза при первичном эндопротезировании у детей и подростков:
• Наличие бесцементного способа фиксации эндопротеза;
• Раздвижной механизм эндопротеза (инвазивный и неинвазивный).
• Рекомендуется проведение ревизионных операций у онкологических больных, вне зависимости от их причин, в клиниках с подготовленной командой онкоортопедов, специализированного инновационного наукоемкого оборудования, высокотехнологического хирургического инструментария. Вследствие чего этот вид хирургического лечения пациентов должен производиться в крупных специализированных стационарах онкологического профиля, где накоплен опыт и отработаны методики ревизионного эндопротезирования.
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - IV).
Комментарии. В современной онкоортопедии рост числа первичного эндопротезирования, успехи в химиотерапии костных сарком приводят к ежегодному увеличению числа пациентов, требующих проведения повторных ортопедических операцией, связанных с нестабильностью или поломкой эндопротеза.
Каждый ревизионный эндопротез изготавливается индивидуально. Применение модульной системы эндопротезирования упрощает выполнение последующих ревизионных операций, увеличивает биологический резерв кости. Возможность изготовления индивидуальных компонентов эндопротеза для ревизионных операций, при развитии нестабильности позволяет, не удаляя весь эндопротез, заменить его часть.
Уровень убедительности рекомендаций. А (уровень достоверности доказательств - Iа).
Комментарии. Только хирургическое лечение нецелесообразно, так как у 80-90 % больных в течение 1,5 лет после операции диагностируются метастазы в легких и локальные рецидивы. Химиотерапия как часть комплексного лечения значительно улучшает 5-летнюю выживаемость у больных с локализованным процессом (с 20 % до 60 %).
• Рекомендуется проводить предоперационную химиотерапию. Преимущества предоперационной химиотерапии заключаются в возможности оценки in vivo активности химиотерапевтических препаратов и облегчении выполнения операции [11,20,21].
Уровень убедительности рекомендаций. А (уровень достоверности доказательств - Iа).
Комментарии. Обычно проводится 3-4 цикла предоперационной химиотерапии. Степень некроза опухоли после предоперационной химиотерапии - надежный независимый прогностический фактор. При выраженном ответе опухоли на проводимое лечение (некроз опухоли 90 % и более) имеется большая вероятность увеличения безрецидивной и общей выживаемости. У больных с отсутствием эффективности послеоперационная химиотерапия не приводит к улучшению выживаемости.
• Рекомендуется проводить послеоперационную химиотерапию. Послеоперационная химиотерапия определяется степенью лекарственного патоморфоза. При III-IV степени повреждения опухоли (более 90 % опухолевой ткани некротизировано в результате предоперационной химиотерапии) послеоперационно проводится 4 курса химиотерапии без замены цитостатиков, при меньшей степени некроза длительность лечения составляет около 12 месяцев с использованием альтернирующих схем, включающих 5-6 цитостатиков [11].
Уровень убедительности рекомендаций. А (уровень достоверности доказательств - Iа).
Комментарии. Оценка степени лечебного патоморфоза должна проводиться только опытным морфологом, специализирующимся на костной онкопатологии в специализированных центрах.
• Рекомендуется при лечении локализованного опухолевого процесса применять интенсивную химиотерапию на основе комбинации доксорубицина и цисплатина. При явной низкой клинической и рентгенологической эффективностью после двух курсов схема лечения меняется и проводятся два курса высокодозного ифосфамида. Многие центры включают в схему ифосфамид или высокие дозы метотрексата с кальцием фолината, при крайне низкой степени лечебного патоморфоза также используется комбинация гемцитабина и доцетаксела. Продолжительность химиотерапии варьирует от 7 до 12 месяцев. Обязательным условием проведения химиотерапии должно быть строгое соблюдение методики введения высоких доз метотрексата, ифосфамида, цисплатина. Использование меторексата более оправдано у пациентов молодого возраста, считается, что эффективность у больных старше 25-30 лет сомнительна [2,10].
Уровень убедительности рекомендаций. А (уровень достоверности доказательств - Ib).
Комментарии. Проведение высокодозной химиотерапии возможно только в специализированных центрах, при наличии оборудования для контроля концентрации препаратов в сыворотке крови и отделений интенсивной терапии и реанимации.
• Рекомендуются следующие режимы химиотерапии остеосаркомы кости:
• AP :
Доксорубицин 90 мг/м2 в/в, 96-часовая инфузия +.
Цисплатин 120 мг/м2 в/в инфузия в 1-й день каждые 4 недели 4 цикла.
Филграстим 300мкг п/к в 5-й - 14-й дни.
• HD I (используется при низкой эффективности после 2 циклов АР):
Ифосфамид 2000 мг/м2 в/в в 1-й (с месной 2400 мг/м2) - 7-й дни, 2 цикла;
Филграстим 300мкг п/к в 8-й - 17-й дни [9,11,20].
Уровень убедительности рекомендаций. А (уровень достоверности доказательств - Ib).
• Рекомендуется, как альтернативный вариант после операции, следующий режим:
• Некроз опухоли более 90 %:
• HD AI (75/10):
Доксорубицин 75 г/м2 в 1-й день в/в в виде 72-часовой непрерывной инфузии;
Ифосфамид 2500 мг/м2 в 1-й - 4-й дни в/в с месной 1000 мг/м2 3 раза в день [9,11,20];
Филграстим 300мкг п/к в 5-й - 14-й дни, 4 цикла с интервалом 3 недели;
Или повторение схемы АР, также 4 цикла.
• Некроз опухоли от 50 до 90 %:
• HD I:
Ифосфамид 2 г/м2 (с месной 2400 мг/м2) в/в инфузия в 1-й - 7-й дни, 2 цикла с интервалом 3 недели;
Филграстим 300мкг п/к в 8-й - 17-й дни.
• Через 3 недели - HD MTX:
Метотрексат 12 г/м2 в/в инфузия с кальцием фолинатом 15 мг/м² в 1-5-й дни, 4 введения с интервалом в 14 дней для пациентов молодого возраста.
• Через 3 недели - HD AI (75/10):
Доксорубицин 75 г/м2 в 1-й день в/в в виде 72-часовой непрерывной инфузии;
Ифосфамид 2500 мг/м2 в 1-й - 4-й дни в/в на фоне месны 1000 мг/м² 3 раза в день в 1 - 4-й дни по схеме;
Филграстим 300мкг п/к в 5-й - 14-й дни, 4 цикла с интервалом 3 недели;
• Все 3 схемы повторяются 3 раза.
• Некроз опухоли менее 50 %:
• Применяются те же схемы трижды, но с заменой режима HD AI на режим GemTax:
Гемцитабин 900 мг/м2 в 1-й, 8-й дни в виде 90-минутной инфузии;
Доцетаксел 100 мг/м2 в 8-й день;
Филграстим 300мкг п/к в 9-й - 18-й дни, 2 цикла [9,11,20].
Уровень убедительности рекомендаций. А (уровень достоверности доказательств - Ib).
• Рекомендуемое стадирование не отличается от общепринятой классификации для первичных опухолей костей, детально описанной в разделе остеосарком. При внекостной форме стадирование проводится по системе для опухолей мягких тканей. [2,6].
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - IV).
• Рекомендуется дополнительно включать в стандартный алгоритм диагностических процедур для первичных опухолей костей, сцинтиграфию костей скелета и трепанобиопсия костного мозга.
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - IV).
Комментарии. С учетом высокой частоты метастазирования в кости и костный мозг. Рекомендуемое локальное лечение (операция или лучевая терапия) должно обязательно сопровождаться комбинированной химиотерапией, при клинически локализованной форме заболевания к моменту установления диагноза 90 % больных имеют микрометастазы. Комбинация химиотерапии, операции и/или лучевой терапии повысила уровень 5-летней выживаемости с 10 % до 60 %. После биопсии опухоли и тщательного обследования проводится от 4 до 6 циклов индукционной химиотерапии в течение 12-24 недель, далее следует локальный метод лечения с последующим назначением от 6 до 10 циклов химиотерапии с 3-недельным интервалом. Продолжительность лечения составляет 12 месяцев. Наиболее активными цитостатиками являются доксорубицин, циклофосфамид, ифосфамид, винкристин, дактиномицин и этопозид. Фактически все режимы лечения основаны на комбинациях из 4-6 перечисленных препаратов. Наиболее эффективные режимы лечения включали как минимум один алкилирующий химиопрепарат (ифосфамид или циклофосфамид) и доксорубицин. Добавление ифосфамида и этопозида в программу лечения значительно улучшило результаты терапии у пациентов с неметастатической саркомой Юинга / ПНЭТ.
Радикальная операция в тех случаях, когда она выполнима, расценивается как наилучшая возможность локального контроля.
Лучевая терапия показана при невозможности выполнения радикального оперативного вмешательства и обсуждается в тех случаях, когда при гистологическом исследовании удаленного материала определяется недостаточный лечебный патоморфоз (то есть выявляется более 10 % жизнеспособных опухолевых клеток). Нерадикальная операция с последующей лучевой терапией не более эффективна, чем только лучевая терапия. Лучевая терапия проводится в дозах 40-45 Гр при микроскопических остаточных опухолях и 50-60 Гр при наличии макроскопических изменений.
• Рекомендуется применять дистанционную 3-D и интенсивно модулированную (IMRT) лучевую терапию в комбинации с химиотерапией при отказе от операции или нерадикально выполненной операции в качестве локального лечения. РОД = 2-2,5 Гр, СОД = 60 Гр. При метастазах в легкие - крупнопольная лучевая терапия РОД = 2 Гр, СОД = 20 Гр [8,10,18].
Уровень убедительности рекомендаций. А (уровень достоверности доказательств - Iа).
• Рекомендуются следующие режимы химиотерапии [8,10,19]:
• Чередование IE и VAC каждые 3-4 недели:
• IE:
Этопозид 100 мг/м2 в/в в 1-й - 5-й дни;
Ифосфамид 1,8 г/м2 в/в инфузия в 1-й - 5-й дни с месной 720 мг/м² 3 раза в день (длительность курса 21 день).
• VAC:
Винкристин 1,5 мг/м2 в/в в 1-й день;
Доксорубицин 75 мг/м2 в/в в 1-й день;
Циклофосфамид 1200 мг/м2 в/в в 1-й день;
Филграстим 300 мкг в 5-12-й дни (длительность курса 21 день).
• HD VAI.
Винкристин ОД 2 мг в 1-й день.
Доксорубицин 75 мг/м2 в виде 72-часовой инфузии.
Ифосфамид 2,5 гр/м2 в/в в виде 3-часовой инфузии в 1-й - 4-й дни в/в на фоне месны 1000 мг/м² 3 раза в день в/в в 1 - 4-й дни;
Филграстим 300 мкг п/к в 5-й - 14 й дни или до восстановления уровня нейтрофилов.
Длительность цикла - 21 день.
Уровень убедительности рекомендаций. А (уровень достоверности доказательств - Iа).
• Рекомендуются следующие режимы химиотерапии при раннем прогрессировании опухолевого процесса (менее 1 года после завершения комбинированного лечения).
• Иринотекан 250 мг/м2 в/в в 6-й день;
Темозоламид 150 мг/м2 внутрь или в/в в 1-й - 5-й дни;
Повторение цикла каждые 4 недели.
• GemTax гемцитабин 900 мг/м2 в 1-й, 8-й дни в виде 90-минутной инфузии;
Доцетаксел 100 мг/м2 в 8-й день;
Филграстим 300мкг п/к в 9-й - 18-й дни (длительность курса 21 день).
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - IV).
Уровень убедительности рекомендаций. А (уровень достоверности доказательств - Iа).
Комментарии. Чаще всего используются высокие дозы метотрексата, ифосфамид. Использование этопозида неоправдано, так как пока не доказана его эффективность в лечении остеосарком. Если метастазы появились более чем через 6 месяцев после комплексного лечения, возможно повторение ранее используемого режима химиотерапии. При более раннем прогрессировании следует применять другие комбинации цитостатиков.
• Рекомендуется при метастатическом поражении легких обсудить возможность оперативного вмешательства: метастазэктомии, повторной торакотомии в комплексе с химиотерапией [9,11,16].
Уровень убедительности рекомендаций. А (уровень достоверности доказательств - Iа).
Комментарии. При метастазах в легких полное хирургическое удаление метастазов может обеспечить достижение 40-процентной 5-летней выживаемости.
• Рекомендуется использовать те же режимы химиотерапии в такой же последовательности, как и для лечения первичной опухоли [9,11].
Уровень убедительности рекомендаций. А (уровень достоверности доказательств - Iа).
Комментарии. При наличии только легочных метастазов у нелеченых больных химиотерапия должна проводиться не с паллиативной, а лечебной целью с соблюдением режимов, сроков и дозировок, так как в 20 % случаев можно достичь 5-летней выживаемости без признаков заболевания. Кроме стандартных режимов, в качестве третьей и более линий терапии возможно применение сорафениба по 400 мг 2 раза в сутки per os ежедневно.
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - IV).
Комментарии:
• Единственным прогностическим фактором, имеющим значение при рецидиве, является время его возникновения: пациенты, у которых рецидив возник позже, чем через 2 года после установки диагноза, имеют лучшие результаты.
• Пациенты с метастатической формой заболевания должны получать такую же стандартизированную химиотерапию, как и больные с локализованным процессом, с соответствующим локальным воздействием на метастазы (в основном с помощью лучевой терапии).
• У больных с метастазами в легкие повышение выживаемости может быть достигнуто путем резекции остаточных метастазов только после эффективной химиотерапии и тотальным облучением легкого.
• Пациенты с метастазами в кости или костный мозг имеют плохой прогноз (5-летняя выживаемость менее 20 %). При наличии костных метастазов показано проведение лучевой терапии.
• Применение интенсивных и высокодозных режимов химиотерапии с последующей аутологичной трансплантацией костного мозга оправдано у отдельных пациентов после тщательного обследования.
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - IV).
3,1 Хирургическое лечение.
3,1,1 Хирургическое лечение пациентов с остеосаркомой кости.
• Рекомендуется выполнение органосохранных операций для пациентов с диагнозом саркома кости. Главным условием операбельности пациентов с диагнозом саркома кости является радикальность и абластичность удаления опухоли, что гарантирует отсутствие местного рецидива [3,4,13].Уровень убедительности рекомендаций. С (уровень достоверности доказательств - IV).
Комментарии. В первую очередь следует рассматривать возможность выполнения органосохранных операций. Размер первичного очага опухоли, степень распространения внекостного компонента не могут использоваться как самостоятельные независимые критерии в решении вопроса о проведении калечащей операции. Костные резекции при наличии минимального необходимого отступа от предполагаемого края опухоли не менее 3-5 см (при условии отсутствия распространения опухоли в костномозговом канале оставшейся части кости).
При невозможности выполнения органосохранных операций необходимо выполнение калечащих операций в радикальном объеме. Ампутация или экзартикуляция конечности выполняются в следующих случаях:
• обширное первично-множественное распространение опухоли;
• вовлечение в опухолевый процесс магистрального сосудисто-нервного пучка, технически исключающий проведение реконструктивно-пластического этапа операции;
• прогрессирование на фоне предоперационной химиотерапии;
• отказ пациента от органосохранной операции;
• жизненные показания к экстренной хирургии - распад опухоли, кровотечения.
В специализированных центрах операции с сохранением конечности удается выполнить у 80 % больных. Широкое отступление от опухоли важно для профилактики местных рецидивов вне зависимости от опухолевого ответа.
• Рекомендуются следующие тактики лечения в зависимости от формы остеосаркомы:
• Паростальная (юкстакортикальная) остеосаркома - только радикальное хирургическое лечение (вне зависимости от степени распространения опухоли);
• Периостальная остеосаркома - радикальное хирургическое лечение. В зависимости от размера первичного очага и степени распространения опухоли на консилиуме в составе хирурга-онкоортопеда и химиотерапевта принимается решение о целесообразности консервативного лечения. Применяемая химиотерапия в ряде случаев может уменьшить размеры первичного очага и метастазов опухоли, способствовать ее отграничению псевдокапсулой и перевести в резектабельное состояние;
• Остеосаркома высокой степени злокачественности - проведение комбинированного лечения: блока неоадъювантной химиотерапии, радикальное хирургическое лечение, блок адъювантной химиотерапии [2,6].
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - IV).
• Рекомендуется использование модульных систем эндопротезирования, что признано наиболее актуальным и современным, отвечающим основным требованиям реконструкции костных дефектов при саркомах костей [3].
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - IV).
Комментарии. Выделяют следующие виды реконструктивных операций в объеме эндопротезирования:
• Стандартные первичные операции у взрослых;
• Стандартные первичные операции у детей и подростков;
• Эндопротезирование редких анатомических зон;
• Ревизионное эндопротезиование.
Требования, предъявляемые к конструкции эндопротеза при первичном эндопротезировании у взрослых:
• Модульность конструкции эндопротеза;
• Максимальная надежность и ремонтопригодность эндопротеза;
• Универсальность компонентов эндопротеза;
• Максимальный срок службы;
• Стабильная фиксация эндопротеза;
• Хороший функциональный результат;
• Короткий срок изготовления эндопротеза.
Особенности эндопротеза при первичном эндопротезировании у детей и подростков:
• Наличие бесцементного способа фиксации эндопротеза;
• Раздвижной механизм эндопротеза (инвазивный и неинвазивный).
• Рекомендуется проведение ревизионных операций у онкологических больных, вне зависимости от их причин, в клиниках с подготовленной командой онкоортопедов, специализированного инновационного наукоемкого оборудования, высокотехнологического хирургического инструментария. Вследствие чего этот вид хирургического лечения пациентов должен производиться в крупных специализированных стационарах онкологического профиля, где накоплен опыт и отработаны методики ревизионного эндопротезирования.
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - IV).
Комментарии. В современной онкоортопедии рост числа первичного эндопротезирования, успехи в химиотерапии костных сарком приводят к ежегодному увеличению числа пациентов, требующих проведения повторных ортопедических операцией, связанных с нестабильностью или поломкой эндопротеза.
Каждый ревизионный эндопротез изготавливается индивидуально. Применение модульной системы эндопротезирования упрощает выполнение последующих ревизионных операций, увеличивает биологический резерв кости. Возможность изготовления индивидуальных компонентов эндопротеза для ревизионных операций, при развитии нестабильности позволяет, не удаляя весь эндопротез, заменить его часть.
3,1,2 Хирургическое лечение пациентов с саркомой Юинга.
Рекомендуемая хирургическая тактика лечения пациентов с саркомой Юинга кости и остеосаркомой не имеет принципиальных различий и проводиться с соблюдением онкологических и ортопедических правил выполнения такого вида операций, описанных в разделе 3,1,1.3,2 Консервативное лечение.
3,2,1 Химиотерапия пациентам с остеосаркомой кости.
• Рекомендуется проводить комбинированное лечение пациентам с локализованной формой остеосаркомы, которое включает предоперационную химиотерапию, операцию, послеоперационную химиотерапию [2,9,11,20].Уровень убедительности рекомендаций. А (уровень достоверности доказательств - Iа).
Комментарии. Только хирургическое лечение нецелесообразно, так как у 80-90 % больных в течение 1,5 лет после операции диагностируются метастазы в легких и локальные рецидивы. Химиотерапия как часть комплексного лечения значительно улучшает 5-летнюю выживаемость у больных с локализованным процессом (с 20 % до 60 %).
• Рекомендуется проводить предоперационную химиотерапию. Преимущества предоперационной химиотерапии заключаются в возможности оценки in vivo активности химиотерапевтических препаратов и облегчении выполнения операции [11,20,21].
Уровень убедительности рекомендаций. А (уровень достоверности доказательств - Iа).
Комментарии. Обычно проводится 3-4 цикла предоперационной химиотерапии. Степень некроза опухоли после предоперационной химиотерапии - надежный независимый прогностический фактор. При выраженном ответе опухоли на проводимое лечение (некроз опухоли 90 % и более) имеется большая вероятность увеличения безрецидивной и общей выживаемости. У больных с отсутствием эффективности послеоперационная химиотерапия не приводит к улучшению выживаемости.
• Рекомендуется проводить послеоперационную химиотерапию. Послеоперационная химиотерапия определяется степенью лекарственного патоморфоза. При III-IV степени повреждения опухоли (более 90 % опухолевой ткани некротизировано в результате предоперационной химиотерапии) послеоперационно проводится 4 курса химиотерапии без замены цитостатиков, при меньшей степени некроза длительность лечения составляет около 12 месяцев с использованием альтернирующих схем, включающих 5-6 цитостатиков [11].
Уровень убедительности рекомендаций. А (уровень достоверности доказательств - Iа).
Комментарии. Оценка степени лечебного патоморфоза должна проводиться только опытным морфологом, специализирующимся на костной онкопатологии в специализированных центрах.
• Рекомендуется при лечении локализованного опухолевого процесса применять интенсивную химиотерапию на основе комбинации доксорубицина и цисплатина. При явной низкой клинической и рентгенологической эффективностью после двух курсов схема лечения меняется и проводятся два курса высокодозного ифосфамида. Многие центры включают в схему ифосфамид или высокие дозы метотрексата с кальцием фолината, при крайне низкой степени лечебного патоморфоза также используется комбинация гемцитабина и доцетаксела. Продолжительность химиотерапии варьирует от 7 до 12 месяцев. Обязательным условием проведения химиотерапии должно быть строгое соблюдение методики введения высоких доз метотрексата, ифосфамида, цисплатина. Использование меторексата более оправдано у пациентов молодого возраста, считается, что эффективность у больных старше 25-30 лет сомнительна [2,10].
Уровень убедительности рекомендаций. А (уровень достоверности доказательств - Ib).
Комментарии. Проведение высокодозной химиотерапии возможно только в специализированных центрах, при наличии оборудования для контроля концентрации препаратов в сыворотке крови и отделений интенсивной терапии и реанимации.
• Рекомендуются следующие режимы химиотерапии остеосаркомы кости:
• AP :
Доксорубицин 90 мг/м2 в/в, 96-часовая инфузия +.
Цисплатин 120 мг/м2 в/в инфузия в 1-й день каждые 4 недели 4 цикла.
Филграстим 300мкг п/к в 5-й - 14-й дни.
• HD I (используется при низкой эффективности после 2 циклов АР):
Ифосфамид 2000 мг/м2 в/в в 1-й (с месной 2400 мг/м2) - 7-й дни, 2 цикла;
Филграстим 300мкг п/к в 8-й - 17-й дни [9,11,20].
Уровень убедительности рекомендаций. А (уровень достоверности доказательств - Ib).
• Рекомендуется, как альтернативный вариант после операции, следующий режим:
• Некроз опухоли более 90 %:
• HD AI (75/10):
Доксорубицин 75 г/м2 в 1-й день в/в в виде 72-часовой непрерывной инфузии;
Ифосфамид 2500 мг/м2 в 1-й - 4-й дни в/в с месной 1000 мг/м2 3 раза в день [9,11,20];
Филграстим 300мкг п/к в 5-й - 14-й дни, 4 цикла с интервалом 3 недели;
Или повторение схемы АР, также 4 цикла.
• Некроз опухоли от 50 до 90 %:
• HD I:
Ифосфамид 2 г/м2 (с месной 2400 мг/м2) в/в инфузия в 1-й - 7-й дни, 2 цикла с интервалом 3 недели;
Филграстим 300мкг п/к в 8-й - 17-й дни.
• Через 3 недели - HD MTX:
Метотрексат 12 г/м2 в/в инфузия с кальцием фолинатом 15 мг/м² в 1-5-й дни, 4 введения с интервалом в 14 дней для пациентов молодого возраста.
• Через 3 недели - HD AI (75/10):
Доксорубицин 75 г/м2 в 1-й день в/в в виде 72-часовой непрерывной инфузии;
Ифосфамид 2500 мг/м2 в 1-й - 4-й дни в/в на фоне месны 1000 мг/м² 3 раза в день в 1 - 4-й дни по схеме;
Филграстим 300мкг п/к в 5-й - 14-й дни, 4 цикла с интервалом 3 недели;
• Все 3 схемы повторяются 3 раза.
• Некроз опухоли менее 50 %:
• Применяются те же схемы трижды, но с заменой режима HD AI на режим GemTax:
Гемцитабин 900 мг/м2 в 1-й, 8-й дни в виде 90-минутной инфузии;
Доцетаксел 100 мг/м2 в 8-й день;
Филграстим 300мкг п/к в 9-й - 18-й дни, 2 цикла [9,11,20].
Уровень убедительности рекомендаций. А (уровень достоверности доказательств - Ib).
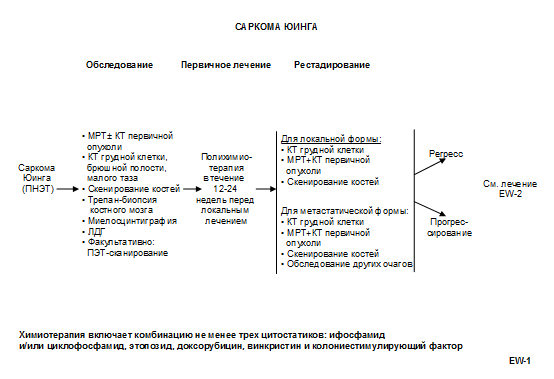
3,2,2 Консервативное лечение пациентов с саркомой Юинга.
Саркомы семейства Юинга / PNET являются редкими опухолями, преимущественно молодого возраста, характеризующимися повышенной чувствительностью к лучевой и химиотерапии, лечение их требует комплексного подхода и должно проводиться в специализированных центрах.• Рекомендуемое стадирование не отличается от общепринятой классификации для первичных опухолей костей, детально описанной в разделе остеосарком. При внекостной форме стадирование проводится по системе для опухолей мягких тканей. [2,6].
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - IV).
• Рекомендуется дополнительно включать в стандартный алгоритм диагностических процедур для первичных опухолей костей, сцинтиграфию костей скелета и трепанобиопсия костного мозга.
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - IV).
Комментарии. С учетом высокой частоты метастазирования в кости и костный мозг. Рекомендуемое локальное лечение (операция или лучевая терапия) должно обязательно сопровождаться комбинированной химиотерапией, при клинически локализованной форме заболевания к моменту установления диагноза 90 % больных имеют микрометастазы. Комбинация химиотерапии, операции и/или лучевой терапии повысила уровень 5-летней выживаемости с 10 % до 60 %. После биопсии опухоли и тщательного обследования проводится от 4 до 6 циклов индукционной химиотерапии в течение 12-24 недель, далее следует локальный метод лечения с последующим назначением от 6 до 10 циклов химиотерапии с 3-недельным интервалом. Продолжительность лечения составляет 12 месяцев. Наиболее активными цитостатиками являются доксорубицин, циклофосфамид, ифосфамид, винкристин, дактиномицин и этопозид. Фактически все режимы лечения основаны на комбинациях из 4-6 перечисленных препаратов. Наиболее эффективные режимы лечения включали как минимум один алкилирующий химиопрепарат (ифосфамид или циклофосфамид) и доксорубицин. Добавление ифосфамида и этопозида в программу лечения значительно улучшило результаты терапии у пациентов с неметастатической саркомой Юинга / ПНЭТ.
Радикальная операция в тех случаях, когда она выполнима, расценивается как наилучшая возможность локального контроля.
Лучевая терапия показана при невозможности выполнения радикального оперативного вмешательства и обсуждается в тех случаях, когда при гистологическом исследовании удаленного материала определяется недостаточный лечебный патоморфоз (то есть выявляется более 10 % жизнеспособных опухолевых клеток). Нерадикальная операция с последующей лучевой терапией не более эффективна, чем только лучевая терапия. Лучевая терапия проводится в дозах 40-45 Гр при микроскопических остаточных опухолях и 50-60 Гр при наличии макроскопических изменений.
• Рекомендуется применять дистанционную 3-D и интенсивно модулированную (IMRT) лучевую терапию в комбинации с химиотерапией при отказе от операции или нерадикально выполненной операции в качестве локального лечения. РОД = 2-2,5 Гр, СОД = 60 Гр. При метастазах в легкие - крупнопольная лучевая терапия РОД = 2 Гр, СОД = 20 Гр [8,10,18].
Уровень убедительности рекомендаций. А (уровень достоверности доказательств - Iа).
• Рекомендуются следующие режимы химиотерапии [8,10,19]:
• Чередование IE и VAC каждые 3-4 недели:
• IE:
Этопозид 100 мг/м2 в/в в 1-й - 5-й дни;
Ифосфамид 1,8 г/м2 в/в инфузия в 1-й - 5-й дни с месной 720 мг/м² 3 раза в день (длительность курса 21 день).
• VAC:
Винкристин 1,5 мг/м2 в/в в 1-й день;
Доксорубицин 75 мг/м2 в/в в 1-й день;
Циклофосфамид 1200 мг/м2 в/в в 1-й день;
Филграстим 300 мкг в 5-12-й дни (длительность курса 21 день).
• HD VAI.
Винкристин ОД 2 мг в 1-й день.
Доксорубицин 75 мг/м2 в виде 72-часовой инфузии.
Ифосфамид 2,5 гр/м2 в/в в виде 3-часовой инфузии в 1-й - 4-й дни в/в на фоне месны 1000 мг/м² 3 раза в день в/в в 1 - 4-й дни;
Филграстим 300 мкг п/к в 5-й - 14 й дни или до восстановления уровня нейтрофилов.
Длительность цикла - 21 день.
Уровень убедительности рекомендаций. А (уровень достоверности доказательств - Iа).
• Рекомендуются следующие режимы химиотерапии при раннем прогрессировании опухолевого процесса (менее 1 года после завершения комбинированного лечения).
• Иринотекан 250 мг/м2 в/в в 6-й день;
Темозоламид 150 мг/м2 внутрь или в/в в 1-й - 5-й дни;
Повторение цикла каждые 4 недели.
• GemTax гемцитабин 900 мг/м2 в 1-й, 8-й дни в виде 90-минутной инфузии;
Доцетаксел 100 мг/м2 в 8-й день;
Филграстим 300мкг п/к в 9-й - 18-й дни (длительность курса 21 день).
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - IV).
3,3,1 Лечение при метастатическом и рецидивном течении остеосаркомы кости.
• Рекомендуется при лечении метастатических форм заболевания применять комбинированную химиотерапию в сочетании с возможным оперативным лечением. Выбор второй линии химиотерапии зависит от первичного лечения [9,11].Уровень убедительности рекомендаций. А (уровень достоверности доказательств - Iа).
Комментарии. Чаще всего используются высокие дозы метотрексата, ифосфамид. Использование этопозида неоправдано, так как пока не доказана его эффективность в лечении остеосарком. Если метастазы появились более чем через 6 месяцев после комплексного лечения, возможно повторение ранее используемого режима химиотерапии. При более раннем прогрессировании следует применять другие комбинации цитостатиков.
• Рекомендуется при метастатическом поражении легких обсудить возможность оперативного вмешательства: метастазэктомии, повторной торакотомии в комплексе с химиотерапией [9,11,16].
Уровень убедительности рекомендаций. А (уровень достоверности доказательств - Iа).
Комментарии. При метастазах в легких полное хирургическое удаление метастазов может обеспечить достижение 40-процентной 5-летней выживаемости.
• Рекомендуется использовать те же режимы химиотерапии в такой же последовательности, как и для лечения первичной опухоли [9,11].
Уровень убедительности рекомендаций. А (уровень достоверности доказательств - Iа).
Комментарии. При наличии только легочных метастазов у нелеченых больных химиотерапия должна проводиться не с паллиативной, а лечебной целью с соблюдением режимов, сроков и дозировок, так как в 20 % случаев можно достичь 5-летней выживаемости без признаков заболевания. Кроме стандартных режимов, в качестве третьей и более линий терапии возможно применение сорафениба по 400 мг 2 раза в сутки per os ежедневно.
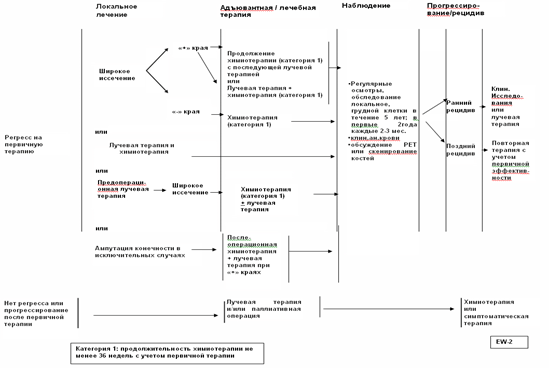
3,3,2 Лечение при метастатическом и рецидивном течении саркомы Юинга.
• Рекомендуется терапия паллиативного характера, за исключением больных с ограниченным рецидивом после длительного безрецидивного периода.Уровень убедительности рекомендаций. С (уровень достоверности доказательств - IV).
Комментарии:
• Единственным прогностическим фактором, имеющим значение при рецидиве, является время его возникновения: пациенты, у которых рецидив возник позже, чем через 2 года после установки диагноза, имеют лучшие результаты.
• Пациенты с метастатической формой заболевания должны получать такую же стандартизированную химиотерапию, как и больные с локализованным процессом, с соответствующим локальным воздействием на метастазы (в основном с помощью лучевой терапии).
• У больных с метастазами в легкие повышение выживаемости может быть достигнуто путем резекции остаточных метастазов только после эффективной химиотерапии и тотальным облучением легкого.
• Пациенты с метастазами в кости или костный мозг имеют плохой прогноз (5-летняя выживаемость менее 20 %). При наличии костных метастазов показано проведение лучевой терапии.
• Применение интенсивных и высокодозных режимов химиотерапии с последующей аутологичной трансплантацией костного мозга оправдано у отдельных пациентов после тщательного обследования.
|
|
Реабилитация и амбулаторное лечение
• Рекомендуются следующие реабилитационные мероприятия:
• Экзопротезирование для пациентов перенесших калечащие операции;
• Проведение курсов ранней и отсроченной реабилитации больных после органосохраняющего лечения в специализированных стационарах и центрах реабилитации.
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - IV).
• Экзопротезирование для пациентов перенесших калечащие операции;
• Проведение курсов ранней и отсроченной реабилитации больных после органосохраняющего лечения в специализированных стационарах и центрах реабилитации.
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - IV).
Профилактика
• Пациентам, закончившим этап комбинированного лечения, рекомендуется динамическое наблюдение каждые 3 месяца в течение первых 2 лет, далее раз в 6 месяцев до 5 лет. Обязательными процедурами являются: КТ грудной клетки, УЗИ области послеоперационного рубца.
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - IV).
Комментарии. Задачей наблюдения является раннее выявление прогрессирования заболевания с целью раннего начала химиотерапии или хирургического лечения резектабельных метастатических очагов, рецидивных опухолей, профилактика ортопедических осложнений, выявление нестабильности эндопротеза в ранних сроках. Информация по данному разделу представлена в приложении Г1.
• Пациентам с остеосаркомой дополнительно рекомендуется рентгенография зоны костного поражения [2,3,4,9,11].
Уровень убедительности рекомендаций. А (уровень достоверности доказательств - Iа).
• Пациентам с саркомой Юинга дополнительно рекомендуется УЗИ брюшной полости, периферических лимфоузлов.
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - IV).
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - IV).
Комментарии. Задачей наблюдения является раннее выявление прогрессирования заболевания с целью раннего начала химиотерапии или хирургического лечения резектабельных метастатических очагов, рецидивных опухолей, профилактика ортопедических осложнений, выявление нестабильности эндопротеза в ранних сроках. Информация по данному разделу представлена в приложении Г1.
• Пациентам с остеосаркомой дополнительно рекомендуется рентгенография зоны костного поражения [2,3,4,9,11].
Уровень убедительности рекомендаций. А (уровень достоверности доказательств - Iа).
• Пациентам с саркомой Юинга дополнительно рекомендуется УЗИ брюшной полости, периферических лимфоузлов.
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - IV).
Дополнительно
Неблагоприятные факторы, влияющие на исход лечения:
• Присоединение инфекционных осложнений;
• Развитие нестабильности при протезировании;
• Наличие патологического перелома;
• Развитие анемического, тромбоцитопенического синдромов, требующие трансфузий компонентов крови;
• Удлинение интервалов между введениями химиопрепаратов;
• Редукция доз химиопрепаратов;
• Несоблюдение пациентом рекомендаций, как в ходе лечения, так и при динамическом наблюдении.
• Присоединение инфекционных осложнений;
• Развитие нестабильности при протезировании;
• Наличие патологического перелома;
• Развитие анемического, тромбоцитопенического синдромов, требующие трансфузий компонентов крови;
• Удлинение интервалов между введениями химиопрепаратов;
• Редукция доз химиопрепаратов;
• Несоблюдение пациентом рекомендаций, как в ходе лечения, так и при динамическом наблюдении.
Критерии оценки качества медицинской помощи
| № | Критерии качества | Уровень достоверности доказательств | Уровень убедительности рекомендаций |
| 1 | Выполнена морфологическая верификация саркомы кости | Ia | A |
| 2 | Выполнены обследования перед началом лечения в соответствии с рекомендациями | III | в |
| 3 | Выполнено хирургическое лечение в объёме, соответствующем указанным в рекомендациях | IIb | в |
| 4 | Выполнена анестезия в соответствии с объемом оперативного вмешательства и тяжестью состояния пациента | IV | с |
| 5 | Отсутствие незапланированной интраоперационной травмы соседних органов (магистральных сосудов, мочеточников, мочевого пузыря, селезенки, тонкой кишки) (у больных, кому выполнено хирургическое лечение) | III | в |
| 6 | Выполнено гистологическое исследование удаленного препарата, с указанием параметров в соответствии с рекомендациями (у больных, кому выполнено хирургическое лечение) | Ib | A |
| 7 | Выполнена послеоперационная терапия (химиотерапия) в соответствии с рекомендациями | Ia | A |
| 8 | Выполнена периоперационная антибиотикопрофилактика (у больных, кому выполнено хирургическое лечение) | Ia | A |
| 9 | Выполнена тромбопрофилактика послеоперационных осложнений (при условии отсутствия противопоказаний к её проведению; у больных, кому выполнено хирургическое лечение) | Ia | A |
Список литературы
• Алиев М.Д., Сушенцов Е.А. современная онкоортопедия. Саркомы костей, мягких тканей и опухоли кожи. 2012. №4. - сс3-10.
• Алиев М.Д. Злокачественные опухоли костей Саркомы костей, мягких тканей и опухоли кожи. 2010. №2. - сс3-8.
• Алиев М.Д. Эндопротезирование как основа онкоортопедии Саркомы костей, мягких тканей и опухоли кожи. 2010. №4. - сс7-12.
• А.А. Курильчик, А.Л. Зубарев, Г.Т. Кудрявцева, А.Л. Стародубцев. Интраоперационная лучевая терапия (ИОЛТ) в комбинированном лечении остеосаркомы. Саркомы костей, мягких тканей и опухоли кожи. 2010. №3. - сс30-33.
• Тепляков В.В., Карпенко В.Ю., Бухаров А.В., Державин В.А., Урлова А.Н., Рубцова Н.А. Результаты хирургического лечения пациентов с метастазами в длинные трубчатые кости. Саркомы костей, мягких тканей и опухоли кожи. 2010. №3. - сс10-15.
• Malawer M.M., Helman L.J., O’Sullivan в. Sarcomas of bone. DeVita, Hellman, and Rosenberg s сancer: Principles & Practice of Oncology. 2008. 8th ed. - vol.2. - pp.1794-1833.
• Kalra S1, Grimer RJ, Spooner D. et al. Radiation-induced sarcomas of bone: factors that affect outcome. J вone Joint Surg вr. 2007 Jun;89(6):808-13.
• Grier HE, Krailo MD, Tarbell NJ, et al. Addition of ifosfamide and etoposide to standard chemotherapy for Ewing s sarcoma and primitive neuroectodermal tumor of bone. N Engl J Med 2003;348:694-701.
• Lewis IJ, Nooij MA, Whelan J, et al. Improvement in histologic response but not survival in osteosarcoma patients treated with intensified chemotherapy: a randomized phase III trial of the European Osteosarcoma Intergroup. J Natl сancer Inst 2007;99:112-128.
• Womer RB, West DC, Krailo MD, et al. Randomized controlled trial of interval-compressed chemotherapy for the treatment of localized Ewing sarcoma: A report from the сhildren’s Oncology Group. J сlin Oncol 2012 Nov 20;30(33):4148-54.
• Souhami RL, сraft AW, Van der Eijken JW, et al. Randomised trial of two regimens of chemotherapy in operable osteosarcoma: a study of the European Osteosarcoma Intergroup. Lancet 1997;350:911-917.
• Lewis IJ, Nooij MA, Whelan J, et al. Improvement in histologic response but not survival in osteosarcoma patients treated with intensi ed chemotherapy: a randomized phase III trial of the European Osteosarcoma Intergroup. J Natl сancer Inst 2007;99:112-128.
• Fiorenza F, Abudu A, Grimer RJ, et al. Risk factors for survival and local control in chondrosarcoma of bone. J вone Joint Surg вr 2002;84:93-99.
• Marulanda GA, Henderson ER, Johnson DA, et al. Orthopedic surgery options for the treatment of primary osteosarcoma. сancer сontrol 2008;15:13-20.
• вacci G, Ferrari S, Lari S, et al. Osteosarcoma of the limb. Amputation or limb salvage in patients treated by neoadjuvant chemotherapy. J вone Joint Surg вr 2002;84:88-92.
• Kager L1, Zoubek A, Pötschger U. et al. Primary metastatic osteosarcoma: presentation and outcome of patients treated on neoadjuvant сooperative Osteosarcoma Study Group protocols. J сlin Oncol. 2003 May 15;21(10):2011-8.
• Gogna A1, Peh WC, Munk PL. Image-guided musculoskeletal biopsy. Radiol сlin North Am. 2008 May;46(3):455-73.
• Gupta AA1, Pappo A, Saunders N. et al. сlinical outcome of children and adults with localized Ewing sarcoma: impact of chemotherapy dose and timing of local therapy. сancer. 2010 Jul 1;116(13):3189-94.
• вacci G1, Forni с, Longhi A, Ferrari S. et al. Long-term outcome for patients with non-metastatic Ewing s sarcoma treated with adjuvant and neoadjuvant chemotherapies. 402 patients treated at Rizzoli between 1972 and 1992. Eur J сancer. 2004 Jan;40(1):73-83.
• вielack SS1, Kempf-Bielack в, Delling G. et al. Prognostic factors in high-grade osteosarcoma of the extremities or trunk: an analysis of 1,702 patients treated on neoadjuvant cooperative osteosarcoma study group protocols. J сlin Oncol. 2002 Feb 1;20(3):776-90.
• вernthal NM1, Federman N, Eilber FR. et al. Long-term results (>25 years) of a randomized, prospective clinical trial evaluating chemotherapy in patients with high-grade, operable osteosarcoma. сancer. 2012 Dec 1;118(23):5888-93.
• Smeland S1, вruland OS, Hjorth L. et al. Results of the Scandinavian Sarcoma Group XIV protocol for classical osteosarcoma: 63 patients with a minimum follow-up of 4 years. Acta Orthop. 2011 Apr;82(2):211-6.
• Алиев М.Д. Злокачественные опухоли костей Саркомы костей, мягких тканей и опухоли кожи. 2010. №2. - сс3-8.
• Алиев М.Д. Эндопротезирование как основа онкоортопедии Саркомы костей, мягких тканей и опухоли кожи. 2010. №4. - сс7-12.
• А.А. Курильчик, А.Л. Зубарев, Г.Т. Кудрявцева, А.Л. Стародубцев. Интраоперационная лучевая терапия (ИОЛТ) в комбинированном лечении остеосаркомы. Саркомы костей, мягких тканей и опухоли кожи. 2010. №3. - сс30-33.
• Тепляков В.В., Карпенко В.Ю., Бухаров А.В., Державин В.А., Урлова А.Н., Рубцова Н.А. Результаты хирургического лечения пациентов с метастазами в длинные трубчатые кости. Саркомы костей, мягких тканей и опухоли кожи. 2010. №3. - сс10-15.
• Malawer M.M., Helman L.J., O’Sullivan в. Sarcomas of bone. DeVita, Hellman, and Rosenberg s сancer: Principles & Practice of Oncology. 2008. 8th ed. - vol.2. - pp.1794-1833.
• Kalra S1, Grimer RJ, Spooner D. et al. Radiation-induced sarcomas of bone: factors that affect outcome. J вone Joint Surg вr. 2007 Jun;89(6):808-13.
• Grier HE, Krailo MD, Tarbell NJ, et al. Addition of ifosfamide and etoposide to standard chemotherapy for Ewing s sarcoma and primitive neuroectodermal tumor of bone. N Engl J Med 2003;348:694-701.
• Lewis IJ, Nooij MA, Whelan J, et al. Improvement in histologic response but not survival in osteosarcoma patients treated with intensified chemotherapy: a randomized phase III trial of the European Osteosarcoma Intergroup. J Natl сancer Inst 2007;99:112-128.
• Womer RB, West DC, Krailo MD, et al. Randomized controlled trial of interval-compressed chemotherapy for the treatment of localized Ewing sarcoma: A report from the сhildren’s Oncology Group. J сlin Oncol 2012 Nov 20;30(33):4148-54.
• Souhami RL, сraft AW, Van der Eijken JW, et al. Randomised trial of two regimens of chemotherapy in operable osteosarcoma: a study of the European Osteosarcoma Intergroup. Lancet 1997;350:911-917.
• Lewis IJ, Nooij MA, Whelan J, et al. Improvement in histologic response but not survival in osteosarcoma patients treated with intensi ed chemotherapy: a randomized phase III trial of the European Osteosarcoma Intergroup. J Natl сancer Inst 2007;99:112-128.
• Fiorenza F, Abudu A, Grimer RJ, et al. Risk factors for survival and local control in chondrosarcoma of bone. J вone Joint Surg вr 2002;84:93-99.
• Marulanda GA, Henderson ER, Johnson DA, et al. Orthopedic surgery options for the treatment of primary osteosarcoma. сancer сontrol 2008;15:13-20.
• вacci G, Ferrari S, Lari S, et al. Osteosarcoma of the limb. Amputation or limb salvage in patients treated by neoadjuvant chemotherapy. J вone Joint Surg вr 2002;84:88-92.
• Kager L1, Zoubek A, Pötschger U. et al. Primary metastatic osteosarcoma: presentation and outcome of patients treated on neoadjuvant сooperative Osteosarcoma Study Group protocols. J сlin Oncol. 2003 May 15;21(10):2011-8.
• Gogna A1, Peh WC, Munk PL. Image-guided musculoskeletal biopsy. Radiol сlin North Am. 2008 May;46(3):455-73.
• Gupta AA1, Pappo A, Saunders N. et al. сlinical outcome of children and adults with localized Ewing sarcoma: impact of chemotherapy dose and timing of local therapy. сancer. 2010 Jul 1;116(13):3189-94.
• вacci G1, Forni с, Longhi A, Ferrari S. et al. Long-term outcome for patients with non-metastatic Ewing s sarcoma treated with adjuvant and neoadjuvant chemotherapies. 402 patients treated at Rizzoli between 1972 and 1992. Eur J сancer. 2004 Jan;40(1):73-83.
• вielack SS1, Kempf-Bielack в, Delling G. et al. Prognostic factors in high-grade osteosarcoma of the extremities or trunk: an analysis of 1,702 patients treated on neoadjuvant cooperative osteosarcoma study group protocols. J сlin Oncol. 2002 Feb 1;20(3):776-90.
• вernthal NM1, Federman N, Eilber FR. et al. Long-term results (>25 years) of a randomized, prospective clinical trial evaluating chemotherapy in patients with high-grade, operable osteosarcoma. сancer. 2012 Dec 1;118(23):5888-93.
• Smeland S1, вruland OS, Hjorth L. et al. Results of the Scandinavian Sarcoma Group XIV protocol for classical osteosarcoma: 63 patients with a minimum follow-up of 4 years. Acta Orthop. 2011 Apr;82(2):211-6.
|
|
Приложения
Приложение А1.
Состав рабочей группы.• Алиев Мамед Джавадович, д.м.н., профессор, академик РАН, заместитель директора по научной и лечебной работе ФГБУ ФГБУ «НМИЦ онкологии им. Н. Н. Блохина» Минздрава России, директор НИИ ДОГ ФГБУ «НМИЦ онкологии им. Н. Н. Блохина» Минздрава России, заведующий отделом общей онкологии НИИ КО ФГБУ «НМИЦ онкологии им. Н. Н. Блохина», Президент «Восточно-европейской группы по изучению сарком».
• Бохян Бениамин Юрикович, м.н., старший научный сотрудник отделения опухолей опорно-двигательного аппарата НИИ КО ФГБУ «НМИЦ онкологии им. Н. Н. Блохина».
• Иванов Станислав Михайлович, м.н., старший научный сотрудник радиологического отделения ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России.
• Соколовский Владимир Александрович, д.м.н. ведущий научный сотрудник отделения опухолей опорно-двигательного аппарата НИИ КО ФГБУ «НМИЦ онкологии им. Н. Н. Блохина».
• Сушенцов Евгений Александрович, м.н., старший научный сотрудник отделения опухолей опорно-двигательного аппарата НИИ КО ФГБУ «НМИЦ онкологии им. Н. Н. Блохина».
• Феденко Александр Александрович, д.м.н., ведущий научный сотрудник отделения химиотерапии НИИ КО ФГБУ «НМИЦ онкологии им. Н.Н. Блохина».
• Конев Андрей Андреевич, врач-онколог отделения опухолей опорно-двигательного аппарата НИИ КО ФГБУ «НМИЦ онкологии им. Н. Н. Блохина».
Все члены рабочей группы заявляют об отсутствии конфликта интересов.
Приложение А2.
Методология разработки клинических рекомендаций.Целевая аудитория данных клинических рекомендаций:
• Врачи - онкологи, травматологи, ортопеды, общие хирурги, врачи общей практики, радиологи, педиатры;
• Преподаватели и студенты медицинских образовательных учреждений, ординаторы и аспиранты.
Методы, использованные для сбора/селекции доказательств. Поиск в электронных базах данных; анализ современных научных разработок по проблеме диагностики и лечения сарком в России и за рубежом; обобщение практического опыта российских и зарубежных специалистов.
Таблица П1. Уровни достоверности доказательств в соответствии с классификацией Агентства по политике медицинского обслуживания и исследований (AHCPR, 1992).
| Уровни достоверности доказательств | Описание |
| Ia | Доказательность, основанная на мета-анализе рандомизированных контролируемых исследований |
| Ib | Доказательность, основанная как минимум на одном рандомизированном контролируемом исследовании с хорошим дизайном |
| IIa | Доказательность, основанная как минимум на одном крупном нерандомизированном контролируемом исследовании |
| IIb | Доказательность, основанная как минимум на одном квазиэксперементальном исследовании с хорошим дизайном |
| III | Доказательность, основанная на неэкспериментальных описательных исследованиях с хорошим дизайном, типа сравнительных исследований, корреляционных исследований и исследований случай-контроль |
| IV | Доказательность, основанная на мнении экспертов, на опыте или мнении авторов |
Таблица П2. Уровни убедительности рекомендаций в соответствии с классификацией Агентства исследований и оценки качества медицинского обслуживания (AHRQ, 1994).
| Уровень убедительности рекомендации | Уровни достоверности доказательств | Описание |
| A | Ia, Ib | Доказательность, основанная как минимум на одном рандомизированном контролируемом исследовании с хорошим дизайном |
| в | IIa, IIb, III | Доказательность, основанная на хорошо выполненных нерандомизированных клинических исследованиях |
| с | IV | Доказательность, основанная на мнении экспертов, на опыте или мнении авторов. Указывает на отсутствие исследований высокого качества |
Методы, использованные для формулирования рекомендаций. Консенсус экспертов.
Экономический анализ.
Анализ стоимости не проводился и публикации по фармакоэкономике не анализировались.
Метод валидизации рекомендаций:
• Внешняя экспертная оценка.
• Внутренняя экспертная оценка.
Описание метода валидизации рекомендаций:
Настоящие рекомендации в предварительной версии рецензированы независимыми экспертами, которые попросили прокомментировать, прежде всего, насколько интерпретация доказательств, лежащих в основе рекомендаций, доступна для понимания.
Получены комментарии со стороны врачей- онкологов первичного звена в отношении доходчивости изложения рекомендаций и их оценки важности рекомендаций как рабочего инструмента повседневной практики.
Комментарии, полученные от экспертов, тщательно систематизировались и обсуждались председателем и членами рабочей группы. Каждый пункт обсуждался и вносимые в результате этого изменения в рекомендации регистрировались. Если же изменения не вносились, то регистрировались причины отказа от внесения изменений.
Консультации и экспертная оценка: Проект рекомендаций рецензирован также независимыми экспертами, которых попросили прокомментировать, прежде всего, доходчивость и точность интерпретации доказательной базы, лежащей в основе рекомендаций.
Для окончательной редакции и контроля качества рекомендации повторно проанализированы членами рабочей группы, которые пришли к заключению, что все замечания и комментарии экспертов приняты во внимание, риск систематических ошибок при разработке рекомендаций сведен к минимуму.
Обновления клинических рекомендаций: актуализация проводится не реже чем один раз в три года с учетом появившейся новой информации о диагностике и тактике ведения пациентов с саркомами костей. Решение об обновлении принимает МЗ РФ на основе предложений, представленных медицинскими профессиональными сообществами. Сформированные предложения должны учитывать результаты комплексной оценки лекарственных препаратов, медицинских изделий, а также результаты клинической апробации.
При отборе публикаций, как потенциальных источников доказательств, использованная в каждом исследовании методология изучается для того, чтобы убедиться в ее достоверности. Результат изучения влияет на уровень доказательств, присваиваемый публикации, что в свою очередь влияет на силу, вытекающих из нее рекомендаций.
Приложение А3.
Связанные документы.• Приказ Минздрава России от 7 июля 2015 г. N 422ан «Об утверждении критериев оценки качества медицинской помощи»;
• Перечень жизненно необходимых и важнейших лекарственных препаратов на 2016 г. Распоряжение Правительства РФ от 26,12,2015 № 2724-р.
• Постановление Правительства Российской Федерации «О порядке и условиях признания лица инвалидом» от 20 февраля 2006 г. №95 (в ред. Постановлений Правительства РФ от 07,04,2008 № 247, от 30,12,2009 № 1121, от 06,02,2012 №89, от 16,04,2012 № 318, от 04,09,2012 № 882).
• Изменения, которые вносятся в Правила признания лица инвалидом, утвержденные Постановлением Правительства Российской Федерации от 7 апреля 2008г. 24;
• Приказ Министерства Здравоохранения и Социального развития Российской Федерации от 17 декабря 2015 г. 1024н «О классификации и критериях, используемых при осуществлении медико-социальной экспертизы граждан федеральными государственными учреждениями медико-социальной экспертизы»;
• Федеральный закон от 9 декабря 2010г. 351-ФЗ «О внесении изменений в Федеральный закон «О ветеранах» и статьи 11 и 11,1 Федерального закона «О социальной защите инвалидов в Российской Федерации»;
• Порядок выплаты компенсации за самостоятельно приобретенное инвалидом техническое средство реабилитации и (или) оказанную услугу, включая порядок определения ее размера и порядок информирования граждан о размере указанной компенсации (Приказ Минздравсоцразвития России №57н от 31 января 2011 г.
КР400. Хронический болевой синдром (ХБС) у взрослых пациентов, нуждающихся в паллиативной медицинской помощи.
Приложение В.
Информация для пациентов.• Пациенты с любой формой саркомы кости с диспансерного учета не снимаются.
• Рекомендации при осложнениях химиотерапии - связаться с химиотерапевтом.
1) При повышении температуры тела 38°C и выше:
• Начать прием антибиотиков: по рекомендации химиотерапевта.
2) При стоматите:
• Диета - механическое, термическое щажение;
• Частое полоскание рта (каждый час) - ромашка, кора дуба, шалфей, смазывать рот облепиховым (персиковым) маслом;
• Обрабатывать полость рта по рекомендации химиотерапевта.
3) При диарее:
• Диета - исключить жирное, острое, копченое, сладкое, молочное, клетчатку. Можно нежирное мясо, мучное, кисломолочное, рисовый отвар. Обильное питье;
• Принимать препараты по рекомендации химиотерапевта.
4) При тошноте:
• Принимать препараты по рекомендации химиотерапевта.
Приложение Г.
| Методы исследования | Сроки контрольных обследований после достижения ремиссии, мес. | |||||||||||
| 1 | 3 | 6 | 9 | 12 | 18 | 24 | 30 | 36 | 42 | 48 | Пожизненно 1 раз в год | |
| Консультация онкоортопеда | х | х | х | х | х | х | х | х | х | х | х | х |
| Рентгенография оперированной области в двух проекциях | х | х | х | х | х | х | х | х | х | х | х | х |
| УЗИ области операции, брюшной полости, забрюшинного пространства, периферических лимфоузлов | х | х | х | х | х | х | х | х | х | х | х | х |
| КТ органов грудной клетки | - | - | - | - | х | - | х | - | х | - | х | * |
|
|
Год актуализации информации
2018.
Связанные заболевания
Связанные клинические рекомендации
Связанные стандарты мед. помощи
- Стандарт медицинской помощи больным с заболеваниями нервной и других систем, требующих дистанционной многоисточниковой прецизионной лучевой терапии со стереотаксическим наведением
- Стандарт медицинской помощи больным злокачественными новообразованиями костей, суставов и суставных хрящей конечностей, других и неуточненных локализаций (при оказании специализированной помощи)
- Стандарт медицинской помощи больным со злокачественным новообразованием позвоночного столба, костей таза, крестца и копчика, вторичным злокачественным новообразованием костей и костного мозга
- Стандарт специализированной медицинской помощи при злокачественных новообразованиях костей II-IV стадии (неоадьювантная, адьювантная, самостоятельная химиотерапия)
- Стандарт медицинской помощи больным со злокачественным новообразованием костей, суставов и суставных хрящей конечностей, других и неуточненных локализаций
- Стандарт специализированной медицинской помощи при злокачественных новообразованиях костей I-IV стадии (самостоятельная дистанционная лучевая терапия)
- Стандарт специализированной медицинской помощи при злокачественных новообразованиях костей I-IV стадии (самостоятельная лучевая терапия)
- Стандарт первичной медико-санитарной помощи при злокачественных новообразованиях костей и суставных хрящей I-IV стадии (обследование в целях установления диагноза заболевания и подготовки к противоопухолевому лечению)