Другие названия и синонимы
Ewing 's sarcoma.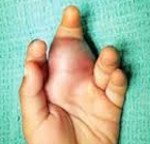
МКБ-10 коды
|
|
Описание
Саркома Юинга (лат. endothelial myeloma) - злокачественная опухоль костного скелета. Саркома Юинга, как правило, поражает нижнюю часть длинных трубчатых костей, ребра, таз, лопатку, позвоночник и ключицу.
Саркома Юинга была открыта Джеймсом Юингом (1866-1943) в 1921 году. Ученый охарактеризовал её как опухоль, поражающую в основном длинные трубчатые кости.
Саркома Юинга является одной из самых агрессивных злокачественных опухолей. До применения системной терапии почти у 90% больных развивались метастазы. Наиболее частая локализация метастазов на момент первичной диагностики - легкие, кости, костный мозг. 14%- 50% пациентов к моменту установления диагноза уже имеют метастазы, выявляемые рутинными методами исследования, и гораздо больше больных имеют микрометастазы. Лимфогенное распространение метастазов встречается редко и всегда связано с плохим прогнозом. Редко также имеет место ретроперитонеальное и медиастинальное распространение метастазов. 2,2% пациентов имеют метастазы в ЦНС при первичной диагностике, и почти все - при генерализации процесса.
Саркома Юинга была открыта Джеймсом Юингом (1866-1943) в 1921 году. Ученый охарактеризовал её как опухоль, поражающую в основном длинные трубчатые кости.
Саркома Юинга является одной из самых агрессивных злокачественных опухолей. До применения системной терапии почти у 90% больных развивались метастазы. Наиболее частая локализация метастазов на момент первичной диагностики - легкие, кости, костный мозг. 14%- 50% пациентов к моменту установления диагноза уже имеют метастазы, выявляемые рутинными методами исследования, и гораздо больше больных имеют микрометастазы. Лимфогенное распространение метастазов встречается редко и всегда связано с плохим прогнозом. Редко также имеет место ретроперитонеальное и медиастинальное распространение метастазов. 2,2% пациентов имеют метастазы в ЦНС при первичной диагностике, и почти все - при генерализации процесса.
Клиническая картина
• Боль.
Первым признаком является боль, которая, в отличие от воспалительного процесса, не стихает в покое (усиление по ночам, отсутствие облегчения при фиксации конечностей).
По мере роста опухоли начинает страдать функция близлежащего сустава, и затем развивается прощупываемая опухоль, нередко с патологическим переломом (поздний признак).
На третьем - четвёртом месяце от начала заболевания из-за боли сначала нарушается, а затем прекращается движение в ближайшем суставе.
• Повышение температуры тела больного.
• Наличие опухолевого образования.
В области растущей опухоли появляется припухлость, покраснение, расширенные подкожные вены и местное повышение температуры.
• Возможны нарушения функций пораженной конечности.
• Иногда возникает лихорадка.
Примерно у 50 % больных, по данным литературы, симптомы болезни отмечались в течение более чем 3 месяцев до установления правильного диагноза.
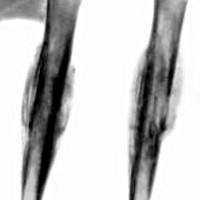
Наиболее частая локализация саркомы Юинга - кости таза, бедро, большеберцовая кость, малоберцовая кость, ребра, лопатка, позвонки, плечевая кость. В противоположность остеогенной саркоме, саркома Юинга чаще всего поражает плоские кости. В трубчатых костях опухоль локализуется преимущественно в диафизе и имеет тенденцию к распространению к эпифизам кости. В 91% случаев опухоль располагается интрамедуллярно, причем распространение по костномозговому каналу часто больше, чем по кости.
Ассоциированные симптомы: Боль в бедре. Боль в костях таза. Боль в ребрах. Изменение аппетита. Изменение веса. Истощение. Кровохарканье. Ломота в мышцах. Лихорадка. Отсутствие аппетита. Потеря веса. Общая слабость. Хромота.
Первым признаком является боль, которая, в отличие от воспалительного процесса, не стихает в покое (усиление по ночам, отсутствие облегчения при фиксации конечностей).
По мере роста опухоли начинает страдать функция близлежащего сустава, и затем развивается прощупываемая опухоль, нередко с патологическим переломом (поздний признак).
На третьем - четвёртом месяце от начала заболевания из-за боли сначала нарушается, а затем прекращается движение в ближайшем суставе.
• Повышение температуры тела больного.
• Наличие опухолевого образования.
В области растущей опухоли появляется припухлость, покраснение, расширенные подкожные вены и местное повышение температуры.
• Возможны нарушения функций пораженной конечности.
• Иногда возникает лихорадка.
Примерно у 50 % больных, по данным литературы, симптомы болезни отмечались в течение более чем 3 месяцев до установления правильного диагноза.
Наиболее частая локализация саркомы Юинга - кости таза, бедро, большеберцовая кость, малоберцовая кость, ребра, лопатка, позвонки, плечевая кость. В противоположность остеогенной саркоме, саркома Юинга чаще всего поражает плоские кости. В трубчатых костях опухоль локализуется преимущественно в диафизе и имеет тенденцию к распространению к эпифизам кости. В 91% случаев опухоль располагается интрамедуллярно, причем распространение по костномозговому каналу часто больше, чем по кости.
Ассоциированные симптомы: Боль в бедре. Боль в костях таза. Боль в ребрах. Изменение аппетита. Изменение веса. Истощение. Кровохарканье. Ломота в мышцах. Лихорадка. Отсутствие аппетита. Потеря веса. Общая слабость. Хромота.
Причины
Для костных сарком характерен быстрый рост и раннее метастазирование. Саркома Юинга является второй по частоте среди злокачественных опухолей костей у детей - составляет 10-15 %. Эта опухоль редко встречается у детей моложе 5 лет и у взрослых старше 30 лет. Пик заболеваемости приходится на 10−15 лет.
Причина появления злокачественных опухолей костей пока не известна, однако доказано, что в 40 % возникновение костной саркомы провоцирует травма.
Существует некоторая связь между возникновением саркомы Юинга и наличием скелетных аномалий (энхондрома, аневризмальная костная киста ) и аномалиями мочеполовой системы (гипоспадии, редупликация почечной системы). В отличие от остеосаркомы, ионизирующая иррадиация не ассоциируется с возникновением саркомы Юинга.
Цитогенетический анализ показывает в 85% случаев хромосомную транслокацию t(11,22) (q24, q12) в большинстве клеток, выделенных из этой опухоли. Аналогичные изменения выявляются в другой мелкоклеточной опухоли - PNET (примитивной нейроэктодермальной опухоли). И хотя саркома Юинга не имеет анатомической связи со структурами ЦНС или автономной симпатической нервной системы, эти цитогенетические изменения доказывают нейроэктодермальную природу опухоли. Кроме того, в большинстве случаев в клетках опухоли выявляется экспрессия РАХ3 протеина, который в норме определяется в период эмбрионального развития нейроэктодермальной ткани. При саркоме Юинга часто можно определить и другой опухолевый маркер - NSE (сывороточная нейрон-специфичная энолаза).
Саркома Юинга состоит из мелких круглых клеток со скудной цитоплазмой, круглым ядром, содержащим нежный хроматин и слабо просматривающиеся базофильные нуклеолы. В отличие от остеосаркомы, она не продуцирует остеоид.
Идея эндотелиальной природы опухоли Юинга превалировала до 1980 года. Исследования, проведенные в последние годы, показали нейрогенную природу опухоли Юинга. Хотя чаще саркома Юинга является недифференцированной опухолью костей, имеются данные о поражении мягких тканей (экстраоссальная саркома Юинга). В специальной литературе появился термин «семейство опухолей типа саркомы Юинга».
Факторы риска развития саркомы Юинга.
В настоящее время известно несколько факторов риска, связанных с возникновением саркомы Юинга.
Пол. Саркома Юинга несколько чаще встречается среди мальчиков по сравнению с девочками.
Возраст. В 64% случаев саркома Юинга встречается в возрасте от 10 до 20 лет.
Раса. Наиболее часто саркома Юинга наблюдается у белого населения.
Причина появления злокачественных опухолей костей пока не известна, однако доказано, что в 40 % возникновение костной саркомы провоцирует травма.
Существует некоторая связь между возникновением саркомы Юинга и наличием скелетных аномалий (энхондрома, аневризмальная костная киста ) и аномалиями мочеполовой системы (гипоспадии, редупликация почечной системы). В отличие от остеосаркомы, ионизирующая иррадиация не ассоциируется с возникновением саркомы Юинга.
Цитогенетический анализ показывает в 85% случаев хромосомную транслокацию t(11,22) (q24, q12) в большинстве клеток, выделенных из этой опухоли. Аналогичные изменения выявляются в другой мелкоклеточной опухоли - PNET (примитивной нейроэктодермальной опухоли). И хотя саркома Юинга не имеет анатомической связи со структурами ЦНС или автономной симпатической нервной системы, эти цитогенетические изменения доказывают нейроэктодермальную природу опухоли. Кроме того, в большинстве случаев в клетках опухоли выявляется экспрессия РАХ3 протеина, который в норме определяется в период эмбрионального развития нейроэктодермальной ткани. При саркоме Юинга часто можно определить и другой опухолевый маркер - NSE (сывороточная нейрон-специфичная энолаза).
Саркома Юинга состоит из мелких круглых клеток со скудной цитоплазмой, круглым ядром, содержащим нежный хроматин и слабо просматривающиеся базофильные нуклеолы. В отличие от остеосаркомы, она не продуцирует остеоид.
Идея эндотелиальной природы опухоли Юинга превалировала до 1980 года. Исследования, проведенные в последние годы, показали нейрогенную природу опухоли Юинга. Хотя чаще саркома Юинга является недифференцированной опухолью костей, имеются данные о поражении мягких тканей (экстраоссальная саркома Юинга). В специальной литературе появился термин «семейство опухолей типа саркомы Юинга».
Факторы риска развития саркомы Юинга.
В настоящее время известно несколько факторов риска, связанных с возникновением саркомы Юинга.
Пол. Саркома Юинга несколько чаще встречается среди мальчиков по сравнению с девочками.
Возраст. В 64% случаев саркома Юинга встречается в возрасте от 10 до 20 лет.
Раса. Наиболее часто саркома Юинга наблюдается у белого населения.
Лечение
• Многокомпонентная химиотерапия (используются препараты - винкристин, адриамицин, ифосфамид, циклофосфан, актиномицин, вепезид в комбинации). В современных программах лечения применяется предоперационная и послеоперационная полихимиотерапия, при этом учитывается также гистологический ответ опухоли на лечение. Хорошим ответом опухоли на химиотерапию считается наличие менее 5 % живых опухолевых клеток.
• Лучевая терапия на очаг в высоких дозах. При развитии метастазов в легкие проводится лучевая терапия на легкие.
• Если возможно, радикальное удаление опухоли (включая кость и мягкотканный компонент). Радикальная резекция возможна при очаге в малоберцовой кости, костях предплечья, ребрах, ключице, лопатке.
Операция улучшает локальный контроль опухоли. В сочетании с интенсивной химиотерапией и лучевой терапией значительно снижается риск местного рецидива. Уменьшение частоты местного рецидива отмечается даже после нерадикальных операций. Современная хирургическая техника позволяет проводить органосохраняющие операции при поражении бедренной, плечевой костей, а также резекцию костей таза.
Пациентам с плохим прогнозом, в частности с метастазами в кости и костный мозг, имеющих выживаемость менее 10 %, в последнее время назначают более интенсивное лечение - химиотерапия мегадозами препаратов с тотальным облучением тела и трансплантацией аутологичного костного мозга или периферических стволовых клеток. Эта терапия позволяет излечить более 30 % больных с распространенным процессом (при метастазах в кости и костный мозг). У больных с хорошей чувствительностью опухоли удается достичь ещё более высоких результатов лечения (7-летняя выживаемость составляет около 50 %).
Пациентам с плохим прогнозом, в частности с метастазами в кости и костный мозг, имеющих выживаемость менее 10%, в последнее время применяется более интенсивное лечение - химиотерапия мегадозами препаратов с тотальным облучением тела и трансплантацией аутологичного костного мозга или периферических стволовых клеток. Эта терапия позволяет излечить более 30% больных с распространенным процессом (при метастазах в кости и костный мозг). У больных с хорошей чувствительностью опухоли к ХТ удается достичь еще более высоких результатов лечения (7-летняя выживаемость составляет около 50%).
• Лучевая терапия на очаг в высоких дозах. При развитии метастазов в легкие проводится лучевая терапия на легкие.
• Если возможно, радикальное удаление опухоли (включая кость и мягкотканный компонент). Радикальная резекция возможна при очаге в малоберцовой кости, костях предплечья, ребрах, ключице, лопатке.
Операция улучшает локальный контроль опухоли. В сочетании с интенсивной химиотерапией и лучевой терапией значительно снижается риск местного рецидива. Уменьшение частоты местного рецидива отмечается даже после нерадикальных операций. Современная хирургическая техника позволяет проводить органосохраняющие операции при поражении бедренной, плечевой костей, а также резекцию костей таза.
Пациентам с плохим прогнозом, в частности с метастазами в кости и костный мозг, имеющих выживаемость менее 10 %, в последнее время назначают более интенсивное лечение - химиотерапия мегадозами препаратов с тотальным облучением тела и трансплантацией аутологичного костного мозга или периферических стволовых клеток. Эта терапия позволяет излечить более 30 % больных с распространенным процессом (при метастазах в кости и костный мозг). У больных с хорошей чувствительностью опухоли удается достичь ещё более высоких результатов лечения (7-летняя выживаемость составляет около 50 %).
Пациентам с плохим прогнозом, в частности с метастазами в кости и костный мозг, имеющих выживаемость менее 10%, в последнее время применяется более интенсивное лечение - химиотерапия мегадозами препаратов с тотальным облучением тела и трансплантацией аутологичного костного мозга или периферических стволовых клеток. Эта терапия позволяет излечить более 30% больных с распространенным процессом (при метастазах в кости и костный мозг). У больных с хорошей чувствительностью опухоли к ХТ удается достичь еще более высоких результатов лечения (7-летняя выживаемость составляет около 50%).
|
|
Связанные клинические рекомендации
Связанные стандарты мед. помощи
- Стандарт медицинской помощи больным злокачественными новообразованиями костей, суставов и суставных хрящей конечностей, других и неуточненных локализаций (при оказании специализированной помощи)
- Стандарт специализированной медицинской помощи при злокачественных новообразованиях костей II-IV стадии (неоадьювантная, адьювантная, самостоятельная химиотерапия)
- Стандарт медицинской помощи больным со злокачественным новообразованием костей, суставов и суставных хрящей конечностей, других и неуточненных локализаций
- Стандарт специализированной медицинской помощи при злокачественных новообразованиях костей I-IV стадии (самостоятельная дистанционная лучевая терапия)
- Стандарт специализированной медицинской помощи при злокачественных новообразованиях костей I-IV стадии (самостоятельная лучевая терапия)
- Стандарт первичной медико-санитарной помощи при злокачественных новообразованиях костей и суставных хрящей I-IV стадии (обследование в целях установления диагноза заболевания и подготовки к противоопухолевому лечению)
- Стандарт специализированной медицинской помощи при злокачественных новообразованиях костей I-IV стадии (предоперационная лучевая терапия)
- Стандарт специализированной медицинской помощи при злокачественных новообразованиях костей I-IV стадии (предоперационная дистанционная лучевая терапия)