Другие названия и синонимы
Orlistat.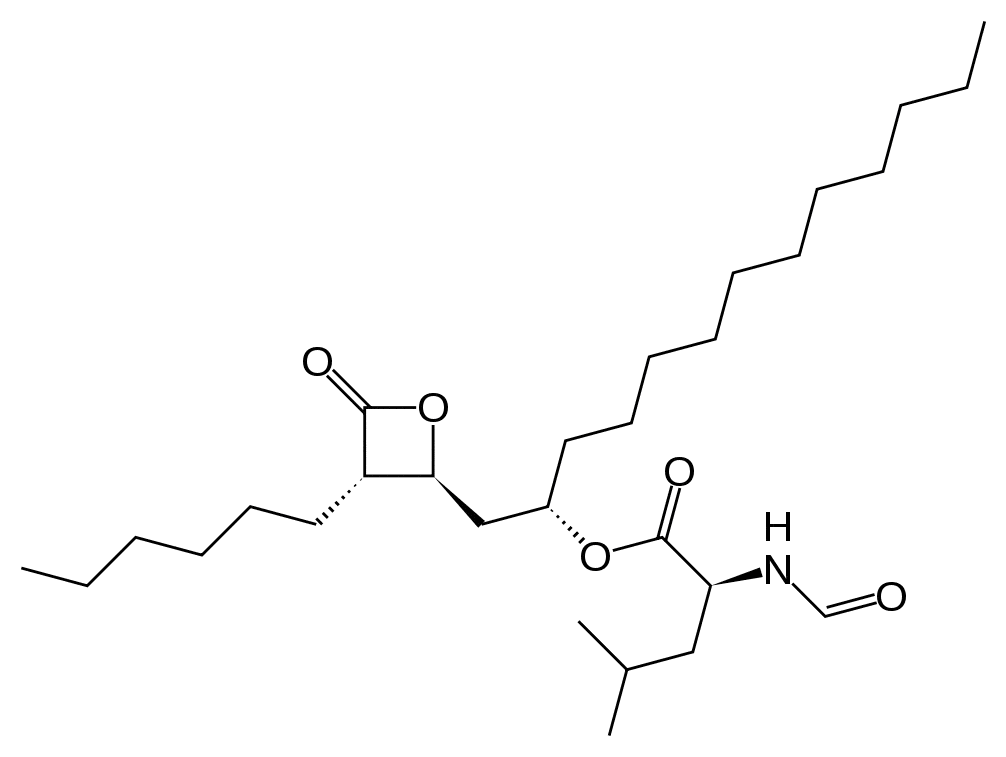
Фармакологическая группа
|
|
Латинское название
Orlistatum ( Orlistati).
Химическое название
[2S-[2альфа(R*), 3 бета]]-1-[(3-Гексил-4оксо-2-оксетанил)-метил]додециловый эфир N-формил-L-лейцина.
Используется в лечении
Код CAS
96829-58-2.
Фармакологическое действие
Ингибирующее желудочно-кишечные липазы.
Характеристика вещества
Кристаллический порошок от белого до не совсем белого цвета, практически нерастворим в воде, свободно растворим в хлороформе и очень хорошо растворим в метаноле и этаноле. Не имеет pKa в пределах физиологического диапазона рН. Молекулярная масса составляет 495,7 Да.
Фармакодинамика
Механизм действия.
Орлистат является обратимым ингибитором желудочно-кишечных липаз. Действует в просвете желудка и тонкой кишки, образуя ковалентную связь с активным участком остатка серина желудочной и панкреатической липаз. Инактивированные ферменты неспособны гидролизовать поступающие с пищей жиры в форме триглицеридов до абсорбируемых свободных жирных кислот и моноглицеридов. Поскольку непереваренные триглицериды не усваиваются, возникающий дефицит калорий может оказать положительное влияние на контроль массы тела.
Фармакодинамика.
Эффект орлистата оценивался долей выделяемого с фекалиями жира, поступившего с пищей. В рекомендуемой терапевтической дозе 120 мг 3 раза в день орлистат ингибирует всасывание пищевых жиров примерно на 30%. Этанол не влияет на действие орлистата на предотвращение всасывания жира.
В нескольких исследованиях продолжительностью до 6 нед оценивалось влияние терапевтических доз орлистата на желудочно-кишечные и системные физиологические процессы у взрослых лиц с нормальным весом и ожирением. Концентрация холецистокинина в плазме крови после приема пищи уменьшалась после многократных доз орлистата в двух исследованиях, в двух других исследованиях - существенно не отличалась от таковой при приеме плацебо. Не наблюдалось клинически значимых изменений в двигательной активности желчного пузыря, составе или литогенности желчи, скорости пролиферации клеток толстой кишки, а также клинически значимого сокращения времени опорожнения желудка или понижения кислотности желудка. Кроме того, в этих исследованиях не наблюдалось влияния на уровни триглицеридов в плазме или системные липазы при введении орлистата. В 3-недельном исследовании с участием 28 здоровых добровольцев мужского пола орлистат в дозе 120 мг 3 раза в день существенно не влиял на баланс кальция, магния, фосфора, цинка, меди и железа.
В 3-недельном исследовании с участием 32 подростков от 12 до 16 лет с ожирением орлистат в дозе 120 мг 3 раза в день существенно не влиял на баланс кальция, магния, фосфора, цинка или меди. Баланс железа был снижен соответственно на 64,7 и 40,4 мкмоль/сут в группах получавших орлистат и плацебо.
Орлистат является обратимым ингибитором желудочно-кишечных липаз. Действует в просвете желудка и тонкой кишки, образуя ковалентную связь с активным участком остатка серина желудочной и панкреатической липаз. Инактивированные ферменты неспособны гидролизовать поступающие с пищей жиры в форме триглицеридов до абсорбируемых свободных жирных кислот и моноглицеридов. Поскольку непереваренные триглицериды не усваиваются, возникающий дефицит калорий может оказать положительное влияние на контроль массы тела.
Фармакодинамика.
Эффект орлистата оценивался долей выделяемого с фекалиями жира, поступившего с пищей. В рекомендуемой терапевтической дозе 120 мг 3 раза в день орлистат ингибирует всасывание пищевых жиров примерно на 30%. Этанол не влияет на действие орлистата на предотвращение всасывания жира.
В нескольких исследованиях продолжительностью до 6 нед оценивалось влияние терапевтических доз орлистата на желудочно-кишечные и системные физиологические процессы у взрослых лиц с нормальным весом и ожирением. Концентрация холецистокинина в плазме крови после приема пищи уменьшалась после многократных доз орлистата в двух исследованиях, в двух других исследованиях - существенно не отличалась от таковой при приеме плацебо. Не наблюдалось клинически значимых изменений в двигательной активности желчного пузыря, составе или литогенности желчи, скорости пролиферации клеток толстой кишки, а также клинически значимого сокращения времени опорожнения желудка или понижения кислотности желудка. Кроме того, в этих исследованиях не наблюдалось влияния на уровни триглицеридов в плазме или системные липазы при введении орлистата. В 3-недельном исследовании с участием 28 здоровых добровольцев мужского пола орлистат в дозе 120 мг 3 раза в день существенно не влиял на баланс кальция, магния, фосфора, цинка, меди и железа.
В 3-недельном исследовании с участием 32 подростков от 12 до 16 лет с ожирением орлистат в дозе 120 мг 3 раза в день существенно не влиял на баланс кальция, магния, фосфора, цинка или меди. Баланс железа был снижен соответственно на 64,7 и 40,4 мкмоль/сут в группах получавших орлистат и плацебо.
Фармакокинетика
Абсорбция.
Системное воздействие орлистата минимально. После перорального приема 360 мг 14С-орлистата радиоактивность плазмы достигла максимума примерно через 8 концентрация интактного орлистата в плазме была близка к порогу обнаружения (≈5 нг/мл). В терапевтических исследованиях с мониторингом образцов плазмы обнаружение интактного орлистата в плазме было спорадическим, а концентрации - низкими (≈10 нг/мл или 0,02 мкМ) без признаков накопления и указывали на минимальную абсорбцию.
Распределение.
In vitro орлистат на 99% связывался с белками плазмы (в основном с липопротеинами и альбумином).
Метаболизм.
Масс-балансовое исследование с участием пациентов с ожирением, получавших перорально 14C-орлистат, показало, что два метаболита, M1 (продукт гидролиза β-лактонового кольца орлистата) и M3 ( метаболит M1, образующийся после расщепления боковой цепи N-формиллейцина), составляли приблизительно 42% от общей радиоактивности в плазме. M1 и M3 имеют открытое β-лактоновое кольцо и чрезвычайно слабую ингибирующую активность в отношении липаз (соответственно в 1000 и 2500 раз меньше, чем у орлистата). Ввиду слабой ингибирующей активности и низкого уровня в плазме крови при терапевтической дозе (в среднем 26 и 108 нг/мл для M1 и M3 соответственно через 2-4 ч после приема дозы) эти метаболиты считаются фармакологически незначимыми. Первичный метаболит M1 имел короткий 1/2T1/2 (приблизительно 3 ч), тогда как вторичный M3 выводился более медленно (T1/2 приблизительно 13,5 ч).
Выведение.
После однократной пероральной дозы 360 мг 14С-орлистата как у лиц с нормальным весом, так и у лиц с ожирением было установлено, что основным путем выведения является экскреция с калом неабсорбированного препарата. Орлистат и его метаболиты M1 и M3 также выводились с желчью. Приблизительно 97% введенной радиоактивности обнаруживалось в кале, 83% этого количества - в виде неизмененного вещества. Кумулятивная почечная экскреция общей радиоактивности составила <2% полученной дозы 360 мг 14С-орлистата. Время достижения полного выведения (с калом и мочой) составляло от 3 до 5 дней. Распределение орлистата, по-видимому, было одинаковым у пациентов с нормальным весом и ожирением. Основываясь на ограниченных данных, 1/2T1/2 абсорбированного орлистата составляет от 1 до 2.
Особые группы населения.
Фармакокинетическое исследование не проводилось для конкретных групп населения, таких как пожилые люди, представители разных рас и пациенты с почечной и печеночной недостаточностью.
Канцерогенность, мутагеннность, влияние на фертильность.
Исследования канцерогенности на крысах и мышах не показали канцерогенного потенциала орлистата в дозах до 1000 мг/кг/сут и 1500 мг/кг/сут соответственно. Для мышей и крыс эти дозы в 38 и 46 раз превышают суточную дозу для человека, рассчитанную на основе AUC.
Орлистат не показал мутагенной или генотоксической активности, определенной с помощью теста Эймса, анализа прямой мутации млекопитающих (V79/HPRT), анализа кластогенеза in vitro >in vitro в периферических лимфоцитах человека, незапланированного анализа синтеза ДНК в гепатоцитах крыс и микроядерного теста у мышей in vivo >in vivo.
При введении крысам в дозе 400 мг/кг/сут в исследовании фертильности и репродукции орлистат не оказывал заметных побочных эффектов. Эта доза в 12 раз превышает суточную дозу для человека в расчете на площадь поверхности тела.
Клинические исследования.
Долгосрочные эффекты орлистата на заболеваемость и смертность, связанные с ожирением, не установлены.
Влияние орлистата на снижение, поддержание и восстановление веса, а также на ряд сопутствующих заболеваний (например, диабет типа 2, АГ, дислипидемия) было оценено в 4-летнем исследовании XENDOS и в семи долгосрочных (продолжительностью от 1 до 2 лет) многоцентровых двойных слепых плацебо-контролируемых клинических исследованиях. В течение первого года терапии в исследованиях продолжительностью 2 года оценивалась потеря веса и поддержание веса. В течение второго года терапии в некоторых исследованиях оценивалась продолжающаяся потеря веса и поддержание веса, а в других оценивалось влияние орлистата на восстановление веса. В эти исследования было включено более 2800 пациентов, получавших орлистат, и 1400 пациентов, получавших плацебо (возрастной диапазон 17-78 лет, 80,2 % были женского пола, 91% представителями европеоидной расы, 5,7% афроамериканцами, 2,3% латиноамериканцами, 0,1% представителями других этнических групп). Большинство этих пациентов имели факторы риска, связанные с ожирением, и сопутствующие заболевания. В исследовании XENDOS, в котором приняли участие 3304 пациента (возрастной диапазон 30-58 лет, 55% были женского пола, 99% представителями европеоидной расы, 1% - других этнических групп), в дополнение к влиянию на массу тела оценивалось время до начала развития диабета типа 2. Во всех этих исследованиях лечение орлистатом и плацебо означало лечение орлистатом плюс диета и плацебо плюс диета соответственно.
Во время периода похудения и поддержания веса всем пациентам была рекомендована хорошо сбалансированная низкокалорийная диета, которая должна была привести примерно к 20% снижению потребления калорий и обеспечить поступление 30% калорий из жира. Кроме того, всем пациентам была предложена консультация по питанию.
Результаты одного года исследований. Снижение веса, поддержание веса и факторы риска.
Объединенные данные пяти клинических исследований показали, что общая средняя потеря веса с момента рандомизации до конца 1 года лечения в популяции пациентов с назначенным лечением составила 13,4 фунта (1 фунт=0,45 кг) у пациентов, получавших орлистат, и 5,8 фунта у пациентов, получавших плацебо. После 1 года лечения средняя разница в потере веса между пациентами, получавшими орлистат и плацебо, составила 3%. Завершили 1 год лечения 1072 (69%) пациента, получавших орлистат, и 701 (63%) пациент, получавший плацебо. Из пациентов, которые закончили 1 год лечения, 57% получавших орлистат (120 мг 3 раза в день), и 31% получавших плацебо потеряли не менее 5% от своей исходной массы тела (таблица 1).
Таблица 1.
Доля пациентов со снижением веса ≥5 и ≥10% с момента рандомизации после одного года лечения1.
1 Лечение включало применение орлистата в дозе 120 мг 3 раза в день или плацебо в сочетании с низкокалорийной диетой.
2 Последнее наблюдение перенесено на последующий период.
3 Все другие исследования были проведены в центрах, специализирующихся на лечении ожирения и его осложнений. Исследование 14161 было проведено с участием врачей первичной медицинской помощи.
Относительные изменения значений факторов риска, связанных с ожирением, после 1 года терапии орлистатом и плацебо представлены для популяции в целом и для популяции с аномальными значениями при рандомизации.
Участники исследования в целом.
Изменения метаболических, сердечно-сосудистых и антропометрических факторов риска, связанных с ожирением, на основе объединенных данных пяти клинических исследований, независимо от статуса фактора риска пациента при рандомизации, представлены в таблице 2. Один год терапии орлистатом привел к относительному улучшению значений нескольких факторов риска.
Таблица 2.
Среднее изменение значений факторов риска с момента рандомизации после одного года лечения в популяции в целом1.
1 Лечение включало применение орлистата в дозе 120 мг 3 раза в день или плацебо в сочетании с низкокалорийной диетой.
2 Популяция с назначенным лечением на 52-й нед, объединенные данные наблюдений в 5 исследованиях.
Участники исследования с аномальными значениями факторов риска при рандомизации.
Изменения параметров, по сравнению с исходными значениями при рандомизации, после 1 года лечения в популяции с аномальным уровнем липидов (ЛПНП ≥130 мг/дл, ЛПНП/ЛПВП ≥3,5, ЛПВП <35 мг/дл) были больше у получавших орлистат по сравнению с получавшими плацебо в отношении Хс-ЛПНП (−7,83 против +1,14%) и ЛПНП/ЛПВП (−0,64 против −0,46). Уровень ЛПВП увеличился в группе плацебо на 20,1%, а в группе орлистата на 18,8%. В популяции с аномальным исходным АД (сАД ≥140 мм ) изменение сАД со времени рандомизации до 1 года лечения было больше в группе получавших орлистат (−10,89 мм ), чем в группе получавших плацебо (−5,07 мм ). У пациентов с дАД ≥90 мм ст при приеме орлистата дАД снизилось на −7,9 мм , в то время как у пациентов, получавших плацебо, - на −5,5 мм Уровень инсулина натощак снижался больше в группе получавших орлистат, чем в группе плацебо (−39 против −16 пмоль/л) со времени рандомизации до 1 года в популяции с аномальными исходными значениями (≥120 пмоль/л). Большее уменьшение окружности талии у получавших орлистат по сравнению с плацебо (−7,29 против −4,53 см) наблюдалось в популяции с аномальными исходными значениями (≥100 см).
Влияние на восстановление веса.
Три исследования были разработаны для оценки эффектов орлистата по сравнению с плацебо в снижении восстановления веса после его предыдущей потери, достигнутой либо только после диеты (одно исследование, 14302), либо до лечения орлистатом (два исследования, 14119C и 14185). Диета, используемая в течение 1 года исследований по восстановлению веса, была диетой для поддержания веса, а не диетой для похудения, и пациенты получали меньше консультаций по питанию, чем пациенты в исследованиях по снижению веса. В исследованиях 14119C и 14185 предыдущая потеря веса пациентов была обусловлена 1 годом лечения орлистатом в сочетании с умеренно гипокалорийной диетой. Исследование 14302 было проведено для оценки влияния 1 года лечения орлистатом на восстановление веса у пациентов, которые потеряли 8% или более массы тела за предыдущие 6 мес только на диете.
В исследовании 14119C восстановление веса у пациентов, получавших плацебо, составило 52% от потерянного ранее в то время у пациентов, получавших орлистат, оно составило 26% (р<0,001). В исследовании 14185 пациенты, получавшие плацебо, восстановили 63% веса, который они ранее потеряли, в то время как пациенты, получавшие орлистат, восстановил 35% веса, который они потеряли (р<0,001). В исследовании 14302 пациенты, получавшие плацебо, восстановили 53% веса, который они ранее потеряли, в то время как пациенты, получавшие орлистат, восстановили 32% веса, который они потеряли (р<0,001).
Результаты двух лет исследований. Долгосрочный контроль веса и факторы риска.
Лечебные эффекты орлистата изучались в течение 2 лет в 4 из 5 клинических исследований по снижению веса по результатам 1 года лечения. В конце 1-го года рацион питания пациентов был пересмотрен и при необходимости изменен. Диета, назначенная на второй год, была разработана для поддержания текущего веса пациента. В 4 крупных многоцентровых 2-летних двойных слепых плацебо-контролируемых исследованиях было показано, что орлистат более эффективен, чем плацебо, в долгосрочном контроле веса.
Объединенные данные 4 клинических исследований показывают, что 74% всех пациентов, получавших орлистат в дозе 120 мг 3 раза в день, и 76% пациентов, получавших плацебо, завершили 2 года одинаковой терапии. Средняя разница в потере веса между группами, получавшими орлистат в дозе 120 мг 3 раза в день, и группами, получавшими плацебо, на 2-м году у пациентов, завершивших 1 год лечения, составила 3%. В тех же иследованиях, которые указаны в таблице 1 (после одного года лечения), доля пациентов, достигших потери веса ≥5 и ≥10% после двух лет лечения, приведена в таблице 3.
Таблица 3.
Доля пациентов со снижением веса ≥5 и ≥10% с момента рандомизации после двух лет лечения1.
1 Диета, используемая в течение 2-го года, была разработана для поддержания веса, а не для похудения. Лечение включало прием орлистата в дозе 120 мг 3 раза в день или плацебо в сочетании с диетой.
2 Последнее наблюдение перенесено на последующий период.
3 Все другие исследования были проведены в центрах, специализирующихся на лечении ожирения и его осложнений. Исследование 14161 было проведено с участием врачей первичной медицинской помощи.
Относительные изменения значений факторов риска, связанных с ожирением, после 2 лет терапии также оценивались в популяции в целом и популяции с повышенными факторами риска при рандомизации.
Участники исследования в целом.
Относительные различия в значениях факторов риска между группами, получавшими орлистат и плацебо, были аналогичны результатам после 1 года терапии по таким показателям, как общий Хс, Хс-ЛПНП, соотношение ЛПНП/ЛПВП, триглицериды, уровень глюкозы натощак, уровень инсулина натощак, дАД, окружность талии и окружность бедер. Относительные различия между группами лечения по уровню ЛПВП и значению сАД были меньше, чем наблюдалось по результатам первого года лечения.
Участники исследования с аномальными значениями факторов риска при рандомизации.
Относительные различия в значениях факторов риска между группами, получавшими орлистат и плацебо, были аналогичны результатам после 1 года терапии для ЛПНП и ЛПВП, уровня триглицеридов, инсулина натощак, дАД и окружности талии. Относительные различия между группами лечения по соотношению ЛПНП/ЛПВП и изолированному сАД были меньше, чем наблюдалось по результатам первого года лечения.
Результаты четырех лет исследований. Долгосрочный контроль веса и факторы риска.
В 4-летнем двойном слепом плацебо-контролируемом исследовании XENDOS влияние орлистата на задержку начала развития диабета типа 2 и на массу тела сравнивалось с плацебо у 3304 пациентов с ожирением, у которых исходно была нормальная или нарушенная толерантность к глюкозе. 34% из 1655 пациентов, которые были рандомизированы в группу плацебо, и 52% из 1649 пациентов, которые были рандомизированы в группу орлистата, завершили 4-летнее исследование.
В конце исследования средняя потеря веса в группе плацебо составила −2,75% по сравнению с −5,17% в группе орлистата (р<0,001). 45% пациентов, получавших плацебо, и 73% пациентов, получавших орлистат, потеряли ≥5% от исходной массы тела, а 21% пациентов, получавших плацебо, и 41% пациентов, получавших орлистат, потеряли ≥10% от исходной массы тела после первого года лечения. После 4 лет лечения 28% пациентов, получавших плацебо, и 45% пациентов, получавших орлистат, потеряли ≥5% от исходной массы тела, а 10% пациентов, получавших плацебо, и 21% пациентов, получавших орлистат, потеряли ≥10% от исходной массы тела. После 4 лет лечения средняя разница в потере веса между пациентами, получавшими орлистат и плацебо, составила 2,5%.
Относительные изменения в значениях факторов риска, ассоциированных с ожирением, после 4 лет терапии, оцененные в исследовании XENDOS, представлены в таблице 4.
Таблица 4.
Среднее изменение значений факторов риска с момента рандомизации после 4 лет лечения1.
1 Лечение включало назначение орлистата в дозе 120 мг 3 раза в день или плацебо в сочетании с диетой.
2 Популяция с назначенным лечением.
Начало диабета типа 2 у пациентов с ожирением.
В исследовании XENDOS в общей популяции орлистат отсрочил начало диабета типа 2 и в конце 4 лет лечения совокупный показатель заболеваемости диабетом составил 8,3% в группе плацебо по сравнению с 5,5% в группе орлистата (р=0,01). Этот вывод был обусловлен статистически значимым снижением частоты развития диабета типа 2 у пациентов с исходно нарушенной толерантностью к глюкозе. Орлистат не снижал риск развития сахарного диабета у пациентов с нормальной толерантностью к глюкозе на исходном уровне.
Влияние орлистата на задержку начала диабета типа 2 у пациентов с ожирением и нарушенной толерантностью к глюкозе, по-видимому, обусловлен потерей веса, а не каким-либо независимым воздействием орлистата на метаболизм глюкозы или инсулина. Влияние орлистата на снижение веса является дополнением к диете и физическим упражнениям.
Исследование с участием пациентов с сахарным диабетом типа 2.
Было проведено 1-летнее двойное слепое плацебо-контролируемое исследование с участием пациентов с сахарным диабетом типа 2 (n=321), состояние которых было стабилизировано применением ЛС на основе производных сульфонилмочевины. У 30% пациентов, получавших орлистат, снижение массы тела составило как минимум 5% или более после рандомизации по сравнению с 13% пациентов, получавших плацебо (р<0,001). Средние изменения отдельных показателей у таких пациентов приведены в таблице 5.
Таблица 5.
Средние изменения массы тела и показателей гликемического контроля в сравнении с периодом рандомизации после одного года лечения у пациентов с сахарным диабетом типа 2.
1 Лечение включало применение орлистата в дозе 120 мг 3 раза в день или плацебо в сочетании с диетой.
Кроме того, применение орлистата (n=162) по сравнению с плацебо (n=159) было связано со значительным снижением уровня общего Хс (−1 против +9%, р≤0,05), ЛПНП (−3 против +10%, р<0,05), соотношения ЛПНП/ЛПВП (−0,26 против −0,02, р≤0,05) и триглицеридов (+2,54 против +16,2%, р<0,05) соответственно. Уровень Хс-ЛПВП увеливался на 6,49% при применении орлистата и на 8,6% при применении плацебо, р>0,05. сАД увеличилось на 0,61 мм у получавших орлистат и на 4,33 мм - плацебо, р>0,05. дАД снижалось на 0,47 мм у получавших орлистат и на 0,5 мм - плацебо, р>0,05.
Толерантность к глюкозе у пациентов с ожирением.
Двухлетние исследования, включавшие пероральные тесты на толерантность к глюкозе (ПТТГ), проводились с участием пациентов с ожирением, у которых ранее не диагностировался или не лечился диабет типа 2 и чей базовый статус ПТТГ при рандомизации был либо нормальным, либо нарушенным, либо диабетическим.
Сравнивали прогрессирование от нормальных результатов ПТТГ при рандомизации до значений, соответствующих нарушению или диабету после 2 лет лечения орлистатом (n=251) или плацебо (n=207). После лечения орлистатом 0 и 7,2% пациентов прогрессировали от нормального к диабетическому и от нормального к нарушенному статусу соответственно, по сравнению с 1,9 и 12,6% в группе лечения плацебо соответственно.
У части пациентов с нарушенным статусом ПТТГ состояние улучшилось до нормального или ухудшилось до диабетического после 1 и 2 лет лечения орлистатом по сравнению с плацебо. После 1 года лечения 45,8% пациентов, получавших плацебо, и 73% пациентов, получавших орлистат, имели нормальные результаты ПТТГ, в то время как 10,4% пациентов, получавших плацебо, и 2,6% пациентов, получавших орлистат, заболели диабетом. После 2 лет лечения у 50% пациентов, получавших плацебо, и у 71,7% пациентов, получавших орлистат, был нормальный статус ПТТГ, в то время как у 7,5% пациентов, получавших плацебо, и у 1,7% пациентов, получавших орлистат, был обнаружен диабет после лечения.
Педиатрические клинические исследования.
Влияние орлистата на ИМТ и потерю веса оценивали в 54-недельном многоцентровом двойном слепом плацебо-контролируемом исследовании с участием 539 подростков от 12 до 16 лет с ожирением (357 получали орлистат в дозе 120 мг 3 раза в день и 182 получали плацебо). У всех участников исследования исходный ИМТ был на 2 единицы больше, чем средневзвешенное значение по США с учетом возраста и пола. ИМТ был основным параметром оценки эффективности, поскольку он учитывает изменения роста и массы тела, которые происходят у растущих детей. В ходе исследования всем пациентам было предписано принимать поливитамины, содержащие жирорастворимые витамины, по крайней мере за 2 ч до или после приема орлистата. Пациенты также придерживались сбалансированной, низкокалорийной диеты, которая должна была обеспечивать поступление 30% калорий из жира. Кроме того, все пациенты были включены в программу модификации поведения и получили консультации по физическим упражнениям.
Примерно 65 % пациентов в каждой группе лечения завершили исследование.
После одного года лечения ИМТ снизился в среднем на 0,55 кг/м2 у пациентов, получавших орлистат, и увеличился в среднем на 0,31 кг/м2 у пациентов, получавших плацебо (р=0,001).
Таблица 6.
Доля пациентов со снижением ИМТ и массы тела ≥5 и ≥10% с момента рандомизации после одного года лечения1.
1 Лечение включало применение орлистата в дозе 120 мг 3 раза в день или плацебо в сочетании с диетой.
2 Последнее наблюдение перенесено на последующий период.
Системное воздействие орлистата минимально. После перорального приема 360 мг 14С-орлистата радиоактивность плазмы достигла максимума примерно через 8 концентрация интактного орлистата в плазме была близка к порогу обнаружения (≈5 нг/мл). В терапевтических исследованиях с мониторингом образцов плазмы обнаружение интактного орлистата в плазме было спорадическим, а концентрации - низкими (≈10 нг/мл или 0,02 мкМ) без признаков накопления и указывали на минимальную абсорбцию.
Распределение.
In vitro орлистат на 99% связывался с белками плазмы (в основном с липопротеинами и альбумином).
Метаболизм.
Масс-балансовое исследование с участием пациентов с ожирением, получавших перорально 14C-орлистат, показало, что два метаболита, M1 (продукт гидролиза β-лактонового кольца орлистата) и M3 ( метаболит M1, образующийся после расщепления боковой цепи N-формиллейцина), составляли приблизительно 42% от общей радиоактивности в плазме. M1 и M3 имеют открытое β-лактоновое кольцо и чрезвычайно слабую ингибирующую активность в отношении липаз (соответственно в 1000 и 2500 раз меньше, чем у орлистата). Ввиду слабой ингибирующей активности и низкого уровня в плазме крови при терапевтической дозе (в среднем 26 и 108 нг/мл для M1 и M3 соответственно через 2-4 ч после приема дозы) эти метаболиты считаются фармакологически незначимыми. Первичный метаболит M1 имел короткий 1/2T1/2 (приблизительно 3 ч), тогда как вторичный M3 выводился более медленно (T1/2 приблизительно 13,5 ч).
Выведение.
После однократной пероральной дозы 360 мг 14С-орлистата как у лиц с нормальным весом, так и у лиц с ожирением было установлено, что основным путем выведения является экскреция с калом неабсорбированного препарата. Орлистат и его метаболиты M1 и M3 также выводились с желчью. Приблизительно 97% введенной радиоактивности обнаруживалось в кале, 83% этого количества - в виде неизмененного вещества. Кумулятивная почечная экскреция общей радиоактивности составила <2% полученной дозы 360 мг 14С-орлистата. Время достижения полного выведения (с калом и мочой) составляло от 3 до 5 дней. Распределение орлистата, по-видимому, было одинаковым у пациентов с нормальным весом и ожирением. Основываясь на ограниченных данных, 1/2T1/2 абсорбированного орлистата составляет от 1 до 2.
Особые группы населения.
Фармакокинетическое исследование не проводилось для конкретных групп населения, таких как пожилые люди, представители разных рас и пациенты с почечной и печеночной недостаточностью.
Канцерогенность, мутагеннность, влияние на фертильность.
Исследования канцерогенности на крысах и мышах не показали канцерогенного потенциала орлистата в дозах до 1000 мг/кг/сут и 1500 мг/кг/сут соответственно. Для мышей и крыс эти дозы в 38 и 46 раз превышают суточную дозу для человека, рассчитанную на основе AUC.
Орлистат не показал мутагенной или генотоксической активности, определенной с помощью теста Эймса, анализа прямой мутации млекопитающих (V79/HPRT), анализа кластогенеза in vitro >in vitro в периферических лимфоцитах человека, незапланированного анализа синтеза ДНК в гепатоцитах крыс и микроядерного теста у мышей in vivo >in vivo.
При введении крысам в дозе 400 мг/кг/сут в исследовании фертильности и репродукции орлистат не оказывал заметных побочных эффектов. Эта доза в 12 раз превышает суточную дозу для человека в расчете на площадь поверхности тела.
Клинические исследования.
Долгосрочные эффекты орлистата на заболеваемость и смертность, связанные с ожирением, не установлены.
Влияние орлистата на снижение, поддержание и восстановление веса, а также на ряд сопутствующих заболеваний (например, диабет типа 2, АГ, дислипидемия) было оценено в 4-летнем исследовании XENDOS и в семи долгосрочных (продолжительностью от 1 до 2 лет) многоцентровых двойных слепых плацебо-контролируемых клинических исследованиях. В течение первого года терапии в исследованиях продолжительностью 2 года оценивалась потеря веса и поддержание веса. В течение второго года терапии в некоторых исследованиях оценивалась продолжающаяся потеря веса и поддержание веса, а в других оценивалось влияние орлистата на восстановление веса. В эти исследования было включено более 2800 пациентов, получавших орлистат, и 1400 пациентов, получавших плацебо (возрастной диапазон 17-78 лет, 80,2 % были женского пола, 91% представителями европеоидной расы, 5,7% афроамериканцами, 2,3% латиноамериканцами, 0,1% представителями других этнических групп). Большинство этих пациентов имели факторы риска, связанные с ожирением, и сопутствующие заболевания. В исследовании XENDOS, в котором приняли участие 3304 пациента (возрастной диапазон 30-58 лет, 55% были женского пола, 99% представителями европеоидной расы, 1% - других этнических групп), в дополнение к влиянию на массу тела оценивалось время до начала развития диабета типа 2. Во всех этих исследованиях лечение орлистатом и плацебо означало лечение орлистатом плюс диета и плацебо плюс диета соответственно.
Во время периода похудения и поддержания веса всем пациентам была рекомендована хорошо сбалансированная низкокалорийная диета, которая должна была привести примерно к 20% снижению потребления калорий и обеспечить поступление 30% калорий из жира. Кроме того, всем пациентам была предложена консультация по питанию.
Результаты одного года исследований. Снижение веса, поддержание веса и факторы риска.
Объединенные данные пяти клинических исследований показали, что общая средняя потеря веса с момента рандомизации до конца 1 года лечения в популяции пациентов с назначенным лечением составила 13,4 фунта (1 фунт=0,45 кг) у пациентов, получавших орлистат, и 5,8 фунта у пациентов, получавших плацебо. После 1 года лечения средняя разница в потере веса между пациентами, получавшими орлистат и плацебо, составила 3%. Завершили 1 год лечения 1072 (69%) пациента, получавших орлистат, и 701 (63%) пациент, получавший плацебо. Из пациентов, которые закончили 1 год лечения, 57% получавших орлистат (120 мг 3 раза в день), и 31% получавших плацебо потеряли не менее 5% от своей исходной массы тела (таблица 1).
Таблица 1.
Доля пациентов со снижением веса ≥5 и ≥10% с момента рандомизации после одного года лечения1.
| Номер исследования | Доля пациентов со снижением веса в популяции с назначенным лечением, % (n)2 | |||||
| Потеря веса ≥5% | Потеря веса ≥10% | |||||
| Орлистат | Плацебо | Значение p | Орлистат | Плацебо | Значение p | |
| 14119B | 35,5 (110) | 21,3 (108) | 0,021 | 16,4 (110) | 6,5 (108) | 0,022 |
| 14119С | 54,8 (343) | 27,4 (340) | <0,001 | 24,8 (343) | 8,2 (340) | <0,001 |
| 14149 | 50,6 (241) | 26,3 (236) | <0,001 | 22,8 (241) | 11,9 (236) | 0,02 |
| 141613 | 37,1 (210) | 16 (212) | <0,001 | 19,5 (210) | 3,8 (212) | <0,001 |
| 14185 | 42,6 (657) | 22,4 (223) | <0,001 | 17,7 (657) | 9,9 (223) | 0,006 |
1 Лечение включало применение орлистата в дозе 120 мг 3 раза в день или плацебо в сочетании с низкокалорийной диетой.
2 Последнее наблюдение перенесено на последующий период.
3 Все другие исследования были проведены в центрах, специализирующихся на лечении ожирения и его осложнений. Исследование 14161 было проведено с участием врачей первичной медицинской помощи.
Относительные изменения значений факторов риска, связанных с ожирением, после 1 года терапии орлистатом и плацебо представлены для популяции в целом и для популяции с аномальными значениями при рандомизации.
Участники исследования в целом.
Изменения метаболических, сердечно-сосудистых и антропометрических факторов риска, связанных с ожирением, на основе объединенных данных пяти клинических исследований, независимо от статуса фактора риска пациента при рандомизации, представлены в таблице 2. Один год терапии орлистатом привел к относительному улучшению значений нескольких факторов риска.
Таблица 2.
Среднее изменение значений факторов риска с момента рандомизации после одного года лечения в популяции в целом1.
| Факторы риска | Орлистат2 | Плацебо2 |
| Метаболические | ||
| Общий Хс | −2% | +5% |
| ЛПНП | −4% | +5% |
| ЛПВП | +9,3% | +12,8% |
| ЛПНП/ЛПВП | −0,37 | −0,2 |
| Триглицериды | +1,34% | +2,9% |
| Уровень глюкозы натощак, ммоль/л | −0,04 | +0,0 |
| Уровень инсулина натощак, пмоль/л | −6,7 | +5,2 |
| Сердечно-сосудистые | ||
| сАД, мм | −1,01 | +0,58 |
| дАД, мм | −1,19 | +0,46 |
| Антропометрические | ||
| Окружность талии, см | −6,45 | −4,04 |
| Окружность бедер, см | −5,31 | −2,96 |
1 Лечение включало применение орлистата в дозе 120 мг 3 раза в день или плацебо в сочетании с низкокалорийной диетой.
2 Популяция с назначенным лечением на 52-й нед, объединенные данные наблюдений в 5 исследованиях.
Участники исследования с аномальными значениями факторов риска при рандомизации.
Изменения параметров, по сравнению с исходными значениями при рандомизации, после 1 года лечения в популяции с аномальным уровнем липидов (ЛПНП ≥130 мг/дл, ЛПНП/ЛПВП ≥3,5, ЛПВП <35 мг/дл) были больше у получавших орлистат по сравнению с получавшими плацебо в отношении Хс-ЛПНП (−7,83 против +1,14%) и ЛПНП/ЛПВП (−0,64 против −0,46). Уровень ЛПВП увеличился в группе плацебо на 20,1%, а в группе орлистата на 18,8%. В популяции с аномальным исходным АД (сАД ≥140 мм ) изменение сАД со времени рандомизации до 1 года лечения было больше в группе получавших орлистат (−10,89 мм ), чем в группе получавших плацебо (−5,07 мм ). У пациентов с дАД ≥90 мм ст при приеме орлистата дАД снизилось на −7,9 мм , в то время как у пациентов, получавших плацебо, - на −5,5 мм Уровень инсулина натощак снижался больше в группе получавших орлистат, чем в группе плацебо (−39 против −16 пмоль/л) со времени рандомизации до 1 года в популяции с аномальными исходными значениями (≥120 пмоль/л). Большее уменьшение окружности талии у получавших орлистат по сравнению с плацебо (−7,29 против −4,53 см) наблюдалось в популяции с аномальными исходными значениями (≥100 см).
Влияние на восстановление веса.
Три исследования были разработаны для оценки эффектов орлистата по сравнению с плацебо в снижении восстановления веса после его предыдущей потери, достигнутой либо только после диеты (одно исследование, 14302), либо до лечения орлистатом (два исследования, 14119C и 14185). Диета, используемая в течение 1 года исследований по восстановлению веса, была диетой для поддержания веса, а не диетой для похудения, и пациенты получали меньше консультаций по питанию, чем пациенты в исследованиях по снижению веса. В исследованиях 14119C и 14185 предыдущая потеря веса пациентов была обусловлена 1 годом лечения орлистатом в сочетании с умеренно гипокалорийной диетой. Исследование 14302 было проведено для оценки влияния 1 года лечения орлистатом на восстановление веса у пациентов, которые потеряли 8% или более массы тела за предыдущие 6 мес только на диете.
В исследовании 14119C восстановление веса у пациентов, получавших плацебо, составило 52% от потерянного ранее в то время у пациентов, получавших орлистат, оно составило 26% (р<0,001). В исследовании 14185 пациенты, получавшие плацебо, восстановили 63% веса, который они ранее потеряли, в то время как пациенты, получавшие орлистат, восстановил 35% веса, который они потеряли (р<0,001). В исследовании 14302 пациенты, получавшие плацебо, восстановили 53% веса, который они ранее потеряли, в то время как пациенты, получавшие орлистат, восстановили 32% веса, который они потеряли (р<0,001).
Результаты двух лет исследований. Долгосрочный контроль веса и факторы риска.
Лечебные эффекты орлистата изучались в течение 2 лет в 4 из 5 клинических исследований по снижению веса по результатам 1 года лечения. В конце 1-го года рацион питания пациентов был пересмотрен и при необходимости изменен. Диета, назначенная на второй год, была разработана для поддержания текущего веса пациента. В 4 крупных многоцентровых 2-летних двойных слепых плацебо-контролируемых исследованиях было показано, что орлистат более эффективен, чем плацебо, в долгосрочном контроле веса.
Объединенные данные 4 клинических исследований показывают, что 74% всех пациентов, получавших орлистат в дозе 120 мг 3 раза в день, и 76% пациентов, получавших плацебо, завершили 2 года одинаковой терапии. Средняя разница в потере веса между группами, получавшими орлистат в дозе 120 мг 3 раза в день, и группами, получавшими плацебо, на 2-м году у пациентов, завершивших 1 год лечения, составила 3%. В тех же иследованиях, которые указаны в таблице 1 (после одного года лечения), доля пациентов, достигших потери веса ≥5 и ≥10% после двух лет лечения, приведена в таблице 3.
Таблица 3.
Доля пациентов со снижением веса ≥5 и ≥10% с момента рандомизации после двух лет лечения1.
| Номер исследования | Доля пациентов со снижением веса в популяции с назначенным лечением, % (n)2 | |||||
| Потеря веса ≥5% | Потеря веса ≥10% | |||||
| Орлистат | Плацебо | Значение p | Орлистат | Плацебо | Значение p | |
| 14119C | 45,1 (133) | 23,6 (123) | <0,001 | 24,8 (133) | 6,5 (123) | <0,001 |
| 14149 | 43,3 (178) | 27,2 (158) | 0,002 | 18 (178) | 9,5 (158) | 0,025 |
| 141613 | 25 (148) | 15 (113) | 0,049 | 16,9 (148) | 3,5 (113) | 0,001 |
| 14185 | 34 (147) | 27,9 (122) | 0,279 | 17,7 (147) | 11,5 (122) | 0,154 |
1 Диета, используемая в течение 2-го года, была разработана для поддержания веса, а не для похудения. Лечение включало прием орлистата в дозе 120 мг 3 раза в день или плацебо в сочетании с диетой.
2 Последнее наблюдение перенесено на последующий период.
3 Все другие исследования были проведены в центрах, специализирующихся на лечении ожирения и его осложнений. Исследование 14161 было проведено с участием врачей первичной медицинской помощи.
Относительные изменения значений факторов риска, связанных с ожирением, после 2 лет терапии также оценивались в популяции в целом и популяции с повышенными факторами риска при рандомизации.
Участники исследования в целом.
Относительные различия в значениях факторов риска между группами, получавшими орлистат и плацебо, были аналогичны результатам после 1 года терапии по таким показателям, как общий Хс, Хс-ЛПНП, соотношение ЛПНП/ЛПВП, триглицериды, уровень глюкозы натощак, уровень инсулина натощак, дАД, окружность талии и окружность бедер. Относительные различия между группами лечения по уровню ЛПВП и значению сАД были меньше, чем наблюдалось по результатам первого года лечения.
Участники исследования с аномальными значениями факторов риска при рандомизации.
Относительные различия в значениях факторов риска между группами, получавшими орлистат и плацебо, были аналогичны результатам после 1 года терапии для ЛПНП и ЛПВП, уровня триглицеридов, инсулина натощак, дАД и окружности талии. Относительные различия между группами лечения по соотношению ЛПНП/ЛПВП и изолированному сАД были меньше, чем наблюдалось по результатам первого года лечения.
Результаты четырех лет исследований. Долгосрочный контроль веса и факторы риска.
В 4-летнем двойном слепом плацебо-контролируемом исследовании XENDOS влияние орлистата на задержку начала развития диабета типа 2 и на массу тела сравнивалось с плацебо у 3304 пациентов с ожирением, у которых исходно была нормальная или нарушенная толерантность к глюкозе. 34% из 1655 пациентов, которые были рандомизированы в группу плацебо, и 52% из 1649 пациентов, которые были рандомизированы в группу орлистата, завершили 4-летнее исследование.
В конце исследования средняя потеря веса в группе плацебо составила −2,75% по сравнению с −5,17% в группе орлистата (р<0,001). 45% пациентов, получавших плацебо, и 73% пациентов, получавших орлистат, потеряли ≥5% от исходной массы тела, а 21% пациентов, получавших плацебо, и 41% пациентов, получавших орлистат, потеряли ≥10% от исходной массы тела после первого года лечения. После 4 лет лечения 28% пациентов, получавших плацебо, и 45% пациентов, получавших орлистат, потеряли ≥5% от исходной массы тела, а 10% пациентов, получавших плацебо, и 21% пациентов, получавших орлистат, потеряли ≥10% от исходной массы тела. После 4 лет лечения средняя разница в потере веса между пациентами, получавшими орлистат и плацебо, составила 2,5%.
Относительные изменения в значениях факторов риска, ассоциированных с ожирением, после 4 лет терапии, оцененные в исследовании XENDOS, представлены в таблице 4.
Таблица 4.
Среднее изменение значений факторов риска с момента рандомизации после 4 лет лечения1.
| Факторы риска | Орлистат2 | Плацебо2 |
| Метаболические | ||
| Общий Хс | −7,02% | −2,03% |
| ЛПНП | −11,66% | −3,85% |
| ЛПВП | +5,92% | +7,01% |
| ЛПНП/ЛПВП | −0,53 | −0,33 |
| Триглицериды | +3,64% | +1,3% |
| Уровень гюкозы натощак, ммоль/л | +0,12 | +0,23 |
| Уровень инсулина натощак, пмоль/л | −24,93 | −15,71 |
| Сердечно-сосудистые | ||
| сАД, мм | −4,12 | −2,6 |
| дАД, мм | −1,93 | −0,87 |
| Антропометрические | ||
| Окружность талии, см | −5,78 | −3,99 |
1 Лечение включало назначение орлистата в дозе 120 мг 3 раза в день или плацебо в сочетании с диетой.
2 Популяция с назначенным лечением.
Начало диабета типа 2 у пациентов с ожирением.
В исследовании XENDOS в общей популяции орлистат отсрочил начало диабета типа 2 и в конце 4 лет лечения совокупный показатель заболеваемости диабетом составил 8,3% в группе плацебо по сравнению с 5,5% в группе орлистата (р=0,01). Этот вывод был обусловлен статистически значимым снижением частоты развития диабета типа 2 у пациентов с исходно нарушенной толерантностью к глюкозе. Орлистат не снижал риск развития сахарного диабета у пациентов с нормальной толерантностью к глюкозе на исходном уровне.
Влияние орлистата на задержку начала диабета типа 2 у пациентов с ожирением и нарушенной толерантностью к глюкозе, по-видимому, обусловлен потерей веса, а не каким-либо независимым воздействием орлистата на метаболизм глюкозы или инсулина. Влияние орлистата на снижение веса является дополнением к диете и физическим упражнениям.
Исследование с участием пациентов с сахарным диабетом типа 2.
Было проведено 1-летнее двойное слепое плацебо-контролируемое исследование с участием пациентов с сахарным диабетом типа 2 (n=321), состояние которых было стабилизировано применением ЛС на основе производных сульфонилмочевины. У 30% пациентов, получавших орлистат, снижение массы тела составило как минимум 5% или более после рандомизации по сравнению с 13% пациентов, получавших плацебо (р<0,001). Средние изменения отдельных показателей у таких пациентов приведены в таблице 5.
Таблица 5.
Средние изменения массы тела и показателей гликемического контроля в сравнении с периодом рандомизации после одного года лечения у пациентов с сахарным диабетом типа 2.
| Показатель | Орлистат1 (n=162) | Плацебо1 (n=159) | Значение p |
| Доля пациентов, прекративших пероральный прием производных сульфонилмочевины, % | 11,7 | 7,5 | ≤0,05 |
| Доля пациентов, уменьшивших дозу перорального производного сульфонилмочевины, % | 31,5 | 21,4 | ≤0,05 |
| Среднее снижение дозы производного сульфонилмочевины, % | −22,8 | −9,1 | ≤0,05 |
| Изменение массы тела, фунт | −8,9 | −4,2 | ≤0,05 |
| Уровень HbA1c, % | −0,18 | +0,28 | ≤0,05 |
| Уровень глюкозы натощак, ммоль/л | −0,02 | +0,54 | ≤0,05 |
| Уровень инсулина натощак, пмоль/л | −19,68 | −18,02 | >0,05 |
1 Лечение включало применение орлистата в дозе 120 мг 3 раза в день или плацебо в сочетании с диетой.
Кроме того, применение орлистата (n=162) по сравнению с плацебо (n=159) было связано со значительным снижением уровня общего Хс (−1 против +9%, р≤0,05), ЛПНП (−3 против +10%, р<0,05), соотношения ЛПНП/ЛПВП (−0,26 против −0,02, р≤0,05) и триглицеридов (+2,54 против +16,2%, р<0,05) соответственно. Уровень Хс-ЛПВП увеливался на 6,49% при применении орлистата и на 8,6% при применении плацебо, р>0,05. сАД увеличилось на 0,61 мм у получавших орлистат и на 4,33 мм - плацебо, р>0,05. дАД снижалось на 0,47 мм у получавших орлистат и на 0,5 мм - плацебо, р>0,05.
Толерантность к глюкозе у пациентов с ожирением.
Двухлетние исследования, включавшие пероральные тесты на толерантность к глюкозе (ПТТГ), проводились с участием пациентов с ожирением, у которых ранее не диагностировался или не лечился диабет типа 2 и чей базовый статус ПТТГ при рандомизации был либо нормальным, либо нарушенным, либо диабетическим.
Сравнивали прогрессирование от нормальных результатов ПТТГ при рандомизации до значений, соответствующих нарушению или диабету после 2 лет лечения орлистатом (n=251) или плацебо (n=207). После лечения орлистатом 0 и 7,2% пациентов прогрессировали от нормального к диабетическому и от нормального к нарушенному статусу соответственно, по сравнению с 1,9 и 12,6% в группе лечения плацебо соответственно.
У части пациентов с нарушенным статусом ПТТГ состояние улучшилось до нормального или ухудшилось до диабетического после 1 и 2 лет лечения орлистатом по сравнению с плацебо. После 1 года лечения 45,8% пациентов, получавших плацебо, и 73% пациентов, получавших орлистат, имели нормальные результаты ПТТГ, в то время как 10,4% пациентов, получавших плацебо, и 2,6% пациентов, получавших орлистат, заболели диабетом. После 2 лет лечения у 50% пациентов, получавших плацебо, и у 71,7% пациентов, получавших орлистат, был нормальный статус ПТТГ, в то время как у 7,5% пациентов, получавших плацебо, и у 1,7% пациентов, получавших орлистат, был обнаружен диабет после лечения.
Педиатрические клинические исследования.
Влияние орлистата на ИМТ и потерю веса оценивали в 54-недельном многоцентровом двойном слепом плацебо-контролируемом исследовании с участием 539 подростков от 12 до 16 лет с ожирением (357 получали орлистат в дозе 120 мг 3 раза в день и 182 получали плацебо). У всех участников исследования исходный ИМТ был на 2 единицы больше, чем средневзвешенное значение по США с учетом возраста и пола. ИМТ был основным параметром оценки эффективности, поскольку он учитывает изменения роста и массы тела, которые происходят у растущих детей. В ходе исследования всем пациентам было предписано принимать поливитамины, содержащие жирорастворимые витамины, по крайней мере за 2 ч до или после приема орлистата. Пациенты также придерживались сбалансированной, низкокалорийной диеты, которая должна была обеспечивать поступление 30% калорий из жира. Кроме того, все пациенты были включены в программу модификации поведения и получили консультации по физическим упражнениям.
Примерно 65 % пациентов в каждой группе лечения завершили исследование.
После одного года лечения ИМТ снизился в среднем на 0,55 кг/м2 у пациентов, получавших орлистат, и увеличился в среднем на 0,31 кг/м2 у пациентов, получавших плацебо (р=0,001).
Таблица 6.
Доля пациентов со снижением ИМТ и массы тела ≥5 и ≥10% с момента рандомизации после одного года лечения1.
| Показатель | Доля пациентов со снижением веса в популяции с назначенным лечением, % (n)2 | |||
| Снижение ≥5% | Снижение ≥10% | |||
| Орлистат | Плацебо | Орлистат | Плацебо | |
| ИМТ | 25,6 (347) | 15,7 (178) | 13,3 (347) | 4,5 (178) |
| Масса тела | 19 (348) | 11,7 (180) | 9,5 (348) | 3,3 (180) |
1 Лечение включало применение орлистата в дозе 120 мг 3 раза в день или плацебо в сочетании с диетой.
2 Последнее наблюдение перенесено на последующий период.
|
|
Показания к применению
Лечение ожирения, включая потерю веса и поддержание веса при использовании в сочетании с низкокалорийной диетой; снижение риска восстановления веса после его предыдущей потери. Орлистат показан пациентам с ожирением с начальным ИМТ ≈30 кг/м2 или ≈27 кг/м2 при наличии других факторов риска (например, гипертония, диабет, дислипидемия).
Противопоказания
Известная гиперчувствительность к орлистату; синдром хронической мальабсорбции; холестаз; беременность.
При беременности и кормлении грудью
Категория действия на плод по FDA. X.
Орлистат противопоказан во время беременности, поскольку потеря веса не приносит потенциальной пользы беременной женщине и может нанести вред плоду. В настоящее время всем беременным женщинам, включая тех, кто уже имеет избыточный вес или страдает ожирением, рекомендуется минимальное увеличение веса и отсутствие потери веса из-за обязательного увеличения веса, которое происходит в тканях матери во время беременности.
Эмбриотоксичности или тератогенности у животных, получавших орлистат в дозах, значительно превышающих МРДЧ, не наблюдалось. Исследования репродукции проводились на крысах и кроликах в дозах до 800 мг/кг/сут, что в 23 и 47 раз превышает суточную дозу для человека в расчете на площадь поверхности тела.
Если орлистат используется во время беременности или если пациентка забеременеет во время приема орлистата, она должна быть проинформирована о потенциальной опасности потери веса матерью для плода.
Неизвестно, присутствует ли орлистат в женском молоке. Следует соблюдать осторожность при назначении орлистата кормящей женщине.
Орлистат противопоказан во время беременности, поскольку потеря веса не приносит потенциальной пользы беременной женщине и может нанести вред плоду. В настоящее время всем беременным женщинам, включая тех, кто уже имеет избыточный вес или страдает ожирением, рекомендуется минимальное увеличение веса и отсутствие потери веса из-за обязательного увеличения веса, которое происходит в тканях матери во время беременности.
Эмбриотоксичности или тератогенности у животных, получавших орлистат в дозах, значительно превышающих МРДЧ, не наблюдалось. Исследования репродукции проводились на крысах и кроликах в дозах до 800 мг/кг/сут, что в 23 и 47 раз превышает суточную дозу для человека в расчете на площадь поверхности тела.
Если орлистат используется во время беременности или если пациентка забеременеет во время приема орлистата, она должна быть проинформирована о потенциальной опасности потери веса матерью для плода.
Неизвестно, присутствует ли орлистат в женском молоке. Следует соблюдать осторожность при назначении орлистата кормящей женщине.
Побочные эффекты
Результаты клинических исследований.
Поскольку клинические исследования проводятся в различных условиях. частота побочных реакций. наблюдаемых в одном клиническом исследовании ЛС. не может быть напрямую сопоставлена с данными другого клинического исследования и может не отражать частоту побочных реакций. наблюдаемых у пациентов.
Часто наблюдавшиеся побочные реакции (на основе данных за первый и второй годы).
Желудочно-кишечные симптомы были наиболее часто наблюдавшимися побочными реакциями при применении орлистата в семи двойных слепых плацебо-контролируемых клинических исследованиях. и в первую очередь являлись проявлением механизма действия (часто наблюдавшиеся определены как отмечавшиеся с частотой ≥5% при приеме орлистата в дозе 120 мг и как минимум в 2 раза чаще. чем в группе плацебо).
Таблица 7.
Часто наблюдавшиеся побочные реакции (доля пациентов, %).
1 Маслянистые выделения могут быть прозрачными или иметь окраску, например оранжевую или коричневую.
В целом первый случай развития этих событий происходил в течение 3 мес после начала терапии. Всего примерно 50% эпизодов побочных реакций со стороны ЖКТ, связанных с применением орлистата, длились менее 1 нед, а большинство - не более 4 нед. Однако побочные эффекты со стороны ЖКТ могут возникать у некоторых людей в течение 6 мес или дольше.
Прекращение лечения.
В контролируемых клинических исследованиях 8,8% пациентов, получавших орлистат, прекратили лечение из-за побочных реакций по сравнению с 5% пациентов, получавших плацебо. Для орлистата наиболее распространенными побочными реакциями, приведшими к прекращению лечения, были реакции со стороны ЖКТ.
Другие побочные реакции.
В таблице 8 перечислены другие побочные явления. связанные с лечением. отмечавшиеся в семи многоцентровых двойных слепых плацебо-контролируемых клинических исследованиях с частотой ≥2% у пациентов. получавших орлистат в дозе 120 мг 3 раза в день. и чаще чем при применении плацебо. в течение 1 и 2 лет. независимо от их связи с применением изучаемого ЛС.
Таблица 8.
Другие побочные реакции, связанные с лечением, возникавшие в семи плацебо-контролируемых клинических исследованиях (доля пациентов, %).
1 Нет случаев с частотой ≥2% и чаще чем при применении плацебо.
В 4-летнем исследовании XENDOS общий профиль побочных реакций был аналогичным наблюдавшемуся в 1- и 2-летних исследованиях. при этом общая частота побочных реакций со стороны ЖКТ. отмечавшаяся в 1-й год. ежегодно снижалась в течение 4-летнего периода.
В клинических исследованиях с участием пациентов с сахарным диабетом и ожирением также наблюдались гипогликемия и вздутие живота.
Педиатрические пациенты.
В клинических исследованиях орлистата у пациентов-подростков от 12 до 16 лет профиль побочных реакций в целом был аналогичен тому, что наблюдался у взрослых.
Результаты пострегистрационных наблюдений.
Во время применения орлистата после его регистрации были выявлены следующие побочные реакции. Поскольку данные об этих реакциях поступают в добровольном порядке от популяции неопределенного размера. не всегда возможно достоверно оценить их частоту или установить причинно-следственную связь с воздействием орлистата.
Сообщалось о редких случаях повышения уровня трансаминаз и ЩФ, а также возникновения гепатита, которые могут иметь серьезные последствия. Поступали сообщения о печеночной недостаточности. наблюдаемой при применении орлистата в ходе пострегистрационного наблюдения. причем некоторые из этих случаев приводили к необходимости пересадки печени или смерти.
Сообщалось о случаях снижения концентрации циклоспорина при одновременном применении циклоспорина с орлистатом.
Сообщалось о редких случаях гиперчувствительности при применении орлистата. Признаки и симптомы включали зуд, сыпь, крапивницу, ангионевротический отек, бронхоспазм и анафилаксию. Сообщалось об очень редких случаях буллезного высыпания.
Сообщалось о снижении уровня протромбина. повышении МНО и несбалансированном лечении антикоагулянтами. приводящем к изменению параметров гемостаза у пациентов. получавших одновременно орлистат и антикоагулянтную терапию.
Сообщалось о случаях развития гипотиреоза у пациентов, получавших одновременно орлистат и левотироксин.
Сообщалось об острой оксалатной нефропатии после лечения орлистатом у пациентов с заболеваниями почек или с риском их развития.
Сообщалось о развитии панкреатита при применении орлистата в пострегистрационном наблюдении. Причинно-следственная связь или физиопатологический механизм между панкреатитом и терапией ожирения окончательно не установлены.
Сообщалось о случаях развития желудочно-кишечных кровотечений у пациентов, получавших орлистат. Большинство этих случаев были нетяжелыми, серьезные или продолжительные побочные эффекты следует исследовать дополнительно.
Поскольку клинические исследования проводятся в различных условиях. частота побочных реакций. наблюдаемых в одном клиническом исследовании ЛС. не может быть напрямую сопоставлена с данными другого клинического исследования и может не отражать частоту побочных реакций. наблюдаемых у пациентов.
Часто наблюдавшиеся побочные реакции (на основе данных за первый и второй годы).
Желудочно-кишечные симптомы были наиболее часто наблюдавшимися побочными реакциями при применении орлистата в семи двойных слепых плацебо-контролируемых клинических исследованиях. и в первую очередь являлись проявлением механизма действия (часто наблюдавшиеся определены как отмечавшиеся с частотой ≥5% при приеме орлистата в дозе 120 мг и как минимум в 2 раза чаще. чем в группе плацебо).
Таблица 7.
Часто наблюдавшиеся побочные реакции (доля пациентов, %).
| Побочные эффекты | Первый год | Второй год | ||
| Орлистат (n=1913) | Плацебо (n=1466) | Орлистат (n=613) | Плацебо (n=524) | |
| Жиросодержащие выделения 1 | 26,6 | 1,3 | 4,4 | 0,2 |
| Метеоризм | 23,9 | 1,4 | 2,1 | 0,2 |
| Императивные позывы на испражнение | 22,1 | 6,7 | 2,8 | 1,7 |
| Жирный/маслянистый стул1 | 20 | 2,9 | 5,5 | 0,6 |
| Маслянистое опорожнение кишечника1 | 11,9 | 0,8 | 2,3 | 0,2 |
| Учащенная дефекация | 10,8 | 4,1 | 2,6 | 0,8 |
| Недержание кала | 7,7 | 0,9 | 1,8 | 0,2 |
1 Маслянистые выделения могут быть прозрачными или иметь окраску, например оранжевую или коричневую.
В целом первый случай развития этих событий происходил в течение 3 мес после начала терапии. Всего примерно 50% эпизодов побочных реакций со стороны ЖКТ, связанных с применением орлистата, длились менее 1 нед, а большинство - не более 4 нед. Однако побочные эффекты со стороны ЖКТ могут возникать у некоторых людей в течение 6 мес или дольше.
Прекращение лечения.
В контролируемых клинических исследованиях 8,8% пациентов, получавших орлистат, прекратили лечение из-за побочных реакций по сравнению с 5% пациентов, получавших плацебо. Для орлистата наиболее распространенными побочными реакциями, приведшими к прекращению лечения, были реакции со стороны ЖКТ.
Другие побочные реакции.
В таблице 8 перечислены другие побочные явления. связанные с лечением. отмечавшиеся в семи многоцентровых двойных слепых плацебо-контролируемых клинических исследованиях с частотой ≥2% у пациентов. получавших орлистат в дозе 120 мг 3 раза в день. и чаще чем при применении плацебо. в течение 1 и 2 лет. независимо от их связи с применением изучаемого ЛС.
Таблица 8.
Другие побочные реакции, связанные с лечением, возникавшие в семи плацебо-контролируемых клинических исследованиях (доля пациентов, %).
| Система организма/побочная реакция | Первый год | Второй год | ||
| Орлистат (n=1913) | Плацебо (n=1466) | Орлистат (n=613) | Плацебо (n=524) | |
| Со стороны ЖКТ | ||||
| Боль в животе/дискомфорт | 25,5 | 21,4 | −1 | − |
| Тошнота | 8,1 | 7,3 | 3,6 | 2,7 |
| Инфекционная диарея | 5,3 | 4,4 | − | − |
| Ректальная боль/дискомфорт | 5,2 | 4 | 3,3 | 1,9 |
| Патология зубов | 4,3 | 3,1 | 2,9 | 2,3 |
| Патология десен | 4,1 | 2,9 | 2 | 1,5 |
| Рвота | 3,8 | 3,5 | − | − |
| Со стороны органов дыхания | ||||
| Грипп | 39,7 | 36,2 | − | − |
| Инфекции верхних дыхательных путей | 38,1 | 32,8 | 26,1 | 25,8 |
| Инфекции нижних дыхательных путей | 7,8 | 6,6 | − | − |
| ЛОР-симптомы | 2 | 1,6 | − | − |
| Со стороны скелетно-мышечной системы | ||||
| Боль в спине | 13,9 | 12,1 | − | − |
| Боль в нижних конечностях | − | − | 10,8 | 10,3 |
| Артрит | 5,4 | 4,8 | − | − |
| Миалгия | 4,2 | 3,3 | − | − |
| Патология суставов | 2,3 | 2,2 | − | − |
| Тендинит | − | − | 2 | 1,9 |
| Со стороны ЦНС | ||||
| Головная боль | 30,6 | 27,6 | − | − |
| Головокружение | 5,2 | 5 | - | - |
| Со стороны организма в целом | ||||
| Повышенная утомляемость | 7,2 | 6,4 | 3,1 | 1,7 |
| Расстройство сна | 3,9 | 3,3 | − | − |
| Со стороны кожи и подкожных тканей | ||||
| Сыпь | 4,3 | 4 | − | − |
| Сухость кожи | 2,1 | 1,4 | − | − |
| Со стороны женской репродуктивной системы | ||||
| Нарушение менструального цикла | 9,8 | 7,5 | − | − |
| Вагинит | 3,8 | 3,6 | 2,6 | 1,9 |
| Со стороны мочевыводящей системы | ||||
| Инфекция мочевых путей | 7,5 | 7,3 | 5,9 | 4,8 |
| Нарушения психики | ||||
| Тревожность | 4,7 | 2,9 | 2,8 | 2,1 |
| Депрессия | − | − | 3,4 | 2,5 |
| Нарушения слуха и вестибулярного аппарата | ||||
| Отит | 4,3 | 3,4 | 2,9 | 2,5 |
| Со стороны ССС | ||||
| Отеки нижних конечностей | − | − | 2,8 | 1,9 |
1 Нет случаев с частотой ≥2% и чаще чем при применении плацебо.
В 4-летнем исследовании XENDOS общий профиль побочных реакций был аналогичным наблюдавшемуся в 1- и 2-летних исследованиях. при этом общая частота побочных реакций со стороны ЖКТ. отмечавшаяся в 1-й год. ежегодно снижалась в течение 4-летнего периода.
В клинических исследованиях с участием пациентов с сахарным диабетом и ожирением также наблюдались гипогликемия и вздутие живота.
Педиатрические пациенты.
В клинических исследованиях орлистата у пациентов-подростков от 12 до 16 лет профиль побочных реакций в целом был аналогичен тому, что наблюдался у взрослых.
Результаты пострегистрационных наблюдений.
Во время применения орлистата после его регистрации были выявлены следующие побочные реакции. Поскольку данные об этих реакциях поступают в добровольном порядке от популяции неопределенного размера. не всегда возможно достоверно оценить их частоту или установить причинно-следственную связь с воздействием орлистата.
Сообщалось о редких случаях повышения уровня трансаминаз и ЩФ, а также возникновения гепатита, которые могут иметь серьезные последствия. Поступали сообщения о печеночной недостаточности. наблюдаемой при применении орлистата в ходе пострегистрационного наблюдения. причем некоторые из этих случаев приводили к необходимости пересадки печени или смерти.
Сообщалось о случаях снижения концентрации циклоспорина при одновременном применении циклоспорина с орлистатом.
Сообщалось о редких случаях гиперчувствительности при применении орлистата. Признаки и симптомы включали зуд, сыпь, крапивницу, ангионевротический отек, бронхоспазм и анафилаксию. Сообщалось об очень редких случаях буллезного высыпания.
Сообщалось о снижении уровня протромбина. повышении МНО и несбалансированном лечении антикоагулянтами. приводящем к изменению параметров гемостаза у пациентов. получавших одновременно орлистат и антикоагулянтную терапию.
Сообщалось о случаях развития гипотиреоза у пациентов, получавших одновременно орлистат и левотироксин.
Сообщалось об острой оксалатной нефропатии после лечения орлистатом у пациентов с заболеваниями почек или с риском их развития.
Сообщалось о развитии панкреатита при применении орлистата в пострегистрационном наблюдении. Причинно-следственная связь или физиопатологический механизм между панкреатитом и терапией ожирения окончательно не установлены.
Сообщалось о случаях развития желудочно-кишечных кровотечений у пациентов, получавших орлистат. Большинство этих случаев были нетяжелыми, серьезные или продолжительные побочные эффекты следует исследовать дополнительно.
|
|
Взаимодействие
Циклоспорин. Данные исследования лекарственного взаимодействия орлистата и циклоспорина указывают на снижение уровня циклоспорина в плазме крови при одновременном применении орлистата и циклоспорина. Орлистат и циклоспорин не следует назначать одновременно. Циклоспорин следует вводить через 3 ч после приема орлистата.
Жирорастворимые витаминные добавки и их аналоги. Клинические исследования ФКВ показали, что абсорбция бета-каротиновой добавки снижается при одновременном применении с орлистатом. Орлистат ингибировал всасывание ацетата витамина Е. Влияние орлистата на всасывание дополнительного витамина D, витамина А и витамина получаемых из пищевых продуктов, в настоящее время неизвестно.
Левотироксин. Сообщалось о случаях развития гипотиреоза у пациентов, получавших одновременно орлистат и левотироксин. Пациенты, получающие одновременно орлистат и левотироксин, должны находиться под наблюдением на предмет изменений функции щитовидной железы. Необходимо назначать левотироксин и орлистат с интервалом не менее 4.
Варфарин. Всасывание витамина К может быть снижено при применении орлистата. Пациентов, получающих постоянные стабильные дозы варфарина, которым назначают орлистат, необходимо тщательно контролировать на предмет изменений параметров свертывания крови.
Жирорастворимые витаминные добавки и их аналоги. Клинические исследования ФКВ показали, что абсорбция бета-каротиновой добавки снижается при одновременном применении с орлистатом. Орлистат ингибировал всасывание ацетата витамина Е. Влияние орлистата на всасывание дополнительного витамина D, витамина А и витамина получаемых из пищевых продуктов, в настоящее время неизвестно.
Левотироксин. Сообщалось о случаях развития гипотиреоза у пациентов, получавших одновременно орлистат и левотироксин. Пациенты, получающие одновременно орлистат и левотироксин, должны находиться под наблюдением на предмет изменений функции щитовидной железы. Необходимо назначать левотироксин и орлистат с интервалом не менее 4.
Варфарин. Всасывание витамина К может быть снижено при применении орлистата. Пациентов, получающих постоянные стабильные дозы варфарина, которым назначают орлистат, необходимо тщательно контролировать на предмет изменений параметров свертывания крови.
Передозировка
Однократные дозы орлистата по 800 мг и многократные дозы до 400 мг 3 раза в день в течение 15 дней у пациентов с нормальным весом и ожирением не привели к развитию существенных побочных эффектов. В случае значительной передозировки орлистата рекомендуется наблюдать за состоянием пациента в течение 24 Основываясь на исследованиях, проведенных у людей и животных, системные эффекты, обусловленные ингибирующими липазу свойствами орлистата, должны быть быстро обратимыми.
Способ применения и дозы
Перорально, 3 раза в день с основным приемом пищи, содержащей жир, во время еды или не позднее 1 ч после приема пищи, при соблюдении сбалансированной по питательным веществам низкокалорийной диеты, которая содержит примерно 30% калорий в виде жира. Ежедневное потребление жиров, углеводов и белков должно быть распределено на три основных приема пищи. Если прием пищи иногда пропускается или не содержит жира, дозу орлистата можно пропустить.
Меры предосторожности применения
Сопутствующее применение ЛС и витаминов.
Данные исследования лекарственного взаимодействия орлистата и циклоспорина указывают на снижение уровня циклоспорина в плазме крови при одновременном применении орлистата и циклоспорина. Поэтому орлистат и циклоспорин не следует назначать одновременно. Чтобы уменьшить вероятность лекарственного взаимодействия, циклоспорин следует принимать не менее чем за 3 ч до или после орлистата у пациентов, принимающих эти ЛС одновременно. Кроме того, у тех пациентов, у которых измеряются уровни циклоспорина, следует рассмотреть возможность более частого мониторинга их состояния.
Пациентам следует настоятельно рекомендовать принимать поливитаминную добавку, содержащую жирорастворимые витамины, для обеспечения адекватного питания, поскольку было показано, что орлистат снижает всасывание некоторых жирорастворимых витаминов и бета-каротина. Кроме того, уровни витамина D и бета-каротина могут быть низкими у пациентов с ожирением по сравнению с лицами, не страдающими ожирением. Добавку следует принимать 1 раз в день не менее чем за 2 ч до или после приема орлистата, например перед сном.
Таблица 9.
Частота случаев (%) низкого содержания витаминов при двух или более последовательных посещениях (взрослые пациенты без поддержки с нормальными исходными значениями; первый и второй год).
1 Лечение включало применение плацебо или орлистата в сочетании с диетой.
Таблица 10.
Частота случаев (%) низкого содержания витаминов при двух или более последовательных посещениях (педиатрические пациенты с нормальными исходными значениями, все пациенты получали витаминные добавки на протяжении всего исследования).
1 Лечение включало применение плацебо или орлистата в сочетании с диетой.
Повреждение печени.
Были зарегистрированы редкие пострегистрационные сообщения о тяжелом повреждении печени с развитием гепатоцеллюлярного некроза или острой печеночной недостаточности у пациентов, получавших орлистат, причем некоторые из этих случаев приводили к необходимости пересадки печени или смерти. Пациенты должны быть проинформированы о том, что необходимо сообщать о любых симптомах нарушения функции печени (анорексия, зуд, желтуха, темная моча, светлый стул или боль в правом подреберье) во время приема орлистата. При появлении этих симптомов следует немедленно прекратить прием орлистата и других вызывающих подозрение ЛС, а также провести функциональные тесты печени и определить уровни АЛТ и АСТ.
Увеличение содержания оксалата в моче.
У некоторых пациентов может повышаться уровень оксалата в моче после лечения орлистатом. Сообщалось о случаях оксалатного нефролитиаза и оксалатной нефропатии с почечной недостаточностью. Необходимо контролировать функцию почек при назначении орлистата пациентам с риском нарушения функции почек и с осторожностью применять его у пациентов с гипероксалурией в анамнезе или оксалатным нефролитиазом кальция.
Желчнокаменная болезнь.
Значительная потеря веса может увеличить риск развития желчнокаменной болезни. В клиническом исследовании орлистата для профилактики диабета типа 2 частота желчнокаменной болезни как нежелательного явления составила 2,9% (47 из 1649) у пациентов, рандомизированных в группу с применением орлистата, и 1,8% (30 из 1655) - в группу плацебо.
Разное.
Органические причины ожирения (например, гипотиреоз) следует исключить перед назначением орлистата. Пациентам следует рекомендовать придерживаться диетических рекомендаций. Желудочно-кишечные осложнения могут усиливаться при приеме орлистата с диетой с высоким содержанием жира (>30% от общего количества ежедневных калорий, поступающих из жира). Ежедневное потребление жира должно быть распределено на три основных приема пищи. Если орлистат принимать с одним любым приемом пищи с очень высоким содержанием жира, вероятность возникновения побочных эффектов со стороны ЖКТ возрастает.
Злоупотребление и зависимость.
Как и в случае с любым средством для похудения, существует вероятность злоупотребления орлистатом в некоторых особых группах пациентов (например, у пациентов с нервной анорексией или булимией).
Особые группы пациентов.
Педиатрические пациенты. Безопасность и эффективность применения орлистата у детей до 12 лет не установлены.
Безопасность и эффективность орлистата были оценены у подростков от 12 до 16 лет с ожирением. Применение орлистата в этой возрастной группе подтверждается данными адекватных и хорошо контролируемых исследований орлистата у взрослых с дополнительными данными 54-недельного исследования эффективности и безопасности и 21-дневного исследования минерального баланса у подростков от 12 до 16 лет с ожирением. Пациенты, получавшие орлистат в 54-недельном исследовании эффективности и безопасности (64,8% женского пола, 75% представители европеоидной расы, 18,8% афроамериканцы и 6,3% других этнических групп), имели среднее снижение ИМТ на 0,55 кг/м2 по сравнению со средним увеличением на 0,31 кг/м2 у пациентов, получавших плацебо (р=0,001). В обоих подростковых исследованиях побочные эффекты были в целом аналогичны тем, которые описаны у взрослых, и включали жирный/маслянистый стул, маслянистые выделения и маслянистую эвакуацию. В подгруппе из 152 пациентов, получавших орлистат, и 77 пациентов, получавших плацебо, из 54-недельного исследования изменения в составе тела, измеренные с помощью DEXA, были одинаковыми в обеих группах лечения, за исключением массы жира, которая была значительно снижена у пациентов, получавших орлистат, по сравнению с пациентами, получавшими плацебо (−2,5 кг против −0,6 кг, р=0,033). Поскольку орлистат может препятствовать усвоению жирорастворимых витаминов, всем пациентам следует ежедневно принимать поливитамины, содержащие витамины А, D, Е, К и бета-каротин. Витамины следует принимать по крайней мере за 2 ч до или после приема орлистата.
Концентрация орлистата и его метаболитов M1 и M3 в плазме крови была аналогична таковой у взрослых при том же уровне дозы. Суточное выделение жира с калом составляло 27 и 7% от потребляемого жира с пищей в группах лечения орлистатом и плацебо соответственно.
Пожилой возраст. Клинические исследования орлистата не включали достаточное количество пациентов в возрасте 65 лет и старше, чтобы определить, отличаются ли они по реакции от более молодых пациентов.
Данные исследования лекарственного взаимодействия орлистата и циклоспорина указывают на снижение уровня циклоспорина в плазме крови при одновременном применении орлистата и циклоспорина. Поэтому орлистат и циклоспорин не следует назначать одновременно. Чтобы уменьшить вероятность лекарственного взаимодействия, циклоспорин следует принимать не менее чем за 3 ч до или после орлистата у пациентов, принимающих эти ЛС одновременно. Кроме того, у тех пациентов, у которых измеряются уровни циклоспорина, следует рассмотреть возможность более частого мониторинга их состояния.
Пациентам следует настоятельно рекомендовать принимать поливитаминную добавку, содержащую жирорастворимые витамины, для обеспечения адекватного питания, поскольку было показано, что орлистат снижает всасывание некоторых жирорастворимых витаминов и бета-каротина. Кроме того, уровни витамина D и бета-каротина могут быть низкими у пациентов с ожирением по сравнению с лицами, не страдающими ожирением. Добавку следует принимать 1 раз в день не менее чем за 2 ч до или после приема орлистата, например перед сном.
Таблица 9.
Частота случаев (%) низкого содержания витаминов при двух или более последовательных посещениях (взрослые пациенты без поддержки с нормальными исходными значениями; первый и второй год).
| Витамин | Плацебо1 | Орлистат1 |
| Витамин А | 1 | 2,2 |
| Витамин D | 6,6 | 12 |
| Витамин E | 1 | 5,8 |
| Бета-каротин | 1,7 | 6,1 |
1 Лечение включало применение плацебо или орлистата в сочетании с диетой.
Таблица 10.
Частота случаев (%) низкого содержания витаминов при двух или более последовательных посещениях (педиатрические пациенты с нормальными исходными значениями, все пациенты получали витаминные добавки на протяжении всего исследования).
| Витамин | Плацебо1 | Орлистат1 |
| Витамин А | 0 | 0 |
| Витамин D | 0,7 | 1,4 |
| Витамин E | 0 | 0 |
| Бета-каротин | 0,8 | 1,5 |
1 Лечение включало применение плацебо или орлистата в сочетании с диетой.
Повреждение печени.
Были зарегистрированы редкие пострегистрационные сообщения о тяжелом повреждении печени с развитием гепатоцеллюлярного некроза или острой печеночной недостаточности у пациентов, получавших орлистат, причем некоторые из этих случаев приводили к необходимости пересадки печени или смерти. Пациенты должны быть проинформированы о том, что необходимо сообщать о любых симптомах нарушения функции печени (анорексия, зуд, желтуха, темная моча, светлый стул или боль в правом подреберье) во время приема орлистата. При появлении этих симптомов следует немедленно прекратить прием орлистата и других вызывающих подозрение ЛС, а также провести функциональные тесты печени и определить уровни АЛТ и АСТ.
Увеличение содержания оксалата в моче.
У некоторых пациентов может повышаться уровень оксалата в моче после лечения орлистатом. Сообщалось о случаях оксалатного нефролитиаза и оксалатной нефропатии с почечной недостаточностью. Необходимо контролировать функцию почек при назначении орлистата пациентам с риском нарушения функции почек и с осторожностью применять его у пациентов с гипероксалурией в анамнезе или оксалатным нефролитиазом кальция.
Желчнокаменная болезнь.
Значительная потеря веса может увеличить риск развития желчнокаменной болезни. В клиническом исследовании орлистата для профилактики диабета типа 2 частота желчнокаменной болезни как нежелательного явления составила 2,9% (47 из 1649) у пациентов, рандомизированных в группу с применением орлистата, и 1,8% (30 из 1655) - в группу плацебо.
Разное.
Органические причины ожирения (например, гипотиреоз) следует исключить перед назначением орлистата. Пациентам следует рекомендовать придерживаться диетических рекомендаций. Желудочно-кишечные осложнения могут усиливаться при приеме орлистата с диетой с высоким содержанием жира (>30% от общего количества ежедневных калорий, поступающих из жира). Ежедневное потребление жира должно быть распределено на три основных приема пищи. Если орлистат принимать с одним любым приемом пищи с очень высоким содержанием жира, вероятность возникновения побочных эффектов со стороны ЖКТ возрастает.
Злоупотребление и зависимость.
Как и в случае с любым средством для похудения, существует вероятность злоупотребления орлистатом в некоторых особых группах пациентов (например, у пациентов с нервной анорексией или булимией).
Особые группы пациентов.
Педиатрические пациенты. Безопасность и эффективность применения орлистата у детей до 12 лет не установлены.
Безопасность и эффективность орлистата были оценены у подростков от 12 до 16 лет с ожирением. Применение орлистата в этой возрастной группе подтверждается данными адекватных и хорошо контролируемых исследований орлистата у взрослых с дополнительными данными 54-недельного исследования эффективности и безопасности и 21-дневного исследования минерального баланса у подростков от 12 до 16 лет с ожирением. Пациенты, получавшие орлистат в 54-недельном исследовании эффективности и безопасности (64,8% женского пола, 75% представители европеоидной расы, 18,8% афроамериканцы и 6,3% других этнических групп), имели среднее снижение ИМТ на 0,55 кг/м2 по сравнению со средним увеличением на 0,31 кг/м2 у пациентов, получавших плацебо (р=0,001). В обоих подростковых исследованиях побочные эффекты были в целом аналогичны тем, которые описаны у взрослых, и включали жирный/маслянистый стул, маслянистые выделения и маслянистую эвакуацию. В подгруппе из 152 пациентов, получавших орлистат, и 77 пациентов, получавших плацебо, из 54-недельного исследования изменения в составе тела, измеренные с помощью DEXA, были одинаковыми в обеих группах лечения, за исключением массы жира, которая была значительно снижена у пациентов, получавших орлистат, по сравнению с пациентами, получавшими плацебо (−2,5 кг против −0,6 кг, р=0,033). Поскольку орлистат может препятствовать усвоению жирорастворимых витаминов, всем пациентам следует ежедневно принимать поливитамины, содержащие витамины А, D, Е, К и бета-каротин. Витамины следует принимать по крайней мере за 2 ч до или после приема орлистата.
Концентрация орлистата и его метаболитов M1 и M3 в плазме крови была аналогична таковой у взрослых при том же уровне дозы. Суточное выделение жира с калом составляло 27 и 7% от потребляемого жира с пищей в группах лечения орлистатом и плацебо соответственно.
Пожилой возраст. Клинические исследования орлистата не включали достаточное количество пациентов в возрасте 65 лет и старше, чтобы определить, отличаются ли они по реакции от более молодых пациентов.
|
|
Список литературы
Www.fda.gov и www.rxlist.com, 2021.
Входит в состав
- 764-824₽ Орлистат (10 фирм)
- 569-1782₽ Листата Мини (Изварино Фарма ООО )
- 735-1645₽ Ксеналтен
- 743-1704₽ Орсотен слим (КРКА-Рус )
- 923-2749₽ Орлистат-Акрихин (Polpharma )
- 875-2859₽ Листата (Изварино Фарма ООО )
- 500-3606₽ Ксеникал (3 фирмы)
- 941-3406₽ Орсотен (2 фирмы)
- — КСЕНАЛТЕН СЛИМ
- — Ксеналтен Лайт
- — Ксеналтен Лого
- — ОРЛИСТАТ-ЛекТ (Тюменский химико-фармацевтический завод )
- — Орликсен 120
- — Орликсен 60
- — Орлимакс
- — Орлимакс-Лайт
- — Орлистат Канон
- — Орлистат Мини (2 фирмы)
- — Орлистат-алиум