МКБ-10 коды
|
|
Вступление
Кодирование по Международной статистической классификации болезней и проблем, связанных со здоровьем: с79.3.
Год утверждения (частота пересмотра): 2020.
Возрастная категория: Взрослые.
Пересмотр не позднее: 2022.
ID: 534.
Разработчик клинической рекомендации.
• Ассоциация онкологов России.
• Ассоциация нейрохирургов России.
• Общероссийская общественная организация «Российское общество клинической онкологии».
Одобрено Научно-практическим Советом Минздрава РФ.
Год утверждения (частота пересмотра): 2020.
Возрастная категория: Взрослые.
Пересмотр не позднее: 2022.
ID: 534.
Разработчик клинической рекомендации.
• Ассоциация онкологов России.
• Ассоциация нейрохирургов России.
• Общероссийская общественная организация «Российское общество клинической онкологии».
Одобрено Научно-практическим Советом Минздрава РФ.
|
|
 Список сокращений
Список сокращений
TNM - (аббревиатура от tumor, nodus и metastasis) международная классификация стадий развития злокачественных опухолей.
WHO - World Health Organization (Всемирная организация здравоохранения).
В/в бол. - внутривенно, болюсно.
В/в инф. - внутривенная инфузия.
Гр - Грей.
КТ - компьютерная томография.
Мг/м2 - миллиграмм на метр квадратный.
МГМ - метастазы в головной мозг.
МКБ-10 - Международная классификация болезней 10-го пересмотра.
МРТ - магнитно-резонансная томография.
МРЛ - мелкоклеточный рак легкого.
НМРЛ - немелкоклеточный рак легкого.
ОВГМ - облучение всего головного мозга.
ПХТ - полихимиотерапия.
ПЭТ/КТ - позитронно-эмиссионная томография, совмещенная с компьютерной томографией.
РКИ - рандомизированное контролируемое исследование.
РОД - разовая очаговая доза.
СОД - суммарная очаговая доза.
СРТ - стереотаксическая радиотерапия.
УЗИ - ультразвуковое исследование.
WHO - World Health Organization (Всемирная организация здравоохранения).
В/в бол. - внутривенно, болюсно.
В/в инф. - внутривенная инфузия.
Гр - Грей.
КТ - компьютерная томография.
Мг/м2 - миллиграмм на метр квадратный.
МГМ - метастазы в головной мозг.
МКБ-10 - Международная классификация болезней 10-го пересмотра.
МРТ - магнитно-резонансная томография.
МРЛ - мелкоклеточный рак легкого.
НМРЛ - немелкоклеточный рак легкого.
ОВГМ - облучение всего головного мозга.
ПХТ - полихимиотерапия.
ПЭТ/КТ - позитронно-эмиссионная томография, совмещенная с компьютерной томографией.
РКИ - рандомизированное контролируемое исследование.
РОД - разовая очаговая доза.
СОД - суммарная очаговая доза.
СРТ - стереотаксическая радиотерапия.
УЗИ - ультразвуковое исследование.
Термины и определения
• ECOG (Eastern сooperative Oncology Group). Шкала оценки общего состояния онкологического пациента до начала лечения, в процессе и после его окончания по 5-степенной системе (рекомендована Восточной кооперативной онкологической группой).
• PD1. Рецептор программируемой смерти 1.
• Блокатор PD1. Моноклональное антитело, блокирующее взаимодействие между рецептором программируемой смерти (PD-1) и его лигандами.
• Буст. Дополнительное облучение опухоли или ложа удаленной опухоли.
• Дистантные метастазы. Это появление новых метастатических очагов вне зоны ранее проведенного локального лечения.
• Единичный метастаз в головном мозге. Наличие одного метастатического очага в головном мозге.
• Иммуногистохимическое исследование. Метод микроскопического исследования тканей, обеспечивающий наиболее специфическое выявление в них искомых веществ и основанный на обработке срезов маркированными специфическими антителами к выявляемому веществу (антигену).
• Лекарственное противоопухолевое лечение. Введение препаратов внутрь, подкожно, внутривенно, внутримышечно, рассчитанное на системный противоопухолевый эффект.
• Локальные рецидивы. Это развитие рецидива (или продолженный рост) в зоне ранее облученных или удаленных метастатических очагах.
• Множественное метастатическое поражение. Количество очагов в головном мозге 5 и более.
• Ограниченное метастатическое поражение. Количество очагов в головном мозге 4 и меньше.
• Паллиативная терапия. Это лечение, направленное на улучшение качества жизни пациентов путем создания максимального комфорта и поддержки на последнем этапе развития онкологического заболевания.
• Солитарный метастаз в головном мозге. Наличие одного метастатического очага в головном мозге и отсутствие других проявлений отдаленного метастазирования опухолевого процесса.
• Сопроводительная терапия. Это лечение, направленное на уменьшение негативных последствий основного лечения (химиотерапии, таргетной терапии, лучевого лечения). Поддерживающая» терапия имеет целью сохранение позитивного ответа на основное лечение.
• Стереотаксическая радиотерапия. Вариант дистанционной лучевой терапии с использованием методов стереотаксической навигации и соответствующего технического оборудования, обеспечивающие прецизионную доставку максимальной дозы ионизирующего излучения к четко отграниченной мишени за минимально возможное число фракций. Величина дозы ионизирующего излучения при проведении стереотаксической радиотерапии ограничивается риском развития лучевых осложнений. Стереотаксическая радиотерапия может быть реализована в режиме радиохирургии, когда доза ионизирующего излучения подводится за одну фракцию и в режиме гипофракционирования, когда доза ионизирующего излучения подводится за несколько (чаще от 2 до 7) фракций.
• PD1. Рецептор программируемой смерти 1.
• Блокатор PD1. Моноклональное антитело, блокирующее взаимодействие между рецептором программируемой смерти (PD-1) и его лигандами.
• Буст. Дополнительное облучение опухоли или ложа удаленной опухоли.
• Дистантные метастазы. Это появление новых метастатических очагов вне зоны ранее проведенного локального лечения.
• Единичный метастаз в головном мозге. Наличие одного метастатического очага в головном мозге.
• Иммуногистохимическое исследование. Метод микроскопического исследования тканей, обеспечивающий наиболее специфическое выявление в них искомых веществ и основанный на обработке срезов маркированными специфическими антителами к выявляемому веществу (антигену).
• Лекарственное противоопухолевое лечение. Введение препаратов внутрь, подкожно, внутривенно, внутримышечно, рассчитанное на системный противоопухолевый эффект.
• Локальные рецидивы. Это развитие рецидива (или продолженный рост) в зоне ранее облученных или удаленных метастатических очагах.
• Множественное метастатическое поражение. Количество очагов в головном мозге 5 и более.
• Ограниченное метастатическое поражение. Количество очагов в головном мозге 4 и меньше.
• Паллиативная терапия. Это лечение, направленное на улучшение качества жизни пациентов путем создания максимального комфорта и поддержки на последнем этапе развития онкологического заболевания.
• Солитарный метастаз в головном мозге. Наличие одного метастатического очага в головном мозге и отсутствие других проявлений отдаленного метастазирования опухолевого процесса.
• Сопроводительная терапия. Это лечение, направленное на уменьшение негативных последствий основного лечения (химиотерапии, таргетной терапии, лучевого лечения). Поддерживающая» терапия имеет целью сохранение позитивного ответа на основное лечение.
• Стереотаксическая радиотерапия. Вариант дистанционной лучевой терапии с использованием методов стереотаксической навигации и соответствующего технического оборудования, обеспечивающие прецизионную доставку максимальной дозы ионизирующего излучения к четко отграниченной мишени за минимально возможное число фракций. Величина дозы ионизирующего излучения при проведении стереотаксической радиотерапии ограничивается риском развития лучевых осложнений. Стереотаксическая радиотерапия может быть реализована в режиме радиохирургии, когда доза ионизирующего излучения подводится за одну фракцию и в режиме гипофракционирования, когда доза ионизирующего излучения подводится за несколько (чаще от 2 до 7) фракций.
Описание
Метастатическое поражение головного мозга - это гетерогенная группа интракраниальных новообразований, объединяющих различные по происхождению, гистологической структуре, клиническому течению и результатам лечения новообразования, являющихся следствием гематогенного метастазирования экстракраниальных злокачественных опухолей.
Причины
Мозг - это уникальный орган-мишень , который характеризуется наличием гематоэнцефалического барьера и недостатком лимфатического дренажа. Развитие МГМ (происходит вследствие гематогенной диссеминации опухолевых клеток из первичного очага, с последующей фиксацией на эндотелии микрососудистого русла, проникновением в паренхиму мозга, что сопровождается неоангиогенезом и пролиферацией в ответ на выделяемые факторы роста. Высокое содержание хлорида в межклеточной жидкости препятствует образованию клонов из клеток эпителиального происхождения. Вероятно, что особая среда мозга привлекает клетки нейроэпителиального происхождения, такие как небольших размеров клетки рака легкого или меланомы. Это объясняет различия во встречаемости метастазов в головной мозг при разных первичных опухолях. Клетки метастатической меланомы тропны к ткани мозга, так как меланоциты и клетки нейронных субпопуляций имеют общий эмбриогенез, что обусловливает высокую частоту развития МГМ (метастазов в головной мозг).
Интракраниальные метастазы могут локализоваться в разных анатомических образованиях мозга. По данным Patchell R.A. и Tibbs P.A. (1998), супратенториальные метастазы составляют 80-85 %, метастазы в мозжечок - 10-15 %, в ствол мозга - 3-5 %, поражение мозговых оболочек - 1-2 %. Такое распределение, вероятно, зависит от кровоснабжения. Чаще опухолевые клетки фиксируются на эндотелии капилляров в области перехода серого и белого вещества головного мозга.
Злокачественные эпителиальные опухоли и саркомы чаще метастазируют в паренхиму мозга. МГМ при лейкозах преимущественно поражают мягкие мозговые оболочки, аденокарцинома молочной железы имеет тенденцию к метастазированию как в мозговые оболочки, так и в ткань мозга. Для карциномы предстательной железы наиболее распространенным является непосредственное поражение костей черепа, что приводит к развитию субдуральных поражений. Прорастая через твердую мозговую оболочку, метастазы могут врастать и дислоцировать ткань головного и спинного мозга.
При определенных биологических подтипах злокачественных опухолей метастазы в головном мозге встречаются чаще. Например, у больных раком молочной железы с гиперэкспрессией HER-2 риск метастатического поражения головного мозга достигает 30-55%.
Интракраниальные метастазы могут локализоваться в разных анатомических образованиях мозга. По данным Patchell R.A. и Tibbs P.A. (1998), супратенториальные метастазы составляют 80-85 %, метастазы в мозжечок - 10-15 %, в ствол мозга - 3-5 %, поражение мозговых оболочек - 1-2 %. Такое распределение, вероятно, зависит от кровоснабжения. Чаще опухолевые клетки фиксируются на эндотелии капилляров в области перехода серого и белого вещества головного мозга.
Злокачественные эпителиальные опухоли и саркомы чаще метастазируют в паренхиму мозга. МГМ при лейкозах преимущественно поражают мягкие мозговые оболочки, аденокарцинома молочной железы имеет тенденцию к метастазированию как в мозговые оболочки, так и в ткань мозга. Для карциномы предстательной железы наиболее распространенным является непосредственное поражение костей черепа, что приводит к развитию субдуральных поражений. Прорастая через твердую мозговую оболочку, метастазы могут врастать и дислоцировать ткань головного и спинного мозга.
При определенных биологических подтипах злокачественных опухолей метастазы в головном мозге встречаются чаще. Например, у больных раком молочной железы с гиперэкспрессией HER-2 риск метастатического поражения головного мозга достигает 30-55%.
|
|
Эпидемиология
У 8%-10% онкологических пациентов развиваются МГМ, которые часто определяют основную клиническую симптоматику. По данным популяционного канцер-регистра (Population-based Maastricht сancer Registry) из 2724 больных злокачественными опухолями, которые получили специфическое лечение в период с 1986 по 1995 гг., МГМ развились у 232 пациентов (8,5%). При этом, в течение первого месяца после постановки диагноза, МГМ развились у 84 пациентов (3,1%), в течение 1 года - у 82 (3,0%) пациентов, после 1 года от момента постановки диагноза - у 66 (2,4%) пациентов. Актуриальная частота развития МГМ после 5 лет наблюдения составила 16,3% у пациентов с диагнозом рак легких, 9,8% при почечно-клеточном раке, 7,4% при меланоме, 5,1% при раке молочной железы, 1,2% при колоректальном раке.
По данным другого канцер регистра (Metropolitan Detroit сancer Surveillance System, 1973-2001 гг.) частота метастатического поражения головного мозга составила 9,5% от всех случаев онкологических заболеваний. Частота метастатического поражения головного мозга составляет: при раке легкого - 19,9%, меланоме - 6,5%, раке почки - 6,5%, РМЖ - 5,1% и 1,8% в случае колоректального рака.
По данным другого канцер регистра (Metropolitan Detroit сancer Surveillance System, 1973-2001 гг.) частота метастатического поражения головного мозга составила 9,5% от всех случаев онкологических заболеваний. Частота метастатического поражения головного мозга составляет: при раке легкого - 19,9%, меланоме - 6,5%, раке почки - 6,5%, РМЖ - 5,1% и 1,8% в случае колоректального рака.
1,4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем.
C79,3 - Вторичное злокачественное новообразование головного мозга и мозговых оболочек.Классификация
1,5 Классификация заболевания или состояния (группы заболеваний или состояний).
Метастатическое поражение головного мозга - это всегда IV стадия опухолевого процесса, по классификации TNM ― М1.В зависимости от количества очагов в головном мозге выделяют: единичные - 1 очаг в головном мозге (или солитарные - один очаг в головном мозге и отсутствие других проявлений отдаленного метастазирования опухолевого процесса); олигометастатическое поражение головного мозга - 2-4 очага в головном мозге; множественные метастазы - 5 и более очагов в головном мозге. В зависимости от макроструктуры метастазы в головном мозге могут быть cолидной, кистозной и кистозно-солидной структуры.
Клиническая картина
Симптоматика зависима от размеров метастатических очагов, их количества и локализации в головном мозге. Клиническая картина может проявляться в виде появления очаговой неврологической симптоматики в случае локализации очага в определенной функциональной зоне и в виде общемозговой симптоматики, связанной с наличием масс-эффекта в головном мозге. Перифокальный отёк, часто обуславливающий повышение внутричерепного давления (ВЧД) вызывают общемозговые симптомы в виде головной боли, головокружения, двоения, рвоты при малейшем движении или даже при открывании глаз, постоянной икоты.
Выделяют варианты развития первичной симптоматики при метастатическом поражении головного мозга в соответствии с превалирующим комплексом симптомов. Острое течение: развивается быстро и проявляется очаговыми нарушениями - свидетельством поражения определённого участка мозга. Такой вариант, как правило, связан со сдавлением функциональных участков мозга растущим метастатическим очагом, либо кровоизлиянием. Хроническое течение характеризуется волнообразным течением, когда симптомы то уменьшаются, то прогрессируют. У некоторых больных метастазы головного мозга протекают бессимптомно и обнаруживаются только во время обследования.
Выделяют варианты развития первичной симптоматики при метастатическом поражении головного мозга в соответствии с превалирующим комплексом симптомов. Острое течение: развивается быстро и проявляется очаговыми нарушениями - свидетельством поражения определённого участка мозга. Такой вариант, как правило, связан со сдавлением функциональных участков мозга растущим метастатическим очагом, либо кровоизлиянием. Хроническое течение характеризуется волнообразным течением, когда симптомы то уменьшаются, то прогрессируют. У некоторых больных метастазы головного мозга протекают бессимптомно и обнаруживаются только во время обследования.
Диагностика
Критерии установления диагноза/состояния:
Диагноз устанавливается на основании:
• анамнестических данных: наличия в анамнезе онкологического заболевания.
• результатов физикального обследования: наличие неврологической симптоматики.
• рентгенологических данных: наличие очагового метастатического поражения головного мозга.
• результатов патологоанатомического исследования биопсийного (операционного) материала первичного опухолевого очага, экстракраниального метастаза или метастатического очага в головном мозге.
В случае наличия очагового поражения головного мозга как единственного проявления болезни целесообразно проведение нейрохирургического лечения (или стереотаксической биопсии) для морфологического подтверждения диагноза. Однако проведение указанных процедур не всегда возможно, и поэтому диагноз метастатического поражения головного мозга ставится по клинико-рентгенологическим данным. В этой клинической ситуации решение вопроса об объеме диагностических процедур и возможных вариантов лечения принимается на основании решения врачебной комиссии с участием нейрохирурга, онколога, радиотерапевта и врача-рентгенолога.
Пациенту также проводятся все необходимые исследования, направленные на установление диагноза, оценку функционального состояния, распространённости опухолевого процесса с последующим определением алгоритма оказания медицинской помощи в соответствии с клиническими рекомендациями по ЗНО первичных локализаций.
• Пациенту с метастатическим поражением головного мозга рекомендуется проведение клинических и инструментальных исследований, направленных на установление диагноза, оценку функционального состояния, распространённости опухолевого процесса с последующим определением алгоритма оказания медицинской помощи, в соответствии с клиническими рекомендациями по ЗНО первичных локализаций [1, 2].
Уровень убедительности рекомендаций - С (уровень достоверности доказательств - 5).
Уровень убедительности рекомендаций - С (уровень достоверности доказательств - 5).
Комментарии. Головная боль, тошнота, рвота, головокружение и являются наиболее частыми симптомами у пациентов с метастатическим поражением головного мозга. Эти симптомы, как правило, отражают повышение внутричерепного давления и смещение структур мозга (общемозговая симптоматика).
Нарушение чувствительности, памяти, двигательные нарушения (парезы и параличи), нарушение зрения и слуха, эпилептические припадки определяются локализацией метастатического очага в различных структурах мозга (очаговая симптоматика).
Множественные метастатические очаги в головном мозге часто сопровождаются нарушением координации, когнитивными расстройствами, нарушением памяти и эмоциональной сферы.
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - 5).
• Рекомендуется оценить функциональный статус пациента с бальной оценкой по шкале Карновского или ECOG (Приложение Г1 и Г2) [1, 2].
Уровень убедительности рекомендаций - С (уровень достоверности доказательств - 5).
Комментарии. Оценка роста и массы тела позволяет рассчитать площадь тела, необходимую для расчёта доз химиотерапевтических препаратов. Пальпация периферических лимфоузлов позволяет выявить метастатические лимфоузлы и оценить распространённость болезни. Общий физикальный осмотр проводится для изучения общего состояния пациента с последующей оценкой функционального статуса по шкале Карновского или ECOG. Точная оценка функционального статуса необходима для дальнейшего планирования лечения.
Уровень убедительности рекомендаций - С (уровень достоверности доказательств - 5).
Комментарии. Результаты лабораторных исследований необходимы для оценки функционального состояния организма пациента с МГМ перед проведением хирургического, химиотерапевтического и лучевого лечения, а также для своевременной коррекции выявленных изменений на этапе лечения и наблюдения.
• в случае подозрения на метастатическое поражение головного мозга;
• сразу после окончания локального лечения по поводу МГМ;
• через каждые 2 курса после проведения химиотерапии по поводу МГМ и на этапе наблюдения после лечения.[2, 3].
Уровень убедительности рекомендаций - С (уровень достоверности доказательств - 5).
• Проведение магнитно-резонансной томографии (МРТ) головного мозга и позвоночника с оценкой ликвородинамики рекомендуется у пациентов с лептоменингиальными метастатическим поражением с целью исключения ликвородинамических нарушений.[2-4].
Уровень убедительности рекомендаций - С (уровень достоверности доказательств - 5).
• Рекомендуется использовать шкалу RANO вM ( см Приложение Г3) для оценки динамики метастатических очагов в головном мозге после проведенной терапии [3, 5].
Уровень убедительности рекомендаций - С (уровень достоверности доказательств - 5).
• Рекомендуется проведение компьютерной томографии (КТ) с контрастированием для диагностики метастатического поражения головного мозга только при наличии противопоказаний к проведению магнитно-резонансной томографии [2, 3].
Уровень убедительности рекомендаций - С (уровень достоверности доказательств - 5).
Комментарии. МРТ головного мозга рекомендуется выполнять в следующих режимах - до внутривенного введения контрастного вещества в режимах Т1в аксиальной проекции (толщина среза 1-1,5 мм), Т2, ДВИ, FLAIR (толщина среза 3-5 мм). После внутривенного введения контрастного вещества: Т1 в аксиальной проекции (толщина среза 1-1,5 мм), 3D T1 взвешенные изображения высокого разрешения в аксиальной (или сагиттальной) плоскости с захватом всей головы с применением технологии изотропного воксела (1мм×1мм×1мм).
Целесообразно проведение МРТ головного мозга с контрастным усилением в течение 24-48 часов после проведения нейрохирургического лечения для определения степени полноты резекции опухоли.
Целесообразно проведение КТ головного мозга с/без контрастирования в течение 24-48 часов после проведения нейрохирургического лечения для диагностики возможных послеоперационных осложнений.
Выполнение СКТ перфузии позволяет измерить объем церебрального кровотока опухоли и нормальной ткани мозга. Применяется для дифференциальной диагностики рецидива опухоли и радиационного некроза.
• ПЭТ головного мозга с использованием радиоактивно меченных индикаторов (фторэтилтирозином и 11С метионином) рекомендовано для определения злокачественности опухоли, дифференциации рецидива опухоли от радиационного некроза [2].
Уровень убедительности рекомендаций С (уровень достоверности доказательств -5).
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5).
Комментарии: Консультация онколога, нейрохирурга и радиотерапевта необходима для определения оптимальной тактики лечения в рамках мультидисциплинарного подхода.
Диагноз устанавливается на основании:
• анамнестических данных: наличия в анамнезе онкологического заболевания.
• результатов физикального обследования: наличие неврологической симптоматики.
• рентгенологических данных: наличие очагового метастатического поражения головного мозга.
• результатов патологоанатомического исследования биопсийного (операционного) материала первичного опухолевого очага, экстракраниального метастаза или метастатического очага в головном мозге.
В случае наличия очагового поражения головного мозга как единственного проявления болезни целесообразно проведение нейрохирургического лечения (или стереотаксической биопсии) для морфологического подтверждения диагноза. Однако проведение указанных процедур не всегда возможно, и поэтому диагноз метастатического поражения головного мозга ставится по клинико-рентгенологическим данным. В этой клинической ситуации решение вопроса об объеме диагностических процедур и возможных вариантов лечения принимается на основании решения врачебной комиссии с участием нейрохирурга, онколога, радиотерапевта и врача-рентгенолога.
Пациенту также проводятся все необходимые исследования, направленные на установление диагноза, оценку функционального состояния, распространённости опухолевого процесса с последующим определением алгоритма оказания медицинской помощи в соответствии с клиническими рекомендациями по ЗНО первичных локализаций.
• Пациенту с метастатическим поражением головного мозга рекомендуется проведение клинических и инструментальных исследований, направленных на установление диагноза, оценку функционального состояния, распространённости опухолевого процесса с последующим определением алгоритма оказания медицинской помощи, в соответствии с клиническими рекомендациями по ЗНО первичных локализаций [1, 2].
Уровень убедительности рекомендаций - С (уровень достоверности доказательств - 5).
2,1 Жалобы и анамнез.
• Рекомендуется сбор жалоб и анамнеза у пациента с подозрением на метастатическое поражение головного мозга с целью выявления факторов, которые могут повлиять на выбор тактики лечения [1, 2].Уровень убедительности рекомендаций - С (уровень достоверности доказательств - 5).
Комментарии. Головная боль, тошнота, рвота, головокружение и являются наиболее частыми симптомами у пациентов с метастатическим поражением головного мозга. Эти симптомы, как правило, отражают повышение внутричерепного давления и смещение структур мозга (общемозговая симптоматика).
Нарушение чувствительности, памяти, двигательные нарушения (парезы и параличи), нарушение зрения и слуха, эпилептические припадки определяются локализацией метастатического очага в различных структурах мозга (очаговая симптоматика).
Множественные метастатические очаги в головном мозге часто сопровождаются нарушением координации, когнитивными расстройствами, нарушением памяти и эмоциональной сферы.
2,2 Физикальное обследование.
• Рекомендуется всем пациентам, как при подозрении на метастатическое поражение головного мозга, так и при установленном диагнозе производить физикальное обследование, включающий осмотр кожных покровов пациента, оценки состояние периферических лимфоузлов, молочных желез с целью установления клинической стадии заболевания [1, 2].Уровень убедительности рекомендаций. С (уровень достоверности доказательств - 5).
• Рекомендуется оценить функциональный статус пациента с бальной оценкой по шкале Карновского или ECOG (Приложение Г1 и Г2) [1, 2].
Уровень убедительности рекомендаций - С (уровень достоверности доказательств - 5).
Комментарии. Оценка роста и массы тела позволяет рассчитать площадь тела, необходимую для расчёта доз химиотерапевтических препаратов. Пальпация периферических лимфоузлов позволяет выявить метастатические лимфоузлы и оценить распространённость болезни. Общий физикальный осмотр проводится для изучения общего состояния пациента с последующей оценкой функционального статуса по шкале Карновского или ECOG. Точная оценка функционального статуса необходима для дальнейшего планирования лечения.
2,3 Лабораторные диагностические исследования.
• Пациентам с метастатическим поражением головного мозга рекомендуется проведение общего анализа крови с исследованием лейкоцитарной формулы, общего анализа мочи, биохимического анализа крови (общий белок, альбумин, мочевина, креатинин, аланинаминотрансфераза, аспартатаминотрансфераза, натрий, калий) до начала лечения, в процессе лечения и на этапе наблюдения. [1, 2].Уровень убедительности рекомендаций - С (уровень достоверности доказательств - 5).
Комментарии. Результаты лабораторных исследований необходимы для оценки функционального состояния организма пациента с МГМ перед проведением хирургического, химиотерапевтического и лучевого лечения, а также для своевременной коррекции выявленных изменений на этапе лечения и наблюдения.
2,4 Инструментальные диагностические исследования.
• Проведение магнитно-резонансной томографии (МРТ) головного мозга с внутривенным контрастированием рекомендуется у пациентов с онкологическим заболеванием:• в случае подозрения на метастатическое поражение головного мозга;
• сразу после окончания локального лечения по поводу МГМ;
• через каждые 2 курса после проведения химиотерапии по поводу МГМ и на этапе наблюдения после лечения.[2, 3].
Уровень убедительности рекомендаций - С (уровень достоверности доказательств - 5).
• Проведение магнитно-резонансной томографии (МРТ) головного мозга и позвоночника с оценкой ликвородинамики рекомендуется у пациентов с лептоменингиальными метастатическим поражением с целью исключения ликвородинамических нарушений.[2-4].
Уровень убедительности рекомендаций - С (уровень достоверности доказательств - 5).
• Рекомендуется использовать шкалу RANO вM ( см Приложение Г3) для оценки динамики метастатических очагов в головном мозге после проведенной терапии [3, 5].
Уровень убедительности рекомендаций - С (уровень достоверности доказательств - 5).
• Рекомендуется проведение компьютерной томографии (КТ) с контрастированием для диагностики метастатического поражения головного мозга только при наличии противопоказаний к проведению магнитно-резонансной томографии [2, 3].
Уровень убедительности рекомендаций - С (уровень достоверности доказательств - 5).
Комментарии. МРТ головного мозга рекомендуется выполнять в следующих режимах - до внутривенного введения контрастного вещества в режимах Т1в аксиальной проекции (толщина среза 1-1,5 мм), Т2, ДВИ, FLAIR (толщина среза 3-5 мм). После внутривенного введения контрастного вещества: Т1 в аксиальной проекции (толщина среза 1-1,5 мм), 3D T1 взвешенные изображения высокого разрешения в аксиальной (или сагиттальной) плоскости с захватом всей головы с применением технологии изотропного воксела (1мм×1мм×1мм).
Целесообразно проведение МРТ головного мозга с контрастным усилением в течение 24-48 часов после проведения нейрохирургического лечения для определения степени полноты резекции опухоли.
Целесообразно проведение КТ головного мозга с/без контрастирования в течение 24-48 часов после проведения нейрохирургического лечения для диагностики возможных послеоперационных осложнений.
Выполнение СКТ перфузии позволяет измерить объем церебрального кровотока опухоли и нормальной ткани мозга. Применяется для дифференциальной диагностики рецидива опухоли и радиационного некроза.
• ПЭТ головного мозга с использованием радиоактивно меченных индикаторов (фторэтилтирозином и 11С метионином) рекомендовано для определения злокачественности опухоли, дифференциации рецидива опухоли от радиационного некроза [2].
Уровень убедительности рекомендаций С (уровень достоверности доказательств -5).
2,5 Иные диагностические исследования.
• Пациентам с метастатическим поражением головного мозга рекомендуется проведение мультидисциплинарного консилиума с участием врача-онколога, врача-радиотерапевта и врача-нейрохирурга с целью определения объема диагностики и лечения.[1, 2].Уровень убедительности рекомендаций С (уровень достоверности доказательств 5).
Комментарии: Консультация онколога, нейрохирурга и радиотерапевта необходима для определения оптимальной тактики лечения в рамках мультидисциплинарного подхода.
|
|
Лечение
У пациентов с МГМ применяются локальные и системные методы лечения. К локальным методам лечения относятся: нейрохирургическое лечение и дистанционная лучевая терапия, которая может быть реализована в виде облучения всего головного мозга (ОВГМ) и в виде стереотаксической радиотерапии (в режиме радиохирургии или гипофракционирования). Оптимальной методикой лечения у пациентов с МГМ является комбинация методов локального лечения. Варианты комбинации локальных методов лечения определяются числом и объемом метастазов в головном мозге.
К системным методам лечения относится противоопухолевая лекарственная терапия. В последнее время важное значение в лечении пациентов с МГМ имеет таргетная терапия.
• Нейрохирургическое лечение. Удаление новообразований головного мозга микрохирургическое - рекомендуется пациентам с МГМ в следующих случаях:
• при наличии локальных рецидивов после ранее проведенного локальных методов лечения (нейрохирургического и/или лучевого) метастатических очагов в головном мозге [9].
Уровень убедительности рекомендаций С (уровень достоверности доказательств -4).
• при наличии метастатического очага с максимальным диаметром 2,5 см и более [2, 7].
• при наличии метастатического очага, определяющего клиническую картину внутричерепной гипертензии, дислокации срединных структур мозга, обширного перифокального отека, а также при наличии угрозы блокирования ликворных путей [2, 6, 8].
• при наличии крупного метастатического очага с целью установления/уточнения морфологического диагноза в случае если другие методы морфологической верификации болезни невозможны [2].
Уровень убедительности рекомендаций С (уровень достоверности доказательств -5).
Комментарии. Необходимым условием проведения нейрохирургического лечения является расположение метастатического очага в зонах мозга, где его удаление не сопровождается развитием неврологического дефицита. Лучшие показатели общей выживаемости достигаются у пациентов с высоким функциональным статусом (индекс Карновского ≥ 80) и контролем экстракраниального опухолевого процесса.
Не имеется достаточно клинических данных, чтобы рекомендовать плановое хирургическое лечение для пациентов с плохим прогнозом или с множественными метастазами в головном мозге.
Метастатический очаг в головном мозге, в ряде случаев, может быть единственным проявлением болезни. В этом случае удаление очага с последующим патологоанатомическим исследованием с уточнением молекулярно-биологических характеристик опухоли, что позволит установить диагноз и начать проведение противоопухолевого лекарственного лечения.
Целесообразно проводить нейрохирургического лечение в комбинации со стереотаксической радиотерапией (предоперационная радиохирургия или послеоперационная стереотаксическая радиотерапия ложа удаленного метастатического очага) для снижения риска локального рецидива.
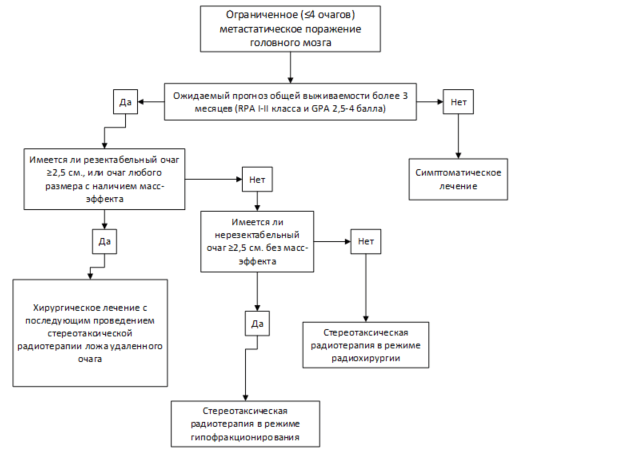
• У пациентов с ограниченным метастатическим поражением головного мозга и хорошим прогнозом общей выживаемости рекомендуется:
• при наличии метастатических очагов в головном мозге с максимальным диаметром 2,5 см и меньше без клинических проявлений масс-эффекта проведение стереотаксической радиохирургии [10, 11].
Уровень убедительности рекомендаций С (уровень достоверности доказательств -5).
Комментарии. Хороший прогноз общей выживаемости определяется наличием у пациентов - индекса Карновского ≥80 (или ECOG 0-1), GPA-2,5-4, отсутствием или ограниченным числом экстракраниальных метастазов и наличием резервов системного противоопухолевого лечения.
Дозы ионизирующего излучения при проведении радиохирургии в соответствии с исследованием RTOG 90-05 [13] являются: 15 Гр для МГМ с максимальным диаметром 3-4 18 Гр для МГМ с максимальным диаметром 2-3 24 Гр для МГМ с максимальным диаметром до 2 см.
• при наличии метастатических очагов в головном мозге с максимальным диаметром 2,5 см и больше, без клинических проявлений масс-эффекта, при наличии противопоказаний к проведению нейрохирургического лечения проведение стереотаксической радиотерапии в режиме гипофракционирования [14].
Уровень убедительности рекомендаций в (уровень достоверности доказательств - 3).
Комментарии. Эквивалентными режимами гипофракционирования являются - 3 фракции по 8 Гр (или по 9Гр), СОД = 24 Гр (27Гр); 5 фракций по 6 Гр, СОД = 30 Гр; 7 фракций по 5 Гр, СОД = 35 Гр. Число постлучевых осложнений возрастает по мере увеличения разовой дозы: так число пациентов с развитием радионекроза при режиме 3 фракции по 8Гр достигает 23%.
• при наличии ложа удаленного метастатического очага после нейрохирургического лечения и других метастатических очагов в случае их наличия проведение стереотаксической радиотерапии [15].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
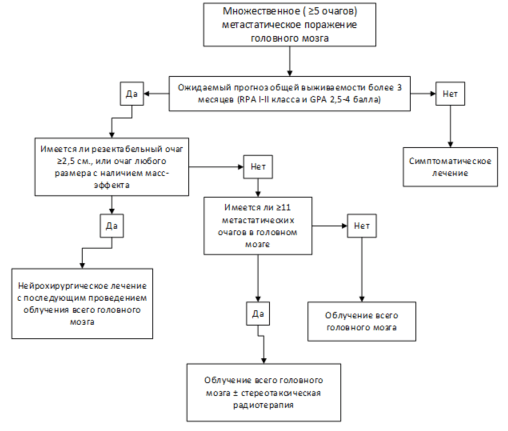
• У пациентов с наличием от 5 до 10 метастатических очагов в головном мозге и хорошим прогнозом общей выживаемости рекомендуется проведение облучения всего головного мозга в самостоятельном варианте лечения или в комбинации со стереотаксической радиотерапией [16, 17].
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 3).
Комментарии. В случае комбинации стереотаксической радиотерапии и облучения всего головного мозга целесообразно редуцировать дозы стереотаксического буста на 20%-25% от первоначальной дозы с целью уменьшения риска развития радионекроза.
С учетом риска развития нейрокогнитивных расстройств у пациентов с МГМ после проведения ОВГМ альтернативной методикой является применение стереотаксической радиотерапии в самостоятельном варианте лечения с последующим проведением МРТ-мониторинга головного мозга и проведением локального лечения в соответствии с пунктом 3,4 текущих рекомендаций в случае дальнейшей интракраниальной прогрессии.
• У пациентов с наличием от 11 и более метастатических очагов в головном мозге и хорошим прогнозом общей выживаемости рекомендуется проведение облучения всего головного мозга в самостоятельном варианте лечения [2].
Уровень убедительности рекомендаций С (уровень достоверности доказательств -5).
Комментарии. Стандартным режимом фракционирования ОВГМ является СОД 30 Гр, РОД 3 Гр (10 фракций) или СОД 37,5 РОД 2,5 (15 фракций). Увеличение при ОВГМ, более 3 Гр приводит к увеличению частоты нейрокогнитивных расстройств и не улучшает результаты лечения.
Пожилой возраст и повышение разовой дозы ОВГМ являются наиболее значимыми прогностическими факторами нарушения когнитивных функций после проведения ОВГМ.
В отдельных клинических ситуациях у пациентов множественными МГМ, изолированной интракраниальной прогрессией (отсутствие или стабилизация экстракраниальных метастазов и наличие резервов лекарственной противоопухолевой терапии), хорошим прогнозом общей выживаемости возможно проведение стереотаксической радиотерапии в комбинации с ОВГМ или в самостоятельном варианте лечения.
• У пациентов с мелкоклеточным раком легкого (МРЛ) рекомендуется:
• проведение профилактического ОВГМ в случае частичного или полного ответа экстракраниальных метастатических очагов после проведения ПХТ целью снижения риска развития МГМ [18].
• проведение ОВГМ в случае наличия МГМ [2].
Уровень убедительности рекомендаций С (уровень достоверности доказательств -5).
Комментарии. У пациентов с МРЛ, с хорошим ответом опухолевых очагов на противоопухолевую лекарственную терапию профилактическое ОВГМ уменьшает риск развития МГМ (при всех стадиях заболевания) и увеличивает общую выживаемость (при 1-2 стадии болезни).
Профилактическое ОВГМ у пациентов с МРЛ проводится в СОД 25 Гр за 10 ежедневных фракций. Короткий курс (20 Гр в 5 фракциях) может проводиться у пациентов с низким функциональным статусом и 3-4 стадией болезни.
У пациентов с метастазами МРЛ в головной мозг, как правило, рекомендуется проведение ОВГМ; однако в случае ограниченного метастатического поражения головного мозга может быть проведена стереотаксическая радиотерапия.
• При проведении ОВГМ рекомендуется применение мемантина (5 мг каждое утро; 2я неделя - 5 мг каждое утро и вечер; 3-я неделя - 10 мг каждое утро и 5 мг каждый вечер; 4я-24я недели по 10 мг утром и вечером) во время и после проведения ОВГМ, для уменьшения риска развития когнитивных нарушений [19].
Уровень убедительности рекомендаций в (уровень достоверности доказательств -2).
Комментарии. Альтернативной методикой, снижающей риск развития когнитивных расстройств, является проведение ОВГМ с применением IMRT/VIMAT методик с защитой гиппокампальных извилин с обеих сторон [20].
Системное противоопухолевое лечение проводится в режимах, согласно рекомендациям по лечению первичного опухолевого очага с учетом биологических характеристик опухоли.
• Рекомендуется проведение системной противоопухолевой терапии (химиотерапия, таргетная терапия, иммунотерапия) в самостоятельном варианте лечения у пациентов с небольшими по размеру, бессимптомными МГМ при наличии в арсенале лечения препаратов с установленной эффективностью в головном мозге [21].
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 3).
Комментарии. Выбор схемы противоопухолевого лекарственного лечения пациента с метастатическим опухолевым процессом в головном мозге зависит, в первую очередь, от типа первичной опухоли, ее биологических характеристик и наличия препаратов с установленной эффективностью в головном мозге [2, 21].
Противоопухолевая лекарственная терапия в самостоятельном варианте лечения проводится только у пациентов с бессимптомным метастатическим поражением головного мозга и при наличии препаратов с установленной эффективностью в головном мозге. Во всех остальных случаях противоопухолевая лекарственная терапия проводится в соответствии с клиническими рекомендациями по лечению первичного опухолевого очага в комбинации с локальным лечением МГМ в соответствии с пунктом 4 текущих клинических рекомендаций.
В случае выявления МГМ на фоне стабилизации (или регрессии) экстракраниальных метастазов вследствие эффективной противоопухолевой лекарственной терапии, целесообразно проведение локального лечения МГМ в соответствии с пунктами 3,1-3,2 текущих клинических рекомендаций и сохранение режима проводимой противоопухолевой лекарственной терапии.
В случае выявления МГМ (или появления дистантных метастатических очагов в головном мозге) и прогрессирования экстракраниальных метастазов на фоне проведения противоопухолевой лекарственной терапии необходимо изменение режима лекарственного лечения. Предпочтение отдается препаратам с установленной противоопухолевой эффективностью в головном мозге.
В случае отсутствия таковых препаратов противоопухолевая лекарственная терапия проводится в соответствии с клиническими рекомендациями по лечению первичного опухолевого очага в комбинации с локальным лечением МГМ в соответствии с пунктами 3,1-3,2 текущих клинических рекомендаций.
Решение о начале или продолжении противоопухолевой лекарственной терапии после проведения локального лечения принимается индивидуально, однако целесообразно отложить ее начало до ликвидации/уменьшения проявлений постлучевых реакций и/или послеоперационных осложнений и прекращения (или снижения доз) стероидной терапии.
Нежелательно проведение иммунотерапии на фоне продолжающейся стероидной терапии в высоких дозах (>8 мг/сутки дексаметазона).
Возможно одновременное проведение таргетной терапии и радиотерапии у пациентов с хорошим функциональным статусам при условии адекватного мониторинга общего состояния пациента. В случае проведения цикловой химиотерапии возможно проведение радиохирургии между курсами проводимой противоопухолевой лекарственной терапии.
В случае проведения противоопухолевой лекарственной терапии в самостоятельном варианте лечения МРТ-мониторинг головного мозга проводится через 2 месяца от начала лекарственного лечения (или после 2-3-х курсов циклового лечения) для оценки эффективности проводимой терапии и своевременного проведения локального лечения МГМ соответствии с пунктом 3,1-3,2 текущих клинических рекомендаций в случае дальнейшей интракраниальной прогрессии.
• Рекомендуется проведение системной противоопухолевой терапии (химиотерапия, таргетная терапия, иммунотерапия) в самостоятельном варианте лечения или как компонент комбинированного (с лучевой терапией) лечения у пациентов с лептоменингиальными метастатическим поражением головного мозга [2, 4].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии.
Лечение проводится при наличии клинических и рентгенологических данных поражения лептоменингеальная оболочек и/или цитологического обнаружения опухолевых клеток в спинномозговой жидкости.
Целесообразно проведение стереотаксической радиотерапии на наиболее крупные опухолевые очаги с целью снижения неврологической симптоматики и сохранения качества жизни.
В случае исчерпанности резервов противоопухолевой лекарственной терапии возможно проведение интратекальной химиотерапии.
• Не рекомендуется проведение стероидной терапии у пациентов с МГМ без клинической неврологической симптоматики [22].
Уровень убедительности рекомендаций С (уровень достоверности доказательств -5).
• У пациентов с МГМ и умеренно выраженными симптомами, связанными с масс-эффектом: рекомендуется проведение стероидной терапии (дексаметазон) для ликвидации или временного облегчения симптомов, связанных с повышением внутричерепного давления и вторичным отеком мозга. Начальная доза дексаметазона 4-8 мг/сутки [22].
Уровень убедительности рекомендаций С (уровень достоверности доказательств -5).
• У пациентов с МГМ и сильно выраженными симптомами, связанными с масс-эффектом. Рекомендуется назначение стероидной терапии (дексаметазон) для временного облегчения симптомов, связанных с повышением внутричерепного давления и вторичным отеком мозга. Начальная доза дексаметазона - от 12 мг/сутки [22].
Уровень убедительности рекомендаций С (уровень достоверности доказательств -5).
Комментарии. Дозы дексаметазона снижаются постепенно, в течение 2-х недель и более, основываясь на индивидуальной динамике клинической симптоматике и учитывая осложнения стероидной терапии. В отдельных клинических ситуациях возможно длительное/постоянное применение дексаметазона в минимально эффективных поддерживающих дозах (0,5-4 мг/сутки).
Снижение/отмена дозировки дексаметазона до хирургического удаления и/или проведения радиотерапии нецелесообразно.
Назначение и прием стероидных гормонов рекомендуется в 1-3 приема, перорально (при суточных дозах менее 4 мг) или внутримышечно, в соответствии с циркадным (солнечным) ритмом, с максимальными дозами в утренние часы, с последним приемом не позднее 16-17 часов.
• Рекомендуется проведение терапии бевацизумабом при наличии стойкого или нарастающего симптоматического отёка или радионекроза после проведения стереотаксической радиотерапии, резистентного к проводимой стероидной терапии [23-25] .
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - 4).
Комментарии: доза бевацизумаба составляет 7,5 мг/кг с интервалом 3 недели, не менее 4 введений, и проводится до регресса симптоматики или улучшения рентгенологической картины.
Уровень убедительности рекомендаций. С (уровень достоверности доказательств 5).
• Не рекомендуется профилактическое проведение противосудорожной терапии у пациентов без судорожного синдрома [26].
Уровень убедительности рекомендаций. С (уровень достоверности доказательств 5).
• Проведение паллиативной терапии рекомендуется у пациентов с МГМ и/или с распространенным лептоменингиальными поражением головного мозга при наличии плохого прогноза общей выживаемости (индекс Карновского ≤70, ECOG 2-4, GPA 0-2 балла, множественными экстракраниальными метастазами, не контролируемыми проявлениями экстракраниальной болезни и с отсутствием резервов системного лечения) [4, 10, 27].
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - 5).
Уровень убедительности рекомендаций С (уровень достоверности доказательств 5).
Комментарии. Объем лечения интракраниальных рецидивов определяется на совместном консилиуме врача онколога, радиотерапевта, нейрохирурга и проводится с учетом вида рецидива (дистантные метастазы и/или локальные рецидивы) и метода предшествующего лечения.
В случае развития интракраниальных рецидивов после ОВГМ рекомендуется проведение стереотаксической радиотерапии или нейрохирургического лечения.
В случае развития дистантных метастазов после нейрохирургического лечения и/или после стереотаксической радиотерапии лечение проводится также, как в случае первично-выявленных МГМ в соответствии с пунктами 3,1-3,2 текущих клинических рекомендаций.
При наличии локальных рецидивов после стереотаксической радиотерапии, возможно, проведения нейрохирургического лечения или повторной стереотаксической радиотерапии.
В случае проведения повторной стереотаксической радиотерапии дозы ионизирующего излучения назначаются строго индивидуально, исходя из объема рецидива, его локализации и наличия постлучевых осложнений. Лечение проводится на фоне стероидной терапии в соответствии с пунктом 3,5 текущих клинических рекомендаций.
К системным методам лечения относится противоопухолевая лекарственная терапия. В последнее время важное значение в лечении пациентов с МГМ имеет таргетная терапия.
3,1 Нейрохирургическое лечение.
Цель нейрохирургического лечения (удаления новообразований головного мозга микрохирургического) - обеспечение локального контроля метастатических очагов, уменьшение/ликвидация неврологической симптоматики, ликвидация угрожающих жизни состояний, уменьшение риска смерти от интракраниальной прогрессии, сохранения качества жизни и увеличения общей выживаемости в отдельных клинических ситуациях [6, 7].• Нейрохирургическое лечение. Удаление новообразований головного мозга микрохирургическое - рекомендуется пациентам с МГМ в следующих случаях:
• при наличии локальных рецидивов после ранее проведенного локальных методов лечения (нейрохирургического и/или лучевого) метастатических очагов в головном мозге [9].
Уровень убедительности рекомендаций С (уровень достоверности доказательств -4).
• при наличии метастатического очага с максимальным диаметром 2,5 см и более [2, 7].
• при наличии метастатического очага, определяющего клиническую картину внутричерепной гипертензии, дислокации срединных структур мозга, обширного перифокального отека, а также при наличии угрозы блокирования ликворных путей [2, 6, 8].
• при наличии крупного метастатического очага с целью установления/уточнения морфологического диагноза в случае если другие методы морфологической верификации болезни невозможны [2].
Уровень убедительности рекомендаций С (уровень достоверности доказательств -5).
Комментарии. Необходимым условием проведения нейрохирургического лечения является расположение метастатического очага в зонах мозга, где его удаление не сопровождается развитием неврологического дефицита. Лучшие показатели общей выживаемости достигаются у пациентов с высоким функциональным статусом (индекс Карновского ≥ 80) и контролем экстракраниального опухолевого процесса.
Не имеется достаточно клинических данных, чтобы рекомендовать плановое хирургическое лечение для пациентов с плохим прогнозом или с множественными метастазами в головном мозге.
Метастатический очаг в головном мозге, в ряде случаев, может быть единственным проявлением болезни. В этом случае удаление очага с последующим патологоанатомическим исследованием с уточнением молекулярно-биологических характеристик опухоли, что позволит установить диагноз и начать проведение противоопухолевого лекарственного лечения.
Целесообразно проводить нейрохирургического лечение в комбинации со стереотаксической радиотерапией (предоперационная радиохирургия или послеоперационная стереотаксическая радиотерапия ложа удаленного метастатического очага) для снижения риска локального рецидива.
3,2 Консервативное лечение.
3,2,1 Дистанционная лучевая терапия.
Цель дистанционной лучевой терапии - обеспечение локального контроля метастатических очагов для снижения риска смерти от интракраниальной прогрессии, сохранения качества жизни и улучшения общей выживаемости [10-12].• У пациентов с ограниченным метастатическим поражением головного мозга и хорошим прогнозом общей выживаемости рекомендуется:
• при наличии метастатических очагов в головном мозге с максимальным диаметром 2,5 см и меньше без клинических проявлений масс-эффекта проведение стереотаксической радиохирургии [10, 11].
Уровень убедительности рекомендаций С (уровень достоверности доказательств -5).
Комментарии. Хороший прогноз общей выживаемости определяется наличием у пациентов - индекса Карновского ≥80 (или ECOG 0-1), GPA-2,5-4, отсутствием или ограниченным числом экстракраниальных метастазов и наличием резервов системного противоопухолевого лечения.
Дозы ионизирующего излучения при проведении радиохирургии в соответствии с исследованием RTOG 90-05 [13] являются: 15 Гр для МГМ с максимальным диаметром 3-4 18 Гр для МГМ с максимальным диаметром 2-3 24 Гр для МГМ с максимальным диаметром до 2 см.
• при наличии метастатических очагов в головном мозге с максимальным диаметром 2,5 см и больше, без клинических проявлений масс-эффекта, при наличии противопоказаний к проведению нейрохирургического лечения проведение стереотаксической радиотерапии в режиме гипофракционирования [14].
Уровень убедительности рекомендаций в (уровень достоверности доказательств - 3).
Комментарии. Эквивалентными режимами гипофракционирования являются - 3 фракции по 8 Гр (или по 9Гр), СОД = 24 Гр (27Гр); 5 фракций по 6 Гр, СОД = 30 Гр; 7 фракций по 5 Гр, СОД = 35 Гр. Число постлучевых осложнений возрастает по мере увеличения разовой дозы: так число пациентов с развитием радионекроза при режиме 3 фракции по 8Гр достигает 23%.
• при наличии ложа удаленного метастатического очага после нейрохирургического лечения и других метастатических очагов в случае их наличия проведение стереотаксической радиотерапии [15].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
• У пациентов с наличием от 5 до 10 метастатических очагов в головном мозге и хорошим прогнозом общей выживаемости рекомендуется проведение облучения всего головного мозга в самостоятельном варианте лечения или в комбинации со стереотаксической радиотерапией [16, 17].
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 3).
Комментарии. В случае комбинации стереотаксической радиотерапии и облучения всего головного мозга целесообразно редуцировать дозы стереотаксического буста на 20%-25% от первоначальной дозы с целью уменьшения риска развития радионекроза.
С учетом риска развития нейрокогнитивных расстройств у пациентов с МГМ после проведения ОВГМ альтернативной методикой является применение стереотаксической радиотерапии в самостоятельном варианте лечения с последующим проведением МРТ-мониторинга головного мозга и проведением локального лечения в соответствии с пунктом 3,4 текущих рекомендаций в случае дальнейшей интракраниальной прогрессии.
• У пациентов с наличием от 11 и более метастатических очагов в головном мозге и хорошим прогнозом общей выживаемости рекомендуется проведение облучения всего головного мозга в самостоятельном варианте лечения [2].
Уровень убедительности рекомендаций С (уровень достоверности доказательств -5).
Комментарии. Стандартным режимом фракционирования ОВГМ является СОД 30 Гр, РОД 3 Гр (10 фракций) или СОД 37,5 РОД 2,5 (15 фракций). Увеличение при ОВГМ, более 3 Гр приводит к увеличению частоты нейрокогнитивных расстройств и не улучшает результаты лечения.
Пожилой возраст и повышение разовой дозы ОВГМ являются наиболее значимыми прогностическими факторами нарушения когнитивных функций после проведения ОВГМ.
В отдельных клинических ситуациях у пациентов множественными МГМ, изолированной интракраниальной прогрессией (отсутствие или стабилизация экстракраниальных метастазов и наличие резервов лекарственной противоопухолевой терапии), хорошим прогнозом общей выживаемости возможно проведение стереотаксической радиотерапии в комбинации с ОВГМ или в самостоятельном варианте лечения.
• У пациентов с мелкоклеточным раком легкого (МРЛ) рекомендуется:
• проведение профилактического ОВГМ в случае частичного или полного ответа экстракраниальных метастатических очагов после проведения ПХТ целью снижения риска развития МГМ [18].
• проведение ОВГМ в случае наличия МГМ [2].
Уровень убедительности рекомендаций С (уровень достоверности доказательств -5).
Комментарии. У пациентов с МРЛ, с хорошим ответом опухолевых очагов на противоопухолевую лекарственную терапию профилактическое ОВГМ уменьшает риск развития МГМ (при всех стадиях заболевания) и увеличивает общую выживаемость (при 1-2 стадии болезни).
Профилактическое ОВГМ у пациентов с МРЛ проводится в СОД 25 Гр за 10 ежедневных фракций. Короткий курс (20 Гр в 5 фракциях) может проводиться у пациентов с низким функциональным статусом и 3-4 стадией болезни.
У пациентов с метастазами МРЛ в головной мозг, как правило, рекомендуется проведение ОВГМ; однако в случае ограниченного метастатического поражения головного мозга может быть проведена стереотаксическая радиотерапия.
• При проведении ОВГМ рекомендуется применение мемантина (5 мг каждое утро; 2я неделя - 5 мг каждое утро и вечер; 3-я неделя - 10 мг каждое утро и 5 мг каждый вечер; 4я-24я недели по 10 мг утром и вечером) во время и после проведения ОВГМ, для уменьшения риска развития когнитивных нарушений [19].
Уровень убедительности рекомендаций в (уровень достоверности доказательств -2).
Комментарии. Альтернативной методикой, снижающей риск развития когнитивных расстройств, является проведение ОВГМ с применением IMRT/VIMAT методик с защитой гиппокампальных извилин с обеих сторон [20].
3,2,2 Противоопухолевое лекарственное лечение.
Противоопухолевое лекарственное лечение является основным для пациентов с метастазами в головном мозге. Целью противоопухолевого лекарственного лечения пациентов с МГМ является достижение контроля экстракраниальных очагов, профилактика развития новых (дистантных) МГМ, а также лечение первичных МГМ в отдельных клинических ситуациях [2, 21].Системное противоопухолевое лечение проводится в режимах, согласно рекомендациям по лечению первичного опухолевого очага с учетом биологических характеристик опухоли.
• Рекомендуется проведение системной противоопухолевой терапии (химиотерапия, таргетная терапия, иммунотерапия) в самостоятельном варианте лечения у пациентов с небольшими по размеру, бессимптомными МГМ при наличии в арсенале лечения препаратов с установленной эффективностью в головном мозге [21].
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 3).
Комментарии. Выбор схемы противоопухолевого лекарственного лечения пациента с метастатическим опухолевым процессом в головном мозге зависит, в первую очередь, от типа первичной опухоли, ее биологических характеристик и наличия препаратов с установленной эффективностью в головном мозге [2, 21].
Противоопухолевая лекарственная терапия в самостоятельном варианте лечения проводится только у пациентов с бессимптомным метастатическим поражением головного мозга и при наличии препаратов с установленной эффективностью в головном мозге. Во всех остальных случаях противоопухолевая лекарственная терапия проводится в соответствии с клиническими рекомендациями по лечению первичного опухолевого очага в комбинации с локальным лечением МГМ в соответствии с пунктом 4 текущих клинических рекомендаций.
В случае выявления МГМ на фоне стабилизации (или регрессии) экстракраниальных метастазов вследствие эффективной противоопухолевой лекарственной терапии, целесообразно проведение локального лечения МГМ в соответствии с пунктами 3,1-3,2 текущих клинических рекомендаций и сохранение режима проводимой противоопухолевой лекарственной терапии.
В случае выявления МГМ (или появления дистантных метастатических очагов в головном мозге) и прогрессирования экстракраниальных метастазов на фоне проведения противоопухолевой лекарственной терапии необходимо изменение режима лекарственного лечения. Предпочтение отдается препаратам с установленной противоопухолевой эффективностью в головном мозге.
В случае отсутствия таковых препаратов противоопухолевая лекарственная терапия проводится в соответствии с клиническими рекомендациями по лечению первичного опухолевого очага в комбинации с локальным лечением МГМ в соответствии с пунктами 3,1-3,2 текущих клинических рекомендаций.
Решение о начале или продолжении противоопухолевой лекарственной терапии после проведения локального лечения принимается индивидуально, однако целесообразно отложить ее начало до ликвидации/уменьшения проявлений постлучевых реакций и/или послеоперационных осложнений и прекращения (или снижения доз) стероидной терапии.
Нежелательно проведение иммунотерапии на фоне продолжающейся стероидной терапии в высоких дозах (>8 мг/сутки дексаметазона).
Возможно одновременное проведение таргетной терапии и радиотерапии у пациентов с хорошим функциональным статусам при условии адекватного мониторинга общего состояния пациента. В случае проведения цикловой химиотерапии возможно проведение радиохирургии между курсами проводимой противоопухолевой лекарственной терапии.
В случае проведения противоопухолевой лекарственной терапии в самостоятельном варианте лечения МРТ-мониторинг головного мозга проводится через 2 месяца от начала лекарственного лечения (или после 2-3-х курсов циклового лечения) для оценки эффективности проводимой терапии и своевременного проведения локального лечения МГМ соответствии с пунктом 3,1-3,2 текущих клинических рекомендаций в случае дальнейшей интракраниальной прогрессии.
• Рекомендуется проведение системной противоопухолевой терапии (химиотерапия, таргетная терапия, иммунотерапия) в самостоятельном варианте лечения или как компонент комбинированного (с лучевой терапией) лечения у пациентов с лептоменингиальными метастатическим поражением головного мозга [2, 4].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии.
Лечение проводится при наличии клинических и рентгенологических данных поражения лептоменингеальная оболочек и/или цитологического обнаружения опухолевых клеток в спинномозговой жидкости.
Целесообразно проведение стереотаксической радиотерапии на наиболее крупные опухолевые очаги с целью снижения неврологической симптоматики и сохранения качества жизни.
В случае исчерпанности резервов противоопухолевой лекарственной терапии возможно проведение интратекальной химиотерапии.
3,2,3 Стероидная и противоотечная терапия.
Целью стероидной терапии является временное облегчение клинической симптоматики, связанной с повышением внутричерепного давления вследствие перифокального отека вокруг метастатических очагов [22].• Не рекомендуется проведение стероидной терапии у пациентов с МГМ без клинической неврологической симптоматики [22].
Уровень убедительности рекомендаций С (уровень достоверности доказательств -5).
• У пациентов с МГМ и умеренно выраженными симптомами, связанными с масс-эффектом: рекомендуется проведение стероидной терапии (дексаметазон) для ликвидации или временного облегчения симптомов, связанных с повышением внутричерепного давления и вторичным отеком мозга. Начальная доза дексаметазона 4-8 мг/сутки [22].
Уровень убедительности рекомендаций С (уровень достоверности доказательств -5).
• У пациентов с МГМ и сильно выраженными симптомами, связанными с масс-эффектом. Рекомендуется назначение стероидной терапии (дексаметазон) для временного облегчения симптомов, связанных с повышением внутричерепного давления и вторичным отеком мозга. Начальная доза дексаметазона - от 12 мг/сутки [22].
Уровень убедительности рекомендаций С (уровень достоверности доказательств -5).
Комментарии. Дозы дексаметазона снижаются постепенно, в течение 2-х недель и более, основываясь на индивидуальной динамике клинической симптоматике и учитывая осложнения стероидной терапии. В отдельных клинических ситуациях возможно длительное/постоянное применение дексаметазона в минимально эффективных поддерживающих дозах (0,5-4 мг/сутки).
Снижение/отмена дозировки дексаметазона до хирургического удаления и/или проведения радиотерапии нецелесообразно.
Назначение и прием стероидных гормонов рекомендуется в 1-3 приема, перорально (при суточных дозах менее 4 мг) или внутримышечно, в соответствии с циркадным (солнечным) ритмом, с максимальными дозами в утренние часы, с последним приемом не позднее 16-17 часов.
• Рекомендуется проведение терапии бевацизумабом при наличии стойкого или нарастающего симптоматического отёка или радионекроза после проведения стереотаксической радиотерапии, резистентного к проводимой стероидной терапии [23-25] .
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - 4).
Комментарии: доза бевацизумаба составляет 7,5 мг/кг с интервалом 3 недели, не менее 4 введений, и проводится до регресса симптоматики или улучшения рентгенологической картины.
3,2,4 Противосудорожная терапия.
• В случаях наличия у пациентов эпилептического синдрома (в анамнезе) рекомендуется консультация врача-невролога с целью назначения/коррекции противосудорожной терапии [26].Уровень убедительности рекомендаций. С (уровень достоверности доказательств 5).
• Не рекомендуется профилактическое проведение противосудорожной терапии у пациентов без судорожного синдрома [26].
Уровень убедительности рекомендаций. С (уровень достоверности доказательств 5).
3,2,5 Паллиативная и симптоматическая терапия.
Сопроводительная терапия у пациентов с метастатическим поражением головного мозга проводится в соответствии с практическими рекомендациями общества клинической онкологии RUSSCO [28].• Проведение паллиативной терапии рекомендуется у пациентов с МГМ и/или с распространенным лептоменингиальными поражением головного мозга при наличии плохого прогноза общей выживаемости (индекс Карновского ≤70, ECOG 2-4, GPA 0-2 балла, множественными экстракраниальными метастазами, не контролируемыми проявлениями экстракраниальной болезни и с отсутствием резервов системного лечения) [4, 10, 27].
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - 5).
3,3 Лечение интракраниальных рецидивов.
• Рекомендуется проведение лечения интракраниальных рецидивов в соответствии с рекомендациями по лечению первично выявленных метастазов (пункты 4,1-4,5 текущих рекомендаций) [9, 29].Уровень убедительности рекомендаций С (уровень достоверности доказательств 5).
Комментарии. Объем лечения интракраниальных рецидивов определяется на совместном консилиуме врача онколога, радиотерапевта, нейрохирурга и проводится с учетом вида рецидива (дистантные метастазы и/или локальные рецидивы) и метода предшествующего лечения.
В случае развития интракраниальных рецидивов после ОВГМ рекомендуется проведение стереотаксической радиотерапии или нейрохирургического лечения.
В случае развития дистантных метастазов после нейрохирургического лечения и/или после стереотаксической радиотерапии лечение проводится также, как в случае первично-выявленных МГМ в соответствии с пунктами 3,1-3,2 текущих клинических рекомендаций.
При наличии локальных рецидивов после стереотаксической радиотерапии, возможно, проведения нейрохирургического лечения или повторной стереотаксической радиотерапии.
В случае проведения повторной стереотаксической радиотерапии дозы ионизирующего излучения назначаются строго индивидуально, исходя из объема рецидива, его локализации и наличия постлучевых осложнений. Лечение проводится на фоне стероидной терапии в соответствии с пунктом 3,5 текущих клинических рекомендаций.
|
|
Реабилитация и амбулаторное лечение
Целесообразно проведение реабилитационных мероприятий для восстановления неврологических функций в соответствии с клиническими рекомендациями по оказанию медицинской помощи пациентам с первичной опухолью.
В настоящее время для большинства видов медицинской реабилитации отсутствуют клинические исследования с участием пациентов с метастатическим поражением головного мозга. Имеющиеся данные систематических обзоров свидетельствуют о том, что различные виды медицинской реабилитации ускоряют функциональное восстановление, сокращают сроки пребывания в стационаре после операции и снижают частоту развития осложнений и летальных исходов у пациентов со злокачественными опухолями. Реабилитационные мероприятия у пациентов с метастазами в головной мозг проводятся после проведения локального лечения. Объем реабилитационных мероприятий определяется степенью выраженности неврологического дефицита и проводится в специализированных лечебно-реабилитационных отделениях по общим принципам реабилитации пациентов с неврологической патологией с учетом типа и особенностей заболевания.
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - 5).
• Рекомендуются психообразовательные мероприятия и психологическая поддержка (самодиагностика патологических психических реакций; способы совладания со стрессом; отслеживание взаимовлияния психических реакций и физического состояния), что может рассматриваться как основной механизм трансформации стрессовых событий в личный опыт, способствующий социальной и психической адаптации в условиях заболевания и лечения [30].
Уровень убедительности рекомендаций. С (уровень достоверности доказательств -5).
• Рекомендуется проводить прицельные психокоррекционные мероприятия психических реакций, ассоциированных с метастатическим поражением головного мозга (реакции по астено-тревожно-депрессивному типу, нарциссические реакции и пр.), что приводит к уменьшению тревожности, расстройств, связанных со здоровьем, а также приводит к положительным изменениям в борьбе с болезнью [30].
Уровень убедительности рекомендаций. С (уровень достоверности доказательств -5).
В настоящее время для большинства видов медицинской реабилитации отсутствуют клинические исследования с участием пациентов с метастатическим поражением головного мозга. Имеющиеся данные систематических обзоров свидетельствуют о том, что различные виды медицинской реабилитации ускоряют функциональное восстановление, сокращают сроки пребывания в стационаре после операции и снижают частоту развития осложнений и летальных исходов у пациентов со злокачественными опухолями. Реабилитационные мероприятия у пациентов с метастазами в головной мозг проводятся после проведения локального лечения. Объем реабилитационных мероприятий определяется степенью выраженности неврологического дефицита и проводится в специализированных лечебно-реабилитационных отделениях по общим принципам реабилитации пациентов с неврологической патологией с учетом типа и особенностей заболевания.
4,1 Принципы психологической реабилитации пациентов с метастатическим поражением головного мозга.
• Рекомендуется информировать пациентов о заболевании, психических реакциях; зоне ответственности в процессе лечения; способах коммуникации с родственниками, медицинским персоналом; способах получения дополнительной информации о своем заболевании или состоянии; способах получения социальной поддержки, что приводит к улучшению качества жизни и исхода заболевания [4, 30].Уровень убедительности рекомендаций. С (уровень достоверности доказательств - 5).
• Рекомендуются психообразовательные мероприятия и психологическая поддержка (самодиагностика патологических психических реакций; способы совладания со стрессом; отслеживание взаимовлияния психических реакций и физического состояния), что может рассматриваться как основной механизм трансформации стрессовых событий в личный опыт, способствующий социальной и психической адаптации в условиях заболевания и лечения [30].
Уровень убедительности рекомендаций. С (уровень достоверности доказательств -5).
• Рекомендуется проводить прицельные психокоррекционные мероприятия психических реакций, ассоциированных с метастатическим поражением головного мозга (реакции по астено-тревожно-депрессивному типу, нарциссические реакции и пр.), что приводит к уменьшению тревожности, расстройств, связанных со здоровьем, а также приводит к положительным изменениям в борьбе с болезнью [30].
Уровень убедительности рекомендаций. С (уровень достоверности доказательств -5).
Профилактика
• Рекомендуется после проведения лечения по поводу метастатического поражения головного мозга проводить обследование пациента с целью своевременного выявления рецидива заболевания с проведением МРТ головного мозга с контрастированием со следующей периодичностью: в первые 2 года - каждые 3 месяца, в дальнейшем - 1 раз в 6 месяцев при отсутствии признаков экстра- и интра- кранильной прогрессии [2, 4].
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - 5).
Комментарии. У пациентов с высоким риском интракраниального рецидива перерыв между обследованиями может быть сокращен. Обследование на наличие экстракраниальных метастазов проводится в соответствии с первичным очагом [1].
Задачей наблюдения является раннее выявление прогрессирования заболевания с целью раннего начала лучевого, лекарственного или хирургического лечения интракраниальных рецидивов.
При возникновении неврологической симптоматики в случае наблюдения пациента в центре амбулаторной онкологической помощи (либо в первичном онкологическом кабинете, онкологическом отделении или поликлиническом отделении онкологического диспансера) необходимо проведение консультации невролога (нейрохирурга) и офтальмолога (при наличии показаний).
Уровень убедительности рекомендаций. С (уровень достоверности доказательств - 5).
Комментарии. У пациентов с высоким риском интракраниального рецидива перерыв между обследованиями может быть сокращен. Обследование на наличие экстракраниальных метастазов проводится в соответствии с первичным очагом [1].
Задачей наблюдения является раннее выявление прогрессирования заболевания с целью раннего начала лучевого, лекарственного или хирургического лечения интракраниальных рецидивов.
При возникновении неврологической симптоматики в случае наблюдения пациента в центре амбулаторной онкологической помощи (либо в первичном онкологическом кабинете, онкологическом отделении или поликлиническом отделении онкологического диспансера) необходимо проведение консультации невролога (нейрохирурга) и офтальмолога (при наличии показаний).
Организация оказания медицинской помощи
Медицинская помощь, за исключением медицинской помощи в рамках клинической апробации, в соответствии с федеральным законом от 21,11,2011 №323-ФЗ (ред. От 25,05,2019) «Об основах охраны здоровья граждан в Российской Федерации», организуется и оказывается:
• в соответствии с положением об организации оказания медицинской помощи по видам медицинской помощи, которое утверждается уполномоченным федеральным органом исполнительной власти;
• в соответствии с порядком оказания помощи по профилям «онкология», «нейрохирургия», «радиотерапия» обязательными для исполнения на территории Российской Федерации всеми медицинскими организациями на основе настоящих клинических рекомендаций;
• с учетом стандартов медицинской помощи, утвержденных уполномоченным федеральным органом исполнительной власти.
Первичная специализированная медико-санитарная помощь онкологическим пациентам оказывается врачом-онкологом и иными врачами-специалистами в центре амбулаторной онкологической помощи либо в первичном онкологическом кабинете, первичном онкологическом отделении, поликлиническом отделении онкологического диспансера.
В случае манифестации онкологического заболевания с неврологической симптоматики или в случае ее развития в процессе лечения онкологического заболевания пациент должен быть осмотрен врачом-неврологом (нейрохирургом) с последующим направлением на проведение МРТ головного мозга с контрастированием (или КТ головного мозга с контрастированием в случае наличия противопоказаний к проведению МРТ).
В случае клинико-рентгенологического подтверждения метастатического поражения ГМ пациентов переводят или направляют в медицинские организации, оказывающие медицинскую помощь пациентам по профилю «нейрохирургия», «онкология», для определения тактики лечения и необходимости применения дополнительно других методов специализированного противоопухолевого лечения.
Специализированная, в том числе высокотехнологичная, медицинская помощь пациентам с метастатическим поражением головного мозга оказывается врачами: нейрохирургом, онкологом, радиотерапевтом в онкологическом диспансере или в других медицинских организациях, оказывающих медицинскую помощь больным с метастатическим поражением головного мозга, имеющих лицензию, необходимую материально-техническую базу, сертифицированных специалистов, в условиях стационара (дневного или круглосуточного) и амбулаторных условиях и включает в себя профилактику, диагностику, лечение онкологических заболеваний, требующих использования специальных методов и сложных уникальных медицинских технологий, а также медицинскую реабилитацию.
Тактика медицинского обследования и лечения пациентов с метастатическим поражением головного мозга устанавливается консилиумом врачей: нейрохирурга, онколога и радиотерапевта с привлечением, при необходимости, других врачей-специалистов. Решение консилиума врачей оформляется протоколом, участниками консилиума врачей и вносится в медицинскую документацию пациента.
После завершения каждого этапа специализированного лечения пациент направляется с рекомендациями по проведению специфического противоопухолевого лечения в центр амбулаторной онкологической помощи либо в первичный онкологический кабинет, первичное онкологическое отделение, поликлиническое отделение онкологического диспансера.
• наличие осложнений лечения (хирургического, лучевого, лекарственного ) у пациентов с метастазами в головном мозге, требующей оказания медицинской помощи в экстренной и неотложной форме.
• наличие показаний к специализированному лечению (хирургическое лучевое, лекарственное), требующему наблюдения в условиях круглосуточного или дневного стационара.
• документально зарегистрированный отказ пациента или его законного представителя от специализированной, в том числе высокотехнологичной, медицинской помощи в условиях круглосуточного или дневного стационаров, установленной консилиумом медицинской организации, оказывающей онкологическую помощь.
• необходимость перевода пациента в другую медицинскую организацию по соответствующему профилю оказания медицинской помощи. Заключение о целесообразности перевода пациента в профильную медицинскую организацию осуществляется после предварительной консультации по предоставленным медицинским документам и/или данным предварительного осмотра пациента врачами специалистами медицинской организации, в которую планируется перевод.
• проведение стероидной терапии в случае наличия показаний;
• направление на проведение КТ, МРТ, ПЭТ при наличии показаний;
• проведение таргетной терапии при наличии соответствующих показаний.
• клинические рекомендации не позволяют описать все многообразие реальной клинической практики и охватывают лишь наиболее частые и типовые клинические ситуации. Если практикующий врач или медицинская организация сталкивается с клинической ситуацией, не имеющей соответствующего отражения в настоящей клинической рекомендации, рекомендуется воспользоваться системой телемедицинских консультаций или маршрутизации в федеральные и национальные медицинские исследовательские центры для уточнения тактики лечения;
• выявление клинических ситуаций или обострение сопутствующей патологии, не относящейся к профилю онкологического учреждения, которая препятствует проведению данного этапа лечения (например, острый инфаркт миокарда, острое нарушение мозгового кровообращения, необходимость проведения нейрохирургического лечения ) требует маршрутизации в профильные медицинские организации.
• в соответствии с положением об организации оказания медицинской помощи по видам медицинской помощи, которое утверждается уполномоченным федеральным органом исполнительной власти;
• в соответствии с порядком оказания помощи по профилям «онкология», «нейрохирургия», «радиотерапия» обязательными для исполнения на территории Российской Федерации всеми медицинскими организациями на основе настоящих клинических рекомендаций;
• с учетом стандартов медицинской помощи, утвержденных уполномоченным федеральным органом исполнительной власти.
Первичная специализированная медико-санитарная помощь онкологическим пациентам оказывается врачом-онкологом и иными врачами-специалистами в центре амбулаторной онкологической помощи либо в первичном онкологическом кабинете, первичном онкологическом отделении, поликлиническом отделении онкологического диспансера.
В случае манифестации онкологического заболевания с неврологической симптоматики или в случае ее развития в процессе лечения онкологического заболевания пациент должен быть осмотрен врачом-неврологом (нейрохирургом) с последующим направлением на проведение МРТ головного мозга с контрастированием (или КТ головного мозга с контрастированием в случае наличия противопоказаний к проведению МРТ).
В случае клинико-рентгенологического подтверждения метастатического поражения ГМ пациентов переводят или направляют в медицинские организации, оказывающие медицинскую помощь пациентам по профилю «нейрохирургия», «онкология», для определения тактики лечения и необходимости применения дополнительно других методов специализированного противоопухолевого лечения.
Специализированная, в том числе высокотехнологичная, медицинская помощь пациентам с метастатическим поражением головного мозга оказывается врачами: нейрохирургом, онкологом, радиотерапевтом в онкологическом диспансере или в других медицинских организациях, оказывающих медицинскую помощь больным с метастатическим поражением головного мозга, имеющих лицензию, необходимую материально-техническую базу, сертифицированных специалистов, в условиях стационара (дневного или круглосуточного) и амбулаторных условиях и включает в себя профилактику, диагностику, лечение онкологических заболеваний, требующих использования специальных методов и сложных уникальных медицинских технологий, а также медицинскую реабилитацию.
Тактика медицинского обследования и лечения пациентов с метастатическим поражением головного мозга устанавливается консилиумом врачей: нейрохирурга, онколога и радиотерапевта с привлечением, при необходимости, других врачей-специалистов. Решение консилиума врачей оформляется протоколом, участниками консилиума врачей и вносится в медицинскую документацию пациента.
После завершения каждого этапа специализированного лечения пациент направляется с рекомендациями по проведению специфического противоопухолевого лечения в центр амбулаторной онкологической помощи либо в первичный онкологический кабинет, первичное онкологическое отделение, поликлиническое отделение онкологического диспансера.
6,1 Показанием для госпитализации в медицинскую организацию в экстренной или неотложной форме является:
• наличие метастатического поражения головного мозга с соответствующей клинической симптоматикой, требующей оказания медицинской помощи в экстренной и неотложной форме;• наличие осложнений лечения (хирургического, лучевого, лекарственного ) у пациентов с метастазами в головном мозге, требующей оказания медицинской помощи в экстренной и неотложной форме.
6,2 Показанием для госпитализации в медицинскую организацию в плановой форме является:
• необходимость выполнения сложных интервенционных диагностических медицинских вмешательств, требующих последующего наблюдения в условиях круглосуточного или дневного стационаров;• наличие показаний к специализированному лечению (хирургическое лучевое, лекарственное), требующему наблюдения в условиях круглосуточного или дневного стационара.
6,3 Показанием к выписке пациента из медицинской организации является:
• завершение курса лечения или одного из этапов оказания специализированной, в том числе высокотехнологичной, медицинской помощи в условиях круглосуточного или дневного стационаров при условиях отсутствия осложнений лечения, требующих медикаментозной коррекции и/или медицинских вмешательств в условиях стационара (круглосуточного или дневного);• документально зарегистрированный отказ пациента или его законного представителя от специализированной, в том числе высокотехнологичной, медицинской помощи в условиях круглосуточного или дневного стационаров, установленной консилиумом медицинской организации, оказывающей онкологическую помощь.
• необходимость перевода пациента в другую медицинскую организацию по соответствующему профилю оказания медицинской помощи. Заключение о целесообразности перевода пациента в профильную медицинскую организацию осуществляется после предварительной консультации по предоставленным медицинским документам и/или данным предварительного осмотра пациента врачами специалистами медицинской организации, в которую планируется перевод.
6,4 Медицинские процедуры, которые могут быть оказаны в рамках первичной специализированной медицинской помощи (т, е, амбулаторно) под контролем врача-онколога:
• организация консультаций профильных врачей-специалистов;• проведение стероидной терапии в случае наличия показаний;
• направление на проведение КТ, МРТ, ПЭТ при наличии показаний;
• проведение таргетной терапии при наличии соответствующих показаний.
6,5 Показания для направления пациента в другую медицинскую организацию:
• При отсутствии в медицинской организации возможности проведения рекомендуемого объема медицинской помощи пациентам с метастатическим поражением головного мозга, рекомендуется воспользоваться системой маршрутизации в другие медицинские организации, в том числе за пределы субъекта федерации, в том числе в федеральные центры, имеющие соответствующую оснащенность и кадры;• клинические рекомендации не позволяют описать все многообразие реальной клинической практики и охватывают лишь наиболее частые и типовые клинические ситуации. Если практикующий врач или медицинская организация сталкивается с клинической ситуацией, не имеющей соответствующего отражения в настоящей клинической рекомендации, рекомендуется воспользоваться системой телемедицинских консультаций или маршрутизации в федеральные и национальные медицинские исследовательские центры для уточнения тактики лечения;
• выявление клинических ситуаций или обострение сопутствующей патологии, не относящейся к профилю онкологического учреждения, которая препятствует проведению данного этапа лечения (например, острый инфаркт миокарда, острое нарушение мозгового кровообращения, необходимость проведения нейрохирургического лечения ) требует маршрутизации в профильные медицинские организации.
|
|
Дополнительно
Пациенты с МГМ является гетерогенной группой пациентов с различными клинико-биологическими характеристиками опухоли и показателями общей выживаемости. Поэтому важно учитывать различные клинические факторы, влияющие на прогноз пациентов с МГМ до принятия лечебных решений.
Понятие «прогностический фактор» определяется как клиническая ситуация, которая может использоваться для оценки вероятности выздоровления или вероятности рецидива болезни (National Institutes of Health et al. National сancer Institute. NCI Dictionary of сancer Terms., 2015).
Многочисленные исследования, хотя и ретроспективные по своей природе, выявили различные прогностические факторы и позволили сформировать различные прогностические инструменты (шкалы) для прогноза общей выживаемости у пациентов с МГМ.
В настоящее время оптимальной прогностической шкалой является диагноз адаптированная шкала, позволяющая оценить прогноз общей выживаемости пациентов в зависимости от ряда факторов, которые различаются у пациентов с различным типом первичной опухоли. Имеется возможность определить прогноз общей выживаемости с использованием онлайн-калькулятора (http://brainmetgpa.com/) [32].
Понятие «прогностический фактор» определяется как клиническая ситуация, которая может использоваться для оценки вероятности выздоровления или вероятности рецидива болезни (National Institutes of Health et al. National сancer Institute. NCI Dictionary of сancer Terms., 2015).
Многочисленные исследования, хотя и ретроспективные по своей природе, выявили различные прогностические факторы и позволили сформировать различные прогностические инструменты (шкалы) для прогноза общей выживаемости у пациентов с МГМ.
В настоящее время оптимальной прогностической шкалой является диагноз адаптированная шкала, позволяющая оценить прогноз общей выживаемости пациентов в зависимости от ряда факторов, которые различаются у пациентов с различным типом первичной опухоли. Имеется возможность определить прогноз общей выживаемости с использованием онлайн-калькулятора (http://brainmetgpa.com/) [32].
Критерии оценки качества медицинской помощи
| № | Критерии качества | Оценка выполнения |
| Этап постановки диагноза | ||
| 1 | Выполнено МРТ исследование головного мозга с контрастным усилением в соответствии с текущими рекомендациями | Да/нет |
| 2 | Выполнен осмотр врачом-нейрохирургом, врачом-онкологом, врачом-радиотерапевтом в соответствии с текущими рекомендациями | Да/нет |
| 3 | Проведено обследование пациента в соответствии с клиническими рекомендациями по лечению первичной опухоли | Да/нет |
| Этап лечения | ||
| 1 | Назначена стероидная терапия (при наличии показаний) в соответствии с текущими рекомендациями | Да/нет |
| 2 | Проведено хирургическое лечение (при наличии показаний) | Да/нет |
| 3 | Проведено облучение всего головного мозга (при наличии показаний), как метода первичного лечения) | Да/нет |
| 4 | Проведена стереотаксическая радиотерапия (при наличии показаний), как метода первичного лечения) | Да/нет |
| Проведено гистологическое, иммуногистохимическое и молекулярно-биологическое исследование в случае проведения нейрохирургического лечения | ||
| 5 | Проведено противоопухолевое лекарственное лечение в соответствии с текущими рекомендациями | Да/нет |
| Этап контроля эффективности лечения | ||
| 1 | Выполнено МРТ исследование головного мозга с контрастным усилением после окончания лечения в соответствии с текущими рекомендациями | Да/нет |
| 2 | Проведено обследование пациента в соответствии с клиническими рекомендациями по лечению первичной опухоли | Да/нет |
| Этап проведения сопроводительной терапии | ||
| 1 | Проведена сопроводительная терапия при наличии показаний в соответствия с рекомендациями Российского общества клинической онкологии (RUSSCO) | Да/нет |
Список литературы
1. вhangoo, S.S. Evidence-based guidelines for the management of brain metastases / S.S. вhangoo, M.E. Linskey, S.N. Kalkanis // Neurosurgery clinics of North America. 2011. Vol. 22, №1. 97-104, viii.
2. National сomprehensive сancer Network. сentral Nervous System сancers. Version 3,2019 - November 11, 2019. National сomprehensive сancer Network. - https://www.nccn.org/professionals/physician_gls/default.aspx.
3. Долгушин, М.Б. Метастазы в головном мозге / М.Б. Долгушин, В.Н. Корниенко, И.Н. Пронин. Москва: ИП Т.А. Алексеева , 2017.
4. EANO-ESMO сlinical Practice Guidelines for diagnosis, treatment and follow-up of patients with leptomeningeal metastasis from solid tumours / E. Le Rhun, M. Weller, D. вrandsma, M. van den вent, E. de Azambuja, R. Henriksson, T. вoulanger, S. Peters, с. Watts, W. Wick, P. Wesseling, R. Rudà, M. Preusser // Annals of oncology : official journal of the European Society for Medical Oncology. 2017. Vol. 28, №suppl_4. - iv84-iv99.
5. New response evaluation criteria in solid tumours: revised RECIST guideline (version 1,1) / E.A. Eisenhauer, P. Therasse, J. вogaerts, L.H. Schwartz, D. Sargent, R. Ford, J. Dancey, S. Arbuck, S. Gwyther, M. Mooney, L. Rubinstein, L. Shankar, L. Dodd, R. Kaplan, D. Lacombe, J. Verweij // European journal of cancer (Oxford, England : 1990). 2009. Vol. 45, №2. P.228-247.
6. Vogelbaum, M.A. Resectable brain metastases / M.A. Vogelbaum, J.H. Suh // Journal of clinical oncology : official journal of the American Society of сlinical Oncology. 2006. Vol. 24, №8. P.1289-1294.
7. сongress of Neurological Surgeons Systematic Review and Evidence-Based Guidelines on the Role of Surgery in the Management of Adults With Metastatic вrain Tumors / в.V. Nahed, с. Alvarez-Breckenridge, P.K. вrastianos, H. Shih, A. Sloan, M. Ammirati, J.S. Kuo, T.C. Ryken, S.N. Kalkanis, J.J. Olson // Neurosurgery. 2019. Vol. 84, №3. E152-E155.
8. The role of surgery in the management of patients with diffuse low grade glioma: A systematic review and evidence-based clinical practice guideline / M.K. Aghi, в.V. Nahed, A.E. Sloan, T.C. Ryken, S.N. Kalkanis, J.J. Olson // Journal of neuro-oncology. 2015. Vol. 125, №3. P.503-530.
9. Results of surgical resection for progression of brain metastases previously treated by gamma knife radiosurgery / M.T. Truong, E.G. St сlair, в.R. Donahue, S.C. Rush, D.C. Miller, S.C. Formenti, E.A. Knopp, K. Han, J.G. Golfinos // Neurosurgery. 2006. Vol. 59, №1. 86-97; discussion 86-97.
10. Tsao, M.N. вrain metastases: advances over the decades / M.N. Tsao // Annals of palliative medicine. 2015. Vol. 4, №4. P.225-232.
11. Graber, J.J. Leptomeningeal Metastases / J.J. Graber, S. Kesari // сurrent treatment options in oncology. 2018. Vol. 19, №1. P.3.
12. сongress of Neurological Surgeons Systematic Review and Evidence-Based Guidelines on the Role of Whole вrain Radiation Therapy in Adults With Newly Diagnosed Metastatic вrain Tumors / L.E. Gaspar, R.S. Prabhu, A. Hdeib, D.J. McCracken, G.F. Lasker, M.W. McDermott, S.N. Kalkanis, J.J. Olson // Neurosurgery. 2019. Vol. 84, №3. E159-E162.
13. Single dose radiosurgical treatment of recurrent previously irradiated primary brain tumors and brain metastases: final report of RTOG protocol 90-05 / E. Shaw, с. Scott, L. Souhami, R. Dinapoli, R. Kline, J. Loeffler, N. Farnan // International Journal of Radiation Oncology*Biology*Physics. 2000. Т.47, №2. - с.291-298.
14. Sujith вaliga,Madhur K Garg,Jana Fox,Shalom Kalnicki,Patrick A Lasala,Mary R Welch,Wolfgang A Tomé,Nitin Ohri. Fractionated stereotactic radiation therapy for brain metastases: a systematic review with tumour control probability modelling / Sujith вaliga,Madhur K Garg,Jana Fox,Shalom Kalnicki,Patrick A Lasala,Mary R Welch,Wolfgang A Tomé,Nitin Ohri // The вritish journal of radiology. 2017. Т.90, №1070.
15. Postoperative Fractionated Stereotactic Radiosurgery to the Tumor вed for Surgically Resected вrain Metastases / R.K. сleary, J. Meshman, M. Dewan, L. Du, A.J. сmelak, G. Luo, M. Morales-Paliza, K. Weaver, R. Thompson, L.B. сhambless, A. Attia // сureus. 2017. Vol. 9, №5. - e1279.
16. International practice survey on the management of brain metastases: Third International сonsensus Workshop on Palliative Radiotherapy and Symptom сontrol / M.N. Tsao, D. Rades, A. Wirth, S.S. Lo, в.L. Danielson, A. Vichare, с. Hahn, E.L. сhang // сlinical oncology (Royal сollege of Radiologists (Great вritain)). 2012. Vol. 24, №6. - e81-92.
17. Stereotactic radiosurgery for patients with multiple brain metastases (JLGK0901): a multi-institutional prospective observational study / M. Yamamoto, T. Serizawa, T. Shuto, A. Akabane, Y. Higuchi, J. Kawagishi, K. Yamanaka, Y. Sato, H. Jokura, S. Yomo, O. Nagano, H. Kenai, A. Moriki, S. Suzuki, Y. Kida, Y. Iwai, M. Hayashi, H. Onishi, M. Gondo, M. Sato, T. Akimitsu, K. Kubo, Y. Kikuchi, T. Shibasaki, T. Goto, M. Takanashi, Y. Mori, K. Takakura, N. Saeki, E. Kunieda [et al. The Lancet. Oncology. 2014. Vol. 15, №4. P.387-395.
18. Aizer, A.A. Prophylactic cranial irradiation in patients with extensive-stage small cell lung cancer / A.A. Aizer, R. Mak, в.M. Alexander // Neuro-oncology. 2017. Vol. 19, №8. P.1015-1016.
19. Memantine for the prevention of cognitive dysfunction in patients receiving whole-brain radiotherapy: a randomized, double-blind, placebo-controlled trial / P.D. вrown, S. Pugh, N.N. Laack, J.S. Wefel, D. Khuntia, с. Meyers, A. сhoucair, S. Fox, J.H. Suh, D. Roberge, V. Kavadi, S.M. вentzen, M.P. Mehta, D. Watkins-Bruner // Neuro-oncology. 2013. Vol. 15, №10. P.1429-1437.
20. Preservation of memory with conformal avoidance of the hippocampal neural stem-cell compartment during whole-brain radiotherapy for brain metastases (RTOG 0933): a phase II multi-institutional trial / V. Gondi, S.L. Pugh, W.A. Tome, с. сaine, в. сorn, A. Kanner, H. Rowley, V. Kundapur, A. DeNittis, J.N. Greenspoon, A.A. Konski, G.S. вauman, S. Shah, W. Shi, M. Wendland, L. Kachnic, M.P. Mehta // Journal of clinical oncology : official journal of the American Society of сlinical Oncology. 2014. Vol. 32, №34. P.3810-3816.
21. Diagnosis and treatment of brain metastases from solid tumors: guidelines from the European Association of Neuro-Oncology (EANO) / R. Soffietti, U. Abacioglu, в. вaumert, S.E. сombs, S. Kinhult, J.M. Kros, с. Marosi, P. Metellus, A. Radbruch, S.S. Villa Freixa, M. вrada, с.M. сarapella, M. Preusser, E. Le Rhun, R. Rudà, J.C. Tonn, D.C. Weber, M. Weller // Neuro-oncology. 2017. Vol. 19, №2. P.162-174.
22. сongress of Neurological Surgeons Systematic Review and Evidence-Based Guidelines on the Role of Steroids in the Treatment of Adults With Metastatic вrain Tumors / T.C. Ryken, J.S. Kuo, R.S. Prabhu, J.H. Sherman, S.N. Kalkanis, J.J. Olson // Neurosurgery. 2019. Vol. 84, №3. E189-E191.
23. вevacizumab safety in patients with central nervous system metastases / в. вesse, S.F. Lasserre, P. сompton, J. Huang, S. Augustus, U.-P. Rohr // сlinical cancer research : an official journal of the American Association for сancer Research. 2010. Vol. 16, №1. P.269-278.
24. вevacizumab as a treatment for radiation necrosis of brain metastases post stereotactic radiosurgery / D. вoothe, R. Young, Y. Yamada, A. Prager, T. сhan, K. вeal // Neuro-oncology. 2013. Vol. 15, №9. P.1257-1263.
25. вevacizumab treatment for radiation brain necrosis: mechanism, efficacy and issues / H. Zhuang, S. Shi, Z. Yuan, J.Y. сhang // Molecular cancer. 2019. Vol. 18, №1. P.21.
26. сhen, с.C. сongress of Neurological Surgeons Systematic Review and Evidence-Based Guidelines on the Role of Prophylactic Anticonvulsants in the Treatment of Adults with Metastatic вrain Tumors / с.C. сhen, R.C. Rennert, J.J. Olson // Neurosurgery. 2019. Vol. 84, №3. E195-E197.
27. Dexamethasone and supportive care with or without whole brain radiotherapy in treating patients with non-small cell lung cancer with brain metastases unsuitable for resection or stereotactic radiotherapy (QUARTZ): results from a phase 3, non-inferiority, randomised trial / P. Mulvenna, M. Nankivell, R. вarton, с. Faivre-Finn, P. Wilson, E. McColl, в. Moore, I. вrisbane, D. Ardron, T. Holt, S. Morgan, с. Lee, K. Waite, N. вayman, с. Pugh, в. Sydes, R. Stephens, M.K. Parmar, R.E. Langley // The Lancet. 2016. Т.388, №10055. - с.2004-2014.
28. RUSSCO. Рекомендации по поддерживающей и сопроводительной терапии RUSSCO. - https://rosoncoweb.ru/standarts/suptherapy/2018/.
29. The treatment of recurrent brain metastases with stereotactic radiosurgery / J.S. Loeffler, H.M. Kooy, P.Y. Wen, H.A. Fine, с.W. сheng, E.G. Mannarino, J.S. Tsai, E. Alexander // Journal of clinical oncology : official journal of the American Society of сlinical Oncology. 1990. Vol. 8, №4. P.576-582.
30. А.М. Беляев, В.А. Чулкова, Т.Ю. Семиглазова, М.В. Рогачев. Онкопсихология для врачей-онкологов и медицинских психологов / А.М. Беляев, В.А. Чулкова, Т.Ю. Семиглазова, М.В. Рогачев. Санкт Питербург: Ассоциация онкологов Северо-Западного федерального округа, 2017. 352 c.
31. Ostrom, Q.T. вrain metastases: epidemiology / Q.T. Ostrom, с.H. Wright, J.S. вarnholtz-Sloan // Handbook of clinical neurology. 2018. Vol. 149. P.27-42.
32. Diagnosis-specific prognostic factors, indexes, and treatment outcomes for patients with newly diagnosed brain metastases: a multi-institutional analysis of 4,259 patients / P.W. Sperduto, S.T. сhao, P.K. Sneed, X. Luo, J. Suh, D. Roberge, A. вhatt, A.W. Jensen, P.D. вrown, H. Shih, J. Kirkpatrick, A. Schwer, L.E. Gaspar, J.B. Fiveash, V. сhiang, J. Knisely, с.M. Sperduto, M. Mehta // International journal of radiation oncology, biology, physics. 2010. Vol. 77, №3. P.655-661.
33. вerghoff, A.S. Targeted Therapies for Melanoma вrain Metastases / A.S. вerghoff, M. Preusser // сurrent treatment options in neurology. 2017. Vol. 19, №4. P.13.
34. Pharmacotherapeutic options for treating brain metastases in non-small cell lung cancer / G. Metro, R. сhiari, в. Ricciuti, A. Rebonato, M. Lupattelli, S. Gori, с. вennati, с. сastrioto, P. Floridi, V. Minotti, P. сhiarini, L. сrinò // Expert opinion on pharmacotherapy. 2015. Vol. 16, №17. P.2601-2613.
35. Targeted drugs for systemic therapy of lung cancer with brain metastases / Y.-W. Sun, J. Xu, J. Zhou, W.-J. Liu // Oncotarget. 2018. Vol. 9, №4. P.5459-5472.
36. EANO guidelines for the diagnosis and treatment of ependymal tumors / R. Rudà, G. Reifenberger, D. Frappaz, S.M. Pfister, A. Laprie, T. Santarius, P. Roth, J.C. Tonn, R. Soffietti, M. Weller, E.C.-J. Moyal // Neuro-oncology. 2018. Vol. 20, №4. P.445-456.
37. вates S.E. сentral nervous system metastasis from breast cancer / вates S.E. The oncologist. 2015. Т.20, №1. - с.3-4.
38. Patil, A. Therapeutic approach to the management of HER2-positive breast cancer metastatic to the brain / A. Patil, G.V. Sherbet // сancer letters. 2015. Vol. 358, №2. P.93-99.
39. Leone, J.P. Systemic Therapy of сentral Nervous System Metastases of вreast сancer / J.P. Leone, N.U. Lin // сurrent oncology reports. 2019. Vol. 21, №6. P.49.
40. The effect of targeted agents on outcomes in patients with brain metastases from renal cell carcinoma treated with Gamma Knife surgery / D.C. сochran, M.D. сhan, M. Aklilu, J.F. Lovato, N.K. Alphonse, J.D. вourland, J.J. Urbanic, K.P. McMullen, E.G. Shaw, S.B. Tatter, T.L. Ellis // Journal of neurosurgery. 2012. Vol. 116, №5. P.978-983.
2. National сomprehensive сancer Network. сentral Nervous System сancers. Version 3,2019 - November 11, 2019. National сomprehensive сancer Network. - https://www.nccn.org/professionals/physician_gls/default.aspx.
3. Долгушин, М.Б. Метастазы в головном мозге / М.Б. Долгушин, В.Н. Корниенко, И.Н. Пронин. Москва: ИП Т.А. Алексеева , 2017.
4. EANO-ESMO сlinical Practice Guidelines for diagnosis, treatment and follow-up of patients with leptomeningeal metastasis from solid tumours / E. Le Rhun, M. Weller, D. вrandsma, M. van den вent, E. de Azambuja, R. Henriksson, T. вoulanger, S. Peters, с. Watts, W. Wick, P. Wesseling, R. Rudà, M. Preusser // Annals of oncology : official journal of the European Society for Medical Oncology. 2017. Vol. 28, №suppl_4. - iv84-iv99.
5. New response evaluation criteria in solid tumours: revised RECIST guideline (version 1,1) / E.A. Eisenhauer, P. Therasse, J. вogaerts, L.H. Schwartz, D. Sargent, R. Ford, J. Dancey, S. Arbuck, S. Gwyther, M. Mooney, L. Rubinstein, L. Shankar, L. Dodd, R. Kaplan, D. Lacombe, J. Verweij // European journal of cancer (Oxford, England : 1990). 2009. Vol. 45, №2. P.228-247.
6. Vogelbaum, M.A. Resectable brain metastases / M.A. Vogelbaum, J.H. Suh // Journal of clinical oncology : official journal of the American Society of сlinical Oncology. 2006. Vol. 24, №8. P.1289-1294.
7. сongress of Neurological Surgeons Systematic Review and Evidence-Based Guidelines on the Role of Surgery in the Management of Adults With Metastatic вrain Tumors / в.V. Nahed, с. Alvarez-Breckenridge, P.K. вrastianos, H. Shih, A. Sloan, M. Ammirati, J.S. Kuo, T.C. Ryken, S.N. Kalkanis, J.J. Olson // Neurosurgery. 2019. Vol. 84, №3. E152-E155.
8. The role of surgery in the management of patients with diffuse low grade glioma: A systematic review and evidence-based clinical practice guideline / M.K. Aghi, в.V. Nahed, A.E. Sloan, T.C. Ryken, S.N. Kalkanis, J.J. Olson // Journal of neuro-oncology. 2015. Vol. 125, №3. P.503-530.
9. Results of surgical resection for progression of brain metastases previously treated by gamma knife radiosurgery / M.T. Truong, E.G. St сlair, в.R. Donahue, S.C. Rush, D.C. Miller, S.C. Formenti, E.A. Knopp, K. Han, J.G. Golfinos // Neurosurgery. 2006. Vol. 59, №1. 86-97; discussion 86-97.
10. Tsao, M.N. вrain metastases: advances over the decades / M.N. Tsao // Annals of palliative medicine. 2015. Vol. 4, №4. P.225-232.
11. Graber, J.J. Leptomeningeal Metastases / J.J. Graber, S. Kesari // сurrent treatment options in oncology. 2018. Vol. 19, №1. P.3.
12. сongress of Neurological Surgeons Systematic Review and Evidence-Based Guidelines on the Role of Whole вrain Radiation Therapy in Adults With Newly Diagnosed Metastatic вrain Tumors / L.E. Gaspar, R.S. Prabhu, A. Hdeib, D.J. McCracken, G.F. Lasker, M.W. McDermott, S.N. Kalkanis, J.J. Olson // Neurosurgery. 2019. Vol. 84, №3. E159-E162.
13. Single dose radiosurgical treatment of recurrent previously irradiated primary brain tumors and brain metastases: final report of RTOG protocol 90-05 / E. Shaw, с. Scott, L. Souhami, R. Dinapoli, R. Kline, J. Loeffler, N. Farnan // International Journal of Radiation Oncology*Biology*Physics. 2000. Т.47, №2. - с.291-298.
14. Sujith вaliga,Madhur K Garg,Jana Fox,Shalom Kalnicki,Patrick A Lasala,Mary R Welch,Wolfgang A Tomé,Nitin Ohri. Fractionated stereotactic radiation therapy for brain metastases: a systematic review with tumour control probability modelling / Sujith вaliga,Madhur K Garg,Jana Fox,Shalom Kalnicki,Patrick A Lasala,Mary R Welch,Wolfgang A Tomé,Nitin Ohri // The вritish journal of radiology. 2017. Т.90, №1070.
15. Postoperative Fractionated Stereotactic Radiosurgery to the Tumor вed for Surgically Resected вrain Metastases / R.K. сleary, J. Meshman, M. Dewan, L. Du, A.J. сmelak, G. Luo, M. Morales-Paliza, K. Weaver, R. Thompson, L.B. сhambless, A. Attia // сureus. 2017. Vol. 9, №5. - e1279.
16. International practice survey on the management of brain metastases: Third International сonsensus Workshop on Palliative Radiotherapy and Symptom сontrol / M.N. Tsao, D. Rades, A. Wirth, S.S. Lo, в.L. Danielson, A. Vichare, с. Hahn, E.L. сhang // сlinical oncology (Royal сollege of Radiologists (Great вritain)). 2012. Vol. 24, №6. - e81-92.
17. Stereotactic radiosurgery for patients with multiple brain metastases (JLGK0901): a multi-institutional prospective observational study / M. Yamamoto, T. Serizawa, T. Shuto, A. Akabane, Y. Higuchi, J. Kawagishi, K. Yamanaka, Y. Sato, H. Jokura, S. Yomo, O. Nagano, H. Kenai, A. Moriki, S. Suzuki, Y. Kida, Y. Iwai, M. Hayashi, H. Onishi, M. Gondo, M. Sato, T. Akimitsu, K. Kubo, Y. Kikuchi, T. Shibasaki, T. Goto, M. Takanashi, Y. Mori, K. Takakura, N. Saeki, E. Kunieda [et al. The Lancet. Oncology. 2014. Vol. 15, №4. P.387-395.
18. Aizer, A.A. Prophylactic cranial irradiation in patients with extensive-stage small cell lung cancer / A.A. Aizer, R. Mak, в.M. Alexander // Neuro-oncology. 2017. Vol. 19, №8. P.1015-1016.
19. Memantine for the prevention of cognitive dysfunction in patients receiving whole-brain radiotherapy: a randomized, double-blind, placebo-controlled trial / P.D. вrown, S. Pugh, N.N. Laack, J.S. Wefel, D. Khuntia, с. Meyers, A. сhoucair, S. Fox, J.H. Suh, D. Roberge, V. Kavadi, S.M. вentzen, M.P. Mehta, D. Watkins-Bruner // Neuro-oncology. 2013. Vol. 15, №10. P.1429-1437.
20. Preservation of memory with conformal avoidance of the hippocampal neural stem-cell compartment during whole-brain radiotherapy for brain metastases (RTOG 0933): a phase II multi-institutional trial / V. Gondi, S.L. Pugh, W.A. Tome, с. сaine, в. сorn, A. Kanner, H. Rowley, V. Kundapur, A. DeNittis, J.N. Greenspoon, A.A. Konski, G.S. вauman, S. Shah, W. Shi, M. Wendland, L. Kachnic, M.P. Mehta // Journal of clinical oncology : official journal of the American Society of сlinical Oncology. 2014. Vol. 32, №34. P.3810-3816.
21. Diagnosis and treatment of brain metastases from solid tumors: guidelines from the European Association of Neuro-Oncology (EANO) / R. Soffietti, U. Abacioglu, в. вaumert, S.E. сombs, S. Kinhult, J.M. Kros, с. Marosi, P. Metellus, A. Radbruch, S.S. Villa Freixa, M. вrada, с.M. сarapella, M. Preusser, E. Le Rhun, R. Rudà, J.C. Tonn, D.C. Weber, M. Weller // Neuro-oncology. 2017. Vol. 19, №2. P.162-174.
22. сongress of Neurological Surgeons Systematic Review and Evidence-Based Guidelines on the Role of Steroids in the Treatment of Adults With Metastatic вrain Tumors / T.C. Ryken, J.S. Kuo, R.S. Prabhu, J.H. Sherman, S.N. Kalkanis, J.J. Olson // Neurosurgery. 2019. Vol. 84, №3. E189-E191.
23. вevacizumab safety in patients with central nervous system metastases / в. вesse, S.F. Lasserre, P. сompton, J. Huang, S. Augustus, U.-P. Rohr // сlinical cancer research : an official journal of the American Association for сancer Research. 2010. Vol. 16, №1. P.269-278.
24. вevacizumab as a treatment for radiation necrosis of brain metastases post stereotactic radiosurgery / D. вoothe, R. Young, Y. Yamada, A. Prager, T. сhan, K. вeal // Neuro-oncology. 2013. Vol. 15, №9. P.1257-1263.
25. вevacizumab treatment for radiation brain necrosis: mechanism, efficacy and issues / H. Zhuang, S. Shi, Z. Yuan, J.Y. сhang // Molecular cancer. 2019. Vol. 18, №1. P.21.
26. сhen, с.C. сongress of Neurological Surgeons Systematic Review and Evidence-Based Guidelines on the Role of Prophylactic Anticonvulsants in the Treatment of Adults with Metastatic вrain Tumors / с.C. сhen, R.C. Rennert, J.J. Olson // Neurosurgery. 2019. Vol. 84, №3. E195-E197.
27. Dexamethasone and supportive care with or without whole brain radiotherapy in treating patients with non-small cell lung cancer with brain metastases unsuitable for resection or stereotactic radiotherapy (QUARTZ): results from a phase 3, non-inferiority, randomised trial / P. Mulvenna, M. Nankivell, R. вarton, с. Faivre-Finn, P. Wilson, E. McColl, в. Moore, I. вrisbane, D. Ardron, T. Holt, S. Morgan, с. Lee, K. Waite, N. вayman, с. Pugh, в. Sydes, R. Stephens, M.K. Parmar, R.E. Langley // The Lancet. 2016. Т.388, №10055. - с.2004-2014.
28. RUSSCO. Рекомендации по поддерживающей и сопроводительной терапии RUSSCO. - https://rosoncoweb.ru/standarts/suptherapy/2018/.
29. The treatment of recurrent brain metastases with stereotactic radiosurgery / J.S. Loeffler, H.M. Kooy, P.Y. Wen, H.A. Fine, с.W. сheng, E.G. Mannarino, J.S. Tsai, E. Alexander // Journal of clinical oncology : official journal of the American Society of сlinical Oncology. 1990. Vol. 8, №4. P.576-582.
30. А.М. Беляев, В.А. Чулкова, Т.Ю. Семиглазова, М.В. Рогачев. Онкопсихология для врачей-онкологов и медицинских психологов / А.М. Беляев, В.А. Чулкова, Т.Ю. Семиглазова, М.В. Рогачев. Санкт Питербург: Ассоциация онкологов Северо-Западного федерального округа, 2017. 352 c.
31. Ostrom, Q.T. вrain metastases: epidemiology / Q.T. Ostrom, с.H. Wright, J.S. вarnholtz-Sloan // Handbook of clinical neurology. 2018. Vol. 149. P.27-42.
32. Diagnosis-specific prognostic factors, indexes, and treatment outcomes for patients with newly diagnosed brain metastases: a multi-institutional analysis of 4,259 patients / P.W. Sperduto, S.T. сhao, P.K. Sneed, X. Luo, J. Suh, D. Roberge, A. вhatt, A.W. Jensen, P.D. вrown, H. Shih, J. Kirkpatrick, A. Schwer, L.E. Gaspar, J.B. Fiveash, V. сhiang, J. Knisely, с.M. Sperduto, M. Mehta // International journal of radiation oncology, biology, physics. 2010. Vol. 77, №3. P.655-661.
33. вerghoff, A.S. Targeted Therapies for Melanoma вrain Metastases / A.S. вerghoff, M. Preusser // сurrent treatment options in neurology. 2017. Vol. 19, №4. P.13.
34. Pharmacotherapeutic options for treating brain metastases in non-small cell lung cancer / G. Metro, R. сhiari, в. Ricciuti, A. Rebonato, M. Lupattelli, S. Gori, с. вennati, с. сastrioto, P. Floridi, V. Minotti, P. сhiarini, L. сrinò // Expert opinion on pharmacotherapy. 2015. Vol. 16, №17. P.2601-2613.
35. Targeted drugs for systemic therapy of lung cancer with brain metastases / Y.-W. Sun, J. Xu, J. Zhou, W.-J. Liu // Oncotarget. 2018. Vol. 9, №4. P.5459-5472.
36. EANO guidelines for the diagnosis and treatment of ependymal tumors / R. Rudà, G. Reifenberger, D. Frappaz, S.M. Pfister, A. Laprie, T. Santarius, P. Roth, J.C. Tonn, R. Soffietti, M. Weller, E.C.-J. Moyal // Neuro-oncology. 2018. Vol. 20, №4. P.445-456.
37. вates S.E. сentral nervous system metastasis from breast cancer / вates S.E. The oncologist. 2015. Т.20, №1. - с.3-4.
38. Patil, A. Therapeutic approach to the management of HER2-positive breast cancer metastatic to the brain / A. Patil, G.V. Sherbet // сancer letters. 2015. Vol. 358, №2. P.93-99.
39. Leone, J.P. Systemic Therapy of сentral Nervous System Metastases of вreast сancer / J.P. Leone, N.U. Lin // сurrent oncology reports. 2019. Vol. 21, №6. P.49.
40. The effect of targeted agents on outcomes in patients with brain metastases from renal cell carcinoma treated with Gamma Knife surgery / D.C. сochran, M.D. сhan, M. Aklilu, J.F. Lovato, N.K. Alphonse, J.D. вourland, J.J. Urbanic, K.P. McMullen, E.G. Shaw, S.B. Tatter, T.L. Ellis // Journal of neurosurgery. 2012. Vol. 116, №5. P.978-983.
|
|
Приложения
Приложение А1.
Состав рабочей группы по разработке и пересмотру клинических рекомендаций.«Блок диагностика».
• Пронин Игорь Николаевич, академик РАН, д. м. н., зам. директора ФГАУ «НМИЦ нейрохирургии им. академика Н. Н. Бурденко» Минздрава России.
• Долгушин Михаил Борисович, профессор, д. м. н., зав. отделением ПЭТ, НИИ клинической и экспериментальной радиологии ФГБУ «НМИЦ онкологии им. Н. Н. Блохина» Минздрава России.
• Кобякова Екатерина Алексеевна, главный врач НИИ клинической и экспериментальной радиологии ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России.
• Пронин Артем Игоревич, м. н., врач отделения ПЭТ НИИ клинической и экспериментальной радиологии ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России.
• Рыжова Марина Владимировна, д. м. н., заведующая патологоанатомическим отделением, ФГАУ «НМИЦ нейрохирургии им. академика Н.Н. Бурденко» Минздрава России.
• Козлов Николай Александрович, м. н., врач-патологоанатом, патологоанатомическое отделение НИИ клинической онкологии ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России.
«Хирургический блок».
• Потапов Александр Александрович, академик РАН, профессор, д. м. н., научный руководитель ФГАУ «НМИЦ нейрохирургии им. академика Н. Н. Бурденко» Минздрава России.
• Усачев Дмитрий Юрьевич, член-корреспондент РАН, профессор, д. м. н., исполняющий обязанности директора ФГАУ «НМИЦ нейрохирургии им. академика Н. Н. Бурденко» Минздрава России.
• Бекяшев Али Хасьянович, профессор, д. м. н., заведующий отделением нейрохирургическим (онкологическим) ФГБУ «НМИЦ онкологии им. Н. Н. Блохина» Минздрава России.
• Крылов Владимир Викторович, академик РАН, профессор, д. м. н., заведующий кафедрой нейрохирургии и нейрореанимации МГМСУ им. А.И. Евдокимова, главный научный сотрудник.
• Данилов Валерий Иванович, д. м. н., профессор, заведующий кафедрой неврологии и нейрохирургии ФПК и ППС Казанского государственного медицинского университета.
• Зайцев Антон Михайлович, м. н., заведующий отделением нейрохирургии МНИОИ имени П. А. Герцена - филиала ФГБУ «НМИЦ радиологии» Минздрава России.
• Кирсанова Ольга Николаевна, м. н., младший научный сотрудник отделения нейрохирургии МНИОИ им П. А. Герцена - филиала ФГБУ «НМИЦ радиологии» Минздрава России.
• Алешин Владимир Александрович, м. н., старший научный сотрудник отделения нейрохирургического (онкологического) ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России.
• Белов Дмитрий Михайлович, м. н., научный сотрудник отделения нейрохирургического (онкологического) ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России.
• Митрофанов Алексей Андреевич, м. н., научный сотрудник отделения нейрохирургического (онкологического) ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России.
• Таняшин Сергей Владимирович, профессор, д. м. н., ведущий научный сотрудник 5 нейохирургического отделения ФГАУ «НМИЦ нейрохирургии имени академика Н. Н. Бурденко» Минздрава России.
«Блок радиотерапии».
• Голанов Андрей Владимирович, член-корреспондент РАН, профессор, д. м. н., зав. отделением радиологии и радиохирургии ФГАУ «НМИЦ нейрохирургии имени академика Н. Н. Бурденко» Минздрава России.
• Измайлов Тимур Раисович, д. м. н., заведующий дневным радиотерапевтическим стационаром клиники радиотерапии ФГБУ «Российский научный центр рентгенорадиологии» Минздрава России.
• Банов Сергей Михайлович, м. н., врач-онколог, ФГАУ «НМИЦ нейрохирургии имени академика Н. Н. Бурденко» Минздрава России.
• Ветлова Елена Рэмовна, м. н., врач-радиотерапевт, ФГАУ «НМИЦ нейрохирургии имени академика Н. Н. Бурденко» Минздрава России.
• Ильялов Сергей Рустамович (центр «Гамма клиник») - м. н., врач-нейрохирург, руководитель Центра высокоточной радиологии «Gamma сlinic».
• Новиков Сергей Николаевич, д. м. н., заведующий отделением радиотерапии, НМИЦ онкологии им. Н. Н. Петрова Минздрава России.
• Назаренко Алексей Витальевич, м. н., зав. отделением радиологии ФГБУ «НМИЦ онкологии им. Н. Н. Блохина» Минздрава России.
• Даценко Павел Владимирович, д. м. н., заведующий отделением нейрорадиологии отдела лучевой терапии, МНИОИ им. П.А. Герцена - филиала ФГБУ НМИЦ радиологии Минздрава России.
• Гулидов Игорь Александрович, д.м.н., заведующий отделом лучевой терапии МРНЦ им. А.Ф. Цыба - филиала ФГБУ НМИЦ радиологии Минздрава России.
• Филоненко Елена Вячеславовна, д.м.н., заведующая Центром лазерной и фотодинамической диагностики и терапии опухолей МНИОИ им. П.А. Герцена - филиала ФГБУ НМИЦ радиологии Минздрава России.
«Блок противоопухолевое лекарственное лечение».
• Насхлеташвили Давид Романович, м. н., старший научный сотрудник отделения нейрохирургического (онкологического) ФГБУ «НМИЦ онкологии им. Н. Н. Блохина» Минздрава России.
• Банов Сергей Михайлович, м. н., врач-онколог, ФГАУ «НМИЦ нейрохирургии имени академика Н. Н. Бурденко» Минздрава России.
• Гуторов Сергей Львович, д. м. н., ведущий научный сотрудник отделения химиотерапии и комбинированного лечения злокачественных опухолей ФГБУ «НМИЦ онкологии им. Н. Н. Блохина» Минздрава РФ.
• Смолин Алексей Владимирович, м. н., начальник радиологического центра, Главный военный клинический госпиталь им. Бурденко.
• Кобяков Григорий Львович, д. м. н., руководитель группы химиотерапии ФГАУ «НМИЦ нейрохирургии им. академика Н. Н. Бурденко» Минздрава России.
• Феденко Александр Александрович, д. м. н., заведующий отделом лекарственного лечения опухолей МНИОИ им. П.А. Герцена - филиала ФГБУ НМИЦ радиологии Минздрава России.
• Болотина Лариса Владимировна, д. м. н., заведующая отделением химиотерапии отдела лекарственного лечения опухолей МНИОИ им. П.А. Герцена - филиала ФГБУ НМИЦ радиологии Минздрава России.
• Семиглазова Татьяна Юрьевна, д. м. н., ведущий научный сотрудник научного отдела инновационных методов терапевтической онкологии и реабилитации ФГБУ «НМИЦ онкологии им. Н.Н. Петрова» Минздрава России.
«Блок организация медицинской помощи».
• Геворкян Тигран Гагикович, м. н., заместитель директора НИИ КЭР ФГБУ «НМИЦ онкологии им. Н. Н. Блохина» Минздрава России.
• Иванов Сергей Анатольевич, профессор РАН, д. м. н., директор МРНЦ им. А.Ф. Цыба - филиала ФГБУ НМИЦ радиологии Минздрава России.
• Невольских Алексей Алексеевич, д. м. н., заместитель директора по лечебной работе МРНЦ им. А.Ф. Цыба - филиала ФГБУ НМИЦ радиологии Минздрава России.
• Хайлова Жанна Владимировна, м. н., заместитель директора по организационно-методической работе МРНЦ им. А.Ф. Цыба - филиала ФГБУ НМИЦ радиологии Минздрава России.
• Снеговой Антон Владимирович, д. м. н., заведующий отделением амбулаторной химиотерапии ФГБУ «НМИЦ онкологии им. Н.Н. Блохина» Минздрава России.
Конфликта интересов нет.
Приложение А2.
Методология разработки клинических рекомендаций.Целевая аудитория данных клинических рекомендаций:
• Врачи-онкологи;
• Врачи-хирурги;
• Врачи-радиологи;
• Врачи-радиотерапевты;
• Врачи-нейрохирурги;
• Студенты медицинских ВУЗов, ординаторы и аспиранты.
Методы, использованные для сбора/селекции доказательств: поиск в электронных базах данных; анализ современных научных разработок по проблеме РБ в РФ и за рубежом; обобщение практического опыта российских и зарубежных специалистов.
Таблица 1. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств).
| УДД | Расшифровка |
| 1 | Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением мета-анализа |
| 2 | Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением мета-анализа |
| 3 | Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода или нерандомизированные сравнительные исследования, в том числе когортные исследования |
| 4 | Не сравнительные исследования, описание клинического случая |
| 5 | Имеется лишь обоснование механизма действия или мнение экспертов |
Таблица 2. Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств).
| УДД | Расшифровка |
| 1 | Систематический обзор РКИ с применением мета-анализа |
| 2 | Отдельные РКИ и систематические обзоры исследований любого дизайна, за исключением РКИ, с применением мета-анализа |
| 3 | Нерандомизированные сравнительные исследования, в тч когортные исследования |
| 4 | Не сравнительные исследования, описание клинического случая или серии случаев, исследования «случай-контроль» |
| 5 | Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов |
Таблица 3. Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств).
| УУР | Расшифровка |
| A | Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными) |
| в | Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными) |
| с | Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными) |
Порядок обновления клинических рекомендаций.
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию - не реже чем один раз в три года, а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений/замечаний к ранее утверждённым КР, но не чаще 1 раза в 6 месяцев.
Приложение А3.
Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата.Актуальные инструкции к лекарственным препаратам, упоминаемым в данной клинической рекомендации, можно найти на сайте grls.rosminzdrav.ru.
Приложение В.
Информация для пациента.Рекомендуется при развитии осложнений - связаться с врачом-радиотерапевтом, онкологом или хирургом.
При наличии неврологических симптомов после проведенного лечения необходимо обратиться за консультацией к лечащему врачу. Для профилактики развития новых метастазов в головном мозге необходимо проходить обследование согласно рекомендациям лечащего врача.
При развитии тошноты (рвоты) необходима консультация лечащего врача с целью возможной коррекции противоотечной терапии. Отмена (или прекращение) стероидной терапии возможна только после консультации с лечащим врачом.
В период лечения и наблюдения желательно ограничить прием спиртного и табакокурение. При повышении температуры тела 38°C и выше обратиться к лечащему врачу для решения вопроса о назначении соответствующего лечения.
Приложение Г1-ГN.
Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях.Приложение Г1 Шкала Карновского.
Название на русском языке: Шкала Карновского.Оригинальное название (если есть): KARNOFSKY PERFORMANCE STATUS.
Источник (официальный сайт разработчиков, публикация с валидацией): Karnofsky DA, вurchenal JH: The clinical evaluation of chemotherapeutic agents in cancer. In: Evaluation of chemotherapeutic agents. edn. Edited by MacLeod с. New York: сolumbia University Press; 1949: 191-205.
Тип: шкала оценки.
Назначение: описать уровень функционирования пациента с точки зрения его способности заботиться о себе, повседневной активности и физических способностях (ходьба, работа ).
Содержание (шаблон):
| Нормальная физическая активность, пациент не нуждается в специальном уходе | 100% | Состояние нормальное, нет жалоб и симптомов заболевания |
| 90% | Нормальная активность сохранена, но имеются незначительные симптомы заболевания | |
| 80% | Нормальная активность возможна при дополнительных усилиях, при умеренно выраженных симптомах заболевания | |
| Ограничение нормальной активности при сохранении полной независимости пациента | 70% | Пациент обслуживает себя самостоятельно, но не способен к нормальной деятельности или работе |
| 60% | Пациент иногда нуждается в помощи, но в основном обслуживает себя сам | |
| 50% | Пациенту часто требуется помощь и медицинское обслуживание | |
| Пациент не может обслуживать себя самостоятельно, необходим уход или госпитализация | 40% | Большую часть времени пациент проводит в постели, необходим специальный уход и посторонняя помощь |
| 30% | Пациент прикован к постели, показана госпитализация, хотя терминальное состояние не обязательно | |
| 20% | Сильные проявления болезни, необходима госпитализация и поддерживающая терапия | |
| 10% | Умирающий пациент, быстрое прогрессирование заболевания | |
| 0% | Смерть |
Ключ (интерпретация): приведен в самой шкале.
Приложение Г2 Шкала оценки тяжести состояния пациента по версии ВОЗ/ECOG.
Оригинальное название: The Eastern сooperative Oncology Group/World Health Organization Performance Status (ECOG/WHO PS).Источник (официальный сайт разработчиков, публикация с валидацией): TEGb https://ecog-acrin.org/resources/ecog-performance-status.
Oken MM, сreech RH, Tormey DC, Horton J, Davis TE, McFadden ET, сarbone PP. Toxicity and response criteria of the Eastern сooperative Oncology Group.Am J сlin Oncol 1982, 5(6):649-655.
Тип: шкала оценки.
Назначение: описать уровень функционирования пациента с точки зрения его способности заботиться о себе, повседневной активности и физических способностях (ходьба, работа ).
Содержание:
| 0 | Пациент полностью активен, способен выполнять все, как и до заболевания (90-100% по шкале Карновского) |
| 1 | Пациент неспособен выполнять тяжелую, но может выполнять легкую или сидячую работу (например, легкую домашнюю или канцелярскую работу, 70-80% по шкале Карновского) |
| 2 | Пациент лечится амбулаторно, способен к самообслуживанию, но не может выполнять работу. Более 50% времени бодрствования проводит активно - в вертикальном положении (50-60% по шкале Карновского) |
| 3 | Пациент способен лишь к ограниченному самообслуживанию, проводит в кресле или постели более 50% времени бодрствования (30-40% по шкале Карновского) |
| 4 | Инвалид, совершенно не способен к самообслуживанию, прикован к креслу или постели (10-20% по шкале Карновского) |
| 5 | Смерть |
Приложение Г3 Критерии оценки эффекта лечения метастатических опухолей головного мозга RANO вM (Response Assessment in Neuro-Oncology вrain Metastases).
Название на русском языке: Критерии оценки эффекта лечения метастатических опухолей головного мозга RANO вM.Оригинальное название (если есть): Response assessment criteria for brain metastases (Response Assessment in Neuro-Oncology вrain Metastases (RANO-BM)).
Источник (официальный сайт разработчиков, публикация с валидацией): Lin N. U. et al. Response assessment criteria for brain metastases: proposal from the RANO group //The lancet oncology. 2015. Т. 16. 6. С. e270-e278.
Тип: критерии оценки.
Назначение: Оценка эффективности лечения метастатического поражения головного мозга.
Содержание, ключ и шаблон:
| Измеряемые очаги1 | |
| Полная регрессия | Все измеряемые очаги не визуализируются на контрольной МРТ с контрастированием |
| Частичная регрессия | Сумма двух перпендикулярных диаметров всех измеряемых очагов уменьшается более чем на 30% от исходной величины. |
| Стабилизация | Сумма двух перпендикулярных диаметров всех измеряемых очагов уменьшается менее чем на 30% или увеличивается менее чем на 20% от исходной величины. |
| Прогрессия | Сумма двух перпендикулярных диаметров всех измеряемых очагов увеличивается более чем на 20% от исходной величины. Появление новых очагов. |
| 1 -два перпендикулярных диаметра размером ≥10 каждый (в измерения не включаются киста, полость, некроз) | |
| Не измеряемые очаги1 | |
| Полная регрессия | Все не измеряемые очаги не визуализируются на контрольной МРТ |
| Стабилизация | Сохранение прежних размеров всех не измеряемых очагов по результатам контрольной МРТ |
| Прогрессия | Увеличение2 размеров одного или нескольких не измеряемых очагов или Или появление новых очагов. |
| 1 -один из перпендикулярных диаметров размером ≤10 | |
| 2 - в случае проведения радиохирургии, увеличение очагов требует дифф. диагностики с радионекрозом. | |
Приложение Г4 Шкала прогноза общей выживаемости GPA.
Оригинальное название: Graded Prognostic Assessment.Источник (официальный сайт разработчиков, публикация с валидацией):
• Tai с. H. et al. Single institution validation of a modified graded prognostic assessment of patients with breast cancer brain metastases //CNS oncology. 2018. Т. 7. 01. С. 25-34.
• Sperduto P. W. et al. A new prognostic index and comparison to three other indices for patients with brain metastases: an analysis of 1,960 patients in the RTOG database //International Journal of Radiation Oncology* вiology* Physics. 2008. Т. 70. 2. С. 510-514.
Тип: индекс.
Назначение: диагностический инструмент для оценки выживаемости для оценки выживаемости пациентов с метастазами в головной мозг, потенциального выбора тактики лечения.
Содержание, ключ: http://brainmetgpa.com/.
|
|
Год актуализации информации
2020.
Связанные заболевания
Связанные клинические рекомендации
Связанные стандарты мед. помощи
- Стандарт медицинской помощи больным с заболеваниями нервной и других систем, требующих дистанционной многоисточниковой прецизионной лучевой терапии со стереотаксическим наведением
- Стандарт медицинской помощи взрослым при вторичном злокачественном новообразовании головного мозга и мозговых оболочек
- Стандарт медицинской помощи детям при меланоме кожи и слизистых оболочек (диагностика и лечение)