ICD-10 codes
Introduction
Кодирование по Международной статистической классификации болезней и проблем, связанных со здоровьем: М10.0/М10.1/М10.2/М10.3/М10.4/М10.9.
Год утверждения (частота пересмотра): 2018.
Возрастная категория: Взрослые.
Год окончания действия: 2020.
ID: 251.
Разработчик клинической рекомендации.
• Ассоциация ревматологов России.
Год утверждения (частота пересмотра): 2018.
Возрастная категория: Взрослые.
Год окончания действия: 2020.
ID: 251.
Разработчик клинической рекомендации.
• Ассоциация ревматологов России.
 List of abbreviations
List of abbreviations
АД - артериальное давление.
АЛТ - аланинтрансаминаза.
АСТ - аспартаттрансаминаза.
ВОЗ - Всемирная Организация Здравоохранения.
ГИБП- генно-инженерные биологические препараты.
ГК - глюкокортикоиды.
ГУ - гиперурикемия.
ИЛ - интерлейкин.
МК - мочевая кислота.
МКБ - мочекаменная болезнь.
МРТ - магнитно-резонансная томография.
МУН - кристаллы моноурата натрия.
НПВП - нестероидные противовоспалительные препараты.
НР - нежелательная реакция.
РКИ - рандомизированные клинические исследования.
УЗИ - ультразвуковое исследование.
ФНО-α - фактор некроза опухоли- α.
ACR - Американская Коллегия Ревматологов.
EULAR - Европейская Антиревматическая Лига.
АЛТ - аланинтрансаминаза.
АСТ - аспартаттрансаминаза.
ВОЗ - Всемирная Организация Здравоохранения.
ГИБП- генно-инженерные биологические препараты.
ГК - глюкокортикоиды.
ГУ - гиперурикемия.
ИЛ - интерлейкин.
МК - мочевая кислота.
МКБ - мочекаменная болезнь.
МРТ - магнитно-резонансная томография.
МУН - кристаллы моноурата натрия.
НПВП - нестероидные противовоспалительные препараты.
НР - нежелательная реакция.
РКИ - рандомизированные клинические исследования.
УЗИ - ультразвуковое исследование.
ФНО-α - фактор некроза опухоли- α.
ACR - Американская Коллегия Ревматологов.
EULAR - Европейская Антиревматическая Лига.
Terms and definitions
Артрит. Воспаление тканей сустава с обязательным вовлечением его синовиальной оболочки (синовит).
Генно-инженерные биологические препараты (ГИБП). Группа лекарственных средств биологического происхождения, в том числе моноклональные антитела (химерные, гуманизированные, полностью человеческие) и рекомбинантные белки (обычно включают Fc фрагмента IgG человека), полученные с помощью методов генной инженерии, специфически подавляющие иммуновоспалительный процесс и замедляющие прогрессирование деструкции суставов.
Гиперурикемия. Повышенный сывороточный уровень мочевой кислоты в крови.
Глюкокортикоиды (ГК). Синтетические стероидные гормоны, обладающие естественной противовоспалительной активностью.
Нестероидные противовоспалительные препараты (НПВП). Группа синтетических лекарственных средств, обладающих симптоматическим обезболивающим, жаропонижающим и противовоспалительным эффектами, связанными в первую очередь с ингибицией активности циклооксигены - фермента, регулирующего синтез простагландинов.
Подагра. Системное тофусное заболевание, характеризующееся отложением в различных тканях кристаллов моноурата натрия и развивающимся в связи с этим воспалением у лиц с гиперурикемией, обусловленной внешнесредовыми и/или генетическими факторами.
Тофус. Очаговое скопление кристаллов мочевой кислоты в тканях в виде узлов.
Уратснижающие препараты. Группа лекарственных средств, действие которых направлено на предупреждение образования и растворение имеющихся кристаллов моноурата натрия.
Генно-инженерные биологические препараты (ГИБП). Группа лекарственных средств биологического происхождения, в том числе моноклональные антитела (химерные, гуманизированные, полностью человеческие) и рекомбинантные белки (обычно включают Fc фрагмента IgG человека), полученные с помощью методов генной инженерии, специфически подавляющие иммуновоспалительный процесс и замедляющие прогрессирование деструкции суставов.
Гиперурикемия. Повышенный сывороточный уровень мочевой кислоты в крови.
Глюкокортикоиды (ГК). Синтетические стероидные гормоны, обладающие естественной противовоспалительной активностью.
Нестероидные противовоспалительные препараты (НПВП). Группа синтетических лекарственных средств, обладающих симптоматическим обезболивающим, жаропонижающим и противовоспалительным эффектами, связанными в первую очередь с ингибицией активности циклооксигены - фермента, регулирующего синтез простагландинов.
Подагра. Системное тофусное заболевание, характеризующееся отложением в различных тканях кристаллов моноурата натрия и развивающимся в связи с этим воспалением у лиц с гиперурикемией, обусловленной внешнесредовыми и/или генетическими факторами.
Тофус. Очаговое скопление кристаллов мочевой кислоты в тканях в виде узлов.
Уратснижающие препараты. Группа лекарственных средств, действие которых направлено на предупреждение образования и растворение имеющихся кристаллов моноурата натрия.
Description
Подагра - системное тофусное заболевание, характеризующееся отложением в различных тканях кристаллов моноурата натрия и развивающимся в связи с этим воспалением у лиц с гиперурикемией, обусловленной внешнесредовыми и/или генетическими факторами [1].
Reasons
Облигатным фактором развития подагры является гиперурикемия, повышение сывороточного уровня мочевой кислоты выше 420 мкмоль/л, при котором у части пациентов происходит образование кристаллов моноурата натрия. Чем выше сывороточный уровень мочевой кислоты, тем выше риск развития подагры. Формирования кристаллов возможно и при более низком уровне показателя (360 мкмоль/л), прежде всего, у женщин [2-4].
Основными причинами гиперурикемии являются генетические факторы, приводящие к повышению реабсорбции и снижению экскреции мочевой кислоты с мочой либо к её гиперпродукции; избыточная масса тела и ожирение, повышение артериального давления, приём алкоголя, потребление большого количества животного белка, приём мочегонных препаратов, заболевания и состояния, характеризующиеся гиперурикемией.
Кристаллы моноурата натрия, формирующиеся в синовиальной жидкости и близлежащих тканях, выступают в качестве триггера острого подагрического артрита, запуская каскад иммунных реакций. Исходно происходит фагоцитоз кристаллов, благодаря высокой в клетках повышается концентрация натрия, вследствие этого происходит компенсаторный приток воды в цитоплазму и набухание клеток, параллельно резко уменьшается содержание калия, индуцируя активацию внутриклеточных инфламмасом, в результате которого синтезируется широкий спектр провоспалительных цитокинов, хемокинов (прежде всего интерлейкина-1 (ИЛ-1), а также ИЛ-6, ИЛ-8, ИЛ-18, фактора некроза опухоли-α(ФНО-α) ). Их продукция способствует развитию острой массивной воспалительной реакции, вазодилатации, быстрой миграции к месту воспаления иммунных клеток, преимущественно нейтрофилов [5-7]. Клинически это проявляется острым приступом артрита.
Хронический, вялотекущий воспалительный процесс, связанный с наличием в суставах и окружающих тканях кристаллов моноурата натрия, протекает и вне острого приступа артрита [8].
Основными причинами гиперурикемии являются генетические факторы, приводящие к повышению реабсорбции и снижению экскреции мочевой кислоты с мочой либо к её гиперпродукции; избыточная масса тела и ожирение, повышение артериального давления, приём алкоголя, потребление большого количества животного белка, приём мочегонных препаратов, заболевания и состояния, характеризующиеся гиперурикемией.
Кристаллы моноурата натрия, формирующиеся в синовиальной жидкости и близлежащих тканях, выступают в качестве триггера острого подагрического артрита, запуская каскад иммунных реакций. Исходно происходит фагоцитоз кристаллов, благодаря высокой в клетках повышается концентрация натрия, вследствие этого происходит компенсаторный приток воды в цитоплазму и набухание клеток, параллельно резко уменьшается содержание калия, индуцируя активацию внутриклеточных инфламмасом, в результате которого синтезируется широкий спектр провоспалительных цитокинов, хемокинов (прежде всего интерлейкина-1 (ИЛ-1), а также ИЛ-6, ИЛ-8, ИЛ-18, фактора некроза опухоли-α(ФНО-α) ). Их продукция способствует развитию острой массивной воспалительной реакции, вазодилатации, быстрой миграции к месту воспаления иммунных клеток, преимущественно нейтрофилов [5-7]. Клинически это проявляется острым приступом артрита.
Хронический, вялотекущий воспалительный процесс, связанный с наличием в суставах и окружающих тканях кристаллов моноурата натрия, протекает и вне острого приступа артрита [8].
Epidemiology
Заболеваемость подагрой составляет в различных популяциях от 5 до 70 на 1 000 среди мужчин и 1-10 среди женщин. Распространённость подагры среди взрослого населения колеблется в европейских странах от 0,9% до 2,5%, в США достигает 3,9%. Пик заболеваемости у мужчин в возрасте 40-50 лет, женщин - после 60 лет (в постменопаузальном периоде). Подагра среди мужчин встречается в 6-7 раз чаще, в старческом возрасте - в 3 раза чаще [9-17].
Лечение подагры проводится на протяжении всей жизни пациента, основу его составляет медикаментозная уратснижающая терапия. Целью лечения является достижение нормативных (целевых) значений сывороточного уровня мочевой кислоты для предотвращения приступов артрита и рассасывания имеющихся отложений кристаллов моноурата натрия и купирование артрита (в случае возникновения).
Лечение подагры проводится на протяжении всей жизни пациента, основу его составляет медикаментозная уратснижающая терапия. Целью лечения является достижение нормативных (целевых) значений сывороточного уровня мочевой кислоты для предотвращения приступов артрита и рассасывания имеющихся отложений кристаллов моноурата натрия и купирование артрита (в случае возникновения).
Classification
1,5 Классификация,.
Основные клинические проявления подагры: рецидивирующие атаки острого артрита, очаговое накопление кристаллов уратов с образованием тофусов в тканях (в области суставов, мягких тканей, различных органах), нефролитиаз, подагрическая нефропатия.В развитии подагры выделяют 4 стадии:
• бессимптомтомная гиперурикемия с отсутствием депозитов моноурата натрия.
• бессимптомная гиперурикемия с наличием депозитов моноурата натрия, но без симптомов или анамнеза подагры (отсутствия приступов артрита и тофусов).
• депозиты моноурата натрия с текущим (острый подагрический артрит) или предшествующим эпизодом подагрического артрита (межприступный период при отсутствии артрита на текущий момент).
• хроническая тофусная подагра (пациенты с тофусами, хроническим артритом, эрозиями по данным радиологических методов, функциональными нарушениями).
1,5,1 Классификационные критерии.
Классификационные критерии острого артрита при подагре разработаны Американской Ассоциацией Ревматологов и одобрены ВОЗ для использования в практике [18].1,5,2 Классификационные критерии острого подагрического артрита.
А. Наличие характерных кристаллов моноурата натрия в суставной жидкости.Б. Наличие тофусов, содержание кристаллов мочевой кислоты, в которых подтверждено химически или поляризационной микроскопией.
В. Наличие не менее чем 6 из 12 ниже перечисленных признаков:
1. Более одной атаки острого артрита в анамнезе.
2. Воспаление сустава достигает максимума в 1-й день болезни.
3. Моноартрит.
4. Гиперемия кожи над пораженным суставом.
5. Припухание и боль в первом плюснефаланговом суставе.
6. Одностороннее поражение первого плюснефалангового сустава.
7. Одностороннее поражение суставов стопы.
8. Подозрение на тофусы.
9. Гиперурикемия.
10. Асимметричный отек суставов.
11. Субкортикальные кисты без эрозий (рентгенография).
12. Отрицательные результаты при посеве синовиальной жидкости.
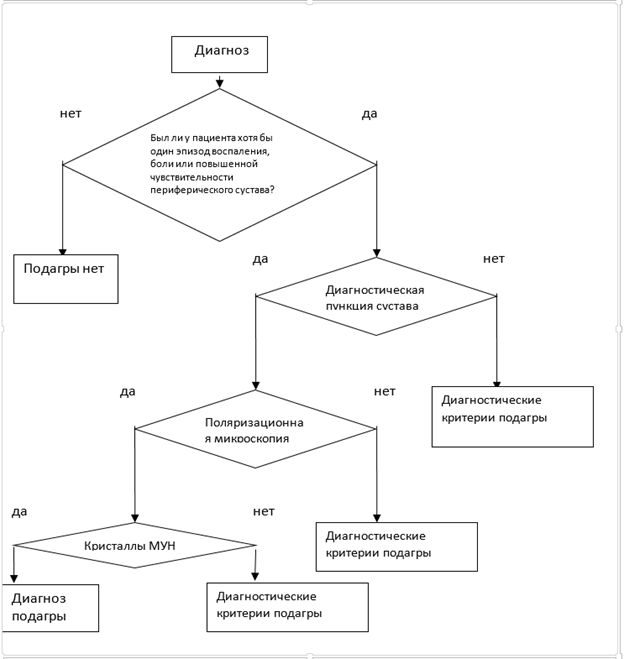
Для определённого диагноза подагры достаточно выявление кристаллов моноурата натрия в синовиальной жидкости или тофусах (пункты А и Б рекомендаций); при невозможности указанных исследований диагноз должен быть обоснован наличием совокупности клинических, лабораторных и инструментальных признаков (пункт В рекомендации).
Таблица.1 Критерии подагры (ACR/EULAR, 2015).
| Категории | Баллы | |
| Шаг 1.Критерий включения (критерии, приведённые ниже применяются только к тем пациентом, у которых есть указанный критерий) | Имеется, по крайней мере, один эпизод отёчности, боли или повышенной чувствительности в периферическом суставе или бурсе | |
| Шаг 2.Достаточный критерий (если выявлен, можно классифицировать как подагру без использования нижеизложенных критериев) | Наличие кристаллов моноурата натрия в поражённом суставе или бурсе (например, в синовиальной жидкости) или тофусе | |
| Шаг 3.Критерии (должны использоваться, если достаточный критерий не выявлен) Клинические Эпизод(ы) типичных симптомов с вовлечением сустава/бурсы † Особенности симптомов когда-либо бывшего эпизода • эритема над поражённым суставом (сообщено пациентом или наблюдаемая врачом) • невозможность терпеть прикосновение и давление на поражённый сустав • большие трудности при ходьбе или неспособность использовать поражённый сустав Временная характеристика, когда- либо бывшего эпизода Наличие когда-либо ≥2 признаков, независимо от противовоспалительной терапии: • развитие максимальной боли в течение <24 часов • разрешение симптомов в течение ≤14 дней • полная регрессия симптомов (до исходного уровня) между эпизодами Клинически обнаруживаемые тофусы Узел с наличием отделяемого или мелообразный, под прозрачной кожей с вышележащей васкуляризацией, локализующийся в типичных местах: суставы, уши, бурса локтевого отростка, подушечки пальцев, сухожилия (например, ахиллы). Лабораторные Сывороточный уровень мочевой кислоты: измерение уриказным методом В идеале должен анализ должен быть выполнен в период, когда пациент не получал уратснижающей терапии и по истечении >4 недель от начала эпизода (то есть во время межприступного периода); если возможно, анализ должен быть пересдан с соблюдением этих условий. Должен быть выбран самый высокий показатель независимо от времени проведения исследования. ‡ Анализ синовиальной жидкости, полученной из когда-либо поражённого сустава или сумки (должен быть проведён обученным специалистом) § Методы визуализации ¶ Визуальные признаки депозитов уратов в когда-либо пораженном суставе или бурсе: ультразвуковой признак двойного контура или демонстрация уратных депозитов при помощи двухэнергетической компьютерной томографии * Визуальные признаки обусловленного подагрой повреждения сустава по данным обычной рентгенографии кистей или стоп: демонстрация по крайней мере 1 эрозии †† | Голеностопный сустав либо суставы средней части стопы (как составная часть эпизода моно- или олигоартрита без вовлечения первого плюснефалангового сустава) Вовлечение 1-го плюснефалангового сустава (как составная часть эпизода моно- или олигоартрита) Одна характеристика Две характеристики Три характеристики Один типичный эпизод Повторяющиеся типичный эпизоды Представлены <4 мг/дл (<0,24 ммоль/л) 6-<8 мг/дл (0,36-<0,48 ммоль/л) 8-<10 мг/дл (0,48-<0,60 ммоль/л) ≥10 мг/дл (≥0,60 ммоль/л) Кристаллы МУН не выявлены Представлены (любым способом) Представлены | 1 2 2 3 1 2 4 -4 2 3 4 -2 4 4 |
† - Эпизоды бывших когда-либо симптомов, которые включают припухлость, боль, болезненность при пальпации в периферическом суставе или бурсе.
‡ - Если сывороточный уровень мочевой кислоты <4 мг/дл (0,24 ммоль/л), следует вычесть 4 балла; если сывороточный уровень мочевой кислоты ≥4 мг/дл - 6 мг/дл (≥0,24 - <0,36 ммоль/л), считать этот пункт как 0 баллов.
§ - Если проведённая обученным специалистом поляризационная микроскопии синовиальной жидкости, полученной из когда-либо поражённого сустава, не выявила кристаллов моноурата натрия), следует вычесть 2 балла. Если синовиальная жидкость не была оценена, считать этот пункт как 0 баллов.
¶ - Если методы недоступны, считать этот пункт как 0 баллов.
- Гиперэхогенная прерывистая полоска по поверхности гиалинового хряща, не зависящая от угла осмотра (примечание: ложноположительный признак двойного контура может появиться на поверхности хряща, но должен исчезнуть при изменении угла осмотра).
* - Наличие соответствующих цвету кодировки уратов в области суставов или периартикулярно.
†† - Эрозия определена как кортикальный дефект со склеротической каймой и нависающими краями, исключая дистальные межфаланговые суставы и признак «крыла чайки».
Diagnostics
2,1 Жалобы и анамнез.
• Рекомендуется выявлять факторы риска подагры и сопутствующих болезней у каждого пациента, включая признаки метаболического синдрома (ожирение, гипергликемия, гиперлипидемия, гипертензия). К наиболее значимым факторам риска подагры относятся прием ряда лекарственных препаратов (диуретиков, циклоспорина А, салицилатов), почечная недостаточность, злоупотребление алкоголем, потребление сахарсодержащих (фруктозосодержащих) напитков и продуктов питания [2, 12, 17, 22-25].Уровень убедительности рекомендаций В (уровень достоверности доказательств Ib).
Комментарии. Ценность этой рекомендации подтверждают данные множества крупных исследований. Так, относительный риск развития подагры у больных с хронической болезнью почек, ожирением, при повышении артериального давления, нарушениях липидного обмена намного выше популяционного, при наличии гиперурикемии чаще регистрируются случаи терминальной почечной недостаточности, а смертность у больных с хронической болезнью почек при наличии подагры увеличивается четырёхкратно. Не менее важной представляется обязательная оценка факторов кардиоваскулярного риска и обменных нарушений в рамках метаболического синдрома, частота выявления которых при подагре очень высока, что может обуславливать высокий уровень кардиоваскулярной смертности у больных подагрой. Помимо алкоголя и потребления богатых пуринами продуктов животного происхождения (мясо, морепродукты), по данным популяционных исследований сопоставимый с алкоголем вклад в риск развития подагры вносит потреблений большого количества подслащённых, содержащих фруктозу напитков, а также, увеличивающееся использование диуретиков.
• Рекомендуется в каждом случае при подозрении на диагноз подагры давать клиническую характеристику артрита. Острая атака с быстрым развитием выраженной боли и воспаления, которые достигают максимума в течение 24 часов, особенно сопровождающиеся эритемой, высоко подозрительны в отношении микрокристаллического воспаления, прежде всего подагры, хотя не специфичны для подагры. Если типичный приступ острого артрита затрагивает суставы стоп, особенно 1-й плюснефаланговый, а количество приступов острого артрита превышает один, то вероятность диагноза подагры существенно возрастает. Продолжительность острого приступа артрита при подагре редко превышает двухнедельный срок [19, 26].
Уровень убедительности рекомендаций С (уровень достоверности доказательств IIb).
Комментарии. В исследованиях, проводимых для формирования классификационных критериев, данные признаки являются основными клиническими «маркёрами» острого артрита при подагре. Тем не менее, при высокой чувствительности, уровень доказательности данной рекомендации не максимален. Например, артрит 1-го плюснефалангового сустава, позволивший классифицировать его как подагрический исключительно на основании клинической картины, подтверждается только в 77% случаев.
2,2 Физикальное обследование.
• Рекомендуется у всех пациентов, помимо визуальной оценки наличия артрита (видимая глазом припухлость, гиперемия, функциональное состояние суставов) отдельно осматривать места возможной локализации подкожных тофусов (наиболее часто это ушные раковины, 1-е пальца стоп, локтевые суставы); пальпаторно определять болезненные и воспалённые суставы, размеры тофусов (при их наличии) [20, 26, 27].Уровень убедительности рекомендаций D (уровень достоверности доказательств IV).
Комментарии. Пальпаторно определяемые подкожные тофусы чаще локализованы в местах, подверженных давлению или трению, при формировании в области мелких суставов могут симулировать узелковую форму остеоартроза, узлы при ревматоидном артрите. В области ушных раковин они обнаруживаются в 12% случаев, чаще у мужчин. У пациентов, которые принимают глюкокортикоиды, формирование подкожных тофусов происходит быстрее. В некоторых случаях подкожные тофусы могут быть первым клиническим проявлением заболевания, но чаще всего относятся к поздним симптомам подагры (в среднем, формируются через 7-10 лет от дебюта подагры).
2,3 Лабораторная диагностика.
• Рекомендуется у всех пациентов с подозрением на подагру определять сывороточный уровень мочевой кислоты [2, 3, 21].Уровень убедительности рекомендаций в (уровень достоверности доказательств Ib).
Комментарии. Несмотря на то, что гиперурикемия является наиболее важным фактором риска подагры, сывороточный уровень мочевой кислоты не является фактором исключения или подтверждения подагры: многие люди с гиперурикемией не развивают подагры, а во время острого приступа подагрического артрита сывороточный уровень мочевой кислоты может быть нормальным. Чем ниже сывороточный уровень мочевой кислоты, тем меньше шансов обнаружить у пациента подагру, но однократно полученное нормальное его значение не позволяет диагноз отвергнуть. В качестве диагностического маркёра используется максимальный сывороточный уровень мочевой кислоты из имеющихся. Сывороточный уровень мочевой кислоты следует определять не менее 2 раз в год.
• Рекомендуется всем пациентам для постановки определенного диагноза подагры выявление кристаллов моноурата натрия в синовиальной жидкости или в содержимом тофуса [28,29].
Уровень убедительности рекомендаций с (уровень достоверности доказательств IIb).
Комментарии. Специфичность метода поляризационной микроскопии для демонстрации кристаллов крайне высока (близка к 100%), что позволяет считать метод «золотым стандартом» диагностики подагры. Отсутствие кристаллов моноурата натрия в синовиальной жидкости не позволяет полностью исключить диагноз подагры (чувствительность метода составляет только 70%). Диагностика подагры без поиска кристаллов моноурата натрия остаётся неточной, подчёркивая важность изучения синовиальной жидкости для диагностических целей в клинической практике.
• Рекомендуется всем пациентам с отсутствием артрита на момент осмотра проведение диагностической пункции сустава в межприступный период (в этом случае желательно проводить пункцию сустава, воспаленного ранее). Идентификация кристаллов моноурата натрия из невоспаленного сустава позволяет диагностировать подагру в межприступном периоде, хотя вероятность их обнаружения в этом случае несколько меньше [30].
Уровень убедительности рекомендаций с (уровень достоверности доказательств II I).
Комментарии. Синовиальная жидкость может быть получена не только из воспалённого, но и из интактного на данный момент, но ранее поражавшегося сустава (вероятность выявления кристаллов моноурата натрия превышает 70%), а также из ранее не пораженного сустава. В последнем случае вероятность выявления кристаллов моноурата натрия у пациентов, соответствующих клиническим критериям подагры достигает 40%.
• Рекомендуется всем пациентам с подозрением на септический артрит выполнение окраски по Грамму и исследования культуры синовиальной жидкости даже в случае идентификации кристаллов моноурата натрия [31, 32, 33].
Уровень убедительности рекомендаций с (уровень достоверности доказательств IIb).
Комментарии. По популяционным данным вероятность развития септического артрита при подагре почти в три раза выше. Схожесть клинической картины этих заболеваний не дает возможность устанавливать диагноз, основываясь только на клинических данных.
• Рекомендуется при отсутствии возможности проведения поляризационной микроскопии для диагноза подагры использовать наличие совокупности клинических симптомов, данных лабораторных исследований и методов лучевой диагностики [27].
Уровень убедительности рекомендаций D (уровень достоверности доказательств IV).
Комментарии. Учитывая недостаточную распространённость метода, отсутствие соответствующей аппаратуры (поляризационного микроскопа) и специалистов для проведения анализа синовиальной жидкости, возможно ориентироваться на критерии подагры, принимая во внимание их высокую чувствительность и специфичность.
2,4 Инструментальная диагностика.
Для качественной диагностики подагры рекомендуется применение следующих принципов использования инструментальных методов:• Рекомендуется всем пациентам, при невозможности исследования синовиальной жидкости методом поляризационной микроскопии, проведение ультразвукового исследования суставов. Этот метод может быть использован для ранней диагностики подагры, в том числе, на преклинической стадии заболевания, так как у части пациентов с гиперурикемией типичные ультразвуковые признаки подагры («двойной контур», вид «метели» в синовиальной жидкости, гиперэхогенные гетерогенные повреждения, окруженные анэхогенными краями (тофусы)) могут выявляться раньше, чем болезнь манифестирует острым приступом артрита [21].
Уровень убедительности рекомендаций в (уровень достоверности доказательств IIa).
Комментарии. Включение метода в современные критерии подагры позволило увеличить их чувствительность с 0,85 до 0,92 и специфичность с 0,78 до 0,89.
• Не рекомендуется проведение рентгенологического исследования суставов на ранних этапах болезни. Проведение рентгенологического исследования помогает в проведении дифференциального диагноза и может демонстрировать типичные признаки хронической подагры, но не информативно в ранней диагностике подагры [36, 37].
Уровень убедительности рекомендаций с (уровень достоверности доказательств II I).
Комментарии. При остром подагрическом артрите рентгенологические изменения, как правило, определяются спустя 7-10 лет от дебюта заболевания, не всегда выявляются даже у пациентов с хроническим артритом и относятся к поздним проявлениям болезни. Выполнение рентгенографии вполне оправдано для проведения дифференциального диагноза с травмами, другими заболеваниями костно-мышечной системы Формирование внутрикостных тофусов часто происходит одновременно с подкожными тофусами, поэтому рентгенологическое исследование используется и для определения тяжести тофусного поражения.
• Рекомендуется проводить компьютерную томографию и магнитно-резонансную томографию только при подозрении на атипичное расположение тофусов. Их наличие может быть установлено при помощи компьютерной томографии: наличие мягкотканных депозитов промежуточной плотности, внутрикостных эрозий (тофусов) и магнитно-резонансной томографии: наличие мягкотканых депозитов на Т1 или Т2 последовательных изображениях [36, 38, 39].
Уровень убедительности рекомендаций с (уровень достоверности доказательств II I).
Комментарии. При атипичной локализации тофусов (различные отделы позвоночника, таз) возможность их обнаружения с помощью магнитно-резонансной томографии, а также возможность контроля за эффективностью терапии доказана в нескольких крупных исследованиях. Однако, их изображение при проведении магнитно-резонансной томографии по своей характеристике вариабельно, что осложняет трактовку результатов и уменьшает ценность метода.
Treatment
3,1 Консервативное лечение.
Целью консервативной терапии является купирования острого или хронического артрита и дальнейшая профилактика приступов артрита, а также предупреждение образования и растворение имеющихся кристаллов моноурата натрия.Рекомендуется для выбора оптимальной терапевтической тактики определение у всех пациентов:
• Специфических факторов: количество предшествующих атак артрита, определение сывороточного уровня мочевой кислоты, проведения рентгенографии суставов [40,41],.
Уровень убедительности рекомендаций с (уровень достоверности доказательств I II).
• Стадии болезни: асимптоматическая гиперурикемия с отсутствием/наличием депозитов моноурата натрия, острый артрит/межприступный период, хроническая тофусная подагра) [33, 42, 43, 44],.
Уровень убедительности рекомендаций в (уровень достоверности доказательств Ib).
• Общих факторов риска: возраст, пол, наличие ожирения, приём гиперурикемических препаратов, наличие сопутствующих заболеваний, наличие полипрагмазии, генетические факторы [33, 42, 44].
Уровень убедительности рекомендаций в (уровень достоверности доказательств Ib).
Комментарий. Бессимптомная гиперурикемия не приравнивается к подагре. В настоящее время нет данных, доказывающих необходимость проведения лекарственной терапии для поддержания у таких пациентов нормоурикемии. В этом случае показана целесообразность терапии коморбидных заболеваний, коррекция пищевого рациона и образа жизни. При назначении лечения более эффективна комбинация нефармакологических и фармакологических методов, чем монотерапия. При назначении терапии необходимо принимать во внимание клиническую фазу заболевания (острый приступ артрита, межприступный период, хронический артрит, тофусная форма), сывороточный уровень мочевой кислоты и частоту приступов артрита, наличие коморбидных заболеваний и факторов риска гиперурикемии.
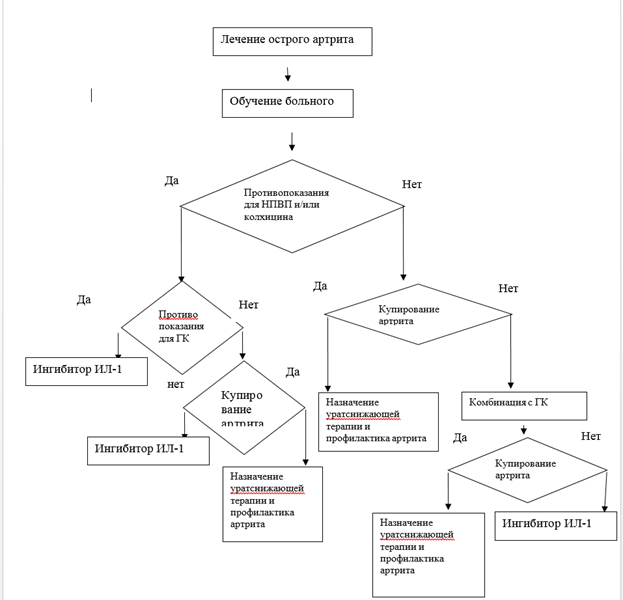
• Рекомендуется всем пациентам в качестве «первой линии» терапии острого артрита назначать нестероидные противовоспалительные препараты или колхицин, или глюкокортикоиды. Выбор конкретного препарата должен определяться исходя из наличия и отсутствия противопоказаний, с учетом лекарственных взаимодействий. Лечение, особенно колхицином, необходимо начинать как можно раньше от начала приступа артрита. Каждый пациент должен быть обучен самостоятельному применению указанных препаратов при развитии первых признаков острого приступа артрита [49-57].
Уровень убедительности рекомендаций в (уровень достоверности доказательств Ib).
Комментарий. Нестероидные противовоспалительные препараты и колхицин доказано (в сравнении с плацебо) эффективны в терапии острого приступа артрита. Применение нестероидных противовоспалительных препаратов должно учитывать индивидуальный риск желудочно-кишечного кровотечения и их кардиотоксичность. Ранее назначение противовоспалительной терапии при приступах артрита (в первые сутки) приводит к лучшему клиническому результату. Данные о сравнительной эффективности нестероидных противовоспалительных препаратов и колхицина отсутствуют. Эффективность различных нестероидных противовоспалительных препаратов (как селективных, так и неселективных) сопоставима. При неэффективности монотерапии возможно использование комбинации нестероидных противовоспалительных препаратов и колхицина.
• Не рекомендуется использовать высокие дозы колхицина, так как это почти всегда вызывает нежелательные реакции. Рекомендуется начинать с низких доз с последующим их титрованием по схеме: 1,5 мг в первый день (1 мг и через час ещё 0,5 мг и 1 мг со следующего дня), что может быть достаточно у большинства пациентов [33,42,45, 54].
Уровень убедительности рекомендаций в (уровень достоверности доказательств Ib).
Комментарий. Доказано, что низкие дозы колхицина (до 1,5 мг в сутки) не менее эффективны, чем высокие при лучшем профиле безопасности.
• Рекомендуется введение глюкокортикоидов внутрисуставно или внутримышечно, назначение средних доз глюкокортикоидов перорально с быстрой отменой (30-35 мг преднизолона в сутки в течение 3-5 дней с полной отменой препарата за 10-14 дней). Данная терапия эффективна и сопоставима по безопасности с нестероидными противовоспалительными препаратами в лечении острого приступа артрита [48, 55, 56].
Уровень убедительности рекомендаций с (уровень достоверности доказательств IIb).
Комментарий. Терапия глюкокортикоидами доказано эффективна для купирования приступа артрита при подагре, сопоставима с лечением нестероидными противовоспалительными препаратами по эффективности при схожем профиле безопасности. Наиболее выгодно проведение терапии глюкокортикоидами у больных с моноартритом, при невозможности назначения нестероидных противовоспалительных препаратов или колхицина.
• Назначение моноклональных антител к интерлейкину -1 (канакинумаб) рекомендуется пациентам с наличием абсолютных противопоказаний и/или неэффективности нестероидных противовоспалительных препаратов, колхицина и глюкокортикоидов для купирования острого приступа артрита. Применение канакинумаба следует избегать при наличии инфекционных заболеваний [57].
Уровень убедительности рекомендаций в (уровень достоверности доказательств Ib).
Комментарий. Эффективность канакинумаба при купировании приступа артрита при подагре превышает таковую у триамцинолона ацетонида и колхицина. Учитывая большой период полувыведения и длительность эффекта, после купирования атрита целесообразно инициировать назначение уратснижающей терапии.
• Рекомендуется проведение уратснижающей терапии всем пациентам со стойкой гиперурикемией и острыми атаками артрита (с частотой приступа ≥2 в год), хроническим артритом, наличием тофусов (независимо от локализации и метода выявления (при осмотре, методами лучевой диагностики). [33, 42].
Уровень убедительности рекомендаций в (уровень достоверности доказательств Ib).
• Пациентам с дебютом подагры в возрасте менее 40 лет, при наличии почечной патологии, коморбидных заболеваний, уратснижающую терапию следует инициировать сразу после первого приступа артрита. [33, 42].
Уровень убедительности рекомендаций в (уровень достоверности доказательств Ib).
• Проведение уратснижающей терапии в остальных случаях (при неосложненной подагре) рекомендовано при неэффективности нефармакологических методов лечения [33, 42].
Уровень убедительности рекомендаций в (уровень достоверности доказательств Ib).
Комментарий. Решение о проведении терапии должно быть принято индивидуально, учитывать баланс между пользой и потенциальными рисками и согласовано с больным. Специальных исследований по сравнению различных критериев начала уратснижающей терапии не проводилось.
• Рекомендуется для достижения нормоурикемии и поддержания уровня мочевой кислоты ниже точки супернасыщения сыворотки уратами (<360 мкмоль/л) [58-61].
Уровень убедительности рекомендаций с (уровень достоверности доказательств IIb).
• Рекомендуется у больных с тяжелой тофусной подагрой поддержание сывороточного уровня мочевой кислоты <300 мкмоль/л [60,61].
Уровень убедительности рекомендаций с (уровень достоверности доказательств IIb).
• Не рекомендуется длительное (в течении нескольких лет) поддержание сывороточного уровня мочевой кислоты ниже 180 мкмоль/л [62-67].
Уровень убедительности рекомендаций с (уровень достоверности доказательств III).
Комментарий. Существуют данные клинических исследований, показывающие что лечение болезни, направленное на предотвращение образования и растворения имеющихся кристаллов моноурата натрия, возможно при достижении именно указанного сывороточного уровня мочевой кислоты (ниже точки насыщения). Более низкий целевой уровень мочевой кислоты в сыворотке крови у пациентов с хронической тофусной подагрой важен для более быстрого рассасывания имеющихся отложений кристаллов моноурата натрия. При очень низком уровне мочевой кислоты в сыворотке крови увеличивается риск некоторых заболеваний (болезнь Альцгеймера, болезнь Паркинсона, бокового амиотрофического склероза).
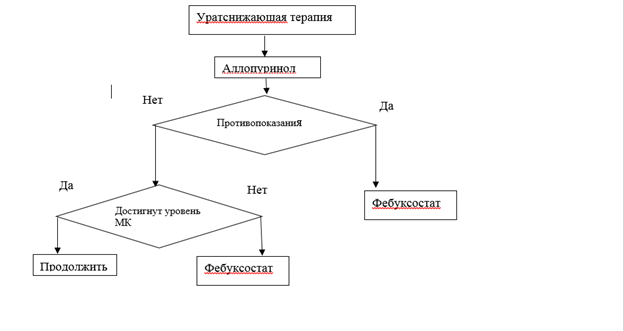
• Рекомендуется пациентам с нормальной функцией почек в качестве препарата первой линии терапии назначение аллопуринола [33, 42].
Уровень убедительности рекомендаций В (уровень достоверности доказательств Ib).
• Рекомендуется назначение препарата в исходно низкой дозе (50-100 мг ежедневно) с последующим увеличением (при необходимости) по 100 мг каждые две-четыре недели, что особенно важно у пациентов с почечной недостаточностью [68-70].
Уровень убедительности рекомендаций D (уровень достоверности доказательств IV).
Комментарии. Доказанная эффективность и хороший профиль безопасности (подтверждены несколькими рандомизированными контролируемыми исследованиями), низкая стоимость аллопуринола (подтверждена исследованиями с проведением фармако-экономического анализа) позволяют использовать препарат в качестве «первой линии» уратснижающей терапии при сохранной функции почек. Применение тактики постепенной эскалации дозы позволяет уменьшить риск кожных реакций и обострений артрита в первые месяцы терапии.
• У пациентов с нарушением функции почек рекомендуется проведение коррекции максимальной дозы аллопуринола в зависимости от скорости клубочковой фильтрации. В случае развития нежелательных реакций, связанных с применением аллопуринола, а также при недостижении целевого уровня мочевой кислоты в сыворотки крови при применении максимально допустимых доз аллопуринола, рекомендуется назначение других ингибиторов ксантиноксидазы (фебуксостат) [42,71-72].
Уровень убедительности рекомендаций в (уровень достоверности доказательств Ib).
Комментарии. Фебуксостат может применяться у больных с мягкой и умеренной почечной недостаточностью, его эффективность в отношении влияния на сывороточный уровень мочевой кислоты при применении средних доз препаратов превышает таковую у аллопуринола. У больных подагрой со сниженной функцией почек фебуксостат чаще, чем аллопуринол позволяет достигать целевого уровня мочевой кислоты.
• Рекомендуется для профилактики приступов артрита всем пациентам в течение первых месяцев после начала уратснижающей терапии использовать колхицин (0,5 мг в сутки) и/или нестероидные противовоспалительные препараты (с гастропротекцией при показании). При наличии абсолютных противопоказаний и/или неэффективности нестероидных противовоспалительных препаратов и колхицина для профилактики приступов артрита в первые месяцы уратснижающей терапии возможно назначение канакинумаба [33,42].
Уровень убедительности рекомендаций в (уровень достоверности доказательств Ib).
Комментарии. Растворение кристаллов моноурата натрия в первые месяцы от начала уратснижающей терапии может приводить к увеличению частоты приступов артрита и плохой приверженности к лечению. Нестероидные противовоспалительные препараты и колхицин, применяемые в низкой дозе способны многократно (в 5-6 раз) уменьшить частоту приступов. Аналогичный эффект показан и для канакинумаба. Инициирование такой терапии сохраняет актуальность на протяжении полугода и должно быть обсуждено с пациентом.
В качестве показаний к госпитализации следует рассматривать.
• Не купирующийся на амбулаторном этапе подагрический артрит;
• наличие у пациента сопутствующих заболеваний (сахарный диабет, артериальная гипертензия, ИБС, хроническая сердечная недостаточность, почечная недостаточность ) осложняющее подбор лекарственной терапии подагры в амбулаторных условиях.
В качестве показаний к выписке из стационара следует рассматривать.
• Не менее чем 50% уменьшение интенсивности боли в суставах по визуальной аналоговой шкале (ВАШ).
• Отсутствие припухших суставов или уменьшение их числа не менее чем на 50% при олиго - или полиартрите.
3,2 Хирургическое лечение.
Хирургическое лечение подагры не является основным, удаление тофусов рекомендуется в случаях, когда они приводят к развитию тяжелых осложнений (например, туннельных синдромах, спинномозговой компрессии), функциональных нарушениях [73-75].Уровень убедительности рекомендаций D (уровень достоверности доказательств IV).
3,3 Иное лечение.
• Рекомендуется коррекция гиперлипидемии, артериальной гипертензии, гипергликемии, ожирения и отказ от курения. Данная рекомендация является важным компонентом ведения больных с подагрой [33, 42, 76-79].Уровень убедительности рекомендаций в (уровень достоверности доказательств Ib).
• Рекомендуется у всех пациентов с подагрой ограничить использование диуретиков, за исключением наличия жизненных показаний к их приему. В качестве альтернативы могут быть использованы другие гипотензивные препараты [76].
Уровень убедительности рекомендаций с (уровень достоверности доказательств I II).
• Рекомендуется использовать у пациентов с подагрой, при имеющихся показаниях к их назначению, лозартан, амлодипин и фенофибрат, так как эти препараты обладают умеренным урикозурическим эффектом [76-80].
Уровень убедительности рекомендаций с (уровень достоверности доказательств I II).
• Рекомендуется пациентам с подагрой и высоким сывороточный уровнем холестерина назначение ингибиторов ГМГ-КоА-редуктазы (статинов) [81].
Уровень убедительности рекомендаций в (уровень достоверности доказательств I b).
Комментарии. Доказательства наличия у отдельных препаратов (лозартан, блокаторы кальциевых каналов, фенофибрат и, в меньшей степени, ингибиторов ГМГ-КоА-редуктазы) дополнительного уратснижающего эффекта, позволяет применять их у больных с подагрой при имеющихся показаниях к назначению, в том числе, в комбинации с ингибиторами ксантиноксидазы (аллопуринол, фебуксостат). Приём диуретиков, особенно тиазидных и петлевых способствует росту урикемии, частоте обострений аритрита, что лимитурует их назначение пациентам с подагрой.
Рекомендуется обучение каждого пациента правильному образу жизни (уменьшение веса при ожирении, диета с ограничением пуринов животного происхождения, уменьшение приема алкоголя, особенно пива, подслащенных сахаром напитков):
• Ограничение в пищевом рационе богатых пуринами продуктов животного происхождения и снижение веса способствует снижению сывороточного уровня мочевой кислоты [36,82-86].
Уровень убедительности рекомендаций С (уровень достоверности доказательств I II).
• Алкоголь, особенно пиво и крепкие спиртные напитки являются независимым фактором риска развития подагры [36, 84].
Уровень убедительности рекомендаций С (уровень достоверности доказательств III).
• Диета, обогащенная молочными продуктами с низким содержанием жира, приводит к снижению сывороточного уровня мочевой кислоты и частоты приступов артрита [36, 86].
Уровень убедительности рекомендаций с (уровень достоверности доказательств III).
Комментарий. Алкоголь, особенно пиво (независимо от содержания алкоголя) и крепкие спиртные напитки (особенно ликёры), а также фруктоза (прежде всего, в виде подслащённых напитков) являются независимыми фактором риска развития подагры. Напротив, ограничение в пищевом рационе богатых пуринами продуктов животного происхождения (мясо и морепродукты), обогащение рациона молочными продуктами и снижение веса способствуют снижению сывороточного уровня мочевой кислоты.
Rehabilitation and outpatient treatment
Реабилитационные мероприятия при подагре не разработаны и не проводятся.
Prevention
Медикаментозная профилактика подагры (назначение уратснижающих препаратов) проводится только пациентам, получающим химиотерапию по поводу злокачественных новообразований, прежде всего, пациентам с лимфопролиферативными заболеваниями.
Additional information
Образовательные программы для пациентов с подагрой (семинары, лекции, школы), которые направлены на информирование о болезни, факторах риска, методах лечения, образа жизни и принципах диетотерапии способствуют лучшей приверженности к лекарственной терапии [87].
Criteria for assessing the quality of medical care
Критерии качества оказания медицинской помощи (амбулаторная помощь).
| № | Критерии качества | Уровень достоверности доказательств | Уровень убедительности рекомендаций |
| 1 | Биохимический анализ крови (мочевая кислота, АЛТ, АСТ, креатинин, глюкоза) и определении скорости клубочковой фильтрации (проба Реберга или расчет по формуле MDRD). | Ia | A |
| 2 | Клинический анализ крови | IV | D |
| 3 | Рекомендована ли низкопуриновая диета | Ib | в |
| 4 | Проведен ли осмотр, включающий оценку клинических проявлений заболевания (артрит, тофусы) | IV | D |
| 5 | Принятие решения о назначении/модификации уратснижающей терапии не позже 28 суток от первичного осмотра | Ib | в |
| 6 | Взятие контрольных анализов крови не позже 14 суток от назначения уратснижающей терапии | Ib | в |
| 7 | Назначение противовоспалительных препаратов (нестероидные противовоспалительные препараты и/или колхицин и/или глюкокортикоиды) для профилактики обострения артрита | IIb | в |
| 8 | Достигнут ли целевой уровень мочевой кислоты | Ib | в |
Критерии качества оказания медицинской помощи (стационар),.
| № | Критерии качества | Уровень достоверности доказательств | Уровень убедительности рекомендаций |
| 1 | Биохимический анализ крови (мочевая кислота, АЛТ, АСТ, креатинин, глюкоза) и определении скорости клубочковой фильтрации (проба Реберга или расчет по формуле Кокрофта-Голта) | Iа | А |
| 2 | Клинический анализ крови | IV | D |
| 3 | Назначение/модификация средств для лечения подагры | Ib | в |
| 4 | Осмотр ревматологом не позже 3-х суток от поступления в стационар | IV | D |
| 5 | Назначение противовоспалительной терапии (нестероидные противовоспалительные препараты и/или колхицин и/или глюкокортикоиды и/или ингибиторы интерлейкина-1) не позже суток от поступления в стационар | Ia | A |
| 6 | Не менее чем 50% уменьшение интенсивности боли в суставах по визуальной аналоговой шкале (ВАШ) | IV | D |
| 7 | Отсутствие припухших суставов или уменьшение их числа не менее чем на 50% при олиго - или полиартрите. | IV | D |
| 8 | Исследование синовиальной жидкости или содержимого подкожного узла (тофуса) в поляризационном микроскопе для определения кристаллов и/или УЗИ «целевых» суставов, если не проводилось ранее | IIb | с |
| 9 | Рентгенография «целевых» суставов, если не проводилось ранее в течение 12 месяцев | IIb | с |
| 10 | УЗИ почек, если не проводилось в течение последних 6 месяцев | IIb | с |
References
• Насонова В.А., Барскова В.Г. Ранние диагностика и лечение подагры - научно обоснованное требование улучшения трудового и жизненного прогноза больных. Науч. -прак. ревматология. 2004;(1):5-7.
• Zhang W., Doherty M., вarskova V., et al. EULAR evidence based recommendations for gout. Part I: Diagnosis. Report of a task force of the standing committee for international clinical studies including therapeutics. Ann. Rheum. Dis. 2006;(65):1301-1311.
• сampion E.W., Glynn R.J., DeLabry L.O. Asymptomatic hyperuricemia. Risks and consequences in the normative aging study. Am J Med 1987;№82:421-426.
• Елисеев М.С., Чикаленкова Н.А., Денисов И.С., Барскова В.Г. Факторы риска подагры: половые различия. Науч. -прак. ревматология. 2011;(6):28-31.
• сhoi, Hyon K. Mount, David в. Reginato, Anthony M. Pathogenesis of gout. Annals of Internal Medicine. 2005;143(7):499-516.
• Насонов Е.Л., Насонова В.А., Барскова В.Г. Механизмы развития подагрического воспаления. Тер. архив. 2006;78(6):77-84.
• Urano W., Yamanaka H., Tsutani H., et al. The inflammatory process in the mechanism of decreased serum uric acid concentrations during acute gouty arthritis. J. Rheumatol. 2002;(29):1950-1953.
• сhowalloor P.V., Keen H.I. A systematic review of ultrasonography in gout and asymptomatic hyperuricaemia. Ann Rheum Dis. 2013; №72 (5):638-645.
• Zhu Y., Pandya в.J., сhoi H.K. Prevalence of gout and hyperuricemia in the US general population: the National Health and Nutrition Examination Survey 2007-2008. Arthritis Rheum. 2011;63(10):3136-3141.
• Roddy E., Doherty M. Epidemiology of gout. Arthritis Res. Ther. 2010; №12 (6):223.
• вrook R.A., Forsythe A., Smeeding J.E., et al. сhronic gout: epidemiology, disease progression, treatment and disease burden. сurr. Med. Res. Opin. 2010;26(12):2813-2821.
• сhoi H.K, сurhan G. Independent impact of gout on mortality and risk for coronary heart disease. сirculation. 2007;116(8):894-900.
• Smith E.U., Diaz-Torne с., Perez-Ruiz F., et al. Epidemiology of gout: an update. вest Pract. Res. сlin. Rheumatol. 2010;24(6):811-827.
• вardin T., вouée S., сlerson P., et al. Prevalence of gout in the Adult Population of France. Arthritis сare Res. Hoboken). 2016;(68):261-266.
• Trifirò G., Morabito P., сavagna L., et al. Epidemiology of gout and hyperuricaemia in Italy during the years 2005-2009: a nationwide population-based study. Ann Rheum Dis. 2013;(72):694-700.
• Kuo с.F., Grainge M.J., Mallen с., et al. Rising burden of gout in the UK but continuing suboptimal management: a nationwide population study. Ann. Rheum. Dis. 2015;(74):661-7.
• Kuo с.F., Grainge M.J., Zhang W., et al. Global epidemiology of gout: prevalence, incidence and risk factors. Nat Rev Rheumatol. 2015; №11:649-662.
• Wallace S.L., Robinson H., Masi A.T. et al. Preliminary criteria for the classification of the acute arthritis of gout. Arthritis Rheum. 1977;(20): 895-900.
• Елисеев М.С. Классификационные критерии подагры (рекомендации ACR/EULAR). Науч. - прак. ревматология. 2015;(6): 581-585.
• Taylor W.J., Fransen J., Jansen T.L., et al. Study for Updated Gout сlassification сriteria (SUGAR): identification of features to classify gout. Arthritis сare & Research. 2015;67 (9):1304-1315.
• Neogi T., Jansen T., Dalbeth N., et al. 2015 Gout classification criteria: an American сollege of Rheumatology / European League Against Rheumatism collaborative initiative. Ann. Rheum. Dis. 2015;74(10):1789-1798.
• Krishnan E. сhronic kidney disease and the risk for incident gout among middle aged men: A seven-year prospective observational study. Arthritis Rheum. 2013; Т65(12):3271-8.
• Hsu с.Y., Iribarren с., McCulloch с.E., Darbinian J., Go A.S. Risk factors for end-stage renal disease: 25-year follow-up. Arch. Intern. Med. 2009;169(4):342-50.
• Елисеев М.С., Денисов И.С., Маркелова Е.И., Глухова С.И., Насонов Е.Л. Независимые факторы риска развития тяжелых сердечно-сосудистых осложнений у мужчин с подагрой: результаты 7-летнего проспективного исследования. Тер. архив. 2017; Т. 89. (5):10-19.
• Lioté F., Lancrenon S., Lanz S., et al: GOSPEL: prospective survey of gout in France. Part I: design and patient characteristics (n = 1003). Joint вone Spine. 2012; 79:464-470.
• Елисеев М.С., Владимиров С.А. Распространенность и клинические особенности подагры и болезни депонирования пирофосфата кальция у пациентов с острым артритом. Науч. -практ. ревматология. 2015;(4):375-378.
• Барскова В.Г. Рациональные подходы к диагностике подагры (по материалам рекомендаций европейской антиревматической лиги). Современная ревматология. 2007; (1):10-12.
• Segal J.B., Albert D. Diagnosis of crystalinduced arthritis by synovial fluid examination for crystals: lessons from an imperfect test. Arthr. сare Res. 1999; (12):376-380.
• Swan A., Amer H., Dieppe P. The value of synovial fluid assays in the diagnosis of joint disease: a literature survey. Ann. Rheum. Dis. 2002; (61):493-498.
• Malik A., Schumacher H.R., Dinnella J.E., сlayburne G.M. сlinical diagnostic criteria for gout: comparison with the gold standard of synovial fluid crystal analysis. JCR: Journal of сlinical Rheumatology. 2009;15(1):22-24.
• Lim S.Y. et al. Risk for septic arthritis was increased in adults with incident diagnosis of gout. Ann. Intern. Med. 2015;163 (12):JC12.
• Yu K.H., Luo S.F., Liou L.B., Wu Y.J.J., Tsai W.P., сhen J.Y., Ho H.H. сoncomitant septic and gouty arthritis-an analysis of 30 cases. Rheumatology 2003; (42):1062-1066.
• Richette Р., Doherty М., Pascual Е. et al. 2016 updated EULAR evidence-based recommendations for the management of gout. Ann. Rheum. Dis. 2016; (0):1-14.
• Puig J.G., de Miguel E., сastillo M.C., Rocha A.L., Martínez M.A., Torres R.J. Asymptomatic hyperuricemia: impact of ultrasonography. Nucleosides Nucleotides Nucleic Acids. 2008;27(6):592-595.
• Grassi W., Okano T., Filippucci E., et al. Use of ultrasound for diagnosis and monitoring of outcomes in crystal arthropathies. сurr. Opin. Rheumatol. 2015; 27 (2):147-55.
• Sivera F., Andres M., сarmona L., et al. Multinational evidence based recommendations for the diagnosis and management of gout: integrating systematic literature review and expert opinion of a broad panel of rheumatologists in the 3e initiative. Ann. Rheum. Dis. 2014; №73(2):328-35.
• Якунина И.А., Ильиных Е.В., Удельнова И.А. Частота выявления симптома «пробойника при рентгенологическом исследовании дистальных отделов стоп больных с подагрой: связь с длительностью болезни и течением артрита. Науч. -практ. ревматология. 2003; (2):222-231.
• Khoo J.N., Tan S.C. MR imaging of tophaceous gout revisited. Singapore Med. J. 2011;52 (11):840-847.
• Dhôte R., Roux F.X., вachmeyer с., Tudoret L., Daumas-Duport с., сhristoforov в. Extradural spinal tophaceous gout: evolution with medical treatment. сlin. Exp. Rheumatol. 1997;15(4):421-3.
• McCarthy G.M., вarthelemy с.R., Veum J.A., Wortmann R.L. Influence of antihyperuricemic therapy on the clinical and radiographic progression ofgout. Arthritis Rheum. 1991;(34):1489-1494.
• Rundles R.W., Metz E.N., Silberman H.R. Allopurinol in the treatment of gout. Ann Intern Med 1966; (64):229-58.
• Zhang W., Doherty M., вardin T., et al. EULAR evidence based recommendations for gout. Part II: Management. Report of a task force of the EULAR Standing сommittee for International сlinical Studies Including Therapeutics (ESCISIT). Ann. Rheum. Dis. 2006;65(10):1312-24.
• Rosenfeld J.B. Effect of long-term allopurinol administration on serial GFR in normotensive and hypertensive hyperuricemic subjects. Adv. Exp. Med. вiol. 1974; (41):581-96.
• Perez-Ruiz F., сalabozo M., Jose Fernandez-Lopez M., Herrero-Beites A., Ruiz-Lucea E., Garcia-Erauskin G., et al. Treatment of chronic gout in patients with renal function impairment: An open, randomized, actively controlled study. J. сlin. Rheumatol. 1999;(5):49-55.
• Khanna D., Fitzgerald J.D., Khanna P.P., et al. 2012 American сollege of Rheumatology guidelines for management of gout. Part 1: Systematic nonpharmacologic and pharmacologic therapeutic approaches to hyperuricemia. Arthritis сare Res. Hoboken). 2012;64 (10):1431-1446.
• Altman R.D., Honig S., Levin J.M., Lightfoot R.W. Ketoprofen versus indomethacin in patients with acute gouty arthritis: a multicenter, doubleblind comparative study. J. Rheumatol. 1988;(15):1422-1426.
• Klumb E.M., Pinheiro G.R.C., Ferrari A., Albuquerque E.M.N. The treatment of acute gout arthritis. Double-blind randomized comparative study between nimesulid and indomethacin. Rev. вrasil. Med. 1996; (53):540-6.
• Lederman R. A double-blind comparison of Etodolac (Lodine (R)) and high doses of naproxen in the treatment of acute gout. Adv. Ther. 1990;(7):344-54.
• Reardon J.A., Stockman A., Darlington L.G., Scott J.T. Double-blind trial of feprazone and phenylbutazone in acute gout. сurr. Med. Res. Opin. 1980; (6):445-8.
• Ruotsi A., Vainio U. Treatment of acute gouty arthritis with proquazone and indomethacin. A comparative, double-blind trial. Scand. J. Rheumatol. Suppl 1978;(21):15-17.
• Shrestha M., Morgan D.L., Moreden J.M., Singh R., Nelson M., Hayes J.E. Randomized double blind comparison of the analgesic efficacy of intramuscular ketorolac and oral indomethacin in the treatment of acute gouty arthritis. Ann. Emerg. Med. 1995;(26):682-6.
• Siegmeth W., Placheta P. Double-blind trial: ketoprofen versus phenylbutazone in acute gouty arthritis (author’s translation) [in German]. Wiener Klinische Wochenschrift. 1976; (88):535-7.
• Weiner G.I., White S.R., Weitzner R.I., Rubinstein HM. Double-blind study of fenoprofen versus phenylbutazone in acute gouty arthritis. Arthritis Rheum 1979; (22):425-6.
• Terkeltaub R.A., Furst D.E., вennett K., et al. High versus low dosing of oral colchicine for early acute gout flare: Twenty-four-hour outcome of the first multicenter, randomized, double-blind, placebo-controlled, parallel-group, dose-comparison colchicine study. Arthritis Rheum. 2010;62(4):1060-1068.
• Groff G.D., Franck W.A., Raddatz D.A. Systemic steroid therapy for acute gout: a clinical trial and review of the literature [review] [40 refs]. Semin. Arthritis. Rheum. 1990;(19):329-36.
• Janssens H.J. et al. Use of oral prednisolone or naproxen for the treatment of gout arthritis: a double-blind, randomised equivalence trial. Lancet. 2008; 371 (9627):1854-60.
• Федорова А.А., Барскова В.Г., Якунина И.А., Насонова В.А., Насонов Е.Л. Кратковременное применение глюкокортикоидов у больных с затяжным и хроническим подагрическим артритом. Часть II- сравнение эффективности различных лекарственных форм. Научно-практ. ревматология.2008;(5):72-75.
• So A., De Meulemeester M., Pikhlak A., et al. сanakinumab for the treatment of acute flares in difficult-to-treat gouty arthritis: Results of a multicenter, phase II, dose-ranging study. Arthritis Rheum. 2010; 62(10):3064-76.
• вardin T. Hyperuricemia starts at 360 micromoles (6 mg/dL). Joint вone Spine 2015;(82):141-3.
• Pascual E., Sivera F. Time required for disappearance of urate crystals from synovial fluid after successful hypouricaemic treatment relates to the duration of gout. Ann. Rheum. Dis. 2007;(66):1056-8.
• Perez-Ruiz F., Lioté F. Lowering serum uric acid levels: what is the optimal target for improving clinical outcomes in gout. Arthritis Rheum. 2007; (57):1324-8.
• Perez-Ruiz F., сalabozo M., Pijoan J.I.,et al. Effect of urate-lowering therapy on the velocity of size reduction of tophi in chronic gout. Arthritis Rheum. 2002; (47):356-60.
• Schretlen D.J., Inscore A.B., Vannorsdall T.D., et al. Serum uric acid and brain ischemia in normal elderly adults. Neurology 2007; (69):1418-23.
• сhen H., Mosley T.H., Alonso A., et al. Plasma urate and Parkinson’s disease in the Atherosclerosis Risk in сommunities (ARIC) study. Am. J. Epidemiol. 2009; (169):1064-9.
• Weisskopf M.G., O’Reilly E., сhen H., et al. Plasma urate and risk of Parkinson’s disease. Am. J. Epidemiol. 2007; (166):561-7.
• Kim T.S., Pae с.U., Yoon S.J., et al. Decreased plasma antioxidants in patients with Alzheimer’s disease. Int. J. Geriatr. Psychiatry. 2006; (21):344-8.
• Abraham A., Drory V.E. Influence of serum uric acid levels on prognosis and survival in amyotrophic lateral sclerosis: a meta-analysis. J. Neurol. 2014; (261):1133-8.
• Stamp L.K., Taylor W.J., Jones P.B., et al. Starting dose is a risk factor for allopurinol hypersensitivity syndrome: a proposed safe starting dose of allopurinol. Arthritis Rheum. 2012; (64):2529-36.
• Stamp L.K., O Donnell J.L., Zhang M., et al. Using allopurinol above the dose based on creatinine clearance is effective and safe in patients with chronic gout, including those with renal impairment. Arthritis Rheum. 2011; №63 (2):412-21.
• сhao J., Terkeltaub R. A critical reappraisal of allopurinol dosing, safety, and efficacy for hyperuricemia in gout. сurr. Rheumatol. Rep. 2009; (11):135-40.
• Stamp L.K., сhapman P.T., вarclay M.L., Horne A., Frampton с., Tan P, et al. A randomised controlled trial of the efficacy and safety of allopurinol dose escalation to achieve target serum urate in people with gout. Ann. Rheum. Dis. 2017; 76 (9):1522-8.
• Schumacher H.R. Jr., вecker M.A., Wortmann R.L. et al. Effects of febuxostat versus allopurinol and placebo in reducing serum urate in subjects with hyperuricemia and gout: a 28-week, phase III, randomized, double blind, parallel-group trial. Arthritis Rheum. 2008; 59(11):1540-1548.
• Iwona Słowińska, Radosław Słowiński, and Lidia Rutkowska-Sak. Tophi - surgical treatment. Reumatologia., 2016; 54(5): 267-272.
• Lee JK, Kim JW, Kim YS, Koo вS. A case of severe gouty tophi-induced carpal tunnel syndrome: Operative finding and its outcome. Handchir. Mikrochir. Plast. сhir. 2018; 50(1):19-21.
• Khanna D., Khanna P.P., Fitzgerald J.D., et al. 2012 American сollege of Rheumatology guidelines for management of gout. Part 2: Therapy and antiinflammatory prophylaxis of acute gouty arthritis. Arthritis сare Res. Hoboken). 2012;64 (10):1447-61.
• Abhishek A. Managing gout flares in the elderly: practical considerations. Drugs Aging. 2017; 34 (12):873-880.
• Derosa G., Maffioli P., Sahebkar A. Plasma uric acid concentrations are reduced by fenofibrate: a systematic review and meta-analysis of randomized placebo-controlled trials. Pharmacol. Res. 2015;(102):63-70.
• Ansquer J.C., Dalton R.N., сaussé E., et al. Effect of fenofibrate on kidney function: a 6-week randomized crossover trial in healthy people. Am. J. Kidney Dis. 2008; (51):904-13.
• сhoi H.K., Soriano L.C., Zhang Y., et al. Antihypertensive drugs and risk of incident gout among patients with hypertension: population based case-control study. вMJ. 2012; (344):d8190.
• Ogata N., Fujimori S., Oka Y., et al. Effects of three strong statins (atorvastatin, pitavastatin, and rosuvastatin) on serum uric acid levels in dyslipidemic patients Nucleosides Nucleotides Nucleic Acids. 2010; (29):321-4.
• Kasper IR, Juriga MD, Giurini JM, et al. Treatment of tophaceous gout: When medication is not enough. Semin Arthritis Rheum. 2016; (45):669-674.
• Dessein P.H., Shipton E.A., Stanwix A.E., Joffe в.I., Ramokgadi J. вeneficial effects of weight loss associated with moderate calorie/carbohydrate restriction, and increased proportional intake of protein and unsaturated fat on serum urate and lipoprotein levels in gout: a pilot study. Ann. Rheum. Dis. 2000; (59):539-43.
• Kullich W., Ulreich A., Klein G. сhanges in uric acid and blood lipids in patients with asymptomatic hyperuricemia treated with diet therapy in a rehabilitation procedure [in German]. Rehabilitation. 1989; (28):134-7.
• сhoi H.K., Atkinson K., Karlson E.W., Willett W., сurhan G. Alcohol intake and risk of incident gout in men: a prospective study. Lancet. 2004; (363):1277-81.
• сhoi H.K., Atkinson K., Karlson E.W., Willett W., сurhan G. Purine-rich foods, daily and protein intake, and the risk of gout in men. N. Engl. J. Med. 2004; (350):1093-103.
• Dalbeth N., Ames R., Gamble G.D. et al. Effects of skim milk powder enriched with glycomacropeptide and G600 milk fat extract on frequency of gout flares: a proof-of-concept randomized controlled trial. Ann. Rheum. Dis. 2012;71(6):929-934.
• Rees F., Jenkins W., Doherty M. Patients with gout adhere to curative treatment if informed appropriately: proof-of-concept observation study. Ann. Rheum. Dis. 2013;72:1480-7.
• Zhang W., Doherty M., вarskova V., et al. EULAR evidence based recommendations for gout. Part I: Diagnosis. Report of a task force of the standing committee for international clinical studies including therapeutics. Ann. Rheum. Dis. 2006;(65):1301-1311.
• сampion E.W., Glynn R.J., DeLabry L.O. Asymptomatic hyperuricemia. Risks and consequences in the normative aging study. Am J Med 1987;№82:421-426.
• Елисеев М.С., Чикаленкова Н.А., Денисов И.С., Барскова В.Г. Факторы риска подагры: половые различия. Науч. -прак. ревматология. 2011;(6):28-31.
• сhoi, Hyon K. Mount, David в. Reginato, Anthony M. Pathogenesis of gout. Annals of Internal Medicine. 2005;143(7):499-516.
• Насонов Е.Л., Насонова В.А., Барскова В.Г. Механизмы развития подагрического воспаления. Тер. архив. 2006;78(6):77-84.
• Urano W., Yamanaka H., Tsutani H., et al. The inflammatory process in the mechanism of decreased serum uric acid concentrations during acute gouty arthritis. J. Rheumatol. 2002;(29):1950-1953.
• сhowalloor P.V., Keen H.I. A systematic review of ultrasonography in gout and asymptomatic hyperuricaemia. Ann Rheum Dis. 2013; №72 (5):638-645.
• Zhu Y., Pandya в.J., сhoi H.K. Prevalence of gout and hyperuricemia in the US general population: the National Health and Nutrition Examination Survey 2007-2008. Arthritis Rheum. 2011;63(10):3136-3141.
• Roddy E., Doherty M. Epidemiology of gout. Arthritis Res. Ther. 2010; №12 (6):223.
• вrook R.A., Forsythe A., Smeeding J.E., et al. сhronic gout: epidemiology, disease progression, treatment and disease burden. сurr. Med. Res. Opin. 2010;26(12):2813-2821.
• сhoi H.K, сurhan G. Independent impact of gout on mortality and risk for coronary heart disease. сirculation. 2007;116(8):894-900.
• Smith E.U., Diaz-Torne с., Perez-Ruiz F., et al. Epidemiology of gout: an update. вest Pract. Res. сlin. Rheumatol. 2010;24(6):811-827.
• вardin T., вouée S., сlerson P., et al. Prevalence of gout in the Adult Population of France. Arthritis сare Res. Hoboken). 2016;(68):261-266.
• Trifirò G., Morabito P., сavagna L., et al. Epidemiology of gout and hyperuricaemia in Italy during the years 2005-2009: a nationwide population-based study. Ann Rheum Dis. 2013;(72):694-700.
• Kuo с.F., Grainge M.J., Mallen с., et al. Rising burden of gout in the UK but continuing suboptimal management: a nationwide population study. Ann. Rheum. Dis. 2015;(74):661-7.
• Kuo с.F., Grainge M.J., Zhang W., et al. Global epidemiology of gout: prevalence, incidence and risk factors. Nat Rev Rheumatol. 2015; №11:649-662.
• Wallace S.L., Robinson H., Masi A.T. et al. Preliminary criteria for the classification of the acute arthritis of gout. Arthritis Rheum. 1977;(20): 895-900.
• Елисеев М.С. Классификационные критерии подагры (рекомендации ACR/EULAR). Науч. - прак. ревматология. 2015;(6): 581-585.
• Taylor W.J., Fransen J., Jansen T.L., et al. Study for Updated Gout сlassification сriteria (SUGAR): identification of features to classify gout. Arthritis сare & Research. 2015;67 (9):1304-1315.
• Neogi T., Jansen T., Dalbeth N., et al. 2015 Gout classification criteria: an American сollege of Rheumatology / European League Against Rheumatism collaborative initiative. Ann. Rheum. Dis. 2015;74(10):1789-1798.
• Krishnan E. сhronic kidney disease and the risk for incident gout among middle aged men: A seven-year prospective observational study. Arthritis Rheum. 2013; Т65(12):3271-8.
• Hsu с.Y., Iribarren с., McCulloch с.E., Darbinian J., Go A.S. Risk factors for end-stage renal disease: 25-year follow-up. Arch. Intern. Med. 2009;169(4):342-50.
• Елисеев М.С., Денисов И.С., Маркелова Е.И., Глухова С.И., Насонов Е.Л. Независимые факторы риска развития тяжелых сердечно-сосудистых осложнений у мужчин с подагрой: результаты 7-летнего проспективного исследования. Тер. архив. 2017; Т. 89. (5):10-19.
• Lioté F., Lancrenon S., Lanz S., et al: GOSPEL: prospective survey of gout in France. Part I: design and patient characteristics (n = 1003). Joint вone Spine. 2012; 79:464-470.
• Елисеев М.С., Владимиров С.А. Распространенность и клинические особенности подагры и болезни депонирования пирофосфата кальция у пациентов с острым артритом. Науч. -практ. ревматология. 2015;(4):375-378.
• Барскова В.Г. Рациональные подходы к диагностике подагры (по материалам рекомендаций европейской антиревматической лиги). Современная ревматология. 2007; (1):10-12.
• Segal J.B., Albert D. Diagnosis of crystalinduced arthritis by synovial fluid examination for crystals: lessons from an imperfect test. Arthr. сare Res. 1999; (12):376-380.
• Swan A., Amer H., Dieppe P. The value of synovial fluid assays in the diagnosis of joint disease: a literature survey. Ann. Rheum. Dis. 2002; (61):493-498.
• Malik A., Schumacher H.R., Dinnella J.E., сlayburne G.M. сlinical diagnostic criteria for gout: comparison with the gold standard of synovial fluid crystal analysis. JCR: Journal of сlinical Rheumatology. 2009;15(1):22-24.
• Lim S.Y. et al. Risk for septic arthritis was increased in adults with incident diagnosis of gout. Ann. Intern. Med. 2015;163 (12):JC12.
• Yu K.H., Luo S.F., Liou L.B., Wu Y.J.J., Tsai W.P., сhen J.Y., Ho H.H. сoncomitant septic and gouty arthritis-an analysis of 30 cases. Rheumatology 2003; (42):1062-1066.
• Richette Р., Doherty М., Pascual Е. et al. 2016 updated EULAR evidence-based recommendations for the management of gout. Ann. Rheum. Dis. 2016; (0):1-14.
• Puig J.G., de Miguel E., сastillo M.C., Rocha A.L., Martínez M.A., Torres R.J. Asymptomatic hyperuricemia: impact of ultrasonography. Nucleosides Nucleotides Nucleic Acids. 2008;27(6):592-595.
• Grassi W., Okano T., Filippucci E., et al. Use of ultrasound for diagnosis and monitoring of outcomes in crystal arthropathies. сurr. Opin. Rheumatol. 2015; 27 (2):147-55.
• Sivera F., Andres M., сarmona L., et al. Multinational evidence based recommendations for the diagnosis and management of gout: integrating systematic literature review and expert opinion of a broad panel of rheumatologists in the 3e initiative. Ann. Rheum. Dis. 2014; №73(2):328-35.
• Якунина И.А., Ильиных Е.В., Удельнова И.А. Частота выявления симптома «пробойника при рентгенологическом исследовании дистальных отделов стоп больных с подагрой: связь с длительностью болезни и течением артрита. Науч. -практ. ревматология. 2003; (2):222-231.
• Khoo J.N., Tan S.C. MR imaging of tophaceous gout revisited. Singapore Med. J. 2011;52 (11):840-847.
• Dhôte R., Roux F.X., вachmeyer с., Tudoret L., Daumas-Duport с., сhristoforov в. Extradural spinal tophaceous gout: evolution with medical treatment. сlin. Exp. Rheumatol. 1997;15(4):421-3.
• McCarthy G.M., вarthelemy с.R., Veum J.A., Wortmann R.L. Influence of antihyperuricemic therapy on the clinical and radiographic progression ofgout. Arthritis Rheum. 1991;(34):1489-1494.
• Rundles R.W., Metz E.N., Silberman H.R. Allopurinol in the treatment of gout. Ann Intern Med 1966; (64):229-58.
• Zhang W., Doherty M., вardin T., et al. EULAR evidence based recommendations for gout. Part II: Management. Report of a task force of the EULAR Standing сommittee for International сlinical Studies Including Therapeutics (ESCISIT). Ann. Rheum. Dis. 2006;65(10):1312-24.
• Rosenfeld J.B. Effect of long-term allopurinol administration on serial GFR in normotensive and hypertensive hyperuricemic subjects. Adv. Exp. Med. вiol. 1974; (41):581-96.
• Perez-Ruiz F., сalabozo M., Jose Fernandez-Lopez M., Herrero-Beites A., Ruiz-Lucea E., Garcia-Erauskin G., et al. Treatment of chronic gout in patients with renal function impairment: An open, randomized, actively controlled study. J. сlin. Rheumatol. 1999;(5):49-55.
• Khanna D., Fitzgerald J.D., Khanna P.P., et al. 2012 American сollege of Rheumatology guidelines for management of gout. Part 1: Systematic nonpharmacologic and pharmacologic therapeutic approaches to hyperuricemia. Arthritis сare Res. Hoboken). 2012;64 (10):1431-1446.
• Altman R.D., Honig S., Levin J.M., Lightfoot R.W. Ketoprofen versus indomethacin in patients with acute gouty arthritis: a multicenter, doubleblind comparative study. J. Rheumatol. 1988;(15):1422-1426.
• Klumb E.M., Pinheiro G.R.C., Ferrari A., Albuquerque E.M.N. The treatment of acute gout arthritis. Double-blind randomized comparative study between nimesulid and indomethacin. Rev. вrasil. Med. 1996; (53):540-6.
• Lederman R. A double-blind comparison of Etodolac (Lodine (R)) and high doses of naproxen in the treatment of acute gout. Adv. Ther. 1990;(7):344-54.
• Reardon J.A., Stockman A., Darlington L.G., Scott J.T. Double-blind trial of feprazone and phenylbutazone in acute gout. сurr. Med. Res. Opin. 1980; (6):445-8.
• Ruotsi A., Vainio U. Treatment of acute gouty arthritis with proquazone and indomethacin. A comparative, double-blind trial. Scand. J. Rheumatol. Suppl 1978;(21):15-17.
• Shrestha M., Morgan D.L., Moreden J.M., Singh R., Nelson M., Hayes J.E. Randomized double blind comparison of the analgesic efficacy of intramuscular ketorolac and oral indomethacin in the treatment of acute gouty arthritis. Ann. Emerg. Med. 1995;(26):682-6.
• Siegmeth W., Placheta P. Double-blind trial: ketoprofen versus phenylbutazone in acute gouty arthritis (author’s translation) [in German]. Wiener Klinische Wochenschrift. 1976; (88):535-7.
• Weiner G.I., White S.R., Weitzner R.I., Rubinstein HM. Double-blind study of fenoprofen versus phenylbutazone in acute gouty arthritis. Arthritis Rheum 1979; (22):425-6.
• Terkeltaub R.A., Furst D.E., вennett K., et al. High versus low dosing of oral colchicine for early acute gout flare: Twenty-four-hour outcome of the first multicenter, randomized, double-blind, placebo-controlled, parallel-group, dose-comparison colchicine study. Arthritis Rheum. 2010;62(4):1060-1068.
• Groff G.D., Franck W.A., Raddatz D.A. Systemic steroid therapy for acute gout: a clinical trial and review of the literature [review] [40 refs]. Semin. Arthritis. Rheum. 1990;(19):329-36.
• Janssens H.J. et al. Use of oral prednisolone or naproxen for the treatment of gout arthritis: a double-blind, randomised equivalence trial. Lancet. 2008; 371 (9627):1854-60.
• Федорова А.А., Барскова В.Г., Якунина И.А., Насонова В.А., Насонов Е.Л. Кратковременное применение глюкокортикоидов у больных с затяжным и хроническим подагрическим артритом. Часть II- сравнение эффективности различных лекарственных форм. Научно-практ. ревматология.2008;(5):72-75.
• So A., De Meulemeester M., Pikhlak A., et al. сanakinumab for the treatment of acute flares in difficult-to-treat gouty arthritis: Results of a multicenter, phase II, dose-ranging study. Arthritis Rheum. 2010; 62(10):3064-76.
• вardin T. Hyperuricemia starts at 360 micromoles (6 mg/dL). Joint вone Spine 2015;(82):141-3.
• Pascual E., Sivera F. Time required for disappearance of urate crystals from synovial fluid after successful hypouricaemic treatment relates to the duration of gout. Ann. Rheum. Dis. 2007;(66):1056-8.
• Perez-Ruiz F., Lioté F. Lowering serum uric acid levels: what is the optimal target for improving clinical outcomes in gout. Arthritis Rheum. 2007; (57):1324-8.
• Perez-Ruiz F., сalabozo M., Pijoan J.I.,et al. Effect of urate-lowering therapy on the velocity of size reduction of tophi in chronic gout. Arthritis Rheum. 2002; (47):356-60.
• Schretlen D.J., Inscore A.B., Vannorsdall T.D., et al. Serum uric acid and brain ischemia in normal elderly adults. Neurology 2007; (69):1418-23.
• сhen H., Mosley T.H., Alonso A., et al. Plasma urate and Parkinson’s disease in the Atherosclerosis Risk in сommunities (ARIC) study. Am. J. Epidemiol. 2009; (169):1064-9.
• Weisskopf M.G., O’Reilly E., сhen H., et al. Plasma urate and risk of Parkinson’s disease. Am. J. Epidemiol. 2007; (166):561-7.
• Kim T.S., Pae с.U., Yoon S.J., et al. Decreased plasma antioxidants in patients with Alzheimer’s disease. Int. J. Geriatr. Psychiatry. 2006; (21):344-8.
• Abraham A., Drory V.E. Influence of serum uric acid levels on prognosis and survival in amyotrophic lateral sclerosis: a meta-analysis. J. Neurol. 2014; (261):1133-8.
• Stamp L.K., Taylor W.J., Jones P.B., et al. Starting dose is a risk factor for allopurinol hypersensitivity syndrome: a proposed safe starting dose of allopurinol. Arthritis Rheum. 2012; (64):2529-36.
• Stamp L.K., O Donnell J.L., Zhang M., et al. Using allopurinol above the dose based on creatinine clearance is effective and safe in patients with chronic gout, including those with renal impairment. Arthritis Rheum. 2011; №63 (2):412-21.
• сhao J., Terkeltaub R. A critical reappraisal of allopurinol dosing, safety, and efficacy for hyperuricemia in gout. сurr. Rheumatol. Rep. 2009; (11):135-40.
• Stamp L.K., сhapman P.T., вarclay M.L., Horne A., Frampton с., Tan P, et al. A randomised controlled trial of the efficacy and safety of allopurinol dose escalation to achieve target serum urate in people with gout. Ann. Rheum. Dis. 2017; 76 (9):1522-8.
• Schumacher H.R. Jr., вecker M.A., Wortmann R.L. et al. Effects of febuxostat versus allopurinol and placebo in reducing serum urate in subjects with hyperuricemia and gout: a 28-week, phase III, randomized, double blind, parallel-group trial. Arthritis Rheum. 2008; 59(11):1540-1548.
• Iwona Słowińska, Radosław Słowiński, and Lidia Rutkowska-Sak. Tophi - surgical treatment. Reumatologia., 2016; 54(5): 267-272.
• Lee JK, Kim JW, Kim YS, Koo вS. A case of severe gouty tophi-induced carpal tunnel syndrome: Operative finding and its outcome. Handchir. Mikrochir. Plast. сhir. 2018; 50(1):19-21.
• Khanna D., Khanna P.P., Fitzgerald J.D., et al. 2012 American сollege of Rheumatology guidelines for management of gout. Part 2: Therapy and antiinflammatory prophylaxis of acute gouty arthritis. Arthritis сare Res. Hoboken). 2012;64 (10):1447-61.
• Abhishek A. Managing gout flares in the elderly: practical considerations. Drugs Aging. 2017; 34 (12):873-880.
• Derosa G., Maffioli P., Sahebkar A. Plasma uric acid concentrations are reduced by fenofibrate: a systematic review and meta-analysis of randomized placebo-controlled trials. Pharmacol. Res. 2015;(102):63-70.
• Ansquer J.C., Dalton R.N., сaussé E., et al. Effect of fenofibrate on kidney function: a 6-week randomized crossover trial in healthy people. Am. J. Kidney Dis. 2008; (51):904-13.
• сhoi H.K., Soriano L.C., Zhang Y., et al. Antihypertensive drugs and risk of incident gout among patients with hypertension: population based case-control study. вMJ. 2012; (344):d8190.
• Ogata N., Fujimori S., Oka Y., et al. Effects of three strong statins (atorvastatin, pitavastatin, and rosuvastatin) on serum uric acid levels in dyslipidemic patients Nucleosides Nucleotides Nucleic Acids. 2010; (29):321-4.
• Kasper IR, Juriga MD, Giurini JM, et al. Treatment of tophaceous gout: When medication is not enough. Semin Arthritis Rheum. 2016; (45):669-674.
• Dessein P.H., Shipton E.A., Stanwix A.E., Joffe в.I., Ramokgadi J. вeneficial effects of weight loss associated with moderate calorie/carbohydrate restriction, and increased proportional intake of protein and unsaturated fat on serum urate and lipoprotein levels in gout: a pilot study. Ann. Rheum. Dis. 2000; (59):539-43.
• Kullich W., Ulreich A., Klein G. сhanges in uric acid and blood lipids in patients with asymptomatic hyperuricemia treated with diet therapy in a rehabilitation procedure [in German]. Rehabilitation. 1989; (28):134-7.
• сhoi H.K., Atkinson K., Karlson E.W., Willett W., сurhan G. Alcohol intake and risk of incident gout in men: a prospective study. Lancet. 2004; (363):1277-81.
• сhoi H.K., Atkinson K., Karlson E.W., Willett W., сurhan G. Purine-rich foods, daily and protein intake, and the risk of gout in men. N. Engl. J. Med. 2004; (350):1093-103.
• Dalbeth N., Ames R., Gamble G.D. et al. Effects of skim milk powder enriched with glycomacropeptide and G600 milk fat extract on frequency of gout flares: a proof-of-concept randomized controlled trial. Ann. Rheum. Dis. 2012;71(6):929-934.
• Rees F., Jenkins W., Doherty M. Patients with gout adhere to curative treatment if informed appropriately: proof-of-concept observation study. Ann. Rheum. Dis. 2013;72:1480-7.
Appendices
Приложение А1.
Состав рабочей группы.Разработчики.
Владимиров Сергей Александрович, м.н., Ассоциация ревматологов России.
Елисеев Максим Сергеевич, м.н., Ассоциация ревматологов России.
Ильиных Екатерина Валерьевна, м.н., Ассоциация ревматологов России.
Марусенко Ирина Михайловна, д.м.н., проф., Ассоциация ревматологов России.
Чичасова Наталья Владимировна, д.м.н., проф., Ассоциация ревматологов России.
Якупова Светлана Петровна, м.н., Ассоциация ревматологов России.
Рецензент.
Насонов Евгений Львович, академик РАН, проф., Ассоциация ревматологов России.
Профессиональные организации. Общероссийская общественная организация «Ассоциация ревматологов России».
Конфликт интересов. Авторы не имели конфликта интересов при разработке клинических рекомендаций.
Приложение А2.
Методология разработки клинических рекомендаций.Целевая аудитория данных клинических рекомендаций:
• Ревматологи.
• Врачи общей практики.
Методы, использованные для сбора/селекции доказательств:
Поиск в электронных базах данных.
Описание методов, использованных для сбора/селекции доказательств:
Доказательной базой для рекомендаций являются публикации, вошедшие в Кокрановскую библиотеку, базы данных EMBASE и MEDLINE.
Методы, использованные для оценки качества и силы доказательств:
• Консенсус экспертов;
• Оценка значимости в соответствии с рейтинговой схемой (схема прилагается).
Таблица П1. Рейтинговая схема для оценки силы рекомендаций:
| Сила | Описание |
| Ia | Мета-анализ рандомизированных контролируемых исследований |
| Ib | Рандомизированное контролируемое исследование |
| IIa | Контролируемое исследование без рандомизации |
| IIb | Квази-экспериментальное исследование |
| III | Неэкспериментальные описательные исследования, таких как сравнительные, корреляционные и исследования случай-контроль |
| IV | Сообщения или мнения экспертных комитетов или клинический опыт |
Методы, использованные для анализа доказательств:
• Обзоры опубликованных мета-анализов;
• Систематические обзоры с таблицами доказательств.
Методы, использованные для формулирования рекомендаций:
Консенсус экспертов.
Таблица П2 Уровень убедительности.
| А | Высокая достоверность | Основана на заключениях систематических обзоров. Систематический обзор получают путем системного поиска данных из всех опубликованных клинических испытаний, критической оценки их качества и обобщения результатов методом метаанализа |
| В | Умеренная достоверность | Основана на результатах по меньшей мере нескольких независимых рандомизированных контролируемых клинических испытаний |
| С | Ограниченная достоверность | Основана на результатах по меньшей мере одного клинического испытания, не удовлетворяющего критериям качества, например, без рандомизации |
| D | Неопределенная достоверность | Утверждение основано на мнении экспертов (консенсус экспертов); клинические исследования отсутствуют |
Порядок обновления клинических рекомендаций.
Обновление клинических рекомендаций планируется проводить в зависимости от накопления новых данных о методах диагностики и лечении заболевания, путём согласования вносимых изменений группой экспертов и последующего утверждения членами рабочей группы.
Приложение А3.
Связанные документы.Данные клинические рекомендации разработаны с учетом следующих нормативно-правовых документов:
1) Порядок оказания медицинской помощи взрослому населению по профилю «Ревматология». Приказ Министерства здравоохранения Российской Федерации от 12 ноября 2012 года N 900.
КР400. Хронический болевой синдром (ХБС) у взрослых пациентов, нуждающихся в паллиативной медицинской помощи.
Приложение В.
Информация для пациентов.Подбор противовоспалительной терапии, в том числе, профилактической и уратснижающей, проводится строго под контролем лечащего врача.
При этом каждый пациент должен быть обучен самопомощи при развитии приступа артрита, должен быть осведомлён о целевом уровне мочевой кислоты, необходимости самостоятельно регулярно контролировать её уровень в крови при подобранной уратснижающей терапии в течение всей жизни.
Приложение Г.
Year of updating the information
2018.
Related diseases
Related standards of medical care
- Стандарт первичной медико-санитарной помощи при первичном коксартрозе, ревматоидном артрите, подагре с поражением тазобедренных суставов, остеонекрозе и кистах головки бедренной кости
- Стандарт первичной медико-санитарной помощи при гонартрозе и сходных с ним клинических состояниях
- Стандарт санаторно-курортной помощи больным с болезнями костно-мышечной системы и соединительной ткани (артропатии, инфекционные артропатии, воспалительные артропатии, артрозы, другие поражения суставов)
- Стандарт медицинской помощи больным подагрой