Pharmacological Group
Latin name
Lacosamidum ( Lacosamidi).
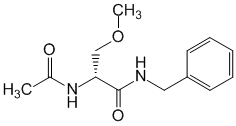
Chemical name
(2R)-2-(Ацетиламино)-N-бензил-3-метоксипропанамид.
Used in the treatment
CAS Code
175481-36-4.
Pharmacological action
Противоэпилептическое.
Characteristics of the substance
Функционализированная аминокислота.
Pharmacodynamics
Точный механизм противоэпилептического действия лакосамида не установлен. В электрофизиологических исследованиях in vitro >in vitro лакосамид избирательно усиливал медленную инактивацию потенциалзависимых натриевых каналов, что приводило к стабилизации гипервозбудимых мембран нейронов. Кроме того, лакосамид связывается с фосфопротеином сRMP-2, который экспрессируется преимущественно в нервной системе и участвует в регуляции дифферинцировки нейронов и роста аксонов.
Фармакодинамика.
Лакосамид предотвращал развитие приступов на большом количестве моделей парциальной и первично генерализованной эпилепсии у животных, а также задерживал развитие повышенной судорожной готовности. В доклинических исследованиях лакосамид в комбинации с леветирацетамом, карбамазепином, фенитоином, вальпроатами, ламотриджином, топираматом или габапентином демонстрировал синергическое или аддитивное противосудорожное действие.
Клиническая эффективность и безопасность.
Эффективность лакосамида в качестве дополнительной терапии в рекомендуемых дозах (200, 400 мг/сут) была доказана в 3 мультицентровых рандомизированных плацебо-контролируемых клинических исследованиях с 12-недельным поддерживающим периодом. Эффективность в дозе 600 мг/сут также была показана в ходе контролируемых дополнительных терапевтических исследований, и хотя она была сопоставимой с наблюдавшейся при дозе 400 мг/сут, переносимость данной дозы (600 мг/сут) была хуже по причине побочных эффектов со стороны ЦНС и ЖКТ. Поэтому использование дозы 600 мг/сут не рекомендуется. Максимальная рекомендованная доза составляет 400 мг/сут. Эти исследования с участием 1308 пациентов, имеющих данные из анамнеза о развитии парциальных припадков на протяжении среднего периода 23 года, были проведены для оценки эффективности и безопасности лакосамида при сопутствующем назначении 1-3 противоэпилептических ЛС у пациентов с неконтролируемыми парциальными припадками с или без вторичной генерализации. Общая доля пациентов с 50% снижением частоты припадков в группах плацебо, лакосамида в дозе 200 мг/сут и лакосамида в дозе 400 мг/сут составила 23, 34 и 40% соответственно.
В настоящее время имеется недостаточное количество данных по возможности отмены сопутствующих противоэпилептических средств для использования монотерапии лакосамидом.
Фармакокинетика и безопасность разовой насыщающей дозы инфузионного лакосамида определялась в многоцентровом открытом исследовании безопасности и переносимости быстрого начала терапии лакосамидом с использованием разовой в/в насыщающей дозы (200 мг) и с последующим пероральным приемом 2 раза в сутки (в дозировке, эквивалентной в/в дозе) в качестве дополнительной терапии у взрослых пациентов от 16 до 60 лет с парциальными приступами.
Фармакодинамика.
Лакосамид предотвращал развитие приступов на большом количестве моделей парциальной и первично генерализованной эпилепсии у животных, а также задерживал развитие повышенной судорожной готовности. В доклинических исследованиях лакосамид в комбинации с леветирацетамом, карбамазепином, фенитоином, вальпроатами, ламотриджином, топираматом или габапентином демонстрировал синергическое или аддитивное противосудорожное действие.
Клиническая эффективность и безопасность.
Эффективность лакосамида в качестве дополнительной терапии в рекомендуемых дозах (200, 400 мг/сут) была доказана в 3 мультицентровых рандомизированных плацебо-контролируемых клинических исследованиях с 12-недельным поддерживающим периодом. Эффективность в дозе 600 мг/сут также была показана в ходе контролируемых дополнительных терапевтических исследований, и хотя она была сопоставимой с наблюдавшейся при дозе 400 мг/сут, переносимость данной дозы (600 мг/сут) была хуже по причине побочных эффектов со стороны ЦНС и ЖКТ. Поэтому использование дозы 600 мг/сут не рекомендуется. Максимальная рекомендованная доза составляет 400 мг/сут. Эти исследования с участием 1308 пациентов, имеющих данные из анамнеза о развитии парциальных припадков на протяжении среднего периода 23 года, были проведены для оценки эффективности и безопасности лакосамида при сопутствующем назначении 1-3 противоэпилептических ЛС у пациентов с неконтролируемыми парциальными припадками с или без вторичной генерализации. Общая доля пациентов с 50% снижением частоты припадков в группах плацебо, лакосамида в дозе 200 мг/сут и лакосамида в дозе 400 мг/сут составила 23, 34 и 40% соответственно.
В настоящее время имеется недостаточное количество данных по возможности отмены сопутствующих противоэпилептических средств для использования монотерапии лакосамидом.
Фармакокинетика и безопасность разовой насыщающей дозы инфузионного лакосамида определялась в многоцентровом открытом исследовании безопасности и переносимости быстрого начала терапии лакосамидом с использованием разовой в/в насыщающей дозы (200 мг) и с последующим пероральным приемом 2 раза в сутки (в дозировке, эквивалентной в/в дозе) в качестве дополнительной терапии у взрослых пациентов от 16 до 60 лет с парциальными приступами.
Pharmacokinetics
Всасывание. Лакосамид быстро и полностью всасывается после приема внутрь. Биодоступность лакосамида составляет примерно 100%. После приема внутрь концентрация лакосамида в плазме быстро увеличивается, maxCmax достигается через 0,5-4 Прием пищи не влияет на скорость и степень всасывания.
При в/в введении maxCmax достигается к моменту окончания инфузии. Концентрация лакосамида в плазме крови увеличивается пропорционально дозе после в/в введения в диапазоне 50-300 мг.
Распределение. dVd составляет примерно 0,6 л/кг, степень связывания с белками плазмы - менее 15%. При применении 2 раза в день ssCss в плазме достигается в течение 3 дней. Кумуляция сопровождается увеличением концентрации в плазме примерно в 2 раза.
Css при применении разовой насыщающей дозы 200 мг сравнима с таковой при пероральном приеме 100 мг 2 раза в сутки.
Метаболизм. 95% дозы выводится через почки, в тч в неизмененном виде (около 40%) и в виде О-дезметилметаболита (менее 30%). Полярная фракция (предположительно производные серина) составляет примерно 20% в моче и лишь в небольших количествах (0-2%) обнаруживается в плазме крови. Другие метаболиты определяются в моче в количестве 0,5-2%.
Данные in vitro >in vitro показывают, что образование О-дезметилметаболита происходит в основном под действием изоферментов сYP2C19, сYP2С9 и сYP3А4. При сравнении фармакокинетики лакосамида у экстенсивных метаболизаторов (с функциональным изоферментом сYP2C19) и медленных метаболизаторов (с недостатком функционального изофермента сYP2C19) клинически значимой разницы выделения лакосамида отмечено не было. Кроме того, исследования по взаимодействию с омепразолом (ингибитор изофермента сYP2C19) показали отсутствие клинически значимых изменений концентрации лакосамида в плазме, что свидетельствует о низкой значимости этого пути.
Концентрация О-дезметиллакосамида в плазме составляет примерно 15% от концентрации лакосамида. Этот метаболит не обладает фармакологической активностью.
Выведение. Лакосамид выводится путем почечной экскреции и биотрансформации. После перорального приема и в/в введения лакосамида, меченного радиоактивным изотопом, около 95% радиоактивности отмечалось в моче и менее 0,5% - в кале. 1/2T1/2 неизмененного лакосамида составляет примерно 13 Фармакокинетические параметры пропорциональны дозе, постоянны во времени и характеризуются низкой индивидуальной вариабельностью.
Особые группы пациентов.
Пол. Клинические исследования показывают, что пол не оказывает значимое влияние на концентрацию лакосамида в плазме крови.
Раса. Клинически значимые различия в фармакокинетике лакосамида у азиатской, негроидной и европеоидной рас отсутствуют.
Почечная недостаточность. AUC увеличивается приблизительно на 30% при легкой и умеренной почечной недостаточности и на 60% при тяжелой и терминальной стадии почечной недостаточности, требующей проведения гемодиализа, по сравнению со здоровыми пациентами, в то время как Сmax не изменяется. Лакосамид удаляется из плазмы при гемодиализе. В течение 4 ч процедуры гемодиализа AUC снижается приблизительно на 50%. Поэтому после процедуры гемодиализа рекомендуется принятие дополнительной дозы. У пациентов с умеренной и тяжелой почечной недостаточностью выделение О-дезметилметаболита увеличивается в несколько раз. У пациентов с терминальной стадией почечной недостаточности при отсутствии гемодиализа плазменный уровень увеличивается и непрерывно возрастает в течение 24-часового наблюдения. До конца не изучено, может ли повышенное выделение метаболита у пациентов с терминальной стадией почечной недостаточности приводить к увеличению числа побочных эффектов, но было подтверждено, что фармакологической активностью О-дезметилметаболит не обладает.
Печеночная недостаточность. У пациентов с умеренной печеночной недостаточностью наблюдалось повышение концентрации лакосамида в плазме крови (приблизительно на 50% больше AUCнорм). Одной из причин повышенной экспозиции было снижение функции почек у пациентов, принимавших участие в исследованиях. Снижение непочечного клиренса у пациентов из исследования оценивалось как увеличение AUC лакосамида на 20%. У пациентов с тяжелой печеночной недостаточностью фармакокинетика не изучалась.
Пожилые пациенты. В исследованиях принимало участие 4 пациента пожилого возраста старше 75 лет. AUC было увеличено приблизительно на 30% у мужчин и 50% у женщин по сравнению с молодыми пациентами. Частично это объясняется сниженной массой тела - на 26% у мужчин и 23% у женщин от нормальной массы тела. Также наблюдалось увеличенное выделение лакосамида. В исследованиях у пожилых больных почечный клиренс лакосамида был уменьшен незначительно.
При в/в введении maxCmax достигается к моменту окончания инфузии. Концентрация лакосамида в плазме крови увеличивается пропорционально дозе после в/в введения в диапазоне 50-300 мг.
Распределение. dVd составляет примерно 0,6 л/кг, степень связывания с белками плазмы - менее 15%. При применении 2 раза в день ssCss в плазме достигается в течение 3 дней. Кумуляция сопровождается увеличением концентрации в плазме примерно в 2 раза.
Css при применении разовой насыщающей дозы 200 мг сравнима с таковой при пероральном приеме 100 мг 2 раза в сутки.
Метаболизм. 95% дозы выводится через почки, в тч в неизмененном виде (около 40%) и в виде О-дезметилметаболита (менее 30%). Полярная фракция (предположительно производные серина) составляет примерно 20% в моче и лишь в небольших количествах (0-2%) обнаруживается в плазме крови. Другие метаболиты определяются в моче в количестве 0,5-2%.
Данные in vitro >in vitro показывают, что образование О-дезметилметаболита происходит в основном под действием изоферментов сYP2C19, сYP2С9 и сYP3А4. При сравнении фармакокинетики лакосамида у экстенсивных метаболизаторов (с функциональным изоферментом сYP2C19) и медленных метаболизаторов (с недостатком функционального изофермента сYP2C19) клинически значимой разницы выделения лакосамида отмечено не было. Кроме того, исследования по взаимодействию с омепразолом (ингибитор изофермента сYP2C19) показали отсутствие клинически значимых изменений концентрации лакосамида в плазме, что свидетельствует о низкой значимости этого пути.
Концентрация О-дезметиллакосамида в плазме составляет примерно 15% от концентрации лакосамида. Этот метаболит не обладает фармакологической активностью.
Выведение. Лакосамид выводится путем почечной экскреции и биотрансформации. После перорального приема и в/в введения лакосамида, меченного радиоактивным изотопом, около 95% радиоактивности отмечалось в моче и менее 0,5% - в кале. 1/2T1/2 неизмененного лакосамида составляет примерно 13 Фармакокинетические параметры пропорциональны дозе, постоянны во времени и характеризуются низкой индивидуальной вариабельностью.
Особые группы пациентов.
Пол. Клинические исследования показывают, что пол не оказывает значимое влияние на концентрацию лакосамида в плазме крови.
Раса. Клинически значимые различия в фармакокинетике лакосамида у азиатской, негроидной и европеоидной рас отсутствуют.
Почечная недостаточность. AUC увеличивается приблизительно на 30% при легкой и умеренной почечной недостаточности и на 60% при тяжелой и терминальной стадии почечной недостаточности, требующей проведения гемодиализа, по сравнению со здоровыми пациентами, в то время как Сmax не изменяется. Лакосамид удаляется из плазмы при гемодиализе. В течение 4 ч процедуры гемодиализа AUC снижается приблизительно на 50%. Поэтому после процедуры гемодиализа рекомендуется принятие дополнительной дозы. У пациентов с умеренной и тяжелой почечной недостаточностью выделение О-дезметилметаболита увеличивается в несколько раз. У пациентов с терминальной стадией почечной недостаточности при отсутствии гемодиализа плазменный уровень увеличивается и непрерывно возрастает в течение 24-часового наблюдения. До конца не изучено, может ли повышенное выделение метаболита у пациентов с терминальной стадией почечной недостаточности приводить к увеличению числа побочных эффектов, но было подтверждено, что фармакологической активностью О-дезметилметаболит не обладает.
Печеночная недостаточность. У пациентов с умеренной печеночной недостаточностью наблюдалось повышение концентрации лакосамида в плазме крови (приблизительно на 50% больше AUCнорм). Одной из причин повышенной экспозиции было снижение функции почек у пациентов, принимавших участие в исследованиях. Снижение непочечного клиренса у пациентов из исследования оценивалось как увеличение AUC лакосамида на 20%. У пациентов с тяжелой печеночной недостаточностью фармакокинетика не изучалась.
Пожилые пациенты. В исследованиях принимало участие 4 пациента пожилого возраста старше 75 лет. AUC было увеличено приблизительно на 30% у мужчин и 50% у женщин по сравнению с молодыми пациентами. Частично это объясняется сниженной массой тела - на 26% у мужчин и 23% у женщин от нормальной массы тела. Также наблюдалось увеличенное выделение лакосамида. В исследованиях у пожилых больных почечный клиренс лакосамида был уменьшен незначительно.
Indications for use
Парциальные судорожные приступы, сопровождающиеся или не сопровождающиеся вторичной генерализацией, у пациентов с эпилепсией в возрасте от 16 лет и старше (в качестве дополнительной терапии).
Contraindications
Повышенная чувствительность к лакосамиду; AV-блокада II или III степени; возраст до 16 лет.
Restrictions on use
Тяжелая почечная недостаточность (Cl креатинина <30 мл/мин); нарушение проводимости в анамнезе или тяжелые заболевания сердца, такие как сердечная недостаточность и инфаркт миокарда в анамнезе; пожилые пациенты с повышенным риском заболеваний сердца; комбинация с ЛС, вызывающими удлинение интервала PR.
Use during pregnancy and lactation
Категория действия на плод по FDA. с.
Общий риск, связанный с эпилепсией и применением противоэпилептических средств.
В отношении всех противоэпилептических средств было показано, что частота врожденных пороков развития у детей женщин с эпилепсией, получающих такую терапию, в 2-3 раза выше по сравнению с общей популяцией (в последнем случае этот показатель составляет 3%). У пациентов, получающих лечение, было отмечено увеличение частоты врожденных пороков развития у детей на фоне политерапии, однако степень влияния лечения и/или заболевания на увеличение этого риска до настоящего времени неизвестна.
Кроме того, эффективное противоэпилептическое лечение прекращать не следует, поскольку ухудшение течения заболевания оказывает отрицательное влияние на мать и плод.
Риск, связанный с применением лакосамида.
Клинических данных о применении лакосамида у беременных женщин нет. В исследованиях на животных не были зарегистрированы тератогенные эффекты, однако при применении доз, токсичных для материнского организма, была отмечена эмбриотоксичность у кроликов и крыс. Потенциальный риск для человека неизвестен.
Лакосамид не следует применять во время беременности за исключением тех случаев, когда польза для матери явно перевешивает возможный риск для плода. Если женщина планирует беременность, то необходимо тщательно взвесить целесообразность применения лакосамида. Для осуществления мониторинга последствий применения лакосамида у беременных женщин врачам рекомендуется регистрировать данных пациентов в Европейском и международном регистре по противоэпилептическим препаратам и беременности.
Данные об экскреции лакосамида с грудным молоком человека отсутствуют. В исследованиях на животных отмечена экскреция лакосамида с молоком. Во время лечения лакосамидом следует прекратить кормление грудью.
Фертильность. Нe было отмечено никаких нежелательных реакций со стороны фертильности или репродуктивности у крыс обоих полов в дозах, создающих концентрацию в плазме (AUC) приблизительно в 2 раза выше AUC в плазме человека при применении МРДЧ.
Общий риск, связанный с эпилепсией и применением противоэпилептических средств.
В отношении всех противоэпилептических средств было показано, что частота врожденных пороков развития у детей женщин с эпилепсией, получающих такую терапию, в 2-3 раза выше по сравнению с общей популяцией (в последнем случае этот показатель составляет 3%). У пациентов, получающих лечение, было отмечено увеличение частоты врожденных пороков развития у детей на фоне политерапии, однако степень влияния лечения и/или заболевания на увеличение этого риска до настоящего времени неизвестна.
Кроме того, эффективное противоэпилептическое лечение прекращать не следует, поскольку ухудшение течения заболевания оказывает отрицательное влияние на мать и плод.
Риск, связанный с применением лакосамида.
Клинических данных о применении лакосамида у беременных женщин нет. В исследованиях на животных не были зарегистрированы тератогенные эффекты, однако при применении доз, токсичных для материнского организма, была отмечена эмбриотоксичность у кроликов и крыс. Потенциальный риск для человека неизвестен.
Лакосамид не следует применять во время беременности за исключением тех случаев, когда польза для матери явно перевешивает возможный риск для плода. Если женщина планирует беременность, то необходимо тщательно взвесить целесообразность применения лакосамида. Для осуществления мониторинга последствий применения лакосамида у беременных женщин врачам рекомендуется регистрировать данных пациентов в Европейском и международном регистре по противоэпилептическим препаратам и беременности.
Данные об экскреции лакосамида с грудным молоком человека отсутствуют. В исследованиях на животных отмечена экскреция лакосамида с молоком. Во время лечения лакосамидом следует прекратить кормление грудью.
Фертильность. Нe было отмечено никаких нежелательных реакций со стороны фертильности или репродуктивности у крыс обоих полов в дозах, создающих концентрацию в плазме (AUC) приблизительно в 2 раза выше AUC в плазме человека при применении МРДЧ.
Side effects
Основываясь на анализе объединенных плацебо-контролируемых клинических исследований, при лечении лакосамидом самыми частыми побочными реакциями были головокружение, головная боль, тошнота и диплопия. Как правило, они были легкими или умеренно выраженными. Выраженность некоторых побочных реакций зависела от дозы и уменьшалась после ее снижения. Частота и тяжесть побочных реакций со стороны ЦНС и ЖКТ обычно уменьшалась со временем. Самой частой нежелательной реакцией, приводившей к отмене терапии лакосамидом, являлось головокружение. Процент побочных реакций со стороны ЦНС, таких как головокружение, может быть выше после применения насыщающей дозы.
Побочные реакции классифицированы по частоте в соответствии со следующими категориями: очень часто (≥1/10); часто (от ≥1/100 до <1/10); нечасто (от ≥1/1000 до <1/100); частота неизвестна. Частота нижеперечисленных побочных реакций указана в соответствии с данными, полученными в ходе клинических исследований и в постмаркегинговой практике.
Со стороны крови и лимфатической системы. Частота неизвестна - агранулоцитоз.
Со стороны иммунной системы. Нечасто - реакции гиперчувствительности. частота неизвестна - реакции гиперчувствительности с поражением различных органов и систем. включая лекарственную реакцию с эозинофилией и системными проявлениями (DRESS-синдром).
Нарушения психики. Часто - депрессия. спутанность сознания. бессонница. нечасто - агрессия. возбуждение. эйфория. психические расстройства. суицидальные попытки. суицидальные мысли. галлюцинации.
Со стороны ЦНС. Очень часто - головокружение. головная боль. часто - нарушение равновесия. нарушение координации движений. нарушение памяти. когнитивные нарушения. сонливость. тремор. нистагм. гипестезия. дизартрия. нарушение внимания. парестезии.
Со стороны органа зрения. Очень часто - диплопия; часто - нечеткость зрения.
Со стороны органа слуха и вестибулярного аппарата. Часто - вертиго, шум в ушах.
Со стороны сердца. Нечасто - AV-блокада, брадикардия, фибрилляция и трепетание предсердий.
Со стороны органов пищеварения. Очень часто - тошнота. часто - рвота. запор. метеоризм. диспепсия. сухость во рту. диарея.
Со стороны печени и желчевыводящих путей. Нечасто - изменение печеночных проб.
Со стороны кожи и подкожных тканей. Часто - зуд. сыпь. нечасто - ангионевротический отек. крапивница. частота неизвестна - токсический эпидермальный некролиз. синдром Стивенса -Джонсона.
Со стороны скелетно-мышечной системы и соединительной ткани. Часто - мышечный спазм.
Общие расстройства и нарушения в месте введения. Часто - нарушение походки, астения, повышенная утомляемость, раздражительность, чувство опьянения.
Травмы, интоксикации и осложнения манипуляций. Часто - падения, повреждения кожи, повышенный риск получения травм (из-за нарушения координации движений и головокружения), ушибы.
Описание отдельных побочных реакций.
Использование лакосамида связано с дозозависимым удлинением интервата PR. Могут наблюдаться побочные реакции, связанные с удлинением интервала PR (например AV-блокада, обморок, брадикардия).
В клинических исследованиях у пациентов с эпилепсией процент эпизодов AV I степени был невысок - 0,7; 0; 0,5 и 0% при применении лакосамида в дозировке 200, 400, 600 мг и плацебо соответственно. AV-блокады II степени и выше в данных исследованиях отмечено не было. Тем не менее в постмаркетинговой практике сообщалось о случаях появления AV-блокады II и III степени при лечении лакосамидом.
В клинических исследованиях обморок встречался нечасто и процент случившихся эпизодов не отличался в группах больных эпилепсией, получавших лакосамид (0,1%) и плацебо (0,3%).
Фибрилляция и трепетание предсердий не были отмечены в краткосрочных клинических исследованиях; однако оба явления были отмечены в открытых исследованиях по эпилепсии, а также в постмаркетинговой практике.
Отклонения лабораторных показателей.
В контролируемых исследованиях наблюдалось изменение печеночных проб у взрослых пациентов с парциальными судорожными приступами при применении от 1 до 3 противоэпилептических средств одновременно. Повышение АЛТ в 3 раза и более наблюдалось у 0,7% (7 из 935) пациентов, получавших лакосамид, и 0% (0 из 356) - плацебо.
Реакции гиперчувствительности с поражением различных органов и систем.
Были отмечены реакции гиперчувствительности с поражением различных органов и систем. включая лекарственную реакцию с эозинофилией и системными проявлениями (DRESS-синдром). у пациентов. получавших некоторые противоэпилептические средства. Данные реакции различны в проявлении, но чаще всего проявляются в виде жара и сыпи и могут затрагивать другие системы. Если есть подозрение на реакцию гиперчувствительности с поражением различных органов и систем, то прием лакосамида следует прекратить.
Побочные реакции классифицированы по частоте в соответствии со следующими категориями: очень часто (≥1/10); часто (от ≥1/100 до <1/10); нечасто (от ≥1/1000 до <1/100); частота неизвестна. Частота нижеперечисленных побочных реакций указана в соответствии с данными, полученными в ходе клинических исследований и в постмаркегинговой практике.
Со стороны крови и лимфатической системы. Частота неизвестна - агранулоцитоз.
Со стороны иммунной системы. Нечасто - реакции гиперчувствительности. частота неизвестна - реакции гиперчувствительности с поражением различных органов и систем. включая лекарственную реакцию с эозинофилией и системными проявлениями (DRESS-синдром).
Нарушения психики. Часто - депрессия. спутанность сознания. бессонница. нечасто - агрессия. возбуждение. эйфория. психические расстройства. суицидальные попытки. суицидальные мысли. галлюцинации.
Со стороны ЦНС. Очень часто - головокружение. головная боль. часто - нарушение равновесия. нарушение координации движений. нарушение памяти. когнитивные нарушения. сонливость. тремор. нистагм. гипестезия. дизартрия. нарушение внимания. парестезии.
Со стороны органа зрения. Очень часто - диплопия; часто - нечеткость зрения.
Со стороны органа слуха и вестибулярного аппарата. Часто - вертиго, шум в ушах.
Со стороны сердца. Нечасто - AV-блокада, брадикардия, фибрилляция и трепетание предсердий.
Со стороны органов пищеварения. Очень часто - тошнота. часто - рвота. запор. метеоризм. диспепсия. сухость во рту. диарея.
Со стороны печени и желчевыводящих путей. Нечасто - изменение печеночных проб.
Со стороны кожи и подкожных тканей. Часто - зуд. сыпь. нечасто - ангионевротический отек. крапивница. частота неизвестна - токсический эпидермальный некролиз. синдром Стивенса -Джонсона.
Со стороны скелетно-мышечной системы и соединительной ткани. Часто - мышечный спазм.
Общие расстройства и нарушения в месте введения. Часто - нарушение походки, астения, повышенная утомляемость, раздражительность, чувство опьянения.
Травмы, интоксикации и осложнения манипуляций. Часто - падения, повреждения кожи, повышенный риск получения травм (из-за нарушения координации движений и головокружения), ушибы.
Описание отдельных побочных реакций.
Использование лакосамида связано с дозозависимым удлинением интервата PR. Могут наблюдаться побочные реакции, связанные с удлинением интервала PR (например AV-блокада, обморок, брадикардия).
В клинических исследованиях у пациентов с эпилепсией процент эпизодов AV I степени был невысок - 0,7; 0; 0,5 и 0% при применении лакосамида в дозировке 200, 400, 600 мг и плацебо соответственно. AV-блокады II степени и выше в данных исследованиях отмечено не было. Тем не менее в постмаркетинговой практике сообщалось о случаях появления AV-блокады II и III степени при лечении лакосамидом.
В клинических исследованиях обморок встречался нечасто и процент случившихся эпизодов не отличался в группах больных эпилепсией, получавших лакосамид (0,1%) и плацебо (0,3%).
Фибрилляция и трепетание предсердий не были отмечены в краткосрочных клинических исследованиях; однако оба явления были отмечены в открытых исследованиях по эпилепсии, а также в постмаркетинговой практике.
Отклонения лабораторных показателей.
В контролируемых исследованиях наблюдалось изменение печеночных проб у взрослых пациентов с парциальными судорожными приступами при применении от 1 до 3 противоэпилептических средств одновременно. Повышение АЛТ в 3 раза и более наблюдалось у 0,7% (7 из 935) пациентов, получавших лакосамид, и 0% (0 из 356) - плацебо.
Реакции гиперчувствительности с поражением различных органов и систем.
Были отмечены реакции гиперчувствительности с поражением различных органов и систем. включая лекарственную реакцию с эозинофилией и системными проявлениями (DRESS-синдром). у пациентов. получавших некоторые противоэпилептические средства. Данные реакции различны в проявлении, но чаще всего проявляются в виде жара и сыпи и могут затрагивать другие системы. Если есть подозрение на реакцию гиперчувствительности с поражением различных органов и систем, то прием лакосамида следует прекратить.
Interaction
Лакосамид следует применять осторожно в сочетании с ЛС, вызывающими удлинение интервала PR (например карбамазепин, ламотриджин, прегабалин) и антиаритмическими средствами I класса. Однако в подгрупповом анализе клинических исследований не было отмечено дополнительное удлинение интервала PR у больных, которые получали лакосамид в комбинации с карбамазеиином или ламотриджином.
Данные in vitro.
Результаты исследований свидетельствуют о низкой вероятности взаимодействия лакосамида с другими ЛС.
Исследования метаболизма in vitro >in vitro показывают, что лакосамид не индуцирует изоферменты сYP1A2, сYP2В6 и сYP2С9. В концентрациях, которые наблюдались в крови во время клинических исследований, лакосамид не ингибировал изоферменты сYP1A1, сYP1А2, сYP2А6, сYP2В6, сYP2С8, сYP2С9, сYP2D6 и сYP2Е1. Исследования in vitro >in vitro свидетельствуют, что лакосамид не транспортируется Р-gp в кишечнике. Данные in vitro >in vitro показывают, что изоферменты сYP2C9, сYP2C19 и сYP3A4 способны катализировать образование О-дезметилметаболита.
Данные in vivo.
Клинические данные свидетельствуют, что лакосамид не ингибирует и не индуцирует изоферменты сYP2C19 и сYP3А4 до клинически значимого уровня.
Лакосамид не оказывает действие на AUC мидазолама, метаболизирующегося посредством изофермента сYP3A4, при дозировке лакосамида 200 мг 2 раза в день, но при этом Сmах мидазолама немного увеличивается (30%). Лакосамид не влияет на фармакокинетику омепразола, метаболизирующегося посредством изоферментов сYP2C19 и сYP3А4, при дозировке лакосамида 300 мг 2 раза в день.
Омепразол - ингибитор изофермента сYP2C19 (40 мг 4 раза в день) не увеличивал клинически значимо экспозицию лакосамида. Таким образом маловероятно, что умеренные ингибиторы изофермента сYP2C19 могут оказывать клинически значимое влияние на системную экспозицию лакосамида.
Следует соблюдать осторожность при одновременном применении с сильными ингибиторами изофермента сYP2C19 (например флуконазол) и изофермента сYP3A4 (например итраконазол, кетоконазол, ритонавир, кларитромицин), которое может привести к увеличению системной экспозиции лакосамида. Данные взаимодействия не доказаны in vivo >in vivo, но возможны на основании данных in vitro >in vitro.
Сильные индукторы микросомальных ферментов печени, такие как рифампицин или зверобой продырявленный (Hypericum perforatum), могут вызвать умеренное снижение системной концентрации лакосамида. В связи с этим при назначении или отмене подобных средств следует соблюдать осторожность.
Противоэпилептические средства. В исследованиях по взаимодействию лакосамид не оказывал существенное влияние на концентрацию карбамазепина и вальпроевой кислоты в плазме крови. Карбамазепин и вальпроевая кислота не оказывали влияния на концентрацию лакосамида в плазме.
Фармакокинетический анализ популяции показал, что сопутствующая терапия противоэпилептическими средствами, индуцирующими микросомальные ферменты печени (карбамазепин, фенитоин, фенобарбитал в различных дозах), снижала общую системную экспозицию лакосамида на 25%.
Пероральные контрацептивы. Не выявлено признаков значимого взаимодействия между лакосамидом и пероральными контрацептивами: этинилэстрадиолом и левоноргестрелом. Лакосамид не оказывал влияние на концентрацию прогестерона.
Прочие взаимодействия.
Лакосамид не влияет на фармакокинетику дигоксина. Клинически значимое взаимодействие лакосамида и метформина не выявлено.
Данных о взаимодействии лакосамида с алкоголем нет.
Степень связывания лакосамида с белками плазмы крови составляет менее 15%. В связи с этим клинически значимое взаимодействие с другими ЛС, связывающимися с белками плазмы, маловероятно.
При одновременном применении с варфарином лакосамид не оказывает клинически значимое влияние на фармакодинамику и фармакокинетику варфарина.
Данные in vitro.
Результаты исследований свидетельствуют о низкой вероятности взаимодействия лакосамида с другими ЛС.
Исследования метаболизма in vitro >in vitro показывают, что лакосамид не индуцирует изоферменты сYP1A2, сYP2В6 и сYP2С9. В концентрациях, которые наблюдались в крови во время клинических исследований, лакосамид не ингибировал изоферменты сYP1A1, сYP1А2, сYP2А6, сYP2В6, сYP2С8, сYP2С9, сYP2D6 и сYP2Е1. Исследования in vitro >in vitro свидетельствуют, что лакосамид не транспортируется Р-gp в кишечнике. Данные in vitro >in vitro показывают, что изоферменты сYP2C9, сYP2C19 и сYP3A4 способны катализировать образование О-дезметилметаболита.
Данные in vivo.
Клинические данные свидетельствуют, что лакосамид не ингибирует и не индуцирует изоферменты сYP2C19 и сYP3А4 до клинически значимого уровня.
Лакосамид не оказывает действие на AUC мидазолама, метаболизирующегося посредством изофермента сYP3A4, при дозировке лакосамида 200 мг 2 раза в день, но при этом Сmах мидазолама немного увеличивается (30%). Лакосамид не влияет на фармакокинетику омепразола, метаболизирующегося посредством изоферментов сYP2C19 и сYP3А4, при дозировке лакосамида 300 мг 2 раза в день.
Омепразол - ингибитор изофермента сYP2C19 (40 мг 4 раза в день) не увеличивал клинически значимо экспозицию лакосамида. Таким образом маловероятно, что умеренные ингибиторы изофермента сYP2C19 могут оказывать клинически значимое влияние на системную экспозицию лакосамида.
Следует соблюдать осторожность при одновременном применении с сильными ингибиторами изофермента сYP2C19 (например флуконазол) и изофермента сYP3A4 (например итраконазол, кетоконазол, ритонавир, кларитромицин), которое может привести к увеличению системной экспозиции лакосамида. Данные взаимодействия не доказаны in vivo >in vivo, но возможны на основании данных in vitro >in vitro.
Сильные индукторы микросомальных ферментов печени, такие как рифампицин или зверобой продырявленный (Hypericum perforatum), могут вызвать умеренное снижение системной концентрации лакосамида. В связи с этим при назначении или отмене подобных средств следует соблюдать осторожность.
Противоэпилептические средства. В исследованиях по взаимодействию лакосамид не оказывал существенное влияние на концентрацию карбамазепина и вальпроевой кислоты в плазме крови. Карбамазепин и вальпроевая кислота не оказывали влияния на концентрацию лакосамида в плазме.
Фармакокинетический анализ популяции показал, что сопутствующая терапия противоэпилептическими средствами, индуцирующими микросомальные ферменты печени (карбамазепин, фенитоин, фенобарбитал в различных дозах), снижала общую системную экспозицию лакосамида на 25%.
Пероральные контрацептивы. Не выявлено признаков значимого взаимодействия между лакосамидом и пероральными контрацептивами: этинилэстрадиолом и левоноргестрелом. Лакосамид не оказывал влияние на концентрацию прогестерона.
Прочие взаимодействия.
Лакосамид не влияет на фармакокинетику дигоксина. Клинически значимое взаимодействие лакосамида и метформина не выявлено.
Данных о взаимодействии лакосамида с алкоголем нет.
Степень связывания лакосамида с белками плазмы крови составляет менее 15%. В связи с этим клинически значимое взаимодействие с другими ЛС, связывающимися с белками плазмы, маловероятно.
При одновременном применении с варфарином лакосамид не оказывает клинически значимое влияние на фармакодинамику и фармакокинетику варфарина.
Overdose
Симптомы.
Данные клинических исследований. Профиль нежелательных реакций у пациентов, принимавших сверхтерапевтические дозы, не отличался от профиля нежелательных реакций, у пациентов, принимавших рекомендованные дозы.
После приема лакосамида в дозе 1200 мг/сут наблюдалась клиническая симптоматика со стороны ЦНС и ЖКТ (головокружение и тошнота), которая исчезала после снижения дозы.
Наивысшая заявленная передозировка лакосамида составила 12000 мг (приняты вместе с токсическими дозами других противоэпилептических средств). Вначале возникла AV-блокада, пациент впал в коматозное состояние, а затем полностью восстановился без необратимых последствий.
Данные постмаркетингового применения. В результате острой передозировки после приема лакосамида в дозах от 1000 до 12000 мг были отмечены судороги (генерализованные тонико-клонические судороги, эпилептический статус) и нарушения проводимости сердца.
Фатальная блокада сердца наблюдалась при острой передозировке после приема 7000 мг лакосамида у пациента, имевшего кардиоваскулярные факторы риска.
Лечение. Антидота лакосамида не существует. Лечение передозировки - симптоматическое. При необходимости возможно использование гемодиализа.
Данные клинических исследований. Профиль нежелательных реакций у пациентов, принимавших сверхтерапевтические дозы, не отличался от профиля нежелательных реакций, у пациентов, принимавших рекомендованные дозы.
После приема лакосамида в дозе 1200 мг/сут наблюдалась клиническая симптоматика со стороны ЦНС и ЖКТ (головокружение и тошнота), которая исчезала после снижения дозы.
Наивысшая заявленная передозировка лакосамида составила 12000 мг (приняты вместе с токсическими дозами других противоэпилептических средств). Вначале возникла AV-блокада, пациент впал в коматозное состояние, а затем полностью восстановился без необратимых последствий.
Данные постмаркетингового применения. В результате острой передозировки после приема лакосамида в дозах от 1000 до 12000 мг были отмечены судороги (генерализованные тонико-клонические судороги, эпилептический статус) и нарушения проводимости сердца.
Фатальная блокада сердца наблюдалась при острой передозировке после приема 7000 мг лакосамида у пациента, имевшего кардиоваскулярные факторы риска.
Лечение. Антидота лакосамида не существует. Лечение передозировки - симптоматическое. При необходимости возможно использование гемодиализа.
Method of drug use and dosage
В/в, внутрь, 2 раза в день.
Application precautions
Головокружение.
Лечение лакосамидом может сопровождаться головокружением, потенциально приводящим к травмам и падениям. В связи с этим пациентам следует соблюдать осторожность до тех пор, пока они не испытают на себе потенциальные эффекты лакосамида.
Сердечный ритм и проводимость.
В клинических исследованиях лакосамида описано увеличение интервала PR.
В постмаркетинговой практике наблюдалась AV-блокада II или более высокой степени. В плацебо-контролируемых исследованиях лакосамида у пациентов с эпилепсией не были отмечены фибрилляция или трепетание предсердий, однако оба явления были отмечены в открытых исследованиях по эпилепсии, а также в постмаркетинговой практике.
Необходимо проинформировать пациента о симптомах AV-блокады II степени и выше (редкий или нерегулярный пульс, чувство легкого головокружения и потеря сознания), а также о симптомах фибрилляции и трепетания предсердий (ощущение сердцебиения, частый или нерегулярный пульс, одышка). В случае их появления необходимо обратиться к врачу. Рекомендуется периодический контроль ЭКГ.
Суицидальные мысли и поведение.
У пациентов, получавших противоэпилептические средства по нескольким показаниям, были отмечены суицидальные мысли и поведение. Мета-анализ рандомизированных плацебо-контролируемых клинических исследований противоэпилептических средств свидетельствует о небольшом увеличении риска возникновения суицидальных мыслей и суицидального поведения. Механизм повышения риска неясен, существующие данные не позволяют отрицать существование такого риска при приеме лакосамида. Таким образом, у пациентов следует проводить мониторинг признаков суицидальных мыслей и поведения, а также рассматривать вопрос о соответствующем лечении. Пациенты и лица, ухаживающие за пациентами, должны быть предупреждены о существующем риске и необходимости консультации у специалиста в случае появления суицидального поведения.
Влияние на способность управлять автомобилем и работать с механизмами. Лакосамид может оказывать влияние на способность управлять автомобилем или пользоваться сложной техникой. Лечение лакосамидом может сопровождаться развитием головокружения или нечеткостью зрения. Соответственно, пациентам не рекомендуется водить автомобиль или управлять сложной техникой.
Лечение лакосамидом может сопровождаться головокружением, потенциально приводящим к травмам и падениям. В связи с этим пациентам следует соблюдать осторожность до тех пор, пока они не испытают на себе потенциальные эффекты лакосамида.
Сердечный ритм и проводимость.
В клинических исследованиях лакосамида описано увеличение интервала PR.
В постмаркетинговой практике наблюдалась AV-блокада II или более высокой степени. В плацебо-контролируемых исследованиях лакосамида у пациентов с эпилепсией не были отмечены фибрилляция или трепетание предсердий, однако оба явления были отмечены в открытых исследованиях по эпилепсии, а также в постмаркетинговой практике.
Необходимо проинформировать пациента о симптомах AV-блокады II степени и выше (редкий или нерегулярный пульс, чувство легкого головокружения и потеря сознания), а также о симптомах фибрилляции и трепетания предсердий (ощущение сердцебиения, частый или нерегулярный пульс, одышка). В случае их появления необходимо обратиться к врачу. Рекомендуется периодический контроль ЭКГ.
Суицидальные мысли и поведение.
У пациентов, получавших противоэпилептические средства по нескольким показаниям, были отмечены суицидальные мысли и поведение. Мета-анализ рандомизированных плацебо-контролируемых клинических исследований противоэпилептических средств свидетельствует о небольшом увеличении риска возникновения суицидальных мыслей и суицидального поведения. Механизм повышения риска неясен, существующие данные не позволяют отрицать существование такого риска при приеме лакосамида. Таким образом, у пациентов следует проводить мониторинг признаков суицидальных мыслей и поведения, а также рассматривать вопрос о соответствующем лечении. Пациенты и лица, ухаживающие за пациентами, должны быть предупреждены о существующем риске и необходимости консультации у специалиста в случае появления суицидального поведения.
Влияние на способность управлять автомобилем и работать с механизмами. Лакосамид может оказывать влияние на способность управлять автомобилем или пользоваться сложной техникой. Лечение лакосамидом может сопровождаться развитием головокружения или нечеткостью зрения. Соответственно, пациентам не рекомендуется водить автомобиль или управлять сложной техникой.
References
Обобщенные материалы www.grls.rosminzdrav.ru, 2010-2015 гг.
Included in the composition
- 2.2-39.2€ Vimpat (7 firms)
- — Лакосамид ПСК (ПСК Фарма ООО )