Pharmacological Group
Latin name
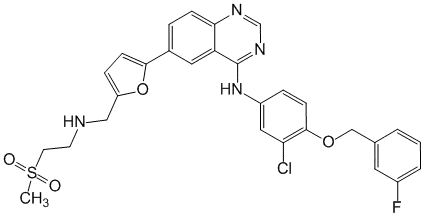
Lapatinibum ( Lapatinibi)[[c.
N-[3-Хлор-4-(3-фторбензилокси)фенил]-6-[5-[[[2-(метилсульфонил)этил]амино]метил]-2-фурил]хиназолин-4 амин (в виде дитосилата моногидрата)[[g.
Противоопухолевые средства - ингибиторы протеинкиназ.
N-[3-Хлор-4-(3-фторбензилокси)фенил]-6-[5-[[[2-(метилсульфонил)этил]амино]метил]-2-фурил]хиназолин-4 амин (в виде дитосилата моногидрата)[[g.
Противоопухолевые средства - ингибиторы протеинкиназ.
CAS Code
231277-92-2.
Use during pregnancy and lactation
Неизвестны случаи применения лапатиниба во время беременности. Женщины детородного возраста должны быть предупреждены об использовании адекватной контрацепции, а также необходимости прерывания наступившей беременности в период лечения лапатинибом.
Лапатиниб не обладал тератогенными свойствами в исследованиях на беременных мышах и кроликах, но, в то же время, был причиной возникновения некоторых отклонений в развитии в дозах, токсичных для матери.
Неизвестно, выводится ли лапатиниб в грудное молоко. Во время терапии лапатинибом рекомендуется прекратить грудное вскармливание из-за возможного возникновения характерных нежелательных явлений у грудного ребенка.[[d.
Фармакологическое действие - противоопухолевое.[[f.
Лапатиниб - это новый обратимый, селективный ингибитор внутриклеточной тирозинкиназы, связывающийся с EGFR (epidermal growth factor receptor - рецептор эпидермального фактора роста, ErbB1) и HER2/neu (human epidermal growth factor receptor - рецептор эпидермального фактора роста человека, ErbB2) рецепторами. Отличается от других быстрообратимых ингибиторов тирозинкиназы более медленной диссоциацией с ErbB1- и с ErbB2-рецепторами (период диссоциации 50% лиганда из лиганд-рецепторного комплекса составляет приблизительно 300 мин).
Помимо собственной активности in vitro была показана аддитивная активность лапатиниба и 5-фторурацила (активный метаболит капецитабина) при использовании в комбинации на четырех линиях опухолевых клеток. Ингибирующий эффект оценивался на обработанных трастузумабом клетках. Лапатиниб продемонстрировал значительную активность на линиях иммортализованных опухолевых клеток в средах, содержащих трастузумаб, что показывает отсутствие перекрестной резистентности между двумя лигандами HER2/neu (ErbB2).
Исследования in vitro показали, что лапатиниб является субстратом для переносчиков ВСRP (breast cancer resistance protein - белок резистентности рака молочной железы) - ABCGI (ATP-binding cassette subfamily G1 - АТФ-связывающий кассетный транспортер G1), P-гликопротеина (P-gp) и ABCB1 (ATP-binding cassette subfamily в1 - АТФ-связывающий кассетный транспортер в1). Также in vitro лапатиниб оказывал ингибирующий эффект в отношении данных переносчиков. Клиническое значение этих эффектов и влияние на фармакокинетику других препаратов, а также препаратов, обладающих противоопухолевой активностью, пока неизвестно.
Клиническая эффективность и безопасность.
Сочетанная терапия лапатинибом и капецитабином. Согласно результатам исследований, лапатиниб является активным веществом при его назначении в качестве монотерапии пациенткам с метастатическим раком молочной железы. Результаты исследования показали, что сочетанное применение лапатиниба с капецитабином при лечении пациенток с ErbB2-позитивным распространенным раком молочной железы увеличивает время до прогрессии, достоверно и значимо снижает риск прогрессии заболевания.
Были выявлены тенденции к улучшению показателя общей выживаемости и снижению риска летального исхода.
Комбинация лапатиниба и летрозола. Согласно результатам исследований применения лапатиниба в комбинации с летрозолом для лечения положительной по эстрогеновым и/или прогестероновым рецепторам распространенной или метастазирующей опухоли молочной железы с гиперэкспрессией HER2 у женщин в постменопаузе, была доказана эффективность комбинации лапатиниба и летрозола по сравнению с монотерапией летрозолом в отношении показателя беспрогрессивной выживаемости и клинического ответа на лечение.[[k.
Всасывание. Абсорбция после приема внутрь - неполная и вариабельная. Коэффициент вариабельности АUC - около 70%. Определяется в системном кровотоке в среднем через 0,25 ч (диапазон - 0-1,5 ч). Сmах в плазме крови достигается примерно через 4 ч после приема.
Cmax в равновесном состоянии при ежедневном приеме 1250 мг составляет в среднем 2,43 (1,57-3,77) мкг/мл, а АUC - 36,2 (23,4-56) мкг·ч/мл.
Системная экспозиция лапатиниба увеличивается при приеме препарата одновременно с пищей. AUC возрастает в 3 или 4 раза, сmax - приблизительно в 2,5 и 3 раза при приеме с пищей с низким или высоким содержанием жиров соответственно.
Связь с белками плазмы крови и распределение. Лапатиниб обладает высокой степенью связывания (более чем 99%) с альбумином и кислым альфа1-гликопротеином плазмы крови.
Метаболизм. Лапатиниб подвергается интенсивному метаболизму, главным образом изоферментами сYP3A4 и сYP3A5, в меньшей степени - сYP2C19 и сYP2C8, с образованием различных окисленных метаболитов.
Лапатиниб в клинически значимых концентрациях ингибирует сYP3A и сYP2C8 in vitro.
Лапатиниб незначительно ингибирует следующие микросомальные ферменты печени: сYP1A2, сYP2C9, сYP2C19 и сYP2D6.
У здоровых добровольцев, получающих кетоконазол (ингибитор изофермента сYP3A4) в дозе 200 мг 2 раза в сутки в течение 7 дней, системное распределение лапатиниба увеличивалось примерно в 3,6 раза, Т1/2 - в 1,7 раза.
У здоровых добровольцев, получающих карбамазепин (индуктор изофермента сYP3A4) в дозе 100 мг 2 раза в сутки в течение 3 дней и 200 мг 2 раза в сутки в течение 17 дней, системное распределение лапатиниба снижалось на 72%.
Выведение. T1/2 увеличивается дозозависимо при приеме однократных доз. Равновесное состояние достигается через 6-7 суток приема, T1/2 в равновесном состоянии составляет 24.
В основном выводится кишечником: в среднем 27% - в неизмененном виде; менее 2% принятой дозы выводится почками в неизмененном виде и в виде метаболитов.
Особые популяции пациентов.
Пациенты с нарушением функции почек. Маловероятно влияние нарушения функции почек на фармакокинетику лапатиниба.
Пациенты с нарушением функции печени. Фармакокинетика лапатиниба изучалась при умеренных (n=8) и тяжелых (n=4) нарушениях функции печени. AUC лапатиниба после приема однократной дозы 100 мг внутрь увеличивается на 56 и 85% у пациентов с умеренными и тяжелыми нарушениями функции печени соответственно.[[p.
Распространенная и/или метастазирующая опухоль молочной железы с гиперэкспрессией HER2 в составе сочетанной терапии с капецитабином у пациентов с распространенной и/или метастазирующей опухолью молочной железы с гиперэкспрессией HER2. ранее получавших терапию. включавшую антрациклины. таксаны и трастузумаб;
Гормоночувствительная распространенная и/или метастазирующая опухоль молочной железы с гиперэкспрессией HER2 в комбинации с ингибитором ароматазы для лечения пациентов с гормоночувствительной распространенной и/или метастазирующей опухолью молочной железы с гиперэкспрессией HER2.[[r.
Повышенная чувствительность к лапатинибу или любому другому компоненту препарата;
Беременность;
Период кормления грудью;
Детский возраст (отсутствие опыта применения).
С осторожностью. Состояния. которые могут приводить к левожелудочковой недостаточности. нарушения функции печени умеренной или тяжелой степени (7 баллов и более по шкале Чайлд-Пью). возраст старше 65 лет. тяжелая почечная недостаточность. одновременный прием с индукторами или мощными ингибиторами изофермента сYP3A4. грейпфрутовым соком. одновременный прием с умеренными ингибиторами изофермента сYP3A4. одновременный прием с лекарственными препаратами. являющимися субстратами изоферментов сYP3A4 и сYP2C8 с узким терапевтическим диапазоном. одновременный прием с лекарственными препаратами. повышающими рН желудочного сока (снижение растворимости и абсорбции лапатиниба).[[e.
Безопасность лапатиниба оценивалась как при монотерапии, так и при сочетанном применении с капецитабином, а также в комбинации с летрозолом. Частота возникновения нежелательных явлений классифицировалась следующим образом: очень часто - 1/10; часто - 1/100, < 1/10; нечасто - 1/1000, < 1/100; редко - 1/10000, < 1/1000; очень редко -.
Монотерапия лапатинибом.
Со стороны обмена веществ и питания. Очень часто - анорексия.
Со стороны ССС. Часто - снижение фракции выброса левого желудочка наблюдалось примерно у 1% пациентов - в 75% случаев - бессимптомное течение; разрешалось спонтанно у 60% пациентов после отмены препарата. Симптоматическое течение наблюдалось у 0,2% пациентов; симптомы включали: одышку, сердечную недостаточность, сердцебиение.
Со стороны дыхательной системы. Нечасто - интерстициальная болезнь легких/пневмонит.
Со стороны ЖКТ. Очень часто - диарея (которая может приводить к дегидратации, однако в большинстве случаев диарея 1-й или 2-й степени не приводила к отмене препарата), тошнота, рвота.
Со стороны печени и желчевыводящих путей. Нечасто - гипербилирубинемия, гепатотоксичность.
Повышение концентрации билирубина возможно вследствие угнетения лапатинибом конъюгации в печени ОАТР1В1 (полипептид, переносящий органические анионы 1В1) или угнетения выделения билирубина с желчью посредством Р-gp или вCRP.
Со стороны кожи и подкожно-жировой клетчатки. Очень часто - сыпь (включая акнеформный дерматит, в большинстве случаев проходящий, не требующий отмены препарата); часто - поражение ногтей, включая паронихию.
Со стороны иммунной системы. Редко - реакции гиперчувствительности, включая анафилаксию.
Со стороны организма в целом. Очень часто - слабость.
Лапатиниб в комбинации с капецитабином.
Дополнительно к вышеописанным, следующие нежелательные реакции наблюдались на фоне сочетанного применения лапатиниба и капецитабина с частотой выше 5% по сравнению с монотерапией капецитабином.
Со стороны ЖКТ. Очень часто - диспепсия.
Со стороны кожи и подкожно-жировой клетчатки. Очень часто - сухость кожи.
Нежелательные реакции, регистрировавшиеся при применении лапатиниба в комбинации с летрозолом с разницей в частоте встречаемости выше 5% по сравнению с монотерапией летрозолом.
Со стороны дыхательной системы, органов грудной клетки и средостения. Очень часто - носовое кровотечение.
Со стороны кожи и подкожно-жировой клетчатки. Очень часто - алопеция, сухость кожи.[[v.
Ингибиторы или индукторы изофермента сYP3A могут влиять на фармакокинетику лапатиниба. При одновременном применении лапатиниба и некоторых ингибиторов изофермента сYP3A4 (например кетоконазол, итраконазол, грейпфрутовый сок) необходимо соблюдать осторожность и тщательно наблюдать за клиническим состоянием пациента и возможными нежелательными реакциями. При необходимости одновременного назначения пациенту мощного ингибитора изофермента сYP3A4 необходимо уменьшить дозу лапатиниба до 500 мг/сут, рассчитав так, чтобы скорректировать AUC лапатиниба до величины, соответствующей применению лапатиниба без ингибиторов. Однако в настоящее время нет клинических данных о применении лапатиниба при такой коррекции дозы у пациентов, получающих мощный ингибитор изофермента сYP3A4. После отмены мощного ингибитора и выведения его из организма, спустя приблизительно 1 нед, следует вновь увеличить дозу лапатиниба до рекомендованной.
При одновременном применении лапатиниба и известных индукторов изофермента сYP3A4 (например рифампицин, карбамазепин, фенитоин) необходимо соблюдать осторожность и тщательно наблюдать за клиническим состоянием пациента и возможными нежелательными реакциями.
При необходимости одновременного назначения пациенту мощного индуктора изофермента сYP3A4 дозу лапатиниба необходимо подбирать, основываясь на переносимости, постепенно повышая ее с 1250 до 4500 мг/сут или с 1500 до 5500 мг/сут. Эта доза рассчитывается так, чтобы скорректировать AUC лапатиниба до величины, соответствующей применению лапатиниба без индукторов изофермента сYP3A4. Однако в настоящее время нет клинических данных о применении лапатиниба у пациентов, получающих сильный индуктор изофермента сYP3A4. После отмены мощного индуктора изофермента, только спустя приблизительно 2 нед, следует вновь уменьшить дозу лапатиниба до рекомендованной.
Лапатиниб ингибирует in vitro изофермент сYP3A4 в клинически значимых концентрациях. Одновременное применение лапатиниба с перорально назначаемым мидазоламом приводит к повышению AUC мидазолама примерно на 45%. При в/в введении мидазолама не обнаруживалось клинически значимого повышения AUC. Необходима осторожность при одновременном назначении лапатиниба с перорально назначаемыми препаратами с узким терапевтическим диапазоном, являющимися субстратами изофермента сYP3A4.
Лапатиниб ингибирует сYP2С8 in vitro в клинически значимых концентрациях. Следует с осторожностью назначать лапатиниб при одновременном применении с препаратами с узким терапевтическим диапазоном, которые являются субстратами сYP2C8.
Одновременное применение лапатиниба с в/в вводимым паклитакселом повышает воздействие паклитаксела на 23% в связи с ингибированием лапатинибом сYP2C8 и/или P-gp. Повышение частоты встречаемости и выраженности диареи и нейтропении наблюдалось при использовании комбинации лапатиниба и паклитаксела в клинических исследованиях. Рекомендуется с осторожностью назначать лапатиниб одновременно с паклитакселом.
Одновременное применение лапатиниба с в/в вводимым доцетакселом не оказывало значительного влияния на AUC или сmax обоих активных веществ. Однако отмечалось повышение частоты возникновения вызванной доцетакселом нейтропении.
Одновременное применение лапатиниба с иринотеканом (при введении в рамках схемы лечения FOLFIRI) приводило к повышению AUC SN-38, активного метаболита иринотекана, примерно на 40%. Точный механизм данного взаимодействия неизвестен. Рекомендуется с осторожностью назначать лапатиниб одновременно с иринотеканом.
Лапатиниб является субстратом для транспортных белков P-gp и вCRP. Ингибиторы и индукторы данных белков могут изменять активность и/или распределение лапатиниба.
Лапатиниб ингибирует транспортный белок P-gp in vitro в клинически значимых концентрациях. Одновременное применение лапатиниба с перорально вводимым дигоксином приводит к повышению AUC дигоксина примерно на 98%. Следует с осторожностью назначать лапатиниб при одновременном применении с препаратами с узким терапевтическим диапазоном, которые являются субстратами P-gp.
Лапатиниб ингибирует транспортные белки вCRP и OATP1B1 in vitro. Клиническое значение данных эффектов не изучалось, но не исключено, что лапатиниб может влиять на фармакокинетику субстратов вCRP (например топотекан) и OATP1B1 (например розувастатин).
Сочетанное применение лапатиниба с капецитабином, летрозолом или трастузумабом не влияет на фармакокинетические параметры препаратов.
Биодоступность лапатиниба зависит от приема пищи.[[a.
Максимальная суточная доза в исследованиях составляла 1800 мг.
Более частый прием препарата может приводить к повышению концентраций лапатиниба в сыворотке крови, поэтому не следует принимать пропущенные дозы, уменьшая интервалы между приемами.
Симптомы. Наблюдавшиеся симптомы включали последствия. связанные с побочными действиями. и в некоторых случаях - изъязвление кожи. синусовую тахикардию (тем не менее. с нормальной ЭКГ) и/или поражение слизистой оболочки.
Лечение. Симптоматическая терапия. Гемодиализ неэффективен. Лечение должно быть назначено врачом или, по-возможности, соответствовать принятым рекомендациям.[[o.
Лечение лапатинибом следует проводить только под контролем специалиста, имеющего опыт применения противоопухолевых препаратов.
Перед началом лечения необходимо обязательно определять фракцию выброса левого желудочка. Контроль фракции выброса левого желудочка должен быть продолжен во время лечения лапатинибом, чтобы не допустить его снижения ниже пределов допустимых значений. Лечение лапатинибом должно быть прекращено в случае снижения фракции выброса до 3-й степени или выше или в случае снижения ниже нормы. Лечение лапатинибом может быть возобновлено не ранее чем через 2 нед в меньшей дозе (1000 мг/сут), и только если фракция выброса левого желудочка находится в допустимых границах нормы. Постоянное снижение фракции выброса левого желудочка в течение 9 нед лечения, как правило, ограничивает длительность проводимой терапии.
Имеются сообщения о случаях развития интерстициальной болезни легких и пневмонита в связи с приемом лапатиниба. Пациенты должны находиться под наблюдением на предмет возникновения легочных симптомов, свидетельствующих о развитии интерстициальной болезни легких/пневмонита.
Рекомендуется назначение противодиарейных препаратов при первом развитии симптомов. При диарее тяжелой степени может потребоваться назначение электролитов и жидкости для предупреждения дегидратации (перорально или в/в), приостановление приема лапатиниба или отмена препарата.
Женщинам и мужчинам во время терапии лапатинибом и как минимум в течение 3 мес после ее окончания необходимо использовать надежные методы контрацепции.
Проявления гепатотоксичности (активность АЛТ или АСТ, превышающая ВГН в 3 раза; содержание общего билирубина, превышающее ВГН в 1,5 раза) наблюдались в клинических исследованиях ( < 1% пациентов) и пострегистрационном периоде. Гепатотоксичность может быть тяжелой. Случаи с летальным исходом были зарегистрированы, хотя причинно-следственная связь с приемом лапатиниба не была установлена. Гепатотоксичность может развиваться в течение от нескольких дней до нескольких месяцев после начала терапии. Необходимо проводить контроль лабораторных показателей функции печени (аминотрансферазы, билирубина и ЩФ) до начала терапии, далее каждые 4-6 нед в течение курса лечения по клиническим показаниям. При возникновении тяжелых нарушений функции печени необходима отмена лапатиниба, повторное назначение препарата недопустимо.
При назначении лапатиниба пациентам с сопутствующими тяжелыми нарушениями функции печени рекомендовано снижение дозы лапатиниба.
Влияние на способность управлять автомобилем и выполнять работы, требующие повышенной скорости физических и психических реакций. Не изучалось. Исходя из механизма действия лапатиниба, нельзя предположить неблагоприятное влияние препарата на такую деятельность. Однако следует принимать во внимание общее состояние пациента и профиль побочных эффектов лапатиниба.[[б.
За дополнительной информацией обращаться в представительство компании GlaxoSmithKline:
Россия, 121614, Москва, ул. Крылатская, 17, корп. 3.
Тел: (495) 777-89-00; факс: (495) 777-89-04.[[ф.
Описание было автоматически дополнено из инструкции препарата «Тайверб», поскольку у самого действующего вещества нет подробного описания.
Лапатиниб не обладал тератогенными свойствами в исследованиях на беременных мышах и кроликах, но, в то же время, был причиной возникновения некоторых отклонений в развитии в дозах, токсичных для матери.
Неизвестно, выводится ли лапатиниб в грудное молоко. Во время терапии лапатинибом рекомендуется прекратить грудное вскармливание из-за возможного возникновения характерных нежелательных явлений у грудного ребенка.[[d.
Фармакологическое действие - противоопухолевое.[[f.
Лапатиниб - это новый обратимый, селективный ингибитор внутриклеточной тирозинкиназы, связывающийся с EGFR (epidermal growth factor receptor - рецептор эпидермального фактора роста, ErbB1) и HER2/neu (human epidermal growth factor receptor - рецептор эпидермального фактора роста человека, ErbB2) рецепторами. Отличается от других быстрообратимых ингибиторов тирозинкиназы более медленной диссоциацией с ErbB1- и с ErbB2-рецепторами (период диссоциации 50% лиганда из лиганд-рецепторного комплекса составляет приблизительно 300 мин).
Помимо собственной активности in vitro была показана аддитивная активность лапатиниба и 5-фторурацила (активный метаболит капецитабина) при использовании в комбинации на четырех линиях опухолевых клеток. Ингибирующий эффект оценивался на обработанных трастузумабом клетках. Лапатиниб продемонстрировал значительную активность на линиях иммортализованных опухолевых клеток в средах, содержащих трастузумаб, что показывает отсутствие перекрестной резистентности между двумя лигандами HER2/neu (ErbB2).
Исследования in vitro показали, что лапатиниб является субстратом для переносчиков ВСRP (breast cancer resistance protein - белок резистентности рака молочной железы) - ABCGI (ATP-binding cassette subfamily G1 - АТФ-связывающий кассетный транспортер G1), P-гликопротеина (P-gp) и ABCB1 (ATP-binding cassette subfamily в1 - АТФ-связывающий кассетный транспортер в1). Также in vitro лапатиниб оказывал ингибирующий эффект в отношении данных переносчиков. Клиническое значение этих эффектов и влияние на фармакокинетику других препаратов, а также препаратов, обладающих противоопухолевой активностью, пока неизвестно.
Клиническая эффективность и безопасность.
Сочетанная терапия лапатинибом и капецитабином. Согласно результатам исследований, лапатиниб является активным веществом при его назначении в качестве монотерапии пациенткам с метастатическим раком молочной железы. Результаты исследования показали, что сочетанное применение лапатиниба с капецитабином при лечении пациенток с ErbB2-позитивным распространенным раком молочной железы увеличивает время до прогрессии, достоверно и значимо снижает риск прогрессии заболевания.
Были выявлены тенденции к улучшению показателя общей выживаемости и снижению риска летального исхода.
Комбинация лапатиниба и летрозола. Согласно результатам исследований применения лапатиниба в комбинации с летрозолом для лечения положительной по эстрогеновым и/или прогестероновым рецепторам распространенной или метастазирующей опухоли молочной железы с гиперэкспрессией HER2 у женщин в постменопаузе, была доказана эффективность комбинации лапатиниба и летрозола по сравнению с монотерапией летрозолом в отношении показателя беспрогрессивной выживаемости и клинического ответа на лечение.[[k.
Всасывание. Абсорбция после приема внутрь - неполная и вариабельная. Коэффициент вариабельности АUC - около 70%. Определяется в системном кровотоке в среднем через 0,25 ч (диапазон - 0-1,5 ч). Сmах в плазме крови достигается примерно через 4 ч после приема.
Cmax в равновесном состоянии при ежедневном приеме 1250 мг составляет в среднем 2,43 (1,57-3,77) мкг/мл, а АUC - 36,2 (23,4-56) мкг·ч/мл.
Системная экспозиция лапатиниба увеличивается при приеме препарата одновременно с пищей. AUC возрастает в 3 или 4 раза, сmax - приблизительно в 2,5 и 3 раза при приеме с пищей с низким или высоким содержанием жиров соответственно.
Связь с белками плазмы крови и распределение. Лапатиниб обладает высокой степенью связывания (более чем 99%) с альбумином и кислым альфа1-гликопротеином плазмы крови.
Метаболизм. Лапатиниб подвергается интенсивному метаболизму, главным образом изоферментами сYP3A4 и сYP3A5, в меньшей степени - сYP2C19 и сYP2C8, с образованием различных окисленных метаболитов.
Лапатиниб в клинически значимых концентрациях ингибирует сYP3A и сYP2C8 in vitro.
Лапатиниб незначительно ингибирует следующие микросомальные ферменты печени: сYP1A2, сYP2C9, сYP2C19 и сYP2D6.
У здоровых добровольцев, получающих кетоконазол (ингибитор изофермента сYP3A4) в дозе 200 мг 2 раза в сутки в течение 7 дней, системное распределение лапатиниба увеличивалось примерно в 3,6 раза, Т1/2 - в 1,7 раза.
У здоровых добровольцев, получающих карбамазепин (индуктор изофермента сYP3A4) в дозе 100 мг 2 раза в сутки в течение 3 дней и 200 мг 2 раза в сутки в течение 17 дней, системное распределение лапатиниба снижалось на 72%.
Выведение. T1/2 увеличивается дозозависимо при приеме однократных доз. Равновесное состояние достигается через 6-7 суток приема, T1/2 в равновесном состоянии составляет 24.
В основном выводится кишечником: в среднем 27% - в неизмененном виде; менее 2% принятой дозы выводится почками в неизмененном виде и в виде метаболитов.
Особые популяции пациентов.
Пациенты с нарушением функции почек. Маловероятно влияние нарушения функции почек на фармакокинетику лапатиниба.
Пациенты с нарушением функции печени. Фармакокинетика лапатиниба изучалась при умеренных (n=8) и тяжелых (n=4) нарушениях функции печени. AUC лапатиниба после приема однократной дозы 100 мг внутрь увеличивается на 56 и 85% у пациентов с умеренными и тяжелыми нарушениями функции печени соответственно.[[p.
Распространенная и/или метастазирующая опухоль молочной железы с гиперэкспрессией HER2 в составе сочетанной терапии с капецитабином у пациентов с распространенной и/или метастазирующей опухолью молочной железы с гиперэкспрессией HER2. ранее получавших терапию. включавшую антрациклины. таксаны и трастузумаб;
Гормоночувствительная распространенная и/или метастазирующая опухоль молочной железы с гиперэкспрессией HER2 в комбинации с ингибитором ароматазы для лечения пациентов с гормоночувствительной распространенной и/или метастазирующей опухолью молочной железы с гиперэкспрессией HER2.[[r.
Повышенная чувствительность к лапатинибу или любому другому компоненту препарата;
Беременность;
Период кормления грудью;
Детский возраст (отсутствие опыта применения).
С осторожностью. Состояния. которые могут приводить к левожелудочковой недостаточности. нарушения функции печени умеренной или тяжелой степени (7 баллов и более по шкале Чайлд-Пью). возраст старше 65 лет. тяжелая почечная недостаточность. одновременный прием с индукторами или мощными ингибиторами изофермента сYP3A4. грейпфрутовым соком. одновременный прием с умеренными ингибиторами изофермента сYP3A4. одновременный прием с лекарственными препаратами. являющимися субстратами изоферментов сYP3A4 и сYP2C8 с узким терапевтическим диапазоном. одновременный прием с лекарственными препаратами. повышающими рН желудочного сока (снижение растворимости и абсорбции лапатиниба).[[e.
Безопасность лапатиниба оценивалась как при монотерапии, так и при сочетанном применении с капецитабином, а также в комбинации с летрозолом. Частота возникновения нежелательных явлений классифицировалась следующим образом: очень часто - 1/10; часто - 1/100, < 1/10; нечасто - 1/1000, < 1/100; редко - 1/10000, < 1/1000; очень редко -.
Монотерапия лапатинибом.
Со стороны обмена веществ и питания. Очень часто - анорексия.
Со стороны ССС. Часто - снижение фракции выброса левого желудочка наблюдалось примерно у 1% пациентов - в 75% случаев - бессимптомное течение; разрешалось спонтанно у 60% пациентов после отмены препарата. Симптоматическое течение наблюдалось у 0,2% пациентов; симптомы включали: одышку, сердечную недостаточность, сердцебиение.
Со стороны дыхательной системы. Нечасто - интерстициальная болезнь легких/пневмонит.
Со стороны ЖКТ. Очень часто - диарея (которая может приводить к дегидратации, однако в большинстве случаев диарея 1-й или 2-й степени не приводила к отмене препарата), тошнота, рвота.
Со стороны печени и желчевыводящих путей. Нечасто - гипербилирубинемия, гепатотоксичность.
Повышение концентрации билирубина возможно вследствие угнетения лапатинибом конъюгации в печени ОАТР1В1 (полипептид, переносящий органические анионы 1В1) или угнетения выделения билирубина с желчью посредством Р-gp или вCRP.
Со стороны кожи и подкожно-жировой клетчатки. Очень часто - сыпь (включая акнеформный дерматит, в большинстве случаев проходящий, не требующий отмены препарата); часто - поражение ногтей, включая паронихию.
Со стороны иммунной системы. Редко - реакции гиперчувствительности, включая анафилаксию.
Со стороны организма в целом. Очень часто - слабость.
Лапатиниб в комбинации с капецитабином.
Дополнительно к вышеописанным, следующие нежелательные реакции наблюдались на фоне сочетанного применения лапатиниба и капецитабина с частотой выше 5% по сравнению с монотерапией капецитабином.
Со стороны ЖКТ. Очень часто - диспепсия.
Со стороны кожи и подкожно-жировой клетчатки. Очень часто - сухость кожи.
Нежелательные реакции, регистрировавшиеся при применении лапатиниба в комбинации с летрозолом с разницей в частоте встречаемости выше 5% по сравнению с монотерапией летрозолом.
Со стороны дыхательной системы, органов грудной клетки и средостения. Очень часто - носовое кровотечение.
Со стороны кожи и подкожно-жировой клетчатки. Очень часто - алопеция, сухость кожи.[[v.
Ингибиторы или индукторы изофермента сYP3A могут влиять на фармакокинетику лапатиниба. При одновременном применении лапатиниба и некоторых ингибиторов изофермента сYP3A4 (например кетоконазол, итраконазол, грейпфрутовый сок) необходимо соблюдать осторожность и тщательно наблюдать за клиническим состоянием пациента и возможными нежелательными реакциями. При необходимости одновременного назначения пациенту мощного ингибитора изофермента сYP3A4 необходимо уменьшить дозу лапатиниба до 500 мг/сут, рассчитав так, чтобы скорректировать AUC лапатиниба до величины, соответствующей применению лапатиниба без ингибиторов. Однако в настоящее время нет клинических данных о применении лапатиниба при такой коррекции дозы у пациентов, получающих мощный ингибитор изофермента сYP3A4. После отмены мощного ингибитора и выведения его из организма, спустя приблизительно 1 нед, следует вновь увеличить дозу лапатиниба до рекомендованной.
При одновременном применении лапатиниба и известных индукторов изофермента сYP3A4 (например рифампицин, карбамазепин, фенитоин) необходимо соблюдать осторожность и тщательно наблюдать за клиническим состоянием пациента и возможными нежелательными реакциями.
При необходимости одновременного назначения пациенту мощного индуктора изофермента сYP3A4 дозу лапатиниба необходимо подбирать, основываясь на переносимости, постепенно повышая ее с 1250 до 4500 мг/сут или с 1500 до 5500 мг/сут. Эта доза рассчитывается так, чтобы скорректировать AUC лапатиниба до величины, соответствующей применению лапатиниба без индукторов изофермента сYP3A4. Однако в настоящее время нет клинических данных о применении лапатиниба у пациентов, получающих сильный индуктор изофермента сYP3A4. После отмены мощного индуктора изофермента, только спустя приблизительно 2 нед, следует вновь уменьшить дозу лапатиниба до рекомендованной.
Лапатиниб ингибирует in vitro изофермент сYP3A4 в клинически значимых концентрациях. Одновременное применение лапатиниба с перорально назначаемым мидазоламом приводит к повышению AUC мидазолама примерно на 45%. При в/в введении мидазолама не обнаруживалось клинически значимого повышения AUC. Необходима осторожность при одновременном назначении лапатиниба с перорально назначаемыми препаратами с узким терапевтическим диапазоном, являющимися субстратами изофермента сYP3A4.
Лапатиниб ингибирует сYP2С8 in vitro в клинически значимых концентрациях. Следует с осторожностью назначать лапатиниб при одновременном применении с препаратами с узким терапевтическим диапазоном, которые являются субстратами сYP2C8.
Одновременное применение лапатиниба с в/в вводимым паклитакселом повышает воздействие паклитаксела на 23% в связи с ингибированием лапатинибом сYP2C8 и/или P-gp. Повышение частоты встречаемости и выраженности диареи и нейтропении наблюдалось при использовании комбинации лапатиниба и паклитаксела в клинических исследованиях. Рекомендуется с осторожностью назначать лапатиниб одновременно с паклитакселом.
Одновременное применение лапатиниба с в/в вводимым доцетакселом не оказывало значительного влияния на AUC или сmax обоих активных веществ. Однако отмечалось повышение частоты возникновения вызванной доцетакселом нейтропении.
Одновременное применение лапатиниба с иринотеканом (при введении в рамках схемы лечения FOLFIRI) приводило к повышению AUC SN-38, активного метаболита иринотекана, примерно на 40%. Точный механизм данного взаимодействия неизвестен. Рекомендуется с осторожностью назначать лапатиниб одновременно с иринотеканом.
Лапатиниб является субстратом для транспортных белков P-gp и вCRP. Ингибиторы и индукторы данных белков могут изменять активность и/или распределение лапатиниба.
Лапатиниб ингибирует транспортный белок P-gp in vitro в клинически значимых концентрациях. Одновременное применение лапатиниба с перорально вводимым дигоксином приводит к повышению AUC дигоксина примерно на 98%. Следует с осторожностью назначать лапатиниб при одновременном применении с препаратами с узким терапевтическим диапазоном, которые являются субстратами P-gp.
Лапатиниб ингибирует транспортные белки вCRP и OATP1B1 in vitro. Клиническое значение данных эффектов не изучалось, но не исключено, что лапатиниб может влиять на фармакокинетику субстратов вCRP (например топотекан) и OATP1B1 (например розувастатин).
Сочетанное применение лапатиниба с капецитабином, летрозолом или трастузумабом не влияет на фармакокинетические параметры препаратов.
Биодоступность лапатиниба зависит от приема пищи.[[a.
Максимальная суточная доза в исследованиях составляла 1800 мг.
Более частый прием препарата может приводить к повышению концентраций лапатиниба в сыворотке крови, поэтому не следует принимать пропущенные дозы, уменьшая интервалы между приемами.
Симптомы. Наблюдавшиеся симптомы включали последствия. связанные с побочными действиями. и в некоторых случаях - изъязвление кожи. синусовую тахикардию (тем не менее. с нормальной ЭКГ) и/или поражение слизистой оболочки.
Лечение. Симптоматическая терапия. Гемодиализ неэффективен. Лечение должно быть назначено врачом или, по-возможности, соответствовать принятым рекомендациям.[[o.
Лечение лапатинибом следует проводить только под контролем специалиста, имеющего опыт применения противоопухолевых препаратов.
Перед началом лечения необходимо обязательно определять фракцию выброса левого желудочка. Контроль фракции выброса левого желудочка должен быть продолжен во время лечения лапатинибом, чтобы не допустить его снижения ниже пределов допустимых значений. Лечение лапатинибом должно быть прекращено в случае снижения фракции выброса до 3-й степени или выше или в случае снижения ниже нормы. Лечение лапатинибом может быть возобновлено не ранее чем через 2 нед в меньшей дозе (1000 мг/сут), и только если фракция выброса левого желудочка находится в допустимых границах нормы. Постоянное снижение фракции выброса левого желудочка в течение 9 нед лечения, как правило, ограничивает длительность проводимой терапии.
Имеются сообщения о случаях развития интерстициальной болезни легких и пневмонита в связи с приемом лапатиниба. Пациенты должны находиться под наблюдением на предмет возникновения легочных симптомов, свидетельствующих о развитии интерстициальной болезни легких/пневмонита.
Рекомендуется назначение противодиарейных препаратов при первом развитии симптомов. При диарее тяжелой степени может потребоваться назначение электролитов и жидкости для предупреждения дегидратации (перорально или в/в), приостановление приема лапатиниба или отмена препарата.
Женщинам и мужчинам во время терапии лапатинибом и как минимум в течение 3 мес после ее окончания необходимо использовать надежные методы контрацепции.
Проявления гепатотоксичности (активность АЛТ или АСТ, превышающая ВГН в 3 раза; содержание общего билирубина, превышающее ВГН в 1,5 раза) наблюдались в клинических исследованиях ( < 1% пациентов) и пострегистрационном периоде. Гепатотоксичность может быть тяжелой. Случаи с летальным исходом были зарегистрированы, хотя причинно-следственная связь с приемом лапатиниба не была установлена. Гепатотоксичность может развиваться в течение от нескольких дней до нескольких месяцев после начала терапии. Необходимо проводить контроль лабораторных показателей функции печени (аминотрансферазы, билирубина и ЩФ) до начала терапии, далее каждые 4-6 нед в течение курса лечения по клиническим показаниям. При возникновении тяжелых нарушений функции печени необходима отмена лапатиниба, повторное назначение препарата недопустимо.
При назначении лапатиниба пациентам с сопутствующими тяжелыми нарушениями функции печени рекомендовано снижение дозы лапатиниба.
Влияние на способность управлять автомобилем и выполнять работы, требующие повышенной скорости физических и психических реакций. Не изучалось. Исходя из механизма действия лапатиниба, нельзя предположить неблагоприятное влияние препарата на такую деятельность. Однако следует принимать во внимание общее состояние пациента и профиль побочных эффектов лапатиниба.[[б.
За дополнительной информацией обращаться в представительство компании GlaxoSmithKline:
Россия, 121614, Москва, ул. Крылатская, 17, корп. 3.
Тел: (495) 777-89-00; факс: (495) 777-89-04.[[ф.
Описание было автоматически дополнено из инструкции препарата «Тайверб», поскольку у самого действующего вещества нет подробного описания.