Pharmacological Group
Latin name
Ganirelixum ( Ganirelixi).
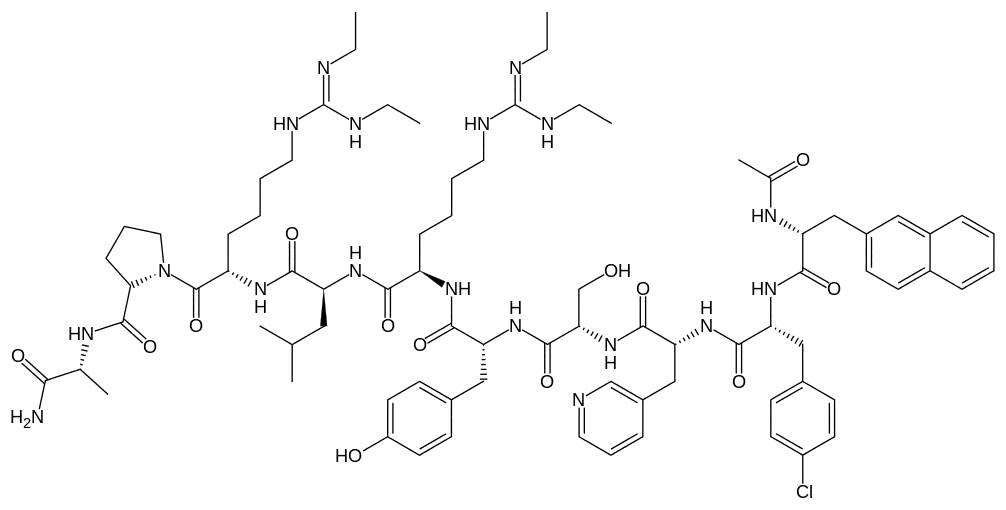
Chemical name
N-Ацетил-3-(2-нафтил)-D-аланил-п-хлор-D-фенилаланил-3-(3-пиридинил)-D-аланил-L-серил-L-тирозил-N6-[(этиламино)(этилимино)метил]-D-лизил-L-лейцил-N6-[(этиламино)(этилимино)метил]-L-лизил-L-пролил-D-аланинамид (в виде диацетата).
Used in the treatment
CAS Code
124904-93-4.
Pharmacological action
Антигонадотропное.
Characteristics of the substance
Антагонист гонадотропин-рилизинг гормона (ГнРГ). Синтетический декапептид с высокой антагонистической активностью по отношению к природному ГнРГ. Ганиреликса ацетат является производным природного ГнРГ с замещениями аминокислот в позициях 1, 2, 3, 6, 8 и 10. Растворим в воде.
Pharmacodynamics
Пульсирующее высвобождение ГнРГ стимулирует синтез и секрецию лютеинизирующего и фолликулостимулирующего гормона. Частота выбросов ЛГ в среднюю и позднюю фолликулярную фазу - примерно 1 выброс в час. Эти пульсации сопровождаются кратковременным повышением уровня ЛГ в сыворотке. В середине цикла значительное повышение высвобождения ГнРГ приводит к подъему уровня ЛГ, который инициирует ряд физиологических процессов, включая овуляцию, возобновление мейоза в ооците, лютеинизацию. Лютеинизация приводит к повышению уровня прогестерона в сыворотке с сопутствующим снижением уровня эстрадиола.
Ганиреликса ацетат конкурентно блокирует рецепторы ГнРГ гонадотрофов аденогипофиза. Вызывает быстрое обратимое подавление секреции эндогенных гонадотропинов гипофизом без начальной стимуляции их высвобождения. Угнетение секреции ЛГ более выражено, чем супрессия секреции ФСГ. После прекращения введения ганиреликса уровень ЛГ и ФСГ полностью возвращается к исходным значениям в течение 48.
Фармакокинетика ганиреликса ацетата оценивалась при его п/к введении в дозе 0,25 мг 1 раз в сутки ежедневно на протяжении 7 дней здоровым женщинам-добровольцам (n=15). После п/к введения быстро абсорбируется, maxCmax достигается примерно в течение 1 ч и составляет после однократного п/к введения 14,8±3,2 нг/мл. Абсолютная биодоступность после однократного введения 0,25 мг составляет 91,1%, объем распределения - 43,7±11,4 л. Связывание с белками плазмы in vitro >in vitro составляет 81,9%. Равновесная концентрация в крови достигается через 3 дня лечения. Фармакокинетика является дозозависимой в диапазоне доз 0,125-0,5 мг.
Исследование метаболизма ганиреликса ацетата показало, что после однократного в/в введения радиоактивно меченного вещества здоровым женщинам-добровольцам ЛС определяется в плазме (50-70% общей радиоактивности) вплоть до 4 ч после инъекции и в моче (17,1-18,4% дозы) вплоть до 24 В фекалиях в неизмененном виде не обнаруживается, но определяется в виде 1-4 пептида и 1-6 пептида. При исследовании экскреции ганиреликса ацетата выявлено, что после в/в однократного введения 1 мг 14C-ганиреликса ацетата в среднем 97,2% радиоактивности обнаруживается в фекалиях и моче (75,1% и 22,1%, соответственно) в течение 288 ч после введения, причем экскреция с мочой завершается фактически в течение 24 тогда как кривая, отражающая экскрецию с фекалиями, выходит на плато через 192 ч после инъекции.
Т1/2 составляло 12,8±4,3 ч при однократном и 16,2±1,6 ч при многократном п/к введении здоровым женщинам-добровольцам (n=15).
Клинические исследования.
Эффективность ганиреликса ацетата оценивалась в контролируемых клинических исследованиях с включением пациенток с нормальным эндокринным статусом, а также нормальными характеристиками УЗИ органов малого таза. Критериями исключения из исследования были синдром поликистозных яичников, а также незначительный овариальный резерв или его отсутствие.
При проведении клинических исследований использовали рекомбинантный фоллитропин бета для инъекций, который вводили по утрам, начиная со 2-3-го дня менструального цикла в дозе 150 МЕ. Утром 7-8-го дня цикла, начиная с 6-го дня введения рекомбинантного ФСГ (рекФСГ) вводили ганиреликса ацетат, при этом дозу рекФСГ корректировали в зависимости от индивидуального ответа яичников на стимуляцию. Введение рекФСГ и ганиреликса продолжали до момента, когда по крайней мере 3 фолликула достигали размера 17 мм и более, после чего для финального созревания фолликулов вводили человеческий гонадотропин хорионический (чГХ) и прекращали введение рекФСГ и ганиреликса. Ооциты извлекали и проводили ЭКО (экстракорпоральное оплодотворение) или ИКСИ (интрацитоплазматическая инъекция сперматозоида).
В многоцентровом двойном слепом рандомизированном исследовании была выявлена оптимальная доза ЛС, необходимая для предупреждения преждевременного высвобождения ЛГ при контролируемой овариальной гиперстимуляции. В исследовании участвовали 332 пациентки, которым проводили контролируемую овариальную гиперстимуляцию с применением рекФСГ. Ганиреликса ацетат использовали в дозах от 0,0625 мг до 2 мг. К моменту введения чГХ медиана сывороточного уровня ЛГ снижалась с увеличением дозы ганиреликса, а медианы (в скобках указаны 5-95 процентили) уровней в сыворотке Е2 (17-бета-эстрадиол) составляли 1475 (645-3720), 1110 (424-3780) и 1160 (384-3910) пг/мл при дозах ганиреликса 0,0625; 0,125 и 0,25 мг, соответственно. Более низкие пики концентраций Е2, равные 823, 703 и 441 пг/мл определялись при более высоких дозах ганиреликса ацетата - 0,5; 1 и 2 мг, соответственно. Самая высокая частота имплантации эмбрионов (21,9%) и наступления беременности (25%) была отмечена при дозе ганиреликса 0,25 мг.
Кратковременное повышение ЛГ не было опасным для достижения беременности при использовании доз ганиреликса 0,125 мг (3 из 6 пациенток) и 0,25 мг (1/1). Кроме того, ни у кого из пациенток при отмеченном повышении ЛГ ≥10 МЕ/л не отмечалось преждевременной лютеинизации (оценивалась по уровню плазменного прогестерона, превышающему 2 нг/мл).
В мультицентровом открытом рандомизированном исследовании оценки эффективности и безопасности ганиреликса (с включением в исследование 463 пациенток, получавших п/к инъекции ганиреликса в дозе 0,25 мг) преждевременный выброс ЛГ до введения чГХ (повышение ЛГ ≥10 МЕ/л с сопутствующим значимым повышением прогестерона сыворотки более 2 нг/мл или значимым снижением эстрадиола сыворотки) наблюдался менее чем в 1% случаев.
Канцерогенность, мутагенность, влияние на фертильность.
Длительные исследования токсичности ганиреликса ацетата на животных с целью оценки его потенциальной канцерогенности не проведены. Не индуцировал мутаций в тесте Эймса (S.typhimurium и E.coli) и хромосомных аберраций in vitro >in vitro в тесте с использованием клеток яичников китайских хомячков.
Ганиреликса ацетат конкурентно блокирует рецепторы ГнРГ гонадотрофов аденогипофиза. Вызывает быстрое обратимое подавление секреции эндогенных гонадотропинов гипофизом без начальной стимуляции их высвобождения. Угнетение секреции ЛГ более выражено, чем супрессия секреции ФСГ. После прекращения введения ганиреликса уровень ЛГ и ФСГ полностью возвращается к исходным значениям в течение 48.
Фармакокинетика ганиреликса ацетата оценивалась при его п/к введении в дозе 0,25 мг 1 раз в сутки ежедневно на протяжении 7 дней здоровым женщинам-добровольцам (n=15). После п/к введения быстро абсорбируется, maxCmax достигается примерно в течение 1 ч и составляет после однократного п/к введения 14,8±3,2 нг/мл. Абсолютная биодоступность после однократного введения 0,25 мг составляет 91,1%, объем распределения - 43,7±11,4 л. Связывание с белками плазмы in vitro >in vitro составляет 81,9%. Равновесная концентрация в крови достигается через 3 дня лечения. Фармакокинетика является дозозависимой в диапазоне доз 0,125-0,5 мг.
Исследование метаболизма ганиреликса ацетата показало, что после однократного в/в введения радиоактивно меченного вещества здоровым женщинам-добровольцам ЛС определяется в плазме (50-70% общей радиоактивности) вплоть до 4 ч после инъекции и в моче (17,1-18,4% дозы) вплоть до 24 В фекалиях в неизмененном виде не обнаруживается, но определяется в виде 1-4 пептида и 1-6 пептида. При исследовании экскреции ганиреликса ацетата выявлено, что после в/в однократного введения 1 мг 14C-ганиреликса ацетата в среднем 97,2% радиоактивности обнаруживается в фекалиях и моче (75,1% и 22,1%, соответственно) в течение 288 ч после введения, причем экскреция с мочой завершается фактически в течение 24 тогда как кривая, отражающая экскрецию с фекалиями, выходит на плато через 192 ч после инъекции.
Т1/2 составляло 12,8±4,3 ч при однократном и 16,2±1,6 ч при многократном п/к введении здоровым женщинам-добровольцам (n=15).
Клинические исследования.
Эффективность ганиреликса ацетата оценивалась в контролируемых клинических исследованиях с включением пациенток с нормальным эндокринным статусом, а также нормальными характеристиками УЗИ органов малого таза. Критериями исключения из исследования были синдром поликистозных яичников, а также незначительный овариальный резерв или его отсутствие.
При проведении клинических исследований использовали рекомбинантный фоллитропин бета для инъекций, который вводили по утрам, начиная со 2-3-го дня менструального цикла в дозе 150 МЕ. Утром 7-8-го дня цикла, начиная с 6-го дня введения рекомбинантного ФСГ (рекФСГ) вводили ганиреликса ацетат, при этом дозу рекФСГ корректировали в зависимости от индивидуального ответа яичников на стимуляцию. Введение рекФСГ и ганиреликса продолжали до момента, когда по крайней мере 3 фолликула достигали размера 17 мм и более, после чего для финального созревания фолликулов вводили человеческий гонадотропин хорионический (чГХ) и прекращали введение рекФСГ и ганиреликса. Ооциты извлекали и проводили ЭКО (экстракорпоральное оплодотворение) или ИКСИ (интрацитоплазматическая инъекция сперматозоида).
В многоцентровом двойном слепом рандомизированном исследовании была выявлена оптимальная доза ЛС, необходимая для предупреждения преждевременного высвобождения ЛГ при контролируемой овариальной гиперстимуляции. В исследовании участвовали 332 пациентки, которым проводили контролируемую овариальную гиперстимуляцию с применением рекФСГ. Ганиреликса ацетат использовали в дозах от 0,0625 мг до 2 мг. К моменту введения чГХ медиана сывороточного уровня ЛГ снижалась с увеличением дозы ганиреликса, а медианы (в скобках указаны 5-95 процентили) уровней в сыворотке Е2 (17-бета-эстрадиол) составляли 1475 (645-3720), 1110 (424-3780) и 1160 (384-3910) пг/мл при дозах ганиреликса 0,0625; 0,125 и 0,25 мг, соответственно. Более низкие пики концентраций Е2, равные 823, 703 и 441 пг/мл определялись при более высоких дозах ганиреликса ацетата - 0,5; 1 и 2 мг, соответственно. Самая высокая частота имплантации эмбрионов (21,9%) и наступления беременности (25%) была отмечена при дозе ганиреликса 0,25 мг.
Кратковременное повышение ЛГ не было опасным для достижения беременности при использовании доз ганиреликса 0,125 мг (3 из 6 пациенток) и 0,25 мг (1/1). Кроме того, ни у кого из пациенток при отмеченном повышении ЛГ ≥10 МЕ/л не отмечалось преждевременной лютеинизации (оценивалась по уровню плазменного прогестерона, превышающему 2 нг/мл).
В мультицентровом открытом рандомизированном исследовании оценки эффективности и безопасности ганиреликса (с включением в исследование 463 пациенток, получавших п/к инъекции ганиреликса в дозе 0,25 мг) преждевременный выброс ЛГ до введения чГХ (повышение ЛГ ≥10 МЕ/л с сопутствующим значимым повышением прогестерона сыворотки более 2 нг/мл или значимым снижением эстрадиола сыворотки) наблюдался менее чем в 1% случаев.
Канцерогенность, мутагенность, влияние на фертильность.
Длительные исследования токсичности ганиреликса ацетата на животных с целью оценки его потенциальной канцерогенности не проведены. Не индуцировал мутаций в тесте Эймса (S.typhimurium и E.coli) и хромосомных аберраций in vitro >in vitro в тесте с использованием клеток яичников китайских хомячков.
Indications for use
Ингибирование преждевременного пикового повышения секреции ЛГ у женщин. подвергающихся контролируемой гиперстимуляции яичников в программах лечения бесплодия с использованием вспомогательных репродуктивных технологий.
Contraindications
Гиперчувствительность, в тч к ГнРГ или любому другому аналогу ГнРГ, беременность или подозрение на беременность.
Use during pregnancy and lactation
Противопоказано при беременности или подозрении на беременность (до начала лечения беременность должна быть исключена).
При введении ганиреликса ацетата беременным крысам и кроликам в период с 7-го дня до близкого к родам срока в дозах до 10 и 30 мкг/сут, соответственно (примерно в 0,4 и 3,2 раза выше дозы для человека, исходя из площади поверхности тела), отмечалось повышение процента резорбции приплода. Не наблюдалось повышения фетальных нарушений. Не было отмечено связанных с лекарством изменений фертильности, физических или поведенческих характеристик у потомства самок крыс, получавших ганиреликса ацетат в период беременности и лактации. Влияние на резорбцию плодов является следствием изменения гормонального уровня за счет антигонадотропных свойств лекарства, что может приводить к потере плода у человека (не следует использовать у беременных женщин).
Категория действия на плод по FDA. X.
Противопоказано при грудном вскармливании (неизвестно, проникает ли ЛС в грудное молоко).
При введении ганиреликса ацетата беременным крысам и кроликам в период с 7-го дня до близкого к родам срока в дозах до 10 и 30 мкг/сут, соответственно (примерно в 0,4 и 3,2 раза выше дозы для человека, исходя из площади поверхности тела), отмечалось повышение процента резорбции приплода. Не наблюдалось повышения фетальных нарушений. Не было отмечено связанных с лекарством изменений фертильности, физических или поведенческих характеристик у потомства самок крыс, получавших ганиреликса ацетат в период беременности и лактации. Влияние на резорбцию плодов является следствием изменения гормонального уровня за счет антигонадотропных свойств лекарства, что может приводить к потере плода у человека (не следует использовать у беременных женщин).
Категория действия на плод по FDA. X.
Противопоказано при грудном вскармливании (неизвестно, проникает ли ЛС в грудное молоко).
Side effects
Побочные реакции. которые наблюдались в завершенных контролируемых клинических исследованиях с первого дня применения ганиреликса ацетата (n=794) до подтверждения беременности с помощью УЗИ у ≥1% пациентов. применявших ЛС. и не были напрямую связаны с приемом лекарства.
Боль в животе (гинекологическая) (4,8%). гибель эмбриона/плода (3,7%). головная боль (3,0%). синдром гиперстимуляции яичников (2,4%). вагинальное кровотечение (1,8%). реакции в месте инъекции (1,1%). тошнота (1,1%). боль в животе (желудочно-кишечная) (1,0%).
В постмаркетинговых исследованиях были отмечены редкие случаи реакций гиперчувствительности, включая анафилактоидные реакции после первой дозы.
Врожденные аномалии.
По результатам клинически завершенных исследований из 283 новорожденных. рожденных женщинами. применявшими ганиреликса ацетат. у 3-х были серьезные врожденные аномалии (в тч гидроцефалия/менингоцеле. омфалоцеле) и у 18 - менее тяжелые врожденные аномалии (в тч невус. кожные метки. сакральный синус. гемангиома. кривошея/асимметрия черепа. косолапость. добавочные пальцы рук. подвывих бедра. кривошея/высокое небо. пупочная грыжа. паховая грыжа. гидроцеле. неопустившееся яичко. гидронефроз. Причинная связь между этими врожденными аномалиями и приемом ганиреликса ацетата не выявлена.
Боль в животе (гинекологическая) (4,8%). гибель эмбриона/плода (3,7%). головная боль (3,0%). синдром гиперстимуляции яичников (2,4%). вагинальное кровотечение (1,8%). реакции в месте инъекции (1,1%). тошнота (1,1%). боль в животе (желудочно-кишечная) (1,0%).
В постмаркетинговых исследованиях были отмечены редкие случаи реакций гиперчувствительности, включая анафилактоидные реакции после первой дозы.
Врожденные аномалии.
По результатам клинически завершенных исследований из 283 новорожденных. рожденных женщинами. применявшими ганиреликса ацетат. у 3-х были серьезные врожденные аномалии (в тч гидроцефалия/менингоцеле. омфалоцеле) и у 18 - менее тяжелые врожденные аномалии (в тч невус. кожные метки. сакральный синус. гемангиома. кривошея/асимметрия черепа. косолапость. добавочные пальцы рук. подвывих бедра. кривошея/высокое небо. пупочная грыжа. паховая грыжа. гидроцеле. неопустившееся яичко. гидронефроз. Причинная связь между этими врожденными аномалиями и приемом ганиреликса ацетата не выявлена.
Interaction
Применение с другими лекарственными препаратами не исследовано в достаточной степени, поэтому нельзя исключать вероятность лекарственного взаимодействия.
Method of drug use and dosage
П/ 0,25 мг 1 раз в сутки. Ганиреликса ацетат обычно вводят на 6-й день применения препарата ФСГ (контролируемая стимуляция овуляции препаратом ФСГ начинается на 2-й или 3-й день менструального цикла). Применение препарата следует продолжать ежедневно до дня начала применения чГХ, до момента образования достаточного числа фолликулов соответствующего размера (преовуляторных фолликулов) (подтверждается УЗИ), затем окончательное созревание фолликулов может быть инициировано путем введения чХГ.
В случае повышенной реакции яичников на стимуляцию, для предупреждения преждевременного повышения уровня ЛГ, лечение ганиреликса ацетатом следует начинать с 5-го дня применения препаратов ФСГ. В случае медленного роста фолликулов введение ганиреликса можно отложить ( начинать позднее 6-го дня применения препаратов ФСГ).
От введения чХГ необходимо воздержаться в случаях, если яичники в последний день ФСГ-терапии чрезмерно увеличены (возможно развитие синдрома гиперстимуляции яичников).
В случае повышенной реакции яичников на стимуляцию, для предупреждения преждевременного повышения уровня ЛГ, лечение ганиреликса ацетатом следует начинать с 5-го дня применения препаратов ФСГ. В случае медленного роста фолликулов введение ганиреликса можно отложить ( начинать позднее 6-го дня применения препаратов ФСГ).
От введения чХГ необходимо воздержаться в случаях, если яичники в последний день ФСГ-терапии чрезмерно увеличены (возможно развитие синдрома гиперстимуляции яичников).
Application precautions
Может назначаться только специалистом, имеющим опыт в лечении бесплодия.
В постмаркетинговых исследованиях были отмечены редкие случаи реакций гиперчувствительности, включая анафилактоидные реакции после первой дозы ( см «Побочные действия»).
До начала терапии пациентка должна быть предупреждена о продолжительности лечения, необходимости проведения мониторинговых процедур и риске возможных побочных реакций. Лечащий врач должен быть проинформирован о лекарственных средствах, которые пациентка принимала незадолго до начала лечения или продолжает принимать параллельно с назначением препарата.
Безопасность и эффективность применения препарата не была установлена в отношении женщин массой тела менее 50 кг или более 90 кг.
При повторных курсах лечения следует использовать препарат только после тщательной оценки степени потенциального риска и эффективности лечения.
В постмаркетинговых исследованиях были отмечены редкие случаи реакций гиперчувствительности, включая анафилактоидные реакции после первой дозы ( см «Побочные действия»).
До начала терапии пациентка должна быть предупреждена о продолжительности лечения, необходимости проведения мониторинговых процедур и риске возможных побочных реакций. Лечащий врач должен быть проинформирован о лекарственных средствах, которые пациентка принимала незадолго до начала лечения или продолжает принимать параллельно с назначением препарата.
Безопасность и эффективность применения препарата не была установлена в отношении женщин массой тела менее 50 кг или более 90 кг.
При повторных курсах лечения следует использовать препарат только после тщательной оценки степени потенциального риска и эффективности лечения.
Included in the composition
- 62.3€ Orgalutran (3 firms)