Pharmacological Group
Latin name
Indinavirum ( Indinaviri).
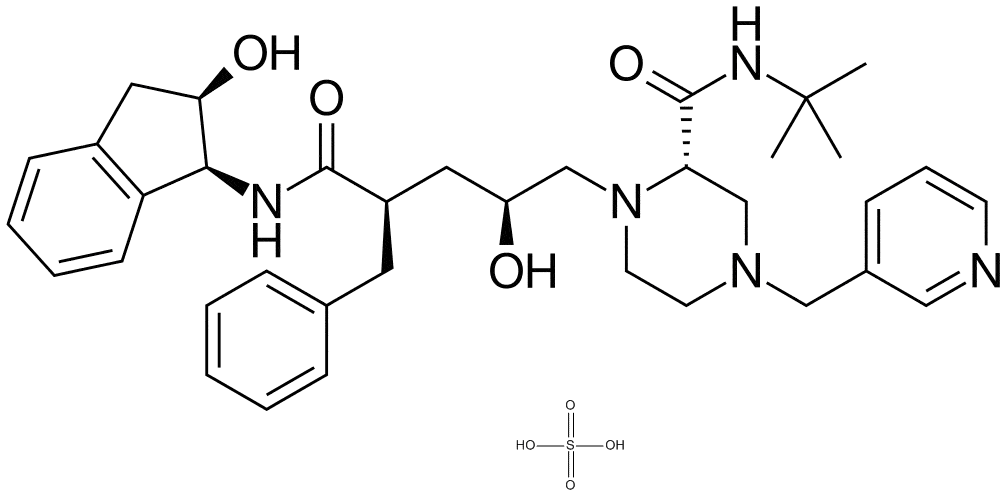
Chemical name
(R,S,2S)-альфа-Бензил-2-(трет-бутилкарбамоил)-бета-гидрокси-N-[(1S,2R)- 2-гидрокси-1-инданил]-4-(3-пиридилметил)-1-пиперазинвалерамид.
Used in the treatment
CAS Code
150378-17-9.
Pharmacological action
Ингибирующее протеазу ВИЧ, противовирусное.
Characteristics of the substance
Ингибитор ВИЧ-протеазы. Белый или почти белый гигроскопичный кристаллический порошок. Хорошо растворим в воде и метаноле.
Pharmacodynamics
Ингибирует ВИЧ-протеазу - фермент, необходимый для протеолитического расщепления полипептидов-предшественников и образования функциональных белков вируса. Связываясь с активным участком протеазы, индинавир ингибирует ее ферментативную активность, вследствие чего предотвращает расщепление полипротеинов вируса, что приводит к образованию незрелых вирусных частиц, неспособных инфицировать другие клетки.
Оценка антиретровирусной активности индинавира in vitro >in vitro показала, что в концентрациях от 25 до 100 нМ он на 95% ингибирует репликацию ВИЧ−1 в культурах клеток лимфоидного и моноцитарного ряда и в культуре лимфоцитов, инфицированных лабораторными штаммами или первичными клиническими изолятами ВИЧ−1, в тч изолятами, устойчивыми к нуклеозидным и ненуклеозидным ингибиторам ВИЧ−1 обратной транскриптазы. В экспериментах на культуре клеток проявлялась синергичная антиретровирусная активность в отношении ВИЧ−1 в комбинации с ингибиторами обратной транскриптазы (зидовудин, диданозин). Взаимосвязь между чувствительностью ВИЧ−1 к индинавиру in vitro >in vitro и подавлением репликации вируса в организме человека не установлена.
От некоторых больных получены изоляты ВИЧ−1 с пониженной чувствительностью к индинавиру. Вирусная резистентность коррелирует с накоплением мутаций в вирусном геноме, приводящих к экспрессии замещенных аминокислотных остатков в ферменте (вирусной протеазе). Идентифицировано по крайней мере 11 положений аминокислотных остатков в этом ферменте, замещение в которых сопровождается развитием резистентности. Причем устойчивость к ингибитору опосредована не одиночным, а множественными и разнообразными замещениями. В целом более высокий уровень резистентности является результатом коэкспрессии большего числа замещений в 11 идентифицированных положениях.
Отмечена перекрестная устойчивость различной степени выраженности между индинавиром и другими ингибиторами ВИЧ−1 протеазы. В исследованиях с использованием ритонавира, саквинавира и ампренавира выраженность и спектр перекрестной устойчивости варьировали. Показано, что степень перекрестной резистентности увеличивается по мере накопления замещений аминокислотных остатков, ассоциируемых с резистентностью. Исследование 29 изолятов от больных, леченных индинавиром, показало, что все они были резистенты к ритонавиру. Среди индинавиррезистентных ВИЧ−1 изолятов 63% были резистентны к саквинавиру и 81% - к ампренавиру.
После приема внутрь (натощак) быстро всасывается из ЖКТ. Время достижения maxCmax составляет 0,8±0,3 ч (n=11). В диапазоне доз 200-1000 мг концентрация индинавира в плазме повышается не пропорционально дозе. Прием вместе с высококалорийной пищей, богатой жирами и белками, приводил к снижению абсорбции, при этом AUC и maxCmax уменьшались примерно на 80% (n=10). Прием легкой пищи (например, подсушенные тосты с желе, яблочный сок, кофе с обезжиренным молоком и сахаром, кукурузные хлопья) практически не вызывал изменения абсорбции. Связывание с белками плазмы крови составляет 60%.
После перорального приема здоровыми добровольцами меченого углеродом (14С) индинавира в дозе 400 мг 83±1% общей радиоактивности обнаруживалось в фекалиях (n=4), 19±3% - в моче (n=6), из них в неизмененном виде - 19,1% и 9,4%, соответственно. Было идентифицировано 7 метаболитов: один конъюгат с глюкуроновой кислотой и 6 продуктов окисления. В исследованиях in vitro >in vitro на микросомах печени показано, что главным изоферментом цитохрома Р450, участвующим в окислительном метаболизме индинавира, является сYP3A4. Менее 20% индинавира выводится с мочой в неизмененном виде. Средняя почечная экскреция неизмененного вещества составляет 10,4±4,9% (n=10) и 12,0±4,9% (n=10) после приема однократной дозы 700 мг и 1000 мг, соответственно. Т1/2 составляет 1,8±0,4 ч (n=10). При приеме многократных доз по 800 мг каждые 8 ч значимой кумуляции не наблюдается.
Проникновение индинавира через плацентарный барьер значительно у крыс и собак, но невелико у кроликов. Индинавир интенсивно выделяется в молоко лактирующих крыс.
Зависимость параметров фармакокинетики от некоторых факторов.
Печеночная недостаточность. У пациентов с легкой и умеренной печеночной недостаточностью и клинически установленным циррозом печени отмечалось снижение метаболизма индинавира, проявлявшееся в повышении AUC примерно на 60% после приема однократной дозы 400 мг (n=12), повышении 1/2T1/2 до 2,8±0,5 Фармакокинетика индинавира у пациентов с тяжелой печеночной недостаточностью не изучалась.
Почечная недостаточность. Фармакокинетика индинавира у пациентов с почечной недостаточностью не изучалась.
Пол. Клинически значимых различий между фармакокинетическими параметрами (в тч AUC, сmax) в зависимости от пола не выявлено.
Раса. Фармакокинетические параметры индинавира у 42 представителей европеоидной расы (26 ВИЧ-позитивных) и 16 представителей негроидной расы (4 ВИЧ-позитивных) были сравнимы.
В двух клинических испытаниях индинавира в комбинации с антиретровирусными средствами продолжительностью примерно 1 год продемонстрировано снижение риска СПИД-ассоциированных заболеваний или смерти, а также длительная супрессия вирусной РНК.
Канцерогенность, мутагенность, влияние на фертильность.
Оценка канцерогенности индинавира проводилась в исследованиях на мышах и крысах. Не было отмечено увеличения частоты возникновения опухолей у мышей. При наивысших тестируемых дозах у крыс (640 мг/кг/сут) было отмечено статистически значимое увеличение частоты возникновения опухолей щитовидной железы у самцов крыс. Не выявлено мутагенноcти или генотоксичности в ряде тестов in vitro >in vitro и in vivo >in vivo, влияния на скрещиваемость, фертильность, эмбриональное выживание потомков у крыс при использовании доз, обеспечивающих системное воздействие, сравнимое или немного большее, чем при использовании терапевтических доз у человека.
Беременность. Изучение токсичности индинавира проводилось у кроликов, собак и крыс при использовании доз, обеспечивающих системное воздействие, сравнимое или незначительно большее, чем у человека. Не было обнаружено внешних или висцеральных нарушений, изменений скелета у кроликов и собак. У крыс выявлено повышение (по сравнению с контролем) частоты образования избыточных ребер (при воздействии равном или меньшем, чем у человека) и шейных ребер (при воздействии сравнимом или большем, чем у человека). Не обнаружено влияния индинавира на эмбрио/фетальное выживание или рост плода у всех трех видов.
Введение индинавира новорожденным обезьянам-резусам (в дозах до 160 мг/кг 2 раза в сутки) вызывало усиление транзиторной физиологической гипербилирубинемии (уровни билирубина в сыворотке примерно в 4 раза превышали контрольные). Введение индинавира обезьянам (в тех же дозах) в матку в III триместре беременности не вызывало таких изменений у новорожденных. При дозах 40, 80 или 160 мг/кг 2 раза в сутки у обезьян уровни индинавира в крови плода составляли примерно 1-2% от уровней в материнском организме.
Оценка антиретровирусной активности индинавира in vitro >in vitro показала, что в концентрациях от 25 до 100 нМ он на 95% ингибирует репликацию ВИЧ−1 в культурах клеток лимфоидного и моноцитарного ряда и в культуре лимфоцитов, инфицированных лабораторными штаммами или первичными клиническими изолятами ВИЧ−1, в тч изолятами, устойчивыми к нуклеозидным и ненуклеозидным ингибиторам ВИЧ−1 обратной транскриптазы. В экспериментах на культуре клеток проявлялась синергичная антиретровирусная активность в отношении ВИЧ−1 в комбинации с ингибиторами обратной транскриптазы (зидовудин, диданозин). Взаимосвязь между чувствительностью ВИЧ−1 к индинавиру in vitro >in vitro и подавлением репликации вируса в организме человека не установлена.
От некоторых больных получены изоляты ВИЧ−1 с пониженной чувствительностью к индинавиру. Вирусная резистентность коррелирует с накоплением мутаций в вирусном геноме, приводящих к экспрессии замещенных аминокислотных остатков в ферменте (вирусной протеазе). Идентифицировано по крайней мере 11 положений аминокислотных остатков в этом ферменте, замещение в которых сопровождается развитием резистентности. Причем устойчивость к ингибитору опосредована не одиночным, а множественными и разнообразными замещениями. В целом более высокий уровень резистентности является результатом коэкспрессии большего числа замещений в 11 идентифицированных положениях.
Отмечена перекрестная устойчивость различной степени выраженности между индинавиром и другими ингибиторами ВИЧ−1 протеазы. В исследованиях с использованием ритонавира, саквинавира и ампренавира выраженность и спектр перекрестной устойчивости варьировали. Показано, что степень перекрестной резистентности увеличивается по мере накопления замещений аминокислотных остатков, ассоциируемых с резистентностью. Исследование 29 изолятов от больных, леченных индинавиром, показало, что все они были резистенты к ритонавиру. Среди индинавиррезистентных ВИЧ−1 изолятов 63% были резистентны к саквинавиру и 81% - к ампренавиру.
После приема внутрь (натощак) быстро всасывается из ЖКТ. Время достижения maxCmax составляет 0,8±0,3 ч (n=11). В диапазоне доз 200-1000 мг концентрация индинавира в плазме повышается не пропорционально дозе. Прием вместе с высококалорийной пищей, богатой жирами и белками, приводил к снижению абсорбции, при этом AUC и maxCmax уменьшались примерно на 80% (n=10). Прием легкой пищи (например, подсушенные тосты с желе, яблочный сок, кофе с обезжиренным молоком и сахаром, кукурузные хлопья) практически не вызывал изменения абсорбции. Связывание с белками плазмы крови составляет 60%.
После перорального приема здоровыми добровольцами меченого углеродом (14С) индинавира в дозе 400 мг 83±1% общей радиоактивности обнаруживалось в фекалиях (n=4), 19±3% - в моче (n=6), из них в неизмененном виде - 19,1% и 9,4%, соответственно. Было идентифицировано 7 метаболитов: один конъюгат с глюкуроновой кислотой и 6 продуктов окисления. В исследованиях in vitro >in vitro на микросомах печени показано, что главным изоферментом цитохрома Р450, участвующим в окислительном метаболизме индинавира, является сYP3A4. Менее 20% индинавира выводится с мочой в неизмененном виде. Средняя почечная экскреция неизмененного вещества составляет 10,4±4,9% (n=10) и 12,0±4,9% (n=10) после приема однократной дозы 700 мг и 1000 мг, соответственно. Т1/2 составляет 1,8±0,4 ч (n=10). При приеме многократных доз по 800 мг каждые 8 ч значимой кумуляции не наблюдается.
Проникновение индинавира через плацентарный барьер значительно у крыс и собак, но невелико у кроликов. Индинавир интенсивно выделяется в молоко лактирующих крыс.
Зависимость параметров фармакокинетики от некоторых факторов.
Печеночная недостаточность. У пациентов с легкой и умеренной печеночной недостаточностью и клинически установленным циррозом печени отмечалось снижение метаболизма индинавира, проявлявшееся в повышении AUC примерно на 60% после приема однократной дозы 400 мг (n=12), повышении 1/2T1/2 до 2,8±0,5 Фармакокинетика индинавира у пациентов с тяжелой печеночной недостаточностью не изучалась.
Почечная недостаточность. Фармакокинетика индинавира у пациентов с почечной недостаточностью не изучалась.
Пол. Клинически значимых различий между фармакокинетическими параметрами (в тч AUC, сmax) в зависимости от пола не выявлено.
Раса. Фармакокинетические параметры индинавира у 42 представителей европеоидной расы (26 ВИЧ-позитивных) и 16 представителей негроидной расы (4 ВИЧ-позитивных) были сравнимы.
В двух клинических испытаниях индинавира в комбинации с антиретровирусными средствами продолжительностью примерно 1 год продемонстрировано снижение риска СПИД-ассоциированных заболеваний или смерти, а также длительная супрессия вирусной РНК.
Канцерогенность, мутагенность, влияние на фертильность.
Оценка канцерогенности индинавира проводилась в исследованиях на мышах и крысах. Не было отмечено увеличения частоты возникновения опухолей у мышей. При наивысших тестируемых дозах у крыс (640 мг/кг/сут) было отмечено статистически значимое увеличение частоты возникновения опухолей щитовидной железы у самцов крыс. Не выявлено мутагенноcти или генотоксичности в ряде тестов in vitro >in vitro и in vivo >in vivo, влияния на скрещиваемость, фертильность, эмбриональное выживание потомков у крыс при использовании доз, обеспечивающих системное воздействие, сравнимое или немного большее, чем при использовании терапевтических доз у человека.
Беременность. Изучение токсичности индинавира проводилось у кроликов, собак и крыс при использовании доз, обеспечивающих системное воздействие, сравнимое или незначительно большее, чем у человека. Не было обнаружено внешних или висцеральных нарушений, изменений скелета у кроликов и собак. У крыс выявлено повышение (по сравнению с контролем) частоты образования избыточных ребер (при воздействии равном или меньшем, чем у человека) и шейных ребер (при воздействии сравнимом или большем, чем у человека). Не обнаружено влияния индинавира на эмбрио/фетальное выживание или рост плода у всех трех видов.
Введение индинавира новорожденным обезьянам-резусам (в дозах до 160 мг/кг 2 раза в сутки) вызывало усиление транзиторной физиологической гипербилирубинемии (уровни билирубина в сыворотке примерно в 4 раза превышали контрольные). Введение индинавира обезьянам (в тех же дозах) в матку в III триместре беременности не вызывало таких изменений у новорожденных. При дозах 40, 80 или 160 мг/кг 2 раза в сутки у обезьян уровни индинавира в крови плода составляли примерно 1-2% от уровней в материнском организме.
Indications for use
По данным Physicians Desk Reference (2003), индинавира сульфат в комбинации с антиретровирусными средствами показан для лечения ВИЧ-инфекции.
Contraindications
Гиперчувствительность. нельзя назначать одновременно с терфенадином. цизапридом. астемизолом. триазоламом. мидазоламом или препаратами на основе экстрактов спорыньи (ингибирование индинавиром изофермента сYP3A4 может привести к повышению концентраций этих ЛС в крови. что может вызывать тяжелые или угрожающие жизни реакции).
Restrictions on use
Беременность, кормление грудью, детский возраст (безопасность и эффективность применения у детей не определены).
Use during pregnancy and lactation
При беременности возможно, только если ожидаемый эффект терапии превышает потенциальный риск для плода (адекватных и строго контролируемых исследований у беременных женщин не проводили).
Категория действия на плод по FDA. с.
Способность индинавира экскретироваться в молоко кормящих женщин не определена. В экспериментальных исследованиях показано, что индинавир проникает в грудное молоко у лактирующих крыс. На время лечения следует прекратить кормление грудью (в связи с возможностью развития серьезных побочных эффектов у младенцев, находящихся на грудном вскармливании).
Неизвестно, усиливает ли индинавир, принимаемый матерью в перинатальный период, физиологическую гипербилирубинемию у новорожденных.
Категория действия на плод по FDA. с.
Способность индинавира экскретироваться в молоко кормящих женщин не определена. В экспериментальных исследованиях показано, что индинавир проникает в грудное молоко у лактирующих крыс. На время лечения следует прекратить кормление грудью (в связи с возможностью развития серьезных побочных эффектов у младенцев, находящихся на грудном вскармливании).
Неизвестно, усиливает ли индинавир, принимаемый матерью в перинатальный период, физиологическую гипербилирубинемию у новорожденных.
Side effects
Побочные эффекты. связанные с приемом индинавира сульфата и наблюдавшиеся более чем у 2% пациентов (по результатам двойного слепого. мультицентрового. рандомизированного. оконченного испытания. проведенного в Бразилии - Study 028). представлены в таблице 1.
Таблица 1.
Клинически выраженные побочные эффекты средней или тяжелой степени выраженности, встречавшиеся у ?2% пациентов (Study 028).
В ходе ряда клинических испытаний примерно у 12,4% (301/2429) пациентов. получавших индинавира сульфат в рекомендуемых дозах. был отмечен нефролитиаз. в тч боль в боку с гематурией (включая микрогематурию) или без нее (в диапазоне от 4,7% до 34,4% в различных исследованиях). средний срок клинических испытаний составлял 47 нед (в диапазоне от 1 дня до 242 нед. 2238 пациентов завершили исследование). В ходе клинических испытаний во время двойной слепой фазы при развитии нефролитиаза на фоне лечения индинавира сульфатом у 2,8% (7/246) пациентов развился гидронефроз, у 4,5% (11/246) - установлен стент. После острых приступов у 4,9% (12/246) пациентов лечение было отменено.
При лечении индинавира сульфатом наблюдались случаи бессимптомной гипербилирубинемии (общий билирубин ?2,5 мг/дл). которая проявлялась главным образом повышением непрямого билирубина (примерно 14%) и менее чем в 1% случаев сопровождалась повышением АЛТ или АСТ.
Гипербилирубинемия и нефролитиаз встречались с большей частотой при приеме доз, превышающих 2,4 г/сут (по сравнению с приемом доз ?2,4 г/сут).
Некоторые лабораторные параметры представлены в таблице 2.
Таблица 2.
Данные некоторых лабораторных анализов тяжелой и угрожающей жизни степени выраженности (Study 028).
* ВГН - верхняя граница нормы.
Данные постмаркетинговых исследований.
Организм в целом. Перераспределение/накопление жира в области затылка, грудной клетки, живота и забрюшинной области.
Сердечно-сосудистая система и кровь: сердечно-сосудистые заболевания. в тч инфаркт миокарда. стенокардия. цереброваскулярные нарушения. повышение частоты спонтанных кровотечений у больных гемофилией. острая гемолитическая анемия ( см «Меры предосторожности»).
Желудочно-кишечный тракт. Нарушение функции печени. гепатит. печеночная недостаточность ( см «Меры предосторожности»). панкреатит. вздутие живота. желтуха. диспепсия.
Аллергические реакции. Анафилактоидные реакции, крапивница, васкулит.
Нервная система и органы чувств. Оральная парестезия, депрессия.
Кожа и ее придатки. Сыпь. в тч многоформная эритема и синдром Стивенса - Джонсона. гиперпигментация. алопеция. врастание ногтей пальцев стоп и/или паронихия. зуд.
Мочеполовая система. Нефролитиаз. в тч с нарушением функции почек. включая острую почечную недостаточность ( см «Меры предосторожности»). пиелонефрит с бактериемией или без нее. кристаллурия. интерстициальный нефрит. иногда с отложением кристаллов индинавира. у некоторых пациентов интерстициальный нефрит не прекращался после окончания приема индинавира сульфата. лейкоцитурия. дизурия.
Прочие. Впервые выявленный сахарный диабет. обострение имеющегося сахарного диабета. гипергликемия ( см «Меры предосторожности»). артралгия. повышение триглицеридов сыворотки. повышение холестерина сыворотки.
Таблица 1.
Клинически выраженные побочные эффекты средней или тяжелой степени выраженности, встречавшиеся у ?2% пациентов (Study 028).
| Системы организма/Побочные эффекты | Частота возникновения, % | ||
| Индинавира сульфат (n=332) | Индинавира сульфат + зидовудин (n=332) | Зидовудин (n=332) | |
| Организм в целом | |||
| Боль в животе | 16,6 | 16,0 | 12,0 |
| Слабость/утомляемость | 2,1 | 4,2 | 3,6 |
| Лихорадка | 1,5 | 1,5 | 2,1 |
| Недомогание | 2,1 | 2,7 | 1,8 |
| Желудочно-кишечный тракт | |||
| Тошнота | 11,7 | 31,9 | 19,6 |
| Диарея | 3,3 | 3,0 | 2,4 |
| Рвота | 8,4 | 17,8 | 9,0 |
| Кислая отрыжка | 2,7 | 5,4 | 1,8 |
| Анорексия | 2,7 | 5,4 | 3,0 |
| Повышение аппетита | 2,1 | 1,5 | 1,2 |
| Диспепсия | 1,5 | 2,7 | 0,9 |
| Желтуха | 1,5 | 2,1 | 0,3 |
| Сердечно-сосудистая система и кровь | |||
| Анемия | 0,6 | 1,2 | 2,1 |
| Опорно-двигательный аппарат | |||
| Боль в спине | 8,4 | 4,5 | 1,5 |
| Нервная система и органы чувств | |||
| Головная боль | 5,4 | 9,6 | 6,0 |
| Головокружение | 3,0 | 3,9 | 0,9 |
| Сонливость | 2,4 | 3,3 | 3,3 |
| Извращение вкуса | 2,7 | 8,4 | 1,2 |
| Кожные покровы | |||
| Зуд | 4,2 | 2,4 | 1,8 |
| Сыпь | 1,2 | 0,6 | 2,4 |
| Мочеполовая система | |||
| Нефролитиаз (включая почечную колику, боль в боку с/без гематурии) | 8,7 | 7,8 | 8,1 |
| Дизурия | 1,5 | 2,4 | 0,3 |
В ходе ряда клинических испытаний примерно у 12,4% (301/2429) пациентов. получавших индинавира сульфат в рекомендуемых дозах. был отмечен нефролитиаз. в тч боль в боку с гематурией (включая микрогематурию) или без нее (в диапазоне от 4,7% до 34,4% в различных исследованиях). средний срок клинических испытаний составлял 47 нед (в диапазоне от 1 дня до 242 нед. 2238 пациентов завершили исследование). В ходе клинических испытаний во время двойной слепой фазы при развитии нефролитиаза на фоне лечения индинавира сульфатом у 2,8% (7/246) пациентов развился гидронефроз, у 4,5% (11/246) - установлен стент. После острых приступов у 4,9% (12/246) пациентов лечение было отменено.
При лечении индинавира сульфатом наблюдались случаи бессимптомной гипербилирубинемии (общий билирубин ?2,5 мг/дл). которая проявлялась главным образом повышением непрямого билирубина (примерно 14%) и менее чем в 1% случаев сопровождалась повышением АЛТ или АСТ.
Гипербилирубинемия и нефролитиаз встречались с большей частотой при приеме доз, превышающих 2,4 г/сут (по сравнению с приемом доз ?2,4 г/сут).
Некоторые лабораторные параметры представлены в таблице 2.
Таблица 2.
Данные некоторых лабораторных анализов тяжелой и угрожающей жизни степени выраженности (Study 028).
| Показатели | Частота, % | |||
| Индинавира сульфат (n=329) | Индинавира сульфат + зидовудин (n=320) | Зидовудин (n=330) | ||
| Гематология | ||||
| Понижение гемоглобина менее 70 г/л | 0,6 | 0,9 | 3,3 | |
| Понижение числа тромбоцитов менее 50·109/л | 0,9 | 0,9 | 1,8 | |
| Понижение числа нейтрофилов менее 0,75·109/л | 2,4 | 2,2 | 6,7 | |
| Биохимия крови | ||||
| Повышение АЛТ более 500% ВГН* | 4,9 | 4,1 | 3,0 | |
| Повышение АСТ более 500% ВГН | 3,7 | 2,8 | 2,7 | |
| Общий билирубин сыворотки более 250% ВГН | 11,9 | 9,7 | 0,6 | |
| Повышение амилазы сыворотки более 200% ВГН | 2,1 | 1,9 | 1,8 | |
| Повышение глюкозы более 13,875 ммоль/л | 0,9 | 0,9 | 0,6 | |
| Повышение креатинина более 300% ВГН | 0 | 0 | 0,6 | |
* ВГН - верхняя граница нормы.
Данные постмаркетинговых исследований.
Организм в целом. Перераспределение/накопление жира в области затылка, грудной клетки, живота и забрюшинной области.
Сердечно-сосудистая система и кровь: сердечно-сосудистые заболевания. в тч инфаркт миокарда. стенокардия. цереброваскулярные нарушения. повышение частоты спонтанных кровотечений у больных гемофилией. острая гемолитическая анемия ( см «Меры предосторожности»).
Желудочно-кишечный тракт. Нарушение функции печени. гепатит. печеночная недостаточность ( см «Меры предосторожности»). панкреатит. вздутие живота. желтуха. диспепсия.
Аллергические реакции. Анафилактоидные реакции, крапивница, васкулит.
Нервная система и органы чувств. Оральная парестезия, депрессия.
Кожа и ее придатки. Сыпь. в тч многоформная эритема и синдром Стивенса - Джонсона. гиперпигментация. алопеция. врастание ногтей пальцев стоп и/или паронихия. зуд.
Мочеполовая система. Нефролитиаз. в тч с нарушением функции почек. включая острую почечную недостаточность ( см «Меры предосторожности»). пиелонефрит с бактериемией или без нее. кристаллурия. интерстициальный нефрит. иногда с отложением кристаллов индинавира. у некоторых пациентов интерстициальный нефрит не прекращался после окончания приема индинавира сульфата. лейкоцитурия. дизурия.
Прочие. Впервые выявленный сахарный диабет. обострение имеющегося сахарного диабета. гипергликемия ( см «Меры предосторожности»). артралгия. повышение триглицеридов сыворотки. повышение холестерина сыворотки.
Interaction
Не следует назначать одновременно с терфенадином, цизапридом, астемизолом, триазоламом, мидазоламом или препаратами на основе экстрактов спорыньи (ингибирование индинавиром сYP3A4 ферментной системы цитохрома Р450 может привести к повышению концентраций этих ЛС в крови и к развитию тяжелых или угрожающих жизни реакций).
Рифампицин является мощным индуктором изофермента сYP3А4 и заметно снижает концентрацию индинавира в плазме (не следует назначать одновременно).
Взаимодействие индинавира с препаратами, которые являются менее мощными индукторами сYP3A4, чем рифампицин, например, фенобарбитал, фенитоин, карбамазепин и дексаметазон не изучали; при совместном приеме следует соблюдать осторожность (возможно понижение концентрации индинавира в плазме).
Препараты, содержащие экстракт зверобоя, снижают плазменный уровень индинавира (возможно снижение эффективности лечения).
Одновременное назначение рифабутина и индинавира сопровождается увеличением концентрации рифабутина и снижением концентрации индинавира в плазме (необходимо снижение дозы рифабутина и повышение дозы индинавира).
В связи с увеличением концентрации в плазме индинавира, при одновременном назначении индинавира и кетоконазола следует рассмотреть возможность снижения дозы индинавира.
Итраконазол является ингибитором сYPЗА4, что повышает концентрации индинавира в плазме (при одновременном назначении требуется снижение дозы индинавира).
При одновременном назначении индинавира и эфавиренза в связи с ферментной индукцией понижается концентрация индинавира в плазме крови (необходимо увеличение дозы индинавира).
По результатам одного опубликованного исследования, у ВИЧ-инфицированных мужчин (n=6) совместное применение индинавира и силденафила цитрата приводило к взаимному повышению концентрации индинавира (в тч AUC в интервале 0-8 ч после приема - на 11%, сmax - на 48%) и силденафила (AUC повышалось на 340%) в крови (следует соблюдать особую осторожность ввиду повышения риска развития неблагоприятных эффектов силденафила).
Одновременное применение индинавира сульфата с ловастатином или симвастатином не рекомендуется. Следует соблюдать осторожность при приеме ингибиторов протеаз (включая индинавира сульфат) одновременно и с другими ингибиторами ГМГ-КoA-редуктазы, метаболизирующимися при участии сYP3A4 (например, аторвастатин кальций или церивастатин натрия), при таком сочетании лекарственных средств может увеличиваться риск миопатии, включая рабдомиолиз.
В исследованиях не наблюдалось клинически значимых взаимодействий со следующими лекарствами: зидовудин, зидовудин/ламивудин, триметоприм/сульфаметоксазол, флуконазол, изониазид, кларитромицин, метадон, циметидин, хинидин, норэтистерон/этинилэстрадиолсодержащий контрацептив.
Рифампицин является мощным индуктором изофермента сYP3А4 и заметно снижает концентрацию индинавира в плазме (не следует назначать одновременно).
Взаимодействие индинавира с препаратами, которые являются менее мощными индукторами сYP3A4, чем рифампицин, например, фенобарбитал, фенитоин, карбамазепин и дексаметазон не изучали; при совместном приеме следует соблюдать осторожность (возможно понижение концентрации индинавира в плазме).
Препараты, содержащие экстракт зверобоя, снижают плазменный уровень индинавира (возможно снижение эффективности лечения).
Одновременное назначение рифабутина и индинавира сопровождается увеличением концентрации рифабутина и снижением концентрации индинавира в плазме (необходимо снижение дозы рифабутина и повышение дозы индинавира).
В связи с увеличением концентрации в плазме индинавира, при одновременном назначении индинавира и кетоконазола следует рассмотреть возможность снижения дозы индинавира.
Итраконазол является ингибитором сYPЗА4, что повышает концентрации индинавира в плазме (при одновременном назначении требуется снижение дозы индинавира).
При одновременном назначении индинавира и эфавиренза в связи с ферментной индукцией понижается концентрация индинавира в плазме крови (необходимо увеличение дозы индинавира).
По результатам одного опубликованного исследования, у ВИЧ-инфицированных мужчин (n=6) совместное применение индинавира и силденафила цитрата приводило к взаимному повышению концентрации индинавира (в тч AUC в интервале 0-8 ч после приема - на 11%, сmax - на 48%) и силденафила (AUC повышалось на 340%) в крови (следует соблюдать особую осторожность ввиду повышения риска развития неблагоприятных эффектов силденафила).
Одновременное применение индинавира сульфата с ловастатином или симвастатином не рекомендуется. Следует соблюдать осторожность при приеме ингибиторов протеаз (включая индинавира сульфат) одновременно и с другими ингибиторами ГМГ-КoA-редуктазы, метаболизирующимися при участии сYP3A4 (например, аторвастатин кальций или церивастатин натрия), при таком сочетании лекарственных средств может увеличиваться риск миопатии, включая рабдомиолиз.
В исследованиях не наблюдалось клинически значимых взаимодействий со следующими лекарствами: зидовудин, зидовудин/ламивудин, триметоприм/сульфаметоксазол, флуконазол, изониазид, кларитромицин, метадон, циметидин, хинидин, норэтистерон/этинилэстрадиолсодержащий контрацептив.
Overdose
Имеется более 60 сообщений об острой или хронической передозировке у человека (в тч при приеме доз до 23 раз превышающих рекомендуемую суточную дозу 2,4 г). В большинстве случаев наблюдались почечные симптомы (нефролитиаз, боль в боку, гематурия) и желудочно-кишечные симптомы (тошнота, рвота, диарея).
Неизвестно, эффективен ли перитонеальный или гемодиализ.
Неизвестно, эффективен ли перитонеальный или гемодиализ.
Method of drug use and dosage
Внутрь, за 1 ч до или через 2 ч после приема пищи с небольшим количеством воды или жидкости (обезжиренное молоко, сок, кофе, чай) или одновременно с приемом легкой пищи (кукурузные хлопья с обезжиренным молоком и сахаром ). Рекомендуемая доза - 2,4 г/сут (по 800 мг каждые 8 ч).
Application precautions
При терапии индинавиром развивается нефролитиаз. В некоторых случаях нефролитиаз сопровождается нарушением функции почек или острой почечной недостаточностью, пиелонефритом с бактериемией или без нее. При появлении признаков или симптомов нефролитиаза, включая боль в боку с гематурией (в тч микрогематурия) или без нее, следует рассмотреть возможность временной приостановки (например, на 1-3 дня) или прекращения терапии. Всем пациентам во время лечения рекомендуется достаточная гидратация (не менее 1,5 л жидкости в сутки).
Во время постмаркетинговых наблюдений у больных, леченных индинавиром, были отмечены редкие случаи интерстициального нефрита с медуллярной кальцификацией и кортикальной атрофией, наблюдавшиеся у пациентов с тяжелой асимптоматической лейкоцитурией (более 100 клеток/поле зрения). Пациенты с тяжелой асимптоматической лейкоцитурией нуждаются в дальнейшем обследовании.
Имеются сообщения о развитии острой гемолитической анемии, в тч с летальным исходом (после подтверждения диагноза следует начать мероприятия по лечению гемолитической анемии, в число которых может входить и отмена препарата).
Сообщалось о случаях развития во время лечения индинавира сульфатом гепатита, сопровождавшегося печеночной недостаточностью и смертью. Однако у большинства этих пациентов имелись и другие заболевания и/или они получали одновременно и другое лечение, поэтому причинная связь между приемом индинавира сульфата и этими явлениями не установлена.
Имеются сообщения, полученные в постмаркетинговых исследованиях, о первичном выявлении сахарного диабета или гипергликемии, а также об обострении имеющегося сахарного диабета у ВИЧ-инфицированных пациентов, получавших лечение ингибиторами протеаз. Некоторым больным для коррекции этих нарушений требовалось назначение или коррекция доз инсулина или пероральных гипогликемических средств. В некоторых случаях развивался диабетический кетоацидоз. У некоторых больных после отмены ингибитора протеазы гипергликемия сохранялась. Частота и причинная связь между этими явлениями и терапией ингибитором протеазы не установлена.
Имеются сообщения о спонтанных кровотечениях у больных гемофилией А и В, получающих лечение ингибиторами протеаз. У некоторых больных потребовалось дополнительное введение фактора VIII. Во многих из этих случаев лечение ингибиторами протеаз было продолжено или возобновлено. Причинная связь между лечением ингибитором протеаз и подобными эпизодами не установлена.
У больных с печеночной недостаточностью, обусловленной циррозом, дозировка должна быть уменьшена в связи со сниженным метаболизмом индинавира сульфата.
При необходимости совместного применения индинавира и диданозина следует принимать их на пустой желудок с интервалом не менее 1 для оптимального всасывания индинавира требуется нормальная (кислая) среда в желудке, а при приеме диданозина pH в желудке повышается.
Во время постмаркетинговых наблюдений у больных, леченных индинавиром, были отмечены редкие случаи интерстициального нефрита с медуллярной кальцификацией и кортикальной атрофией, наблюдавшиеся у пациентов с тяжелой асимптоматической лейкоцитурией (более 100 клеток/поле зрения). Пациенты с тяжелой асимптоматической лейкоцитурией нуждаются в дальнейшем обследовании.
Имеются сообщения о развитии острой гемолитической анемии, в тч с летальным исходом (после подтверждения диагноза следует начать мероприятия по лечению гемолитической анемии, в число которых может входить и отмена препарата).
Сообщалось о случаях развития во время лечения индинавира сульфатом гепатита, сопровождавшегося печеночной недостаточностью и смертью. Однако у большинства этих пациентов имелись и другие заболевания и/или они получали одновременно и другое лечение, поэтому причинная связь между приемом индинавира сульфата и этими явлениями не установлена.
Имеются сообщения, полученные в постмаркетинговых исследованиях, о первичном выявлении сахарного диабета или гипергликемии, а также об обострении имеющегося сахарного диабета у ВИЧ-инфицированных пациентов, получавших лечение ингибиторами протеаз. Некоторым больным для коррекции этих нарушений требовалось назначение или коррекция доз инсулина или пероральных гипогликемических средств. В некоторых случаях развивался диабетический кетоацидоз. У некоторых больных после отмены ингибитора протеазы гипергликемия сохранялась. Частота и причинная связь между этими явлениями и терапией ингибитором протеазы не установлена.
Имеются сообщения о спонтанных кровотечениях у больных гемофилией А и В, получающих лечение ингибиторами протеаз. У некоторых больных потребовалось дополнительное введение фактора VIII. Во многих из этих случаев лечение ингибиторами протеаз было продолжено или возобновлено. Причинная связь между лечением ингибитором протеаз и подобными эпизодами не установлена.
У больных с печеночной недостаточностью, обусловленной циррозом, дозировка должна быть уменьшена в связи со сниженным метаболизмом индинавира сульфата.
При необходимости совместного применения индинавира и диданозина следует принимать их на пустой желудок с интервалом не менее 1 для оптимального всасывания индинавира требуется нормальная (кислая) среда в желудке, а при приеме диданозина pH в желудке повышается.
References
1. Physicians Desk Reference. 57th ed. Thomson PDR. 2003. P. 1970-1976.
2. Physicians Desk Reference. 57th ed. Suppl. A. Thomson PDR. 2003. P. A189.
3. Physicians Desk Reference. 57th ed. Suppl. в. Thomson PDR. 2003. P. в59.
2. Physicians Desk Reference. 57th ed. Suppl. A. Thomson PDR. 2003. P. A189.
3. Physicians Desk Reference. 57th ed. Suppl. в. Thomson PDR. 2003. P. в59.
Included in the composition
- — Crixivan (2 firms)