ICD-10 codes
- ICD-10
- A41 Other sepsis
Description
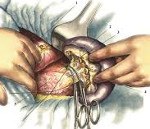
Септицемия постпленэктомии. Септическое состояние, которое возникает после спленэктомии и которое патогенетически связано с операцией. Это проявляется в сверхбыстром развитии гриппоподобного синдрома с последующим резким падением артериального давления, снижением диуреза, судорогами, изменением сознания. Бактериальная диагностика крови, ПЦР, тест на прокальцитонин, рентгенография грудной клетки. Для лечения используются антибиотики, внутривенные иммуноглобулины, прессованные амины, антикоагулянты, антиагреганты, проводится интенсивная детоксикация, инфузионная терапия.
Additional facts
Возникновение сепсиса после спленэктомии (синдром ОРСИ, усугубляемый инфекцией после спленэктомии) является наиболее серьезным инфекционным осложнением, вызванным гипоспленизмом после спленэктомии. Впервые молниеносное септическое состояние у детей, перенесших удаление селезенки, было описано в 1952 году. Сепсис в период после спленэктомии встречается у 0,23-2,4% пациентов, оперированных по поводу черепно-мозговой травмы, и более чем у 20%. при наличии гематологических заболеваний. Патология может быть обнаружена через различные промежутки времени после операции, согласно результатам наблюдений, минимальный из известных периодов составляет 24 дня, а максимальный - 65 лет. Возможно повторное возникновение синдрома ORSI у того же пациента.
Reasons
Септическое расстройство у пациентов, перенесших спленэктомию, вызвано быстрой генерализацией местной инфекции вследствие послеоперационного иммунодефицита. В 50-90% случаев возбудителем сепсиса при синдроме OPSI являются пневмококки, реже заболевание вызывается гемофильным гриппом типа В, менингококками. В отдельных случаях из крови пациентов высеваются кишечная палочка, псевдомонады, стрептококки, стафилококки, сальмонеллы. По мнению специалистов в области инфекционных заболеваний, общей хирургии, гастроэнтерологии, основным фактором, способствующим появлению септического воспаления после спленэктомии, является угнетение различных звеньев иммунной системы:
• Уменьшение количества Т-клеток _ _. Из-за отсутствия антиген-зависимой пролиферации и дифференцировки, которые обычно происходят в тимус-зависимых периартериальных областях селезенки, уровень зрелых эффекторных Т-лимфоцитов (Т-хелперов, Т-киллеров) в крови пациентов снижается. В результате нарушается быстрое удаление клеток, поврежденных бактериями, и уменьшается стимуляция В-лимфоцитов, моноцитов и NK-клеток.
_ Дефицит иммуноглобулинов и комплемента. Одним из проявлений гипоспленизма после спленэктомии, связанным со снижением созревания и стимуляцией В-клеток, является снижение количества IgA, IgE сразу после операции, снижение уровня IgG и IgM в отдаленном периоде. При дефиците антител возникают условия для быстрого развития бактериемии. Ситуация усугубляется снижением уровня общей похвалы, фракции С3-, С4.
• Дефицит туфтсинов. В крови больных с удаленной селезенкой концентрация туфтсина (туфтсина) - тетрапептида опсонина, который синтезируется преимущественно в селезенке, уменьшается в 3 раза, улучшает миграцию и дифференцировку макрофагов, стимулирует их усвояемость. Дефицит туфтсина, при котором наблюдается неполный фагоцитоз, становится предпосылкой развития смертельных инфекций.
• Уменьшение количества Т-клеток _ _. Из-за отсутствия антиген-зависимой пролиферации и дифференцировки, которые обычно происходят в тимус-зависимых периартериальных областях селезенки, уровень зрелых эффекторных Т-лимфоцитов (Т-хелперов, Т-киллеров) в крови пациентов снижается. В результате нарушается быстрое удаление клеток, поврежденных бактериями, и уменьшается стимуляция В-лимфоцитов, моноцитов и NK-клеток.
_ Дефицит иммуноглобулинов и комплемента. Одним из проявлений гипоспленизма после спленэктомии, связанным со снижением созревания и стимуляцией В-клеток, является снижение количества IgA, IgE сразу после операции, снижение уровня IgG и IgM в отдаленном периоде. При дефиците антител возникают условия для быстрого развития бактериемии. Ситуация усугубляется снижением уровня общей похвалы, фракции С3-, С4.
• Дефицит туфтсинов. В крови больных с удаленной селезенкой концентрация туфтсина (туфтсина) - тетрапептида опсонина, который синтезируется преимущественно в селезенке, уменьшается в 3 раза, улучшает миграцию и дифференцировку макрофагов, стимулирует их усвояемость. Дефицит туфтсина, при котором наблюдается неполный фагоцитоз, становится предпосылкой развития смертельных инфекций.
Pathogenesis
Большинство возбудителей сепсиса после спленэктомии характеризуются длительным периодом бессимптомного транспорта: пневмококки высеяны у 5-70% здоровых людей, менингококки у 4-15%, гемофильные палочки типа В - у 4,5-6% Начальная точка заболевания Активация бактерий основана на снижении иммунитета, в частности на снижении уровня типозависимых PGM иммуноглобулинов. Возможна инфекция в воздухе от инфекционного носителя. Первичное поражение обычно образуется в носоглотке, воспаление характеризуется выраженным аллергическим компонентом с недостаточным иммуногистогенным и фагоцитарным макрофагом.
В связи с быстрым накоплением эндотоксинов наблюдается большое количество медиаторов воспаления, массового разрушения тканей, увеличения токсемии, синдрома гиперреактивной системной воспалительной реакции с нарушениями гемодинамики, микроциркуляции и гиперкоагуляции. Проникновение микробов в системный кровоток приводит к их быстрому распространению в организме, оседанию в различных органах с образованием вторичных гнойных очагов, обостряет системные и полиорганные нарушения. Пиемические очаги становятся постоянными источниками вирулентных бактерий, поддерживают состояние патологической реактивности.
В связи с быстрым накоплением эндотоксинов наблюдается большое количество медиаторов воспаления, массового разрушения тканей, увеличения токсемии, синдрома гиперреактивной системной воспалительной реакции с нарушениями гемодинамики, микроциркуляции и гиперкоагуляции. Проникновение микробов в системный кровоток приводит к их быстрому распространению в организме, оседанию в различных органах с образованием вторичных гнойных очагов, обостряет системные и полиорганные нарушения. Пиемические очаги становятся постоянными источниками вирулентных бактерий, поддерживают состояние патологической реактивности.
Symptoms
Клиническая картина заболевания возникает внезапно. У пациента развивается лихорадка, озноб и повышенное потоотделение, сильные головные боли, миалгия, тошнота и рвота, незначительные катаральные симптомы (кашель, боль в горле). При прогрессировании сепсиса наблюдается быстрое нарастание симптомов и ухудшение общего состояния со значительным снижением артериального давления, снижением выделения мочи, нарушением сознания и судорогами. В структуре гнойно-септического состояния постпленэктомии могут появляться симптомы менингита (светобоязнь, неукротимая рвота, ригидность мышц шеи) и пневмонии (боль в груди, одышка, кашель с выделением мокроты, цианоз кожи).
Ассоциированные симптомы: Боль в грудной клетке. Влажный кашель. Истощение. Кашель. Лейкопения. Лейкоцитоз. Одышка. Озноб. Потливость. Рвота. Судороги. Судороги в ногах. Тошнота. Увеличение СОЭ.
Ассоциированные симптомы: Боль в грудной клетке. Влажный кашель. Истощение. Кашель. Лейкопения. Лейкоцитоз. Одышка. Озноб. Потливость. Рвота. Судороги. Судороги в ногах. Тошнота. Увеличение СОЭ.
Possible complications
В рамках септического состояния синдром ДВС-синдрома часто возникает из-за чрезмерного потребления факторов свертывания крови на начальной стадии, что приводит к сильной гипокоагуляции и системному кровотечению. При распространении инфекции абсцессы могут образовываться в мозге, легких и других органах. Наиболее опасным осложнением после спленэктомического сепсиса является развитие синдрома Уотерхауса-Фридрихсена (острая надпочечниковая недостаточность), который проявляется в виде снижения артериального давления вплоть до коллапса, потери сознания и общего цианоза.
Diagnostics
Можно предположить развитие сепсиса после спленэктомии при наличии анамнестической информации об удалении селезенки в сочетании с характерной клинической картиной (короткий продромальный период и быстрое ухудшение состояния пациента). Для проверки диагноза проводится полное обследование. Наиболее информативными с септическим синдромом после спленэктомии являются:
• Бактериологическое посев крови. Сбор венозной крови перед антибактериальной терапией и инокуляция материала, полученного на различных питательных средах, позволяет обнаружить возбудителя сепсиса. Также определяют чувствительность микроорганизмов к антибактериальным препаратам.
Выполнение полимеразной цепной реакции выявляет ДНК патогена в плазме, что служит подтверждением постспленэктомической инфекции крови. Способ характеризуется высокой чувствительностью, специфичностью и быстрыми результатами (в течение 1 дня).
• Тест на прокальцитонин. Определение концентрации прокальцитонина в крови необходимо для оценки степени тяжести осложнений после спленэктомии. Показатель выше 10 нг / мл является неблагоприятным прогнозом и указывает на системный гнойно-септический процесс.
• Рентгенография грудной клетки. Во время рентгенологического исследования в передней и боковой проекциях обнаруживаются признаки пневмонии, которая обычно сочетается с сепсисом. На рентгенографии видно однородное потемнение, занимающее несколько сегментов или долю легкого.
В клиническом анализе крови на сепсис определяются повышенный лейкоцитоз (более 15 г / л) или лейкопения, увеличение СОЭ, уменьшение количества тромбоцитов и эритроцитов. При проведении биохимического анализа крови выявляется снижение концентрации альбумина, повышение уровня общего билирубина и мочевины, снижение концентрации хлоридов. На иммунограмме количество активированных моноцитов составляет менее 30%, что является признаком септического процесса. В общем анализе мочи присутствуют лейкоциты, гиалиновые цилиндры и эритроциты.
Дифференциальный диагноз ставится при сепсисе различной этиологии, анафилактическом шоке, малярии, системной красной волчанке, лимфоме Ходжкина, системном васкулите, внутрибольничной инфекции, гнойно-резорбтивной лихорадке, туберкулезе. Помимо специалиста по инфекционным заболеваниям пациент нуждается в консультациях у хирурга, гастроэнтеролога, пульмонолога, гематолога, иммунолога.
• Бактериологическое посев крови. Сбор венозной крови перед антибактериальной терапией и инокуляция материала, полученного на различных питательных средах, позволяет обнаружить возбудителя сепсиса. Также определяют чувствительность микроорганизмов к антибактериальным препаратам.
Выполнение полимеразной цепной реакции выявляет ДНК патогена в плазме, что служит подтверждением постспленэктомической инфекции крови. Способ характеризуется высокой чувствительностью, специфичностью и быстрыми результатами (в течение 1 дня).
• Тест на прокальцитонин. Определение концентрации прокальцитонина в крови необходимо для оценки степени тяжести осложнений после спленэктомии. Показатель выше 10 нг / мл является неблагоприятным прогнозом и указывает на системный гнойно-септический процесс.
• Рентгенография грудной клетки. Во время рентгенологического исследования в передней и боковой проекциях обнаруживаются признаки пневмонии, которая обычно сочетается с сепсисом. На рентгенографии видно однородное потемнение, занимающее несколько сегментов или долю легкого.
В клиническом анализе крови на сепсис определяются повышенный лейкоцитоз (более 15 г / л) или лейкопения, увеличение СОЭ, уменьшение количества тромбоцитов и эритроцитов. При проведении биохимического анализа крови выявляется снижение концентрации альбумина, повышение уровня общего билирубина и мочевины, снижение концентрации хлоридов. На иммунограмме количество активированных моноцитов составляет менее 30%, что является признаком септического процесса. В общем анализе мочи присутствуют лейкоциты, гиалиновые цилиндры и эритроциты.
Дифференциальный диагноз ставится при сепсисе различной этиологии, анафилактическом шоке, малярии, системной красной волчанке, лимфоме Ходжкина, системном васкулите, внутрибольничной инфекции, гнойно-резорбтивной лихорадке, туберкулезе. Помимо специалиста по инфекционным заболеваниям пациент нуждается в консультациях у хирурга, гастроэнтеролога, пульмонолога, гематолога, иммунолога.
Treatment
Синдром характеризуется высокой терапевтической устойчивостью. Пациентам рекомендуется комбинированная терапия для борьбы с инфекционным агентом и коррекции последствий гиперреактивной реакции. Основу лечебного режима составляют препараты, которые непосредственно воздействуют на возбудителя сепсиса:
• Антибактериальные препараты. Как правило, базовая терапия включает цефалоспорины 2-3 поколения в сочетании с аминогликозидами. Учитывая чувствительность микрофлоры, лечение дополняют фторхинолоны последних поколений, парентеральные карбапенемы, полусинтетические уреидопенициллины, ингибиторы β-лактамазы.
• Внутривенные иммуноглобулины (IVIG). Эффективность пассивной иммунизации при пост-спленэктомическом варианте сепсиса остается сомнительным предметом. Однако, согласно наблюдениям, введение больших и повторных доз готовых антител положительно влияет на устранение микробной флоры и улучшает общее состояние пациента.
Во избежание общего отравления назначают инфузии плазмозаменителей, форсированный диурез, гемосорбцию, плазмаферез и гемодиализ. Кортикостероиды используются в противовоспалительных целях. При значительном падении артериального давления рекомендуются прессорамины. Учитывая тяжесть метаболических и энергетических нарушений, активную инфузионную терапию проводят с инфузией коллоидных, кристаллоидных растворов, белковых и жировых эмульсий. В случае нарушений гемостаза указываются ингибиторы агрегации тромбоцитов, прямые и непрямые антикоагулянты, переливания свежезамороженной плазмы и массы тромбоцитов. Хирургическое лечение используется только в формировании обширных вторичных пемических очагов, которые поддерживают интоксикацию и гиперреактивность.
• Антибактериальные препараты. Как правило, базовая терапия включает цефалоспорины 2-3 поколения в сочетании с аминогликозидами. Учитывая чувствительность микрофлоры, лечение дополняют фторхинолоны последних поколений, парентеральные карбапенемы, полусинтетические уреидопенициллины, ингибиторы β-лактамазы.
• Внутривенные иммуноглобулины (IVIG). Эффективность пассивной иммунизации при пост-спленэктомическом варианте сепсиса остается сомнительным предметом. Однако, согласно наблюдениям, введение больших и повторных доз готовых антител положительно влияет на устранение микробной флоры и улучшает общее состояние пациента.
Во избежание общего отравления назначают инфузии плазмозаменителей, форсированный диурез, гемосорбцию, плазмаферез и гемодиализ. Кортикостероиды используются в противовоспалительных целях. При значительном падении артериального давления рекомендуются прессорамины. Учитывая тяжесть метаболических и энергетических нарушений, активную инфузионную терапию проводят с инфузией коллоидных, кристаллоидных растворов, белковых и жировых эмульсий. В случае нарушений гемостаза указываются ингибиторы агрегации тромбоцитов, прямые и непрямые антикоагулянты, переливания свежезамороженной плазмы и массы тромбоцитов. Хирургическое лечение используется только в формировании обширных вторичных пемических очагов, которые поддерживают интоксикацию и гиперреактивность.
References
1. Постспленэктомический сепсис/ Шапкин Ю.Г. Масляков В.В. Чалык Ю.В. Вестник хирургии - 2009 - Т.168, №5.
2. Многофункциональное обоснование операций на гастроспленопанкреатическом комплексе и профилактика осложнений при вынужденной спленэктомии: диссертация/ Алексеев В.С. 2016.
3. Диагностика и лечение закрытых повреждений селезенки у детей/ Катько В.А., Аверин В.И., Свирский А.А. 2009.
2. Многофункциональное обоснование операций на гастроспленопанкреатическом комплексе и профилактика осложнений при вынужденной спленэктомии: диссертация/ Алексеев В.С. 2016.
3. Диагностика и лечение закрытых повреждений селезенки у детей/ Катько В.А., Аверин В.И., Свирский А.А. 2009.