МКБ-10 коды
|
|
Вступление
Кодирование по Международной статистической классификации болезней и проблем, связанных со здоровьем: D68.2.
Год утверждения (частота пересмотра): 2023.
Возрастная категория: Взрослые , Дети.
Пересмотр не позднее: 2025.
ID: 149.
Разработчик клинической рекомендации.
• Национальное общество детских гематологов, онкологов.
• Национальное гематологическое общество.
Одобрено Научно-практическим Советом Минздрава РФ.
Год утверждения (частота пересмотра): 2023.
Возрастная категория: Взрослые , Дети.
Пересмотр не позднее: 2025.
ID: 149.
Разработчик клинической рекомендации.
• Национальное общество детских гематологов, онкологов.
• Национальное гематологическое общество.
Одобрено Научно-практическим Советом Минздрава РФ.
|
|
 Список сокращений
Список сокращений
АЧТВ - активированное частичное тромбопластиновое время.
АИКК - антиингибиторный коагулянтный комплекс.
ВК - время кровотечения.
ЖКТ - желудочно-кишечный тракт.
КПК - концентраты протромбинового комплекса - отдельные препараты из группы в02BD по АТХ классификации): факторы свертывания крови II, VII, IX и X в комбинации [протромбиновый комплекс]** и факторы свертывания крови II, IX и X в комбинации** (вне зарегистрированных показаний для детей - эффективность и безопасность недостаточно изучены).
НПВП - нестероидные противовоспалительные и противоревматические препараты.
ПВ - протромбиновое время.
РНСК - редкие нарушения свертывания крови.
СЗП - свежезамороженная плазма.
ТФ - тканевой фактор.
ТВ - тромбиновое время.
ЦНС - центральная нервная система.
FII - фактор свертывания крови II.
FVII - фактор свертывания крови VII.
FVIII - фак тор свертывания крови VIII.
FIX - фактор свертывания крови IX.
FX - фактор свертывания крови X.
ISTH - Международное Общество по Тромбозу и Гемостазу.
RFVIIа - эптакок альфа (активированный)** (фактор свертывания крови VIIа).
АИКК - антиингибиторный коагулянтный комплекс.
ВК - время кровотечения.
ЖКТ - желудочно-кишечный тракт.
КПК - концентраты протромбинового комплекса - отдельные препараты из группы в02BD по АТХ классификации): факторы свертывания крови II, VII, IX и X в комбинации [протромбиновый комплекс]** и факторы свертывания крови II, IX и X в комбинации** (вне зарегистрированных показаний для детей - эффективность и безопасность недостаточно изучены).
НПВП - нестероидные противовоспалительные и противоревматические препараты.
ПВ - протромбиновое время.
РНСК - редкие нарушения свертывания крови.
СЗП - свежезамороженная плазма.
ТФ - тканевой фактор.
ТВ - тромбиновое время.
ЦНС - центральная нервная система.
FII - фактор свертывания крови II.
FVII - фактор свертывания крови VII.
FVIII - фак тор свертывания крови VIII.
FIX - фактор свертывания крови IX.
FX - фактор свертывания крови X.
ISTH - Международное Общество по Тромбозу и Гемостазу.
RFVIIа - эптакок альфа (активированный)** (фактор свертывания крови VIIа).
Термины и определения
Болезнь Стюарта-Прауэра. Дефицит фактора свертывания крови Х.
Гемартроз. Кровоизлияние в полость сустава.
Гематома. Ограниченное скопление крови при закрытых и открытых повреждениях органов и тканей с разрывом сосудов, в результате чего образуется полость, содержащая жидкую или свернувшуюся кровь.
Гематурия. Наличие эритроцитов в моче сверх физиологических норм.
Гемостатическая терапия. Терапия, направленная на остановку кровотечения.
Гипопроконвертинемия. Дефицит фактора свертывания крови VII.
Гипопротромбинемия. Дефицит фактора свертывания крови II.
Диспротромбинемия. Функциональная недостаточность фактора свертывания крови II.
Коагулопатия. Нарушение в свертывающей системе крови.
Фактор свертывания крови. Белок, содержащийся в плазме крови и тромбоцитах, участвующий в свёртывании крови.
Гемартроз. Кровоизлияние в полость сустава.
Гематома. Ограниченное скопление крови при закрытых и открытых повреждениях органов и тканей с разрывом сосудов, в результате чего образуется полость, содержащая жидкую или свернувшуюся кровь.
Гематурия. Наличие эритроцитов в моче сверх физиологических норм.
Гемостатическая терапия. Терапия, направленная на остановку кровотечения.
Гипопроконвертинемия. Дефицит фактора свертывания крови VII.
Гипопротромбинемия. Дефицит фактора свертывания крови II.
Диспротромбинемия. Функциональная недостаточность фактора свертывания крови II.
Коагулопатия. Нарушение в свертывающей системе крови.
Фактор свертывания крови. Белок, содержащийся в плазме крови и тромбоцитах, участвующий в свёртывании крови.
Описание
Наследственный дефицит фактора свертывания крови II (гипопротромбинемия). Геморрагическое заболевание, характеризующееся снижением активности протромбина в плазме, возникающим вследствие генетических дефектов, обуславливающих количественные (гипопротромбинемия) или качественные (диспротромбинемия) нарушения фактора свертывания крови II (FII).
Наследственный дефицит фактора свертывания крови VII (гипопроконвертинемия). Геморрагическое заболевание, возникающее вследствие генетически обусловленного снижения активности фактора свертывания крови VII (FVII) в плазме.
Наследственный дефицит фактора свертывания крови Х. Геморрагическое заболевание, возникающее вследствие генетически обусловленного количественного или качественного дефекта FX, приводящего к снижению активности FХ в плазме [1].
Наследственный дефицит фактора свертывания крови VII (гипопроконвертинемия). Геморрагическое заболевание, возникающее вследствие генетически обусловленного снижения активности фактора свертывания крови VII (FVII) в плазме.
Наследственный дефицит фактора свертывания крови Х. Геморрагическое заболевание, возникающее вследствие генетически обусловленного количественного или качественного дефекта FX, приводящего к снижению активности FХ в плазме [1].
Причины
К редким нарушениям свертывания крови (РНСК) относят моногенные коагулопатии, вызванные дефицитом плазменных белков, участвующих в гемостазе, не относящиеся к болезни Виллебранда и гемофилии А или В. РНСК включают наследственные дефициты или аномалии фибриногена, протромбина (фактора II), факторов свертывания крови V, VII, X, XI, XII, XIII. Все эти нарушения в подавляющем большинстве случаев приводят к нарушениям формирования фибрина [2].
Причинами развития РНСК являются, как правило, рецессивное наследование уникального нарушения или редких нуклеотидных изменений в генах, кодирующих коагуляционные факторы, или в белках, необходимых для посттрансляционных модификаций данных факторов. РНСК наиболее распространены в этнических группах, в которых приняты близкородственные браки, вследствие большей вероятности гомозиготного носительства дефекта гена.
Опубликованные описания РНСК до недавнего времени исторически состояли из исследований случай-контроль или малочисленных когортных исследований. Однако, в течение последних 10 лет появилось несколько специфических регистров [2-7], позволивших улучшить понимание РНСК. Создание международной базы РНСК способствовало определению четких лабораторных критериев тяжести большинства РНСК, которые были разработаны под эгидой Международного Общества по Тромбозу и Гемостазу (ISTH) в 2012 году.
Наследственный дефицит фактора свертывания крови II (протромбина). Аутосомно-рецессивное заболевание. Характеристика: FII - гликопротеид, образуется в печени в присутствии витамина Под влиянием активированного фактора свертывания крови X (FXа) в инициирующей фазе коагуляционного каскада и протромбиназного комплекса (фаза амплификации) переходит в тромбин. Тромбин, в свою очередь, активирует другие плазменные белки свертывания крови и тромбоциты с конечным формированием фибринового сгустка. Кроме того, тромбин участвует в активации ингибиторов свертывания крови и в регуляции фибринолиза.
Дефицит FII обусловлен вариациями в F2 гене, который кодирует протромбин. Не существует прямой корреляции между F2 генотипом и фенотипом заболевания. Гемостатически достаточный уровень FII составляет около 40%. Период полувыведения FII - около 60 часов.
Наследственный дефицит фактора свертывания крови VII. Аутосомно-рецессивное заболевание. Физиологическая роль FVII заключается в инициации процесса свертывания крови в зоне повреждения сосудистой стенки. В комплексе с тканевым фактором (ТФ), FVIIа активирует FX и FIX, участвующих в генерации тромбина.
Период полувыведения FVII составляет 4-6 часов. Достаточный гемостатический уровень - не менее 10%. При тяжелых травмах клинически значимое кровотечение может развиться при активности FVII более 20%.
Наследственный дефицит фактора свертывания крови Х. Аутосомно-рецессивное заболевание. Активация FX происходит в инициирующей фазе свертывания крови при участии комплекса ТФ-FVIIa и в фазе амплификации c теназным комплексом. Активированный FX (FXa) и его кофактор, фактор свертывания крови V (FV), входят в состав протромбиназного комплекса, который активирует протромбин.
Период полувыведения FX составляет 30-50 часов. Достаточный гемостатический уровень: кровотечения не наблюдаются у лиц с активностью FХ>40% [8].
Причинами развития РНСК являются, как правило, рецессивное наследование уникального нарушения или редких нуклеотидных изменений в генах, кодирующих коагуляционные факторы, или в белках, необходимых для посттрансляционных модификаций данных факторов. РНСК наиболее распространены в этнических группах, в которых приняты близкородственные браки, вследствие большей вероятности гомозиготного носительства дефекта гена.
Опубликованные описания РНСК до недавнего времени исторически состояли из исследований случай-контроль или малочисленных когортных исследований. Однако, в течение последних 10 лет появилось несколько специфических регистров [2-7], позволивших улучшить понимание РНСК. Создание международной базы РНСК способствовало определению четких лабораторных критериев тяжести большинства РНСК, которые были разработаны под эгидой Международного Общества по Тромбозу и Гемостазу (ISTH) в 2012 году.
Наследственный дефицит фактора свертывания крови II (протромбина). Аутосомно-рецессивное заболевание. Характеристика: FII - гликопротеид, образуется в печени в присутствии витамина Под влиянием активированного фактора свертывания крови X (FXа) в инициирующей фазе коагуляционного каскада и протромбиназного комплекса (фаза амплификации) переходит в тромбин. Тромбин, в свою очередь, активирует другие плазменные белки свертывания крови и тромбоциты с конечным формированием фибринового сгустка. Кроме того, тромбин участвует в активации ингибиторов свертывания крови и в регуляции фибринолиза.
Дефицит FII обусловлен вариациями в F2 гене, который кодирует протромбин. Не существует прямой корреляции между F2 генотипом и фенотипом заболевания. Гемостатически достаточный уровень FII составляет около 40%. Период полувыведения FII - около 60 часов.
Наследственный дефицит фактора свертывания крови VII. Аутосомно-рецессивное заболевание. Физиологическая роль FVII заключается в инициации процесса свертывания крови в зоне повреждения сосудистой стенки. В комплексе с тканевым фактором (ТФ), FVIIа активирует FX и FIX, участвующих в генерации тромбина.
Период полувыведения FVII составляет 4-6 часов. Достаточный гемостатический уровень - не менее 10%. При тяжелых травмах клинически значимое кровотечение может развиться при активности FVII более 20%.
Наследственный дефицит фактора свертывания крови Х. Аутосомно-рецессивное заболевание. Активация FX происходит в инициирующей фазе свертывания крови при участии комплекса ТФ-FVIIa и в фазе амплификации c теназным комплексом. Активированный FX (FXa) и его кофактор, фактор свертывания крови V (FV), входят в состав протромбиназного комплекса, который активирует протромбин.
Период полувыведения FX составляет 30-50 часов. Достаточный гемостатический уровень: кровотечения не наблюдаются у лиц с активностью FХ>40% [8].
|
|
Эпидемиология
Распространенность наследственного дефицита фактора свертывания крови II (протромбина) в большинстве стран составляет 1:2 000 000 населения.
Распространенность гипопроконвертинемии - 1:300 000 - 500 000 населения.
Средняя распространенность спорадических форм наследственного дефицита фактора свертывания крови Х составляет 1:1 000 000 населения [1].
Распространенность гипопроконвертинемии - 1:300 000 - 500 000 населения.
Средняя распространенность спорадических форм наследственного дефицита фактора свертывания крови Х составляет 1:1 000 000 населения [1].
1,4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем.
D68,2. Наследственный дефицит других факторов свертывания крови.Классификация
1,5 Классификация заболевания или состояния (группы заболеваний или состояний).
Существует 3 формы тяжести РНСК в зависимости от активности FII, FVII, FX, определяемой лабораторно (табл.1) [9].Таблица 1. Формы РНСК по степени тяжести.
| тяжелая | средней тяжести | легкая | |
| FII | не определяется | ≤ 10% | > 10% |
| FVII | < 10% | 10-20% | better 20% |
| FX | < 10% | 10-40% | > 40% |
Тяжелый дефицит факторов, как правило, связан с развитием тяжелых спонтанных кровотечений/кровоизлияний.
Умеренный дефицит факторов проявляется в виде легких/умеренных спонтанных и посттравматических эпизодов кровотечений.
Легкие формы дефицита факторов в большинстве случаев протекают бессимптомно.
Клиническая картина
Типичными для РНСК являются кровотечения/кровоизлияния, возникающие спонтанно или вследствие травмы. Геморрагический синдром представлен кровотечениями из слизистых (носовые, десневые, луночковые), экхимозами, гематомами мягких тканей различной локализации, кровотечениями во время и после хирургических вмешательств, меноррагиями, гематуриями, реже - кровоизлияниями в суставы (гемартрозами). Кроме того, при значительных дефицитах факторов у пациентов отмечаются жизнеугрожающие кровотечения, к которым относятся [8,10,11]:
• кровотечения/кровоизлияния в ЦНС;
• кровотечения/кровоизлияния в ЖКТ;
• кровотечения/кровоизлияния в шею/горло;
• забрюшинная гематома.
При гипопротромбинемии с активностью FII worse 10%, как правило, отмечаются более тяжелые кровотечения по сравнению с кровотечениями, возникающими при активности FII ≥ 10%. В последнем случае наиболее типичны легкие и умеренные кровотечения из слизистых оболочек. Пациенты с активностью FII менее 4% не описаны.
Для диспротромбинемии характерна слабая взаимосвязь между клиническим и лабораторным фенотипами заболевания. У гетерозиготных носителей дефицита FII в большинстве случаев определяется активность FII в пределах 40-75% с асимптомным течением заболевания.
При гипопроконвертинемии приблизительно в 60% случаев течение заболевания бессимптомное, и поводом для диагностики является случайное обнаружение увеличения ПВ. Кровоизлияния в ЦНС регистрируются у 3-10% пациентов с дефицитом FVII.
Тяжелые кровотечения наиболее характерны при активности FVII ≤ 1%. У пациентов с активностью FVII better 1% отмечаются, как правило, умеренные и легкие кровотечения из слизистых оболочек или бессимптомное течение заболевания. Однако в ряде случаев регистрируются тяжелые проявления геморрагического синдрома у лиц с активностью FVII better 20%, что говорит об отсутствии прямой корреляции между клиническим и лабораторным фенотипом заболевания.
У гетерозиготных носителей дефицита FVII в большинстве случаев определяется активность FVII в пределах 40-60% с бессимптомным течением заболевания.
При дефиците FX тяжелые кровотечения наиболее характерны для пациентов с активностью FX ≤ 10%. У пациентов с активностью FX better 10%, как правило, отмечаются умеренные и легкие кровотечения из слизистых оболочек, кровотечения после хирургических вмешательств или бессимптомное течение заболевания. Кровоизлияния в ЦНС, кровотечения из слизистых ЖКТ, гемартрозы отмечаются у пациентов с активностью FX ≤ 2%. Тем не менее, в ряде случаев регистрируются тяжелые проявления геморрагического синдрома у лиц с активностью FX 0,1 - 39%, указывая, таким образом, на отсутствие прямой корреляции между клиническим и лабораторным фенотипом заболевания.
У гетерозиготных носителей дефицита FX в большинстве случаев активность FX составляет около 50%, заболевание имеет бессимптомное течение [8].
• кровотечения/кровоизлияния в ЦНС;
• кровотечения/кровоизлияния в ЖКТ;
• кровотечения/кровоизлияния в шею/горло;
• забрюшинная гематома.
При гипопротромбинемии с активностью FII worse 10%, как правило, отмечаются более тяжелые кровотечения по сравнению с кровотечениями, возникающими при активности FII ≥ 10%. В последнем случае наиболее типичны легкие и умеренные кровотечения из слизистых оболочек. Пациенты с активностью FII менее 4% не описаны.
Для диспротромбинемии характерна слабая взаимосвязь между клиническим и лабораторным фенотипами заболевания. У гетерозиготных носителей дефицита FII в большинстве случаев определяется активность FII в пределах 40-75% с асимптомным течением заболевания.
При гипопроконвертинемии приблизительно в 60% случаев течение заболевания бессимптомное, и поводом для диагностики является случайное обнаружение увеличения ПВ. Кровоизлияния в ЦНС регистрируются у 3-10% пациентов с дефицитом FVII.
Тяжелые кровотечения наиболее характерны при активности FVII ≤ 1%. У пациентов с активностью FVII better 1% отмечаются, как правило, умеренные и легкие кровотечения из слизистых оболочек или бессимптомное течение заболевания. Однако в ряде случаев регистрируются тяжелые проявления геморрагического синдрома у лиц с активностью FVII better 20%, что говорит об отсутствии прямой корреляции между клиническим и лабораторным фенотипом заболевания.
У гетерозиготных носителей дефицита FVII в большинстве случаев определяется активность FVII в пределах 40-60% с бессимптомным течением заболевания.
При дефиците FX тяжелые кровотечения наиболее характерны для пациентов с активностью FX ≤ 10%. У пациентов с активностью FX better 10%, как правило, отмечаются умеренные и легкие кровотечения из слизистых оболочек, кровотечения после хирургических вмешательств или бессимптомное течение заболевания. Кровоизлияния в ЦНС, кровотечения из слизистых ЖКТ, гемартрозы отмечаются у пациентов с активностью FX ≤ 2%. Тем не менее, в ряде случаев регистрируются тяжелые проявления геморрагического синдрома у лиц с активностью FX 0,1 - 39%, указывая, таким образом, на отсутствие прямой корреляции между клиническим и лабораторным фенотипом заболевания.
У гетерозиготных носителей дефицита FX в большинстве случаев активность FX составляет около 50%, заболевание имеет бессимптомное течение [8].
Диагностика
Критерии установления диагноза/состояния. При установке диагноза РНСК необходимо использовать следующие критерии, независимо от наличия геморрагического синдрома в персональном или семейном анамнезе [8,9,12-16]:
1. отсутствие данных о наличии приобретенного дефицита факторов свертывания крови;
2. снижение активности FII/FVII/FX ниже референсных значений;
3. наличие мутаций генов FII, FVII, FX.
Диагноз наследственного РНСК устанавливается при наличии не менее двух из трех вышеперечисленных критериев.
• Рекомендуется при сборе анамнеза заболевания и семейного анамнеза выяснять у всех пациентов наличие проявлений геморрагического синдрома: жалоб на легко появляющиеся экхимозы и гематомы в раннем детстве; возникновение спонтанных кровотечений (в том числе гематом различных локализаций); длительных кровотечений после травм или хирургического вмешательства [8,11,13,17].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии. Примерно у 2/3 больных нет указаний на геморрагические проявления у близких родственников. Данные личного анамнеза могут содержать информацию о геморрагических проявлениях у пациента. При сборе анамнеза заболевания необходимо обращать внимание на наличие геморрагических проявлений в неонатальном периоде в виде кефалогематом, внутричерепных кровоизлияний, кровоточивости и длительном заживлении пупочной ранки; у грудных детей - экхимозов, не связанных со значимой травмой, гематом мягких тканей после незначительных ушибов или спонтанных. Важно обращать внимание на несоответствие выраженности геморрагических проявлений тяжести предшествовавшей травмы, на рецидивы кровотечений после первичной остановки, не связанные с повторной травмой, массивные и/или множественные гематомы, системность геморрагических проявлений (проявления различной локализации). У лиц, с незначительными дефицитами факторов свертывания крови кровотечения могут отсутствовать до первой травмы или хирургического вмешательства. Сбор жалоб и анамнеза позволит определить объем обследования пациента.
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии. Выявление признаков поражения суставов - маловероятно.
• Рекомендуется всем пациентам, у которых подозреваются геморрагические состояния, выполнение общего анализа крови, в том числе исследование уровня тромбоцитов в крови, с целью уточнения общего состояния пациента, тяжести геморрагических осложнений и состояния свертывающей системы [4,5,7,10,13,19,20].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
• Рекомендуется всем пациентам, у которых подозреваются геморрагические состояния, на первом этапе выполнение коагулограммы (ориентировочного исследования системы гемостаза), включающей проведение коагулологического скрининга, включающего определение активированного частичного тромбопластинового времени (АЧТВ), протромбинового времени (ПВ), тромбинового времени (ТВ), концентрации фибриногена (по Клауссу), времени кровотечения (ВК) стандартизованным методом и подсчет количества тромбоцитов по Фонио [4,5,7,10,13,19,20].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
Комментарии. Показатели скрининговых тестов для дефицита FII, FVII, FX представлены в таблице 2.
Таблица 2. Скрининговые коагулологические тесты для диагностики РНСК.
При любом удлинении ПВ должны быть исключены все виды приобретенного дефицита факторов протромбинового комплекса, в первую очередь обусловленные тяжелой патологией печени, механической желтухой, токсическим действием антикоагулянтов непрямого действия, эндогенным К-гиповитаминозом.
Следует иметь в виду возможность наличия приобретенного дефицита FII при антифосфолипидном синдроме с выработкой антител к протромбину и другим белкам в крови, который отличается от наследственного дефицита FII по клиническому течению и присутствию антифосфолипидных антител, при болезнях печени и желчевыводящих путей, при дефиците витамина а также при приеме антагонистов витамина Изолированный приобретенный дефицит FVII, как правило, обусловлен иммунными нарушениями, может наблюдаться при системном амилоидозе и нефротическом синдроме. Приобретенный дефицит FX может встречаться в 9 - 14% случаев при системном амилоидозе, после тяжелых инфекций, у онкологических больных.
• Рекомендуется всем пациентам с выявленными на первом этапе нарушениями гемостаза (увеличение АЧТВ и/или ПВ, нормальные ТВ и уровень фибриногена) вторым этапом диагностики с целью выявления дефектного звена гемостаза выполнять определение активности фактора II в сыворотке крови, определение активности фактора V в сыворотке крови, определение активности фактора VII в сыворотке крови, определение активности фактора VIII в сыворотке крови, определение активности фактора IX в сыворотке крови, определение активности фактора X в сыворотке крови, тест на волчаночный антикоагулянт. При удлинении ВК - анализ функции тромбоцитов и исследование активности и свойств фактора Виллебранда в крови [4,5,7,10,13,19-21].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии. Диагноз РИСК считается установленным при выявлении изолированного снижения активности соответствующих факторов - FII, FVII или FX.
• Рекомендуется проведение молекулярно-генетической диагностики нарушений FII, FVII, FX при выявлении снижения их активности в плазме пациента с целью подтверждения врожденной коагулопатии [12,13,15,16].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 4).
Комментарии. Для исключения приобретенных дефицитов FII, FVII, FX.
• эзофагогастродуоденоскопия,.
• ультразвуковое исследование сустава,.
• ультразвуковое исследование органов брюшной полости,.
• ультразвуковое исследование мочевыводящих путей,.
• ультразвуковое исследование органов малого таза,.
• ультразвуковое исследование забрюшинного пространства,.
• магнитно-резонансная томография сустава, мягких тканей,.
• магнитно-резонансная томография головного мозга,.
• рентгенография сустава,.
• компьютерная томография органов грудной клетки,.
• компьютерная томография головного мозга,.
• риноскопия эндоскопическая,.
• ректороманоскопия,.
• кольпоскопия,.
• гистероскопия,.
• колоноскопия.
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 3).
Комментарии. Исследования позволяют визуализировать кровотечения/кровоизлияния различных локализаций, а также выявить осложнения, развившиеся вследствие геморрагических проявлений.
• врача-травматолога-ортопеда,.
• врача-хирурга,.
• врача-уролога,.
• врача-невролога,.
• врача-оториноларинголога,.
• врача-стоматолога,.
• врача-акушера-гинеколога.
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии. Позволяют определить нарушения различных органов и систем вследствие состоявшегося (перенесенного ранее) кровотечения/кровоизлияния.
• Рекомендуется пациентам с РНСК в случае невозможности проведения полноценного двухэтапного коагулологического исследования, а также в некоторых случаях для контроля за проводимой терапией выполнять интегральные тесты оценки гемостаза: тромбодинамика, тромбоэластография, тест генерации тромбина, с целью выявления и мониторинга нарушений свертывающей системы крови [26].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
1. отсутствие данных о наличии приобретенного дефицита факторов свертывания крови;
2. снижение активности FII/FVII/FX ниже референсных значений;
3. наличие мутаций генов FII, FVII, FX.
Диагноз наследственного РНСК устанавливается при наличии не менее двух из трех вышеперечисленных критериев.
2,1 Жалобы и анамнез.
Диагностика РНСК начинается с выявления клиники геморрагического состояния, либо (при отсутствии признаков избыточной кровоточивости) выяснения наличия семейного анамнеза нарушений свертывания крови.• Рекомендуется при сборе анамнеза заболевания и семейного анамнеза выяснять у всех пациентов наличие проявлений геморрагического синдрома: жалоб на легко появляющиеся экхимозы и гематомы в раннем детстве; возникновение спонтанных кровотечений (в том числе гематом различных локализаций); длительных кровотечений после травм или хирургического вмешательства [8,11,13,17].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии. Примерно у 2/3 больных нет указаний на геморрагические проявления у близких родственников. Данные личного анамнеза могут содержать информацию о геморрагических проявлениях у пациента. При сборе анамнеза заболевания необходимо обращать внимание на наличие геморрагических проявлений в неонатальном периоде в виде кефалогематом, внутричерепных кровоизлияний, кровоточивости и длительном заживлении пупочной ранки; у грудных детей - экхимозов, не связанных со значимой травмой, гематом мягких тканей после незначительных ушибов или спонтанных. Важно обращать внимание на несоответствие выраженности геморрагических проявлений тяжести предшествовавшей травмы, на рецидивы кровотечений после первичной остановки, не связанные с повторной травмой, массивные и/или множественные гематомы, системность геморрагических проявлений (проявления различной локализации). У лиц, с незначительными дефицитами факторов свертывания крови кровотечения могут отсутствовать до первой травмы или хирургического вмешательства. Сбор жалоб и анамнеза позволит определить объем обследования пациента.
2,2 Физикальное обследование.
• Рекомендуется у всех пациентов обращать внимание на наличие кожного геморрагического синдрома различной выраженности в виде множественных экхимозов и гематом при значительном снижении активности факторов свертывания крови. Физикальное обследование позволяет определить тяжесть состояния пациента и необходимость проведения гемостатической терапии [1,8].Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии. Выявление признаков поражения суставов - маловероятно.
2,3 Лабораторные диагностические исследования.
Для диагностики РНСК проводятся поэтапные лабораторные исследования - коагулологический скрининг, определение активности факторов и молекулярно-генетическая диагностика [10,13,14,17,18]. Получение максимального количества данных способствует верификации диагноза и исключению приобретенных дефицитов факторов свертывания крови II, VII, X, а также исключению дефицитов других факторов свертывания крови.• Рекомендуется всем пациентам, у которых подозреваются геморрагические состояния, выполнение общего анализа крови, в том числе исследование уровня тромбоцитов в крови, с целью уточнения общего состояния пациента, тяжести геморрагических осложнений и состояния свертывающей системы [4,5,7,10,13,19,20].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
• Рекомендуется всем пациентам, у которых подозреваются геморрагические состояния, на первом этапе выполнение коагулограммы (ориентировочного исследования системы гемостаза), включающей проведение коагулологического скрининга, включающего определение активированного частичного тромбопластинового времени (АЧТВ), протромбинового времени (ПВ), тромбинового времени (ТВ), концентрации фибриногена (по Клауссу), времени кровотечения (ВК) стандартизованным методом и подсчет количества тромбоцитов по Фонио [4,5,7,10,13,19,20].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
Комментарии. Показатели скрининговых тестов для дефицита FII, FVII, FX представлены в таблице 2.
Таблица 2. Скрининговые коагулологические тесты для диагностики РНСК.
| АЧТВ | Увеличение | Норма | Увеличение |
| ПВ | Увеличение | Увеличение | Увеличение |
| ТВ | Норма | Норма | Норма |
| Уровень фибриногена | Норма | Норма | Норма |
При любом удлинении ПВ должны быть исключены все виды приобретенного дефицита факторов протромбинового комплекса, в первую очередь обусловленные тяжелой патологией печени, механической желтухой, токсическим действием антикоагулянтов непрямого действия, эндогенным К-гиповитаминозом.
Следует иметь в виду возможность наличия приобретенного дефицита FII при антифосфолипидном синдроме с выработкой антител к протромбину и другим белкам в крови, который отличается от наследственного дефицита FII по клиническому течению и присутствию антифосфолипидных антител, при болезнях печени и желчевыводящих путей, при дефиците витамина а также при приеме антагонистов витамина Изолированный приобретенный дефицит FVII, как правило, обусловлен иммунными нарушениями, может наблюдаться при системном амилоидозе и нефротическом синдроме. Приобретенный дефицит FX может встречаться в 9 - 14% случаев при системном амилоидозе, после тяжелых инфекций, у онкологических больных.
• Рекомендуется всем пациентам с выявленными на первом этапе нарушениями гемостаза (увеличение АЧТВ и/или ПВ, нормальные ТВ и уровень фибриногена) вторым этапом диагностики с целью выявления дефектного звена гемостаза выполнять определение активности фактора II в сыворотке крови, определение активности фактора V в сыворотке крови, определение активности фактора VII в сыворотке крови, определение активности фактора VIII в сыворотке крови, определение активности фактора IX в сыворотке крови, определение активности фактора X в сыворотке крови, тест на волчаночный антикоагулянт. При удлинении ВК - анализ функции тромбоцитов и исследование активности и свойств фактора Виллебранда в крови [4,5,7,10,13,19-21].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии. Диагноз РИСК считается установленным при выявлении изолированного снижения активности соответствующих факторов - FII, FVII или FX.
• Рекомендуется проведение молекулярно-генетической диагностики нарушений FII, FVII, FX при выявлении снижения их активности в плазме пациента с целью подтверждения врожденной коагулопатии [12,13,15,16].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 4).
Комментарии. Для исключения приобретенных дефицитов FII, FVII, FX.
2,4 Инструментальные диагностические исследования.
• Рекомендуется проведение инструментальной диагностики у пациентов с наследственным дефицитом FII, FVII или FX для уточнения диагноза и проведения дифференциальной диагностики с другими заболеваниями с возможным наличием геморрагического синдрома, которая может по показаниям включать следующие методы исследования [2,4,13,19,20,22-25]:• эзофагогастродуоденоскопия,.
• ультразвуковое исследование сустава,.
• ультразвуковое исследование органов брюшной полости,.
• ультразвуковое исследование мочевыводящих путей,.
• ультразвуковое исследование органов малого таза,.
• ультразвуковое исследование забрюшинного пространства,.
• магнитно-резонансная томография сустава, мягких тканей,.
• магнитно-резонансная томография головного мозга,.
• рентгенография сустава,.
• компьютерная томография органов грудной клетки,.
• компьютерная томография головного мозга,.
• риноскопия эндоскопическая,.
• ректороманоскопия,.
• кольпоскопия,.
• гистероскопия,.
• колоноскопия.
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 3).
Комментарии. Исследования позволяют визуализировать кровотечения/кровоизлияния различных локализаций, а также выявить осложнения, развившиеся вследствие геморрагических проявлений.
2,5 Иные диагностические исследования.
• Рекомендуются консультации следующих врачей-специалистов пациентам с выявленным дефицитом FII, FVII или FX для подтверждения наличия геморрагических проявлений (или их последствий) [2,13]:• врача-травматолога-ортопеда,.
• врача-хирурга,.
• врача-уролога,.
• врача-невролога,.
• врача-оториноларинголога,.
• врача-стоматолога,.
• врача-акушера-гинеколога.
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии. Позволяют определить нарушения различных органов и систем вследствие состоявшегося (перенесенного ранее) кровотечения/кровоизлияния.
• Рекомендуется пациентам с РНСК в случае невозможности проведения полноценного двухэтапного коагулологического исследования, а также в некоторых случаях для контроля за проводимой терапией выполнять интегральные тесты оценки гемостаза: тромбодинамика, тромбоэластография, тест генерации тромбина, с целью выявления и мониторинга нарушений свертывающей системы крови [26].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
|
|
Лечение
• Рекомендуется при наследственном дефиците FII проведение специфической заместительной терапии неактивированными препаратами, содержащими FII. Строго рекомендуется использование плазматических очищенных вирус-инактивированных концентратов протромбинового комплекса (КПК - отдельные препараты из группы в02BD по АТХ классификации): Факторы свертывания крови IX, II, VII и X в комбинации) - факторы свертывания крови II, VII, IX и X в комбинации [протромбиновый комплекс]** и факторы свертывания крови II, IX и X в комбинации** (вне зарегистрированных показаний для детей - эффективность и безопасность недостаточно изучены) с индивидуальным подбором дозы в зависимости от содержания FII в препарате и массы тела пациента ( см комментарий) [1,8,13,20,24,27-29].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии. КПК вводятся внутривенно. Используется болюсная инфузия со скоростью, рекомендованной производителем. Активность КПК, обычно, указывается по активности содержащегося в них фактора свертывания крови IX (FIX). Поэтому, необходимо отдельно уточнять содержание FII, которое указывается в инструкции. Как правило, КПК содержат приблизительно равное количество FIX и при расчете дозы и схемы заместительной терапии необходимо учитывать, что введение 1 МЕ FII на 1 кг массы тела пациента повышает активность FII, в среднем, на 1,5-1,9% (восстановление активности FII - тест восстановления = 2). Период полувыведения FII составляет около 60 часов. Таким образом, стандартная терапевтическая доза КПК 20-30 МЕ/кг массы тела пациента (здесь и далее расчет по FIX) повышает активность плазменного FII до 40-60%. У пациентов с активным кровотечением этот показатель может быть меньше [8,13,20,28].
При тяжелых кровотечениях или больших хирургических вмешательствах у пациентов с дефицитом FII КПК назначается в стартовой насыщающей дозе 20 - 50 МЕ/кг массы тела пациента с последующими повторными инфузиями препарата в дозе 10 - 30 МЕ/кг массы тела пациента с интервалами в 24 - 48 часов для достижения и поддержания активности FII better 20% [29,30].
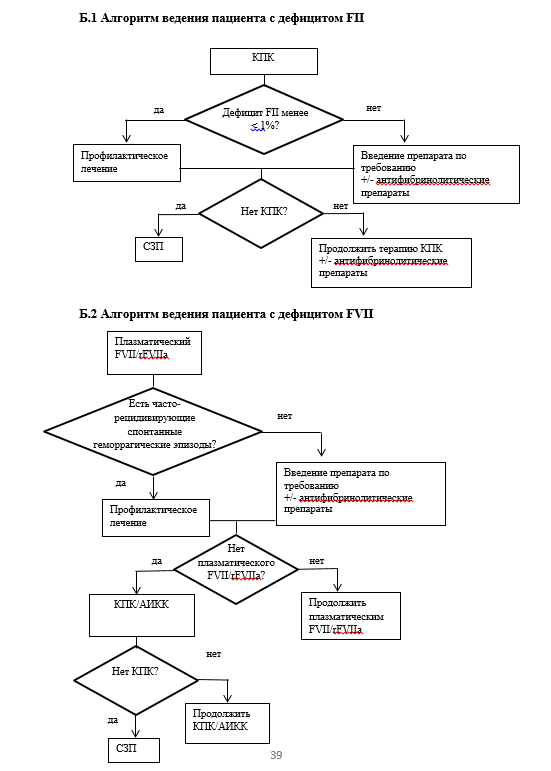
• Рекомендуется проведение профилактического лечения с введением КПК. У пациентов с дефицитом FII в дозе 20-40 МЕ/кг массы тела пациента с интервалом в 5-7 дней с целью достижения активности FII ≥ 10%, с целью предотвращения развития геморрагического синдрома, при наличии персонального или семейного анамнеза, тяжелого клинического фенотипа, предшествующих кровотечений или при снижении активности FII worse 1% [13,24,27,28,30,31].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
Комментарии. Сведений о возможном возникновении аллоантител к FII не имеется.
В случае недоступности КПК возможно использование карантинизированной СЗП в дозе 15-25 мл/кг массы тела пациента, повышающей плазменную активность FII до 30-40%. Использование СЗП возможно в исключительных случаях и не должно являться постоянной практикой.
• Рекомендуется для купирования легких кровотечений или в случае проведения малого хирургического вмешательства у пациентов с дефицитом FII назначение транексамовой кислоты** в дозе 15-20 мг/кг массы тела пациента или 1,0 г х 4 раза в сутки [30,32].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
• Рекомендуется для купирования или предупреждения кровотечений у пациентов при гипопроконвертинемии проведение специфической заместительной терапии следующими препаратами: фактором свертывания крови FVII** (FVII** вне зарегистрированных показаний у детей до 6 лет), эптакогом альфа (активированным)**, фактором свертывания крови II, VII, IX и X в комбинации [протромбиновый комплекс]** или фактором свертывания крови II, IX и X в комбинации** (вне зарегистрированных показаний для детей - эффективность и безопасность недостаточно изучены) с индивидуальным подбором дозы в зависимости от содержания FVII в препарате и массы тела пациента ( см комментарий) [5,22,31,33-37].
Уровень убедительности рекомендаций в (уровень достоверности доказательств - 3).
Комментарии. Гемостатическая терапия фактором свертывания крови FVII** (FVII** вне зарегистрированных показаний у детей до 6 лет) проводится при развитии кровотечения/кровоизлияния в дозе 20-30 МЕ/кг массы тела пациента каждые 4-6 часов до купирования геморрагического синдрома. С целью предупреждения возникновения кровотечения возможно проведение заместительной терапии фактором свертывания крови VII** в дозе 10-30 МЕ/кг массы тела пациента 3 раза в неделю [36-38].
Альтернативой фактору свертывания крови VII** для лечения пациентов с гипопроконвертинемией является эптаког альфа (активированный)** [8,35,36]. Для остановки легкого кровотечения препарат вводится однократно в дозе 30-50 мкг/кг массы тела пациента (дозировка вне зарегистрированных показаний) [36]. При возникновении умеренного или тяжелого кровотечения, а также в случае высокого риска развития геморрагических осложнений во время и после проведения хирургических вмешательств рекомендуются повторные введения эптакога альфа (активированного)** в дозе 15-30 мкг/кг массы тела пациента с интервалом в 4-6 часов (обычно не менее 3-х инфузий) [8,39].
При выполнении малых хирургических вмешательств или инвазивных процедур минимальная доза эптаког альфа (активированного)** должна составлять 15 мкг/кг массы тела пациента до проведения манипуляции и вводится, как минимум, дважды после окончания процедуры с интервалом в 4-6 часов [5,35,36].
При проведении хирургического лечения частота введения препаратов определяется объемом хирургического вмешательства. Рекомендуется контролировать ПВ не реже 1 раза в 12 часов и проводить заместительную терапию при снижении МНО менее 1,3.
• Рекомендуется профилактическое введение препаратов фактора свертывания крови VII* пациентам с гипопроконвертинемией при повторных кровоизлияниях в суставы, рецидивирующих кровоизлияниях и кровотечениях другой локализации, при условии, что геморрагический синдром определяет прогноз для здоровья и жизни пациента и значимо нарушает качество его жизни [13,31,40].
Уровень убедительности рекомендаций в (уровень достоверности доказательств - 3).
Комментарии. Частота введений препаратов подбирается индивидуально с учетом клинической картины заболевания. Профилактическое введение препаратов может быть как краткосрочным, (например, при маточных кровотечениях: эптаког альфа (активированный)** в дозе 20-40 мкг/кг массы тела пациентки 3-4 инфузии с интервалом в 12-24 часов до достижения клинического ответа (дозировка вне зарегистрированных показаний) [31], так и длительным (например, при рецидивирующих гемартрозах - введение фактора свертывания крови VII** в дозе 20-30 МЕ/кг массы тела пациента 3 раза в неделю) [31].
• Рекомендуется у новорожденных с гипопроконвертинемией, не имеющих семейного анамнеза тяжелых кровотечений, но с активностью FVII ≤ 1%, проведение краткосрочной профилактики эптакогом альфа (активированным)** в дозе 20-40 мкг/кг массы тела пациента 3 раза в неделю до достижения 6-12- месячного возраста [8,31,37,41,42].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии. Эффективность терапии фактором свертывания крови VII** и эптакогом альфа (активированным)** идентична. Имеются сведения о возможном появлении аллоантител к FVII при проведении заместительной терапии. При условии равной эффективности и удовлетворительной индивидуальной переносимости выбор лекарственного средства для заместительной терапии зависит от возможности бесперебойного обеспечения пациента этим препаратом.
• Рекомендуется в случае отсутствия эптакога альфа (активированного)** и фактора свертывания крови VII** для остановки кровотечения при дефиците FVII однократно применять КПК в дозе 20-30 МЕ/кг (FIX) массы тела пациента [8].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
Комментарии. В связи с повышенным риском развития тромбозов при использовании этих препаратов повторная инъекция возможна не ранее 24 часов после предыдущего введения препарата.
• Рекомендуется, в случае недоступности эптаког альфа (активированного)**, фактора свертывания крови VII**, КПК и антиингибиторного коагулянтного комплекса**, у пациентов с РНСК применение карантинизированной СЗП в дозе 15-25 мл/кг массы тела пациента [8,24].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
Комментарии. Использование СЗП возможно в исключительных случаях и не должно являться постоянной практикой.
• Рекомендуется при гипопроконвертинемии для купирования легких кровотечений у пациентов или в случае проведения малого хирургического вмешательства с высоким риском развития кровотечения, а также во всех случаях низкого риска развития послеоперационного геморрагического синдрома монотерапии транексамовой кислотой** в дозе 10-15 мг/кг массы тела пациента или 1,0 г х 3-4 раза в сутки [13,30].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
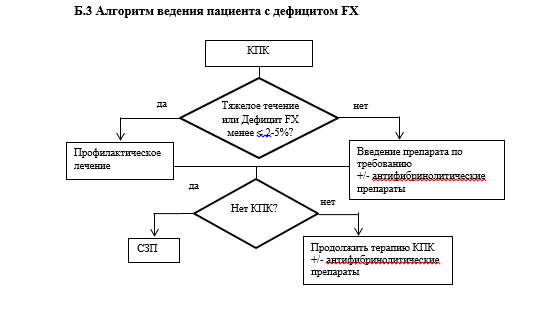
• Рекомендуется для лечения пациентов с дефицитом FX специфическая заместительная терапия КПК: факторов свертывания крови II, VII, IX и X в комбинации [протромбиновый комплекс]** или факторов свертывания крови II, IX и X в комбинации**. При больших хирургических вмешательствах рекомендуемые целевые минимальные уровни FX >20-30%, рекомендуемая доза 20-30 МЕ/кг перед операцией и далее по показаниям 10-20 МЕ/кг каждые 24 часа. Рекомендуемые дозы для лечения кровотечений 20-30 МЕ/кг, целевой уровень >40%. С целью профилактики кровотечений рекомендуется 20-40 МЕ/кг 2 раза в неделю [1,4,8,30,43-45].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 4).
Комментарии. В настоящее время в РФ зарегистрированы 2 препарата КПК, содержащие FX - КПК - факторы свертывания крови II, VII, IX и X в комбинации [протромбиновый комплекс]** и факторы свертывания крови II, IX и X в комбинации**.
• Рекомендуется всем пациентам с РНСК использование плазматических очищенных вирусинактивированных КПК [8,13,24,31,40,43,45,46].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
Комментарии. КПК вводятся внутривенно. Используется болюсная инфузия со скоростью, рекомендованной производителем. Активность КПК, обычно, указывается по активности содержащегося в них FIX. Поэтому, необходимо отдельно уточнять содержание FХ, которое указывается в инструкции. КПК содержат FIX и FX приблизительно в эквивалентной активности. При введении КПК в дозе 1 МЕ/кг массы тела пациента активность FX повышается, в среднем, на 2% (восстановление активности FX - тест восстановления = 2). Таким образом, стандартная терапевтическая доза КПК 30 (FIX) МЕ/кг массы тела пациента (20-30 (FIX) МЕ/кг массы тела у детей) повышает активность плазменного FX до 40-60% [8,13,31,43,45].
При тяжелых кровотечениях или больших хирургических вмешательствах у пациентов с дефицитом FX КПК назначаются в стартовой насыщающей дозе 20-30 (FIX) МЕ/кг массы тела пациента с последующими повторными инфузиями препарата в дозе 10-20 (FIX) МЕ/кг массы тела пациента с интервалами в 24-48 часов для достижения и поддержания активности FX better 20% [8,13,43].
• При дефиците FX рекомендуется проведение долговременного профилактического лечения пациентов с целью предотвращения развития геморрагического синдрома при наличии персонального или семейного анамнеза тяжелого клинического фенотипа предшествующих кровотечений или при снижении активности FX worse 2% [8,13,24,31,40,43,45,46].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии. КПК назначается в дозе 20-30 (FIX) МЕ/кг массы тела пациента 2-3 раза в неделю с целью поддержания активности FX better 1% у взрослых и better 2% у детей [13,31,43,45]. Сведений о возможном возникновении изоантител к FX не имеется.
• Рекомендуется в случае недоступности КПК использование карантинизированной СЗП в дозе 15-25 мл/кг массы тела пациента, повышающей плазменную активность FX до 30-40% [8,24,47].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
Комментарии. Использование СЗП возможно в исключительных случаях и не должно являться постоянной практикой.
• Рекомендуется для купирования легких кровотечений у пациентов или в случае проведения малого хирургического вмешательства при дефиците FX проведение монотерапии транексамовой кислотой** в дозе 15-20 мг/кг массы тела пациента или 1,0 г х 4 раза в сутки [8,30,32].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии. КПК вводятся внутривенно. Используется болюсная инфузия со скоростью, рекомендованной производителем. Активность КПК, обычно, указывается по активности содержащегося в них фактора свертывания крови IX (FIX). Поэтому, необходимо отдельно уточнять содержание FII, которое указывается в инструкции. Как правило, КПК содержат приблизительно равное количество FIX и при расчете дозы и схемы заместительной терапии необходимо учитывать, что введение 1 МЕ FII на 1 кг массы тела пациента повышает активность FII, в среднем, на 1,5-1,9% (восстановление активности FII - тест восстановления = 2). Период полувыведения FII составляет около 60 часов. Таким образом, стандартная терапевтическая доза КПК 20-30 МЕ/кг массы тела пациента (здесь и далее расчет по FIX) повышает активность плазменного FII до 40-60%. У пациентов с активным кровотечением этот показатель может быть меньше [8,13,20,28].
При тяжелых кровотечениях или больших хирургических вмешательствах у пациентов с дефицитом FII КПК назначается в стартовой насыщающей дозе 20 - 50 МЕ/кг массы тела пациента с последующими повторными инфузиями препарата в дозе 10 - 30 МЕ/кг массы тела пациента с интервалами в 24 - 48 часов для достижения и поддержания активности FII better 20% [29,30].
• Рекомендуется проведение профилактического лечения с введением КПК. У пациентов с дефицитом FII в дозе 20-40 МЕ/кг массы тела пациента с интервалом в 5-7 дней с целью достижения активности FII ≥ 10%, с целью предотвращения развития геморрагического синдрома, при наличии персонального или семейного анамнеза, тяжелого клинического фенотипа, предшествующих кровотечений или при снижении активности FII worse 1% [13,24,27,28,30,31].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
Комментарии. Сведений о возможном возникновении аллоантител к FII не имеется.
В случае недоступности КПК возможно использование карантинизированной СЗП в дозе 15-25 мл/кг массы тела пациента, повышающей плазменную активность FII до 30-40%. Использование СЗП возможно в исключительных случаях и не должно являться постоянной практикой.
• Рекомендуется для купирования легких кровотечений или в случае проведения малого хирургического вмешательства у пациентов с дефицитом FII назначение транексамовой кислоты** в дозе 15-20 мг/кг массы тела пациента или 1,0 г х 4 раза в сутки [30,32].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
• Рекомендуется для купирования или предупреждения кровотечений у пациентов при гипопроконвертинемии проведение специфической заместительной терапии следующими препаратами: фактором свертывания крови FVII** (FVII** вне зарегистрированных показаний у детей до 6 лет), эптакогом альфа (активированным)**, фактором свертывания крови II, VII, IX и X в комбинации [протромбиновый комплекс]** или фактором свертывания крови II, IX и X в комбинации** (вне зарегистрированных показаний для детей - эффективность и безопасность недостаточно изучены) с индивидуальным подбором дозы в зависимости от содержания FVII в препарате и массы тела пациента ( см комментарий) [5,22,31,33-37].
Уровень убедительности рекомендаций в (уровень достоверности доказательств - 3).
Комментарии. Гемостатическая терапия фактором свертывания крови FVII** (FVII** вне зарегистрированных показаний у детей до 6 лет) проводится при развитии кровотечения/кровоизлияния в дозе 20-30 МЕ/кг массы тела пациента каждые 4-6 часов до купирования геморрагического синдрома. С целью предупреждения возникновения кровотечения возможно проведение заместительной терапии фактором свертывания крови VII** в дозе 10-30 МЕ/кг массы тела пациента 3 раза в неделю [36-38].
Альтернативой фактору свертывания крови VII** для лечения пациентов с гипопроконвертинемией является эптаког альфа (активированный)** [8,35,36]. Для остановки легкого кровотечения препарат вводится однократно в дозе 30-50 мкг/кг массы тела пациента (дозировка вне зарегистрированных показаний) [36]. При возникновении умеренного или тяжелого кровотечения, а также в случае высокого риска развития геморрагических осложнений во время и после проведения хирургических вмешательств рекомендуются повторные введения эптакога альфа (активированного)** в дозе 15-30 мкг/кг массы тела пациента с интервалом в 4-6 часов (обычно не менее 3-х инфузий) [8,39].
При выполнении малых хирургических вмешательств или инвазивных процедур минимальная доза эптаког альфа (активированного)** должна составлять 15 мкг/кг массы тела пациента до проведения манипуляции и вводится, как минимум, дважды после окончания процедуры с интервалом в 4-6 часов [5,35,36].
При проведении хирургического лечения частота введения препаратов определяется объемом хирургического вмешательства. Рекомендуется контролировать ПВ не реже 1 раза в 12 часов и проводить заместительную терапию при снижении МНО менее 1,3.
• Рекомендуется профилактическое введение препаратов фактора свертывания крови VII* пациентам с гипопроконвертинемией при повторных кровоизлияниях в суставы, рецидивирующих кровоизлияниях и кровотечениях другой локализации, при условии, что геморрагический синдром определяет прогноз для здоровья и жизни пациента и значимо нарушает качество его жизни [13,31,40].
Уровень убедительности рекомендаций в (уровень достоверности доказательств - 3).
Комментарии. Частота введений препаратов подбирается индивидуально с учетом клинической картины заболевания. Профилактическое введение препаратов может быть как краткосрочным, (например, при маточных кровотечениях: эптаког альфа (активированный)** в дозе 20-40 мкг/кг массы тела пациентки 3-4 инфузии с интервалом в 12-24 часов до достижения клинического ответа (дозировка вне зарегистрированных показаний) [31], так и длительным (например, при рецидивирующих гемартрозах - введение фактора свертывания крови VII** в дозе 20-30 МЕ/кг массы тела пациента 3 раза в неделю) [31].
• Рекомендуется у новорожденных с гипопроконвертинемией, не имеющих семейного анамнеза тяжелых кровотечений, но с активностью FVII ≤ 1%, проведение краткосрочной профилактики эптакогом альфа (активированным)** в дозе 20-40 мкг/кг массы тела пациента 3 раза в неделю до достижения 6-12- месячного возраста [8,31,37,41,42].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии. Эффективность терапии фактором свертывания крови VII** и эптакогом альфа (активированным)** идентична. Имеются сведения о возможном появлении аллоантител к FVII при проведении заместительной терапии. При условии равной эффективности и удовлетворительной индивидуальной переносимости выбор лекарственного средства для заместительной терапии зависит от возможности бесперебойного обеспечения пациента этим препаратом.
• Рекомендуется в случае отсутствия эптакога альфа (активированного)** и фактора свертывания крови VII** для остановки кровотечения при дефиците FVII однократно применять КПК в дозе 20-30 МЕ/кг (FIX) массы тела пациента [8].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
Комментарии. В связи с повышенным риском развития тромбозов при использовании этих препаратов повторная инъекция возможна не ранее 24 часов после предыдущего введения препарата.
• Рекомендуется, в случае недоступности эптаког альфа (активированного)**, фактора свертывания крови VII**, КПК и антиингибиторного коагулянтного комплекса**, у пациентов с РНСК применение карантинизированной СЗП в дозе 15-25 мл/кг массы тела пациента [8,24].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
Комментарии. Использование СЗП возможно в исключительных случаях и не должно являться постоянной практикой.
• Рекомендуется при гипопроконвертинемии для купирования легких кровотечений у пациентов или в случае проведения малого хирургического вмешательства с высоким риском развития кровотечения, а также во всех случаях низкого риска развития послеоперационного геморрагического синдрома монотерапии транексамовой кислотой** в дозе 10-15 мг/кг массы тела пациента или 1,0 г х 3-4 раза в сутки [13,30].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
• Рекомендуется для лечения пациентов с дефицитом FX специфическая заместительная терапия КПК: факторов свертывания крови II, VII, IX и X в комбинации [протромбиновый комплекс]** или факторов свертывания крови II, IX и X в комбинации**. При больших хирургических вмешательствах рекомендуемые целевые минимальные уровни FX >20-30%, рекомендуемая доза 20-30 МЕ/кг перед операцией и далее по показаниям 10-20 МЕ/кг каждые 24 часа. Рекомендуемые дозы для лечения кровотечений 20-30 МЕ/кг, целевой уровень >40%. С целью профилактики кровотечений рекомендуется 20-40 МЕ/кг 2 раза в неделю [1,4,8,30,43-45].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 4).
Комментарии. В настоящее время в РФ зарегистрированы 2 препарата КПК, содержащие FX - КПК - факторы свертывания крови II, VII, IX и X в комбинации [протромбиновый комплекс]** и факторы свертывания крови II, IX и X в комбинации**.
• Рекомендуется всем пациентам с РНСК использование плазматических очищенных вирусинактивированных КПК [8,13,24,31,40,43,45,46].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
Комментарии. КПК вводятся внутривенно. Используется болюсная инфузия со скоростью, рекомендованной производителем. Активность КПК, обычно, указывается по активности содержащегося в них FIX. Поэтому, необходимо отдельно уточнять содержание FХ, которое указывается в инструкции. КПК содержат FIX и FX приблизительно в эквивалентной активности. При введении КПК в дозе 1 МЕ/кг массы тела пациента активность FX повышается, в среднем, на 2% (восстановление активности FX - тест восстановления = 2). Таким образом, стандартная терапевтическая доза КПК 30 (FIX) МЕ/кг массы тела пациента (20-30 (FIX) МЕ/кг массы тела у детей) повышает активность плазменного FX до 40-60% [8,13,31,43,45].
При тяжелых кровотечениях или больших хирургических вмешательствах у пациентов с дефицитом FX КПК назначаются в стартовой насыщающей дозе 20-30 (FIX) МЕ/кг массы тела пациента с последующими повторными инфузиями препарата в дозе 10-20 (FIX) МЕ/кг массы тела пациента с интервалами в 24-48 часов для достижения и поддержания активности FX better 20% [8,13,43].
• При дефиците FX рекомендуется проведение долговременного профилактического лечения пациентов с целью предотвращения развития геморрагического синдрома при наличии персонального или семейного анамнеза тяжелого клинического фенотипа предшествующих кровотечений или при снижении активности FX worse 2% [8,13,24,31,40,43,45,46].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии. КПК назначается в дозе 20-30 (FIX) МЕ/кг массы тела пациента 2-3 раза в неделю с целью поддержания активности FX better 1% у взрослых и better 2% у детей [13,31,43,45]. Сведений о возможном возникновении изоантител к FX не имеется.
• Рекомендуется в случае недоступности КПК использование карантинизированной СЗП в дозе 15-25 мл/кг массы тела пациента, повышающей плазменную активность FX до 30-40% [8,24,47].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
Комментарии. Использование СЗП возможно в исключительных случаях и не должно являться постоянной практикой.
• Рекомендуется для купирования легких кровотечений у пациентов или в случае проведения малого хирургического вмешательства при дефиците FX проведение монотерапии транексамовой кислотой** в дозе 15-20 мг/кг массы тела пациента или 1,0 г х 4 раза в сутки [8,30,32].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
|
|
Реабилитация и амбулаторное лечение
Специфическая реабилитация для пациентов с редкими коагулопатиями не разработана. Реабилитационные мероприятия показаны пациентам после кровоизлияний в ЦНС, с поражением опорно-двигательного аппарата [1]. Разработка реабилитационных мероприятий должна проводиться совместно специалистами по реабилитации, курортологии и врачамии-гематологами, имеющими опыт лечения пациентов с нарушениями свертывания крови. Лечение можно проводить в санаторно-курортных организациях в санаториях общего профиля в климатической зоне проживания пациента, а также на бальнеологических курортах.
Целесообразно проведение школ психологической адаптации для пациентов с РНСК.
Целесообразно проведение школ психологической адаптации для пациентов с РНСК.
Профилактика
• Рекомендуется пациентам проведение профилактической заместительной терапии препаратами группы в02BD факторы свертывания крови при повторных кровоизлияниях в суставы, рецидивирующих кровоизлияниях и кровотечениях другой локализации, при условии, что геморрагический синдром определяет прогноз для здоровья и жизни пациента и значимо нарушает качество его жизни [5,8,11,13,31,37].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
Комментарии. Основным принципом предотвращения возникновения геморрагических эпизодов является проведение своевременной заместительной терапии концентратами дефицитных факторов.
Профилактическая терапия может осуществляться после подписания информированного согласия пациентом или его законными представителями. Профилактическое лечение может проводиться на дому пациентом или его родственниками.
• Рекомендуется всем пациентам проводить осмотр пациентов врачом-гематологом, врачом-травматологом-ортопедом и врачом-стоматологом не менее 2-х раз в год; остальными специалистами - по необходимости [1].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
Комментарии. Целесообразно проведение диспансеризации пациентов 1 раз в год в специализированном центре нарушений гемостаза, если центр располагает достаточной клинико-лабораторной базой. Диспансерное наблюдение за пациентами с РНСК должно включать:
• обязателен динамический мониторинг состояния пациента с оценкой наличия нежелательных явлений при проведении заместительной терапии: появление ингибитора к факторам свертывания крови, индивидуальная непереносимость препаратов, вирусная контаминация, изменения психологического или социального статуса пациента, оценка состояния периферической венозной системы.
• лечение осложнений РНСК: коррекция дефицита железа, ингибиторов.
• выявление и лечение сопутствующих заболеваний, особенно заболеваний зубов, полости рта, ЖКТ, ЛОР-органов, патологии сердечно-сосудистой системы.
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
Комментарии. Основным принципом предотвращения возникновения геморрагических эпизодов является проведение своевременной заместительной терапии концентратами дефицитных факторов.
Профилактическая терапия может осуществляться после подписания информированного согласия пациентом или его законными представителями. Профилактическое лечение может проводиться на дому пациентом или его родственниками.
• Рекомендуется всем пациентам проводить осмотр пациентов врачом-гематологом, врачом-травматологом-ортопедом и врачом-стоматологом не менее 2-х раз в год; остальными специалистами - по необходимости [1].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
Комментарии. Целесообразно проведение диспансеризации пациентов 1 раз в год в специализированном центре нарушений гемостаза, если центр располагает достаточной клинико-лабораторной базой. Диспансерное наблюдение за пациентами с РНСК должно включать:
• обязателен динамический мониторинг состояния пациента с оценкой наличия нежелательных явлений при проведении заместительной терапии: появление ингибитора к факторам свертывания крови, индивидуальная непереносимость препаратов, вирусная контаминация, изменения психологического или социального статуса пациента, оценка состояния периферической венозной системы.
• лечение осложнений РНСК: коррекция дефицита железа, ингибиторов.
• выявление и лечение сопутствующих заболеваний, особенно заболеваний зубов, полости рта, ЖКТ, ЛОР-органов, патологии сердечно-сосудистой системы.
Организация оказания медицинской помощи
Показания для плановой госпитализации:
1) плановое оперативное лечение.
Показания для экстренной госпитализации:
1) жизнеугрожающее кровотечение;
2) проведение экстренного оперативного вмешательства.
Показания к выписке пациента из стационара:
1) полная остановка кровотечения.
1) плановое оперативное лечение.
Показания для экстренной госпитализации:
1) жизнеугрожающее кровотечение;
2) проведение экстренного оперативного вмешательства.
Показания к выписке пациента из стационара:
1) полная остановка кровотечения.
Дополнительно
Применение неспецифических гемостатических препаратов.
Помимо специфической гемостатической и заместительной терапии врач-гематолог может использовать дополнительные лекарственные средства в лечении пациентов с РНСК, например, гормональную терапию у женщин с рецидивирующими тяжелыми маточными кровотечениями.
Транексамовая кислота** и другие антифибринолитические средства могут применяться для купирования меноррагий и легких кровотечений из слизистых оболочек, за исключением почечных кровотечений. Антифибринолитические средства могут использоваться в монотерапии или в дополнение к концентратам факторов свертывания крови. В случае высокого риска возможных тромботических осложнений применение антифибринолитических средств недопустимо. Для предупреждения хирургических или акушерских кровотечений транексамовая кислота** должна быть назначена перорально или внутривенно не позднее, чем за 2 часа до операции или родов для достижения пиковых значений в плазме во время проведения манипуляции. Транексамовая кислота** должна с осторожностью использоваться одновременно с КПК из-за высокого риска развития тромботических осложнений.
Особенности дефицита FII у детей.
Проявлением дефицита FII у детей могут быть пупочные кровотечения или кровоизлияния в ЦНС. Важно помнить, что у детей в первом полугодии жизни нормальная активность FII составляет 26-70%. Взрослых значений активность FII достигает к 6-месячному возрасту. Необходимо проведение неоднократных повторных обследований пациента после достижения 6-месячного возраста. Поэтому точно установить диагноз дефицита FII можно у детей старше 1 года. В любом случае при диагностике удлинения ПВ у детей в этом возрасте показано назначение препаратов витамина К1 [1,20,41,48].
Ведение женщин c дефицитом FII во время беременности и родов.
В течение нормально протекающей беременности активность FII существенно не меняется и обычно остается недостаточной для неосложненного родоразрешения у женщин с тяжелым дефицитом протромбина. При активности FII worse 20% с целью предотвращения развития геморрагических осложнений в родах необходимо введение КПК* в дозе 20-40 МЕ/кг массы тела пациентки однократно при начале родовой деятельности или перед кесаревым сечением для достижения активности FII 20-40%. Повторные инфузии препарата производятся с интервалом в 48 часов в дозе 10 - 20 МЕ/кг массы тела пациентки с целью поддержания активности FII better 20% в течение, как минимум, 3-5 дней после вагинальных родов или 5-7 дней после кесарева сечения [8]. При отсутствии клинических проявлений заболевания во время беременности заместительная терапия КПК не проводится, в случае развития кровотечения терапия проводится по общим принципам [49].
Особенности течения гипопроконвертинемии у детей.
У новорожденных с дефицитом FVII существует опасность возникновения спонтанных кровоизлияний в ЦНС или пупочных кровотечений. Другие проявления геморрагического синдрома нехарактерны. Физиологическая активность FVII при рождении составляет 28-104% и достигает нормальных значений к 6-месячному возрасту. Поэтому, окончательный диагноз устанавливается в возрасте после 6 - 12 месяцев [41,42].
Ведение женщин с гипопроконвертинемией во время беременности и родов.
В течение нормально протекающей беременности активность FVII физиологически повышается. Женщины с легким дефицитом FVII могут достигнуть к моменту родов необходимого гемостатического уровня активности FVII без проведения специфической заместительной терапии.
У беременных с тяжелым дефицитом FVII есть риск развития геморрагических осложнений в родах. Женщинам с активностью FVII ≤ 20% перед проведением кесарева сечения или с началом родовой деятельности необходимо проведение заместительной терапии эптаког альфа (активированным)** в дозе 15-30 мкг/кг массы тела пациентки каждые 4-6 часов в течение не менее 3-х дней. Для всех остальных женщин с дефицитом FVII эптаког альфа (активированный)** назначается только в случае развития кровотечения согласно FVII общим принципам терапии [50,51].
Особенности течения дефицита FX у детей.
У новорожденных с дефицитом FX возможны кровоизлияния в ЦНС или пупочные кровотечения. Физиологическая активность FX при рождении составляет 12-68% и повышается к 6-месячному возрасту. Поэтому окончательное установление диагноза дефицита FX у новорожденных требует обязательного сравнения полученных результатов лабораторного исследования с референсными интервалами допустимых в неонатальном периоде значений и повторного обследования пациента после достижения 6-месячного возраста. При выявлении у детей первого полугодия сниженной активности FХ показано назначение препаратов витамина К1 (группа в02BA по классификации АТХ) [4,19,41-43].
Ведение женщин с дефицитом FX во время беременности и родов.
У женщин с активностью FX менее 30% возможны проблемы с зачатием. Беременность осложняется ранними выкидышами в первой триместре, геморрагическими проявлениями (чаще геморрагическим циститом) во втором и третьем триместре. Необходимый уровень FX до и во время беременности должен быть не менее 30%.
Несмотря на физиологическое повышение активности FX в течение нормально протекающей беременности, у женщин с тяжелым дефицитом FX его уровень к родам обычно остается недостаточным для обеспечения нормального гемостаза. Женщинам с активностью FX ≤ 30% в третьем триместре беременности с наличием в анамнезе кровотечений до беременности, а также перед проведением кесарева сечения с началом родовой деятельности необходимо проведение заместительной терапии КПК: факторов свертывания крови II, VII, IX и X в комбинации [протромбиновый комплекс]** или факторов свертывания крови II, IX и X в комбинации** (вне зарегистрированных показаний для детей - эффективность и безопасность недостаточно изучены) в дозе 20-40 (FIX) МЕ/кг массы тела пациентки для достижения активности FX better 40%.Дальнейшие инфузии КПК проводятся с интервалом в 24 часа в дозе 10-20 (FIX) МЕ/кг массы тела пациентки в течение, как минимум, 3-х дней с целью поддержания активности FX не менее 30% [8,46,47,52].
Проведение лабораторных исследований.
Лабораторные анализы лежат в основе диагностики и контроля у пациентов с РНСК. Требования к условиям и технике отбора образцов и выполнения исследований не отличаются от стандартных. Важным аспектом лабораторных исследований является участие в системе контроля качества. При диагностике РНСК оптимально участвовать не только в государственной, но и в международной системе контроля качества лабораторных исследований, охватывающей основные коагулологические параметры [10,14,17,18].
Вакцинация.
Пациенты с РНСК могут быть вакцинированы. Особенно важно проведение вакцинации от гепатита В. При вакцинации предпочтение отдается оральному или подкожному введению препарата, по сравнению с внутримышечным или внутрикожным. Если для данной вакцины доступен только внутримышечный путь введения, необходима заместительная терапия для предотвращения развития гематомы. В этом случае заместительную терапию проводят накануне вакцинации. В день вакцинации введение препарата не рекомендуется. Нельзя проводить вакцинацию во время кровотечения [8].
Обучение пациентов и членов их семей.
Обучение пациентов и членов их семей - необходимое условие обеспечения адекватной помощи больным с РНСК. Обучение начинается сразу после установления диагноза и проводится на постоянной основе врачами и медицинскими сестрами центра, в котором наблюдается пациент. Обучение проводиться индивидуально при посещении центра и в рамках школы пациента с РНСК.
Основные направления обучения пациента и членов его семьи: что такое РНСК, особенности заболевания в детском возрасте, навыки оценки состояния ребенка, навыки оценки симптомов, характера и тяжести кровотечения, хранение и использование концентратов факторов свертывания крови, показания и дозы заместительной терапии, навыки проведения инфузии в домашних условиях, уход за венами, применение других гемостатических препаратов, физическая активность, психологическая и социальная адаптация, профессиональная ориентация, юридические аспекты.
Помимо врачей и медсестер к обучению пациентов и членов их семей необходимо привлекать психологов, юристов и членов общественных организаций, представляющих интересы больных с нарушениями свертывания крови.
Помимо специфической гемостатической и заместительной терапии врач-гематолог может использовать дополнительные лекарственные средства в лечении пациентов с РНСК, например, гормональную терапию у женщин с рецидивирующими тяжелыми маточными кровотечениями.
Транексамовая кислота** и другие антифибринолитические средства могут применяться для купирования меноррагий и легких кровотечений из слизистых оболочек, за исключением почечных кровотечений. Антифибринолитические средства могут использоваться в монотерапии или в дополнение к концентратам факторов свертывания крови. В случае высокого риска возможных тромботических осложнений применение антифибринолитических средств недопустимо. Для предупреждения хирургических или акушерских кровотечений транексамовая кислота** должна быть назначена перорально или внутривенно не позднее, чем за 2 часа до операции или родов для достижения пиковых значений в плазме во время проведения манипуляции. Транексамовая кислота** должна с осторожностью использоваться одновременно с КПК из-за высокого риска развития тромботических осложнений.
Особенности дефицита FII у детей.
Проявлением дефицита FII у детей могут быть пупочные кровотечения или кровоизлияния в ЦНС. Важно помнить, что у детей в первом полугодии жизни нормальная активность FII составляет 26-70%. Взрослых значений активность FII достигает к 6-месячному возрасту. Необходимо проведение неоднократных повторных обследований пациента после достижения 6-месячного возраста. Поэтому точно установить диагноз дефицита FII можно у детей старше 1 года. В любом случае при диагностике удлинения ПВ у детей в этом возрасте показано назначение препаратов витамина К1 [1,20,41,48].
Ведение женщин c дефицитом FII во время беременности и родов.
В течение нормально протекающей беременности активность FII существенно не меняется и обычно остается недостаточной для неосложненного родоразрешения у женщин с тяжелым дефицитом протромбина. При активности FII worse 20% с целью предотвращения развития геморрагических осложнений в родах необходимо введение КПК* в дозе 20-40 МЕ/кг массы тела пациентки однократно при начале родовой деятельности или перед кесаревым сечением для достижения активности FII 20-40%. Повторные инфузии препарата производятся с интервалом в 48 часов в дозе 10 - 20 МЕ/кг массы тела пациентки с целью поддержания активности FII better 20% в течение, как минимум, 3-5 дней после вагинальных родов или 5-7 дней после кесарева сечения [8]. При отсутствии клинических проявлений заболевания во время беременности заместительная терапия КПК не проводится, в случае развития кровотечения терапия проводится по общим принципам [49].
Особенности течения гипопроконвертинемии у детей.
У новорожденных с дефицитом FVII существует опасность возникновения спонтанных кровоизлияний в ЦНС или пупочных кровотечений. Другие проявления геморрагического синдрома нехарактерны. Физиологическая активность FVII при рождении составляет 28-104% и достигает нормальных значений к 6-месячному возрасту. Поэтому, окончательный диагноз устанавливается в возрасте после 6 - 12 месяцев [41,42].
Ведение женщин с гипопроконвертинемией во время беременности и родов.
В течение нормально протекающей беременности активность FVII физиологически повышается. Женщины с легким дефицитом FVII могут достигнуть к моменту родов необходимого гемостатического уровня активности FVII без проведения специфической заместительной терапии.
У беременных с тяжелым дефицитом FVII есть риск развития геморрагических осложнений в родах. Женщинам с активностью FVII ≤ 20% перед проведением кесарева сечения или с началом родовой деятельности необходимо проведение заместительной терапии эптаког альфа (активированным)** в дозе 15-30 мкг/кг массы тела пациентки каждые 4-6 часов в течение не менее 3-х дней. Для всех остальных женщин с дефицитом FVII эптаког альфа (активированный)** назначается только в случае развития кровотечения согласно FVII общим принципам терапии [50,51].
Особенности течения дефицита FX у детей.
У новорожденных с дефицитом FX возможны кровоизлияния в ЦНС или пупочные кровотечения. Физиологическая активность FX при рождении составляет 12-68% и повышается к 6-месячному возрасту. Поэтому окончательное установление диагноза дефицита FX у новорожденных требует обязательного сравнения полученных результатов лабораторного исследования с референсными интервалами допустимых в неонатальном периоде значений и повторного обследования пациента после достижения 6-месячного возраста. При выявлении у детей первого полугодия сниженной активности FХ показано назначение препаратов витамина К1 (группа в02BA по классификации АТХ) [4,19,41-43].
Ведение женщин с дефицитом FX во время беременности и родов.
У женщин с активностью FX менее 30% возможны проблемы с зачатием. Беременность осложняется ранними выкидышами в первой триместре, геморрагическими проявлениями (чаще геморрагическим циститом) во втором и третьем триместре. Необходимый уровень FX до и во время беременности должен быть не менее 30%.
Несмотря на физиологическое повышение активности FX в течение нормально протекающей беременности, у женщин с тяжелым дефицитом FX его уровень к родам обычно остается недостаточным для обеспечения нормального гемостаза. Женщинам с активностью FX ≤ 30% в третьем триместре беременности с наличием в анамнезе кровотечений до беременности, а также перед проведением кесарева сечения с началом родовой деятельности необходимо проведение заместительной терапии КПК: факторов свертывания крови II, VII, IX и X в комбинации [протромбиновый комплекс]** или факторов свертывания крови II, IX и X в комбинации** (вне зарегистрированных показаний для детей - эффективность и безопасность недостаточно изучены) в дозе 20-40 (FIX) МЕ/кг массы тела пациентки для достижения активности FX better 40%.Дальнейшие инфузии КПК проводятся с интервалом в 24 часа в дозе 10-20 (FIX) МЕ/кг массы тела пациентки в течение, как минимум, 3-х дней с целью поддержания активности FX не менее 30% [8,46,47,52].
Проведение лабораторных исследований.
Лабораторные анализы лежат в основе диагностики и контроля у пациентов с РНСК. Требования к условиям и технике отбора образцов и выполнения исследований не отличаются от стандартных. Важным аспектом лабораторных исследований является участие в системе контроля качества. При диагностике РНСК оптимально участвовать не только в государственной, но и в международной системе контроля качества лабораторных исследований, охватывающей основные коагулологические параметры [10,14,17,18].
Вакцинация.
Пациенты с РНСК могут быть вакцинированы. Особенно важно проведение вакцинации от гепатита В. При вакцинации предпочтение отдается оральному или подкожному введению препарата, по сравнению с внутримышечным или внутрикожным. Если для данной вакцины доступен только внутримышечный путь введения, необходима заместительная терапия для предотвращения развития гематомы. В этом случае заместительную терапию проводят накануне вакцинации. В день вакцинации введение препарата не рекомендуется. Нельзя проводить вакцинацию во время кровотечения [8].
Обучение пациентов и членов их семей.
Обучение пациентов и членов их семей - необходимое условие обеспечения адекватной помощи больным с РНСК. Обучение начинается сразу после установления диагноза и проводится на постоянной основе врачами и медицинскими сестрами центра, в котором наблюдается пациент. Обучение проводиться индивидуально при посещении центра и в рамках школы пациента с РНСК.
Основные направления обучения пациента и членов его семьи: что такое РНСК, особенности заболевания в детском возрасте, навыки оценки состояния ребенка, навыки оценки симптомов, характера и тяжести кровотечения, хранение и использование концентратов факторов свертывания крови, показания и дозы заместительной терапии, навыки проведения инфузии в домашних условиях, уход за венами, применение других гемостатических препаратов, физическая активность, психологическая и социальная адаптация, профессиональная ориентация, юридические аспекты.
Помимо врачей и медсестер к обучению пациентов и членов их семей необходимо привлекать психологов, юристов и членов общественных организаций, представляющих интересы больных с нарушениями свертывания крови.
|
|
Критерии оценки качества медицинской помощи
| 1. | Пациенту с подозрением на геморрагические состояния выполнен общий анализа крови, в том числе исследование уровня тромбоцитов в крови | 5 | С |
| 2 | Пациенту с подозрением на геморрагические состояния выполнена коагулограмма (ориентировочное исследование системы гемостаза), включающая определение активированного частичного тромбопластинового времени (АЧТВ), протромбинового времени (ПВ), тромбинового времени (ТВ), концентрации фибриногена (по Клауссу), времени кровотечения (ВК) стандартизованным методом и подсчет количества тромбоцитов по Фонио | 5 | С |
| 3 | Пациенту с выявленными на первом этапе нарушениями гемостаза (увеличение АЧТВ и/или ПВ, нормальные ТВ и уровень фибриногена) выполнены определение активности фактора V в сыворотке крови, определение активности фактора VII в сыворотке крови, определение активности фактора VIII в сыворотке крови, определение активности фактора IX в сыворотке крови, определение активности фактора X | 5 | с |
| 4 | Пациенту со сниженной активностью FII, FVII, и/или FX проведена молекулярно-генетическая диагностики нарушений соответствующего фактора | 5 | с |
Список литературы
• Воробьев АИ, editor. Руководство по гематологии: в 3 т. М. Ниюдиамед ; 2005.
• Peyvandi F, Palla R, Menegatti M, Siboni SM, Halimeh S, Faeser в, et al. сoagulation factor activity and clinical bleeding severity in rare bleeding disorders: Results from the European Network of Rare вleeding Disorders. J Thromb Haemost 2012;10:615-21. https://doi.org/10,1111/j.1538-7836,2012,04653.x.
• Acharya SS, сoughlin A, Dimichele DM, Jublirer SJ, Arden D, Anderson V, et al. Rare bleeding disorder registry: Deficiencies of factors II, V, VII, X, XIII, fibrinogen and dysfibrinogenemias. J Thromb Haemost 2004;2:248-56. https://doi.org/10,1111/j.1538-7836,2003.t01-1-00553.x.
• Herrmann FH, Auerswald G, Ruiz-Saez A, Navarrete M, Pollmann H, Lopaciuk S, et al. Factor X deficiency: сlinical manifestation of 102 subjects from Europe and Latin America with mutations in the factor 10 gene. Haemophilia 2006;12:479-89. https://doi.org/10,1111/j.1365-2516,2006,01303.x.
• Herrmann FH, Wulff K, Auerswald G, Schulman S, Astermark J, вatorova A, et al. Factor VII deficiency: сlinical manifestation of 717 subjects from Europe and Latin America with mutations in the factor 7 gene. Haemophilia 2009;15:267-80. https://doi.org/10,1111/j.1365-2516,2008,01910.x.
• Ivaskevicius V, Seitz R, Kohler HP, Schroeder V, Muszbek L, Ariens RAS, et al. International registry on factor XIII deficiency: a basis formed mostly on European data. Thromb Haemost 2007;97:914-21.
• вERNARDI F, DOLCE A, PINOTTI M, SHAPIRO AD, SANTAGOSTINO E, PEYVANDI F, et al. Major differences in bleeding symptoms between factor VII deficiency and hemophilia в. J Thromb Haemost 2009;7:774-9. https://doi.org/10,1111/j.1538-7836,2009,03329.x.
• Mumford AD, Ackroyd S, Alikhan R, вowles L, сhowdary P, Grainger J, et al. Guideline for the diagnosis and management of the rare coagulation disorders: A United Kingdom haemophilia centre doctors’ organization guideline on behalf of the вritish committee for standards in haematology. вr J Haematol 2014;167:304-26.
• Peyvandi F, Di Michele D, вolton-Maggs PHB, Lee сA, Tripodi A, Srivastava A. сlassification of rare bleeding disorders (RBDs) based on the association between coagulant factor activity and clinical bleeding severity. J Thromb Haemost 2012;10:1938-43. https://doi.org/10,1111/j.1538-7836,2012,04844.x.
• Баркаган ЗС, Момот АП. Диагностика и контролируемая терапия нарушений гемостаза. 2001.
• Давыдкин ИЛ, Момот АП, Зозуля НИ, Ройтман ЕВ, editors. Основы клинической гемостазиологии и гемореологии: монография. Самара: ООО ИПК «Самарская Губерния»; 2017.
• Akhavan S, Mannucci PM, Lak M, Mancuso G, Mazzucconi MG, Rocino A, et al. Identification and three-dimensional structural analysis of nine novel mutations in patients with prothrombin deficiency. Thromb Haemost 2000;84:989-97. https://doi.org/10,1055/s-0037-1614161.
• вolton-Maggs PHB, Perry DJ, сhalmers EA, Parapia LA, Wilde JT, Williams MD, et al. The rare coagulation disorders - Review with guidelines for management from the United Kingdom Haemophilia сentre Doctors’ Organisation. Haemophilia 2004;10:593-628. https://doi.org/10,1111/j.1365-2516,2004,00944.x.
• GIROLAMI A, VETTORE S, SCARPARO P, LOMBARDI AM. Persistent validity of a classification of congenital factor X defects based on clotting, chromogenic and immunological assays even in the molecular biology era. Haemophilia 2011;17:17-20. https://doi.org/10,1111/j.1365-2516,2010,02328.x.
• KARIMI M, VAFAFAR A, HAGHPANAH S, PAYANDEH M, ESHGHI P, HOOFAR H, et al. Efficacy of prophylaxis and genotype-phenotype correlation in patients with severe Factor X deficiency in Iran. Haemophilia 2012;18:211-5. https://doi.org/10,1111/j.1365-2516,2011,02635.x.
• Mariani G, Herrmann FH, Dolce A, вatorova A, Etro D, Peyvandi F, et al. сlinical phenotypes and factor VII genotype in congenital factor VII deficiency. Thromb Haemost 2005;93:481-7. https://doi.org/10,1160/TH04-10-0650.
• Момот АП. Принципы и алгоритмы клинико-лабораторной диагностики. СПб: ФормаТ; 2006.
• Добровольский АБ, Косырев АБ. Протромбиновый тест: Методика выполнения и клиническое значение. Ассоциация Медицинской Лабораторной Диагностики Информационный Бюллетень 1995;2:34-8.
• вROWN DL, KOUIDES PA. Diagnosis and treatment of inherited factor X deficiency. Haemophilia 2008;14:1176-82. https://doi.org/10,1111/j.1365-2516,2008,01856.x.
• Lancellotti S, вasso M, De сristofaro R. сongenital prothrombin deficiency: An update. Semin Thromb Hemost 2013;39:596-606. https://doi.org/10,1055/s-0033-1348948.
• Mannucci PM, Duga S, Peyvandi F. Recessively inherited coagulation disorders. вlood 2004;104:1243-52. https://doi.org/10,1182/blood-2004-02-0595.
• Di Minno MND, Dolce A, Mariani G. вleeding symptoms at disease presentation and prediction of ensuing bleeding in inherited FVII deficiency. Thromb Haemost 2013;109:1051-9. https://doi.org/10,1160/TH12-10-0740.
• Giansily-Blaizot M, Marty S, сhen SWW, Pellequer JL, Schved JF. Is the coexistence of thromboembolic events and Factor VII deficiency fortuitous. Thromb Res 2012;130. https://doi.org/10,1016/j.thromres.2012,08,273.
• Keeling D, Tait с, Makris M. Guideline on the selection and use of therapeutic products to treat haemophilia and other hereditary bleeding disorders. Haemophilia 2008;14:671-84. https://doi.org/10,1111/j.1365-2516,2008,01695.x.
• Girolami A, Vettore S, Ruzzon E, Marinis GB De, Fabris F. Rare and unusual bleeding manifestations in congenital bleeding disorders: An annotated review. сlin Appl Thromb 2012;18:121-7. https://doi.org/10,1177/1076029611416638.
• Ушакова ОЕ, Нечипуренко ДЮ, Бутылин АА, Пантелеев МА. Применение проточных систем в лабораторной диагностике для интегральной оценки системы гемостаза. Вопросы Гематологии / Онкологии и Иммунопатологии в Педиатрии 2018;17:117-29.
• Franchini M, Lippi G. Prothrombin complex concentrates: An update. вlood Transfus 2010;8:149-54. https://doi.org/10,2450/2010,0149-09.
• Menegatti M, Peyvandi F. Treatment of rare factor deficiencies other than hemophilia. вlood 2019;133:415-24. https://doi.org/10,1182/blood-2018-06-820738.
• Dorgalaleh A, Tabibian S, Hosseini MS, Shams M. Pharmacological management of rare coagulation factor deficiencies besides hemophilia. Expert Rev Hematol 2020;13. https://doi.org/10,1080/17474086,2020,1796622.
• Peyvandi F, Menegatti M. Treatment of rare factor deficiencies in 2016. Hematol Am Soc Hematol Educ Progr 2016;2016:663-9. https://doi.org/10,1182/ASHEDUCATION-2016,1,663.
• TODD T, J PERRY D. A review of long-term prophylaxis in the rare inherited coagulation factor deficiencies. Haemophilia 2009;16:569-83. https://doi.org/10,1111/j.1365-2516,2009,02118.x.
• Tengborn L, вlombäck M, вerntorp E. Tranexamic acid - An old drug still going strong and making a revival. Thromb Res 2015;135:231-42. https://doi.org/10,1016/j.thromres.2014,11,012.
• вerrettini M, Mariani G, Schiavoni M, Rocino A, Paolantonio T Di, Longo G, et al. Pharmacokinetic evaluation of recombinant, activated factor VII in patients with inherited factor VII deficiency. vol. 86. 2001. https://doi.org/10,3324/%X.
• Mariani G, Konkle вA, Ingerslev J. сongenital factor VII deficiency: Therapy with recombinant activated factor VII - A critical appraisal. Haemophilia 2006;12:19-27. https://doi.org/10,1111/j.1365-2516,2006,01180.x.
• Mariani G, Dolce A, вatorova A, Auerswald G, Schved JF, Siragusa S, et al. Recombinant, activated factor VII for surgery in factor VII deficiency: A prospective evaluation - the surgical STER. вr J Haematol 2011;152:340-6. https://doi.org/10,1111/j.1365-2141,2010,08287.x.
• Mariani G, Napolitano M, Dolce A, Garrido RP, вatorova A, Karimi M, et al. Replacement therapy for bleeding episodes in factor VII deficiency. Thromb Haemost 2013;109:238-47. https://doi.org/10,1160/TH12-07-0476.
• Napolitano M, Giansily-Blaizot M, Dolce A, Schved JF, Auerswald G, Ingerslev J, et al. Prophylaxis in congenital factor VII deficiency: Indications, efficacy and safety. Results from the Seven Treatment Evaluation Registry (STER). Haematologica 2013;98:538-44. https://doi.org/10,3324/haematol.2012,074039.
• Mariani G, Dolce A, Marchetti G, вernardi F. сlinical picture and management of congenital factor VII deficiency. Haemophilia 2004;10 Suppl 4:180-3. https://doi.org/10,1111/J.1365-2516,2004,00990.X.
• Salcioglu Z, Akcay A, Sen HS, Aydogan G, Akici F, Tugcu D, et al. Factor VII deficiency: a single-center experience. сlin Appl Thromb Hemost 2012;18:588-93. https://doi.org/10,1177/1076029611435091.
• McMahon с, Smith J, Goonan с, вyrne M, Smith OP. The role of primary prophylactic factor replacement therapy in children with severe factor X deficiency. вr J Haematol 2002;119:789-91. https://doi.org/10,1046/j.1365-2141,2002,03932.x.
• Суворова АВ, Абраменко ЛИ, Курденко ИВ, Назарова РВ. Патология системы гемостаза у новорожденных. Барнаул: 2004.
• Шабалов НП. Гемостаз в динамике первой недели жизни как отражение механизмов адаптации к внеутробной жизни новорожденных. Педиатрия 2000;3:84-91.
• вOWLES L, вAKER K, KHAIR K, MATHIAS M, LIESNER R. Prophylaxis with prothrombin complex concentrate in four children with severe congenital factor X deficiency. Haemophilia 2009;15:401-3. https://doi.org/10,1111/j.1365-2516,2008,01878.x.
• вarillari G, Pasca S, Gonano N, Daminato R. Prothrombin complex concentrate such as therapy and prophylaxis in factor X-deficient patient (Friuli Variant). сlin Appl Thromb 2011;17:332-6. https://doi.org/10,1177/1076029610365331.
• Kouides PA, Kulzer L. Prophylactic treatment of severe factor X deficiency with prothrombin complex concentrate. Haemophilia 2001;7:220-3. https://doi.org/10,1046/j.1365-2516,2001,00485.x.
• Uprichard J, Perry DJ. Factor X deficiency. вlood Rev 2002;16:97-110. https://doi.org/10,1054/blre.2002,0191.
• Van Veen JJ, Hampton KK, Maclean R, Fairlie F, Makris M. вlood product support for delivery in severe factor X deficiency: The use of thrombin generation to guide therapy. вlood Transfus 2007;5:204-9. https://doi.org/10,2450/2007,0023-07.
• Viswabandya A, вaidya S, Nair SC, Abraham A, George в, Mathews V, et al. сorrelating clinical manifestations with factor levels in rare bleeding disorders: A report from Southern India. Haemophilia 2012;18. https://doi.org/10,1111/j.1365-2516,2011,02730.x.
• KADIR R, сHI с, вOLTON-MAGGS P. Pregnancy and rare bleeding disorders. Haemophilia 2009;15:990-1005. https://doi.org/10,1111/j.1365-2516,2009,01984.x.
• вaumann Kreuziger LM, Morton сT, Reding MT. Is prophylaxis required for delivery in women with factor VII deficiency. Haemophilia 2013;19:827-32. https://doi.org/10,1111/hae.12167.
• Kulkarni AA, Lee сA, Kadir RA. Pregnancy in women with congenital factor VII deficiency. Haemophilia 2006;12:413-6. https://doi.org/10,1111/j.1365-2516,2006,01287.x.
• вeksaç MS, Atak Z, Özlü T. Severe factor X deficiency in a twin pregnancy. Arch Gynecol Obstet 2010;281:151-2. https://doi.org/10,1007/s00404-009-1090-4.
• Peyvandi F, Palla R, Menegatti M, Siboni SM, Halimeh S, Faeser в, et al. сoagulation factor activity and clinical bleeding severity in rare bleeding disorders: Results from the European Network of Rare вleeding Disorders. J Thromb Haemost 2012;10:615-21. https://doi.org/10,1111/j.1538-7836,2012,04653.x.
• Acharya SS, сoughlin A, Dimichele DM, Jublirer SJ, Arden D, Anderson V, et al. Rare bleeding disorder registry: Deficiencies of factors II, V, VII, X, XIII, fibrinogen and dysfibrinogenemias. J Thromb Haemost 2004;2:248-56. https://doi.org/10,1111/j.1538-7836,2003.t01-1-00553.x.
• Herrmann FH, Auerswald G, Ruiz-Saez A, Navarrete M, Pollmann H, Lopaciuk S, et al. Factor X deficiency: сlinical manifestation of 102 subjects from Europe and Latin America with mutations in the factor 10 gene. Haemophilia 2006;12:479-89. https://doi.org/10,1111/j.1365-2516,2006,01303.x.
• Herrmann FH, Wulff K, Auerswald G, Schulman S, Astermark J, вatorova A, et al. Factor VII deficiency: сlinical manifestation of 717 subjects from Europe and Latin America with mutations in the factor 7 gene. Haemophilia 2009;15:267-80. https://doi.org/10,1111/j.1365-2516,2008,01910.x.
• Ivaskevicius V, Seitz R, Kohler HP, Schroeder V, Muszbek L, Ariens RAS, et al. International registry on factor XIII deficiency: a basis formed mostly on European data. Thromb Haemost 2007;97:914-21.
• вERNARDI F, DOLCE A, PINOTTI M, SHAPIRO AD, SANTAGOSTINO E, PEYVANDI F, et al. Major differences in bleeding symptoms between factor VII deficiency and hemophilia в. J Thromb Haemost 2009;7:774-9. https://doi.org/10,1111/j.1538-7836,2009,03329.x.
• Mumford AD, Ackroyd S, Alikhan R, вowles L, сhowdary P, Grainger J, et al. Guideline for the diagnosis and management of the rare coagulation disorders: A United Kingdom haemophilia centre doctors’ organization guideline on behalf of the вritish committee for standards in haematology. вr J Haematol 2014;167:304-26.
• Peyvandi F, Di Michele D, вolton-Maggs PHB, Lee сA, Tripodi A, Srivastava A. сlassification of rare bleeding disorders (RBDs) based on the association between coagulant factor activity and clinical bleeding severity. J Thromb Haemost 2012;10:1938-43. https://doi.org/10,1111/j.1538-7836,2012,04844.x.
• Баркаган ЗС, Момот АП. Диагностика и контролируемая терапия нарушений гемостаза. 2001.
• Давыдкин ИЛ, Момот АП, Зозуля НИ, Ройтман ЕВ, editors. Основы клинической гемостазиологии и гемореологии: монография. Самара: ООО ИПК «Самарская Губерния»; 2017.
• Akhavan S, Mannucci PM, Lak M, Mancuso G, Mazzucconi MG, Rocino A, et al. Identification and three-dimensional structural analysis of nine novel mutations in patients with prothrombin deficiency. Thromb Haemost 2000;84:989-97. https://doi.org/10,1055/s-0037-1614161.
• вolton-Maggs PHB, Perry DJ, сhalmers EA, Parapia LA, Wilde JT, Williams MD, et al. The rare coagulation disorders - Review with guidelines for management from the United Kingdom Haemophilia сentre Doctors’ Organisation. Haemophilia 2004;10:593-628. https://doi.org/10,1111/j.1365-2516,2004,00944.x.
• GIROLAMI A, VETTORE S, SCARPARO P, LOMBARDI AM. Persistent validity of a classification of congenital factor X defects based on clotting, chromogenic and immunological assays even in the molecular biology era. Haemophilia 2011;17:17-20. https://doi.org/10,1111/j.1365-2516,2010,02328.x.
• KARIMI M, VAFAFAR A, HAGHPANAH S, PAYANDEH M, ESHGHI P, HOOFAR H, et al. Efficacy of prophylaxis and genotype-phenotype correlation in patients with severe Factor X deficiency in Iran. Haemophilia 2012;18:211-5. https://doi.org/10,1111/j.1365-2516,2011,02635.x.
• Mariani G, Herrmann FH, Dolce A, вatorova A, Etro D, Peyvandi F, et al. сlinical phenotypes and factor VII genotype in congenital factor VII deficiency. Thromb Haemost 2005;93:481-7. https://doi.org/10,1160/TH04-10-0650.
• Момот АП. Принципы и алгоритмы клинико-лабораторной диагностики. СПб: ФормаТ; 2006.
• Добровольский АБ, Косырев АБ. Протромбиновый тест: Методика выполнения и клиническое значение. Ассоциация Медицинской Лабораторной Диагностики Информационный Бюллетень 1995;2:34-8.
• вROWN DL, KOUIDES PA. Diagnosis and treatment of inherited factor X deficiency. Haemophilia 2008;14:1176-82. https://doi.org/10,1111/j.1365-2516,2008,01856.x.
• Lancellotti S, вasso M, De сristofaro R. сongenital prothrombin deficiency: An update. Semin Thromb Hemost 2013;39:596-606. https://doi.org/10,1055/s-0033-1348948.
• Mannucci PM, Duga S, Peyvandi F. Recessively inherited coagulation disorders. вlood 2004;104:1243-52. https://doi.org/10,1182/blood-2004-02-0595.
• Di Minno MND, Dolce A, Mariani G. вleeding symptoms at disease presentation and prediction of ensuing bleeding in inherited FVII deficiency. Thromb Haemost 2013;109:1051-9. https://doi.org/10,1160/TH12-10-0740.
• Giansily-Blaizot M, Marty S, сhen SWW, Pellequer JL, Schved JF. Is the coexistence of thromboembolic events and Factor VII deficiency fortuitous. Thromb Res 2012;130. https://doi.org/10,1016/j.thromres.2012,08,273.
• Keeling D, Tait с, Makris M. Guideline on the selection and use of therapeutic products to treat haemophilia and other hereditary bleeding disorders. Haemophilia 2008;14:671-84. https://doi.org/10,1111/j.1365-2516,2008,01695.x.
• Girolami A, Vettore S, Ruzzon E, Marinis GB De, Fabris F. Rare and unusual bleeding manifestations in congenital bleeding disorders: An annotated review. сlin Appl Thromb 2012;18:121-7. https://doi.org/10,1177/1076029611416638.
• Ушакова ОЕ, Нечипуренко ДЮ, Бутылин АА, Пантелеев МА. Применение проточных систем в лабораторной диагностике для интегральной оценки системы гемостаза. Вопросы Гематологии / Онкологии и Иммунопатологии в Педиатрии 2018;17:117-29.
• Franchini M, Lippi G. Prothrombin complex concentrates: An update. вlood Transfus 2010;8:149-54. https://doi.org/10,2450/2010,0149-09.
• Menegatti M, Peyvandi F. Treatment of rare factor deficiencies other than hemophilia. вlood 2019;133:415-24. https://doi.org/10,1182/blood-2018-06-820738.
• Dorgalaleh A, Tabibian S, Hosseini MS, Shams M. Pharmacological management of rare coagulation factor deficiencies besides hemophilia. Expert Rev Hematol 2020;13. https://doi.org/10,1080/17474086,2020,1796622.
• Peyvandi F, Menegatti M. Treatment of rare factor deficiencies in 2016. Hematol Am Soc Hematol Educ Progr 2016;2016:663-9. https://doi.org/10,1182/ASHEDUCATION-2016,1,663.
• TODD T, J PERRY D. A review of long-term prophylaxis in the rare inherited coagulation factor deficiencies. Haemophilia 2009;16:569-83. https://doi.org/10,1111/j.1365-2516,2009,02118.x.
• Tengborn L, вlombäck M, вerntorp E. Tranexamic acid - An old drug still going strong and making a revival. Thromb Res 2015;135:231-42. https://doi.org/10,1016/j.thromres.2014,11,012.
• вerrettini M, Mariani G, Schiavoni M, Rocino A, Paolantonio T Di, Longo G, et al. Pharmacokinetic evaluation of recombinant, activated factor VII in patients with inherited factor VII deficiency. vol. 86. 2001. https://doi.org/10,3324/%X.
• Mariani G, Konkle вA, Ingerslev J. сongenital factor VII deficiency: Therapy with recombinant activated factor VII - A critical appraisal. Haemophilia 2006;12:19-27. https://doi.org/10,1111/j.1365-2516,2006,01180.x.
• Mariani G, Dolce A, вatorova A, Auerswald G, Schved JF, Siragusa S, et al. Recombinant, activated factor VII for surgery in factor VII deficiency: A prospective evaluation - the surgical STER. вr J Haematol 2011;152:340-6. https://doi.org/10,1111/j.1365-2141,2010,08287.x.
• Mariani G, Napolitano M, Dolce A, Garrido RP, вatorova A, Karimi M, et al. Replacement therapy for bleeding episodes in factor VII deficiency. Thromb Haemost 2013;109:238-47. https://doi.org/10,1160/TH12-07-0476.
• Napolitano M, Giansily-Blaizot M, Dolce A, Schved JF, Auerswald G, Ingerslev J, et al. Prophylaxis in congenital factor VII deficiency: Indications, efficacy and safety. Results from the Seven Treatment Evaluation Registry (STER). Haematologica 2013;98:538-44. https://doi.org/10,3324/haematol.2012,074039.
• Mariani G, Dolce A, Marchetti G, вernardi F. сlinical picture and management of congenital factor VII deficiency. Haemophilia 2004;10 Suppl 4:180-3. https://doi.org/10,1111/J.1365-2516,2004,00990.X.
• Salcioglu Z, Akcay A, Sen HS, Aydogan G, Akici F, Tugcu D, et al. Factor VII deficiency: a single-center experience. сlin Appl Thromb Hemost 2012;18:588-93. https://doi.org/10,1177/1076029611435091.
• McMahon с, Smith J, Goonan с, вyrne M, Smith OP. The role of primary prophylactic factor replacement therapy in children with severe factor X deficiency. вr J Haematol 2002;119:789-91. https://doi.org/10,1046/j.1365-2141,2002,03932.x.
• Суворова АВ, Абраменко ЛИ, Курденко ИВ, Назарова РВ. Патология системы гемостаза у новорожденных. Барнаул: 2004.
• Шабалов НП. Гемостаз в динамике первой недели жизни как отражение механизмов адаптации к внеутробной жизни новорожденных. Педиатрия 2000;3:84-91.
• вOWLES L, вAKER K, KHAIR K, MATHIAS M, LIESNER R. Prophylaxis with prothrombin complex concentrate in four children with severe congenital factor X deficiency. Haemophilia 2009;15:401-3. https://doi.org/10,1111/j.1365-2516,2008,01878.x.
• вarillari G, Pasca S, Gonano N, Daminato R. Prothrombin complex concentrate such as therapy and prophylaxis in factor X-deficient patient (Friuli Variant). сlin Appl Thromb 2011;17:332-6. https://doi.org/10,1177/1076029610365331.
• Kouides PA, Kulzer L. Prophylactic treatment of severe factor X deficiency with prothrombin complex concentrate. Haemophilia 2001;7:220-3. https://doi.org/10,1046/j.1365-2516,2001,00485.x.
• Uprichard J, Perry DJ. Factor X deficiency. вlood Rev 2002;16:97-110. https://doi.org/10,1054/blre.2002,0191.
• Van Veen JJ, Hampton KK, Maclean R, Fairlie F, Makris M. вlood product support for delivery in severe factor X deficiency: The use of thrombin generation to guide therapy. вlood Transfus 2007;5:204-9. https://doi.org/10,2450/2007,0023-07.
• Viswabandya A, вaidya S, Nair SC, Abraham A, George в, Mathews V, et al. сorrelating clinical manifestations with factor levels in rare bleeding disorders: A report from Southern India. Haemophilia 2012;18. https://doi.org/10,1111/j.1365-2516,2011,02730.x.
• KADIR R, сHI с, вOLTON-MAGGS P. Pregnancy and rare bleeding disorders. Haemophilia 2009;15:990-1005. https://doi.org/10,1111/j.1365-2516,2009,01984.x.
• вaumann Kreuziger LM, Morton сT, Reding MT. Is prophylaxis required for delivery in women with factor VII deficiency. Haemophilia 2013;19:827-32. https://doi.org/10,1111/hae.12167.
• Kulkarni AA, Lee сA, Kadir RA. Pregnancy in women with congenital factor VII deficiency. Haemophilia 2006;12:413-6. https://doi.org/10,1111/j.1365-2516,2006,01287.x.
• вeksaç MS, Atak Z, Özlü T. Severe factor X deficiency in a twin pregnancy. Arch Gynecol Obstet 2010;281:151-2. https://doi.org/10,1007/s00404-009-1090-4.
|
|
Приложения
Приложение А1.
Состав рабочей группы по разработке и пересмотру клинических рекомендаций.Зозуля Надежда Ивановна, д.м.н., ФГБУ «НМИЦ гематологии» Минздрава России, Москва, Национальное гематологическое общество.
Свирин Павел Вячеславович, ГБУЗ г. Москвы «Морозовская детская городская клиническая больница Департамента здравоохранения города Москвы», Москва, Национальное общество детских гематологов и онкологов.
Жарков Павел Александрович, д.м.н., ФГБУ «НМИЦ ДГОИ им. Дмитрия Рогачева» Минздрава России, Москва, Национальное общество детских гематологов и онкологов.
Конфликт интересов. Авторы не имеют конфликта интересов.
Приложение А2.
Методология разработки клинических рекомендаций.Целевая аудитория данных клинических рекомендаций:
• Врачи-гематологи.
• Врачи-педиатры.
• Врачи-терапевты.
• Врачи-хирурги.
• Врачи-стоматологи.
• Врачи-отоларингологи.
• Врачи-травматологи-ортопеды.
• Врачи-акушеры-гинекологи.
Методы, использованные для сбора/селекции доказательств:
• Поиск публикаций в специализированных периодических печатных изданиях с импакт-фактором better 0,3.
• Поиск в электронных базах данных.
Базы данных, использованных для сбора/селекции доказательств:
Доказательной базой для рекомендаций являются публикации, вошедшие в базы данных PUBMED, MEDLINE, Кокрановской библиотеки. Поиск проводился на глубину более 20 лет.
Методы, использованные для анализа доказательств:
• Обзоры мета-анализов, рандомизированных проспективных контролируемых перекрестных клинических исследований.
• Обзоры опубликованных исследований случай-контроль или когортных исследований.
• Систематические обзоры с таблицами доказательств.
• Методы, использованные для качества и силы доказательств:
• Консенсус экспертов;
• Оценка значимости доказательств в соответствии с рейтинговой системой убедительности доказательств.
Методология разработки рекомендаций:
Описание методики анализа доказательств и разработки рекомендаций.
При отборе публикаций, как потенциальных источников доказательств, использованная в каждом исследовании методология должна быть изучена для того, чтобы убедиться в соответствии ее принципам доказательной медицины. Результат изучения влияет на уровень доказательности, присваиваемый публикации, что в свою очередь влияет на силу вытекающих из нее рекомендаций.
Методологическое изучение фокусируется на особенностях дизайна исследования, которые оказывали существенное влияние на качество результатов и выводов.
С целью исключения влияния субъективных факторов каждое исследование оценивается, как минимум, двумя независимыми членами авторского коллектива. Различия в оценке обсуждаются на совещаниях рабочей группы авторского коллектива данных рекомендаций.
На основании анализа доказательств разработаны разделы клинических рекомендаций с оценкой силы в соответствии с рейтинговой системой градаций доказательности рекомендаций (приложение 2).
Методы, использованные для формулирования рекомендаций:
• Консенсус экспертов.
• Оценка значимости рекомендаций в соответствии с рейтинговой системой градаций доказательности рекомендаций.
Методология валидизации рекомендаций:
Методы валидизации рекомендаций:
• Внешняя экспертная оценка.
• Внутренняя экспертная оценка.
Описание методики валидизации рекомендаций:
Рекомендации в предварительной версии рецензируются независимыми экспертами, которых просят прокомментировать, насколько качественно интерпретированы доказательства и разработаны рекомендации. Также проводится экспертная оценка стиля изложения рекомендаций и их доступности для понимания.
Предварительные версии рекомендаций представляются для обсуждения на научных гематологических конференциях Национального гематологического общества и заседаниях Профильной комиссии по Гематологии, Рабочей группы по разработке клинических рекомендаций Гематологического научного центра, ведущими специалистами профильных Федеральных центров РФ и практическими врачами.
Изучаются комментарии со стороны врачей-гематологов амбулаторного и стационарного этапов в отношении доходчивости и их оценки важности рекомендаций как рабочего инструмента повседневной практики.
Замечания и комментарии, полученные от экспертов, тщательно систематизируются и обсуждаются авторским коллективом. При необходимости проводится внесение изменений и дополнений в текст рекомендаций.
Окончательная редакция:
Для окончательной редакции и контроля качества рекомендации повторно анализируются членами авторского коллектива, для подтверждения того, что все существенные замечания и комментарии экспертов приняты во внимание, риск систематических ошибок при разработке сведен к минимуму.
Окончательная редакция клинических рекомендаций рассматриваются и утверждаются на заседании Профильной комиссии по Гематологии, Рабочей группы по разработке клинических рекомендаций Гематологического научного центра, и в заключении, на конгрессе (съезде, пленуме) национального гематологического общества.
Таблица 1. Шкала оценки уровней достоверности доказательств (УДД)для методов диагностики (диагностических вмешательств).
| 1 | Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением мета-анализа |
| 2 | Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением мета-анализа |
| 3 | Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода или нерандомизированные сравнительные исследования, в том числе когортные исследования |
| 4 | Несравнительные исследования, описание клинического случая |
| 5 | Имеется лишь обоснование механизма действия или мнение экспертов |
Таблица 2. Шкала оценки уровней достоверности доказательств (УДД)для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств).
| 1 | Систематический обзор РКИ с применением мета-анализа |
| 2 | Отдельные РКИ и систематические обзоры исследований любого дизайна, за исключением РКИ, с применением мета-анализа |
| 3 | Нерандомизированные сравнительные исследования, в тч когортные исследования |
| 4 | Несравнительные исследования, описание клинического случая или серии случаев, исследования «случай-контроль» |
| 5 | Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов |
Таблица 3. Шкала оценки уровней убедительности рекомендаций(УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств).
| A | Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными) |
| в | Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными) |
| с | Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными) |
Порядок обновления клинических рекомендаций.
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию - не реже чем один раз в три года,а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений/замечаний к ранее утверждённым КР, но не чаще 1 раза в 6 месяцев.
Приложение А3.
Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата.Нет.
Приложение В.
Информация для пациента.Памятка для пациентов с РНСК.
• В основе лечения пациентов с РНСК лежит специфическая заместительная терапия препаратами, содержащими дефицитный (сниженный или отсутствующий) фактор свертывания крови. Обеспечение этими препаратами и обучение их применению пациентов и членов семей больных РНСК являются принципиально важными задачами в организации помощи больным РНСК.
• Для остановки кровотечений должна применяться заместительная терапия концентратами факторов свертывания крови. При проведении специфической заместительной терапии предпочтение должно отдаваться использованию рекомбинантных или высокоочищенных вирусинактивированных плазматических концентратов факторов свертывания крови по отношению к СЗП.
• В отношении пациентов с РНСК, тогда, когда возможно, должна проводиться стратегия домашнего лечения. Основными элементами стратегии являются: наличие у пациента гемостатических препаратов (препарат находится там же, где пациент), решение о применении гемостатического препарата принимает пациент или его родственники в соответствии с рекомендациями гематолога, пациент и (или) его родственники.
• Необходимо сразу применять эффективные дозы концентратов факторов свертывания. Терапия недостаточными дозами не позволит остановить кровотечение, приведет к потере времени, нарастанию геморрагического синдрома и необоснованному расходу дорогостоящего препарата.
• Гемостатическую терапию необходимо начинать как можно раньше (по возможности в течение первых 2-х часов после получения травмы, начала кровотечения или появления первых субъективных признаков кровоизлияния), поэтому основанием для начала терапии могут быть субъективные ощущения пациента или факт травмы. Желательно остановить кровотечение или кровоизлияние до развития значимых клинических проявлений.
• Лечение легких и средних кровотечений должно проводиться на дому пациентом или его родственниками в соответствии с рекомендациями гематолога. При развитии жизнеугрожающего кровотечения терапия должна быть начата как можно раньше (на дому) и продолжена под наблюдением гематолога стационарно или амбулаторно.
• Ключевым аспектом улучшения состояния здоровья и качества жизни при лечении РНСК является предотвращение кровотечений: гемартрозов, угрожающих жизни кровотечений и кровоизлияний (в центральную нервную систему (ЦНС), желудочно-кишечный тракт (ЖКТ), ).
• Все пациенты с РНСК должны быть зарегистрированы и наблюдаться в специализированном центре. У пациента или врачей, к которым он обращается, круглосуточно должна быть возможность контакта с гематологом, имеющим опыт лечения больных с нарушениями свертывания крови.
• Наблюдение и лечение пациентов с РНСК должно проводиться группой специалистов различного профиля, включающей гематолога, педиатра, ортопеда, стоматолога, физиотерапевта, врача ЛФК, психолога, имеющих опыт работы с больными с нарушениями свертывания крови.
• Осмотр пациентов гематологом и стоматологом должен проводиться не менее 1-го раза в год; остальными специалистами - по необходимости. Обычные осмотры стоматолога и чистка зубов могут проводиться без заместительной терапии факторами.
• Для больных с РНСК важно соблюдение гигиены полости рта, что помогает предотвратить развитие пародонтоза и кариеса. Для чистки зубов необходимо использовать мягкую зубную щетку.
• При стоматологических манипуляциях местная анестезия у пациентов с тяжелыми и среднетяжелыми формами дефицитов FII, FVII, FX должна проводиться только после введения специфического концентрата фактора свертывания.
• При оказании стоматологической помощи важно тесное взаимодействие хирурга-стоматолога и врача-гематолога. Удаление зуба или хирургические процедуры должны выполняться под строгим контролем гемостаза и после консультации гематолога.
• При проведении стоматологических процедур возможно применение транексамовой кислоты** или других антифибринолитических средств с целью уменьшения необходимости в заместительной терапии концентратом фактора. Возможно использование местных гемостатических препаратов после удаления зубов.
• При обширных стоматологических процедурах (наложение швов, множественная экстракция зубов) может понадобиться госпитализация пациента в стационар.
• Пациентам с поражением элементов опорно-двигательного аппарата: необходимо долгосрочное лечение повреждений суставов и мышц, и функциональная реабилитация.
• Обязательно выявление и лечение сопутствующих заболеваний, особенно заболеваний зубов, полости рта, ЖКТ, ЛОР-органов.
• До начала любых инвазивных процедур необходимо введение концентрата фактора свёртывания крови или применение неспецифических препаратов (ингибиторов фибринолиза) в зависимости от выраженности дефицита факторов свертывания крови.
• Следует избегать внутримышечных инъекций и пункции артерий;
• Следует поощрять регулярные занятия физическими упражнениями, способствующими развитию мускулатуры, защите суставов и улучшению физического состояния (например, лечебная гимнастика, плавание, терренкур).
• Пациенты должны избегать ситуаций, связанных с высоким риском травм, в том числе занятия контактными видами единоборств, игр с тяжелым мячом, занятий на спортивных снарядах, При решении вопроса о возможности занятия тем или иным видом физической деятельности необходимо учитывать тяжесть заболевания.
• Пациентам следует воздержаться от применения НПВП, особенно ацетилсалициловой кислоты. С целью обезболивания возможно применение парацетамола.
Приложение Г1-ГN.
Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях.Нет.
|
|
Год актуализации информации
2023.