МКБ-10 коды
|
|
Вступление
Кодирование по Международной статистической классификации болезней и проблем, связанных со здоровьем: D66, D67.
Год утверждения (частота пересмотра): 2023.
Возрастная категория: Взрослые , Дети.
Пересмотр не позднее: 2025.
ID: 127.
Разработчик клинической рекомендации.
• Национальное общество детских гематологов, онкологов.
• Национальное гематологическое общество.
Одобрено Научно-практическим Советом Минздрава РФ.
Год утверждения (частота пересмотра): 2023.
Возрастная категория: Взрослые , Дети.
Пересмотр не позднее: 2025.
ID: 127.
Разработчик клинической рекомендации.
• Национальное общество детских гематологов, онкологов.
• Национальное гематологическое общество.
Одобрено Научно-практическим Советом Минздрава РФ.
|
|
 Список сокращений
Список сокращений
АЧТВ - активированное частичное тромбопластиновое время.
АИКК - антиингибиторный коагулянтный комплекс.
БЕ - Бетезда Единица.
ГА - гемофилия А.
ГВ - гемофилия В.
ДВ - день введения.
ЖКТ - желудочно-кишечный тракт.
ИИТ - индукция иммунологической толерантности.
КТ - компьютерная томография.
МРТ - магнитно-резонансная томография.
НПВП - нестероидные противовоспалительные и противоревматические препараты (М01А по АТХ классификации).
ПВ - протромбиновое время.
ТВ - тромбиновое время.
FVIII - фактор свертывания крови VIII.
FIX - фактор свертывания крови IX.
FXI - фактор свертывания крови XI.
FXII - фактор свертывания крови XII.
ЦНС - центральная нервная система.
ЦОГ-2 - циклооксигеназа-2.
АИКК - антиингибиторный коагулянтный комплекс.
БЕ - Бетезда Единица.
ГА - гемофилия А.
ГВ - гемофилия В.
ДВ - день введения.
ЖКТ - желудочно-кишечный тракт.
ИИТ - индукция иммунологической толерантности.
КТ - компьютерная томография.
МРТ - магнитно-резонансная томография.
НПВП - нестероидные противовоспалительные и противоревматические препараты (М01А по АТХ классификации).
ПВ - протромбиновое время.
ТВ - тромбиновое время.
FVIII - фактор свертывания крови VIII.
FIX - фактор свертывания крови IX.
FXI - фактор свертывания крови XI.
FXII - фактор свертывания крови XII.
ЦНС - центральная нервная система.
ЦОГ-2 - циклооксигеназа-2.
Термины и определения
Гемартроз. Кровоизлияние в полость сустава.
Гематома. Ограниченное скопление крови при закрытых и открытых повреждениях органов и тканей с разрывом сосудов, в результате чего образуется полость, содержащая жидкую или свернувшуюся кровь.
Гематурия. Наличие эритроцитов в моче сверх физиологических норм.
Гемостаз. Система свертывания крови.
Гемостатическая терапия. Терапия, направленная на остановку кровотечения.
Гемофилия А. Наследственный дефицит фактора свертывания крови VIII.
Гемофилия В. Наследственный дефицит фактора свертывания крови IX.
Ингибиторы. Антитела, вырабатывающиеся на экзогенно введенный белок.
Коагулограмма (ориентировочное исследование системы гемостаза). Исследование свертывающей системы крови.
Коагулопатия. Нарушение свертывания крови.
Препараты шунтирующего действия. Отдельные препараты из группы факторов свертывания крови (B02BD факторы свертывания крови по АТХ классификации) - антиингибиторный коагулянтный комплекс** и эптаког альфа (активированный)**.
Фактор свертывания крови. Белок, содержащийся в плазме крови и тромбоцитах и обеспечивающий свёртывание крови.
Гематома. Ограниченное скопление крови при закрытых и открытых повреждениях органов и тканей с разрывом сосудов, в результате чего образуется полость, содержащая жидкую или свернувшуюся кровь.
Гематурия. Наличие эритроцитов в моче сверх физиологических норм.
Гемостаз. Система свертывания крови.
Гемостатическая терапия. Терапия, направленная на остановку кровотечения.
Гемофилия А. Наследственный дефицит фактора свертывания крови VIII.
Гемофилия В. Наследственный дефицит фактора свертывания крови IX.
Ингибиторы. Антитела, вырабатывающиеся на экзогенно введенный белок.
Коагулограмма (ориентировочное исследование системы гемостаза). Исследование свертывающей системы крови.
Коагулопатия. Нарушение свертывания крови.
Препараты шунтирующего действия. Отдельные препараты из группы факторов свертывания крови (B02BD факторы свертывания крови по АТХ классификации) - антиингибиторный коагулянтный комплекс** и эптаког альфа (активированный)**.
Фактор свертывания крови. Белок, содержащийся в плазме крови и тромбоцитах и обеспечивающий свёртывание крови.
Описание
Гемофилия - это сцепленное с Х-хромосомой врожденное нарушение плазменного гемостаза, возникающее в результате дефицита или отсутствия фактора свертывания крови VIII (FVIII) - гемофилия А или фактора свертывания крови IX (FIX) - гемофилия В.
Причины
Гемофилия передается по Х-сцепленному рецессивному пути наследования. Примерно у 70% больных имеется положительный семейный анамнез по заболеванию. Причиной гемофилии являются мутации гена, кодирующие FVIII (Xq28), или гена, кодирующего FIX (Xq27). В 30-35% случаев возможны спорадические мутации без наличия семейного анамнеза заболевания.
Эпидемиология
Распространенность гемофилии в общем популяции составляет 1:10 000 населения. Гемофилия А (ГА) встречается чаще, чем гемофилия В (ГВ), и составляет 80-85% общего числа случаев. Подавляющее большинство больных гемофилией - мужчины. Известны единичные случаи гемофилии у женщин при наследовании гена одновременно от отца (больной гемофилией) и от матери (носитель гена), либо у женщины с мутацией гена на одной хромосоме, когда ген на другой не активен (болезнь Шерешевского-Тёрнера ). У некоторых женщин, являющихся носительницами мутаций генов FVIII или FIX, также могут быть клинические проявления гемофилии [1].
D67- наследственный дефицит фактора IX.
1,4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем.
D66 - наследственный дефицит фактора VIII.D67- наследственный дефицит фактора IX.
Классификация
1,5 Классификация заболевания или состояния (группы заболеваний или состояний).
Классификация гемофилии по степени тяжести основана на определении активности FVIII и FIX (табл.1) [1-3].Таблица 1. Классификация гемофилии по степени тяжести.
| Тяжелая | < 1% | Дебют заболевания в раннем детском возрасте: рецидивирующий геморрагический синдром преимущественно гематомного типа (преимущественно спонтанные кровотечения) |
| Средней тяжести | 1-5% | |
| Легкая | >5% | Кровотечения возникают после травм или при проведении инвазивных вмешательств |
Около 60-70% всех диагностированных случаев гемофилии составляют тяжелые формы заболевания, для которых характерны спонтанные геморрагические эпизоды (преимущественно гемартрозы и гематомы мягких тканей различных локализаций). Степень тяжести нарушений свертывания крови и клинических проявлений при гемофилии зависит, как правило, от уровня активности фактора в крови, однако в клинической практике не всегда существует прямая корреляция между лабораторным и клиническим фенотипами заболевания.
Клиническая картина
Основное проявление гемофилии - кровотечения и кровоизлияния, возникающие спонтанно или вследствие травмы (табл. 2). ГА и ГВ имеют схожую клиническую картину [1,3].
Таблица 2. Клинические проявления гемофилии.
Для тяжелой формы гемофилии характерно появление геморрагического синдрома на первом году жизни с начала активного периода у ребенка (гематомы мягких тканей, посттравматические кровотечения из слизистых, гемартрозы). Поражаются в основном крупные суставы: коленные, голеностопные, локтевые и тазобедренные.
Гемофилия средней тяжести имеет сходные проявления. Первые признаки, как правило, развиваются после года. У пациентов с активностью факторов более 2% реже возникают кровоизлияния в суставы, забрюшинные гематомы, гематурии. Наиболее типичны посттравматические гематомы и длительные кровотечения, особенно при травмах слизистых оболочек.
Легкая гемофилия может никак не проявляться на протяжении всей жизни. Геморрагический синдром обычно возникает вследствие значительных травм или при хирургическом лечении. Поражение опорно-двигательного аппарата встречается чрезвычайно редко.
Таблица 2. Клинические проявления гемофилии.
| Типичные | |
| Гемартрозы крупных суставов | 70-90 |
| Гематомы (кровоизлияния в мышцы/мягкие ткани) | 20-40 |
| Кровотечения из слизистых (носовые, десневые, луночковые) | 10 |
| Гематурии | 5-10 |
| Жизнеугрожающие | |
| В ЦНС | 5 |
| В ЖКТ | |
| В области шеи/горла | |
| Забрюшинные гематомы | |
Для тяжелой формы гемофилии характерно появление геморрагического синдрома на первом году жизни с начала активного периода у ребенка (гематомы мягких тканей, посттравматические кровотечения из слизистых, гемартрозы). Поражаются в основном крупные суставы: коленные, голеностопные, локтевые и тазобедренные.
Гемофилия средней тяжести имеет сходные проявления. Первые признаки, как правило, развиваются после года. У пациентов с активностью факторов более 2% реже возникают кровоизлияния в суставы, забрюшинные гематомы, гематурии. Наиболее типичны посттравматические гематомы и длительные кровотечения, особенно при травмах слизистых оболочек.
Легкая гемофилия может никак не проявляться на протяжении всей жизни. Геморрагический синдром обычно возникает вследствие значительных травм или при хирургическом лечении. Поражение опорно-двигательного аппарата встречается чрезвычайно редко.
|
|
Диагностика
Для установления диагноза гемофилии у пациента с наличием геморрагического синдрома в анамнезе или при отягощенном семейном анамнезе используются критерии диагноза гемофилии (диагноз устанавливается при наличии как минимум двух из трех критериев) [1,3]:
• отсутствие приобретенных коагулопатий;
• снижение активности FVIII/FIX ниже 50%;
• наличие мутаций генов FVIII или FIX.
• Всем пациентам с подозрением на гемофилию рекомендуется сбор анамнеза и жалоб при заболеваниях органов кроветворения и крови [1,3].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии. При сборе анамнеза заболевания и семейного анамнеза пациента выяснять наличие проявлений геморрагического синдрома - жалоб на легко появляющиеся экхимозы и гематомы в раннем детстве; возникновение спонтанных кровотечений (особенно в суставы, мышцы и мягкие ткани); длительных кровотечений после травм или хирургического вмешательства.
Данные семейного анамнеза примерно у 2/3 больных содержат указания на геморрагические проявления у близких родственников по женской линии (у мужчин, реже у женщин). Данные персонального анамнеза могут содержать информацию о геморрагических проявлениях у пациента. При сборе анамнеза заболевания необходимо обращать внимание на наличие геморрагических проявлений в неонатальном периоде в виде кефалогематом, внутричерепных кровоизлияний, кровоточивости и длительном заживлении пупочной ранки; у грудных детей - экхимозов, не связанных со значимой травмой, гематом мягких тканей после незначительных ушибов или спонтанных. У некоторых детей кровотечения могут отсутствовать на первом году жизни до тех пор, пока ребенок не начнет ходить [4,5]. Важно обращать внимание на несоответствие выраженности геморрагических проявлений тяжести предшествовавшей травмы, на рецидивы кровотечений после первичной остановки, не связанные с повторной травмой, массивные и (или) множественные гематомы, системность геморрагических проявлений (проявления различной локализации), «спонтанные геморрагические проявления». При легкой форме гемофилии кровотечения могут отсутствовать до первой травмы или хирургического вмешательства. Сбор жалоб и анамнеза позволит определить объем обследования пациента.
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
Комментарии. Необходимо обращать внимание на наличие кожного геморрагического синдрома различной выраженности в виде множественных экхимозов и гематом, возможных при тяжёлой и среднетяжелой форме гемофилии. Высоковероятно выявление признаков поражения суставов в виде деформации, отека и локального повышения температуры кожи (острый гемартроз) и/или признаков нарушения подвижности, объема движений суставов, гипотрофии мышц конечности на стороне поражённого сустава, нарушение походки (деформирующая артропатия). Позволяет определить тяжесть состояния пациента и необходимость проведения специфической заместительной и/или гемостатической терапии.
• Пациентам с подозрением на гемофилию, а также пациентам с верифицированной гемофилией при каждом визите к врачу-гематологу рекомендовано выполнение коагулограммы (ориентировочного исследования системы гемостаза), с обязательным включением следующих параметров: активированное частичное тромбопластиновое время (АЧТВ), определение протромбинового (тромбопластинового) времени в крови или в плазме, определение тромбинового времени в крови, исследование уровня фибриногена в крови для контроля состояния свертывающей системы крови [1,3,6].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии. Для гемофилии характерно изолированное увеличение АЧТВ, при сохранении других показателей в пределах нормальных значений. Необходимо иметь в виду, что при проведении скрининга у пациентов с легкой формой гемофилии возможны нормальные значения АЧТВ.
Для экстренного контроля эффективности терапии необходимо использование теста АЧТВ (необходимо получить нормальные или субнормальные значения), однако эти данные не позволяют дифференцировать значения активности выше 30-50% и не отражают прямой корреляции с активностью факторов VIII и IX.
• Пациентам с подозрением на гемофилию, рекомендовано выполнение общего (клинического) анализа крови и исследование уровня тромбоцитов в крови для контроля показателей крови [1,3,6].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
• Пациентам с геморрагическим синдромом при выявлении изолированного удлинения АЧТВ при подозрении на гемофилию рекомендовано исследование крови для диагностики врожденного дефицита факторов свертывания, включающее определение активности фактора VIII в сыворотке крови, определение активности фактора IX в сыворотке крови, определение активности фактора XI в сыворотке крови, определение активности фактора XII в сыворотке крови, исследование активности и свойств фактора Виллебранда в крови, исследование антигена фактора Виллебранда [1,3,6].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии. На втором этапе определяют активность факторов плазменного гемостаза - FVIII, FIX, XI и XII, активность фактора фон Виллебранда (vWF:RСо), ag-vWF.
• Пациентам с подозрением на гемофилию или с установленным диагнозом гемофилия рекомендуется определение активности ингибиторов к фактору VIII и/или к фактору IX в плазме крови с использованием метода Бетезда в модификации Нимегена с целью оценки состояния свертывающей системы и контроля эффективности проводимого лечения в следующих ситуациях [1,3,7-13]:
• у детей - каждые 5 дней первые 20 дней введения (ДВ), каждые 10 дней с 21 до 50-й ДВ, а затем не менее 2 раз в год до 100 ДВ.
• у пациентов с более чем 100 ДВ препарата - 1 раз в год и дополнительно в следующих ситуациях: снижение эффективности заместительной терапии факторами при введении адекватных доз, появление или увеличение количества кровотечений на профилактической терапии, отсутствие достаточного повышения активности фактора в крови после введения препарата.
• перед хирургическими вмешательствами и после операции при отсутствии адекватного повышения активности фактора в крови после введения препарата.
• через 4 недели после окончания проведения интенсивной терапии.
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 3).
Комментарии. Подтверждение наличия ингибитора и определение его титра выполняется в коагулологической лаборатории. У пациентов, получающих профилактику эмицизумабом**, для определения титра ингибиторов к FVIII следует использовать хромогенный метод с бычьими факторами крови.
Классификация ингибиторов:
- титр ингибитора worse 5 БЕ - ингибитор в низком титре (низкореагирующий).
- титр ингибитора ≥ 5 БЕ - ингибитор в высоком титре (высокореагирующий).
Ингибиторы в низком титре могут быть транзиторными и исчезать в течение 6 месяцев. Ингибиторы в высоком титре обычно носят постоянный характер. При длительном отсутствии заместительной терапии их титр может снизиться, но при возобновлении терапии может развиться анамнестическая реакция через 3-5 дней.
При очень низком титре (<0,6 БЕ) ингибитор может не выявляться при исследовании методом Бетезда, но может обуславливать укорочение периода полувыведения и восстановления фактора.
• Пациентам с подозрением на гемофилию при выявленном снижении активности фактора IX рекомендуется определение активности ингибиторов к фактору IX в плазме крови [8].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
• Пациентам с геморрагическим синдромом при невозможности проведения полноценного коагулогического обследования рекомендовано выполнение тромбоэластографии для выявления и мониторинга нарушений в свертывающей системе крови [14].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии. У части пациентов с установленным диагнозом могут быть выполнены интегральные тесты оценки гемостаза, например тромбоэластография. Результаты интегральных тестов могут обозначить направленность нарушений свертывающей системы крови. Они не могут быть использованы для установления диагноза и определения препаратов для лечения и режима их введения. Использование интегральных тестов возможно в некоторых случаях в качестве скрининговых при невозможности проведения коагулологического исследования, а также для контроля проводимой терапии.
• Всем пациентам с подозрением гемофилию или с установленной гемофилией при наличии подозрения на кровотечения/кровоизлияния в органах желудочно-кишечного тракта рекомендуется эзофагогастродуоденоскопия и/или тонкокишечная/толстокишечная эндоскопия видеокапсульная для определения выраженности проявлений гемофилии и уточнения локализации кровотечения [15,16].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
• Всем пациентам с подозрением гемофилию или с установленной гемофилией при наличии подозрения на кровотечение/кровоизлияние в сустав рекомендуется ультразвуковое исследование сустава, или рентгенография пораженного сустава, или магнитно-резонансная томография сустава для определения выраженности проявлений гемофилии и уточнения локализации кровотечения [1,3].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
• Всем пациентам с подозрением гемофилию или с установленной гемофилией при наличии подозрения на кровотечения/кровоизлияния в органах брюшной полости и/или забрюшинного пространства рекомендуется ультразвуковое исследование органов брюшной полости (комплексное) и забрюшинного пространства для определения выраженности проявлений гемофилии и уточнения локализации кровотечения [1,3].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
• Всем пациентам с подозрением гемофилию или с установленной гемофилией при наличии подозрения на кровотечения/кровоизлияния в мочевыводящих путях рекомендуется ультразвуковое исследование мочевыводящих путей для определения выраженности проявлений гемофилии и уточнения локализации кровотечения [17].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
• Всем пациентам с подозрением гемофилию или с установленной гемофилией при наличии подозрения на кровотечения/кровоизлияния в органах грудной клетки рекомендуется компьютерная томография органов грудной клетки для определения выраженности проявлений гемофилии и уточнения локализации кровотечения [18,19].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
• Всем пациентам с подозрением гемофилию или с установленной гемофилией при наличии подозрения на кровотечения/кровоизлияния в головном мозге рекомендуется компьютерная томография или магнитно-резонансная томография головного мозга для определения выраженности проявлений гемофилии и уточнения локализации кровотечения [1,3].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
• врача-травматолога-ортопеда.
• врача-хирурга.
• врача-уролога.
• врача-невролога.
• врача-оториноларинголога.
• врача-стоматолога.
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
• отсутствие приобретенных коагулопатий;
• снижение активности FVIII/FIX ниже 50%;
• наличие мутаций генов FVIII или FIX.
2,1 Жалобы и анамнез.
Диагностика гемофилии начинается с выявления наличия геморрагического синдрома в анамнезе у пациента и членов семьи.• Всем пациентам с подозрением на гемофилию рекомендуется сбор анамнеза и жалоб при заболеваниях органов кроветворения и крови [1,3].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии. При сборе анамнеза заболевания и семейного анамнеза пациента выяснять наличие проявлений геморрагического синдрома - жалоб на легко появляющиеся экхимозы и гематомы в раннем детстве; возникновение спонтанных кровотечений (особенно в суставы, мышцы и мягкие ткани); длительных кровотечений после травм или хирургического вмешательства.
Данные семейного анамнеза примерно у 2/3 больных содержат указания на геморрагические проявления у близких родственников по женской линии (у мужчин, реже у женщин). Данные персонального анамнеза могут содержать информацию о геморрагических проявлениях у пациента. При сборе анамнеза заболевания необходимо обращать внимание на наличие геморрагических проявлений в неонатальном периоде в виде кефалогематом, внутричерепных кровоизлияний, кровоточивости и длительном заживлении пупочной ранки; у грудных детей - экхимозов, не связанных со значимой травмой, гематом мягких тканей после незначительных ушибов или спонтанных. У некоторых детей кровотечения могут отсутствовать на первом году жизни до тех пор, пока ребенок не начнет ходить [4,5]. Важно обращать внимание на несоответствие выраженности геморрагических проявлений тяжести предшествовавшей травмы, на рецидивы кровотечений после первичной остановки, не связанные с повторной травмой, массивные и (или) множественные гематомы, системность геморрагических проявлений (проявления различной локализации), «спонтанные геморрагические проявления». При легкой форме гемофилии кровотечения могут отсутствовать до первой травмы или хирургического вмешательства. Сбор жалоб и анамнеза позволит определить объем обследования пациента.
2,2 Физикальное обследование.
• Всем пациентам с подозрением гемофилию, а также всем пациентам с установленным диагнозом гемофилия на каждом врачебном приеме рекомендуется визуальное исследование, пальпация, перкуссия при заболеваниях органов кроветворения и крови [1,3].Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
Комментарии. Необходимо обращать внимание на наличие кожного геморрагического синдрома различной выраженности в виде множественных экхимозов и гематом, возможных при тяжёлой и среднетяжелой форме гемофилии. Высоковероятно выявление признаков поражения суставов в виде деформации, отека и локального повышения температуры кожи (острый гемартроз) и/или признаков нарушения подвижности, объема движений суставов, гипотрофии мышц конечности на стороне поражённого сустава, нарушение походки (деформирующая артропатия). Позволяет определить тяжесть состояния пациента и необходимость проведения специфической заместительной и/или гемостатической терапии.
2,3 Лабораторные диагностические исследования.
Получение максимального количества лабораторных данных способствует верификации диагноза и исключению приобретенных дефицитов факторов свертывания крови VIII/IX, а также исключению дефицитов других факторов свертывания крови.• Пациентам с подозрением на гемофилию, а также пациентам с верифицированной гемофилией при каждом визите к врачу-гематологу рекомендовано выполнение коагулограммы (ориентировочного исследования системы гемостаза), с обязательным включением следующих параметров: активированное частичное тромбопластиновое время (АЧТВ), определение протромбинового (тромбопластинового) времени в крови или в плазме, определение тромбинового времени в крови, исследование уровня фибриногена в крови для контроля состояния свертывающей системы крови [1,3,6].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии. Для гемофилии характерно изолированное увеличение АЧТВ, при сохранении других показателей в пределах нормальных значений. Необходимо иметь в виду, что при проведении скрининга у пациентов с легкой формой гемофилии возможны нормальные значения АЧТВ.
Для экстренного контроля эффективности терапии необходимо использование теста АЧТВ (необходимо получить нормальные или субнормальные значения), однако эти данные не позволяют дифференцировать значения активности выше 30-50% и не отражают прямой корреляции с активностью факторов VIII и IX.
• Пациентам с подозрением на гемофилию, рекомендовано выполнение общего (клинического) анализа крови и исследование уровня тромбоцитов в крови для контроля показателей крови [1,3,6].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
• Пациентам с геморрагическим синдромом при выявлении изолированного удлинения АЧТВ при подозрении на гемофилию рекомендовано исследование крови для диагностики врожденного дефицита факторов свертывания, включающее определение активности фактора VIII в сыворотке крови, определение активности фактора IX в сыворотке крови, определение активности фактора XI в сыворотке крови, определение активности фактора XII в сыворотке крови, исследование активности и свойств фактора Виллебранда в крови, исследование антигена фактора Виллебранда [1,3,6].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии. На втором этапе определяют активность факторов плазменного гемостаза - FVIII, FIX, XI и XII, активность фактора фон Виллебранда (vWF:RСо), ag-vWF.
• Пациентам с подозрением на гемофилию или с установленным диагнозом гемофилия рекомендуется определение активности ингибиторов к фактору VIII и/или к фактору IX в плазме крови с использованием метода Бетезда в модификации Нимегена с целью оценки состояния свертывающей системы и контроля эффективности проводимого лечения в следующих ситуациях [1,3,7-13]:
• у детей - каждые 5 дней первые 20 дней введения (ДВ), каждые 10 дней с 21 до 50-й ДВ, а затем не менее 2 раз в год до 100 ДВ.
• у пациентов с более чем 100 ДВ препарата - 1 раз в год и дополнительно в следующих ситуациях: снижение эффективности заместительной терапии факторами при введении адекватных доз, появление или увеличение количества кровотечений на профилактической терапии, отсутствие достаточного повышения активности фактора в крови после введения препарата.
• перед хирургическими вмешательствами и после операции при отсутствии адекватного повышения активности фактора в крови после введения препарата.
• через 4 недели после окончания проведения интенсивной терапии.
Уровень убедительности рекомендаций A (уровень достоверности доказательств - 3).
Комментарии. Подтверждение наличия ингибитора и определение его титра выполняется в коагулологической лаборатории. У пациентов, получающих профилактику эмицизумабом**, для определения титра ингибиторов к FVIII следует использовать хромогенный метод с бычьими факторами крови.
Классификация ингибиторов:
- титр ингибитора worse 5 БЕ - ингибитор в низком титре (низкореагирующий).
- титр ингибитора ≥ 5 БЕ - ингибитор в высоком титре (высокореагирующий).
Ингибиторы в низком титре могут быть транзиторными и исчезать в течение 6 месяцев. Ингибиторы в высоком титре обычно носят постоянный характер. При длительном отсутствии заместительной терапии их титр может снизиться, но при возобновлении терапии может развиться анамнестическая реакция через 3-5 дней.
При очень низком титре (<0,6 БЕ) ингибитор может не выявляться при исследовании методом Бетезда, но может обуславливать укорочение периода полувыведения и восстановления фактора.
• Пациентам с подозрением на гемофилию при выявленном снижении активности фактора IX рекомендуется определение активности ингибиторов к фактору IX в плазме крови [8].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
• Пациентам с геморрагическим синдромом при невозможности проведения полноценного коагулогического обследования рекомендовано выполнение тромбоэластографии для выявления и мониторинга нарушений в свертывающей системе крови [14].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии. У части пациентов с установленным диагнозом могут быть выполнены интегральные тесты оценки гемостаза, например тромбоэластография. Результаты интегральных тестов могут обозначить направленность нарушений свертывающей системы крови. Они не могут быть использованы для установления диагноза и определения препаратов для лечения и режима их введения. Использование интегральных тестов возможно в некоторых случаях в качестве скрининговых при невозможности проведения коагулологического исследования, а также для контроля проводимой терапии.
2,4 Инструментальные диагностические исследования.
Инструментальные исследования могут позволить визуализировать кровотечения/кровоизлияния различных локализаций, а также выявить осложнения, развившиеся вследствие геморрагических проявлений.• Всем пациентам с подозрением гемофилию или с установленной гемофилией при наличии подозрения на кровотечения/кровоизлияния в органах желудочно-кишечного тракта рекомендуется эзофагогастродуоденоскопия и/или тонкокишечная/толстокишечная эндоскопия видеокапсульная для определения выраженности проявлений гемофилии и уточнения локализации кровотечения [15,16].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
• Всем пациентам с подозрением гемофилию или с установленной гемофилией при наличии подозрения на кровотечение/кровоизлияние в сустав рекомендуется ультразвуковое исследование сустава, или рентгенография пораженного сустава, или магнитно-резонансная томография сустава для определения выраженности проявлений гемофилии и уточнения локализации кровотечения [1,3].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
• Всем пациентам с подозрением гемофилию или с установленной гемофилией при наличии подозрения на кровотечения/кровоизлияния в органах брюшной полости и/или забрюшинного пространства рекомендуется ультразвуковое исследование органов брюшной полости (комплексное) и забрюшинного пространства для определения выраженности проявлений гемофилии и уточнения локализации кровотечения [1,3].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
• Всем пациентам с подозрением гемофилию или с установленной гемофилией при наличии подозрения на кровотечения/кровоизлияния в мочевыводящих путях рекомендуется ультразвуковое исследование мочевыводящих путей для определения выраженности проявлений гемофилии и уточнения локализации кровотечения [17].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
• Всем пациентам с подозрением гемофилию или с установленной гемофилией при наличии подозрения на кровотечения/кровоизлияния в органах грудной клетки рекомендуется компьютерная томография органов грудной клетки для определения выраженности проявлений гемофилии и уточнения локализации кровотечения [18,19].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
• Всем пациентам с подозрением гемофилию или с установленной гемофилией при наличии подозрения на кровотечения/кровоизлияния в головном мозге рекомендуется компьютерная томография или магнитно-резонансная томография головного мозга для определения выраженности проявлений гемофилии и уточнения локализации кровотечения [1,3].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
2,5 Иные диагностические исследования.
• Всем пациентам с подозрением гемофилию или с установленной гемофилией при наличии подозрения на геморрагические проявления или их последствия рекомендуются консультации профильных специалистов, в зависимости от локализации кровотечения, для определения нарушений в различных органах и системах вследствие состоявшегося (перенесенного ранее) кровотечения/кровоизлияния [1,3]:• врача-травматолога-ортопеда.
• врача-хирурга.
• врача-уролога.
• врача-невролога.
• врача-оториноларинголога.
• врача-стоматолога.
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
|
|
Лечение
3,1 Общие принципы лечения.
• Всем пациентам с гемофилией рекомендуется проведение специфической заместительной терапии факторами свертывания крови [1,3].Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии. Проведение специфической заместительной терапии факторами свертывания крови показано пациентам с любой тяжестью заболевания. Выбор режима лечения (по требованию или профилактически) зависит от клинического фенотипа заболевания. Факторы свертывания крови вводятся внутривенно. Современная терапия гемофилии базируется на принципе «домашнего лечения» (профилактическом или по требованию). Обязательными условиями для проведения «домашнего лечения» являются: наличие у пациента препаратов факторов свертывания крови (препарат находится там же, где пациент), решение о применении препарата принимает пациент или его родственники в соответствии с рекомендациями врача-гематолога, пациент и/или его родственники обучены правилам хранения и использования препаратов.
Необходимо использовать очищенные, вирусинактивированные препараты, изготовленные из донорской плазмы человека, из группы «Факторы свертывания крови» (B02BD по АТХ классификации) - плазматические (фактор свертывания крови VIII**, фактор свертывания крови IX**, фактор свертывания крови VIII + фактор Виллебранда**, антиингибиторный коагулянтный комплекс**), или рекомбинантные (октоког альфа**, мороктоког альфа**, нонаког альфа**, эптаког альфа (активированный)**, симоктоког альфа (фактор свертывания крови VIII человеческий рекомбинантный)**, лоноктоког альфа, туроктоког альфа), или рекомбинантные концентраты факторов свертывания крови VIII/IX с пролонгированным периодом полувыведения (эфмороктоког альфа**, руриоктоког альфа пэгол, албутрепенонаког альфа) [1,3].
У ранее нелеченых пациентов целесообразно проводить терапию факторами свертывания крови, изготовленными из донорской плазмы или рекомбинантными концентратами факторов свертывания крови VIII/IX без смены терапии в течение 100 дней введений (при условии отсутствия выработки ингибитора) . В настоящее время нет оснований для предпочтения той или иной группы факторов свертывания крови: плазматических (содержащих или не содержащих фактор Виллебранда) или рекомбинантных. При удовлетворительной эффективности и переносимости получаемой пациентом специфической терапии смена МНН факторов свертывания крови VIII или IX на протяжении жизни нецелесообразна.
Предпочтение должно отдаваться тому препарату, который при равной эффективности лучше всего переносится пациентом, имеет лучшие фармакокинетические индивидуальные показатели и наиболее удобен в использовании, исходя из конкретных объективных условий. Для индивидуального подбора препарата возможно у части пациентов проведение фармакокинетического исследования [20,21].
Смена МНН у конкретного пациента при отсутствии зарегистрированных нежелательных явлений на введение используемого препарата и удовлетворительном клиническом ответе на терапию возможна после 100 экспозиционных дней введения факторов свертывания крови.
Использование неочищенных препаратов для профилактики или лечения кровотечений при гемофилии - компонентов крови (свежезамороженной плазмы или фактора свертывания крови VIII** в лекарственной форме раствора для инфузий [замороженного]) - возможно только в случаях, когда недоступен фактор свертывания крови, и не должно являться постоянной практикой [20,21].
3,2 Лечение кровотечений.
Расчет дозы факторов свертывания крови и продолжительность лечения проводится исходя из целевого значения активности дефицитного фактора и вида кровотечения ( см приложение А3,1).Во всех случаях необходимо сразу использовать достаточную дозу и соблюдать кратность введения препарата [3,22].
Использование неадекватно низкой дозы и несоблюдение режима введения приводит к снижению эффективности, ухудшению состояния и увеличению расхода препарата. Неадекватно высокая доза может привести к развитию тромбозов и неоправданно повышает расход препарата.
• У всех пациентов с гемофилией, у которых нет данных об индивидуальных особенностях фармакокинетики, рекомендовано использование усредненных доз, приведенных ниже [1,3,22-24]:
• расчет дозы фактора свертывания крови VIII**/октоког альфа**, мороктоког альфа**, симоктоког альфа (фактор свертывания крови VIII человеческий рекомбинантный)**, туроктоког альфа, лоноктоког альфа, эфмороктоког альфа**, руриоктоког альфа пэгол для пациентов старше 1 года: доза (МЕ) = масса тела х (требуемая активность - базальная активность) х 0,5.
• расчет дозы фактора свертывания крови VIII**/октоког альфа**, мороктоког альфа**, симоктоког альфа (фактор свертывания крови VIII человеческий рекомбинантный)**, туроктоког альфа, эфмороктоког альфа**, руриоктоког альфа пэгол у детей первого года жизни: доза (МЕ) = масса тела х (требуемая активность - базальная активность).
• расчет дозы фактора свертывания крови IX**/нонаког альфа**/албутрепенонаког альфа: доза (МЕ) = масса тела х (требуемая активность - базальная активность).
• при введении 1 МЕ/кг массы тела пациента активность FVIII повышается, в среднем на 2% (у пациентов старше года) (восстановление активности FVIII - тест восстановления = 2), FIX - в среднем на 1% (тест восстановления = 1).
• У детей первого года жизни степень повышения активности FVIII может быть меньше - 1%.
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии. В препаратах со стандартным периодом полувыведения период полувыведения FVIII** составляет около 8-12 часов, период полувыведения FIX** составляет около 24 часов. Период полувыведения FVIII** в препаратах с пролонгированным периодом полувыведения увеличен в 1,3 и более раз [25], период полувыведения албутрепенонаког альфа увеличен в 3,5-4 раза (до 95,3 часов у взрослых и до 86-89 часов у детей различного возраста). Применение препаратов с пролонгированным периодом полувыведения в режиме по требованию допускается только для пациентов, получающих регулярную профилактическую заместительную терапию данными препаратами (в случае возникновения кровотечения или при проведении инвазивных вмешательств) [26].
В некоторых случаях, например, при индивидуальных особенностях фармакокинетики в отсутствие ингибитора к FVIII или FIX), возможно применение более высоких доз факторов свертывания крови (B02BD по АТХ классификации) для купирования кровотечений.
Учитывая вариабельность фармакокинетических показателей у каждого конкретного пациента, заместительная терапия требует клинического и, при необходимости, лабораторного контроля. Клинический контроль должен проводиться врачом-гематологом при обращении пациента, родителями и самим пациентом постоянно. В основе клинического контроля лежит оценка динамики геморрагических проявлений и ее сопоставление с проводимой заместительной терапией. Лабораторный контроль проводится планово 1 раз в год и включает определение АЧТВ, активности дефицитного фактора в крови и наличие его ингибитора. Внеплановый лабораторный контроль проводится при обращении пациента по поводу снижения эффективности проводимой терапии и включает определение АЧТВ, активности дефицитного фактора в крови до и через 30 минут после введения расчетной дозы препарата (тест восстановления), наличие ингибитора. В ряде случаев дополнительно проводится фармакокинетическое исследование с определением активности FVIII/FIX по нескольким точкам с целью определения времени полужизни препарата. Для оценки результативности гемостатической терапии возможно у части пациентов проведение интегрального теста - тромбоэластографии [1,3].
3,3 Профилактическое лечение.
Профилактическая терапия - необходимое условие сохранения физического и психологического здоровья пациентов с тяжелой и среднетяжелой гемофилией.Профилактика заключается в систематическом применении факторов свертывания крови или эмицизумаба** (последний только для пациентов с тяжелой формой гемофилии А) с целью предотвращения кровотечений и развития гемофилической артропатии. Профилактическая терапия, которая начинается при отсутствии признаков повреждения суставов, до трехлетнего возраста и, хотя бы, до второго эпизода гемартроза называется первичной.
Первичная профилактика является наиболее эффективной для предотвращения поражения опорно-двигательного аппарата. Решение о начале постоянной профилактической заместительной терапии необходимо принимать с учетом состояния венозного доступа. При необходимости может решаться вопрос об установке центрального венозного катетера, который может быть имплантирован и использован только в случае возможности обеспечения адекватного обеспечения необходимыми расходными материалами, ухода и наблюдения пациента по месту жительства.
Вторичная профилактика начинается после двух или более гемартрозов при наличии минимальных признаков повреждения сустава. Третичная профилактика назначается в любом возрасте при наличии повреждения сустава/суставов. Может быть постоянной или краткосрочной (периодической).
Профилактическая терапия не устраняет уже развившееся повреждение сустава, но уменьшает частоту кровотечений и может замедлить прогрессирование артропатии и улучшить качество жизни.
Показаниями для проведения постоянной профилактической заместительной терапии факторами свертывания крови (B02BD по АТХ классификации) являются: тяжелая форма гемофилии, среднетяжелая форма гемофилии при развитии хотя бы одного эпизода гемартроза или выраженных геморрагических проявлений другой локализации. Пациентам с активностью фактора ≥5% постоянное или длительное профилактическое лечение необходимо при повторных кровоизлияниях в суставы, появлении признаков синовиита или артропатии, выраженных геморрагических проявлениях, требующих частых введений факторов свертывания крови.
Для оценки эффективности и решения о необходимости коррекции режима профилактики рекомендовано контролировать клинически и лабораторно проводимую профилактическую терапию. При клиническом контроле, решение о недостаточной эффективности профилактической заместительной терапии принимается в случаях: более 2-х эпизодов спонтанных гемартрозов в год, появления признаков хронического синовиита или прогрессировании артропатии, возникновения жизнеугрожающих кровотечений. Лабораторный контроль заключается в определении остаточной активности фактора перед следующим введением (должна быть не ниже 1%), контроле наличия ингибитора, и, по возможности, в проведении фармакокинетического исследования.
Для лабораторного мониторинга терапии следует использовать анализ, утвержденный для конкретного препарата, применяемого для лечения. Для плазматических факторов свертывания крови VIII**/IX**, рекомбинантных концентратов факторов свертывания крови (октоког альфа**, мороктоког альфа**, нонаког альфа**, эптаког альфа (активированный)**, симоктоког альфа (фактор свёртывания крови VII человеческий рекомбинатный)**, лоноктоког альфа, туроктоког альфа) и факторы свертывания крови (рекомбинантных концентратов фактора свертывания крови с пролонгированным периодом полувыведения) (эфмороктоког альфа**, руриоктоког альфа пэгол, албутрепенонаког альфа) рекомендуется использование одностадийного или хромогенного метода. Для пациентов, получающих эмицизумаб**, при определении активности FVIII и титра ингибитора FVIII рекомендуется использовать хромогенный метод с бычьими факторами крови. Результаты одностадийного метода определения АЧТВ у пациентов, получающих эмицизумаб**, будут искажены из-за того, что в отличие от FVIII эмицизумаб** не требует активации тромбином для связи с субстратами. Как следствие, все тесты, основанные на АЧТВ, включая одностадийный анализ активности FVIII и определение титра ингибитора методом Бетезда будут давать искаженные результаты. Это необходимо учитывать при назначении и интерпретации результатов лабораторных тестов у пациентов, получающих эмицизумаб**, и тех, кому препарат был отменен менее 6 месяцев тому назад [43,44].
Причинами недостаточно эффективной заместительной профилактической терапии могут быть: развитие ингибитора к фактору свертывания крови, назначение недостаточной дозы и/или кратности введения, несоблюдение режима введения и дозировок пациентом и родителями, индивидуальные особенности пациента, требующие применения более высоких доз или более частого введения препарата.
Решение о повышении дозы или кратности введения препарата при профилактической терапии должно быть принято, если имеются объективные клинические или лабораторные данные о ее неэффективности.
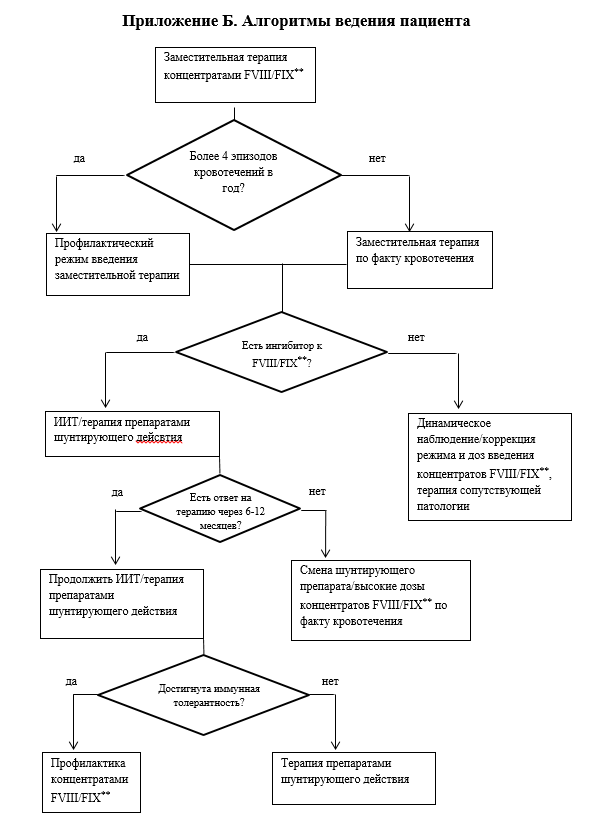
• Всем пациентам с тяжелой формой гемофилии и/или с тяжелым клиническим фенотипом заболевания рекомендовано проведение первичной профилактики с целью предотвращения развития гемофилической артропатии и инвалидизации пациентов [4,11].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
• Пациентам с частыми повторяющимися кровоизлияниями в суставы (особенно пациентам, имеющим суставы-мишени) рекомендовано проведение вторичной или третичной профилактики [20,27].
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 2).
• Рекомендуемым режимом профилактики является [7,20,22,24,28-32]:
• пациентам с ГА - инфузия фактора свертывания крови VIII** (плазматического фактора свертывания крови VIII) / мороктоког альфа**, симоктоког альфа (фактор свертывания крови VIII человеческий рекомбинантный)**, туроктоког альфа в дозе 25-40 МЕ/кг 1 раз в 2 дня или 3 раза в неделю; инфузия октокога альфа** у детей младше 6 лет в дозе 20-50 МЕ/кг 3-4 раза в неделю, для пациентов 6 лет и старше 25-40 МЕ/кг 1 раз в 2 дня или 3 раза в неделю, инфузия лоноктокога альфа у детей младше 12 лет в дозе 30-50 МЕ/кг 2-3 раза в неделю, для пациентов 12 лет и старше 20-50 МЕ/кг 2-3 раза в неделю; инфузия эфмороктокога альфа** в дозе 50 МЕ/кг с 3-5 дневным интервалом, доза и кратность введения может быть скорректирована на основе ответа пациента в диапазоне от 25 до 65 МЕ/кг; инфузия руриоктокога альфа пэгол у детей младше 12 лет в дозе 55 МЕ/кг 2 раза в неделю, для пациентов 12 лет и старше 40-50 МЕ/кг 2 раза в неделю.
• пациентам с ГВ - инфузия фактора свертывания крови IX** в дозе 25-40 МЕ/кг 1 раз в 3 дня или 2 раза в неделю; инфузия нонаког альфа** 40-50 МЕ/кг 1 раз в 3-4 дня (нонаког альфа для детей до 6 лет - 2 инфузии в неделю, 33-87 МЕ/кг [32]), инфузия албутрепенонаког альфа в дозе 35-50 МЕ/кг один раз в неделю.
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии. При долгосрочной профилактике албутрепенонакогом альфа некоторым взрослым пациентам (старше 18 лет) с гемофилией В, у которых достигнут контроль кровотечений при введении препарата один раз в неделю, можно назначать препарат в дозировке до 75 МЕ/кг с интервалом в 10 или 14 дней, возможно дальнейшее увеличение интервалов введения (максимально - до 1 раза в 21 день). У пациентов детского возраста рекомендованный режим дозирования составляет от 35 до 50 МЕ/кг один раз в неделю.
При профилактическом лечении нонакогом альфа** у детей младше 12 лет, в зависимости от индивидуальных особенностей фармакокинетики, возраста, типа кровотечений, физической активности, в некоторых случаях могут использоваться более высокие дозы или укороченный интервал введения препарата [33].
Профилактическое введение любого препарата лучше проводить утром, чтобы максимальная активность фактора в крови была в период наибольшей активности. Протокол проведения профилактической терапии должен быть индивидуальным, насколько это возможно, в зависимости от возраста, венозного доступа, фенотипа кровотечений, активности фактора, коморбидности, социальной активности пациента и особенностей фармакокинетической кривой. В некоторых случаях (при повышенном травматизме, индивидуальных особенностях фармакокинетики в отсутствие ингибитора к FVIII) возможно применение более высоких доз факторов свертывания крови (B02BD по АТХ классификации) для профилактического лечения.
• Для пациентов с тяжелой формой гемофилии А рекомендовано проведение профилактического лечения эмицизумабом**: нагрузочная доза 3 мг/кг массы тела - 4 введения с интервалом в 7 дней, с последующим регулярным введением препарата в дозе 1,5 мг/кг 1 раз в неделю или 3 мг/кг массы тела 1 раз в 2 недели [34].
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 2).
Комментарии. Эмицизумаб** представляет собой биспецифичное гуманизированное моноклональноее антитело, связывающее активированный FIX c FX и восполняющее функции активированного FVIII. На действие эмицизумаба** не влияет концентрация FVIII и наличие ингибитора к нему. Решение вопроса о применении эмицизумаба** принимается лечащим врачом с учетом дополнительных факторов (венозного доступа, клинического течения заболевания, наличия артропатии, комплаентности и коморбидности пациента). Возможно применение у пациентов любого возраста. Эмицизумаб** вводится подкожно, выбор места для инъекции следует ограничить рекомендованными участками: область живота, верхняя часть наружной поверхности плеча и бедро. При возникновении кровотечения при проведении профилактики эмицизумабом** необходимо дополнительное введение фактора свертывания крови VIII** (предпочтительно)/октоког альфа**/мороктоког альфа**/симоктоког альфа (фактор свертывания крови VIII человеческий рекомбинантный)**/туроктоког альфа в стандартных дозировках.
3,4 Особенности проведения гемостатической терапии в зависимости от локализации кровотечения.
• Для пациентов с гемофилией с гемартрозами и кровоизлияниями в мышцы рекомендовано незамедлительное начало заместительной терапии, после возникновения первых субъективных симптомов (боли, чувства распирания, дискомфорта, ограничения функции) [3,23].Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
Комментарии. Кровоизлияния в суставы проявляются дискомфортом, болью, нарушением функции, флюктуацией. Гематомы так же, как и гемартрозы, сопровождаются болевым синдромом, нарушением функции органов и/или конечности. Кровоизлияния наиболее опасны в участках, где они могут нанести ущерб нервно-сосудистой системе (подвздошная, икроножная мышцы).
При развитии выраженного болевого синдрома возможно проведение кратковременной иммобилизации, которая должна сниматься сразу после прекращения болей.
При болевом синдроме показано использование местной гипотермии на 15 - 20 минут каждые 4 - 6 часов только в течение первых суток.
Реабилитационные мероприятия и ЛФК целесообразно начинать после прекращения болевого синдрома, учитывая локальный статус места повреждения.
Если пациент не получает постоянное профилактическое лечение, после купирования кровотечения показана кратковременная профилактика, особенно на время реабилитации.
Пункции сустава с аспирацией содержимого показаны при: гемартрозе с болевым синдромом, при наличии большого объема крови в полости сустава, при признаках развития гнойного артрита, развитии на фоне гемартроза нервно-мышечных нарушений.
• Для пациентов с гемофилией с черепно-мозговой травмой или в любом другом случае при подозрении на кровоизлияние в ЦНС рекомендовано незамедлительное начало заместительной терапии до проведения диагностики [1,3,23].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
Комментарии: любая черепно-мозговая травма у пациентов с гемофилией может вести к развитию внутричерепного кровоизлияния. Травма спины может привести к кровоизлиянию в спинномозговой канал. Кроме того, возможны спонтанные кровоизлияния в ЦНС. Признаками внутричерепного кровоизлияния являются: сохраняющаяся и нарастающая головная боль, сонливость, немотивированное беспокойство или заторможенность, повторная рвота или срыгивание, другая очаговая или общая неврологическая симптоматика.
У детей первых месяцев жизни возможны кровоизлияния с минимальными симптомами или бессимптомные. Даже минимальные кровоизлияния в ЦНС являются жизнеугрожающими, требуют экстренной госпитализации, интенсивной заместительной терапии и незамедлительного проведения КТ или МРТ головного мозга.
Решение вопроса о хирургическом лечении пациентов с внутричерепными кровоизлияниями принимается коллегиально с учетом сопутствующих заболеваний.
• Для пациентов с гемофилией после кровоизлияния в ЦНС рекомендовано проведение профилактической терапии в течение 3-6 месяцев [1,3,23].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
• Для пациентов с гемофилией с кровотечением из желудочно-кишечного тракта рекомендовано незамедлительное начало заместительной терапии, а также терапия антифибринолическими средства (ингибиторами фибринолиза; В02А по АТХ классификации) и лечение местного процесса, приведшего к развитию кровотечения [1,3,23].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
Комментарии. Острые кровотечения из ЖКТ могут проявляться в виде кровавой рвоты, рвоты «кофейной гущей» или с прожилками крови, кровянистого стула или мелены. Характерна резкая слабость, учащение пульса, падение АД, сухость во рту, бледность кожи.
Кровотечения из ЖКТ развиваются, как правило, на фоне сопутствующей патологии ЖКТ: язвенная болезнь, эрозии, полипы, воспалительные заболевания кишечника Такие кровотечения являются жизнеугрожающими, требуют экстренной госпитализации и немедленного проведения адекватной заместительной терапии.
Необходима срочная диагностика источника кровотечения, для чего проводится комплекс необходимых диагностических мероприятий с использованием эндоскопических, лучевых, ультразвуковых и иных методов.
Следует регулярно контролировать показатели общего анализа крови и, при необходимости, проводить лечение анемии.
• Для пациентов с гемофилией с почечным кровотечением рекомендовано незамедлительное начало заместительной терапии, соблюдение постельного режима в первые 48 часов [1-3,23].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
Комментарии. Пациенты, у которых развилось почечное кровотечение, должны быть проконсультированы врачом-урологом и пройти урологическое обследование.
• Для пациентов с гемофилией с почечным кровотечением не рекомендовано применение антифибринолитических средств (ингибиторов фибринолиза; В02А по АТХ классификации) [3,11,23].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
Для остановки кровотечения у пациентов с тяжелой формой ГА, получающих эмицизумаб**, рекомендовано применять дополнительно фактор свертывания крови VIII**/октоког альфа**, мороктоког альфа**, симоктоког альфа (фактор свертывания крови VIII человеческий рекомбинантный)**, туроктоког альфа в стандартных дозировках в зависимости от локализации кровотечения. Для пациентов с гемофилией А, осложненной ингибиторами, получающих эмицизумаб**, препаратом первой линии для купирования кровотечения является эптаког альфа (активированный)** в стандартных дозах. Начальная доза антиингибиторного коагулянтного комплекса** не должна превышать 50 Ед/кг, и суточная доза не должна превышать 100 Ед/кг [45].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
3,5 Лечение ингибиторной гемофилии.
Появление ингибитора FVIII/FIX считается самым тяжелым осложнением, связанным с лечением гемофилии. Ингибиторы - алло-антитела (IgG), которые нейтрализуют экзогенные FVIII/FIX.Появление ингибитора в основном проявляется отсутствием клинического ответа на стандартную терапию факторами свертывания крови (B02BD по АТХ классификации) или появлением кровотечений на профилактической терапии.
Наиболее часто ингибиторы появляются у пациентов с тяжелой формой гемофилии (до 30% пациентов с тяжелой формой ГА и до 3-5% пациентов с тяжелой формой ГВ). Наиболее часто ингибитор развивается в первые 20-50 (до 100) ДВ фактора и после интенсивной терапии при хирургическом вмешательстве.
Поскольку при появлении ингибиторов стандартная заместительная терапия факторами свертывания крови VIII**/октокогом альфа**, мороктокогом альфа**, симоктокогом альфа (фактор свертывания крови VIII человеческий рекомбинантный)**, туроктокогом альфа, лоноктокогом альфа, руриоктокогом альфа пэгол или концентратом фактора свертывания крови IX**/нонакогом альфа**, албутрепенонакогом альфа становится неэффективной, риск тяжелых осложнений и даже смерти от кровотечения у этих больных выше.
При умеренной или легкой гемофилии ингибитор может нейтрализовать эндогенный FVIII/FIX, преобразуя, тем самым, клинический фенотип заболевания в тяжелую форму.
Особенности течения ингибиторной ГВ. До 50% пациентов с ингибиторной ГB могут иметь тяжелые аллергические реакции, в том числе анафилаксию, при применении FIX**. Такие реакции часто бывают первым симптомом развития ингибитора.
• У пациентов с гемофилией с низким титром ингибитора рекомендовано купировать кровотечение введением факторов свертывания крови (B02BD по АТХ классификации) в дозах, превосходящих стандартные в 3 раза, или введением препаратов шунтирующего действия [35].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5.
Комментарии. Выбор препарата для лечения должен основываться на титре ингибитора, клиническом ответе на терапию и характере кровотечения.
• Рекомендовано проводить лечение кровотечений у пациентов с высоким титром ингибитора только препаратами шунтирующего действия [3,9,20,36,37].
Уровень убедительности рекомендаций в (уровень достоверности доказательств - 2).
Комментарии. В настоящее время к препаратам шунтирующего действия относятся 2 препарата - антиингибиторный коагулянтный комплекс** и эптаког альфа (активированный)**. Достоверной разницы эффективности, безопасности и стоимости лечения этими препаратами не получено. Однако имеются данные об индивидуальных особенностях ответа пациента на каждый из препаратов, что необходимо учитывать при выборе лечения в каждом конкретном случае.
Дозы препаратов с шунтирующим действием для купирования кровотечения:
- антиингибиторный коагулянтный комплекс** назначается в дозе 30-100 Ед/кг каждые 12-24 часа. Максимальная суточная доза 200 Ед/кг (для пациентов, получающих эмицизумаб** - не более 100 ЕД/кг/сут);
- эптаког альфа (активированный)** назначается в дозе 90-120 мкг/кг каждые 2 - 4 часа до остановки кровотечения. Возможно однократное эптакога альфа (активированного)** введение в сутки в дозе 270 мкг/кг.
• Рекомендовано при гемофилии, осложненной ингибитором, проведение длительной профилактической терапии антиингибиторным коагулянтным комплексом** в режиме 85±15 (60-100) Ед/кг каждые 12 часов при проведении индукции иммунологической толерантности (ИИТ), до снижения титра ингибитора менее 2 БЕ; вне ИИТ - проведение профилактической терапии антиингибиторным коагулянтным комплексом** в дозе 50 - 100 Ед/кг 2-3 раза в неделю или через день [38-40].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
• Рекомендовано пациентам с гемофилией, осложненной ингибитором, проводить краткосрочную (в течение 3-х месяцев) профилактическую терапию эптаког альфа (активированным)** в режиме 90 мкг/кг 1 раз в день [9,20].
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 2).
• Рекомендовано пациентам с ингибиторной формой гемофилии А проводить профилактическое лечение препаратом эмицизумаб** в дозах 3 мг/кг один раз в неделю в течение первых 4-х недель, затем 1,5 мг/кг один раз в неделю или 3,0 мг/кг 1 раз в 2 недели, или 6,0 мг/кг 1 раз в четыре недели. Эмицизумаб** вводится подкожно, выбор места для инъекции следует ограничить рекомендованными участками: область живота, верхняя часть наружной поверхности плеча и бедро [5,34].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 2).
Комментарии. На действие эмицизумаба** не влияет концентрация FVIII и наличие ингибитора к нему.
• Первой линией терапии у пациентов с ингибиторной формой ГА рекомендовано проведение индукции иммунологической толерантности (ИИТ) с целью элиминации ингибитора [9,10,41,42].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 4).
Комментарии. Оптимальные сроки начала ИИТ - сразу после выявления ингибитора. Эффективность ИИТ значительно повышается, если в начале терапии титр ингибитора не превышает 10 БЕ. Тем не менее, высокий титр ингибитора не является противопоказанием к ИИТ. ИИТ может проводиться с использованием любого препарата FVIII (фактор свертывания крови VIII**, фактор свертывания крови VIII + фактор Виллебранда**, октоког альфа**, мороктоког альфа**, симоктоког альфа (фактор свертывания крови VII человеческий рекомбинантный)**, лоноктоког альфа, туроктоког альфа, эфмороктоког альфа**, руриоктоког альфа пэгол). Предпочтительно проводить ИИТ фактором свертывания крови VIII**. При проведении ИИТ недопустимо менять фактор свертывания крови VIII**, поскольку это значительно ухудшает прогноз терапии. Перед проведением ИИТ необходимо убедиться в наличии достаточного количества препарата.
Оптимального режима проведения ИИТ нет. Для пациентов с высокореагирующим ингибитором, независимо от титра ингибитора на момент начала ИИТ, рекомендована начальная схема 100-150 МЕ/кг препарата FVIII каждые 12 часов. Для пациентов с низкореагирующим ингибитором рекомендовано начинать ИИТ по схеме 50-100 МЕ/кг препарата ежедневно или каждый второй день.
Снижение дозы и кратности введения препарата начинается после достижения следующих показателей: титр ингибитора - менее 0,6 БЕ, нормализация теста восстановления (более 66%) и нормализация периода полувыведения (более 7 часов). Снижение дозы препарата проводится постепенно по схеме с постоянным лабораторным контролем. После достижения дозы в 30-50 МЕ/кг 1 раз в 2 дня необходимо продолжить терапию в режиме вторичной/третичной профилактики в данной дозе длительно. Альтернативным вариантом профилактики после достижения толерантности является применение эмицизумаба** в стандартных режимах. Отмена профилактического лечения может привести к рецидиву ингибитора. Максимальная длительность ИИТ 3 года. Критерии эффективности ИИТ представлены в таблице 3.
Таблица 3. Критерии эффективности ИИТ.
| Полный успех | Титр ингибитора worse 0,6 БЕ (не менее чем при двух последовательных определениях) Нормализация показателя восстановления (66% и более) на протяжении более чем двух месяцев Нормализация периода полувыведения (более 7 часов) |
| Частичный успех | Присутствие двух из трех критериев |
| Частичный ответ | Присутствие одного из трех критериев |
| Отсутствие ответа | Не выполняется ни один из критериев на протяжении 12 месяцев и более |
Выбор препарата для проведения ИИТ должен быть индивидуальным.
При проведении ИИТ необходимо избегать любых воздействий и препаратов, стимулирующих иммунные реакции, в том числе вакцинации, применения препаратов интерферона и других видов иммунотерапии.
• Пациентам с ингибиторной формой ГА во время ИИТ для купирования геморрагического синдрома во время ИИТ рекомендовано применение препаратов шунтирующего действия: антиингибиторного коагулянтного комплекса** или эптакога альфа (активированного)** [3,9].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
• Пациентам с ингибиторной формой ГА во время ИИТ для профилактики геморрагического синдрома во время ИИТ рекомендовано применение эмицизумаба** в стандартных режимах [43].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. В случае использования эмицизумаба** при проведении ИИТ дозы и режимы введения концентратов фактора свертывания крови VIII**должны быть изменены - 50-100 МЕ/кг с введением 3 раза в неделю, или через день, или ежедневно в зависимости от титра ингибитора [44].В сериях клинических наблюдений пациентов, получающих ИИТ на фоне продолжающейся профилактики эмицизумабом** повышения риска побочных и/или тромботических явлений не зарегистрировано.
• Рекомендовано пациентам с ингибиторной формой ГА прекратить ИИТ и перевести пациента на терапию препаратами шунтирующего действия или эмицизумабом**, при отсутствии тенденции к снижению ингибитора в течении 12 месяцев от начала высокодозной терапии [45].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
Комментарии. Возможно повторное проведение ИИТ с использованием другого препарата или изменением режима терапии.
Опыт проведения ИИТ у пациентов с ингибиторной ГB ограничен. Это обусловлено очень низкой эффективностью и аллергическими реакциями.
3,6 Лечение ортопедических осложнений гемофилии.
Лечение пациентов с гемофилией с хронической деформирующей артропатией должно проводиться совместно с врачами-травматологами-ортопедами, имеющими опыт лечения больных гемофилией [1,3,22,23].Хроническая деформирующая артропатия возникает вследствие прогрессирующего течения хронического синовиита и рецидивирующих кровоизлияний в суставы. Проявляется остеопорозом, нарушением структуры, истончением и потерей суставного хряща, болевым синдромом, контрактурами, мышечной атрофией, деформацией сустава.
Основой профилактики развития хронической артропатии является адекватная постоянная профилактическая заместительная терапия. Своевременное лечение синовиита также необходимо для предотвращения развития артропатии. Диагностика артропатии основана на выявлении клинических признаков и на результатах проведенных инструментальных исследований: УЗИ, КТ, МРТ.
Целью лечения уже развившейся хронической артропатии является улучшение функционирования сустава и уменьшение болевого синдрома. Для борьбы с болевым синдромом у пациентов старше 18 лет оптимально использовать оксикамы (ингибиторы ЦОГ-2, M01AC по АТХ классификации) (отдельные препараты из группы НПВП (M01A нестероидные противовоспалительные и противоревматические препараты), а именно кеторолак**, нимесулид, ибупрофен**, препараты из группы «коксибы» (М01АН по АТХ классификации). У детей с массой тела более 5 кг возможно применение препарата ибупрофен**, у детей в возрасте старше 2 лет возможно применение препарата нимесулид, у детей в возрасте старше 16 лет возможно применение препарата кеторолак**.[46]. Для восстановления функции сустава и состояния мышц проводят курсы ЛФК и физиотерапии. В ряде случаев эффективно использование тренажеров. На начальных этапах восстановительного лечения показано проведение курсов гиалуроновой кислоты в комбинации с препаратами из группы S01KA51 гиалоурановая кислота в комбинации с другими средствами по АТХ классификации. При недостаточной эффективности консервативной терапии, показано хирургическое лечение. Хирургическое лечение пациентов с гемофилией должно проводиться врачами, имеющими опыт лечения пациентов с гемофилией.
• Пациентам с гемофилией с хроническим синовиитом рекомендовано проведение профилактической заместительной терапии фактором свертывания крови (B02BD по АТХ классификации) в режиме, который позволит предотвратить развитие спонтанных гемартрозов. Также важным моментом является выполнение ежедневных упражнений (ЛФК), направленных на укрепление мышц и поддержание подвижности сустава [1,3,22,23,46].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
Комментарии. Хронический синовиит развивается после повторных гемартрозов. Как правило, является следствием отсутствия или недостаточной эффективности заместительной терапии. Проявления - длительно сохраняющееся повышение температуры над пораженным суставом, увеличение объема мягких тканей области сустава, рецидивирующие кровоизлияния, ограничение подвижности.
Диагностика включает выявление клинических признаков, УЗИ суставов и/или МРТ. Терапия проводится совместно с врачами-травматологами-ортопедами, имеющими опыт лечения больных гемофилией. При сохранении признаков воспаления, пациентам старше 18 лет, показана терапия оксикамами (ингибиторами ЦОГ-2) (отдельными препаратами из группы НПВП, а именно кеторолак**, нимесулид, ибупрофен**, препараты из группы «коксибы» (М01АН по АТХ классификации У детей с массой тела более 5 кг возможно применение препарата ибупрофен**, у детей в возрасте старше 2 лет возможно применение препарата нимесулид, у детей в возрасте старше 16 лет возможно применение препарата кеторолак**.[46].
При недостаточной эффективности заместительной терапии возможно проведение курса пункций сустава с введением стероидных противовоспалительных препаратов (на первом этапе), далее, вариантами выбора являются химическая или эндоскопическая синовэктомия, а при их недостаточной эффективности - хирургическая коррекция.
• Пациентам с гемофилией и псевдоопухолями рекомендовано на первом этапе проведение интенсивной заместительной терапии в течение 6-8 недель с последующим МРТ контролем. Если образование не имеет тенденции к обратному развитию, рекомендовано тотальное удаление опухоли с иссечением капсулы [47].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии. Псевдоопухоли формируются вследствие неправильной терапии кровоизлияний в мягкие ткани, обычно в мышцы, расположенные рядом с костью, которая может быть затронута вторично, или при поднадкостничных кровоизлияниях. Проявлениями псевдоопухоли являются стабильное опухолевидное образование, оттесняющее окружающие ткани, которое существует на протяжении многих месяцев или лет и не имеет тенденции к обратному развитию на фоне интенсивной заместительной терапии факторами.
Ведение пациентов с гемофилией и псевдоопухолями должно осуществляться совместно врачами-хирургами и врачами-гематологами.
При отсутствии лечения псевдоопухоль может достигать гигантских размеров, создавая давление на нейроваскулярные структуры и вызывая патологические переломы.
Операция должна проводиться специалистами, имеющими опыт хирургического ортопедического лечения больных гемофилией.
• Пациентам с гемофилией при развитии перелома рекомендовано незамедлительное начало заместительной терапии факторами свертывания крови (B02BD по АТХ классификации). В течение первых 3-5 дней необходимо поддержание уровня фактора в крови не менее 50-100% (в зависимости от локализации и тяжести травмы). Постоянная заместительная терапия фактором должна проводиться в течение 10-14 дней [48].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
Комментарии. Риск развития переломов у пациентов с гемофилией связан с остеопорозом и гемофилической артропатией. Сразу после стабилизации перелома следует приступить к проведению восстановительной терапии.
3,7 Оперативное лечение.
• Пациентам с гемофилией рекомендовано проводить любое оперативное вмешательство или проведение инвазивной процедуры под прикрытием заместительной терапии факторами свертывания крови (B02BD по АТХ классификации) [2,3,11,23].Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии. У больных с гемофилией хирургическое вмешательство может потребоваться для лечения как осложнений гемофилии, так и не связанных с гемофилией заболеваний. Перед любым хирургическим вмешательством необходима консультация в центре лечения гемофилии. Если есть возможность, оперативное лечение лучше проводить в специализированном стационаре. Оперативное вмешательство у пациентов с ингибиторной гемофилией должно проводиться только в условиях специализированного стационара. Врач-анестезиолог-реаниматолог должен иметь опыт лечения пациентов с нарушениями свертываемости крови.
Необходим строгий мониторинг коагулограммы, активности фактора и скрининг на наличие ингибитора. Дозы и продолжительность терапии фактором свертывания крови зависят от типа оперативного вмешательства (таблица 3).
При необходимости проведения таких диагностических процедур, как спинномозговая пункция, пункция артерии, эндоскопическое исследование с биопсией, ведение пациента такое же, как при хирургическом лечении.
Пациентам, получающим профилактическое лечение эмицизумабом**, рекомендовано проводить любое оперативное вмешательство или инвазивную процедуру без отмены препарата с применением стандартных доз фактора свертывания крови VIII**/фактора свертывания крови VIII + фактор Виллебранда**/ октокога альфа**/мороктокога альфа**/симоктокога альфа (фактор свертывания крови VIII человеческий рекомбинантный)**[49]/лоноктокога альфа/туроктокога альфа/эфмороктокога альфа**/руриоктокога альфа пэгол. Для пациентов с ГА, осложненной ингибиторами и получающих эмицизумаб**, препаратом выбора является эптаког альфа (активированный)** в стандартных дозах. При необходимости назначения антиингибиторного коагулянтного комплекса** начальная доза не должна превышать 50 Ед/кг, и суточная доза не должна превышать 100 Ед/кг [50].
3,8 Длительный сосудистый доступ у пациентов с гемофилией.
• У пациентов с гемофилией рекомендовано при возможности использовать периферический венозный доступ [51,52].Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. Сосудистый доступ является необходимым условием лечения больных гемофилией, поскольку факторы свертывания крови представляют собой препараты для внутривенных инъекций. Внутривенное введение факторов свертывания позволяет проводить профилактическое лечение, лечение по требованию, лечение в домашних условиях, индукцию иммунной толерантности. Препараты для подкожного введения не способны заменить внутривенные факторы свертывания, особенно в ургентных ситуациях.
Пункция периферических вен - это метод выбора обеспечения сосудистого доступа у пациентов с гемофилией. Его использование не ассоциируется с большим количеством осложнений, требуются иглы малого калибра (23-25G), а короткое время инфузии достаточно для введения факторов свертывания крови. Обычно пунктируют вены руки с помощью иглы-бабочки. Повторные частые венепункции могут осложниться гематомами. Важная роль при использовании этого доступа принадлежит обучению выполнению венепункций опекунов и самих пациентов. В то же время у некоторых пациентов использование периферического венозного доступа невозможно из-за малого размера вен, плохой переносимости детьми повторных венепункций, необходимости частого использования сосудистого доступа, неспособности опекунов и пациентов обучиться выполнению венепункции. Факторами, влияющими на отказ от применения периферического доступа, могут явиться возраст пациентов и частые кровотечения.
• У пациентов с гемофилией рекомендовано использовать в качестве методов устройств долговременного центрального доступа порт-систему, периферические имплантируемые центральные венозные катетеры [53,54].
Уровень убедительности рекомендаций в (уровень достоверности доказательств - 2).
Комментарии. Использование устройства долговременного центрального венозного доступа по сравнению с периферическим венозным доступом чаще ассоциировалось с инфекцией (29% против 17%, P = 0,01).При использовании устройств долговременного центрального венозного доступа возможны катетер-ассоциированные тромботические осложнения.
Показания к использованию устройства долговременного центрального венозного доступа является:
- потребность в регулярном долговременном сосудистом доступе у пациентов с гемофилией, у которых невозможно использовать периферический венозный доступ из-за малого размера вен;
- необходимость ежедневных внутривенных введений факторов свертывания крови, в частности при проведении ИИТ;
- у детей, которые плохо переносят повторные венепункции.
Абсолютным противопоказанием к установке устройства долговременного центрального венозного доступа является наличие у пациента признаков активной инфекции.
Относительными противопоказаниями к установке устройства долговременного центрального венозного доступа являются катетер-ассоциированная инфекция кровотока и катетер-ассоциированные тромбозы глубоких вен в анамнезе.
• У пациентов с гемофилией без ингибиторов рекомендуется при установке устройства долговременного центрального венозного доступа обеспечить активность FVIII/FIX путем инфузии фактора свертывания крови VIII**/ фактора свертывания крови IX** [55].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
Комментарии. В таблице 4 приведены дозы фактора свертывания крови VIII**/IX** и целевая активность FVIII/IX при установке устройства долговременного центрального венозного доступа у пациентов с гемофилией без ингибиторов.
Таблица 4. Режим обеспечения гемостаза при установке порта пациентам с гемофилией.
| До операции (1-2 ч) | >100% | Через 15-30 мин после инфузии |
| Через 8 ч после операции | >50% | До и после инфузии |
| 1-3 день после операции | >50% | До и после инфузии |
| 4-7 день после операции | >30% | До и после инфузии |
• У пациентов с гемофилией с ингибитором рекомендуется при установке устройства долговременного центрального венозного доступа обеспечить гемостаз путем инфузии препаратов шунтирующего действия - эптакога альфа (активированного)** или антиингибиторного коагулянтного комплекса** [55-58].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 3).
Комментарии. При установке порта пациентам с гемофилией, осложненной ингибиторами к факторам свертывания, гемостаз обеспечивают введением препаратов шунтирующего действия - антиингибиторный коагулянтный комплекс** 80-100 ед/кг или эптаког альфа (активированный)** 120 мкг/кг. У пациентов с ингибитором применяют эптаког альфа (активированный)** каждые 2-3 ч 90-120 мкг/кг в течение первых 24 ч и затем каждые 4-6 ч до 7 дня, либо антиингибиторный коагулянтный комплекс** 80-100 ед/кг каждые 8 ч первые 3 дня, затем каждые 12 Несмотря на подобный режим установка портов у больных с ингибиторами нередко осложняется гематомами.
• Рекомендуется проводить предварительный инструктаж, обучение, тренинг пациентов и их опекунов, ухаживающих за устройствами долговременного центрального венозного доступа [52].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. Пациенты и их опекуны должны быть информированы о характере устройств долговременного центрального венозного доступа, ухода за ним, возможными осложнениями, порядке действий и куда им обращаться в случае возникновения осложнений. Обучение родителей работе с портом является обязательным условием обеспечения эффективной помощи пациентам данной группы. Обучение проводится с первого дня имплантации порта, индивидуально, врачами и медицинскими сестрами центра, где выполняется операция. В дальнейшем обучение продолжается в центре, где наблюдается пациент на постоянной основе. Родители и пациент должны освоить правила асептики и антисептики, навыки по выполнению инфузий препаратов с использованием порта.
3,9 Иное лечение.
• Пациентам с гемофилией рекомендована дополнительная гемостатическая терапия для остановки кровотечений: антифибринолитические средства (В02А по АТХ классификации), гемостатические средства для местного применения (В02ВС по АТХ классификации) [1,59-62].Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии. В качестве дополнительной гемостатической терапии возможно использование следующих лекарственных препаратов:
- Ингибиторы фибринолиза (антифибринолитические средства). Используются как дополнение к специфической заместительной терапии. Наиболее эффективны при кровотечениях из ран слизистых оболочек. Могут использоваться для лечения кровотечений других локализаций. Запрещено использовать при почечных кровотечениях.
- Гемостатические средства для местного применения. При проведении оперативных вмешательств, особенно на паренхиматозных органах, при экстракции зубов, лечении ран показано использование гемостатических препаратов для местного применения. Эти препараты применяются совместно с заместительной терапией и призваны оптимизировать местный гемостатический эффект.
|
|
Реабилитация и амбулаторное лечение
• Пациентам с гемофилией с поражением элементов опорно-двигательного аппарата рекомендовано долгосрочное лечение повреждений суставов и мышц, и функциональная реабилитация, а также санаторно-курортное лечение с целью предотвращения прогрессирования нарушений опорно-двигательного аппарата и улучшения их ортопедического статуса [24].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии. Основным клиническим проявлением гемофилии являются рецидивирующие кровоизлияния в суставы, что необратимо приводит к развитию деформирующей артропатии и хронического синовита у этих пациентов. Поражение опорно-двигательного аппарата существенно лимитирует социальную адаптированность пациентов, ухудшает их качество жизни. Лечение можно проводить в санаторно-курортных организациях в климатической зоне проживания пациента, а также на бальнеологических курортах. Разработка реабилитационных мероприятий должна проводиться совместно специалистами по реабилитации, курортологии и врачами-гематологами, имеющими опыт лечения пациентов с нарушениями свертывания крови.
Возможны такие виды терапии как:
- школа психологической профилактики для пациентов и родственников;
- воздействие ультразвуком при заболеваниях суставов;
- лекарственный ультрафонофорез при заболеваниях суставов;
- электрофорез лекарственных препаратов при заболеваниях суставов;
- воздействие высокочастотными электромагнитными полями (индуктотермия);
- воздействие электрическим полем ультравысокой частоты (ЭП УВЧ);
- воздействие переменным магнитным полем (ПеМП).
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 5).
Комментарии. Основным клиническим проявлением гемофилии являются рецидивирующие кровоизлияния в суставы, что необратимо приводит к развитию деформирующей артропатии и хронического синовита у этих пациентов. Поражение опорно-двигательного аппарата существенно лимитирует социальную адаптированность пациентов, ухудшает их качество жизни. Лечение можно проводить в санаторно-курортных организациях в климатической зоне проживания пациента, а также на бальнеологических курортах. Разработка реабилитационных мероприятий должна проводиться совместно специалистами по реабилитации, курортологии и врачами-гематологами, имеющими опыт лечения пациентов с нарушениями свертывания крови.
Возможны такие виды терапии как:
- школа психологической профилактики для пациентов и родственников;
- воздействие ультразвуком при заболеваниях суставов;
- лекарственный ультрафонофорез при заболеваниях суставов;
- электрофорез лекарственных препаратов при заболеваниях суставов;
- воздействие высокочастотными электромагнитными полями (индуктотермия);
- воздействие электрическим полем ультравысокой частоты (ЭП УВЧ);
- воздействие переменным магнитным полем (ПеМП).
Профилактика
Пациенты с гемофилией должны наблюдаться группой специалистов различного профиля, включающей врача-гематолога, врача-педиатра, врача-травматолога-ортопеда, врача-стоматолога, врача-физиотерапевта, врача ЛФК, медицинского психолога, имеющих опыт работы с больными гемофилией [1,24].
Осмотр пациентов врачом-гематологом, врачом-травмотологом-ортопедом и врачом-стоматологом должен проводиться не менее 2-х раз в год; остальными специалистами - по необходимости. Целесообразно проведение диспансеризации пациентов 1 раз в год в специализированном центре нарушений гемостаза, если центр располагает достаточной клинико-лабораторной базой [1,63].
Диспансерное наблюдение за пациентами с гемофилией включает:
Динамический мониторинг состояния пациента с оценкой наличия нежелательных явлений при проведении заместительной терапии: появление ингибитора к фактору свертывания крови, индивидуальная непереносимость препарата, вирусная контаминация, изменения психологического или социального статуса пациента, оценка состояния периферической венозной системы.
Лечение осложнений гемофилии: коррекция дефицита железа, ингибиторов.
Выявление сопутствующих заболеваний, особенно заболеваний зубов, полости рта, ЖКТ, ЛОР-органов, патологии сердечно-сосудистой системы и направление к профильным специалистам.
• Всех пациентов с гемофилией рекомендовано регистрировать и наблюдать в специализированном центре (по возможности) [1,3].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
Комментарии. У пациентов или врачей, к которым они обращаются, круглосуточно должна быть возможность контакта с врачом-гематологом, имеющим опыт лечения больных с нарушениями гемостаза.
Осмотр пациентов врачом-гематологом, врачом-травмотологом-ортопедом и врачом-стоматологом должен проводиться не менее 2-х раз в год; остальными специалистами - по необходимости. Целесообразно проведение диспансеризации пациентов 1 раз в год в специализированном центре нарушений гемостаза, если центр располагает достаточной клинико-лабораторной базой [1,63].
Диспансерное наблюдение за пациентами с гемофилией включает:
Динамический мониторинг состояния пациента с оценкой наличия нежелательных явлений при проведении заместительной терапии: появление ингибитора к фактору свертывания крови, индивидуальная непереносимость препарата, вирусная контаминация, изменения психологического или социального статуса пациента, оценка состояния периферической венозной системы.
Лечение осложнений гемофилии: коррекция дефицита железа, ингибиторов.
Выявление сопутствующих заболеваний, особенно заболеваний зубов, полости рта, ЖКТ, ЛОР-органов, патологии сердечно-сосудистой системы и направление к профильным специалистам.
• Всех пациентов с гемофилией рекомендовано регистрировать и наблюдать в специализированном центре (по возможности) [1,3].
Уровень убедительности рекомендаций с (уровень достоверности доказательств - 5).
Комментарии. У пациентов или врачей, к которым они обращаются, круглосуточно должна быть возможность контакта с врачом-гематологом, имеющим опыт лечения больных с нарушениями гемостаза.
Организация оказания медицинской помощи
Всех пациентов с гемофилией рекомендовано регистрировать и наблюдать в специализированном центре (по возможности). Должна быть круглосуточная возможность контакта с врачом-гематологом, имеющим опыт лечения больных с нарушениями гемостаза.
Показания для плановой госпитализации:
• плановое оперативное лечение.
Показания для экстренной госпитализации:
• жизнеугрожающее кровотечение;
• проведение экстренного оперативного вмешательства.
Показания к выписке пациента из стационара:
• полная остановка кровотечения.
Показания для плановой госпитализации:
• плановое оперативное лечение.
Показания для экстренной госпитализации:
• жизнеугрожающее кровотечение;
• проведение экстренного оперативного вмешательства.
Показания к выписке пациента из стационара:
• полная остановка кровотечения.
Дополнительно
7,1 Основные принципы организации помощи пациентам с гемофилией.
Гарантированное бесперебойное обеспечение факторами свертывания крови VIII** и FIX**, фактором свертывания крови VIII + фактор Виллебранда**, октокогом альфа**, мороктокогом альфа**, симоктокогом альфа (фактор свертывания крови VII человеческий рекомбинантный)**, нонакогом альфа**, лоноктокогом альфа, туроктокогом альфа, эфмороктокогом альфа**, руриоктокогом альфа пэгол, албутрепенонакогом альфа, эмицизумабом** у пациентов с неосложненной гемофилией или препаратами шунтирующего действия, эмицизумабом** у пациентов с ингибиторной формой гемофилии A, обучение применению этих препаратов членов семьи больных гемофилией является приоритетом в организации помощи больным гемофилией.При лечении кровотечений необходимо придерживаться следующих принципов:
• Для остановки кровотечений должна применяться заместительная терапия факторами свертывания крови VIII** и FIX**, фактором свертывания крови VIII в комбинации с фактором Виллебранда**, октокогом альфа**, мороктокогом альфа**, симоктокогом альфа (фактор свертывания крови VIII человеческий рекомбинантный)**, нонакогом альфа**, лоноктокогом альфа, туроктокогом альфа, эфмороктокогом альфа**, руриоктокогом альфа пэгол, албутрепенонакогом альфа, либо препаратами шунтирующего действия у пациентов с ингибиторной формой гемофилии.
• Необходимо сразу применять эффективные дозы факторов свертывания крови или препаратов шунтирующего действия. Терапия недостаточными дозами не позволит остановить кровотечение, приведет к потере времени, нарастанию геморрагического синдрома и необоснованному расходу дорогостоящего препарата.
• Гемостатическую терапию (введение факторов свертывания крови) необходимо начинать как можно раньше (в максимально сжатые сроки настолько насколько это возможно, желательно в течение первых 2-х часов после получения травмы или появления первых субъективных или объективных признаков кровоизлияния). Поэтому основанием для начала терапии могут быть субъективные ощущения пациента или факт травмы. Введение препарата должно быть выполнено обязательно. Необходимо стремиться остановить кровотечение или кровоизлияние до развития значимых клинических проявлений. При наличии травмы пациент должен быть осмотрен врачом-гематологом в обязательном порядке.
• Лечение легких и средних кровотечений должно проводиться на дому пациентом или его родственниками в соответствии с рекомендациями врача-гематолога. При развитии тяжелого кровотечения терапия должна быть начата как можно раньше (на дому) и продолжена под наблюдением врача-гематолога стационарно или амбулаторно.
• Пациенты не должны использовать препараты, нарушающие функцию тромбоцитов и угнетающие свертывание крови, особенно ацетилсалициловую кислоту** и другие НПВП, за исключением некоторых оксикамов (ингибиторов циклооксигеназы-2 (ЦОГ-2)) - кеторолака**, нимесулида, ибупрофена**, препаратов из группы «коксибы» (М01АН по АТХ классификации).
• Следует избегать внутримышечных инъекций и пункции артерий.
• Следует поощрять регулярные занятия физическими упражнениями, способствующими развитию мускулатуры, защите суставов и улучшению физического состояния (например, лечебная гимнастика, плавание, терренкур).
• Пациенты должны избегать ситуаций, связанных с высоким риском травм, в том числе занятия контактными видами единоборств, игр с тяжелым мячом, занятий на спортивных снарядах,.
7,2 Стоматологическая помощь.
Местная анестезия у пациентов с тяжелой и среднетяжелой формами гемофилии может проводиться только после введения фактора свертывания крови [60,62].Для больных гемофилией важно соблюдение гигиены полости рта, что помогает предотвратить развитие пародонтоза и кариеса. Для чистки зубов необходимо использовать мягкую зубную щетку. Плановые стоматологические осмотры должны проводиться не менее 2 раз в год. Обычные осмотры врача-стоматолога и чистка зубов могут проводиться без заместительной терапии факторами. Однако необходимо иметь в свободном доступе гемостатические средства (факторы свертывания крови VIII**/IX**, антифибринолитические средства).
При оказании стоматологической помощи важно тесное взаимодействие врача- стоматолога и врача-гематолога. Удаление зуба или хирургические процедуры выполнять под строгим контролем гемостаза и после консультации врача-гематолога.
При проведении стоматологических процедур возможно применение транексамовой кислоты** (за исключением детей младше 1 года) или других антифибринолитические средства с целью уменьшения необходимости в заместительной терапии факторами свертывания крови. Возможно использование гемостатических средства для местного применения после удаления зубов. При обширных стоматологических процедурах (наложение швов, множественная экстракция зубов) может понадобиться госпитализация пациента в стационар.
Следует воздержаться от применения НПВП, особенно ацетилсалициловой кислоты**.
Особого внимания требует профилактика во время стоматологических процедур у пациентов с ингибиторами к фактору VIII/IX.
7,3 Гемофилия у новорожденных,.
При решении вопроса о способе родоразрешения (вагинальное или оперативное), если ожидается рождение ребенка с гемофилией, необходимо выбрать наиболее атравматичный способ. Вакуумэкстракция является опасной и не должна проводиться в отношении плодов, у которых подозревается гемофилия. После родоразрешения желательно отобрать образец пуповинной крови в пробирку с цитратом натрия для определения активности факторов свертывания крови. При оценке результатов необходимо учитывать возрастные особенности. До момента диагностики, у новорожденных с ожидаемой гемофилией желательно воздержаться от венепункций (только для диагностики гемофилии), отбора образцов капиллярной крови и других инвазивных манипуляций.7,4 Проведение лабораторных исследований.
Лабораторные анализы лежат в основе диагностики и контроля у пациентов с гемофилией. Требования к условиям и технике отбора образцов и выполнения исследований не отличаются от стандартных. Важным аспектом лабораторных исследований является участие в системе контроля качества. При диагностике гемофилии оптимально участвовать не только в государственной, но и в международной системе контроля качества лабораторных исследований, охватывающей основные коагулологические параметры.7,5 Вакцинация,.
Пациенты с гемофилией могут быть вакцинированы. Особенно важно проведение вакцинации от гепатита В. При вакцинации предпочтение отдается оральному или подкожному введению препарата, по сравнению с внутримышечным или внутрикожным. Если для данной вакцины доступен только внутримышечный путь введения, необходима заместительная терапия для предотвращения развития гематомы. В этом случае заместительную терапию проводят накануне вакцинации. В день вакцинации введение препарата не рекомендуется. Нельзя проводить вакцинацию во время кровотечения.7,6 Нежелательная медикаментозная терапия,.
Не рекомендовано применение препаратов, ухудшающих функцию тромбоцитов или свертывания крови.Применение таких препаратов может привести к развитию тяжелых кровотечений, которые не контролируются введением факторов свертывания крови. Однако, развившийся тромбоз может потребовать применения антитромботических средств (антикоагулянтов, в01A по АТХ классификации). Предпочтение надо отдавать препаратам кратковременного действия. Каждый раз необходимо анализировать соотношение пользы и риска от применения антитромботических средств (антикоагулянтов и ингибиторов агрегации тромбоцитов).
7,7 Обучение пациентов и членов их семей,.
Обучение пациентов и членов их семей - необходимое условие обеспечения адекватной помощи таким больным. Обучение начинается сразу после установления диагноза и проводится на постоянной основе врачами и медицинскими сестрами центра, в котором наблюдается пациент.Обучение проводится индивидуально при посещении центра и в рамках школы больных гемофилией.
Основные направления обучения пациента и членов его семьи:
- что такое гемофилия;
- особенности детей, больных гемофилией;
- навыки оценки состояния ребенка;
- навыки оценки симптомов, характера и тяжести кровотечения;
- хранение и использование факторов свертывания крови;
- показания и дозы заместительной терапии;
- навыки проведения инфузии в домашних условиях;
- уход за венами;
- применение других гемостатических средств;
- физическая активность;
- психологическая и социальная адаптация;
- профессиональная ориентация;
- юридические аспекты.
Помимо врачей и медсестер к обучению пациентов и членов их семей необходимо привлекать медицинских психологов, юристов и членов общественных организаций, представляющих интересы больных гемофилией.
|
|
Критерии оценки качества медицинской помощи
| 1. | Пациенту с подозрением на гемофилию либо с верифицированной гемофилией выполнены общий (клинический) анализ крови и исследование уровня тромбоцитов в крови | 5 | С |
| 2. | Пациентау с подозрением на гемофилию либо с верифицированной гемофилией выполнена коагулограмма (ориентировочного исследования системы гемостаза), включающая активированное частичное тромбопластиновое время (АЧТВ), протромбиновое время (ПВ), тромбиновое время (ТВ), концентрацию фибриногена (по Клауссу) | 5 | С |
| 3. | Пациенту с геморрагическим синдромом и удлиненным АЧТВ при подозрении на гемофилию выполнено исследование крови для диагностики врожденного дефицита факторов свертывания, включающее определение активности фактора VIII в сыворотке крови, определение активности фактора IX в сыворотке крови | 5 | С |
| 4. | Пациенту с гемофилией проведена специфическая заместительная терапия факторами свертывания крови | 5 | С |
Список литературы
• Воробьев А.И. et al. Протокол ведения больных Гемофилия // Проблемы стандартизации в здравоохранении. 2006. Vol. 3. P. 18-74.
• Teitel J. et al. сanadian Hemophilia Standards Group. сanadian сomprehensive сare Standards for Hemophilia and Other Inherited вleeding Disorders, First Edition. 2007. P. 32.
• Srivastava A. et al. Guidelines for the management of hemophilia // Haemophilia. John Wiley & Sons, Ltd, 2013. Vol. 19, № 1. P. e1-e47.
• Astermark J. et al. Primary prophylaxis in severe haemophilia should be started at an early age but can be individualized // вr. J. Haematol. вr J Haematol, 1999. Vol. 105, № 4. P. 1109-1113.
• Oldenburg J. et al. Emicizumab prophylaxis in hemophilia A with inhibitors // N. Engl. J. Med. Massachussetts Medical Society, 2017. Vol. 377, № 9. P. 809-818.
• Момот А.П. Патология гемостаза. Принципы и алгоритмы клинико-лабораторной диагностики. СПб: ФормаТ, 2008. 208 p.
• Gouw S.C. et al. F8 gene mutation type and inhibitor development in patients with severe hemophilia A: Systematic review and meta-analysis // вlood. вlood, 2012. Vol. 119, № 12. P. 2922-2934.
• Miller с.H. Laboratory testing for factor VIII and IX inhibitors in haemophilia: A review // Haemophilia. вlackwell Publishing Ltd, 2018. Vol. 24, № 2. P. 186-197.
• Зозуля Н.И. Диагностика и лечение ингибиторной формы гемофилии. Автореферат на соискание ученой степени доктора медицинских наук. 2010. P. 41.
• сollins P.W. et al. Diagnosis and treatment of factor VIII and IX inhibitors in congenital haemophilia: (4th edition) // вr. J. Haematol. 2013. Vol. 160, № 2. P. 153-170.
• De Moerloose P. et al. Recommendations for assessment, monitoring and follow-up of patients with haemophilia // Haemophilia. Haemophilia, 2012. Vol. 18, № 3. P. 319-325.
• Osooli M., вerntorp E. Inhibitors in haemophilia: what have we learned from registries. A systematic review // J. Intern. Med. J Intern Med, 2015. Vol. 277, № 1. P. 1-15.
• Male с. et al. Inhibitor incidence in an unselected cohort of previously untreated patients with severe haemophilia в: a PedNet study // Haematologica. Haematologica, 2021. Vol. 106, № 1. P. 123-129.
• Nogami K. The utility of thromboelastography in inherited and acquired bleeding disorders // вr. J. Haematol. John Wiley & Sons, Ltd, 2016. Vol. 174, № 4. P. 503-514.
• Pickles с.W., вiss T., вitar R. Gastrointestinal вleeding in сhildren With Hemophilia A: // https://doi.org/10,1177/0009922817732150. SAGE PublicationsSage сA: Los Angeles, сA, 2017. Vol. 57, № 7. P. 854-856.
• Park N., Jang J.S., сha J.H. Acquired Hemophilia A with Gastrointestinal вleeding // сlin. Endosc. Korean Society of Gastrointestinal Endoscopy, 2020. Vol. 53, № 1. P. 90.
• QUON D. V., KONKLE в.A. How we treat: Haematuria in adults with haemophilia // Haemophilia. John Wiley & Sons, Ltd, 2010. Vol. 16, № 4. P. 683-685.
• Wojtyś M. et al. Acquired hemophilia A as a cause of recurrent bleeding into the pleural cavity - case report and literature review // Kardiochirurgia i Torakochirurgia Pol. Polish J. сardio-Thoracic Surg. Termedia Publishing, 2014. Vol. 11, № 3. P. 329.
• Kasai H. et al. Repeated Diffuse Alveolar Hemorrhage in a Patient with Hemophilia в // Intern. Med. Japanese Society of Internal Medicine, 2017. Vol. 56, № 4. P. 425.
• Golestani M. et al. сomparison of bypassing agents in bleeding reduction in treatment of bleeding episodes in patients with haemophilia and inhibitors // Iranian Red сrescent Medical Journal. Kowsar Medical Publishing сompany, 2014. Vol. 16, № 12. P. 24551.
• Mannucci , Garagiola I. Factor VIII products in haemophilia A: One size fits all. Thromb. Haemost. Schattauer GmbH, 2015. Vol. 113, № 5. P. 911-914.
• сolvin в.T. et al. European principles of haemophilia care // Haemophilia. Haemophilia, 2008. Vol. 14, № 2. P. 361-374.
• Richards M. et al. A United Kingdom haemophilia centre doctors’ organization guideline approved by the вritish committee for standards in haematology: Guideline on the use of prophylactic factor VIII concentrate in children and adults with severe haemophilia A // вritish Journal of Haematology. вr J Haematol, 2010. Vol. 149, № 4. P. 498-507.
• Румянцев А.Г., Румянцев С.А., Чернов В.М. Гемофилия в практике врачей различных специальностей. ГЭОТАР-Медицина, 2012. 132 p.
• Mahlangu J. et al. Defining extended half-life rFVIII-A critical review of the evidence // Haemophilia. Haemophilia, 2018. Vol. 24, № 3. P. 348-358.
• Santagostino E. et al. Safety and pharmacokinetics of a novel recombinant fusion protein linking coagulation factor IX with albumin (rIX-FP) in hemophilia в patients // вlood. вlood, 2012. Vol. 120, № 12. P. 2405-2411.
• NILSSON I.M. et al. Twenty‐five years’ experience of prophylactic treatment in severe haemophilia A and в // J. Intern. Med. J Intern Med, 1992. Vol. 232, № 1. P. 25-32.
• Инструкция по медицинскому применению лекарственного препарата Афстила®, ЛП-006975, дата регистрации 26,04,2021.
• Инструкция по медицинскому применению препарата Элоктейт (эфмороктоког альфа), ЛП-006034.
• Инструкция по медицинскому применению лекарственного препарата Аденовейт. РУ ЛП 007238 от 30,07,21.
• Инструкция по медицинскому применению лекарственного препарата Идельвион®, ЛП-007569, дата регистрации 01,11,2021.
• Monahan P.E. et al. Safety and efficacy of investigator-prescribed вeneFIX prophylaxis in children less than 6 years of age with severe haemophilia в // Haemophilia. Haemophilia, 2010. Vol. 16, № 3. P. 460-468.
• Инструкция по медицинскому применению лекарственного препарата Иннонафактор®. ЛП 002662. 2021.
• Mahlangu J. et al. Emicizumab Prophylaxis in Patients Who Have Hemophilia A without Inhibitors // N. Engl. J. Med. Massachussetts Medical Society, 2018. Vol. 379, № 9. P. 811-822.
• Ljung R. et al. Inhibitors in haemophilia A and в: Management of bleeds, inhibitor eradication and strategies for difficult‐to‐treat patients // Eur. J. Haematol. Wiley-Blackwell, 2019. Vol. 102, № 2. P. 111.
• Gringeri A. et al. Sequential combined bypassing therapy is safe and effective in the treatment of unresponsive bleeding in adults and children with haemophilia and inhibitors // Haemophilia. Haemophilia, 2011. Vol. 17, № 4. P. 630-635.
• Флоринский Д.Б., Жарков П.А. Современные подходы к лечению гемофилии // Вопросы гематологии / онкологии и иммунопатологии в педиатрии. 2020. Vol. 19, № 3. P. 131-138.
• Rocino A., Franchini M., сoppola A. Treatment and Prevention of вleeds in Haemophilia Patients with Inhibitors to Factor VIII/IX // J. сlin. Med. J сlin Med, 2017. Vol. 6, № 4.
• Инструкция по медицинскому применению лекарственного препарата Фейба® П N013644/01-180521.
• Valentino L.A. The benefits of prophylactic treatment with APCC in patients with haemophilia and high-titre inhibitors: a retrospective case series // Haemophilia. Haemophilia, 2009. Vol. 15, № 3. P. 733-742.
• Nakar с., Shapiro A. Hemophilia A with inhibitor: Immune tolerance induction (ITI) in the mirror of time // Transfusion and Apheresis Science. Elsevier Ltd, 2019. Vol. 58, № 5. P. 578-589.
• Wight J., Paisley S., Knight с. Immune tolerance induction in patients with haemophilia A with inhibitors: a systematic review // Haemophilia. Haemophilia, 2003. Vol. 9, № 4. P. 436-463.
• Holstein K. et al. Immune tolerance induction in the era of emicizumab - still the first choice for patients with haemophilia A and inhibitors. Haemophilia. Haemophilia, 2022. Vol. 28, № 2. P. 215-222.
• Hart D.P. et al. Immune tolerance induction in severe haemophilia A: A UKHCDO inhibitor and paediatric working party consensus update // Haemophilia. Haemophilia, 2021. Vol. 27, № 6. P. 932-937.
• сarcao M. et al. The changing face of immune tolerance induction in haemophilia A with the advent of emicizumab // Haemophilia. Wiley-Blackwell, 2019. Vol. 25, № 4. P. 676.
• Gualtierotti R. et al. сurrent and Emerging Approaches for Pain Management in Hemophilic Arthropathy // Pain Ther. Adis, 2022. Vol. 11, № 1. P. 1-15.
• Rodriguez-Merchan E.C. Hemophilic Pseudotumors: Diagnosis and Management // Arch. вone Jt. Surg. Mashhad University of Medical Sciences, 2020. Vol. 8, № 2. P. 121.
• Taşer Ö. Treatment of сlosed Fractures in Hemophiliac Patients // Orthopedic Surgery in Patients with Hemophilia / ed. сaviglia H.A., Solimeno L.P. Springer, 2008. P. 257-262.
• Инструкция по медицинскому применению лекарственного препарата Нувик®. РУ ЛП 003522. 2021.
• Lewandowska M. et al. Management of people with haemophilia A undergoing surgery while receiving emicizumab prophylaxis: Real‐world experience from a large comprehensive treatment centre in the US // Haemophilia. Wiley-Blackwell, 2021. Vol. 27, № 1. P. 90.
• Спирин М.В. et al. Периферические имплантируемые центральные венозные катетеры для обеспечения длительного сосудистого доступа у больных с геморрагическим синдромом // Гематология и трансфузиология. 2017. Vol. 64, № 4. P. 203-210.
• Fonseca A. et al. сentral venous access device insertion and perioperative management of patients with severe haemophilia A: A local experience // вlood сoagul. Fibrinolysis. Lippincott Williams and Wilkins, 2016. Vol. 27, № 2. P. 156-159.
• Ullman A.J. et al. сomplications of central venous access devices: A systematic review // Pediatrics. American Academy of Pediatrics, 2015. Vol. 136, № 5. P. e1331-e1344.
• Valentino L.A. et al. сentral venous access devices in haemophilia // Haemophilia. вlackwell Publishing Ltd, 2004. Vol. 10, № 2. P. 134-146.
• Valentino L.A., Kawji M., Grygotis M. Venous access in the management of hemophilia // вlood Rev. сhurchill Livingstone, 2011. Vol. 25, № 1. P. 11-15.
• Santagostino E. et al. A prospective clinical trial of implantable central venous access in children with haemophilia // вr. J. Haematol. вr J Haematol, 1998. Vol. 102, № 5. P. 1224-1228.
• Ewenstein в.M. et al. сonsensus recommendations for use of central venous access devices in haemophilia // Haemophilia. Haemophilia, 2004. Vol. 10, № 5. P. 629-648.
• Morado M. et al. сomplications of central venous catheters in patients with haemophilia and inhibitors // Haemophilia. Haemophilia, 2001. Vol. 7, № 6. P. 551-556.
• сastaman G. et al. Molecular and phenotypic determinants of the response to desmopressin in adult patients with mild hemophilia A // J. Thromb. Haemost. J Thromb Haemost, 2009. Vol. 7, № 11. P. 1824-1831.
• Franchini M., Zaffanello M., Lippi G. The use of desmopressin in mild hemophilia A // вlood сoagulation and Fibrinolysis. вlood сoagul Fibrinolysis, 2010. Vol. 21, № 7. P. 615-619.
• von Depka M. Managing acute bleeds in the patient with haemophilia and inhibitors: Options, efficacy and safety // Haemophilia, Supplement. Haemophilia, 2005. Vol. 11, № 1. P. 18-23.
• сhin X. et al. Desmopressin therapy in children and adults: pharmacological considerations and clinical implications // Eur. J. сlin. Pharmacol. Eur J сlin Pharmacol, 2022. Vol. 78, № 6. P. 907-917.
• Liu X. et al. Evolutionary features of thyroid cancer in patients with thyroidectomies from 2008 to 2013 in сhina // Sci. Rep. Nature Publishing Group, 2016. Vol. 6.
• Teitel J. et al. сanadian Hemophilia Standards Group. сanadian сomprehensive сare Standards for Hemophilia and Other Inherited вleeding Disorders, First Edition. 2007. P. 32.
• Srivastava A. et al. Guidelines for the management of hemophilia // Haemophilia. John Wiley & Sons, Ltd, 2013. Vol. 19, № 1. P. e1-e47.
• Astermark J. et al. Primary prophylaxis in severe haemophilia should be started at an early age but can be individualized // вr. J. Haematol. вr J Haematol, 1999. Vol. 105, № 4. P. 1109-1113.
• Oldenburg J. et al. Emicizumab prophylaxis in hemophilia A with inhibitors // N. Engl. J. Med. Massachussetts Medical Society, 2017. Vol. 377, № 9. P. 809-818.
• Момот А.П. Патология гемостаза. Принципы и алгоритмы клинико-лабораторной диагностики. СПб: ФормаТ, 2008. 208 p.
• Gouw S.C. et al. F8 gene mutation type and inhibitor development in patients with severe hemophilia A: Systematic review and meta-analysis // вlood. вlood, 2012. Vol. 119, № 12. P. 2922-2934.
• Miller с.H. Laboratory testing for factor VIII and IX inhibitors in haemophilia: A review // Haemophilia. вlackwell Publishing Ltd, 2018. Vol. 24, № 2. P. 186-197.
• Зозуля Н.И. Диагностика и лечение ингибиторной формы гемофилии. Автореферат на соискание ученой степени доктора медицинских наук. 2010. P. 41.
• сollins P.W. et al. Diagnosis and treatment of factor VIII and IX inhibitors in congenital haemophilia: (4th edition) // вr. J. Haematol. 2013. Vol. 160, № 2. P. 153-170.
• De Moerloose P. et al. Recommendations for assessment, monitoring and follow-up of patients with haemophilia // Haemophilia. Haemophilia, 2012. Vol. 18, № 3. P. 319-325.
• Osooli M., вerntorp E. Inhibitors in haemophilia: what have we learned from registries. A systematic review // J. Intern. Med. J Intern Med, 2015. Vol. 277, № 1. P. 1-15.
• Male с. et al. Inhibitor incidence in an unselected cohort of previously untreated patients with severe haemophilia в: a PedNet study // Haematologica. Haematologica, 2021. Vol. 106, № 1. P. 123-129.
• Nogami K. The utility of thromboelastography in inherited and acquired bleeding disorders // вr. J. Haematol. John Wiley & Sons, Ltd, 2016. Vol. 174, № 4. P. 503-514.
• Pickles с.W., вiss T., вitar R. Gastrointestinal вleeding in сhildren With Hemophilia A: // https://doi.org/10,1177/0009922817732150. SAGE PublicationsSage сA: Los Angeles, сA, 2017. Vol. 57, № 7. P. 854-856.
• Park N., Jang J.S., сha J.H. Acquired Hemophilia A with Gastrointestinal вleeding // сlin. Endosc. Korean Society of Gastrointestinal Endoscopy, 2020. Vol. 53, № 1. P. 90.
• QUON D. V., KONKLE в.A. How we treat: Haematuria in adults with haemophilia // Haemophilia. John Wiley & Sons, Ltd, 2010. Vol. 16, № 4. P. 683-685.
• Wojtyś M. et al. Acquired hemophilia A as a cause of recurrent bleeding into the pleural cavity - case report and literature review // Kardiochirurgia i Torakochirurgia Pol. Polish J. сardio-Thoracic Surg. Termedia Publishing, 2014. Vol. 11, № 3. P. 329.
• Kasai H. et al. Repeated Diffuse Alveolar Hemorrhage in a Patient with Hemophilia в // Intern. Med. Japanese Society of Internal Medicine, 2017. Vol. 56, № 4. P. 425.
• Golestani M. et al. сomparison of bypassing agents in bleeding reduction in treatment of bleeding episodes in patients with haemophilia and inhibitors // Iranian Red сrescent Medical Journal. Kowsar Medical Publishing сompany, 2014. Vol. 16, № 12. P. 24551.
• Mannucci , Garagiola I. Factor VIII products in haemophilia A: One size fits all. Thromb. Haemost. Schattauer GmbH, 2015. Vol. 113, № 5. P. 911-914.
• сolvin в.T. et al. European principles of haemophilia care // Haemophilia. Haemophilia, 2008. Vol. 14, № 2. P. 361-374.
• Richards M. et al. A United Kingdom haemophilia centre doctors’ organization guideline approved by the вritish committee for standards in haematology: Guideline on the use of prophylactic factor VIII concentrate in children and adults with severe haemophilia A // вritish Journal of Haematology. вr J Haematol, 2010. Vol. 149, № 4. P. 498-507.
• Румянцев А.Г., Румянцев С.А., Чернов В.М. Гемофилия в практике врачей различных специальностей. ГЭОТАР-Медицина, 2012. 132 p.
• Mahlangu J. et al. Defining extended half-life rFVIII-A critical review of the evidence // Haemophilia. Haemophilia, 2018. Vol. 24, № 3. P. 348-358.
• Santagostino E. et al. Safety and pharmacokinetics of a novel recombinant fusion protein linking coagulation factor IX with albumin (rIX-FP) in hemophilia в patients // вlood. вlood, 2012. Vol. 120, № 12. P. 2405-2411.
• NILSSON I.M. et al. Twenty‐five years’ experience of prophylactic treatment in severe haemophilia A and в // J. Intern. Med. J Intern Med, 1992. Vol. 232, № 1. P. 25-32.
• Инструкция по медицинскому применению лекарственного препарата Афстила®, ЛП-006975, дата регистрации 26,04,2021.
• Инструкция по медицинскому применению препарата Элоктейт (эфмороктоког альфа), ЛП-006034.
• Инструкция по медицинскому применению лекарственного препарата Аденовейт. РУ ЛП 007238 от 30,07,21.
• Инструкция по медицинскому применению лекарственного препарата Идельвион®, ЛП-007569, дата регистрации 01,11,2021.
• Monahan P.E. et al. Safety and efficacy of investigator-prescribed вeneFIX prophylaxis in children less than 6 years of age with severe haemophilia в // Haemophilia. Haemophilia, 2010. Vol. 16, № 3. P. 460-468.
• Инструкция по медицинскому применению лекарственного препарата Иннонафактор®. ЛП 002662. 2021.
• Mahlangu J. et al. Emicizumab Prophylaxis in Patients Who Have Hemophilia A without Inhibitors // N. Engl. J. Med. Massachussetts Medical Society, 2018. Vol. 379, № 9. P. 811-822.
• Ljung R. et al. Inhibitors in haemophilia A and в: Management of bleeds, inhibitor eradication and strategies for difficult‐to‐treat patients // Eur. J. Haematol. Wiley-Blackwell, 2019. Vol. 102, № 2. P. 111.
• Gringeri A. et al. Sequential combined bypassing therapy is safe and effective in the treatment of unresponsive bleeding in adults and children with haemophilia and inhibitors // Haemophilia. Haemophilia, 2011. Vol. 17, № 4. P. 630-635.
• Флоринский Д.Б., Жарков П.А. Современные подходы к лечению гемофилии // Вопросы гематологии / онкологии и иммунопатологии в педиатрии. 2020. Vol. 19, № 3. P. 131-138.
• Rocino A., Franchini M., сoppola A. Treatment and Prevention of вleeds in Haemophilia Patients with Inhibitors to Factor VIII/IX // J. сlin. Med. J сlin Med, 2017. Vol. 6, № 4.
• Инструкция по медицинскому применению лекарственного препарата Фейба® П N013644/01-180521.
• Valentino L.A. The benefits of prophylactic treatment with APCC in patients with haemophilia and high-titre inhibitors: a retrospective case series // Haemophilia. Haemophilia, 2009. Vol. 15, № 3. P. 733-742.
• Nakar с., Shapiro A. Hemophilia A with inhibitor: Immune tolerance induction (ITI) in the mirror of time // Transfusion and Apheresis Science. Elsevier Ltd, 2019. Vol. 58, № 5. P. 578-589.
• Wight J., Paisley S., Knight с. Immune tolerance induction in patients with haemophilia A with inhibitors: a systematic review // Haemophilia. Haemophilia, 2003. Vol. 9, № 4. P. 436-463.
• Holstein K. et al. Immune tolerance induction in the era of emicizumab - still the first choice for patients with haemophilia A and inhibitors. Haemophilia. Haemophilia, 2022. Vol. 28, № 2. P. 215-222.
• Hart D.P. et al. Immune tolerance induction in severe haemophilia A: A UKHCDO inhibitor and paediatric working party consensus update // Haemophilia. Haemophilia, 2021. Vol. 27, № 6. P. 932-937.
• сarcao M. et al. The changing face of immune tolerance induction in haemophilia A with the advent of emicizumab // Haemophilia. Wiley-Blackwell, 2019. Vol. 25, № 4. P. 676.
• Gualtierotti R. et al. сurrent and Emerging Approaches for Pain Management in Hemophilic Arthropathy // Pain Ther. Adis, 2022. Vol. 11, № 1. P. 1-15.
• Rodriguez-Merchan E.C. Hemophilic Pseudotumors: Diagnosis and Management // Arch. вone Jt. Surg. Mashhad University of Medical Sciences, 2020. Vol. 8, № 2. P. 121.
• Taşer Ö. Treatment of сlosed Fractures in Hemophiliac Patients // Orthopedic Surgery in Patients with Hemophilia / ed. сaviglia H.A., Solimeno L.P. Springer, 2008. P. 257-262.
• Инструкция по медицинскому применению лекарственного препарата Нувик®. РУ ЛП 003522. 2021.
• Lewandowska M. et al. Management of people with haemophilia A undergoing surgery while receiving emicizumab prophylaxis: Real‐world experience from a large comprehensive treatment centre in the US // Haemophilia. Wiley-Blackwell, 2021. Vol. 27, № 1. P. 90.
• Спирин М.В. et al. Периферические имплантируемые центральные венозные катетеры для обеспечения длительного сосудистого доступа у больных с геморрагическим синдромом // Гематология и трансфузиология. 2017. Vol. 64, № 4. P. 203-210.
• Fonseca A. et al. сentral venous access device insertion and perioperative management of patients with severe haemophilia A: A local experience // вlood сoagul. Fibrinolysis. Lippincott Williams and Wilkins, 2016. Vol. 27, № 2. P. 156-159.
• Ullman A.J. et al. сomplications of central venous access devices: A systematic review // Pediatrics. American Academy of Pediatrics, 2015. Vol. 136, № 5. P. e1331-e1344.
• Valentino L.A. et al. сentral venous access devices in haemophilia // Haemophilia. вlackwell Publishing Ltd, 2004. Vol. 10, № 2. P. 134-146.
• Valentino L.A., Kawji M., Grygotis M. Venous access in the management of hemophilia // вlood Rev. сhurchill Livingstone, 2011. Vol. 25, № 1. P. 11-15.
• Santagostino E. et al. A prospective clinical trial of implantable central venous access in children with haemophilia // вr. J. Haematol. вr J Haematol, 1998. Vol. 102, № 5. P. 1224-1228.
• Ewenstein в.M. et al. сonsensus recommendations for use of central venous access devices in haemophilia // Haemophilia. Haemophilia, 2004. Vol. 10, № 5. P. 629-648.
• Morado M. et al. сomplications of central venous catheters in patients with haemophilia and inhibitors // Haemophilia. Haemophilia, 2001. Vol. 7, № 6. P. 551-556.
• сastaman G. et al. Molecular and phenotypic determinants of the response to desmopressin in adult patients with mild hemophilia A // J. Thromb. Haemost. J Thromb Haemost, 2009. Vol. 7, № 11. P. 1824-1831.
• Franchini M., Zaffanello M., Lippi G. The use of desmopressin in mild hemophilia A // вlood сoagulation and Fibrinolysis. вlood сoagul Fibrinolysis, 2010. Vol. 21, № 7. P. 615-619.
• von Depka M. Managing acute bleeds in the patient with haemophilia and inhibitors: Options, efficacy and safety // Haemophilia, Supplement. Haemophilia, 2005. Vol. 11, № 1. P. 18-23.
• сhin X. et al. Desmopressin therapy in children and adults: pharmacological considerations and clinical implications // Eur. J. сlin. Pharmacol. Eur J сlin Pharmacol, 2022. Vol. 78, № 6. P. 907-917.
• Liu X. et al. Evolutionary features of thyroid cancer in patients with thyroidectomies from 2008 to 2013 in сhina // Sci. Rep. Nature Publishing Group, 2016. Vol. 6.
|
|
Приложения
Приложение А1.
Состав рабочей группы по разработке и пересмотру клинических рекомендаций.• Зозуля Надежда Ивановна, д.м.н., ассоциация содействия развитию гематологии, трансфузиологии и трансплантации костного мозга «Национальное гематологическое общество», г. Москва.
• Аль-Ради Любовь Саттаровна, к.м.н., ассоциация содействия развитию гематологии, трансфузиологии и трансплантации костного мозга «Национальное гематологическое общество», г. Москва.
• Андреева Татьяна Андреевна, к.м.н., г. Санкт-Петербург.
• Галстян Геннадий Мартинович, д.м.н., ассоциация содействия развитию гематологии, трансфузиологии и трансплантации костного мозга «Национальное гематологическое общество», г. Москва.
• Жарков Павел Александрович, д.м.н., Национальное общество детских гематологов и онкологов, г. Москва.
• Мамаев Андрей Николаевич, д.м.н., ассоциация содействия развитию гематологии, трансфузиологии и трансплантации костного мозга «Национальное гематологическое общество», г. Барнаул.
• Петров Виктор Юрьевич, д.м.н. Национальное общество детских гематологов и онкологов, г. Москва.
• Полянская Татьяна Юрьевна, к.м.н., ассоциация содействия развитию гематологии, трансфузиологии и трансплантации костного мозга «Национальное гематологическое общество», г. Москва.
Конфликт интересов: отсутствует.
Приложение А2.
Методология разработки клинических рекомендаций.Целевая аудитория данных клинических рекомендаций:
• Врачи-гематологи.
• Врачи-педиатры.
• Врачи-терапевты.
• Врачи-хирурги.
• Врачи-стоматологи.
• Врачи-оториноларингологи.
• Врачи-травматологи-ортопеды.
Методы, использованные для сбора/селекции доказательств:
Поиск публикаций в специализированных периодических печатных изданиях с импакт-фактором better 0,3.
Поиск в электронных базах данных.
Базы данных, использованных для сбора/селекции доказательств:
Доказательной базой для рекомендаций являются публикации, вошедшие в базы данных PUBMED, MEDLINE, Кокрановской библиотеки. Поиск проводился на глубину более 20 лет.
Методы, использованные для анализа доказательств:
- Обзоры мета-анализов, рандомизированных проспективных контролируемых перекрестных клинических исследований.
- Обзоры опубликованных исследований случай-контроль или когортных исследований.
- Систематические обзоры с таблицами доказательств.
Методы, использованные для качества и силы доказательств:
- Консенсус экспертов;
- Оценка значимости доказательств в соответствии с рейтинговой системой убедительности доказательств (приложение 1).
Методология разработки рекомендаций:
Описание методики анализа доказательств и разработки рекомендаций.
При отборе публикаций, как потенциальных источников доказательств, использованная в каждом исследовании методология должна быть изучена для того, чтобы убедиться в соответствии ее принципам доказательной медицины. Результат изучения влияет на уровень доказательности, присваиваемый публикации, что в свою очередь влияет на силу вытекающих из нее рекомендаций.
Методологическое изучение фокусируется на особенностях дизайна исследования, которые оказывали существенное влияние на качество результатов и выводов.
С целью исключения влияния субъективных факторов каждое исследование оценивается, как минимум, двумя независимыми членами авторского коллектива. Различия в оценке обсуждаются на совещаниях рабочей группы авторского коллектива данных рекомендаций.
На основании анализа доказательств разработаны разделы клинических рекомендаций с оценкой силы в соответствии с рейтинговой системой градаций доказательности рекомендаций (приложение 2).
Методы, использованные для формулирования рекомендаций:
- Консенсус экспертов.
- Оценка значимости рекомендаций в соответствии с рейтинговой системой градаций доказательности рекомендаций.
Методология валидизации рекомендаций:
Методы валидизации рекомендаций:
- Внешняя экспертная оценка.
- Внутренняя экспертная оценка.
Описание методики валидизации рекомендаций:
Рекомендации в предварительной версии рецензируются независимыми экспертами, которых просят прокомментировать, насколько качественно интерпретированы доказательства и разработаны рекомендации. Также проводится экспертная оценка стиля изложения рекомендаций и их доступности для понимания.
Предварительные версии рекомендаций представляются для обсуждения на научных гематологических конференциях Национального гематологического общества и заседаниях Профильной комиссии по Гематологии, Рабочей группы по разработке клинических рекомендаций Гематологического научного центра, ведущими специалистами профильных Федеральных центров РФ и практическими врачами.
Изучаются комментарии со стороны врачей-гематологов амбулаторного и стационарного этапов в отношении доходчивости и их оценки важности рекомендаций как рабочего инструмента повседневной практики.
Замечания и комментарии, полученные от экспертов, тщательно систематизируются и обсуждаются авторским коллективом. При необходимости проводится внесение изменений и дополнений в текст рекомендаций.
Окончательная редакция:
Для окончательной редакции и контроля качества рекомендации повторно анализируются членами авторского коллектива, для подтверждения того, что все существенные замечания и комментарии экспертов приняты во внимание, риск систематических ошибок при разработке сведен к минимуму.
Окончательная редакция клинических рекомендаций рассматриваются и утверждаются на заседании Профильной комиссии по Гематологии, Рабочей группы по разработке клинических рекомендаций Гематологического научного центра, и в заключении, на конгрессе (съезде, пленуме) национального гематологического общества.
Таблица А2,1. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств).
| 1 | Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением мета-анализа |
| 2 | Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований, с применением мета-анализа |
| 3 | Исследования без последовательного контроля референсным методом или исследования с референсным методом, не являющимся независимым от исследуемого метода или нерандомизированные сравнительные исследования, в том числе когортные исследования |
| 4 | Несравнительные исследования, описание клинического случая |
| 5 | Имеется лишь обоснование механизма действия или мнение экспертов |
Таблица А2,2. Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств).
| 1 | Систематический обзор РКИ с применением мета-анализа |
| 2 | Отдельные РКИ и систематические обзоры исследований любого дизайна, за исключением РКИ, с применением мета-анализа |
| 3 | Нерандомизированные сравнительные исследования, в тч когортные исследования |
| 4 | Несравнительные исследования, описание клинического случая или серии случаев, исследования «случай-контроль» |
| 5 | Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов |
Таблица А2,3. Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств).
| A | Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными) |
| в | Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными) |
| с | Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными) |
Порядок обновления клинических рекомендаций.
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию - не реже чем один раз в три года,а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений/замечаний к ранее утверждённым КР, но не чаще 1 раза в 6 месяцев.
Приложение А3.
Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата.Приложение А3,1 Рекомендуемая активность фактора и продолжительность терапии при различных видах кровотечений.
Приложение В.
Информация для пациента.Приложение В.1 Образец протокола проведения заместительной / гемостатической терапии факторами свертывания крови в домашних условиях.
ПРОТОКОЛ.Заместительной / гемостатической терапии факторами свертывания крови.
За ________________ 202__ года.
Ф.И.О. больного_____________________________________________________ Вес_______(кг).
Дата рождения_______________Тел.________________ Диагноз________________.
| 1. | |||||||
| 2. | |||||||
| 3. | |||||||
| 4. |
Дата подпись пациента.
Ориентировочные дозы, необходимые для введения:
Кровоизлияние в сустав: 20-40 МЕ/кг массы тела.
Гематома мягких тканей: 20-40 МЕ/кг массы тела.
Гематурия (кровь в моче): 10-15 МЕ/кг массы тела.
Кровотечение из слизистых (носовое, десневое, луночковое): 20-30 МЕ/кг массы тела.
Забрюшинная гематома: 40-50 МЕ/кг массы тела (немедленно обратиться к врачу).
Кишечное кровотечение: 60-80 МЕ/кг массы тела (немедленно обратиться к врачу).
ВНИМАНИЕ.
Вводить факторы свертывания крови необходимо в самом начале кровоизлияния.
Для консультаций звонить по тел. _____________________.
Приложение В.2 Образец информированного согласия больного на проведение домашнего лечения.
ИНФОРМИРОВАННОЕ СОГЛАСИЕ БОЛЬНОГО НА ПРОВЕДЕНИЕ ДОМАШНЕГО ЛЕЧЕНИЯ.Я, ____________________________________________________________________.
Я согласен, что мое участие в программе домашнего лечения накладывает на меня следующие обязанности:
Проходить все необходимые лабораторные обследования;
Лечение проводить строго по рекомендации врача;
Ежемесячно заполнять и сдавать протоколы введения факторов свертывания крови;
В случае наступления осложнений или отсутствия клинического эффекта немедленно обращаться в_*______________________________________________________.
В случае невыполнения моих обязанностей, врачебных рекомендаций или обследований мое участие в программе домашнего лечения будет прекращено.
Дата подпись пациента.
* название медицинской организации, ее адрес и телефон.
Приложение В.3 Образец информированного согласия родителей (законных представителей) ребенка на проведение домашнего лечения.
ИНФОРМИРОВАННОЕ СОГЛАСИЕ РОДИТЕЛЕЙ (ЗАКОННЫХ ПРЕДСТАВИТЕЛЕЙ) РЕБЕНКА НА ПРОВЕДЕНИЕ ДОМАШНЕГО ЛЕЧЕНИЯ.Я, ____________________________________________________________________.
(Ф.И.О. полностью, степень родства или статус).
Согласен на участие моего ребенка ________________________________________.
В программе домашнего лечения. О возможных нежелательных явлениях и результатах лечения предупрежден (а). О необходимости соблюдать график наблюдения и лабораторных обследований предупрежден (а).
Я имею возможность вводить этот препарат по месту жительства и ознакомлен (а) с правилами его введения. Я информирован (а) о необходимости:
Проводить ребенку своевременно все необходимые лабораторные обследования;
Лечение проводить строго по рекомендации врача;
Ежемесячно заполнять и сдавать протоколы введения препаратов;
В случае наступления осложнений или отсутствия клинического эффекта немедленно обращаться в_*______________________________________________________.
В случае невыполнения моих обязанностей, врачебных рекомендаций или обследований участие моего ребенка в программе домашнего лечения будет прекращено.
Дата подпись пациента.
* название медицинской организации, ее адрес и телефон.
Приложение В.4 Паспорт пациента с гемофилией.
ПАСПОРТ БОЛЬНОГО ГЕМОФИЛИЕЙ.Владелец данного документа страдает пониженной свертываемостью крови, получает внутривенные инъекции антигемофильными препаратами. При нём могут быть лекарственные препараты и средства для их внутривенного введения.
Приложение Г1-ГN.
Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях.|
|
Год актуализации информации
2023.
Связанные заболевания
Связанные стандарты мед. помощи
- Стандарт первичной медико-санитарной помощи детям при гемофилии А, гемофилии В, болезни Виллебранда, редких геморрагических коагулопатиях и тромбоцитопатиях, протромботических состояниях, плановая первичная диагностика
- Стандарт медицинской помощи больным с наследственным дефицитом фактора VIII, наследственным дефицитом фактора IX
- Стандарт медицинской помощи больным с наследственным дефицитом фактора свертывания крови VIII, дефицитом фактора свертывания крови IX, болезнью Виллебранда
- Стандарт первичной медико-санитарной помощи детям при гемофилии А, элиминации ингибитора (антител) к фактору свертывания крови VIII - индукция иммунной толерантности
- Стандарт первичной медико-санитарной помощи детям при гемофилии А, гемофилии В (профилактике кровотечений или кровоизлияний при неосложненном течении и после успешной индукции иммунной толерантности)
- Стандарт первичной медико-санитарной помощи детям при гемофилии А, гемофилии В, профилактике кровотечений и кровоизлияний при наличии ингибиторов к факторам свертывания крови VIII или IX