Pharmacological Group
Latin name
Zonisamidum ( Zonisamidi).
Chemical name
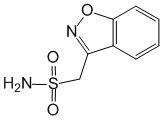
Бензо[d]изоксазол-3-илметансульфонамид.
Used in the treatment
- G40.2 Localization-related (focal)(partial) symptomatic epilepsy and epileptic syndromes with complex partial seizures
- G40.1 Localization-related (focal)(partial) symptomatic epilepsy and epileptic syndromes with simple partial seizures
- G40.0 Localization-related (focal)(partial) idiopathic epilepsy and epileptic syndromes with seizures of localized onset
- G40 Epilepsy
CAS Code
68291-97-4.
Pharmacodynamics
Фармакодинамика.
Зонисамид является противоэпилептическим ЛС, производным бензизоксазола, in vitro >in vitro слабо угнетает карбоангидразу. Химически его структура отличается от других противоэпилептических ЛС.
Механизм действия.
Механизм действия зонисамида полностью не изучен, вероятно, он блокирует потенциалчувствительные натриевые и кальциевые каналы, снижает выраженность синхронизированного нейронного возбуждения, тормозит развитие приступов и предотвращает дальнейшее распространение эпилептической активности. Зонисамид также снижает судорожную активность нейронов посредством усиления тормозного влияния ГАМК.
Фармакодинамические эффекты.
Противосудорожная активность зонисамида была изучена на различных моделях эпилепсии, в группах с индуцированными или врожденными приступами, при этом зонисамид проявил себя как противоэпилептическое ЛС широкого спектра действия. Зонисамид препятствует развитию максимальных электросудорожных приступов, ограничивает развитие судорог, включая распространение очага возбуждения от коры головного мозга до подкорковых структур, а также подавляет активность эпилептогенного фокуса. В отличие от фенитоина и карбамазепина, зонисамид обладает избирательным действием на приступы, возникающие в коре головного мозга.
Клиническая эффективность и безопасность.
Монотерапия парциальных судорожных приступов с вторичной генерализацией или без. Эффективность зонисамида в режиме монотерапии у пациентов с впервые диагностированными парциальными эпилептическими приступами с вторичной генерализацией или без, с генерализованными тонико-клоническими приступами без четкой очаговости была показана в двойном слепом, с параллельными группами, исследовании с участием 583 взрослых пациентов по установлению не меньшей эффективности терапии зонисамидом относительно терапии карбамазепином пролонгированного действия, продолжавшемся до 24 мес, в зависимости от ответа на лечение. Осуществлялось повышение дозы до целевого значения 600 мг карбамазепина или 300 мг зонисамида. При наличии у пациентов приступов осуществлялось повышение до следующей дозы, 800 мг карбамазепина или 400 мг зонисамида. Если приступы сохранялись, то дозу увеличивали максимально до 1200 мг для карбамазепина и до 500 мг для зонисамида. Пациенты, у которых приступы отсутствовали в течение 26 нед на фоне приема целевой дозы, продолжали получать эту же дозу в течение еще 26 нед.
Дополнительная терапия парциальных судорожных приступов с вторичной генерализацией или без у взрослых. Эффективность дополнительной терапии зонисамидом была показана в 4 двойных слепых плацебо-контролируемых исследованиях, продолжавшихся до 24 нед. Эти исследования показали снижение медианы частоты возникновения парциальных эпилептических приступов при приеме зонисамида в суточных дозах 300-500 мг 1 или 2 раза в день.
Дополнительная терапия парциальных судорожных приступов с вторичной генерализацией или без у подростков и детей с 6 лет. У детей (в возрасте 6 лет и старше) эффективность зонисамида была продемонстрирована в двойном слепом плацебо-контролируемом исследовании продолжительностью 24 нед при участии 207 пациентов. При 12-недельном применении целевой дозы наблюдалось снижение частоты приступов на 50% и более у 50% пациентов, получавших зонисамид, и 31% пациентов, получавших плацебо.
Особые проблемы безопасности, которые возникли при проведении исследований у детей, включали ухудшение аппетита и снижение массы тела, снижение уровня бикарбонатов, увеличение риска мочекаменной болезни и дегидратацию. Все эти явления, и особенно снижение массы тела, могут неблагоприятно сказываться на росте и развитии ребенка, а также приводить к ухудшению общего состояния здоровья. В целом получен ограниченный объем данных о долговременном влиянии зонисамида на рост и развитие ребенка.
Зонисамид является противоэпилептическим ЛС, производным бензизоксазола, in vitro >in vitro слабо угнетает карбоангидразу. Химически его структура отличается от других противоэпилептических ЛС.
Механизм действия.
Механизм действия зонисамида полностью не изучен, вероятно, он блокирует потенциалчувствительные натриевые и кальциевые каналы, снижает выраженность синхронизированного нейронного возбуждения, тормозит развитие приступов и предотвращает дальнейшее распространение эпилептической активности. Зонисамид также снижает судорожную активность нейронов посредством усиления тормозного влияния ГАМК.
Фармакодинамические эффекты.
Противосудорожная активность зонисамида была изучена на различных моделях эпилепсии, в группах с индуцированными или врожденными приступами, при этом зонисамид проявил себя как противоэпилептическое ЛС широкого спектра действия. Зонисамид препятствует развитию максимальных электросудорожных приступов, ограничивает развитие судорог, включая распространение очага возбуждения от коры головного мозга до подкорковых структур, а также подавляет активность эпилептогенного фокуса. В отличие от фенитоина и карбамазепина, зонисамид обладает избирательным действием на приступы, возникающие в коре головного мозга.
Клиническая эффективность и безопасность.
Монотерапия парциальных судорожных приступов с вторичной генерализацией или без. Эффективность зонисамида в режиме монотерапии у пациентов с впервые диагностированными парциальными эпилептическими приступами с вторичной генерализацией или без, с генерализованными тонико-клоническими приступами без четкой очаговости была показана в двойном слепом, с параллельными группами, исследовании с участием 583 взрослых пациентов по установлению не меньшей эффективности терапии зонисамидом относительно терапии карбамазепином пролонгированного действия, продолжавшемся до 24 мес, в зависимости от ответа на лечение. Осуществлялось повышение дозы до целевого значения 600 мг карбамазепина или 300 мг зонисамида. При наличии у пациентов приступов осуществлялось повышение до следующей дозы, 800 мг карбамазепина или 400 мг зонисамида. Если приступы сохранялись, то дозу увеличивали максимально до 1200 мг для карбамазепина и до 500 мг для зонисамида. Пациенты, у которых приступы отсутствовали в течение 26 нед на фоне приема целевой дозы, продолжали получать эту же дозу в течение еще 26 нед.
Дополнительная терапия парциальных судорожных приступов с вторичной генерализацией или без у взрослых. Эффективность дополнительной терапии зонисамидом была показана в 4 двойных слепых плацебо-контролируемых исследованиях, продолжавшихся до 24 нед. Эти исследования показали снижение медианы частоты возникновения парциальных эпилептических приступов при приеме зонисамида в суточных дозах 300-500 мг 1 или 2 раза в день.
Дополнительная терапия парциальных судорожных приступов с вторичной генерализацией или без у подростков и детей с 6 лет. У детей (в возрасте 6 лет и старше) эффективность зонисамида была продемонстрирована в двойном слепом плацебо-контролируемом исследовании продолжительностью 24 нед при участии 207 пациентов. При 12-недельном применении целевой дозы наблюдалось снижение частоты приступов на 50% и более у 50% пациентов, получавших зонисамид, и 31% пациентов, получавших плацебо.
Особые проблемы безопасности, которые возникли при проведении исследований у детей, включали ухудшение аппетита и снижение массы тела, снижение уровня бикарбонатов, увеличение риска мочекаменной болезни и дегидратацию. Все эти явления, и особенно снижение массы тела, могут неблагоприятно сказываться на росте и развитии ребенка, а также приводить к ухудшению общего состояния здоровья. В целом получен ограниченный объем данных о долговременном влиянии зонисамида на рост и развитие ребенка.
Pharmacokinetics
Всасывание.
Зонисамид почти полностью абсорбируется после перорального приема, maxCmax в плазме достигается в течение 2-5 ч после приема. Выраженность первичного метаболизма незначительна - абсолютная биодоступность оценивается на уровне 100%. Биодоступность зонисамида при приеме внутрь не зависит от приема пищи, хотя при этом может замедляться Тmax в плазме крови.
Величина AUC и maxCmax зонисамида практически линейно увеличиваются после приема однократной дозы (в диапазоне доз 100-800 мг) и после многократного приема (в диапазоне доз 100-400 мг 1 раз в день). Увеличение этих значений при достижении равновесного состояния несколько превышает предполагавшееся, исходя из принятой дозы, возможно, в связи с насыщаемостью связывания зонисамида с эритроцитами. Равновесное состояние достигается в течение 13 дней. Происходит несколько бóльшая аккумуляция, чем это ожидалось, по сравнению с однократным приемом зонисамида.
Распределение.
Зонисамид связывается с белками плазмы на 40-50%, согласно результатам исследований in vitro >in vitro, различные противосудорожные ЛС (фенитоин, фенобарбитал, карбамазепин и натрия вальпроат) не оказывают существенное влияние на степень его связывания с белками плазмы. Кажущийся dVd у взрослых составляет 1,1-1,7 л/кг, что указывает на значительное распределение зонисамида в тканях. Соотношение концентраций зонисамида в эритроцитах и плазме крови составляет около 15:1 при низких его концентрациях и около 3:1 - при высоких.
Метаболизм.
Зонисамид метаболизируется с участием изофермента сYP3A4, основной путь метаболизма - расщепление бензизоксазольного кольца с образованием 2-сульфамоилацетилфенола (SMAP), а также N-ацетилирование. Исходное вещество и SMAP могут связываться с глюкуроновой кислотой. Метаболиты, которые не определяются в плазме крови, лишены противосудорожной активности. Данные о том, что зонисамид способен индуцировать собственный метаболизм, отсутствуют.
Выведение.
Клиренс зонисамида после достижения ssCss достигает 0,7 л/ конечный T1/2 - около 60 ч (при условии отсутствия одновременного приема индукторов активности изофермента сYP3A4). 1/2T1/2 не зависит ни от величины принимаемой дозы, ни от длительности лечения. Колебания концентрации зонисамида в плазме незначительны (<30%). Метаболиты и неизмененный зонисамид выводятся главным образом через почки. Почечный клиренс неизмененного зонисамида сравнительно низок (около 3,5 мл/мин); около 15-30% принятой дозы выводится в неизмененном виде.
Линейность/нелинейность.
Концентрация зонисамида увеличивается до достижения равновесного состояния, что обычно происходит примерно через 8 нед. При сравнении одинакового уровня доз у пациентов с большей массой тела, как правило, достигаются более низкие ssCss в сыворотке, но эти различия незначительны. Возраст (≥12 лет) и пол, скорректированные по массе тела, не оказывают влияние на концентрации зонисамида у пациентов с эпилепсией при достижении его ssCss. Необходимость снижения дозы при применении каких-либо противоэпилептических ЛС, в тч индукторов изофермента сYP3A4, отсутствует.
Соотношение фармакодинамики и фармакокинетики.
Зонисамид снижает среднюю частоту приступов за 28-дневный период, и это снижение пропорционально (лог-линейная зависимость) средней концентрации зонисамида.
Особые группы пациентов.
Почечная недостаточность. У пациентов с почечной недостаточностью почечный клиренс однократных доз зонисамида прямо пропорционален клиренсу креатинина. AUC зонисамида повышена на 35% у пациентов с тяжелой почечной недостаточностью (Cl креатинина <20 мл/мин).
Печеночная недостаточность. Фармакокинетика зонисамида у пациентов с печеночной недостаточностью изучена недостаточно.
Пациенты пожилого возраста. Нет клинически значимых различий в фармакокинетике зонисамида у молодых (21-40 лет) и пожилых (65-75 лет) пациентов.
Дети (5-18 лет). Ограниченные данные показывают, что фармакокинетические параметры зонисамида в суточной дозе 1; 7 или 12 мг/кг у детей и подростков аналогичны таковым у взрослых пациентов (с учетом поправки на массу тела).
Зонисамид почти полностью абсорбируется после перорального приема, maxCmax в плазме достигается в течение 2-5 ч после приема. Выраженность первичного метаболизма незначительна - абсолютная биодоступность оценивается на уровне 100%. Биодоступность зонисамида при приеме внутрь не зависит от приема пищи, хотя при этом может замедляться Тmax в плазме крови.
Величина AUC и maxCmax зонисамида практически линейно увеличиваются после приема однократной дозы (в диапазоне доз 100-800 мг) и после многократного приема (в диапазоне доз 100-400 мг 1 раз в день). Увеличение этих значений при достижении равновесного состояния несколько превышает предполагавшееся, исходя из принятой дозы, возможно, в связи с насыщаемостью связывания зонисамида с эритроцитами. Равновесное состояние достигается в течение 13 дней. Происходит несколько бóльшая аккумуляция, чем это ожидалось, по сравнению с однократным приемом зонисамида.
Распределение.
Зонисамид связывается с белками плазмы на 40-50%, согласно результатам исследований in vitro >in vitro, различные противосудорожные ЛС (фенитоин, фенобарбитал, карбамазепин и натрия вальпроат) не оказывают существенное влияние на степень его связывания с белками плазмы. Кажущийся dVd у взрослых составляет 1,1-1,7 л/кг, что указывает на значительное распределение зонисамида в тканях. Соотношение концентраций зонисамида в эритроцитах и плазме крови составляет около 15:1 при низких его концентрациях и около 3:1 - при высоких.
Метаболизм.
Зонисамид метаболизируется с участием изофермента сYP3A4, основной путь метаболизма - расщепление бензизоксазольного кольца с образованием 2-сульфамоилацетилфенола (SMAP), а также N-ацетилирование. Исходное вещество и SMAP могут связываться с глюкуроновой кислотой. Метаболиты, которые не определяются в плазме крови, лишены противосудорожной активности. Данные о том, что зонисамид способен индуцировать собственный метаболизм, отсутствуют.
Выведение.
Клиренс зонисамида после достижения ssCss достигает 0,7 л/ конечный T1/2 - около 60 ч (при условии отсутствия одновременного приема индукторов активности изофермента сYP3A4). 1/2T1/2 не зависит ни от величины принимаемой дозы, ни от длительности лечения. Колебания концентрации зонисамида в плазме незначительны (<30%). Метаболиты и неизмененный зонисамид выводятся главным образом через почки. Почечный клиренс неизмененного зонисамида сравнительно низок (около 3,5 мл/мин); около 15-30% принятой дозы выводится в неизмененном виде.
Линейность/нелинейность.
Концентрация зонисамида увеличивается до достижения равновесного состояния, что обычно происходит примерно через 8 нед. При сравнении одинакового уровня доз у пациентов с большей массой тела, как правило, достигаются более низкие ssCss в сыворотке, но эти различия незначительны. Возраст (≥12 лет) и пол, скорректированные по массе тела, не оказывают влияние на концентрации зонисамида у пациентов с эпилепсией при достижении его ssCss. Необходимость снижения дозы при применении каких-либо противоэпилептических ЛС, в тч индукторов изофермента сYP3A4, отсутствует.
Соотношение фармакодинамики и фармакокинетики.
Зонисамид снижает среднюю частоту приступов за 28-дневный период, и это снижение пропорционально (лог-линейная зависимость) средней концентрации зонисамида.
Особые группы пациентов.
Почечная недостаточность. У пациентов с почечной недостаточностью почечный клиренс однократных доз зонисамида прямо пропорционален клиренсу креатинина. AUC зонисамида повышена на 35% у пациентов с тяжелой почечной недостаточностью (Cl креатинина <20 мл/мин).
Печеночная недостаточность. Фармакокинетика зонисамида у пациентов с печеночной недостаточностью изучена недостаточно.
Пациенты пожилого возраста. Нет клинически значимых различий в фармакокинетике зонисамида у молодых (21-40 лет) и пожилых (65-75 лет) пациентов.
Дети (5-18 лет). Ограниченные данные показывают, что фармакокинетические параметры зонисамида в суточной дозе 1; 7 или 12 мг/кг у детей и подростков аналогичны таковым у взрослых пациентов (с учетом поправки на массу тела).
Indications for use
Монотерапия пациентов с парциальными эпилептическими приступами с вторичной генерализацией или без. с впервые диагностированной эпилепсией. в составе дополнительной терапии взрослых. подростков и детей с 6 лет с парциальными эпилептическими приступами с вторичной генерализацией или без.
Contraindications
Гиперчувствительность к зонисамиду. сульфонамидам. тяжелая печеночная недостаточность (применение у данной категории пациентов не изучалось). беременность и период грудного вскармливания (данных по безопасности для данной категории пациентов недостаточно ( см «Применение при беременности и кормлении грудью»). одновременное применение у детей с ингибиторами карбоангидразы. такими как топирамат и ацетазоламид. детский возраст до 6 лет (безопасность и эффективность для данной категории не установлены).
Restrictions on use
Пожилой возраст (имеющийся опыт применения ограничен); почечная недостаточность (вследствие ограниченного клинического опыта; может потребоваться более медленный подбор дозы зонисамида); печеночная недостаточность легкой и умеренной степени тяжести (вследствие ограниченного клинического опыта; может потребоваться более медленный подбор дозы зонисамида); одновременное применение взрослыми с игибиторами карбоангидразы, такими как топирамат и ацетазоламид (недостаточно данных, чтобы исключить фармакодинамическое взаимодействие); одновременное применение взрослыми с пирогенными ЛС, включая ингибиторы карбоангидразы и ЛС с антихолинергическим действием; начало лечения, его отмена или изменение дозы зонисамида при одновременном применении с субстратами P-gp (например дигоксин, хинидин); пациенты с массой тела <20 кг (клинический опыт применения ограничен).
Use during pregnancy and lactation
Категория действия на плод по FDA. с.
Женщины с сохраненным детородным потенциалом должны применять надежные методы контрацепции во время лечения зонисамидом и на протяжении 1 мес после его отмены.
Нет достаточных данных о применении зонисамида у беременных женщин. Исследования на животных показали, что зонисамид потенциально обладает репродуктивной токсичностью, риск возникновения которой у людей неизвестен.
Зонисамид не следует применять во время беременности, за исключением тех случаев, когда потенциальные преимущества, по мнению врача, преобладают над возможным риском для плода. Если женщина планирует беременность, следует проанализировать необходимость противосудорожной терапии. В случае назначения зонисамида рекомендуется тщательное наблюдение.
Риск возникновения врожденных пороков развития у детей, чьи матери принимают противоэпилептические ЛС, возрастает в 2-3 раза. Чаще всего выявляются следующие пороки: расщепление верхней губы, аномалии развития ССС и дефекты нервной трубки. Комбинированная терапия противосудорожными ЛС сопровождается повышением риска развития врожденных пороков в сравнении с монотерапией.
Недопустима резкая отмена противосудорожной терапии из-за риска развития эпилептического приступа, который может привести к серьезным последствиям как для матери, так и для ребенка.
Зонисамид выделяется с грудным молоком в концентрациях, аналогичных таковым в плазме, поэтому следует принять решение о прекращении кормления грудью или об отмене зонисамида у кормящих матерей. Вследствие длительного Т1/2, грудное вскармливание может быть возобновлено не ранее чем через месяц после отмены зонисамида.
Женщины с сохраненным детородным потенциалом должны применять надежные методы контрацепции во время лечения зонисамидом и на протяжении 1 мес после его отмены.
Нет достаточных данных о применении зонисамида у беременных женщин. Исследования на животных показали, что зонисамид потенциально обладает репродуктивной токсичностью, риск возникновения которой у людей неизвестен.
Зонисамид не следует применять во время беременности, за исключением тех случаев, когда потенциальные преимущества, по мнению врача, преобладают над возможным риском для плода. Если женщина планирует беременность, следует проанализировать необходимость противосудорожной терапии. В случае назначения зонисамида рекомендуется тщательное наблюдение.
Риск возникновения врожденных пороков развития у детей, чьи матери принимают противоэпилептические ЛС, возрастает в 2-3 раза. Чаще всего выявляются следующие пороки: расщепление верхней губы, аномалии развития ССС и дефекты нервной трубки. Комбинированная терапия противосудорожными ЛС сопровождается повышением риска развития врожденных пороков в сравнении с монотерапией.
Недопустима резкая отмена противосудорожной терапии из-за риска развития эпилептического приступа, который может привести к серьезным последствиям как для матери, так и для ребенка.
Зонисамид выделяется с грудным молоком в концентрациях, аналогичных таковым в плазме, поэтому следует принять решение о прекращении кормления грудью или об отмене зонисамида у кормящих матерей. Вследствие длительного Т1/2, грудное вскармливание может быть возобновлено не ранее чем через месяц после отмены зонисамида.
Side effects
Опыт применения зонисамида включает клинические исследования более чем 1200 пациентов, 400 из которых получали зонисамид на протяжении не менее года, а также широкое постмаркетинговое применение (в Японии с 1989 г., в США - с 2000 г.
Зонисамид содержит сульфонамидную группу. К серьезным побочным реакциям со стороны иммунной системы. связанным с приемом ЛС. которые содержат сульфонамидную группу. относятся появление кожной сыпи и других аллергических реакций. а также развитие выраженных гематологических нарушений. в тч апластической анемии. в очень редких случаях приводящей к летальному исходу ( см «Меры предосторожности»).
Наиболее частыми нежелательными реакциями в контролируемых исследованиях комплексной терапии были сонливость, головокружение и анорексия. Наиболее частыми нежелательными реакциями в рандомизированном контролируемом исследовании монотерапии зонисамидом в сравнении с карбамазепином пролонгированного высвобождения в группе пациентов. получавших зонисамид. были снижение уровня бикарбонатов. потеря аппетита и снижение массы тела. Частота значительного снижения уровня бикарбонатов в сыворотке (снижение до уровня менее 17 мЭкв/л и более 5 мЭкв/л) составляла 3,8%. Частота значительного снижения массы тела на 20% и более составляла 0,7%.
Частота возникновения определялась как очень часто (≥1/10); часто (≥1/100, <1/10); нечасто (≥1/1000, <1/100) и очень редко (<1/10000).
Ниже представлены побочные реакции, выявленные в ходе клинических исследований комплексной терапии и постмаркетинговых наблюдений.
Инфекционные и паразитарные заболевания. Нечасто - пневмония, урогенитальные инфекции.
Со стороны крови и лимфатической системы. Часто - экхимоз. очень редко - агранулоцитоз. апластическая анемия. лейкоцитоз. лейкопения. лимфаденопатия. панцитопения. тромбоцитопения.
Со стороны иммунной системы. Часто - реакции гиперчувствительности; очень редко - синдром гиперчувствительности к зонисамиду, лекарственная сыпь с эозинофилией и системными симптомами.
Со стороны обмена веществ и питания. Очень часто - анорексия; нечасто - гипокалиемия; очень редко - метаболический ацидоз, тубулярный почечный ацидоз.
Со стороны психики. Очень часто - возбуждение. раздражительность. спутанность сознания. депрессия. часто - аффективная лабильность. тревожность. бессонница. психотические расстройства. нечасто - гнев. агрессия. суицидальные мысли и попытки. очень редко - галлюцинации.
Со стороны нервной системы. Очень часто - атаксия. головокружение. снижение памяти. сонливость. часто - брадифрения. нарушение внимания. нистагм. парестезия. нарушение речи. тремор. нечасто - судороги. очень редко - амнезия. кома. большие эпилептические приступы. миастенический синдром. злокачественный нейролептический синдром. эпилептический статус.
Со стороны органа зрения. Очень часто - диплопия.
Со стороны дыхательной системы, органов грудной клетки и средостения. Очень редко - одышка, аспирационная пневмония, нарушение дыхания, гиперчувствительный пневмонит.
Со стороны ЖКТ. Часто - боль в животе. запор. диарея. диспепсия. тошнота. нечасто - рвота. очень редко - панкреатит.
Со стороны печени и желчевыводящих путей. Нечасто - холецистит, холелитиаз; очень редко - гепатоцеллюлярные повреждения.
Со стороны кожи и подкожных тканей. Часто - сыпь. зуд. алопеция. очень редко - ангидроз. мультиформная эритема. синдром Стивенса-Джонсона. токсический эпидермальный некролиз.
Со стороны мышечно-скелетной и соединительной ткани. Очень редко - рабдомиолиз.
Со стороны почек и мочевыводящих путей. Часто - нефролитиаз; нечасто - уролитиаз; очень редко - гидронефроз, почечная недостаточность, нарушение состава мочи.
Общие расстройства и нарушения в месте введения. Часто - повышенная утомляемость, гриппоподобные состояния, повышение температуры тела, периферический отек.
Лабораторные и инструментальные данные. Очень часто - снижение уровня бикарбонатов. часто - снижение веса. очень редко - повышение уровня КФК. повышение уровня креатинина. повышение уровня мочевины. нарушение биохимических показателей функции печени.
Травмы, интоксикации и осложнения манипуляций. Очень редко - тепловой удар.
Описаны единичные случаи внезапной необъяснимой смерти пациентов с эпилепсией (SUDEP - Sudden Unexpected Death in Epilepsy), принимавших зонисамид.
Ниже представлены побочные реакции, выявленные в рандомизированном контролируемом исследовании монотерапии зонисамидом в сравнении с карбамазепином пролонгированного высвобождения.
Инфекционные и паразитарные заболевания. Нечасто - урогенитальные инфекции, пневмония.
Со стороны крови и лимфатической системы. Нечасто - лейкопения, тромбоцитопения.
Со стороны обмена веществ и питания. Часто - снижение аппетита; нечасто - гипокалиемия.
Со стороны психики. Часто - возбуждение. депрессия. бессонница. эмоциональная лабильность. тревожность. нечасто - спутанность сознания. острый психоз. агрессивность. суицидальные мысли. галлюцинации.
Со стороны нервной системы. Часто - атаксия. головокружение. снижение памяти. сонливость. брадифрения. нарушение внимания. парестезии. нечасто - нистагм. нарушение речи. тремор. судороги.
Со стороны органа зрения. Часто - диплопия.
Со стороны дыхательной системы, органов грудной клетки и средостения. Нечасто - нарушение дыхания.
Со стороны ЖКТ. Часто - запор. диарея. диспепсия. тошнота. рвота. нечасто - боль в животе.
Со стороны печени и желчевыводящих путей. Нечасто - острый холецистит.
Со стороны кожи и подкожных тканей. Часто - сыпь; нечасто - зуд, экхимоз.
Общие расстройства и нарушения в месте введения. Часто - повышенная утомляемость, повышение температуры тела, раздражительность.
Лабораторные и инструментальные данные. Очень часто - снижение уровня бикарбонатов. часто - снижение веса. повышение уровня КФК. повышение уровня АЛТ. повышение уровня АСТ. нечасто - отклонение от нормы данных исследования мочи.
Дополнительная информация по безопасности в особых группах пациентов.
Пациенты пожилого возраста. Сводный анализ данных по безопасности у 95 пациентов пожилого возраста показал относительно более высокую частоту развития периферического отека и зуда в сравнении с более молодыми пациентами.
Обзор постмаркетинговых данных по переносимости терапии зонисамидом у пожилых пациентов (старше 65 лет) позволяет предположить. что у данной категории пациентов развитие синдрома Стивенса-Джонсона и реакция лекарственной гиперчувствительности выявляются чаще. чем в общей популяции.
Дети. Профиль безопасности зонисамида у детей, участвовавших в плацебо-контролируемых клинических исследованиях (в возрасте от 6 до 17 лет), соответствует профилю безопасности у взрослых. Из 465 пациентов. включенных в базу данных по безопасности (в тч 67 пациентов. продолжавших участие в открытой фазе продолженного контролируемого клинического исследования). летальный исход наступил у 7 детей (1,5%. 14,6/1000 пациенто-лет): в 2 случаях в результате эпилептического статуса. из которых один был связан со значительным снижением массы тела (на 10% в течение 3 мес) у пациента с низкой массой тела. с последующей отменой зонисамида. в 1 случае в результате ЧМТ/гематомы и в 4 случаях летальные исходы произошли у пациентов с предшествующим функциональным неврологическим дефицитом различного генеза (2 случая сепсиса. связанного с пневмонией/полиорганной недостаточностью. 1 случай SUDEP и 1 случай ЧМТ). В общей сложности. из 70,4% пациентов. которые в контролируемом исследовании или открытой фазе продолжения этого исследования получали зонисамид. во время терапии по меньшей мере однократно определялся уровень бикарбонатов менее 22 ммоль/л. Низкий уровень бикарбонатов сохранялся в течение длительного периода времени (медиана - 188 дней).
В сводном анализе данных по безопасности. полученных у 420 детей (183 в возрасте от 6 до 11 лет и 237 в возрасте от 12 до 16 лет. у которых средняя продолжительность приема зонисамида составляла примерно 12 мес). было установлено относительно более частое поступление сообщений о возникновении пневмонии. дегидратации. снижения потоотделения. нарушение биохимических показателей функции печени. среднего отита. фарингита. синусита и инфекций верхних дыхательных путей. кашля. носового кровотечения и ринита. боли в животе. рвоты. сыпи и экземы. а также лихорадки по сравнению со взрослыми пациентами (особенно у лиц младше 12 лет). С более низкой частотой поступали сообщения о возникновении амнезии, повышении уровней креатинина, лимфаденопатии и тромбоцитопении. Частота снижения массы тела на 10% и более составляла 10,7% ( см «Меры предосторожности»). В некоторых случаях снижения массы тела наблюдалась задержка при переходе к следующей стадии Таннера и созревания костной ткани.
Извещение о нежелательных реакциях.
Крайне важно извещать о нежелательных реакциях, возникших во время пострегистрационного применения ЛС. Это позволит контролировать соотношение пользы и риска ЛС. Медицинским работникам необходимо сообщать о возникновении любых нежелательных реакций.
Зонисамид содержит сульфонамидную группу. К серьезным побочным реакциям со стороны иммунной системы. связанным с приемом ЛС. которые содержат сульфонамидную группу. относятся появление кожной сыпи и других аллергических реакций. а также развитие выраженных гематологических нарушений. в тч апластической анемии. в очень редких случаях приводящей к летальному исходу ( см «Меры предосторожности»).
Наиболее частыми нежелательными реакциями в контролируемых исследованиях комплексной терапии были сонливость, головокружение и анорексия. Наиболее частыми нежелательными реакциями в рандомизированном контролируемом исследовании монотерапии зонисамидом в сравнении с карбамазепином пролонгированного высвобождения в группе пациентов. получавших зонисамид. были снижение уровня бикарбонатов. потеря аппетита и снижение массы тела. Частота значительного снижения уровня бикарбонатов в сыворотке (снижение до уровня менее 17 мЭкв/л и более 5 мЭкв/л) составляла 3,8%. Частота значительного снижения массы тела на 20% и более составляла 0,7%.
Частота возникновения определялась как очень часто (≥1/10); часто (≥1/100, <1/10); нечасто (≥1/1000, <1/100) и очень редко (<1/10000).
Ниже представлены побочные реакции, выявленные в ходе клинических исследований комплексной терапии и постмаркетинговых наблюдений.
Инфекционные и паразитарные заболевания. Нечасто - пневмония, урогенитальные инфекции.
Со стороны крови и лимфатической системы. Часто - экхимоз. очень редко - агранулоцитоз. апластическая анемия. лейкоцитоз. лейкопения. лимфаденопатия. панцитопения. тромбоцитопения.
Со стороны иммунной системы. Часто - реакции гиперчувствительности; очень редко - синдром гиперчувствительности к зонисамиду, лекарственная сыпь с эозинофилией и системными симптомами.
Со стороны обмена веществ и питания. Очень часто - анорексия; нечасто - гипокалиемия; очень редко - метаболический ацидоз, тубулярный почечный ацидоз.
Со стороны психики. Очень часто - возбуждение. раздражительность. спутанность сознания. депрессия. часто - аффективная лабильность. тревожность. бессонница. психотические расстройства. нечасто - гнев. агрессия. суицидальные мысли и попытки. очень редко - галлюцинации.
Со стороны нервной системы. Очень часто - атаксия. головокружение. снижение памяти. сонливость. часто - брадифрения. нарушение внимания. нистагм. парестезия. нарушение речи. тремор. нечасто - судороги. очень редко - амнезия. кома. большие эпилептические приступы. миастенический синдром. злокачественный нейролептический синдром. эпилептический статус.
Со стороны органа зрения. Очень часто - диплопия.
Со стороны дыхательной системы, органов грудной клетки и средостения. Очень редко - одышка, аспирационная пневмония, нарушение дыхания, гиперчувствительный пневмонит.
Со стороны ЖКТ. Часто - боль в животе. запор. диарея. диспепсия. тошнота. нечасто - рвота. очень редко - панкреатит.
Со стороны печени и желчевыводящих путей. Нечасто - холецистит, холелитиаз; очень редко - гепатоцеллюлярные повреждения.
Со стороны кожи и подкожных тканей. Часто - сыпь. зуд. алопеция. очень редко - ангидроз. мультиформная эритема. синдром Стивенса-Джонсона. токсический эпидермальный некролиз.
Со стороны мышечно-скелетной и соединительной ткани. Очень редко - рабдомиолиз.
Со стороны почек и мочевыводящих путей. Часто - нефролитиаз; нечасто - уролитиаз; очень редко - гидронефроз, почечная недостаточность, нарушение состава мочи.
Общие расстройства и нарушения в месте введения. Часто - повышенная утомляемость, гриппоподобные состояния, повышение температуры тела, периферический отек.
Лабораторные и инструментальные данные. Очень часто - снижение уровня бикарбонатов. часто - снижение веса. очень редко - повышение уровня КФК. повышение уровня креатинина. повышение уровня мочевины. нарушение биохимических показателей функции печени.
Травмы, интоксикации и осложнения манипуляций. Очень редко - тепловой удар.
Описаны единичные случаи внезапной необъяснимой смерти пациентов с эпилепсией (SUDEP - Sudden Unexpected Death in Epilepsy), принимавших зонисамид.
Ниже представлены побочные реакции, выявленные в рандомизированном контролируемом исследовании монотерапии зонисамидом в сравнении с карбамазепином пролонгированного высвобождения.
Инфекционные и паразитарные заболевания. Нечасто - урогенитальные инфекции, пневмония.
Со стороны крови и лимфатической системы. Нечасто - лейкопения, тромбоцитопения.
Со стороны обмена веществ и питания. Часто - снижение аппетита; нечасто - гипокалиемия.
Со стороны психики. Часто - возбуждение. депрессия. бессонница. эмоциональная лабильность. тревожность. нечасто - спутанность сознания. острый психоз. агрессивность. суицидальные мысли. галлюцинации.
Со стороны нервной системы. Часто - атаксия. головокружение. снижение памяти. сонливость. брадифрения. нарушение внимания. парестезии. нечасто - нистагм. нарушение речи. тремор. судороги.
Со стороны органа зрения. Часто - диплопия.
Со стороны дыхательной системы, органов грудной клетки и средостения. Нечасто - нарушение дыхания.
Со стороны ЖКТ. Часто - запор. диарея. диспепсия. тошнота. рвота. нечасто - боль в животе.
Со стороны печени и желчевыводящих путей. Нечасто - острый холецистит.
Со стороны кожи и подкожных тканей. Часто - сыпь; нечасто - зуд, экхимоз.
Общие расстройства и нарушения в месте введения. Часто - повышенная утомляемость, повышение температуры тела, раздражительность.
Лабораторные и инструментальные данные. Очень часто - снижение уровня бикарбонатов. часто - снижение веса. повышение уровня КФК. повышение уровня АЛТ. повышение уровня АСТ. нечасто - отклонение от нормы данных исследования мочи.
Дополнительная информация по безопасности в особых группах пациентов.
Пациенты пожилого возраста. Сводный анализ данных по безопасности у 95 пациентов пожилого возраста показал относительно более высокую частоту развития периферического отека и зуда в сравнении с более молодыми пациентами.
Обзор постмаркетинговых данных по переносимости терапии зонисамидом у пожилых пациентов (старше 65 лет) позволяет предположить. что у данной категории пациентов развитие синдрома Стивенса-Джонсона и реакция лекарственной гиперчувствительности выявляются чаще. чем в общей популяции.
Дети. Профиль безопасности зонисамида у детей, участвовавших в плацебо-контролируемых клинических исследованиях (в возрасте от 6 до 17 лет), соответствует профилю безопасности у взрослых. Из 465 пациентов. включенных в базу данных по безопасности (в тч 67 пациентов. продолжавших участие в открытой фазе продолженного контролируемого клинического исследования). летальный исход наступил у 7 детей (1,5%. 14,6/1000 пациенто-лет): в 2 случаях в результате эпилептического статуса. из которых один был связан со значительным снижением массы тела (на 10% в течение 3 мес) у пациента с низкой массой тела. с последующей отменой зонисамида. в 1 случае в результате ЧМТ/гематомы и в 4 случаях летальные исходы произошли у пациентов с предшествующим функциональным неврологическим дефицитом различного генеза (2 случая сепсиса. связанного с пневмонией/полиорганной недостаточностью. 1 случай SUDEP и 1 случай ЧМТ). В общей сложности. из 70,4% пациентов. которые в контролируемом исследовании или открытой фазе продолжения этого исследования получали зонисамид. во время терапии по меньшей мере однократно определялся уровень бикарбонатов менее 22 ммоль/л. Низкий уровень бикарбонатов сохранялся в течение длительного периода времени (медиана - 188 дней).
В сводном анализе данных по безопасности. полученных у 420 детей (183 в возрасте от 6 до 11 лет и 237 в возрасте от 12 до 16 лет. у которых средняя продолжительность приема зонисамида составляла примерно 12 мес). было установлено относительно более частое поступление сообщений о возникновении пневмонии. дегидратации. снижения потоотделения. нарушение биохимических показателей функции печени. среднего отита. фарингита. синусита и инфекций верхних дыхательных путей. кашля. носового кровотечения и ринита. боли в животе. рвоты. сыпи и экземы. а также лихорадки по сравнению со взрослыми пациентами (особенно у лиц младше 12 лет). С более низкой частотой поступали сообщения о возникновении амнезии, повышении уровней креатинина, лимфаденопатии и тромбоцитопении. Частота снижения массы тела на 10% и более составляла 10,7% ( см «Меры предосторожности»). В некоторых случаях снижения массы тела наблюдалась задержка при переходе к следующей стадии Таннера и созревания костной ткани.
Извещение о нежелательных реакциях.
Крайне важно извещать о нежелательных реакциях, возникших во время пострегистрационного применения ЛС. Это позволит контролировать соотношение пользы и риска ЛС. Медицинским работникам необходимо сообщать о возникновении любых нежелательных реакций.
Interaction
Ферменты системы цитохрома Р450.
Изучение влияния зонисамида in vitro >in vitro на микросомальное окисление в гепатоцитах человека показали отсутствие значимого влияния (<25%) на активность изоферментов цитохрома P450 сYP1A2, сYP2A6, сYP2B6, сYP2C8, сYP2C9, сYP2C19, сYP2D6, сYP2E1 и сYP3A4 при концентрациях зонисамида в плазме крови, в 2 раза и более превышающих терапевтические. Маловероятно, что зонисамид будет влиять на фармакокинетику других ЛС через механизмы, связанные с цитохромом P450, это продемонстрировано in vivo >in vivo для карбамазепина, фенитоина, этинилэстрадиола и дезипрамина.
Потенциально возможное влияние зонисамида на действие других ЛС.
Другие противоэпилептические ЛС. У пациентов с эпилепсией длительный прием зонисамида не оказывает влияние на фармакокинетику карбамазепина, ламотриджина, фенитоина и вальпроата натрия.
Ингибиторы карбоангидразы. Следует соблюдать осторожность при совместном назначении зонисамида с ингибиторами карбоангидразы (например топирамат и ацетазоламид), недостаточно данных для того, чтобы исключить фармакодинамическое взаимодействие ( см «Меры предосторожности»).
Зонисамид не следует назначать детям одновременно с ингибиторами карбоангидразы, такими как топиромат и ацетазоламид ( см «Меры предосторожности»).
Пероральные контрацептивы. Прием зонисамида и КОК в рекомендованных дозах не влияет на концентрацию в сыворотке крови этинилэстрадиола или норэтистерона.
Субстраты P-gp. Результаты исследований in vitro >in vitro показывают, что зонисамид является слабым ингибитором P-gp (белка лекарственной мультирезистентности (MDR1) с IC50 - 267 мкМоль/л, в силу чего существует теоретическая возможность влияния зонисамида на фармакокинетику ЛС, которые являются субстратами P-gp. Рекомендуется с осторожностью начинать или останавливать лечение или изменять дозу зонисамида у пациентов, которые также принимают ЛС, являющиеся субстратами P-gp (например дигоксин, хинидин).
Потенциально возможное влияние других ЛС на действие зонисамида.
При одновременном применении с ламотриджином не выявлено значимое влияние на фармакокинетику зонисамида. При одновременном назначении зонисамида с ЛС, которые могут вызвать развитие мочекаменной болезни, повышается риск развития нефроуролитиаза, в связи с чем следует избегать их одновременного применения.
Зонисамид метаболизируется с участием изофермента сYP3A4 и N-ацетил-трансфераз, а также через конъюгацию с глюкуроновой кислотой. Следовательно, ЛС, которые индуцируют или ингибируют эти ферменты, могут оказывать влияние на фармакокинетику зонисамида.
Индукторы ферментов. Концентрация зонисамида в крови снижается при одновременном приеме ЛС, повышающих активность изофермента сYP3A4 (например фенитоин, карбамазепин и фенобарбитал). Эти эффекты не являются клинически значимыми в случаях, когда зонисамид присоединяется к уже получаемой терапии, однако клинически значимые изменения концентрации зонисамида возможны при отмене, изменении режима дозирования или дополнительном назначении ЛС, индицирующих изофермент сYP3A4 (может потребоваться коррекция дозы зонисамида). Рифампицин является мощным индуктором изофермента сYP3A4, если требуется его совместное назначение с зонисамидом, следует тщательно контролировать состояние пациента, при необходимости корректируя дозу зонисамида.
Ингибиторы ферментов. Клинические данные не показали значимое влияние ингибиторов изофермента сYP3A4 на фармакокинетические параметры зонисамида. Назначение кетоконазола (400 мг/сут) или циметидина (1200 мг/сут) не оказывало клинически значимое воздействие на фармакокинетику зонисамида, принимаемого здоровыми добровольцами (изменение режима дозирования зонисамида при сочетанном приеме с ингибиторами изофермента сYP3A4 не требуется).
Дети.
Исследования лекарственного взаимодействия у детей не проводились.
Изучение влияния зонисамида in vitro >in vitro на микросомальное окисление в гепатоцитах человека показали отсутствие значимого влияния (<25%) на активность изоферментов цитохрома P450 сYP1A2, сYP2A6, сYP2B6, сYP2C8, сYP2C9, сYP2C19, сYP2D6, сYP2E1 и сYP3A4 при концентрациях зонисамида в плазме крови, в 2 раза и более превышающих терапевтические. Маловероятно, что зонисамид будет влиять на фармакокинетику других ЛС через механизмы, связанные с цитохромом P450, это продемонстрировано in vivo >in vivo для карбамазепина, фенитоина, этинилэстрадиола и дезипрамина.
Потенциально возможное влияние зонисамида на действие других ЛС.
Другие противоэпилептические ЛС. У пациентов с эпилепсией длительный прием зонисамида не оказывает влияние на фармакокинетику карбамазепина, ламотриджина, фенитоина и вальпроата натрия.
Ингибиторы карбоангидразы. Следует соблюдать осторожность при совместном назначении зонисамида с ингибиторами карбоангидразы (например топирамат и ацетазоламид), недостаточно данных для того, чтобы исключить фармакодинамическое взаимодействие ( см «Меры предосторожности»).
Зонисамид не следует назначать детям одновременно с ингибиторами карбоангидразы, такими как топиромат и ацетазоламид ( см «Меры предосторожности»).
Пероральные контрацептивы. Прием зонисамида и КОК в рекомендованных дозах не влияет на концентрацию в сыворотке крови этинилэстрадиола или норэтистерона.
Субстраты P-gp. Результаты исследований in vitro >in vitro показывают, что зонисамид является слабым ингибитором P-gp (белка лекарственной мультирезистентности (MDR1) с IC50 - 267 мкМоль/л, в силу чего существует теоретическая возможность влияния зонисамида на фармакокинетику ЛС, которые являются субстратами P-gp. Рекомендуется с осторожностью начинать или останавливать лечение или изменять дозу зонисамида у пациентов, которые также принимают ЛС, являющиеся субстратами P-gp (например дигоксин, хинидин).
Потенциально возможное влияние других ЛС на действие зонисамида.
При одновременном применении с ламотриджином не выявлено значимое влияние на фармакокинетику зонисамида. При одновременном назначении зонисамида с ЛС, которые могут вызвать развитие мочекаменной болезни, повышается риск развития нефроуролитиаза, в связи с чем следует избегать их одновременного применения.
Зонисамид метаболизируется с участием изофермента сYP3A4 и N-ацетил-трансфераз, а также через конъюгацию с глюкуроновой кислотой. Следовательно, ЛС, которые индуцируют или ингибируют эти ферменты, могут оказывать влияние на фармакокинетику зонисамида.
Индукторы ферментов. Концентрация зонисамида в крови снижается при одновременном приеме ЛС, повышающих активность изофермента сYP3A4 (например фенитоин, карбамазепин и фенобарбитал). Эти эффекты не являются клинически значимыми в случаях, когда зонисамид присоединяется к уже получаемой терапии, однако клинически значимые изменения концентрации зонисамида возможны при отмене, изменении режима дозирования или дополнительном назначении ЛС, индицирующих изофермент сYP3A4 (может потребоваться коррекция дозы зонисамида). Рифампицин является мощным индуктором изофермента сYP3A4, если требуется его совместное назначение с зонисамидом, следует тщательно контролировать состояние пациента, при необходимости корректируя дозу зонисамида.
Ингибиторы ферментов. Клинические данные не показали значимое влияние ингибиторов изофермента сYP3A4 на фармакокинетические параметры зонисамида. Назначение кетоконазола (400 мг/сут) или циметидина (1200 мг/сут) не оказывало клинически значимое воздействие на фармакокинетику зонисамида, принимаемого здоровыми добровольцами (изменение режима дозирования зонисамида при сочетанном приеме с ингибиторами изофермента сYP3A4 не требуется).
Дети.
Исследования лекарственного взаимодействия у детей не проводились.
Overdose
Симптомы. Отмечались случаи намеренной и непреднамеренной передозировки зонисамида у взрослых и детей. В некоторых случаях передозировка протекала бессимптомно, особенно при немедленном промывании желудка. В других случаях передозировка сопровождалась следующими симптомами: сонливость. тошнота. симптомы гастрита. нистагм. миоклонус. кома. брадикардия. нарушение функции почек. артериальная гипотензия и угнетение функции дыхания. Очень высокая концентрация зонисамида в плазме крови (100,1 мкг/мл) отмечалась приблизительно через 31 ч после передозировки зонисамида и клоназепама. В данном случае у пациента развились кома и угнетение дыхания. Однако через 5 дней он пришел в сознание, и у него не отмечалось никаких осложнений.
Лечение: специфичного антидота для лечения передозировки зонисамида не существует. После предполагаемой передозировки показано немедленное промывание желудка на фоне обычных мер, направленных на поддержание проходимости дыхательных путей. Проводят поддерживающую терапию, включая регулярный контроль основных показателей состояния организма и тщательное наблюдение. Зонисамид имеет длительный 1/2T1/2, в связи с чем симптомы его передозировки могут иметь стойкий характер. Исследований лечения передозировки не проводилось. вместе с тем известно. что гемодиализ снижает концентрацию зонисамида в плазме крови у пациентов с почечной недостаточностью и может рассматриваться в качестве средства лечения передозировки.
Лечение: специфичного антидота для лечения передозировки зонисамида не существует. После предполагаемой передозировки показано немедленное промывание желудка на фоне обычных мер, направленных на поддержание проходимости дыхательных путей. Проводят поддерживающую терапию, включая регулярный контроль основных показателей состояния организма и тщательное наблюдение. Зонисамид имеет длительный 1/2T1/2, в связи с чем симптомы его передозировки могут иметь стойкий характер. Исследований лечения передозировки не проводилось. вместе с тем известно. что гемодиализ снижает концентрацию зонисамида в плазме крови у пациентов с почечной недостаточностью и может рассматриваться в качестве средства лечения передозировки.
Method of drug use and dosage
Внутрь.
Взрослые пациенты. Зонисамид может назначаться взрослым в виде монотерапии и в качестве дополнения к уже назначенному лечению. Доза подбирается с учетом лечебного эффекта.
Подростки и дети с 6 лет. Зонисамид может назначаться детям с 6 лет в качестве дополнения к уже назначенному лечению. Доза подбирается с учетом клинического эффекта.
Взрослые пациенты. Зонисамид может назначаться взрослым в виде монотерапии и в качестве дополнения к уже назначенному лечению. Доза подбирается с учетом лечебного эффекта.
Подростки и дети с 6 лет. Зонисамид может назначаться детям с 6 лет в качестве дополнения к уже назначенному лечению. Доза подбирается с учетом клинического эффекта.
Application precautions
Кожные высыпания.
При терапии зонисамидом сообщалось о развитии тяжелых кожных реакций, включая синдром Стивенса-Джонсона и токсический эпидермальный некролиз.
Рекомендуется отмена зонисамида у пациентов, у которых появились кожные высыпания, и которые невозможно объяснить другими причинами. Все пациенты с появлением высыпаний на коже во время приема зонисамида должны находиться под тщательным наблюдением, особенно пациенты с одновременным назначением других противоэпилептических ЛС, которые сами способны вызывать кожные высыпания.
Синдром отмены.
Отмену зонисамида производят путем постепенного снижения дозы во избежание возникновения эпилептических приступов. Недостаточно данных об отмене одновременно применяемых противоэпилептических ЛС после достижения контроля над приступами при применении зонисамида в рамках вспомогательной терапии для перехода к монотерапии зонисамидом. Поэтому отмена сопутствующего противоэпилептического лечения должна проводиться с осторожностью.
Реакции, связанные с наличием сульфонамидной группы.
Зонисамид содержит сульфонамидную группу. К серьезным побочным реакциям со стороны иммунной системы, связанным с приемом ЛС, которые содержат сульфонамидную группу, относятся появление кожной сыпи и других аллергических реакций, а также развитие выраженных гематологических нарушений, в тч апластической анемии, в очень редких случаях приводящей к летальному исходу.
Сообщалось о развитии случаев агранулоцитоза, тромбоцитопении, лейкопении, апластической анемии, панцитопении и лейкоцитоза. Информации для оценки возможной взаимосвязи этих явлений с величиной принимаемой дозы зонисамида и продолжительностью лечения недостаточно.
Суицидальное мышление и поведение.
Развитие суицидального мышления и поведения возможно у пациентов, принимавших противоэпилептические ЛС по ряду показаний. Метаанализ рандомизированных плацебо-контролируемых исследований противоэпилептических ЛС также показал повышенный риск возникновения суицидальных мыслей и поведения.
Механизм этого явления неизвестен, имеющиеся данные не исключают возможности повышенного риска формирования суицидального поведения и на фоне приема зонисамида.
Необходимо наблюдать за пациентами на предмет появления суицидальных мыслей и поведения, а также предусмотреть соответствующее лечение. Пациентам (и ухаживающим за ними лицам) следует рекомендовать обратиться за врачебной помощью при появлении суицидальных мыслей и поведения.
Панкреатит.
При развитии у пациентов признаков панкреатита на фоне приема зонисамида необходим мониторинг уровня панкреатических липаз и амилазы. В случае подтвержденного панкреатита при отсутствии других очевидных причин рекомендуется отмена зонисамида и назначение соответствующего лечения.
Рабдомиолиз.
При развитии у пациентов, принимающих зонисамид, сильных мышечных болей и/или слабости, особенно сопровождающихся лихорадкой, требуется оценка содержания маркеров повреждения мышц, включая уровень КФК и альдолазы. При их повышении, в отсутствие других очевидных причин, таких как травма или большой эпилептический приступ, рекомендуется отмена зонисамида и назначение соответствующего лечения.
Женщины с сохраненным детородным потенциалом.
Женщины с сохраненным детородным потенциалом должны применять надежные методы контрацепции во время лечения зонисамидом и на протяжении 1 мес после его отмены ( см «Применение при беременности и кормлении грудью»).
Тепловой удар и дегидратация.
Случаи снижения потоотделения и повышения температуры тела зафиксированы в основном у пациентов до 18 лет. В ряде случаев возникал тепловой удар, требовавший стационарного лечения. Большинство случаев происходило в условиях высокой температуры окружающей среды. Пациенты и/или ухаживающие за ними лица должны быть предупреждены о необходимости поддерживать адекватную гидратацию организма и избегать воздействия повышенных температур. Необходимо соблюдать осторожность при назначении зонисамида одновременно с ЛС, способствующими перегреванию организма, включая ингибиторы карбоангидразы и холиноблокаторы.
Профилактика перегревания и дегидратации у детей. Зонисамид может вызывать снижение потоотделения и приводить к перегреванию, а при отсутствии соответствующей помощи у ребенка может произойти поражение головного мозга и летальный исход. Дети подвержены высокому риску, особенно в жаркую погоду.
Если ребенок принимает зонисамид, следует избегать перегревания и избегать значительной физической нагрузки, особенно в жаркую погоду; увеличить потребление воды; не применять следующие ЛС: ингибиторы карбоангидразы (такие как топирамат и ацетазоламид) и антихолинергические ЛС (такие как кломипрамин, гидроксизин, дифенгидрамин, галоперидол, имипрамин и оксибутинин).
При возникновении какого-либо из нижеперечисленных симптомов, следует немедленно обратиться за медицинской помощью: ощущение сильного жара от кожи при незначительном потоотделении или при его отсутствии, при возникновении у ребенка спутанности сознания, мышечных спазмов, при учащении сердцебиения или дыхания. Необходимо поместить ребенка в прохладное затененное место; смочить кожу водой, чтобы охладить ее; дать выпить прохладной воды.
Сообщалось о случаях снижения потоотделения и повышения температуры тела, главным образом у детей. В некоторых случаях возникал тепловой удар, требующий госпитализации. В ряде случаев сообщалось о тепловом ударе с летальным исходом. В большинстве случаев явление возникало при теплой погоде. Следует предупредить пациента и лиц, осуществляющих уход за ними, о возможной серьезности теплового удара, ситуациях, когда он может возникнуть, а также мерах, которые необходимо предпринять в случае появления каких-либо признаков или симптомов. Пациентов или лиц, осуществляющих уход за ними, необходимо предупредить о необходимости употребления достаточного объема жидкости и избегания чрезмерных физических нагрузок, в зависимости от состояния пациента. В случае появления признаков и симптомов дегидратации, олигогидроза или повышения температуры тела, следует рассмотреть вопрос об отмене зонисамида.
Зонисамид не следует применять у детей, одновременно получающих другие ЛС, при применении которых у пациентов возникает предрасположенность к появлению нарушений, связанных с воздействием избыточного тепла; сюда относятся ингибиторы карбоангидразы и ЛС с антихолинергическим действием.
Снижение массы тела.
Зонисамид может вызывать снижение массы тела, поэтому во время лечения пациентов с пониженной массой тела или при ее снижении необходимо назначение пищевых добавок и усиленного питания. При выраженном снижении массы тела следует рассмотреть возможность отмены зонисамида. Снижение массы тела у детей может быть более выраженным.
Дети. Описывались случаи снижения массы тела, которые приводили к ухудшению общего состояния и прекращению применения противоэпилептического ЛС, приводящие к летальному исходу. Применение зонисамида не рекомендуется у детей с пониженной массой тела или плохим аппетитом.
Частота снижения массы тела одинакова в различных возрастных группах, тем не менее учитывая возможную серьезность снижения массы тела у детей, у этой группы пациентов необходимо контролировать массу тела. При задержке прибавки массы тела у пациента, исходя из карт физического развития, рекомендуется пересмотреть рацион питания или увеличить количество принимаемой пищи, в противном случае следует прекратить применение зонисамида.
В клинических исследованиях получены ограниченные данные у пациентов с массой тела менее 20 кг. В связи с этим при лечении детей в возрасте от 6 лет и старше с массой тела менее 20 кг следует соблюдать осторожность. Влияние длительного сохранения низкой массы тела на рост и развитие у детей неизвестны.
Метаболический ацидоз.
Формирование гиперхлоремического метаболического ацидоза без анионного разрыва (снижение уровня бикарбонатов при отсутствии хронического газового алкалоза) связывают с терапией зонисамидом. Развитие метаболического ацидоза обусловлено потерей бикарбонатов в почках вследствие ингибирующего действия зонисамида на карбоангидразу, и возможно, на любой стадии лечения, хотя чаще отмечается на ранних этапах. Подобные нарушения отмечались как в ходе проведения плацебо-контролируемых клинических исследований, так и в постмаркетинговый период. Снижение уровня бикарбонатов выражено обычно незначительно (среднее значение составляет примерно 3,5 мЭкв/л при суточной дозе 300 мг у взрослых); в редких случаях у пациентов может отмечаться более значительное снижение. Состояния или методы лечения, предрасполагающие к развитию ацидоза (например заболевания почек, тяжелые респираторные расстройства, эпилептический статус, диарея, проводимые хирургические вмешательства, диета, способствующая образованию кетоновых тел, ряд ЛС), могут способствовать усилению влияния зонисамида на уровень бикарбонатов.
Риск возникновения и тяжесть метаболического ацидоза увеличиваются у молодых пациентов. В случае появления признаков или симптомов метаболического ацидоза рекомендуется оценить содержание бикарбонатов в сыворотке. Если развившийся метаболический ацидоз не проходит, следует рассмотреть возможность снижения дозы или полного прекращения приема зонисамида (с постепенным снижением дозы), возможно развитие остеопении. Если принято решение продолжить терапию при наличии стойкого ацидоза, следует рассмотреть возможность применения алкалоидов.
Необходимо проявлять осторожность при назначении одновременно с ингибиторами карбоангидразы (например топирамат и ацетазоламид), недостаточно данных, чтобы исключить фармакодинамическое взаимодействие ( см «Взаимодействие»).
Дети. Риск ацидоза, связанного с применением зонисамида, у детей и подростков может быть выше и носить более тяжелый характер. У этой группы пациентов необходимо осуществлять соответствующее наблюдение и контроль уровней бикарбонатов в сыворотке. Долговременное влияние низких уровней бикарбонатов на рост и развитие неизвестно.
Зонисамид не следует применять у детей одновременно с другими ингибиторами карбоангидразы, такими как топирамат или ацетазоламид.
Нефролитиаз.
У некоторых пациентов, особенно с предрасположенностью к нефролитиазу, возможно увеличение риска образования камней в почках и возникновения таких признаков и симптомов, как почечная колика, боль в почках или в боку.
Нефролитиаз может приводить к хроническому поражению почек. Факторы риска нефролитиаза включают предшествующее образование камней в почках, а также нефролитиаз и гиперкальциурию в семейном анамнезе. Ни один из этих факторов риска не является достоверным признаком, позволяющим спрогнозировать образование камней в почках при лечении зонисамидом. Кроме того, риск может быть повышен у пациентов, принимающих другие ЛС, провоцирующие развитие мочекаменной болезни. Повышение потребления жидкости и форсированный диурез помогает снизить риск образования камней, в тч и у пациентов с предрасположенностью к этому.
Дети. У детей сообщалось о появлении камней в почках. У некоторых пациентов, особенно с предрасположенностью к нефролитиазу, возможно увеличение риска образования камней в почках и возникновения таких признаков и симптомов, как почечная колика, боль в почках или в боку. Мочекаменная болезнь может приводить к хроническому поражению почек. Факторы риска мочекаменной болезни включают предшествующее образование камней в почках и наследственную предрасположенность к нефролитиазу и гиперкальциурии. Ни один из этих факторов риска не является достоверным признаком, позволяющим спрогнозировать образование камней в почках при лечении зонисамидом.
Увеличение потребления жидкости и форсированный диурез могут снизить риск образования камней в почках, особенно у лиц с факторами риска. На усмотрение врача может проводиться УЗИ почек. В случае обнаружения камней в почках зонисамид следует отменить.
Нарушение функции печени.
Дети. У детей и подростков наблюдалось повышение показателей функции печени и желчевыводящих путей, таких как АЛТ, АСТ, ГГТ и билирубин, но каких-либо явных закономерностей для значений, превышающих ВГН, установлено не было. Тем не менее при подозрении на возникновение нежелательных явлений со стороны печени следует оценить функцию печени и решить вопрос об отмене зонисамида.
Когнитивные функции.
Нарушение когнитивных функций у пациентов с эпилепсией связывают с основным заболеванием и/или с применением противоэпилептических ЛС. В плацебо-контролируемом исследовании с применением зонисамида у детей и подростков доля пациентов с нарушением когнитивных функций была количественно выше в группе зонисамида по сравнению с группой плацебо.
Влияние на способность управлять транспортными средствами и работать с механизмами. Специальные исследования влияния зонисамида на способность управлять автотранспортом и работать с механизмами не проводились. Зонисамид может вызвать (особенно в начале терапии или при увеличении дозы) сонливость и затруднения концентрации внимания, в связи с чем в период лечения необходимо соблюдать осторожность при занятии видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций.
При терапии зонисамидом сообщалось о развитии тяжелых кожных реакций, включая синдром Стивенса-Джонсона и токсический эпидермальный некролиз.
Рекомендуется отмена зонисамида у пациентов, у которых появились кожные высыпания, и которые невозможно объяснить другими причинами. Все пациенты с появлением высыпаний на коже во время приема зонисамида должны находиться под тщательным наблюдением, особенно пациенты с одновременным назначением других противоэпилептических ЛС, которые сами способны вызывать кожные высыпания.
Синдром отмены.
Отмену зонисамида производят путем постепенного снижения дозы во избежание возникновения эпилептических приступов. Недостаточно данных об отмене одновременно применяемых противоэпилептических ЛС после достижения контроля над приступами при применении зонисамида в рамках вспомогательной терапии для перехода к монотерапии зонисамидом. Поэтому отмена сопутствующего противоэпилептического лечения должна проводиться с осторожностью.
Реакции, связанные с наличием сульфонамидной группы.
Зонисамид содержит сульфонамидную группу. К серьезным побочным реакциям со стороны иммунной системы, связанным с приемом ЛС, которые содержат сульфонамидную группу, относятся появление кожной сыпи и других аллергических реакций, а также развитие выраженных гематологических нарушений, в тч апластической анемии, в очень редких случаях приводящей к летальному исходу.
Сообщалось о развитии случаев агранулоцитоза, тромбоцитопении, лейкопении, апластической анемии, панцитопении и лейкоцитоза. Информации для оценки возможной взаимосвязи этих явлений с величиной принимаемой дозы зонисамида и продолжительностью лечения недостаточно.
Суицидальное мышление и поведение.
Развитие суицидального мышления и поведения возможно у пациентов, принимавших противоэпилептические ЛС по ряду показаний. Метаанализ рандомизированных плацебо-контролируемых исследований противоэпилептических ЛС также показал повышенный риск возникновения суицидальных мыслей и поведения.
Механизм этого явления неизвестен, имеющиеся данные не исключают возможности повышенного риска формирования суицидального поведения и на фоне приема зонисамида.
Необходимо наблюдать за пациентами на предмет появления суицидальных мыслей и поведения, а также предусмотреть соответствующее лечение. Пациентам (и ухаживающим за ними лицам) следует рекомендовать обратиться за врачебной помощью при появлении суицидальных мыслей и поведения.
Панкреатит.
При развитии у пациентов признаков панкреатита на фоне приема зонисамида необходим мониторинг уровня панкреатических липаз и амилазы. В случае подтвержденного панкреатита при отсутствии других очевидных причин рекомендуется отмена зонисамида и назначение соответствующего лечения.
Рабдомиолиз.
При развитии у пациентов, принимающих зонисамид, сильных мышечных болей и/или слабости, особенно сопровождающихся лихорадкой, требуется оценка содержания маркеров повреждения мышц, включая уровень КФК и альдолазы. При их повышении, в отсутствие других очевидных причин, таких как травма или большой эпилептический приступ, рекомендуется отмена зонисамида и назначение соответствующего лечения.
Женщины с сохраненным детородным потенциалом.
Женщины с сохраненным детородным потенциалом должны применять надежные методы контрацепции во время лечения зонисамидом и на протяжении 1 мес после его отмены ( см «Применение при беременности и кормлении грудью»).
Тепловой удар и дегидратация.
Случаи снижения потоотделения и повышения температуры тела зафиксированы в основном у пациентов до 18 лет. В ряде случаев возникал тепловой удар, требовавший стационарного лечения. Большинство случаев происходило в условиях высокой температуры окружающей среды. Пациенты и/или ухаживающие за ними лица должны быть предупреждены о необходимости поддерживать адекватную гидратацию организма и избегать воздействия повышенных температур. Необходимо соблюдать осторожность при назначении зонисамида одновременно с ЛС, способствующими перегреванию организма, включая ингибиторы карбоангидразы и холиноблокаторы.
Профилактика перегревания и дегидратации у детей. Зонисамид может вызывать снижение потоотделения и приводить к перегреванию, а при отсутствии соответствующей помощи у ребенка может произойти поражение головного мозга и летальный исход. Дети подвержены высокому риску, особенно в жаркую погоду.
Если ребенок принимает зонисамид, следует избегать перегревания и избегать значительной физической нагрузки, особенно в жаркую погоду; увеличить потребление воды; не применять следующие ЛС: ингибиторы карбоангидразы (такие как топирамат и ацетазоламид) и антихолинергические ЛС (такие как кломипрамин, гидроксизин, дифенгидрамин, галоперидол, имипрамин и оксибутинин).
При возникновении какого-либо из нижеперечисленных симптомов, следует немедленно обратиться за медицинской помощью: ощущение сильного жара от кожи при незначительном потоотделении или при его отсутствии, при возникновении у ребенка спутанности сознания, мышечных спазмов, при учащении сердцебиения или дыхания. Необходимо поместить ребенка в прохладное затененное место; смочить кожу водой, чтобы охладить ее; дать выпить прохладной воды.
Сообщалось о случаях снижения потоотделения и повышения температуры тела, главным образом у детей. В некоторых случаях возникал тепловой удар, требующий госпитализации. В ряде случаев сообщалось о тепловом ударе с летальным исходом. В большинстве случаев явление возникало при теплой погоде. Следует предупредить пациента и лиц, осуществляющих уход за ними, о возможной серьезности теплового удара, ситуациях, когда он может возникнуть, а также мерах, которые необходимо предпринять в случае появления каких-либо признаков или симптомов. Пациентов или лиц, осуществляющих уход за ними, необходимо предупредить о необходимости употребления достаточного объема жидкости и избегания чрезмерных физических нагрузок, в зависимости от состояния пациента. В случае появления признаков и симптомов дегидратации, олигогидроза или повышения температуры тела, следует рассмотреть вопрос об отмене зонисамида.
Зонисамид не следует применять у детей, одновременно получающих другие ЛС, при применении которых у пациентов возникает предрасположенность к появлению нарушений, связанных с воздействием избыточного тепла; сюда относятся ингибиторы карбоангидразы и ЛС с антихолинергическим действием.
Снижение массы тела.
Зонисамид может вызывать снижение массы тела, поэтому во время лечения пациентов с пониженной массой тела или при ее снижении необходимо назначение пищевых добавок и усиленного питания. При выраженном снижении массы тела следует рассмотреть возможность отмены зонисамида. Снижение массы тела у детей может быть более выраженным.
Дети. Описывались случаи снижения массы тела, которые приводили к ухудшению общего состояния и прекращению применения противоэпилептического ЛС, приводящие к летальному исходу. Применение зонисамида не рекомендуется у детей с пониженной массой тела или плохим аппетитом.
Частота снижения массы тела одинакова в различных возрастных группах, тем не менее учитывая возможную серьезность снижения массы тела у детей, у этой группы пациентов необходимо контролировать массу тела. При задержке прибавки массы тела у пациента, исходя из карт физического развития, рекомендуется пересмотреть рацион питания или увеличить количество принимаемой пищи, в противном случае следует прекратить применение зонисамида.
В клинических исследованиях получены ограниченные данные у пациентов с массой тела менее 20 кг. В связи с этим при лечении детей в возрасте от 6 лет и старше с массой тела менее 20 кг следует соблюдать осторожность. Влияние длительного сохранения низкой массы тела на рост и развитие у детей неизвестны.
Метаболический ацидоз.
Формирование гиперхлоремического метаболического ацидоза без анионного разрыва (снижение уровня бикарбонатов при отсутствии хронического газового алкалоза) связывают с терапией зонисамидом. Развитие метаболического ацидоза обусловлено потерей бикарбонатов в почках вследствие ингибирующего действия зонисамида на карбоангидразу, и возможно, на любой стадии лечения, хотя чаще отмечается на ранних этапах. Подобные нарушения отмечались как в ходе проведения плацебо-контролируемых клинических исследований, так и в постмаркетинговый период. Снижение уровня бикарбонатов выражено обычно незначительно (среднее значение составляет примерно 3,5 мЭкв/л при суточной дозе 300 мг у взрослых); в редких случаях у пациентов может отмечаться более значительное снижение. Состояния или методы лечения, предрасполагающие к развитию ацидоза (например заболевания почек, тяжелые респираторные расстройства, эпилептический статус, диарея, проводимые хирургические вмешательства, диета, способствующая образованию кетоновых тел, ряд ЛС), могут способствовать усилению влияния зонисамида на уровень бикарбонатов.
Риск возникновения и тяжесть метаболического ацидоза увеличиваются у молодых пациентов. В случае появления признаков или симптомов метаболического ацидоза рекомендуется оценить содержание бикарбонатов в сыворотке. Если развившийся метаболический ацидоз не проходит, следует рассмотреть возможность снижения дозы или полного прекращения приема зонисамида (с постепенным снижением дозы), возможно развитие остеопении. Если принято решение продолжить терапию при наличии стойкого ацидоза, следует рассмотреть возможность применения алкалоидов.
Необходимо проявлять осторожность при назначении одновременно с ингибиторами карбоангидразы (например топирамат и ацетазоламид), недостаточно данных, чтобы исключить фармакодинамическое взаимодействие ( см «Взаимодействие»).
Дети. Риск ацидоза, связанного с применением зонисамида, у детей и подростков может быть выше и носить более тяжелый характер. У этой группы пациентов необходимо осуществлять соответствующее наблюдение и контроль уровней бикарбонатов в сыворотке. Долговременное влияние низких уровней бикарбонатов на рост и развитие неизвестно.
Зонисамид не следует применять у детей одновременно с другими ингибиторами карбоангидразы, такими как топирамат или ацетазоламид.
Нефролитиаз.
У некоторых пациентов, особенно с предрасположенностью к нефролитиазу, возможно увеличение риска образования камней в почках и возникновения таких признаков и симптомов, как почечная колика, боль в почках или в боку.
Нефролитиаз может приводить к хроническому поражению почек. Факторы риска нефролитиаза включают предшествующее образование камней в почках, а также нефролитиаз и гиперкальциурию в семейном анамнезе. Ни один из этих факторов риска не является достоверным признаком, позволяющим спрогнозировать образование камней в почках при лечении зонисамидом. Кроме того, риск может быть повышен у пациентов, принимающих другие ЛС, провоцирующие развитие мочекаменной болезни. Повышение потребления жидкости и форсированный диурез помогает снизить риск образования камней, в тч и у пациентов с предрасположенностью к этому.
Дети. У детей сообщалось о появлении камней в почках. У некоторых пациентов, особенно с предрасположенностью к нефролитиазу, возможно увеличение риска образования камней в почках и возникновения таких признаков и симптомов, как почечная колика, боль в почках или в боку. Мочекаменная болезнь может приводить к хроническому поражению почек. Факторы риска мочекаменной болезни включают предшествующее образование камней в почках и наследственную предрасположенность к нефролитиазу и гиперкальциурии. Ни один из этих факторов риска не является достоверным признаком, позволяющим спрогнозировать образование камней в почках при лечении зонисамидом.
Увеличение потребления жидкости и форсированный диурез могут снизить риск образования камней в почках, особенно у лиц с факторами риска. На усмотрение врача может проводиться УЗИ почек. В случае обнаружения камней в почках зонисамид следует отменить.
Нарушение функции печени.
Дети. У детей и подростков наблюдалось повышение показателей функции печени и желчевыводящих путей, таких как АЛТ, АСТ, ГГТ и билирубин, но каких-либо явных закономерностей для значений, превышающих ВГН, установлено не было. Тем не менее при подозрении на возникновение нежелательных явлений со стороны печени следует оценить функцию печени и решить вопрос об отмене зонисамида.
Когнитивные функции.
Нарушение когнитивных функций у пациентов с эпилепсией связывают с основным заболеванием и/или с применением противоэпилептических ЛС. В плацебо-контролируемом исследовании с применением зонисамида у детей и подростков доля пациентов с нарушением когнитивных функций была количественно выше в группе зонисамида по сравнению с группой плацебо.
Влияние на способность управлять транспортными средствами и работать с механизмами. Специальные исследования влияния зонисамида на способность управлять автотранспортом и работать с механизмами не проводились. Зонисамид может вызвать (особенно в начале терапии или при увеличении дозы) сонливость и затруднения концентрации внимания, в связи с чем в период лечения необходимо соблюдать осторожность при занятии видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций.
References
Обобщенные материалы www.grls.rosminzdrav.ru, 2014.
Included in the composition
- 5.2-40.8€ Zonegran (10 firms)