Pharmacological Group
Latin name
Rasagilinum ( Rasagilini).
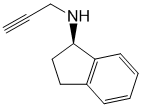
Chemical name
(1R)-2,3-Дигидро-N-2-пропинил-1H-инден-1-амин (и в виде метансульфоната).
CAS Code
136236-51-6.
Use during pregnancy and lactation
Данные о применении разагилина у беременных женщин отсутствуют. Результаты исследований на животных не указывают на наличие прямого или косвенного нежелательного влияния на беременность, эмбриофетальное развитие, роды и постнатальное развитие. При необходимости применения разагилина у беременных необходимо соотнести ожидаемую пользу для матери и предполагаемый риск для плода.
Согласно экспериментальным данным разагилин ингибирует секрецию пролактина и, таким образом, может подавлять лактацию. Сведения о проникновении разагилина в грудное молоко отсутствуют. При необходимости применения разагилина в период грудного вскармливания необходимо соотнести ожидаемую пользу для матери и ребенка.
Согласно экспериментальным данным разагилин ингибирует секрецию пролактина и, таким образом, может подавлять лактацию. Сведения о проникновении разагилина в грудное молоко отсутствуют. При необходимости применения разагилина в период грудного вскармливания необходимо соотнести ожидаемую пользу для матери и ребенка.
ATX code
N04BD02 Разагилин.
Nosology
Список кодов МКБ-10.
• G20 Болезнь Паркинсона.
• G20 Болезнь Паркинсона.
Pharmacokinetics
Всасывание.
Разагилин быстро всасывается после приема внутрь, максимальная концентрация (Cmax) в плазме крови достигается через 0,5 часа. Абсолютная биодоступность препарата после однократного введения составляет около 36%. Пища не влияет на время достижения сmax.
Разагилина в крови, однако, при потреблении жирной пищи сmax.
И площадь под кривой концентрации препарата (AUC) снижаются на 60% и 20%.
Соответственно.
Фармакокинетика препарата имеет линейный характер в диапазоне доз 0,5-2 мг.
Распределение.
Связь с белками плазмы крови колеблется от 60% до 70%.
Метаболизм.
Разагилин почти полностью метаболизируется в печени. Биотрансформация осуществляется путем N‑деалкилирования и/или гидроксилирования с образованием основного биологически малоактивного метаболита - 1‑аминоиндана, а также двух других метаболитов 3‑гидрокси-N‑пропаргил-1‑аминоиндана и 3‑гидрокси-1‑аминоиндана. Метаболизм препарата осуществляется при участии изоформы сYP1A2 системы цитохрома P450.
Выведение.
Разагилин выводится преимущественно почками (более 60%) и в меньшей степени через кишечник (более 20%). Менее 1% введенной дозы препарата выделяется в неизменном виде. Период полувыведения (1/2T1/2) составляет 0,6-2 часа.
Фармакокинетика у отдельных групп пациентов.
Применение у пациентов с почечной недостаточностью.
Параметры фармакокинетики разагилина практически не меняются у пациентов с легкой и умеренной степенью почечной недостаточности.
Применение у пациентов с печеночной недостаточностью.
При легкой степени печеночной недостаточности может наблюдаться повышение значений параметров AUC и сmax.
На 80% и 38%, а у пациентов с умеренными нарушениями функции печени эти параметры достигают более 500% и 80% соответственно.
Разагилин быстро всасывается после приема внутрь, максимальная концентрация (Cmax) в плазме крови достигается через 0,5 часа. Абсолютная биодоступность препарата после однократного введения составляет около 36%. Пища не влияет на время достижения сmax.
Разагилина в крови, однако, при потреблении жирной пищи сmax.
И площадь под кривой концентрации препарата (AUC) снижаются на 60% и 20%.
Соответственно.
Фармакокинетика препарата имеет линейный характер в диапазоне доз 0,5-2 мг.
Распределение.
Связь с белками плазмы крови колеблется от 60% до 70%.
Метаболизм.
Разагилин почти полностью метаболизируется в печени. Биотрансформация осуществляется путем N‑деалкилирования и/или гидроксилирования с образованием основного биологически малоактивного метаболита - 1‑аминоиндана, а также двух других метаболитов 3‑гидрокси-N‑пропаргил-1‑аминоиндана и 3‑гидрокси-1‑аминоиндана. Метаболизм препарата осуществляется при участии изоформы сYP1A2 системы цитохрома P450.
Выведение.
Разагилин выводится преимущественно почками (более 60%) и в меньшей степени через кишечник (более 20%). Менее 1% введенной дозы препарата выделяется в неизменном виде. Период полувыведения (1/2T1/2) составляет 0,6-2 часа.
Фармакокинетика у отдельных групп пациентов.
Применение у пациентов с почечной недостаточностью.
Параметры фармакокинетики разагилина практически не меняются у пациентов с легкой и умеренной степенью почечной недостаточности.
Применение у пациентов с печеночной недостаточностью.
При легкой степени печеночной недостаточности может наблюдаться повышение значений параметров AUC и сmax.
На 80% и 38%, а у пациентов с умеренными нарушениями функции печени эти параметры достигают более 500% и 80% соответственно.
Pharmacodynamics
Разагилин является избирательным необратимым ингибитором моноаминоксидазы типа в.
(МАО‑B), фермента, на 80% определяющего активность моноаминоксидазы в головном мозге и метаболизм дофамина. Разагилин в 30-80 раз более активен в отношении МАО‑B, чем к другому типу этого фермента - МАО‑A.
В результате ингибирующего действия препарата на МАО‑B.
В центральной нервной системе (ЦНС) повышается уровень дофамина, снижается образование токсичных свободных радикалов, избыточное образование которых наблюдается у больных болезнью Паркинсона. Разагилин обладает также нейропротекторным действием.
В отличие от неизбирательных ингибиторов МАО, препарат в терапевтических дозах не блокирует метаболизм поступающих с пищей биогенных аминов (например, тирамина), в связи с чем не вызывает тирамин-обусловленного гипертензивного синдрома («сырный эффект»).
(МАО‑B), фермента, на 80% определяющего активность моноаминоксидазы в головном мозге и метаболизм дофамина. Разагилин в 30-80 раз более активен в отношении МАО‑B, чем к другому типу этого фермента - МАО‑A.
В результате ингибирующего действия препарата на МАО‑B.
В центральной нервной системе (ЦНС) повышается уровень дофамина, снижается образование токсичных свободных радикалов, избыточное образование которых наблюдается у больных болезнью Паркинсона. Разагилин обладает также нейропротекторным действием.
В отличие от неизбирательных ингибиторов МАО, препарат в терапевтических дозах не блокирует метаболизм поступающих с пищей биогенных аминов (например, тирамина), в связи с чем не вызывает тирамин-обусловленного гипертензивного синдрома («сырный эффект»).
Indications for use
-.
Лечение болезни Паркинсона (в виде монотерапии или комбинированной терапии с препаратами леводопы).
Лечение болезни Паркинсона (в виде монотерапии или комбинированной терапии с препаратами леводопы).
Contraindications
-.
Гиперчувствительность к разагилину и/или любому другому компоненту препарата.
Одновременное применение с другими ингибиторами МАО (в том числе лекарственными препаратами и пищевыми добавками, содержащими Зверобой продырявленный), петидином. Перерыв между отменой разагилина и началом терапии этими лекарственными препаратами должен составлять не менее 14 дней.
Печеночная недостаточность средней и тяжелой степени (классы в.
И с.
По шкале Чайлд‑Пью).
Детский возраст до 18 лет (нет данных об эффективности и безопасности).
С осторожностью.
Печеночная недостаточность легкой степени (класс A.
По шкале Чайлд‑Пью). одновременное применение с селективными ингибиторами обратного захвата серотонина (СИОЗС) (в том числе флуоксетином. флувоксамином). селективными ингибиторами обратного захвата серотонина и норадреналина (СИОЗСН). трициклическими и тетрациклическими антидепрессантами. мощными ингибиторами изофермента сYP1A2.
Гиперчувствительность к разагилину и/или любому другому компоненту препарата.
Одновременное применение с другими ингибиторами МАО (в том числе лекарственными препаратами и пищевыми добавками, содержащими Зверобой продырявленный), петидином. Перерыв между отменой разагилина и началом терапии этими лекарственными препаратами должен составлять не менее 14 дней.
Печеночная недостаточность средней и тяжелой степени (классы в.
И с.
По шкале Чайлд‑Пью).
Детский возраст до 18 лет (нет данных об эффективности и безопасности).
С осторожностью.
Печеночная недостаточность легкой степени (класс A.
По шкале Чайлд‑Пью). одновременное применение с селективными ингибиторами обратного захвата серотонина (СИОЗС) (в том числе флуоксетином. флувоксамином). селективными ингибиторами обратного захвата серотонина и норадреналина (СИОЗСН). трициклическими и тетрациклическими антидепрессантами. мощными ингибиторами изофермента сYP1A2.
Side effects
В клинических исследованиях наиболее часто выявлялись следующие нежелательные явления: при монотерапии - головная боль, депрессия, головокружение, грипп, ринит; при терапии в качестве вспомогательной к терапии леводопой -.
Дискинезия, ортостатическая гипотензия, падения, боль в животе, тошнота, рвота, сухость во рту; в обоих режимах терапии - скелетно-мышечная боль, боли в спине и шее, артралгия.
В представленном ниже перечне описаны нежелательные реакции, о которых сообщалось с повышенной частотой в плацебо-контролируемых исследованиях у пациентов, получавших 1 мг/сут разагилина.
Частота нежелательных реакций определена следующим образом: очень часто (≥1/10);
Часто (≥1/100, до <1/10); нечасто (≥1/1000, до <1/100);
Редко (≥1/10000, до <1/1000); очень редко (<1/10000), частота неизвестна (частоту возникновения нежелательных реакций невозможно оценить на основании имеющихся данных).
При применении в качестве монотерапии.
Инфекционные и паразитарные заболевания:
Часто. Грипп.
Доброкачественные, злокачественные и неуточненные новообразования (включая кисты и полипы):
Часто. Рак кожи.
Нарушения со стороны крови и лимфатической системы:
Часто. Лейкопения.
Нарушения со стороны иммунной системы:
Часто. Аллергия.
Нарушения со стороны обмена веществ и питания:
Нечасто. Снижение аппетита.
Нарушения психики:
Часто. Депрессия, галлюцинации*; частота неизвестна.
- импульсивные расстройства*.
Нарушения со стороны нервной системы:
Очень часто.
- головная боль; нечасто -.
Нарушение мозгового кровообращения; частота неизвестна - чрезмерная дневная сонливость, эпизоды внезапного засыпания, серотониновый синдром*.
Нарушения со стороны органа зрения:
Часто. Конъюнктивит.
Нарушения со стороны органа слуха и лабиринта:
Часто. Вертиго.
Нарушения со стороны сердца:
Часто. Стенокардия; нечасто - инфаркт миокарда.
Нарушения со стороны сосудов:
Частота неизвестна.
- гипертензия*.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения:
Часто. Ринит.
Нарушения со стороны желудочно-кишечного тракта:
Часто. Вздутие живота.
Нарушения со стороны кожи и подкожных тканей:
Часто. Дерматит; нечасто - везикулезно-буллезная сыпь.
Нарушения со стороны скелетно-мышечной и соединительной ткани:
Часто -.
Костно-мышечная боль, боль в шее, артрит.
Нарушения со стороны почек и мочевыводящих путей:
Часто. Позывы к мочеиспусканию.
Общие расстройства и нарушения в месте введения:
Часто. Лихорадка, недомогание.
При применении в качестве вспомогательной терапии.
Нечасто. Меланома кожи*.
Часто. Снижение аппетита.
Галлюцинации*, кошмарные сновидения; нечасто.
- спутанность сознания, импульсивные расстройства*.
- дискинезия; часто - дистония, синдром запястного канала, нарушение равновесия; нечасто - нарушение мозгового кровообращения; частота неизвестна - чрезмерная дневная сонливость, эпизоды внезапного засыпания, серотониновый синдром*.
Нечасто. Стенокардия.
Ортостатическая гипотензия*; частота неизвестна - гипертензия*.
Часто. Боль в животе, запор, тошнота и рвота, сухость во рту.
Часто. Сыпь.
Часто. Артралгия, боль в шее.
Часто. Снижение массы тела.
Травмы, интоксикации и осложнения манипуляций:
Часто. Падения.
При болезни Паркинсона возникают галлюцинации и спутанность сознания. Согласно пострегистрационному опыту указанные симптомы отмечались у пациентов с болезнью Паркинсона, получавших разагилин.
*-.
См Описание отдельных нежелательных реакций.
Также раздел «Взаимодействие с другими лекарственными средствами».
Описание отдельных нежелательных реакций.
Ортостатическая гипотензия.
Имеются данные о том, что в слепых плацебо-контролируемых исследованиях сообщалось о случае тяжелой ортостатической гипотензии у одной пациентки (0,3%) в группе разагилина (препарат применялся в качестве вспомогательной терапии); в группе плацебо не было отмечено ни одного. Данные клинических испытаний также свидетельствуют о том, что ортостатическая гипотензия возникает чаще всего в первые два месяца лечения разагилином и со временем уменьшается.
Гипертония.
При применении разагилина в пострегистрационный период сообщалось о повышении артериального давления (АД), включая редкие случаи гипертонических кризов у пациентов, использующих в рационе питания продукты, богатые тирамином.
В пострегистрационном периоде сообщалось о случае повышения АД у пациента, применявшего офтальмологический вазоконстриктор тетрагидрозолин и одновременно получавшего лечение разагилином.
Импульсивное расстройство личности.
Сообщалось о случаях повышения либидо, гиперсексуальности, игромании, компульсивной потребности покупать или приобретать, переедании и компульсивном переедании, клептомании, дерматилломании у пациентов, находящихся на лечении агонистами дофаминовых рецепторов и/или другими дофаминомиметиками. Аналогичная картина импульсивного расстройства личности наблюдалась в пострегистрационном периоде у пациентов, принимавших разагилин, которая характеризовалась компульсивным и импульсивным поведением, навязчивыми идеями.
Чрезмерная дневная сонливость и эпизоды внезапного сна.
Чрезмерная дневная сонливость может возникать у пациентов, принимающих агонисты дофамина и/или другие дофаминергические препараты. Сообщалось о случаях подобной чрезмерной дневной сонливости на фоне лечения разагилином.
Сообщалось также о случаях внезапного засыпания во время выполнения пациентами обычных повседневных занятий на фоне применения разагилина с дофаминергическими препаратами.
У некоторых пациентов перед засыпанием не было никаких предупреждающих признаков, таких как чрезмерная сонливость. В ряде случаев подобные события были зарегистрированы более 1 года после начала лечения.
Галлюцинации.
Серотониновый синдром.
Имеются данные о клинических исследованиях разагилина, в которых одновременное применение его с флуоксетином или флувоксамином не допускалось. Однако были разрешены следующие антидепрессанты в указанных дозах: амитриптилин не более 50 мг/сут, тразодон не более 100 мг/сут, циталопрам не более 20 мг/сут, сертралин не более 100 мг/сут и пароксетин не более 30 мг/сут. Сообщалось о серьезных нежелательных реакциях, поэтому необходимо проявлять осторожность при одновременном применении СИОЗС, СИОЗСН, трициклических/тетрациклических антидепрессантов и ингибиторов МАО.
В пострегистрационном периоде сообщалось о случаях развития потенциально опасного для жизни серотонинового синдрома, проявляющегося возбуждением, спутанностью сознания, ригидностью, лихорадкой и миоклонусом у пациентов, получавших одновременно с разагилином антидепрессанты, меперидин (петидин), трамадол, метадон или пропоксифен.
Меланома.
Имеются данные плацебо-контролируемых клинических исследований, где заболеваемость злокачественной меланомой кожи составила 2/380 (0,5%) в группе разагилина 1 мг, применявшегося в качестве вспомогательной терапии к терапии леводопой, против 1/388 (0,3%) заболеваемости в группе плацебо.
Сообщалось также о случаях меланомы в пострегистрационном периоде ( см также раздел «Особые указания»).
Дискинезия, ортостатическая гипотензия, падения, боль в животе, тошнота, рвота, сухость во рту; в обоих режимах терапии - скелетно-мышечная боль, боли в спине и шее, артралгия.
В представленном ниже перечне описаны нежелательные реакции, о которых сообщалось с повышенной частотой в плацебо-контролируемых исследованиях у пациентов, получавших 1 мг/сут разагилина.
Частота нежелательных реакций определена следующим образом: очень часто (≥1/10);
Часто (≥1/100, до <1/10); нечасто (≥1/1000, до <1/100);
Редко (≥1/10000, до <1/1000); очень редко (<1/10000), частота неизвестна (частоту возникновения нежелательных реакций невозможно оценить на основании имеющихся данных).
При применении в качестве монотерапии.
Инфекционные и паразитарные заболевания:
Часто. Грипп.
Доброкачественные, злокачественные и неуточненные новообразования (включая кисты и полипы):
Часто. Рак кожи.
Нарушения со стороны крови и лимфатической системы:
Часто. Лейкопения.
Нарушения со стороны иммунной системы:
Часто. Аллергия.
Нарушения со стороны обмена веществ и питания:
Нечасто. Снижение аппетита.
Нарушения психики:
Часто. Депрессия, галлюцинации*; частота неизвестна.
- импульсивные расстройства*.
Нарушения со стороны нервной системы:
Очень часто.
- головная боль; нечасто -.
Нарушение мозгового кровообращения; частота неизвестна - чрезмерная дневная сонливость, эпизоды внезапного засыпания, серотониновый синдром*.
Нарушения со стороны органа зрения:
Часто. Конъюнктивит.
Нарушения со стороны органа слуха и лабиринта:
Часто. Вертиго.
Нарушения со стороны сердца:
Часто. Стенокардия; нечасто - инфаркт миокарда.
Нарушения со стороны сосудов:
Частота неизвестна.
- гипертензия*.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения:
Часто. Ринит.
Нарушения со стороны желудочно-кишечного тракта:
Часто. Вздутие живота.
Нарушения со стороны кожи и подкожных тканей:
Часто. Дерматит; нечасто - везикулезно-буллезная сыпь.
Нарушения со стороны скелетно-мышечной и соединительной ткани:
Часто -.
Костно-мышечная боль, боль в шее, артрит.
Нарушения со стороны почек и мочевыводящих путей:
Часто. Позывы к мочеиспусканию.
Общие расстройства и нарушения в месте введения:
Часто. Лихорадка, недомогание.
При применении в качестве вспомогательной терапии.
Нечасто. Меланома кожи*.
Часто. Снижение аппетита.
Галлюцинации*, кошмарные сновидения; нечасто.
- спутанность сознания, импульсивные расстройства*.
- дискинезия; часто - дистония, синдром запястного канала, нарушение равновесия; нечасто - нарушение мозгового кровообращения; частота неизвестна - чрезмерная дневная сонливость, эпизоды внезапного засыпания, серотониновый синдром*.
Нечасто. Стенокардия.
Ортостатическая гипотензия*; частота неизвестна - гипертензия*.
Часто. Боль в животе, запор, тошнота и рвота, сухость во рту.
Часто. Сыпь.
Часто. Артралгия, боль в шее.
Часто. Снижение массы тела.
Травмы, интоксикации и осложнения манипуляций:
Часто. Падения.
При болезни Паркинсона возникают галлюцинации и спутанность сознания. Согласно пострегистрационному опыту указанные симптомы отмечались у пациентов с болезнью Паркинсона, получавших разагилин.
*-.
См Описание отдельных нежелательных реакций.
Также раздел «Взаимодействие с другими лекарственными средствами».
Описание отдельных нежелательных реакций.
Ортостатическая гипотензия.
Имеются данные о том, что в слепых плацебо-контролируемых исследованиях сообщалось о случае тяжелой ортостатической гипотензии у одной пациентки (0,3%) в группе разагилина (препарат применялся в качестве вспомогательной терапии); в группе плацебо не было отмечено ни одного. Данные клинических испытаний также свидетельствуют о том, что ортостатическая гипотензия возникает чаще всего в первые два месяца лечения разагилином и со временем уменьшается.
Гипертония.
При применении разагилина в пострегистрационный период сообщалось о повышении артериального давления (АД), включая редкие случаи гипертонических кризов у пациентов, использующих в рационе питания продукты, богатые тирамином.
В пострегистрационном периоде сообщалось о случае повышения АД у пациента, применявшего офтальмологический вазоконстриктор тетрагидрозолин и одновременно получавшего лечение разагилином.
Импульсивное расстройство личности.
Сообщалось о случаях повышения либидо, гиперсексуальности, игромании, компульсивной потребности покупать или приобретать, переедании и компульсивном переедании, клептомании, дерматилломании у пациентов, находящихся на лечении агонистами дофаминовых рецепторов и/или другими дофаминомиметиками. Аналогичная картина импульсивного расстройства личности наблюдалась в пострегистрационном периоде у пациентов, принимавших разагилин, которая характеризовалась компульсивным и импульсивным поведением, навязчивыми идеями.
Чрезмерная дневная сонливость и эпизоды внезапного сна.
Чрезмерная дневная сонливость может возникать у пациентов, принимающих агонисты дофамина и/или другие дофаминергические препараты. Сообщалось о случаях подобной чрезмерной дневной сонливости на фоне лечения разагилином.
Сообщалось также о случаях внезапного засыпания во время выполнения пациентами обычных повседневных занятий на фоне применения разагилина с дофаминергическими препаратами.
У некоторых пациентов перед засыпанием не было никаких предупреждающих признаков, таких как чрезмерная сонливость. В ряде случаев подобные события были зарегистрированы более 1 года после начала лечения.
Галлюцинации.
Серотониновый синдром.
Имеются данные о клинических исследованиях разагилина, в которых одновременное применение его с флуоксетином или флувоксамином не допускалось. Однако были разрешены следующие антидепрессанты в указанных дозах: амитриптилин не более 50 мг/сут, тразодон не более 100 мг/сут, циталопрам не более 20 мг/сут, сертралин не более 100 мг/сут и пароксетин не более 30 мг/сут. Сообщалось о серьезных нежелательных реакциях, поэтому необходимо проявлять осторожность при одновременном применении СИОЗС, СИОЗСН, трициклических/тетрациклических антидепрессантов и ингибиторов МАО.
В пострегистрационном периоде сообщалось о случаях развития потенциально опасного для жизни серотонинового синдрома, проявляющегося возбуждением, спутанностью сознания, ригидностью, лихорадкой и миоклонусом у пациентов, получавших одновременно с разагилином антидепрессанты, меперидин (петидин), трамадол, метадон или пропоксифен.
Меланома.
Имеются данные плацебо-контролируемых клинических исследований, где заболеваемость злокачественной меланомой кожи составила 2/380 (0,5%) в группе разагилина 1 мг, применявшегося в качестве вспомогательной терапии к терапии леводопой, против 1/388 (0,3%) заболеваемости в группе плацебо.
Сообщалось также о случаях меланомы в пострегистрационном периоде ( см также раздел «Особые указания»).
Interaction
Одновременное применение разагилина с другими ингибиторами МАО, в том числе с лекарственными препаратами и пищевыми добавками, содержащими зверобой продырявленный, противопоказано, так как существует риск развития тяжелого гипертонического криза вследствие неселективного ингибирования МАО.
Сообщалось о развитии серьезных нежелательных реакций при одновременном применении петидина и ингибиторов МАО, в том числе селективных ингибиторов МАО‑B.
Одновременное применение разагилина и петидина противопоказано.
Сообщалось о взаимодействии ингибиторов МАО и симпатомиметических лекарственных препаратов при их одновременном применении. В связи со свойством разагилина ингибировать МАО, одновременное применение разагилина с симпатомиметиками, такими как деконгестанты или комплексные противопростудные препараты для приема внутрь или для назального применения, содержащие эфедрин или псевдоэфедрин, не рекомендуется.
Сообщалось о взаимодействии декстрометорфана и неизбирательных ингибиторов МАО при их одновременном применении. Тем не менее, в связи со свойством разагилина ингибировать МАО, одновременное применение разагилина с декстрометорфаном и комбинированными лекарственными препаратами, его содержащими, не рекомендуется.
Следует избегать одновременного применения разагилина с флуоксетином или флувоксамином ( см раздел «Особые указания»).
Сообщалось о развитии серьезных нежелательных реакций при одновременном применении СИОЗС, СИОЗСН, трициклических и тетрациклических антидепрессантов с ингибиторами МАО. В связи со свойством разагилина ингибировать МАО, необходимо соблюдать осторожность при одновременном его применении с СИОЗС, СИОЗСН, трициклическими и тетрациклическими антидепрессантами.
У пациентов с болезнью Паркинсона, получающих разагилин в качестве вспомогательной терапии к длительной терапии леводопой, леводопа не оказывала значимого влияния на клиренс разагилина.
В исследованиях in vitro.
Показано, что основным ферментом, участвующим в метаболизме разагилина является изофермент сYP1A2. Одновременное применение ципрофлоксацина и разагилина повышает AUC последнего на 83%. Одновременное применение разагилина и теофиллина (субстрата изофермента сYP1A2) не влияло на фармакокинетику ни одного из них. Таким образом, мощные ингибиторы изофермента сYP1A2 могут изменять плазменную концентрацию разагилина и требуют осторожного одновременного применения.
Существует риск того, что в связи с индукцией изофермента сYP1A2 у курящих пациентов, может уменьшаться концентрация разагилина в плазме крови.
Исследования.
In vitro показали, что разагилин в концентрации 1 мкг/мл (что эквивалентно концентрации, превышающей в 160 раз среднюю сmax.
(5,9-8,5 нг/мл) после многократного приема 1 мг разагилина пациентами с болезнью Паркинсона) не ингибирует изоферменты сYP1A2,.
CYP2A6,.
CYP2C9,.
CYP2C19,.
CYP2D6,.
CYP2E1,.
CYP3A4,.
CYP4A.
Это свидетельствует о том, что терапевтические концентрации разагилина, скорее всего, не подвержены клинически значимому влиянию субстратов указанных изоферментов.
При одновременном применении энтакапона с разагилином клиренс последнего увеличивался на 28%.
Клинические исследования взаимодействия тирамина и разагилина у добровольцев и пациентов с болезнью Паркинсона (0,5-1 мг/сут разагилина или плацебо в качестве дополнительной терапии к леводопе в течение 6 месяцев без ограничения приема тирамина) показали, что какое-либо взаимодействие разагилина и тирамина отсутствует и разагилин можно безопасно применять без ограничения тирамина в рационе.
Сообщалось о развитии серьезных нежелательных реакций при одновременном применении петидина и ингибиторов МАО, в том числе селективных ингибиторов МАО‑B.
Одновременное применение разагилина и петидина противопоказано.
Сообщалось о взаимодействии ингибиторов МАО и симпатомиметических лекарственных препаратов при их одновременном применении. В связи со свойством разагилина ингибировать МАО, одновременное применение разагилина с симпатомиметиками, такими как деконгестанты или комплексные противопростудные препараты для приема внутрь или для назального применения, содержащие эфедрин или псевдоэфедрин, не рекомендуется.
Сообщалось о взаимодействии декстрометорфана и неизбирательных ингибиторов МАО при их одновременном применении. Тем не менее, в связи со свойством разагилина ингибировать МАО, одновременное применение разагилина с декстрометорфаном и комбинированными лекарственными препаратами, его содержащими, не рекомендуется.
Следует избегать одновременного применения разагилина с флуоксетином или флувоксамином ( см раздел «Особые указания»).
Сообщалось о развитии серьезных нежелательных реакций при одновременном применении СИОЗС, СИОЗСН, трициклических и тетрациклических антидепрессантов с ингибиторами МАО. В связи со свойством разагилина ингибировать МАО, необходимо соблюдать осторожность при одновременном его применении с СИОЗС, СИОЗСН, трициклическими и тетрациклическими антидепрессантами.
У пациентов с болезнью Паркинсона, получающих разагилин в качестве вспомогательной терапии к длительной терапии леводопой, леводопа не оказывала значимого влияния на клиренс разагилина.
В исследованиях in vitro.
Показано, что основным ферментом, участвующим в метаболизме разагилина является изофермент сYP1A2. Одновременное применение ципрофлоксацина и разагилина повышает AUC последнего на 83%. Одновременное применение разагилина и теофиллина (субстрата изофермента сYP1A2) не влияло на фармакокинетику ни одного из них. Таким образом, мощные ингибиторы изофермента сYP1A2 могут изменять плазменную концентрацию разагилина и требуют осторожного одновременного применения.
Существует риск того, что в связи с индукцией изофермента сYP1A2 у курящих пациентов, может уменьшаться концентрация разагилина в плазме крови.
Исследования.
In vitro показали, что разагилин в концентрации 1 мкг/мл (что эквивалентно концентрации, превышающей в 160 раз среднюю сmax.
(5,9-8,5 нг/мл) после многократного приема 1 мг разагилина пациентами с болезнью Паркинсона) не ингибирует изоферменты сYP1A2,.
CYP2A6,.
CYP2C9,.
CYP2C19,.
CYP2D6,.
CYP2E1,.
CYP3A4,.
CYP4A.
Это свидетельствует о том, что терапевтические концентрации разагилина, скорее всего, не подвержены клинически значимому влиянию субстратов указанных изоферментов.
При одновременном применении энтакапона с разагилином клиренс последнего увеличивался на 28%.
Клинические исследования взаимодействия тирамина и разагилина у добровольцев и пациентов с болезнью Паркинсона (0,5-1 мг/сут разагилина или плацебо в качестве дополнительной терапии к леводопе в течение 6 месяцев без ограничения приема тирамина) показали, что какое-либо взаимодействие разагилина и тирамина отсутствует и разагилин можно безопасно применять без ограничения тирамина в рационе.
Overdose
Симптомы передозировки разагилином сходны с таковыми при передозировке неизбирательными ингибиторами МАО (артериальная гипертензия, постуральная гипотензия и так далее).
Лечение:
Специфического антидота нет. Промывание желудка, прием активированного угля, симптоматическая терапия.
Лечение:
Специфического антидота нет. Промывание желудка, прием активированного угля, симптоматическая терапия.
Special instructions
Следует избегать одновременного применения разагилина и флуоксетина или флувоксамина ( см раздел «Взаимодействие с другими лекарственными средствами»).
Интервал между отменой флуоксетина и началом лечения разагилином должен составлять 5 недель, а между отменой разагилина и началом приема флуоксетина или флувоксамина - 14 дней.
Сообщалось о случаях импульсивного расстройства личности у пациентов, получавших лечение агонистами дофаминовых рецепторов и/или другими дофаминомиметиками. Те же расстройства наблюдались в пострегистрационном периоде у пациентов, принимавших разагилин ( см раздел «Побочное действие»). Необходимо наблюдать за пациентами в связи с возможностью развития импульсивного расстройства личности. Пациенты и лица, осуществляющие уход, должны быть информированы о возможности развития нарушений со стороны поведения у пациентов, принимающих разагилин, включая компульсивное поведение, навязчивые идеи, игроманию, повышение либидо, гиперсексуальность, импульсивное поведение и компульсивные потребности покупать или приобретать.
Одновременное применение разагилина с декстрометорфаном, с симпатомиметиками или комплексными противопростудными препаратами для приема внутрь или для назального применения, содержащие эфедрин или псевдоэфедрин, не рекомендуется ( см раздел «Взаимодействие с другими лекарственными препаратами»).
Имеются данные о том, что болезнь Паркинсона, а не применение какого‑либо лекарственного препарата, в том числе разагилина, является фактором риска для развития рака кожи, в частности меланомы ( см раздел «Побочное действие»). Необходимо предупреждать пациента о необходимости обращаться к врачу при появлении каких‑либо патологических изменений кожи.
Необходимо иметь в виду, что такие симптомы, как галлюцинации и растерянность, которые появляются на фоне лечения разагилином, могут быть рассмотрены и как проявление болезни Паркинсона и как нежелательные реакции разагилина ( см раздел «Побочное действие»).
Необходимо с осторожностью применять разагилин у пациентов с печеночной недостаточностью легкой степени тяжести. Применения разагилина у пациентов с умеренным нарушением функции печени не рекомендуется. В случае изменения степени тяжести печеночной недостаточности с легкой на среднюю, применение разагилина необходимо прекратить ( см раздел «Фармакологические свойства» («Фармакокинетика»)).
Разагилин может вызвать чрезмерную сонливость в дневное время и иногда, особенно при использовании с дофаминергическими препаратами, эпизоды внезапного засыпания. Пациенты должны быть проинформированы об этом.
Пациентов также следует предупредить о возможных аддитивных эффектах седативных препаратов, алкоголя или других депрессантов центральной нервной системы (например, бензодиазепинов, антипсихотиков, антидепрессантов) в сочетании с разагилином или при приеме сопутствующих лекарств, повышающих уровень разагилина в плазме (например, ципрофлоксацина).
Влияние на способность управлять транспортными средствами и механизмами.
Учитывая возможность появления значимых побочных эффектов со стороны центральной нервной системы в период лечения разагилином, следует информировать пациентов о необходимости соблюдать осторожность при вождении автотранспорта и занятия потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций. Пациенты с сонливостью и испытавшие внезапное засыпание не должны управлять автотранспортом и заниматься потенциально опасными видами деятельности до тех пор, пока они не удостоверятся, что препарат не оказывает негативного влияния.
Интервал между отменой флуоксетина и началом лечения разагилином должен составлять 5 недель, а между отменой разагилина и началом приема флуоксетина или флувоксамина - 14 дней.
Сообщалось о случаях импульсивного расстройства личности у пациентов, получавших лечение агонистами дофаминовых рецепторов и/или другими дофаминомиметиками. Те же расстройства наблюдались в пострегистрационном периоде у пациентов, принимавших разагилин ( см раздел «Побочное действие»). Необходимо наблюдать за пациентами в связи с возможностью развития импульсивного расстройства личности. Пациенты и лица, осуществляющие уход, должны быть информированы о возможности развития нарушений со стороны поведения у пациентов, принимающих разагилин, включая компульсивное поведение, навязчивые идеи, игроманию, повышение либидо, гиперсексуальность, импульсивное поведение и компульсивные потребности покупать или приобретать.
Одновременное применение разагилина с декстрометорфаном, с симпатомиметиками или комплексными противопростудными препаратами для приема внутрь или для назального применения, содержащие эфедрин или псевдоэфедрин, не рекомендуется ( см раздел «Взаимодействие с другими лекарственными препаратами»).
Имеются данные о том, что болезнь Паркинсона, а не применение какого‑либо лекарственного препарата, в том числе разагилина, является фактором риска для развития рака кожи, в частности меланомы ( см раздел «Побочное действие»). Необходимо предупреждать пациента о необходимости обращаться к врачу при появлении каких‑либо патологических изменений кожи.
Необходимо иметь в виду, что такие симптомы, как галлюцинации и растерянность, которые появляются на фоне лечения разагилином, могут быть рассмотрены и как проявление болезни Паркинсона и как нежелательные реакции разагилина ( см раздел «Побочное действие»).
Необходимо с осторожностью применять разагилин у пациентов с печеночной недостаточностью легкой степени тяжести. Применения разагилина у пациентов с умеренным нарушением функции печени не рекомендуется. В случае изменения степени тяжести печеночной недостаточности с легкой на среднюю, применение разагилина необходимо прекратить ( см раздел «Фармакологические свойства» («Фармакокинетика»)).
Разагилин может вызвать чрезмерную сонливость в дневное время и иногда, особенно при использовании с дофаминергическими препаратами, эпизоды внезапного засыпания. Пациенты должны быть проинформированы об этом.
Пациентов также следует предупредить о возможных аддитивных эффектах седативных препаратов, алкоголя или других депрессантов центральной нервной системы (например, бензодиазепинов, антипсихотиков, антидепрессантов) в сочетании с разагилином или при приеме сопутствующих лекарств, повышающих уровень разагилина в плазме (например, ципрофлоксацина).
Влияние на способность управлять транспортными средствами и механизмами.
Учитывая возможность появления значимых побочных эффектов со стороны центральной нервной системы в период лечения разагилином, следует информировать пациентов о необходимости соблюдать осторожность при вождении автотранспорта и занятия потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций. Пациенты с сонливостью и испытавшие внезапное засыпание не должны управлять автотранспортом и заниматься потенциально опасными видами деятельности до тех пор, пока они не удостоверятся, что препарат не оказывает негативного влияния.
Additional facts
Описание было автоматически дополнено из инструкции препарата «Разагилин Медисорб», поскольку у самого действующего вещества нет подробного описания.
Year of updating the information
Особые отметки:
Included in the composition
- 45.6-129.8€ Rasagiline Medisorb
- 57.6-154.3€ Azilect (Maprimed )