Pharmacological Group
Latin name
Raltitrexidum ( Raltitrexidi).
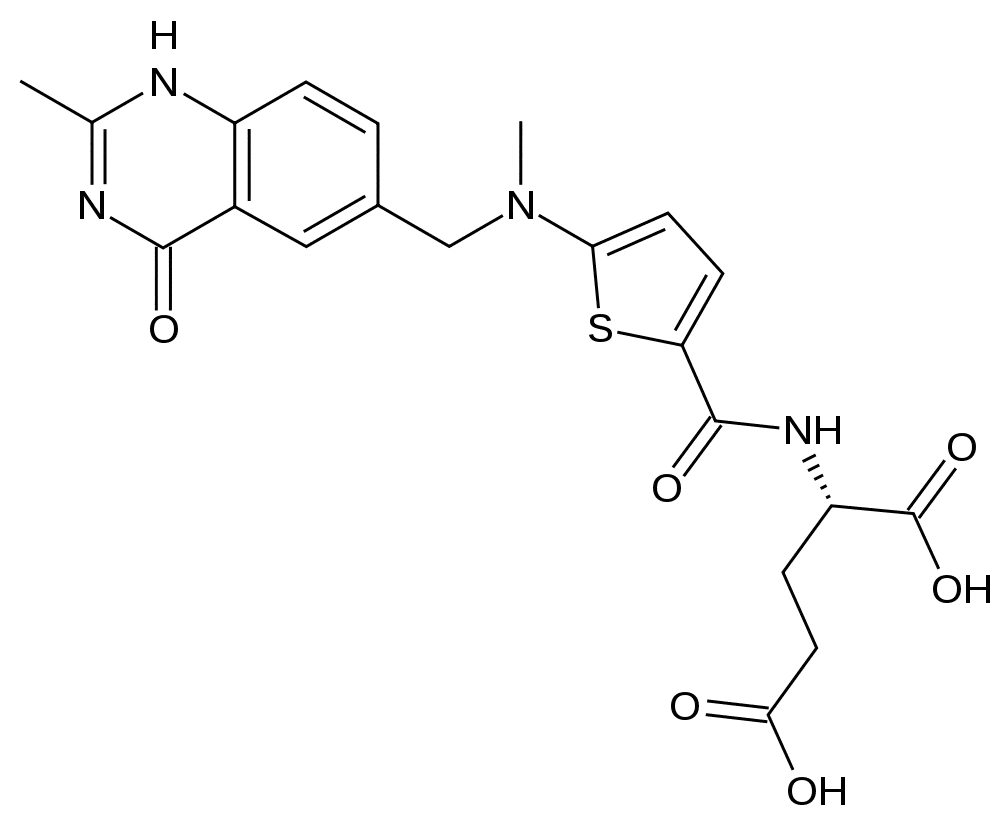
Chemical name
N-[5-[[(3,4-Дигидро-2-метил-4-оксо-6-хиназолинил)метил]метиламино]-2-теноил]-L- глутаминовая кислота.
Used in the treatment
CAS Code
112887-68-0.
Pharmacological action
Противоопухолевое.
Characteristics of the substance
Порошок бледно-желтого цвета. Растворим в воде.
Pharmacodynamics
Антиметаболит, оказывает цитостатическое действие. Прямой и специфический ингибитор тимидилатсинтетазы (ТС) - ключевого фермента в синтезе тимидинтрифосфата, необходимого для образования цепи ДНК. Ингибирование ТС приводит к фрагментации молекулы ДНК, что вызывает гибель клетки. Транспортируется в клетку с помощью восстановленного переносчика фолатов, экстенсивно подвергается полиглутатимированию посредством фермента фолилполиглутаматсинтетазы до полиглутамата, который удерживается в клетке и является мощным ингибитором ТС. Полиглутатимирование ралтитрексида усиливает его ингибирующую активность по отношению к ТС и увеличивает продолжительность этого действия, а также способствует усилению токсичности из-за задержки препарата в нормальных тканях.
После в/в введения в дозе 3 мг/м2 кривая «концентрация-время» имеет 3 фазы: пик концентрации, определяемый в конце введения, быстрое начальное снижение концентрации, фаза медленной элиминации; Сmax - 656 нг/мл; AUC - 1841 нг ч/мл; плазменный сl - 53,1 мл/мин, почечный сl - 25,1 мл/мин; объем распределения в равновесном состоянии - 468 л. Т1/2 для второй фазы - 1,72 Т1/2 для терминальной фазы - 168 Связывание с белками плазмы - 93%. Выводится в основном почками в неизмененном виде, значительная часть введенной дозы задерживается в тканях в виде полиглутамата. При использовании в терапевтических дозах (каждые 3 нед) кумуляции не зафиксировано. Нарушение функции почек (Cl креатинина - 25-65 мл/мин) приводит к увеличению Т1/2 примерно на 50%.
После в/в введения в дозе 3 мг/м2 кривая «концентрация-время» имеет 3 фазы: пик концентрации, определяемый в конце введения, быстрое начальное снижение концентрации, фаза медленной элиминации; Сmax - 656 нг/мл; AUC - 1841 нг ч/мл; плазменный сl - 53,1 мл/мин, почечный сl - 25,1 мл/мин; объем распределения в равновесном состоянии - 468 л. Т1/2 для второй фазы - 1,72 Т1/2 для терминальной фазы - 168 Связывание с белками плазмы - 93%. Выводится в основном почками в неизмененном виде, значительная часть введенной дозы задерживается в тканях в виде полиглутамата. При использовании в терапевтических дозах (каждые 3 нед) кумуляции не зафиксировано. Нарушение функции почек (Cl креатинина - 25-65 мл/мин) приводит к увеличению Т1/2 примерно на 50%.
Indications for use
Распространенный рак толстой кишки (1-я линия химиотерапии).
Contraindications
Гиперчувствительность. почечная недостаточность (клиренс креатинина менее 25 мл/мин). тяжелая печеночная недостаточность (клиническая желтуха. цирроз печени). детский возраст (безопасность и эффективность применения у детей не определены).
Use during pregnancy and lactation
Противопоказано при беременности. На время лечения следует прекратить грудное вскармливание.
Side effects
Со стороны нервной системы и органов чувств. Головная боль. нарушение вкусовых ощущений. астения. конъюнктивит. гипертонус мышц. судороги мышц.
Со стороны сердечно-сосудистой системы и крови (кроветворение, гемостаз): анемия, лейкопения, тромбоцитопения.
Со стороны органов ЖКТ. Тошнота. рвота. диарея/запор. анорексия. менее часто - боль в животе. редко - мукозиты (воспаление слизистых. стоматит). диспепсия. повышение активности печеночных трансаминаз и ЩФ.
Со стороны кожных покровов. Сыпь, иногда в сочетании с зудом, облысение, потливость.
Прочие. Артралгия. лихорадка. гриппоподобный синдром. обострение хронической инфекции и сепсис на фоне нейтропении. целлюлит. дегидратация. периферические отеки. уменьшение массы тела. нарушение фертильности.
Со стороны сердечно-сосудистой системы и крови (кроветворение, гемостаз): анемия, лейкопения, тромбоцитопения.
Со стороны органов ЖКТ. Тошнота. рвота. диарея/запор. анорексия. менее часто - боль в животе. редко - мукозиты (воспаление слизистых. стоматит). диспепсия. повышение активности печеночных трансаминаз и ЩФ.
Со стороны кожных покровов. Сыпь, иногда в сочетании с зудом, облысение, потливость.
Прочие. Артралгия. лихорадка. гриппоподобный синдром. обострение хронической инфекции и сепсис на фоне нейтропении. целлюлит. дегидратация. периферические отеки. уменьшение массы тела. нарушение фертильности.
Interaction
Кальция фолинат, фолиевая кислота и витаминные препараты, ее содержащие, снижают эффект.
Overdose
Симптомы. Развитие токсичности IV степени (шкала ВОЗ) со стороны ЖКТ (диарея или воспаление слизистой) или сочетание токсичности III степени (шкала ВОЗ) со стороны ЖКТ с гематологической токсичностью IV степени требуют прекращения лечения.
Лечение. В случае развития токсичности необходимо начать стандартную поддерживающую терапию - в/в гидратацию, стимуляторы миелопоэза.
На основе клинического опыта использования других антифолатов рекомендуется введение фолиевой кислоты в дозе 25 мг/м2 каждые 6 ч до снятия симптомов. Антидот с доказанной клинической эффективностью неизвестен.
Лечение. В случае развития токсичности необходимо начать стандартную поддерживающую терапию - в/в гидратацию, стимуляторы миелопоэза.
На основе клинического опыта использования других антифолатов рекомендуется введение фолиевой кислоты в дозе 25 мг/м2 каждые 6 ч до снятия симптомов. Антидот с доказанной клинической эффективностью неизвестен.
Method of drug use and dosage
В/в капельно (в течение не менее 15 мин), обычно применяют в дозе 3 мг/м2 (во флакон, содержащий 2 мг вещества, добавляют 4 мл воды для инъекций, рассчитывают необходимую дозу, дополнительно разбавляют 50-250 мл физиологического раствора или 5% раствора глюкозы). Повторное введение - каждые 3 нед при отсутствии токсического эффекта. При сl креатинина 25-54 мл/мин дозу уменьшают на 50%, при сl креатинина 55-65 мл/мин - на 25%, интервал между введениями увеличивают до 4 нед.
Уменьшение дозы на 25% проводят при развитии у пациентов на фоне лечения нейтропении или тромбоцитопении III степени (шкала ВОЗ), или диареи или мукозита II степени (шкала ВОЗ). Уменьшение дозы на 50% - при развитии гематологической токсичности IV степени (шкала ВОЗ) или гастроинтестинальной токсичности III степени (шкала ВОЗ). Если доза была однажды уменьшена, все последующие введения препарата проводят в этой уменьшенной дозе. Увеличение дозы выше 3 мг/м2 не рекомендуется, оно может быть связано с угрожающей жизни токсичностью.
Уменьшение дозы на 25% проводят при развитии у пациентов на фоне лечения нейтропении или тромбоцитопении III степени (шкала ВОЗ), или диареи или мукозита II степени (шкала ВОЗ). Уменьшение дозы на 50% - при развитии гематологической токсичности IV степени (шкала ВОЗ) или гастроинтестинальной токсичности III степени (шкала ВОЗ). Если доза была однажды уменьшена, все последующие введения препарата проводят в этой уменьшенной дозе. Увеличение дозы выше 3 мг/м2 не рекомендуется, оно может быть связано с угрожающей жизни токсичностью.
Application precautions
Ралтитрексид необходимо назначать при постоянном мониторинге состава периферической крови, включая определение числа тромбоцитов, лейкоцитов и лейкоцитарной формулы, уровня креатинина в сыворотке крови. Перед введением препарата число лейкоцитов крови должно быть выше 4·109/л, нейтрофилов - выше 2·109/л, тромбоцитов - выше 100·109/л. В случае токсичности (диарея, воспаление слизистой оболочки ЖКТ, нейтропения, тромбоцитопения) следующее введение препарата переносят до ее полного регрессирования. Рекомендуется постоянный контроль активности трансаминаз и уровня билирубина в сыворотке крови. С осторожностью применяют у пациентов при слабовыраженных или умеренных нарушениях функции печени, с угнетением функции костного мозга, после проведенной ранее лучевой терапии, у больных, находящихся в тяжелом состоянии, а также у людей пожилого возраста.
В период применения препарата и не менее чем в течение 6 мес после его отмены больные детородного возраста должны использовать противозачаточные средства.
Необходимо воздерживаться от занятий потенциально опасными видами деятельности, требующими повышенного внимания и быстроты психических и двигательных реакций.
В период применения препарата и не менее чем в течение 6 мес после его отмены больные детородного возраста должны использовать противозачаточные средства.
Необходимо воздерживаться от занятий потенциально опасными видами деятельности, требующими повышенного внимания и быстроты психических и двигательных реакций.
Special instructions
Пациенты с прогрессированием опухоли после предшествующего лечения фторурацилом могут оказаться нечувствительными к действию препарата.
Применение ралтитрексида должно проводиться при участии или под наблюдением врача, имеющего опыт цитотоксической химиотерапии и лечения токсических реакций. Приготовление раствора для инъекций должно проводиться обученным персоналом в специально оборудованном месте (в специальных шкафах с вытяжкой, рабочая поверхность должна покрываться одноразовой адсорбирующей бумагой с пластиковой основой) с использованием защитной одежды (одноразовых хирургических перчаток, защитных очков). В период беременности медперсонал к работе не допускается.
При попадании на кожу, в глаза следует немедленно смыть проточной водой; промывать глаза, разомкнув веки, не менее 10 мин (обязательно последующее наблюдение офтальмолога).
Пролитый раствор тщательно удаляют с использованием стандартных процедур. Неразбавленный раствор должен быть полностью использован или утилизирован соответствующим образом через 24 ч после растворения сухого препарата в воде для инъекции. Остатки препарата уничтожают в соответствии с требованиями к обращению с цитотоксическими веществами.
Применение ралтитрексида должно проводиться при участии или под наблюдением врача, имеющего опыт цитотоксической химиотерапии и лечения токсических реакций. Приготовление раствора для инъекций должно проводиться обученным персоналом в специально оборудованном месте (в специальных шкафах с вытяжкой, рабочая поверхность должна покрываться одноразовой адсорбирующей бумагой с пластиковой основой) с использованием защитной одежды (одноразовых хирургических перчаток, защитных очков). В период беременности медперсонал к работе не допускается.
При попадании на кожу, в глаза следует немедленно смыть проточной водой; промывать глаза, разомкнув веки, не менее 10 мин (обязательно последующее наблюдение офтальмолога).
Пролитый раствор тщательно удаляют с использованием стандартных процедур. Неразбавленный раствор должен быть полностью использован или утилизирован соответствующим образом через 24 ч после растворения сухого препарата в воде для инъекции. Остатки препарата уничтожают в соответствии с требованиями к обращению с цитотоксическими веществами.
Included in the composition
- — Tomudex (4 firms)