Other names and synonyms
Ergot Fungus, Ergot Rust, Ergot of Rye, Mother of Rye.
Description
Спорынья или маточные рожки - гриб класса аскомицетов, который паразитирует на 170 видах культурных и дикорастущих злаков - чаще на ржи (Secale ceresle L.), а также на тимофеевке, пырее, ячмене, пшенице, райграсе и др Относится к классу сумчатых грибов (Ascomycetes).
Гриб имеет сложный цикл развития, состоящий из трех последовательных стадий, которые ранее считались самостоятельными видами грибов: конидиальная стадия сфацелия, склероции и головчатые стромы с перитециями.
На пораженных рожками растениях в соцветиях (колосьях) хорошо заметны склероции - искривленные трехгранные рожки черно-фиолетового цвета длиной 1-3 шириной 3-5 мм Это покоящаяся стадия гриба. Склероции спорыньи состоят из сердцевины, покрытой корой меланизированных толстостенных клеток. Склероции зимуют в почве, куда они попадают при сборе урожая культурных злаков или из дикорастущих злаков. Прорастание склероциев активируется действием низкой температуры (от -3 до +5°С) на протяжении длительного времени. Прорастают весной при температуре +10-20°С.
Стромы образуются из клеток сердцевины. На поверхности прорастающих склероциев появляются маленькие бугорки, а потом небольшие трещинки коркового слоя. Зачатки стром прорывают кору склероциев и вырастают в виде бугорков, которые быстро удлиняются, и образуются шаровидные головки диаметром 1-1,5 мм По периферии головок стром развиваются перитеции - полузамкнутые плодовые тела с узким отверстием на конце, где и созревают половые споры - аскоспоры. Из склероция обычно развивается несколько стром красноватого цвета, их количество и размеры зависят от размеров склероция. Это генеративная фаза развития гриба, которую еще называют асцигерозной стадией.
Аскоспоры спорыньи заражают злаки в периоде цветения. Они распространяются ветром, попадают на рыльца пестиков или в нектар и прорастают, при этом их ростковые трубки проникают в завязь. Это конидиальная стадия гриба - сфацелия. В завязи образуется плотная масса многоклеточного разветвленного мицелия, покрытая слоем конидиеносцев, которые в свою очередь образовывают огромное количество мелких конидий (неполовых спор), погруженных в капли липкой жидкости - «медовой росы». Она выделяется мицелием, имеет неприятный запах и содержит большое количество сахаров. Медовая роса» играет значительную роль в распространении конидий гриба. Она приманивает насекомых, которые переносят конидии на здоровые растения. Конидии могут распространяться с каплями дождя, при прикосновени колосьев, а после высыхания «медовой росы» - переносятся ветром. Распространение спорыньи происходит в основном за счет вторичной инфекции конидиями. Это неполовая фаза развития растения.
Время образования склероциев зависит от погоды: во влажную - через неделю, а в сухую - через две недели после появления «медовой росы». Развиваются они медленно. Сначала склероции спорыньи изжелта-коричневые, затем окрашиваются в серо-фиолетовый или черно-фиолетовый цвет. Полное их созревание совпадает с созреванием зерна. Пораженная ткань завязи полностью разрушается, и зерновки замещаются мицелием гриба. Сейчас спорынья встречается в основном по краям полей, где источником инфекции служат дикорастущие злаки. Обычно гриб поражает не более 1% растений, что приводит к снижению урожая в пределах 0,3-5%.
Гриб имеет сложный цикл развития, состоящий из трех последовательных стадий, которые ранее считались самостоятельными видами грибов: конидиальная стадия сфацелия, склероции и головчатые стромы с перитециями.
На пораженных рожками растениях в соцветиях (колосьях) хорошо заметны склероции - искривленные трехгранные рожки черно-фиолетового цвета длиной 1-3 шириной 3-5 мм Это покоящаяся стадия гриба. Склероции спорыньи состоят из сердцевины, покрытой корой меланизированных толстостенных клеток. Склероции зимуют в почве, куда они попадают при сборе урожая культурных злаков или из дикорастущих злаков. Прорастание склероциев активируется действием низкой температуры (от -3 до +5°С) на протяжении длительного времени. Прорастают весной при температуре +10-20°С.
Стромы образуются из клеток сердцевины. На поверхности прорастающих склероциев появляются маленькие бугорки, а потом небольшие трещинки коркового слоя. Зачатки стром прорывают кору склероциев и вырастают в виде бугорков, которые быстро удлиняются, и образуются шаровидные головки диаметром 1-1,5 мм По периферии головок стром развиваются перитеции - полузамкнутые плодовые тела с узким отверстием на конце, где и созревают половые споры - аскоспоры. Из склероция обычно развивается несколько стром красноватого цвета, их количество и размеры зависят от размеров склероция. Это генеративная фаза развития гриба, которую еще называют асцигерозной стадией.
Аскоспоры спорыньи заражают злаки в периоде цветения. Они распространяются ветром, попадают на рыльца пестиков или в нектар и прорастают, при этом их ростковые трубки проникают в завязь. Это конидиальная стадия гриба - сфацелия. В завязи образуется плотная масса многоклеточного разветвленного мицелия, покрытая слоем конидиеносцев, которые в свою очередь образовывают огромное количество мелких конидий (неполовых спор), погруженных в капли липкой жидкости - «медовой росы». Она выделяется мицелием, имеет неприятный запах и содержит большое количество сахаров. Медовая роса» играет значительную роль в распространении конидий гриба. Она приманивает насекомых, которые переносят конидии на здоровые растения. Конидии могут распространяться с каплями дождя, при прикосновени колосьев, а после высыхания «медовой росы» - переносятся ветром. Распространение спорыньи происходит в основном за счет вторичной инфекции конидиями. Это неполовая фаза развития растения.
Время образования склероциев зависит от погоды: во влажную - через неделю, а в сухую - через две недели после появления «медовой росы». Развиваются они медленно. Сначала склероции спорыньи изжелта-коричневые, затем окрашиваются в серо-фиолетовый или черно-фиолетовый цвет. Полное их созревание совпадает с созреванием зерна. Пораженная ткань завязи полностью разрушается, и зерновки замещаются мицелием гриба. Сейчас спорынья встречается в основном по краям полей, где источником инфекции служат дикорастущие злаки. Обычно гриб поражает не более 1% растений, что приводит к снижению урожая в пределах 0,3-5%.
Distribution
Спорынья распространена там, где произрастают злаковые - в Европе, Азии, Северной Америке (за исключением крайнего Севера). Они выявлены в Северной Африке, некоторых районах Австралии и Южной Америки (Аргентина).

Collecting and harvesting
В медицине используют высушенные склероции спорыньи (маточных рожков) (Secale cornutum), общее содержание алкалоидов в которых составляет не менее 0,15% в перерасчете на эрготоксин, а количество водорастворимых алкалоидов - не менее 0,01% в эквиваленте эргометрина.
Спрос на маточные рожки достаточно велик. В промышленном производстве используют три основных метода получения алкалоидов рожков: из склероциев, выращенных на растениях, биосинтез алкалоидов в сапрофитной (лабораторной) культуре рожков и их частичный или полный химический синтез.
Наиболее экономически выгодным методом является культивирование гриба на ржи. Ранее склероции собирали на пораженных в естественных условиях полях. В 30-40-е г.г. XX в. были разработаны методы искусственного разведения рожков на ржи. С этой целью озимая рожь высеивается ленточным способом на высоком агрофоне. При этом на одном квадратном метре должно быть не менее 500 колосоносных стеблей. Для заражения используют селекционные штаммы, которые отличаются более высоким и стабильным содержанием алкалоидов (эрготамина) в склероциях - 0,4-0,6% (в дикорастущих склероциях их содержание колеблется в пределах 0,027-0,24%). Культуру гриба выращивают на искусственных питательных средах (сусло-агар, солод-агар, стерилизованные зерна ржи) в колбах в стерильных условиях. Через неделю после внесения в питательную среду чистой культуры маточных рожков появляется белый мицелий гриба. Для заражения посева мицелий вынимают из колбы, помещают на шелковое или капроновое сито и растирают с чистой водой. Потом инфицированную жидкость переносят на планшет-доску с иглами и войлоком, пропитывая его суспензией спор.
Заражают рожь в начале колошения, когда на посевах в 50% растений из влагалищного листа появляется ость. В настоящее время делают инъекцию жидкости в верхнюю колосистую часть ржи. При этом инфицированная жидкость вместе со спорами из игл попадает на колоски ржи, где затем развивается плодовое тело маточных рожков. На тычинках злаков споры прорастают, образовывая грибницу - нитевидный мицелий. На зараженных грибом растениях через 1-2 недели начинают выделяться капли «медовой росы», где содержится большое количество конидиеспор. Конидиеспоры переносятся насекомыми на другие растения. В результате завязь атрофируется и образуется склероций. Для полного образования склероция необходимо 30-40 дней.
Маточные рожки собирают в период созревания, когда они приобретают буро-фиолетовую окраску. Спорынью собирают ручным способом или путем прямого комбайнирования переоборудованными зерновыми комбайнами. При сборе ручным способом следует помнить об отравляющих свойствах алкалоидов и защищать лицо и руки. Урожай рожков составляет 50-100 кг/га, а в годы с благоприятными погодными условиями - до 150-200 кг/га. Рожки должны быть твердыми на ощупь и легко выниматься из колоса. Собранные рожки сушат в затемненном, хорошо проветриваемом помещении. Искусственную сушку проводят при 50°С. Высушенные маточные рожки при изгибании должны ломаться. Спорынья культивируется в Германии, Чехии, Словакии, Венгрии, Швейцарии. Мировыми экспортерами маточных рожков является Испания (экспортируются через Португалию), Россия и Балканские страны.
Недостатками вышеописанного метода является получение только одного урожая склероциев в год и значительная зависимость от погодных условий. Поэтому уже давно предпринимались попытки освоения сапрофитной (лабораторной) культуры рожков для получения алкалоидов. Основные трудности заключаются в том, что на искусственной питательной среде (в сапрофитной культуре) образуется мицелий, который продуцирует только конидиеспоры, последующие стадии развития гриба отсутствуют. А алкалоиды обычно синтезируются на стадии формирования паразитирующих склероциев. Первый патент на такой метод получен еще в 1910 г., но только в последние десятилетия в глубинной и поверхностной культуре рожков удалось получить достаточно высокий и стабильный выход алкалоидов клавиновой группы и простых производных лизергиновой кислоты. В 1960 г. итальянские ученые A. Tonolo, E. в. сhain и соавт. добились высокого уровня продукции простых производных лизергиновой кислоты, в частности метилкарбиноламида (+)-лизергиновой кислоты, в сапрофитной культуре селекционным штаммом сlaviceps paspali Stevens et Hall. Выход продукта при этом составлял от 600 мг до 1-2 г на 1 л культуры после 7-10 дней культивирования, тогда как у начальных диких штаммов - только 10-100 мг/л. Из сапрофитной культуры этого гриба получают также паспаловую кислоту - изомер (+)-лизергиновой кислоты. Эти соединения предложено преобразовывать в лизергиновую кислоту, из которой путем полусинтеза можно получить эрготамин и эргометрин. Такой способ получения пептидных алкалоидов маточных рожков введен в фармацевтическую промышленность во многих странах - России, США, Германии, Канаде, Швеции, Японии и других. Сейчас интенсивно изучаются факторы, которые влияют на биосинтез алкалоидов в сапрофитных культурах рожков.
Недавно (C. Arntz и P. Tudzynski, 1997) с помощью новейших технологий анализа ДНК сделаны попытки идентифицировать гены, отвечающие за синтез алкалоидов культурами маточных рожков. На основе сравнения ДНК культур-продуцентов и культур, не синтезирующих алкалоиды, подтверждены значения гена пускового фермента диметилалилтриптофан-синтетазы, а также генов, отвечающих за дифференциацию гифов склероция.
Учитывая фармакологическую ценность алкалоидов маточных рожков, трудность культивирования данного сырья и получения из него алкалоидов, в некоторых странах разработаны синтетические методы получения алкалоидов маточных рожков. В частности, швейцарской фармацевтической фирмой «Sandoz» запатентован метод получения пептидных алкалоидов рожков на основе L-моногидрата лизергиновой кислоты, а также способ получения пара-R-оксиэрготаминов и их солей (которые обладают адренолитической активностью и являются антагонистами серотонина) на основе лактама L-пролил-L-(о-метил)-тирозина и N-метил-морфолина.
Спрос на маточные рожки достаточно велик. В промышленном производстве используют три основных метода получения алкалоидов рожков: из склероциев, выращенных на растениях, биосинтез алкалоидов в сапрофитной (лабораторной) культуре рожков и их частичный или полный химический синтез.
Наиболее экономически выгодным методом является культивирование гриба на ржи. Ранее склероции собирали на пораженных в естественных условиях полях. В 30-40-е г.г. XX в. были разработаны методы искусственного разведения рожков на ржи. С этой целью озимая рожь высеивается ленточным способом на высоком агрофоне. При этом на одном квадратном метре должно быть не менее 500 колосоносных стеблей. Для заражения используют селекционные штаммы, которые отличаются более высоким и стабильным содержанием алкалоидов (эрготамина) в склероциях - 0,4-0,6% (в дикорастущих склероциях их содержание колеблется в пределах 0,027-0,24%). Культуру гриба выращивают на искусственных питательных средах (сусло-агар, солод-агар, стерилизованные зерна ржи) в колбах в стерильных условиях. Через неделю после внесения в питательную среду чистой культуры маточных рожков появляется белый мицелий гриба. Для заражения посева мицелий вынимают из колбы, помещают на шелковое или капроновое сито и растирают с чистой водой. Потом инфицированную жидкость переносят на планшет-доску с иглами и войлоком, пропитывая его суспензией спор.
Заражают рожь в начале колошения, когда на посевах в 50% растений из влагалищного листа появляется ость. В настоящее время делают инъекцию жидкости в верхнюю колосистую часть ржи. При этом инфицированная жидкость вместе со спорами из игл попадает на колоски ржи, где затем развивается плодовое тело маточных рожков. На тычинках злаков споры прорастают, образовывая грибницу - нитевидный мицелий. На зараженных грибом растениях через 1-2 недели начинают выделяться капли «медовой росы», где содержится большое количество конидиеспор. Конидиеспоры переносятся насекомыми на другие растения. В результате завязь атрофируется и образуется склероций. Для полного образования склероция необходимо 30-40 дней.
Маточные рожки собирают в период созревания, когда они приобретают буро-фиолетовую окраску. Спорынью собирают ручным способом или путем прямого комбайнирования переоборудованными зерновыми комбайнами. При сборе ручным способом следует помнить об отравляющих свойствах алкалоидов и защищать лицо и руки. Урожай рожков составляет 50-100 кг/га, а в годы с благоприятными погодными условиями - до 150-200 кг/га. Рожки должны быть твердыми на ощупь и легко выниматься из колоса. Собранные рожки сушат в затемненном, хорошо проветриваемом помещении. Искусственную сушку проводят при 50°С. Высушенные маточные рожки при изгибании должны ломаться. Спорынья культивируется в Германии, Чехии, Словакии, Венгрии, Швейцарии. Мировыми экспортерами маточных рожков является Испания (экспортируются через Португалию), Россия и Балканские страны.
Недостатками вышеописанного метода является получение только одного урожая склероциев в год и значительная зависимость от погодных условий. Поэтому уже давно предпринимались попытки освоения сапрофитной (лабораторной) культуры рожков для получения алкалоидов. Основные трудности заключаются в том, что на искусственной питательной среде (в сапрофитной культуре) образуется мицелий, который продуцирует только конидиеспоры, последующие стадии развития гриба отсутствуют. А алкалоиды обычно синтезируются на стадии формирования паразитирующих склероциев. Первый патент на такой метод получен еще в 1910 г., но только в последние десятилетия в глубинной и поверхностной культуре рожков удалось получить достаточно высокий и стабильный выход алкалоидов клавиновой группы и простых производных лизергиновой кислоты. В 1960 г. итальянские ученые A. Tonolo, E. в. сhain и соавт. добились высокого уровня продукции простых производных лизергиновой кислоты, в частности метилкарбиноламида (+)-лизергиновой кислоты, в сапрофитной культуре селекционным штаммом сlaviceps paspali Stevens et Hall. Выход продукта при этом составлял от 600 мг до 1-2 г на 1 л культуры после 7-10 дней культивирования, тогда как у начальных диких штаммов - только 10-100 мг/л. Из сапрофитной культуры этого гриба получают также паспаловую кислоту - изомер (+)-лизергиновой кислоты. Эти соединения предложено преобразовывать в лизергиновую кислоту, из которой путем полусинтеза можно получить эрготамин и эргометрин. Такой способ получения пептидных алкалоидов маточных рожков введен в фармацевтическую промышленность во многих странах - России, США, Германии, Канаде, Швеции, Японии и других. Сейчас интенсивно изучаются факторы, которые влияют на биосинтез алкалоидов в сапрофитных культурах рожков.
Недавно (C. Arntz и P. Tudzynski, 1997) с помощью новейших технологий анализа ДНК сделаны попытки идентифицировать гены, отвечающие за синтез алкалоидов культурами маточных рожков. На основе сравнения ДНК культур-продуцентов и культур, не синтезирующих алкалоиды, подтверждены значения гена пускового фермента диметилалилтриптофан-синтетазы, а также генов, отвечающих за дифференциацию гифов склероция.
Учитывая фармакологическую ценность алкалоидов маточных рожков, трудность культивирования данного сырья и получения из него алкалоидов, в некоторых странах разработаны синтетические методы получения алкалоидов маточных рожков. В частности, швейцарской фармацевтической фирмой «Sandoz» запатентован метод получения пептидных алкалоидов рожков на основе L-моногидрата лизергиновой кислоты, а также способ получения пара-R-оксиэрготаминов и их солей (которые обладают адренолитической активностью и являются антагонистами серотонина) на основе лактама L-пролил-L-(о-метил)-тирозина и N-метил-морфолина.
Chemical composition
Склероции спорыньи, или маточных рожков содержат более 30 индоловых алкалоидов, которые разделяют на две основные группы: производные (+)-лизергиновой и (+)-изолизергиновой кислот и клавиновые алкалоиды. Левовращающие алкалоиды (производные лизергиновой кислоты) проявляют более сильную фармакологическую активность, чем правовращающие изомеры (производные изолизергиновой кислоты).
7 пар классических алкалоидов маточных рожков относятся к четырем группам:
• группа эрготамина: левовращающие алкалоиды эрготамин и эргозин, правовращающие - эрготаминин и эргозинин;
• группа эргостина: левовращающий алкалоид эргостин и правовращающий эргостинин;
• группа эрготоксина: левовращающие алкалоиды эргокристин, эргокриптин и эргокорнин, правовращающие - эргокристинин, эргокриптинин и эргокорнинин;
• группа эргометрина - левовращающий алкалоид эргометрин и правовращающий эргометринин.
Алкалоиды групп эрготамина, эргостина и эрготоксина - соединения лизергиновой кислоты с разными пептидами. Термином «эрготоксин» на протяжении многих лет обозначали смесь эргокристина, эргокриптина и эргокорнина. Пептидные алкалоиды являются наиболее ценными для медицины. К непептидным (водорастворимым) алкалоидам относится эргометрин - соединение лизергиновой кислоты с аминопропанолом. Этот алкалоид открыли в 1935 г. 5 независимых групп исследователей (H. W. Dudley и с. Moir и др), в связи с чем ему было присвоено несколько названий. Наиболее распространенное из них - эргометрин. В США официально употребляется название эргоновин, в Швейцарии - эргобазин.
Некоторые производные лизергиновой кислоты (амид, диэтиламид) обладают галлюциногенными свойствами. Первый химически чистый алкалоид этой группы получил в 1918 г. швейцарский ученый A. Stoll. В 1938 г. в лаборатории фирмы «Sandoz» (Шейцария) докторами A. Stoll и A. Hoffman был произведен химический синтез диэтиламида лизергиновой кислоты - препарата ЛСД-25. Сначала предполагалось его применение в акушерстве и гинекологии, а также для лечения мигрени, но после серии лабораторных исследований была признана бесперспективность данного препарата, а дальнейшее изучение прекращено. Через 5 лет в апреле 1943 г. Альберт Хоффман обнаружил психотропные свойства спорыньи и установил наркотическое галлюциногенное действие ЛСД.
Позднее этот стимулятор центральной нервной системы был запрещен не только для использования с лечебной целью, но и для исследований в лабораторных условиях.
Кроме маточных рожков, эргоалкалоиды выявлены в некоторых цветочных растениях семейства березовых, произрастающих в Центральной Америке (ипомея, Rivea corymbosa (L. Hallieri, Argyreia sp. В их семени содержится до 0,05% эргоалкалоидов (эргозин, эргометрин, эргинин, метилкарбиноламид лизергиновой кислоты, некоторые клавиновые алкалоиды). Эти растения входили в состав ритуальных средства «ololiuqui» с галлюциногенными свойствами, которые применялись древними ацтеками и индейцами Мексики. Установлено, что специфическим психотропным компонентом этого средства является эргин - амид (+)-лизергиновой кислоты.
Вторая группа алкалоидов рожков - клавиновые алкалоиды (агроклавин, элимоклавин, ханоклавин I, костаклавин, эргоклавин, лизергин, пенинклавин, сетоклавин) - известна относительно недавно. Они не являются производными лизергиновой кислоты, в основе их структуры лежит скелет эрголена. Эти алкалоиды содержатся в больших количествах в склероциях рожков на дикорастущих злаках в Африке и на Дальнем Востоке. Впервые клавиновые алкалоиды были выделены швейцарскими учеными A. Stoll и соавт. из сапрофитных культур рожков, технология которых была разработана японским ученым M. Abe в 1948 г. Открытие этих алкалоидов стало движущей силой в научных исследованиях продукции алкалоидов рожков в сапрофитных культурах.
Продолжительное время с фармакологической точки зрения клавиновые алкалоиды рожков не представляли интереса. Но в последние годы на их основе получен ценный полусинтетический препарат ницерголин - 1,6-диметил-8β-(5-бром-никотиноил-окисметил)-10α-метоксиэрголин, который, кроме эрголинового ядра, содержит бромзамещенный остаток никотиновой кислоты.
Наряду с индоловыми алкалоидами склероции рожков содержат алкалоид эргомонамин и алкалоиды - производные имидазола, в частности эрготионеин.
Алкалоиды содержатся только в склероциях гриба в количестве 0,0001-0,75%. В некоторых разновидностях рожков, которые походят из Испании и Португалии, содержание алкалоидов достигает 1% и более. Обычно в склероциях присутствует смесь алкалоидов всех групп в разных соотношениях. На количественный и качественный состав алкалоидов в сырье влияют многие факторы: в первую очередь хемовар гриба-продуцента, вид растения-хозяина, на котором гриб развивается, и внешние экологические факторы. В частности, исследования, проведенные в Канаде, показали, что общее содержание алкалоидов в рожках из стойкого гибрида ржи с пшеницей (Triticale) колеблется в пределах 0,042-0,752%, из ячменя - 0,082-1,04%. В среднем в рожках, собранных в Канаде из пшеницы, ржи, тритикале и ячменя, содержание алкалоидов составляло 0,236%. Содержание эргокристина в сумме алкалоидов - 31%, эрготамина - 17%, эргокристинина - 13%, эрготаминина - 8%, эргокриптина и эргометрина - по 5%, эргокорнина и эргозина - по 4%, эргокриптинина - 3%, эргостинина, эргометринина и эргокорнинина - по 2%; 3% - неидентифицированные алкалоиды.
Большое медицинское значение имеют полусинтетические алкалоиды - дигидроэрготамин, метилэргометрин, метисергид, бромокриптин (2-бром-a-эргокриптин).
Кроме алкалоидов, в склероциях ржаных рожков найдены амины (тирамин, гистамин, агматин), алкиламины (эрготиоксин, эрготионеин, герцинин, триметиламин, метиламин, гексиламин) и другие азотсодержащие соединения (холин, ацетилхолин, бетаин, урацил, гуанозин), аминокислоты (аспарагин, аланин, валин, лейцин, фенилаланин), хризогеновая и хризергоновая кислоты, секалоновые кислоты А и В, антрахиноновые пигменты (эндокрицин, клаворубин), эргохромы - производные ксантона (эргохризин, эргофлавин), 3-4% сахаров (трегалоза, глюкоза и др), до 1% многоатомных спиртов, стероиды (около 0,1% эргостерола - эргоста-5,7,22-триен-3β-ола, или провитамина D2), хитин. склероции маточных рожков богаты жирными маслами (до 35%), около 60% липидов представлены триацилглицеролами. В их состав входят остатки рициноолеиновой и негидроксилированных жирных кислот (16:0 - пальмитиновой, 16:1 w-7, 18:0 - стеариновой, 18:1 w-9 - олеиновой и 18:2 w-6,9 - линолевой). Рициноолеиновую кислоту предложено использовать в качестве маркера при установлении факта загрязнения пищевых продуктов рожками.
7 пар классических алкалоидов маточных рожков относятся к четырем группам:
• группа эрготамина: левовращающие алкалоиды эрготамин и эргозин, правовращающие - эрготаминин и эргозинин;
• группа эргостина: левовращающий алкалоид эргостин и правовращающий эргостинин;
• группа эрготоксина: левовращающие алкалоиды эргокристин, эргокриптин и эргокорнин, правовращающие - эргокристинин, эргокриптинин и эргокорнинин;
• группа эргометрина - левовращающий алкалоид эргометрин и правовращающий эргометринин.
Алкалоиды групп эрготамина, эргостина и эрготоксина - соединения лизергиновой кислоты с разными пептидами. Термином «эрготоксин» на протяжении многих лет обозначали смесь эргокристина, эргокриптина и эргокорнина. Пептидные алкалоиды являются наиболее ценными для медицины. К непептидным (водорастворимым) алкалоидам относится эргометрин - соединение лизергиновой кислоты с аминопропанолом. Этот алкалоид открыли в 1935 г. 5 независимых групп исследователей (H. W. Dudley и с. Moir и др), в связи с чем ему было присвоено несколько названий. Наиболее распространенное из них - эргометрин. В США официально употребляется название эргоновин, в Швейцарии - эргобазин.
Некоторые производные лизергиновой кислоты (амид, диэтиламид) обладают галлюциногенными свойствами. Первый химически чистый алкалоид этой группы получил в 1918 г. швейцарский ученый A. Stoll. В 1938 г. в лаборатории фирмы «Sandoz» (Шейцария) докторами A. Stoll и A. Hoffman был произведен химический синтез диэтиламида лизергиновой кислоты - препарата ЛСД-25. Сначала предполагалось его применение в акушерстве и гинекологии, а также для лечения мигрени, но после серии лабораторных исследований была признана бесперспективность данного препарата, а дальнейшее изучение прекращено. Через 5 лет в апреле 1943 г. Альберт Хоффман обнаружил психотропные свойства спорыньи и установил наркотическое галлюциногенное действие ЛСД.
Позднее этот стимулятор центральной нервной системы был запрещен не только для использования с лечебной целью, но и для исследований в лабораторных условиях.
Кроме маточных рожков, эргоалкалоиды выявлены в некоторых цветочных растениях семейства березовых, произрастающих в Центральной Америке (ипомея, Rivea corymbosa (L. Hallieri, Argyreia sp. В их семени содержится до 0,05% эргоалкалоидов (эргозин, эргометрин, эргинин, метилкарбиноламид лизергиновой кислоты, некоторые клавиновые алкалоиды). Эти растения входили в состав ритуальных средства «ololiuqui» с галлюциногенными свойствами, которые применялись древними ацтеками и индейцами Мексики. Установлено, что специфическим психотропным компонентом этого средства является эргин - амид (+)-лизергиновой кислоты.
Вторая группа алкалоидов рожков - клавиновые алкалоиды (агроклавин, элимоклавин, ханоклавин I, костаклавин, эргоклавин, лизергин, пенинклавин, сетоклавин) - известна относительно недавно. Они не являются производными лизергиновой кислоты, в основе их структуры лежит скелет эрголена. Эти алкалоиды содержатся в больших количествах в склероциях рожков на дикорастущих злаках в Африке и на Дальнем Востоке. Впервые клавиновые алкалоиды были выделены швейцарскими учеными A. Stoll и соавт. из сапрофитных культур рожков, технология которых была разработана японским ученым M. Abe в 1948 г. Открытие этих алкалоидов стало движущей силой в научных исследованиях продукции алкалоидов рожков в сапрофитных культурах.
Продолжительное время с фармакологической точки зрения клавиновые алкалоиды рожков не представляли интереса. Но в последние годы на их основе получен ценный полусинтетический препарат ницерголин - 1,6-диметил-8β-(5-бром-никотиноил-окисметил)-10α-метоксиэрголин, который, кроме эрголинового ядра, содержит бромзамещенный остаток никотиновой кислоты.
Наряду с индоловыми алкалоидами склероции рожков содержат алкалоид эргомонамин и алкалоиды - производные имидазола, в частности эрготионеин.
Алкалоиды содержатся только в склероциях гриба в количестве 0,0001-0,75%. В некоторых разновидностях рожков, которые походят из Испании и Португалии, содержание алкалоидов достигает 1% и более. Обычно в склероциях присутствует смесь алкалоидов всех групп в разных соотношениях. На количественный и качественный состав алкалоидов в сырье влияют многие факторы: в первую очередь хемовар гриба-продуцента, вид растения-хозяина, на котором гриб развивается, и внешние экологические факторы. В частности, исследования, проведенные в Канаде, показали, что общее содержание алкалоидов в рожках из стойкого гибрида ржи с пшеницей (Triticale) колеблется в пределах 0,042-0,752%, из ячменя - 0,082-1,04%. В среднем в рожках, собранных в Канаде из пшеницы, ржи, тритикале и ячменя, содержание алкалоидов составляло 0,236%. Содержание эргокристина в сумме алкалоидов - 31%, эрготамина - 17%, эргокристинина - 13%, эрготаминина - 8%, эргокриптина и эргометрина - по 5%, эргокорнина и эргозина - по 4%, эргокриптинина - 3%, эргостинина, эргометринина и эргокорнинина - по 2%; 3% - неидентифицированные алкалоиды.
Большое медицинское значение имеют полусинтетические алкалоиды - дигидроэрготамин, метилэргометрин, метисергид, бромокриптин (2-бром-a-эргокриптин).
Кроме алкалоидов, в склероциях ржаных рожков найдены амины (тирамин, гистамин, агматин), алкиламины (эрготиоксин, эрготионеин, герцинин, триметиламин, метиламин, гексиламин) и другие азотсодержащие соединения (холин, ацетилхолин, бетаин, урацил, гуанозин), аминокислоты (аспарагин, аланин, валин, лейцин, фенилаланин), хризогеновая и хризергоновая кислоты, секалоновые кислоты А и В, антрахиноновые пигменты (эндокрицин, клаворубин), эргохромы - производные ксантона (эргохризин, эргофлавин), 3-4% сахаров (трегалоза, глюкоза и др), до 1% многоатомных спиртов, стероиды (около 0,1% эргостерола - эргоста-5,7,22-триен-3β-ола, или провитамина D2), хитин. склероции маточных рожков богаты жирными маслами (до 35%), около 60% липидов представлены триацилглицеролами. В их состав входят остатки рициноолеиновой и негидроксилированных жирных кислот (16:0 - пальмитиновой, 16:1 w-7, 18:0 - стеариновой, 18:1 w-9 - олеиновой и 18:2 w-6,9 - линолевой). Рициноолеиновую кислоту предложено использовать в качестве маркера при установлении факта загрязнения пищевых продуктов рожками.

Additional facts
В давние времена маточные рожки были известны в Китае как женское средство. Их употребляли для облегчения родов и как абортивное средство.
Первое упоминание о применении маточных рожков с лечебной целью в Европе (при послеродовых болях) встречается в 1557 г. в травнике известного врача эпохи Возрождения из Франкфурта Адама Лоницеруса (1527-1587) «Adami Loniceri Naturalis historiae opus novum». О лечебных свойствах рожков вспоминает в 1588 г. в своем медицинском трактате Joachim сamerarius (1534-1591). К тому времени было известно о кровоостанавливающих свойствах рожков в гинекологической практике, на что указывает австрийский врач и ботаник Thal Johann Thalius (умер в 1587 г.) в книге «Sylva hercynica seu catalogus plantarum sponte nascentium» (1588). Но в официальную медицину маточные рожки были введены только в начале XIX в. Сократительное влияние рожков на мускулатуру матки описал в 1808 г. американский врач John Stearns, а кровоостанавливающее действие при послеродовых кровотечениях - в 1824 г. D. Hosack. В 1836 году маточные рожки были включены в Лондонскую Фармакопею, а в середине XIX в. - в фармакопеи всех стран.
Тогда же было начато изучение алкалоидов, содержащихся в склероциях гриба. Тем не менее задолго до изучения действующих компонентов склероциев их широко применяли в акушерстве. Об использовании маточных рожков в медицине упоминается в работах А. Лоницери (1582) и Р. Я. Камерариуса (1688).
Продолжительное время в народной медицине разных стран маточные рожки применяли для лечения рака матки.
Детальную ботаническую характеристику рожков сделали в 1861-1865 гг. французские ботаники Luis Rene и сharles Tulasne.
Синтезированный в 1938 г. диэтиламид лизергиновой кислоты (препарат ЛСД-25) - наркотик-легенда. В 70-е годы в США мода на ЛСД-25 была подобна эпидемии - количество людей, употребляющих этот наркотик, достигала десятков тысяч. Из них 90% составляли студенты, и столицей этой новой «религии» был Калифорнийский университет в Беркли. Практически все его студенты принимали ЛСД, причем не поодиночке, как героин или морфий, а группами. Идейным вождем этой «религии» был психолог Гарвардского университета доктор Лире, который проповедовал, что ЛСД - не просто наркотик, а средство «освобождения» и «самопознания», «создания собственного рая и ада», что «открывает дверь в мир, где проблемы жизни и смерти возникают в своих истинных измерениях». Но действительность была значительно прозаичнее: пресса ежедневно сообщала об убийствах и самоубийствах, произошедших под влиянием этого препарата, психиатрические клиники были переполнены потребителями ЛСД, которые не смогли избавиться от выпущенного на свободу монстра после того, как действие наркотика прекратилось. Сенатор Роберт Кеннеди начал расследование, в результате которого в США было принято решение о наказании за производство, транспортировку и сбыт ЛСД. По официальным данным, сегодня в Украине и России ЛСД-25 не употребляют.
Первое упоминание о применении маточных рожков с лечебной целью в Европе (при послеродовых болях) встречается в 1557 г. в травнике известного врача эпохи Возрождения из Франкфурта Адама Лоницеруса (1527-1587) «Adami Loniceri Naturalis historiae opus novum». О лечебных свойствах рожков вспоминает в 1588 г. в своем медицинском трактате Joachim сamerarius (1534-1591). К тому времени было известно о кровоостанавливающих свойствах рожков в гинекологической практике, на что указывает австрийский врач и ботаник Thal Johann Thalius (умер в 1587 г.) в книге «Sylva hercynica seu catalogus plantarum sponte nascentium» (1588). Но в официальную медицину маточные рожки были введены только в начале XIX в. Сократительное влияние рожков на мускулатуру матки описал в 1808 г. американский врач John Stearns, а кровоостанавливающее действие при послеродовых кровотечениях - в 1824 г. D. Hosack. В 1836 году маточные рожки были включены в Лондонскую Фармакопею, а в середине XIX в. - в фармакопеи всех стран.
Тогда же было начато изучение алкалоидов, содержащихся в склероциях гриба. Тем не менее задолго до изучения действующих компонентов склероциев их широко применяли в акушерстве. Об использовании маточных рожков в медицине упоминается в работах А. Лоницери (1582) и Р. Я. Камерариуса (1688).
Продолжительное время в народной медицине разных стран маточные рожки применяли для лечения рака матки.
Детальную ботаническую характеристику рожков сделали в 1861-1865 гг. французские ботаники Luis Rene и сharles Tulasne.
Синтезированный в 1938 г. диэтиламид лизергиновой кислоты (препарат ЛСД-25) - наркотик-легенда. В 70-е годы в США мода на ЛСД-25 была подобна эпидемии - количество людей, употребляющих этот наркотик, достигала десятков тысяч. Из них 90% составляли студенты, и столицей этой новой «религии» был Калифорнийский университет в Беркли. Практически все его студенты принимали ЛСД, причем не поодиночке, как героин или морфий, а группами. Идейным вождем этой «религии» был психолог Гарвардского университета доктор Лире, который проповедовал, что ЛСД - не просто наркотик, а средство «освобождения» и «самопознания», «создания собственного рая и ада», что «открывает дверь в мир, где проблемы жизни и смерти возникают в своих истинных измерениях». Но действительность была значительно прозаичнее: пресса ежедневно сообщала об убийствах и самоубийствах, произошедших под влиянием этого препарата, психиатрические клиники были переполнены потребителями ЛСД, которые не смогли избавиться от выпущенного на свободу монстра после того, как действие наркотика прекратилось. Сенатор Роберт Кеннеди начал расследование, в результате которого в США было принято решение о наказании за производство, транспортировку и сбыт ЛСД. По официальным данным, сегодня в Украине и России ЛСД-25 не употребляют.
Pharmacological action
Сумма биологически высокоактивных алкалоидов спорыньи является одним из важнейших источников создания лекарственных средств различного направления и механизма действия.
Алкалоиды спорыньи проявляют три основные вида биологической активности: маточную, адренолитическую (спазмолитическую) и оказывают влияние на центральную нервную систему.
Наиболее характерным и специфическим является их действие на функцию матки. Алкалоиды спорыньи значительно усиливают сокращение матки и повышают ее тонус. В экспериментах на животных небольшие дозы галеновых форм спорыньи, и особенно алкалоидных препаратов (эргометрина, эрготамина, эрготоксина), вызывают значительное усиление ритмических сокращений мускулатуры матки. По мере увеличения дозы препаратов начинает проявляться и их тонизирующий эффект, который сначала выражается уменьшением амплитуды сокращений - повышением мышечного тонуса, а потом наступает резкий спазм гладкой мускулатуры матки и сужение ее сосудов. Особенно чувствительна мускулатура матки к препаратам спорыньи при беременности и в послеродовом периоде. Допускают, что утеротонический эффект связан со стимуляцией a-адренорецепторов миометрия.
Эрготоксин, эрготамин и эргометрин оказывают тонизирующее действие на сократительную способность всех гладкомышечных органов; при введении в больших дозах могут способствовать развитию сильных судорог с ишемией и даже гангреной. Но в терапевтических дозах они выборочно действуют именно на мускулатуру матки. Наиболее выраженным избирательным действием на матку и наименьшей токсичностью (приблизительно в 3-4 раза меньше, чем эрготоксин и эрготамин) отличается эргометрин, который считается наиболее эффективным маточным средством среди алкалоидов спорыньи. После его введения в отдельных случаях эффект проявляется уже через 5 минут (действие эрготоксина и эрготамина развивается приблизительно через 20 минут). Но по продолжительности действия на сократительную способность матки эргометрин уступает эрготоксину и эрготамину. Эффект последних развивается медленнее, чем действие эргометрина.
В эксперименте алкалоиды спорыньи проявляют выраженные a-адренолитические свойства, за счет чего расширяют артериолы и расслабляют прекапиллярные сфинктеры. Они существенным образом уменьшают, но полностью не ликвидируют гипертензию, вызванную адреналином. Такой активностью обладают алкалоиды групп эрготоксина и эрготамина, структуры которых содержат пептидные остатки в сочетании с лизергиновой кислотой. Лишенный пептидного остатка эргометрин адренолитических свойств не проявляет. Вместе с тем связанный с блокадой адренорецепторов сосудорасширяющий эффект, к сожалению, нивелируется прямым сосудосуживающим миотропным действием. В связи с этим введение эрготоксина сопровождается повышением артериального давления. Естественные алкалоиды спорыньи сильно суживают коронарные сосуды, что может вызвать приступ боли ангиоспастического характера. В больших дозах эрготоксин и эрготамин наряду с сужением сосудов вызывают повреждение их эндотелия. Среди естественных алкалоидов спорыньи наименее выраженное отрицательное влияние на сосудистую стенку и артериальное давление проявляет эргометрин. В этом отношении от естественных алкалоидов выгодно отличаются их дигидрированные производные - дигидроэрготамин и дигидроэрготоксин, адренолитическое действие которых выражено значительно сильнее, чем прямое влияние на гладкую мускулатуру сосудов и матки. В связи с угнетением высвобождения норадреналина они снижают артериальное давление и вызывают расширение артериол. По выраженности β-адренолитического эффекта полусинтетические дигидроалкалоиды спорыньи приблизительно в 20 раз превосходят аналогичное действие эрготамина.
Алкалоиды спорыньи влияют на центральную нервную систему. Эрготамин и эрготоксин (и их гидропроизводные) обладают седативным действием, угнетают сосудодвигательный и дыхательный центры, возбуждают центр блуждающего нерва, снижают основной обмен, уменьшают тахикардию (при базедовой болезни, гиперсимпатикотонии); усиливают сердечные сокращения, замедляют пульс и увеличивают диурез. Гидрированные алкалоиды спорыньи обладают более выраженным сосудорасширяющим, гипотензивным и седативным действием, а также сильнее стимулируют деятельность центров блуждающего нерва, вызывая рефлекторную брадикардию. Гипотензивный эффект возникает вследствие угнетения сосудодвигательного центра и частично за счет блокады адренорепепторов сосудистой стенки. Благодаря этому гидрированные алкалоиды спорыньи применяются при неврозах, спазмах сосудов, гипертонической болезни. Они обладают также флеботоническими свойствами, в частности дигидроэргокристин входит в состав венотонического препарата анавенол. Селективное тонизирующее влияние на венозные сосуды проявляет дигидроэрготамин, стимулирующий синтез простациклина (простагландина I2) в венозной стенке.
Гидрированные алкалоиды спорыньи (дигидроэрготоксин, ницерголин) улучшают реологические свойства крови. Они угнетают активацию тромбоцитов, их агрегацию и синтез тромбоксана А2.
В опытах на животных доказано, что гидрированные алкалоиды спорыньи (дигидроэрготоксин, ницерголин) за счет улучшения микроциркуляции стимулируют метаболические процессы в ткани мозга, усиливают утилизацию кислорода и глюкозы нейронами, уменьшают накопление молочной кислоты, нормализуют базальный уровень цАМФ, стимулируют синтез нейронами белка и продукцию нейротрансмиттеров. За счет этого они нормализуют нейрохимические механизмы передачи возбуждения. Вследствие повышения концентрации ацетил-коэнзима А уменьшается холинергическая активность нейронов мозга. Оптимизация метаболических процессов в мозге под влиянием гидрированных алкалоидов спорыньи проявляется положительными электроэнцефалографическими изменениями, в частности уменьшением δ-активности и усилением α- и β-ритмов.
Установлено, что природные алкалоиды спорыньи (эргометрин), особенно его полусинтетические производные (метилэргометрин, метисергид), а также дигидроэргокристин блокируют серотонинергические рецепторы. Некоторые из них также проявляют свойства агонистов центральных дофаминергических рецепторов. Специфическим агонистом дофаминовых рецепторов (главным образом рецепторов типа D2) является бромокриптин - полусинтетическое производное эргокриптина. Бромокриптин также активно влияет на обмен норадреналина в центральной нервной системе и уменьшает выделение серотонина.
В связи со стимуляцией постсинаптических дофаминовых рецепторов нейронов гипоталамуса бромокриптин тормозит секрецию гормонов передней доли гипофиза, особенно пролактина и соматотропина. Эндогенный дофамин является физиологическим ингибитором секреции этих гормонов. Но синтез пролактина бромокриптин не нарушает. Поэтому бромокриптин значительно снижает уровень пролактина в плазме пациентов с гиперпролактинемией. Угнетение физиологической лактации и галакторее при патологическом состоянии гиперпролактинемии достигается уровнями доз, которые не влияют на секрецию других тропных гормонов передней доли гипофиза. Тормозящее влияние препарата на секрецию гормона нейтрализуется блокаторами дофаминовых рецепторов (например, аминозином).
Бромокриптин проявляет прямое влияние на дофаминергические нейроны corpus striatum, которые принимают участие в управлении моторной функцией. В эксперименте бромокриптин стимулирует продолжительное стереотипное поведение грызунов и восстанавливает поведение крыс с односторонним повреждением substantia nigra. Этот эффект отменяется ингибиторами дофамина. Поэтому считают, что бромокриптин оказывает непосредственное влияние на дофаминовые рецепторы corpus striatum.
При подкожном введении на протяжении 20 дней самкам мышей линии с3H/Bl эргокорнин-метансульфата и 2-бромэргокриптина Y. N. Sinha (1974) наблюдалось снижение массы гипофиза, яичников и матки, тогда как масса почек не менялась. При этом также уменьшалась концентрация пролактина в моче при неизменном содержании гормона роста. Кроме того, у животных снижалась масса молочной железы и содержание в ней нуклеиновых кислот. Полученные данные позволили авторам исследования предположить, что алкалоиды спорыньи вследствие первичного снижения секреции пролактина угнетают синтез нуклеиновых кислот в тканях молочной железы. Торможение секреции пролактина наблюдается также под влиянием эргокристина, эргокриптина и метилэргометрина. В связи с этим применение названных препаратов может быть преспективным для лечения опухолей молочной железы.
Бромокриптин, как и другой стимулятор D2-дофаминовых рецепторов апоморфин, вызывает рвотный рефлекс, снижает температуру тела, уменьшает акинезию, вызванную резерпином, тетрабеназином, фенотиазиновими нейролептиками. Препарат обладает гипотензивным действием, которое связано с влиянием на центральную нервную систему, симпатические нервные окончания и гладкую мускулатуру сосудов. Но, в отличие от эргометрина, метилэргометрина и других алкалоидов спорыньи , он не проявляет маточного (окситоциноподобного) действия. Бромокриптин, наоборот, угнетает сокращение матки, вызванные метилэргометрином.
Алкалоиды спорыньи снижают уровень сахара в крови и блокируют гипергликемическое действие адреналина сильнее, чем другие препараты.
Разные фармакологические эффекты проявляют и другие биологически активные соединения спорыньи. Тирамин, который по структуре подобен адреналину, сильно возбуждает сердечную деятельность, сужает артериолы, повышает артериальное давление, а также стимулирует послеродовое сокращение матки животных. Тем не менее повышение давления происходит не в результате прямого действия на сосудистую стенку, а вследствие влияния на центральную нервную систему. В концентрации 25-30 мг/кг тирамин вызывает эпилептиформный приступ, после которого наступают паралич сердца и смерть.
Сокращение матки животных вызывают также агматин и гистамин.
Исследуется возможность применения препаратов спорыньи в качестве контрацептивных средств.
В опытах in vitro продемонстрировано, что алкалоиды спорыньи усиливают лизис культуры E. coli бактериофагом Т4.
Как уже упоминалось ранее, клавиновые алкалоиды спорыньи применения в медицине не нашли. Но отдельные публикации указывают на их способность угнетать выделения пролактина и тормозить развитие злокачественных опухолей соска молочной железы.
Алкалоиды спорыньи проявляют три основные вида биологической активности: маточную, адренолитическую (спазмолитическую) и оказывают влияние на центральную нервную систему.
Наиболее характерным и специфическим является их действие на функцию матки. Алкалоиды спорыньи значительно усиливают сокращение матки и повышают ее тонус. В экспериментах на животных небольшие дозы галеновых форм спорыньи, и особенно алкалоидных препаратов (эргометрина, эрготамина, эрготоксина), вызывают значительное усиление ритмических сокращений мускулатуры матки. По мере увеличения дозы препаратов начинает проявляться и их тонизирующий эффект, который сначала выражается уменьшением амплитуды сокращений - повышением мышечного тонуса, а потом наступает резкий спазм гладкой мускулатуры матки и сужение ее сосудов. Особенно чувствительна мускулатура матки к препаратам спорыньи при беременности и в послеродовом периоде. Допускают, что утеротонический эффект связан со стимуляцией a-адренорецепторов миометрия.
Эрготоксин, эрготамин и эргометрин оказывают тонизирующее действие на сократительную способность всех гладкомышечных органов; при введении в больших дозах могут способствовать развитию сильных судорог с ишемией и даже гангреной. Но в терапевтических дозах они выборочно действуют именно на мускулатуру матки. Наиболее выраженным избирательным действием на матку и наименьшей токсичностью (приблизительно в 3-4 раза меньше, чем эрготоксин и эрготамин) отличается эргометрин, который считается наиболее эффективным маточным средством среди алкалоидов спорыньи. После его введения в отдельных случаях эффект проявляется уже через 5 минут (действие эрготоксина и эрготамина развивается приблизительно через 20 минут). Но по продолжительности действия на сократительную способность матки эргометрин уступает эрготоксину и эрготамину. Эффект последних развивается медленнее, чем действие эргометрина.
В эксперименте алкалоиды спорыньи проявляют выраженные a-адренолитические свойства, за счет чего расширяют артериолы и расслабляют прекапиллярные сфинктеры. Они существенным образом уменьшают, но полностью не ликвидируют гипертензию, вызванную адреналином. Такой активностью обладают алкалоиды групп эрготоксина и эрготамина, структуры которых содержат пептидные остатки в сочетании с лизергиновой кислотой. Лишенный пептидного остатка эргометрин адренолитических свойств не проявляет. Вместе с тем связанный с блокадой адренорецепторов сосудорасширяющий эффект, к сожалению, нивелируется прямым сосудосуживающим миотропным действием. В связи с этим введение эрготоксина сопровождается повышением артериального давления. Естественные алкалоиды спорыньи сильно суживают коронарные сосуды, что может вызвать приступ боли ангиоспастического характера. В больших дозах эрготоксин и эрготамин наряду с сужением сосудов вызывают повреждение их эндотелия. Среди естественных алкалоидов спорыньи наименее выраженное отрицательное влияние на сосудистую стенку и артериальное давление проявляет эргометрин. В этом отношении от естественных алкалоидов выгодно отличаются их дигидрированные производные - дигидроэрготамин и дигидроэрготоксин, адренолитическое действие которых выражено значительно сильнее, чем прямое влияние на гладкую мускулатуру сосудов и матки. В связи с угнетением высвобождения норадреналина они снижают артериальное давление и вызывают расширение артериол. По выраженности β-адренолитического эффекта полусинтетические дигидроалкалоиды спорыньи приблизительно в 20 раз превосходят аналогичное действие эрготамина.
Алкалоиды спорыньи влияют на центральную нервную систему. Эрготамин и эрготоксин (и их гидропроизводные) обладают седативным действием, угнетают сосудодвигательный и дыхательный центры, возбуждают центр блуждающего нерва, снижают основной обмен, уменьшают тахикардию (при базедовой болезни, гиперсимпатикотонии); усиливают сердечные сокращения, замедляют пульс и увеличивают диурез. Гидрированные алкалоиды спорыньи обладают более выраженным сосудорасширяющим, гипотензивным и седативным действием, а также сильнее стимулируют деятельность центров блуждающего нерва, вызывая рефлекторную брадикардию. Гипотензивный эффект возникает вследствие угнетения сосудодвигательного центра и частично за счет блокады адренорепепторов сосудистой стенки. Благодаря этому гидрированные алкалоиды спорыньи применяются при неврозах, спазмах сосудов, гипертонической болезни. Они обладают также флеботоническими свойствами, в частности дигидроэргокристин входит в состав венотонического препарата анавенол. Селективное тонизирующее влияние на венозные сосуды проявляет дигидроэрготамин, стимулирующий синтез простациклина (простагландина I2) в венозной стенке.
Гидрированные алкалоиды спорыньи (дигидроэрготоксин, ницерголин) улучшают реологические свойства крови. Они угнетают активацию тромбоцитов, их агрегацию и синтез тромбоксана А2.
В опытах на животных доказано, что гидрированные алкалоиды спорыньи (дигидроэрготоксин, ницерголин) за счет улучшения микроциркуляции стимулируют метаболические процессы в ткани мозга, усиливают утилизацию кислорода и глюкозы нейронами, уменьшают накопление молочной кислоты, нормализуют базальный уровень цАМФ, стимулируют синтез нейронами белка и продукцию нейротрансмиттеров. За счет этого они нормализуют нейрохимические механизмы передачи возбуждения. Вследствие повышения концентрации ацетил-коэнзима А уменьшается холинергическая активность нейронов мозга. Оптимизация метаболических процессов в мозге под влиянием гидрированных алкалоидов спорыньи проявляется положительными электроэнцефалографическими изменениями, в частности уменьшением δ-активности и усилением α- и β-ритмов.
Установлено, что природные алкалоиды спорыньи (эргометрин), особенно его полусинтетические производные (метилэргометрин, метисергид), а также дигидроэргокристин блокируют серотонинергические рецепторы. Некоторые из них также проявляют свойства агонистов центральных дофаминергических рецепторов. Специфическим агонистом дофаминовых рецепторов (главным образом рецепторов типа D2) является бромокриптин - полусинтетическое производное эргокриптина. Бромокриптин также активно влияет на обмен норадреналина в центральной нервной системе и уменьшает выделение серотонина.
В связи со стимуляцией постсинаптических дофаминовых рецепторов нейронов гипоталамуса бромокриптин тормозит секрецию гормонов передней доли гипофиза, особенно пролактина и соматотропина. Эндогенный дофамин является физиологическим ингибитором секреции этих гормонов. Но синтез пролактина бромокриптин не нарушает. Поэтому бромокриптин значительно снижает уровень пролактина в плазме пациентов с гиперпролактинемией. Угнетение физиологической лактации и галакторее при патологическом состоянии гиперпролактинемии достигается уровнями доз, которые не влияют на секрецию других тропных гормонов передней доли гипофиза. Тормозящее влияние препарата на секрецию гормона нейтрализуется блокаторами дофаминовых рецепторов (например, аминозином).
Бромокриптин проявляет прямое влияние на дофаминергические нейроны corpus striatum, которые принимают участие в управлении моторной функцией. В эксперименте бромокриптин стимулирует продолжительное стереотипное поведение грызунов и восстанавливает поведение крыс с односторонним повреждением substantia nigra. Этот эффект отменяется ингибиторами дофамина. Поэтому считают, что бромокриптин оказывает непосредственное влияние на дофаминовые рецепторы corpus striatum.
При подкожном введении на протяжении 20 дней самкам мышей линии с3H/Bl эргокорнин-метансульфата и 2-бромэргокриптина Y. N. Sinha (1974) наблюдалось снижение массы гипофиза, яичников и матки, тогда как масса почек не менялась. При этом также уменьшалась концентрация пролактина в моче при неизменном содержании гормона роста. Кроме того, у животных снижалась масса молочной железы и содержание в ней нуклеиновых кислот. Полученные данные позволили авторам исследования предположить, что алкалоиды спорыньи вследствие первичного снижения секреции пролактина угнетают синтез нуклеиновых кислот в тканях молочной железы. Торможение секреции пролактина наблюдается также под влиянием эргокристина, эргокриптина и метилэргометрина. В связи с этим применение названных препаратов может быть преспективным для лечения опухолей молочной железы.
Бромокриптин, как и другой стимулятор D2-дофаминовых рецепторов апоморфин, вызывает рвотный рефлекс, снижает температуру тела, уменьшает акинезию, вызванную резерпином, тетрабеназином, фенотиазиновими нейролептиками. Препарат обладает гипотензивным действием, которое связано с влиянием на центральную нервную систему, симпатические нервные окончания и гладкую мускулатуру сосудов. Но, в отличие от эргометрина, метилэргометрина и других алкалоидов спорыньи , он не проявляет маточного (окситоциноподобного) действия. Бромокриптин, наоборот, угнетает сокращение матки, вызванные метилэргометрином.
Алкалоиды спорыньи снижают уровень сахара в крови и блокируют гипергликемическое действие адреналина сильнее, чем другие препараты.
Разные фармакологические эффекты проявляют и другие биологически активные соединения спорыньи. Тирамин, который по структуре подобен адреналину, сильно возбуждает сердечную деятельность, сужает артериолы, повышает артериальное давление, а также стимулирует послеродовое сокращение матки животных. Тем не менее повышение давления происходит не в результате прямого действия на сосудистую стенку, а вследствие влияния на центральную нервную систему. В концентрации 25-30 мг/кг тирамин вызывает эпилептиформный приступ, после которого наступают паралич сердца и смерть.
Сокращение матки животных вызывают также агматин и гистамин.
Исследуется возможность применения препаратов спорыньи в качестве контрацептивных средств.
В опытах in vitro продемонстрировано, что алкалоиды спорыньи усиливают лизис культуры E. coli бактериофагом Т4.
Как уже упоминалось ранее, клавиновые алкалоиды спорыньи применения в медицине не нашли. Но отдельные публикации указывают на их способность угнетать выделения пролактина и тормозить развитие злокачественных опухолей соска молочной железы.

Contraindications
Спорынья (маточные рожки) - один из давно известных токсичных грибов. Все алкалоиды спорыньи очень токсичны. Симптоматика клавицепсотоксикоза (или эрготизма) обусловлена способностью алкалоидов вызывать сокращение гладких мышц и сужение сосудов и оказывать действие на нервную систему. Различают две формы эрготизма: гангренозная - «антонов огонь» (которая сопровождается нарушением трофики тканей вследствие необратимого сужения капилляров преимущественно в конечностях и ушных раковинах) и конвульсивная - «злые корчи». Факторы, обусловливающие эти две формы клавицепсотоксикоза, окончательно не выяснены. Предполагают, что конвульсивный вариант связан с дефицитом витамина А в диете.
Отравление спорыньей сопровождается повышением температуры, головокружением, сильными головными болями и болями в животе, рвотой, поносом, сильными судорогами, нередко возможен летальный исход. При невысоких дозах алкалоидов спорыньи признаки отравления проявляются нарушением зрения, постепенным притуплением слуха и нарушениями психики. Возможны частая рвота, понос, дерматоз, а также симптомы, которые напоминают неврологические нарушения при хорее.
При вскрытии людей, умерших от отравления спорыньей, отмечаются кровоизлияния и изменения в разных органах (легких, почках, матке). В кишечнике констатируются изменения тифозного характера, в глазах - помутнение хрусталика, в головном и спинном мозге - дегенеративные изменения.
В прошлом отравления спорыньей по причине загрязненности муки наблюдались довольно часто и носили характер эпидемий. Во время сильных вспышек число жертв приближалось к количеству жертв во время чумы и холеры. Гангренозная форма эрготизма была распространена во Франции. Во французской рукописи конца Х в. описаны проявления эрготизма: «…страшная беда распространилась среди людей - подлый огонь, который съедает конечности и тело». В этой рукописи описана эпидемия эрготизма в Лиможе в 994 году, которая погубила 40 тыс. человек. В 1129 г. только в округе Камбре от отравления погибло 12 тыс. жителей. Распространение эрготизма в эти годы было настолько обширным, что в 1095 г. папа Урбан II основал орден святого Антония, в задачи которого входило лечение больных эрготизмом. Отсюда и походит старинное название болезни Ignis Sager - «огонь святого Антония», или «антонов огонь». На территории Германии, восточнее от Рейна, встречалась конвульсивная форма эрготизма. В 1581 г. здесь погибло 523 человека. В 1700 г. во Франции погибло еще 2400 человек. Значительная эпидемия возникла в 1736 г. в Ганновере. В Англии эрготизм был менее распространен, единственная эпидемия зарегистрирована в 1762 г.
Длительное время природа эрготизма оставалась загадкой. Хотя спорынья была впервые описана А. Лоницери в 1582 г., предположение о том, что эта болезнь возникает при употреблении в пищу продуктов из муки, изготовленной из зараженного спорыньей зерна, были опубликованы через 200 лет. В средние века частота загрязнения ржи спорыньей достигала 25% и более. Грибковое происхождение спорыньи установил в 1764 г. Munchhausen. Подробное исследование эрготизма и его этиологии было проведено А. Тесье в 1777 г. во время эпидемии эрготизма в Солоне; были подтверждены симптомы токсикоза в экспериментах на животных.
В Х-ХIХ вв. вспышки эрготизма систематически повторялись в Западной и Центральной Европе. В России это заболевание впервые упоминается в Троицкой летописи в 1408 г. Последняя крупная вспышка эрготизма наблюдалась в 1816 г. в Бургундии. В 1929 г. эпидемия эрготизма была зарегистрирована в Ирландии. Небольшие вспышки отмечались в Европе в годы второй мировой войны. В связи с установлением контроля качества зерна и муки на мельницах (допустимо не более 0,05-0,1% примесей спорыньи в ржаной муке) случаи эрготизма стали редкостью. Поэтому в свое время даже бытовало мнение, что эрготизм является болезнью прошлого. Однако в 1951 г. в поселке Понт-Сен-Эспри в Франции снова вспыхнула эпидемия этой страшной болезни. Сначала думали, что это неизвестная вирусная инфекция или отравление ртутью. По опубликованным в 1965 г. данным в поселке болели 300 жителей, а 5 из них умерли. Даже в 1965 г. последствия токсикоза удалось ликвидировать не у всех пациентов. Сегодня явления эрготизма наблюдаются в основном при передозировке препаратов спорыньи, длительном их применении и при повышенной чувствительности к ним пациентов.
Токсические свойства спорыньи обусловлены также довольно высоким содержанием в ней гистамина, который вызывает расширение капилляров с увеличением проницаемости стенок, резкое снижение артериального давления, спазм гладкой мускулатуры бронхов, сопровождающийся одышкой, спазм гладкой мускулатуры кишечника и матки, зуд и отеки.
Нередко наблюдается эрготизм у животных (крупного рогатого скота, лошадей, свиней), что обусловлено потреблением сена, пораженного спорыньей, и проявляется как в гангренозной, так и в конвульсивной формах. У животных при клавицепсотоксикозе также возникают нарушения репродуктивной функции. При экспериментальном скармливании крупному рогатому скоту ячменя, который содержал 0,5% (по массе) спорыньи, у животных наблюдаются признаки гипертермического стресса - повышение ректальной температуры, потеря аппетита и веса тела, депрессия, снижение концентрации пролактина в сыворотке крови. По возвращении животных на нормальную диету указанные симптомы исчезли на протяжении недели.
ЛСД-25, по мнению доктора A. Stoll, является сильнейшим из всех известных психоактивных препаратов. Минимальная доза ЛСД, вызывающая психоз, составляет 0,0005 мг/кг ( 0,035 мг на человека). Оптимальная психотомиметическая доза при пероральном введении LD50 - 0,002 мг/кг, или 0,15 мг на человека (для употребляющих алкоголь, - 0,3-0,5 мг, для неупотребляющих - 0,1-0,2 мг на человека). Смертельная доза ЛСД-25 для человека LD50 составляет 1-5 мг/кг.
Биохимический механизм действия ЛСД сложный и окончательно не выяснен. Диэтиламид лизергиновой кислоты является структурным аналогом серотонина - важного нейротрансмиттера в синапсах головного мозга периферической нервной системы, которая регулирует состояние отдыха, сна и накопления энергии. ЛСД-25 проявляет выразительную антисеротониновую активность и запускает эти процессы, которые, очевидно, и являются причиной галлюцинаций. Считают, что ЛСД-25 - это малоспецифический серотонинолитик. Кроме того, он блокирует фермент моноаминооксидазу (МАО) серотонина и МАО других медиаторов нервной системы, например МАО γ-аминомасляной кислоты, МАО гистамина, МАО норадреналина.
Психотомиметическое действие ЛСД проявляется при введении его всеми возможными путями - перорально, при вдыхании аэрозолей, введении в ткани, внутривенно или непосредственно в ликвор и даже при подкожном применении. Из крови ЛСД очень быстро - через несколько минут- проникает во внутренние органы, в том числе более 70% - в кишечник и только 0,02% - в головной мозг. Тем не менее и этого количества достаточно, чтобы вызвать серьезные расстройства деятельности центральной и периферической нервной системы. Характерно, что местного действия на те органы и ткани, через которые он попадает в организм, ЛСД не проявляет. Не выявлено у ЛСД и кумулятивного действия, хотя после многократных отравлений небольшими дозами наблюдались продолжительные периоды психозов. Привыкание к ЛСД не отмечено.
При отравлении ЛСД наблюдаются разнообразные симптомы - от психических нарушений до вегетативных расстройств. Выделяют три стадии отравления ЛСД: начальную, стадию психоза и завершающую. Начальная стадия характеризуется неприятными субъективными ощущениями. Через 15 минут после попадания ЛСД в организм возникают ощущения сжатия, усталости, тревоги, голода, головокружение и головные боли, неприятные боли в области сердца и тремор рук. Одновременно наблюдаются различные вегетативные нарушения - покраснение или, наоборот, бледность кожи, ощущение жара или холода, потливость, гиперсаливация, слезоточивость, тошнота. Зрачки глаз расширяются, речь становится путанной, пульс ускоряется, дыхание замедляется. Нарушение координации движений приводит к неуверенности при ходьбе. В зависимости от дозы и способа поступления ЛСД в организм начальная стадия длится от 40 минут до 1,5 часов.
Психические нарушения начинаются с изменений эмоционального состояния и поведения, которые зависят от психического состояния человека. У одних возникают настороженность, подавленность, депрессия, у других - эйфория. Постепенно появляется иллюзорное и искаженное восприятие окружающего мира. Люди и предметы видятся в искаженном, деформированном виде и кажутся окрашенными в яркие неестественные цвета. Зрительные галлюцинации в виде ярких образов или картин дополняются слуховыми, обонятельными и тактильными галлюцинациями, которые в свою очередь вызывают зрительные иллюзии. Часто возникают синестезии (смешение восприятий), когда пораженному кажется, что он ощущает запах музыки или прикосновенье запаха, слышит звук цвета. Возникает иллюзия раздвоения личности: пораженный фиксирует все события, происходящие с ним и вокруг него, но считает, что они не имеют никакого отношения к нему. Одновременно теряется ориентация в пространстве и времени, на фоне нарушений мышления и речи обычно снижаются умственные способности. В период психоза настроение может неоднократно изменяться - от эйфории к депрессии и наоборот. У многих пораженных возникает мания преследования, они становятся недоверчивыми и враждебно настроенными. Их агрессивность особенно увеличивается в конце стадии психических расстройств, которая длится 5-8 часов с максимумом через 2-4 часа после приема препарата. Состояние сознания пораженных ЛСД квалифицируется как оглушенность различной степени. Память страдает только при сильных отравлениях, поэтому пораженные после выздоровления могут описать свои ощущения.
В завершающей стадии соматические и вегетативные расстройства постепенно исчезают. Эта стадия длится 16-18 часов, иногда 1,5-2 суток.
В связи с выраженными психотропными свойствами рассматривались перспективы применения ЛСД как боевого химического оружия. Но в связи с тем, что не найдены способы получение ЛСД, приемлемые для крупномасштабного производства, это соединение не было принято на вооружение армиями.
У пациентов препараты спорыньи могут вызывать тошноту, рвоту, диарею, аллергические реакции. Они противопоказаны при гиперчувствительности к составным компонентам препаратов, декомпенсированной недостаточности кровообращения (резистентной к гликозидам наперстянки), митральном стенозе, легочной гипертензии, остром инфаркте миокарда, резистентной к лечению гипертензии, заболеваниях периферических артерий, тяжелых нарушениях функции почек и печени, септических состояниях. Осторожно их следует применять при язвенной болезни желудка, аритмиях. Вызванные алкалоидами спорыньи тонические сокращения мускулатуры матки могут препятствовать нормальному дыханию и приводят к асфиксии новорожденного. Поэтому препараты спорыньи противопоказаны при беременности и во время родов. Опасно применять их непосредственно после рождения ребенка, поскольку спазм мускулатуры может препятствовать отделению плаценты.
При лечении эрготамином в отдельных случаях у пациентов могут возникать тошнота, рвота, диарея; при повышенной возбудимости - бледность лица, похолодание конечностей, парестезии. У лиц с повышенной чувствительностью даже в минимальных дозах возможен синдром Лериша (резкий цианоз и отсутствие пульса в нижних конечностях, боль, нарушение чувствительности по дистальному типу) вследствие нарушения кровообращения в области бифуркации брюшной аорты и ишемии нижних конечностей. Параллельно отмечается снижение пульсации других больших артерий - сонных, аксилярных. Эрготамин не следует применять на протяжении продолжительного времени, поскольку возможно развитие эрготизма. При необходимости длительного лечения после 7 дней делают перерыв на 3-4 дня. Препарат противопоказан при стенокардии и сужении периферических сосудов, выраженном атеросклерозе, в поздних стадиях гипертонической болезни, при приступах мигрени, сопровождаемых очаговыми неврологическими нарушениями, во время беременности, в 1 и 2 периодах родов, при септических состояниях и при нарушениях функции печени и почек.
Метилэргометрин может вызывать угнетение лактации, повышение артериального давления, периферические вазоспастические реакции, головокружение, при применении в высоких дозах - тошноту, рвоту, боль в животе. Описаны одиночные анафилактические реакции на препарат и неврологические осложнения - транзиторные нарушения мозгового кровообращения вследствие повышения артериального давления. Препарат противопоказан во время беременности и в 1 периоде родов, при выраженной артериальной гипертензии, стенокардии, облитерирующих заболеваниях сосудов, острых инфекциях, гиперчувствительности к алкалоидам спорыньи. С осторожностью следует его применять при печеночной и почечной недостаточности, легочном сердце, умеренной гипертензии. Не следует его одновременно применять с бромокриптином в связи с опасностью резкого повышения артериального давления.
При лечении дигидроэрготамином возможны заложенность носа, парестезии конечностей. Препарат противопоказан при коронарной недостаточности, облитерирующих заболеваниях сосудов и резистентной к лечению гипертензии. Противопоказана комбинация препарата с макролидными антибиотиками за исключением спирамицина: при этом замедляется биотрансформация алкалоидов спорыньи в печени и возникает угроза развития эрготизма с развитием некроза конечностей. Не рекомендуется одновременный прием препарата с бромокриптином и метилэргометрином в связи с риском вазоконстрикции и резкого повышения артериального давления. Препарат противопоказан в период беременности и лактации.
Побочными эффектами бромокриптина являются тошнота, иногда рвота, запоры, снижение артериального давления, побледнение пальцев рук и ног при охлаждении. В начале лечения возможны головные боли, отек слизистых оболочек. При применении в правильно подобранных дозах препарат обычно переносится хорошо. Бромокриптин противопоказан при гипотонии, после недавно перенесенного инфаркта миокарда, при выраженных нарушениях сердечного ритма, спазмах периферических сосудов, заболеваниях желудочно-кишечного тракта, психических заболеваниях. Женщины, принимающие препарат, должны находиться под наблюдением гинеколога. При лечении бромокриптином не допускается применение пероральных контрацептивов. Одновременно с бромокриптином нельзя применять антидепрессанты (амитриптилин, мелипрамин, ниаламид и др).
При передозировке препаратов спорыньи наблюдаются тошнота, рвота, спазм сосудов конечностей, угнетение дыхания, возможны судороги, кома. В случае перорального приема рекомендуется промывание желудка, назначение активированного угля. Симптоматическое лечение следует проводить под контролем функции дыхания и сердечно-сосудистой системы. В случае выраженного артериоспазма назначают сильные вазодилятаторы (нитропрусид натрия, фентоламин). При необходимости седативного эффекта можно использовать бензодиазепины.
Отравление спорыньей сопровождается повышением температуры, головокружением, сильными головными болями и болями в животе, рвотой, поносом, сильными судорогами, нередко возможен летальный исход. При невысоких дозах алкалоидов спорыньи признаки отравления проявляются нарушением зрения, постепенным притуплением слуха и нарушениями психики. Возможны частая рвота, понос, дерматоз, а также симптомы, которые напоминают неврологические нарушения при хорее.
При вскрытии людей, умерших от отравления спорыньей, отмечаются кровоизлияния и изменения в разных органах (легких, почках, матке). В кишечнике констатируются изменения тифозного характера, в глазах - помутнение хрусталика, в головном и спинном мозге - дегенеративные изменения.
В прошлом отравления спорыньей по причине загрязненности муки наблюдались довольно часто и носили характер эпидемий. Во время сильных вспышек число жертв приближалось к количеству жертв во время чумы и холеры. Гангренозная форма эрготизма была распространена во Франции. Во французской рукописи конца Х в. описаны проявления эрготизма: «…страшная беда распространилась среди людей - подлый огонь, который съедает конечности и тело». В этой рукописи описана эпидемия эрготизма в Лиможе в 994 году, которая погубила 40 тыс. человек. В 1129 г. только в округе Камбре от отравления погибло 12 тыс. жителей. Распространение эрготизма в эти годы было настолько обширным, что в 1095 г. папа Урбан II основал орден святого Антония, в задачи которого входило лечение больных эрготизмом. Отсюда и походит старинное название болезни Ignis Sager - «огонь святого Антония», или «антонов огонь». На территории Германии, восточнее от Рейна, встречалась конвульсивная форма эрготизма. В 1581 г. здесь погибло 523 человека. В 1700 г. во Франции погибло еще 2400 человек. Значительная эпидемия возникла в 1736 г. в Ганновере. В Англии эрготизм был менее распространен, единственная эпидемия зарегистрирована в 1762 г.
Длительное время природа эрготизма оставалась загадкой. Хотя спорынья была впервые описана А. Лоницери в 1582 г., предположение о том, что эта болезнь возникает при употреблении в пищу продуктов из муки, изготовленной из зараженного спорыньей зерна, были опубликованы через 200 лет. В средние века частота загрязнения ржи спорыньей достигала 25% и более. Грибковое происхождение спорыньи установил в 1764 г. Munchhausen. Подробное исследование эрготизма и его этиологии было проведено А. Тесье в 1777 г. во время эпидемии эрготизма в Солоне; были подтверждены симптомы токсикоза в экспериментах на животных.
В Х-ХIХ вв. вспышки эрготизма систематически повторялись в Западной и Центральной Европе. В России это заболевание впервые упоминается в Троицкой летописи в 1408 г. Последняя крупная вспышка эрготизма наблюдалась в 1816 г. в Бургундии. В 1929 г. эпидемия эрготизма была зарегистрирована в Ирландии. Небольшие вспышки отмечались в Европе в годы второй мировой войны. В связи с установлением контроля качества зерна и муки на мельницах (допустимо не более 0,05-0,1% примесей спорыньи в ржаной муке) случаи эрготизма стали редкостью. Поэтому в свое время даже бытовало мнение, что эрготизм является болезнью прошлого. Однако в 1951 г. в поселке Понт-Сен-Эспри в Франции снова вспыхнула эпидемия этой страшной болезни. Сначала думали, что это неизвестная вирусная инфекция или отравление ртутью. По опубликованным в 1965 г. данным в поселке болели 300 жителей, а 5 из них умерли. Даже в 1965 г. последствия токсикоза удалось ликвидировать не у всех пациентов. Сегодня явления эрготизма наблюдаются в основном при передозировке препаратов спорыньи, длительном их применении и при повышенной чувствительности к ним пациентов.
Токсические свойства спорыньи обусловлены также довольно высоким содержанием в ней гистамина, который вызывает расширение капилляров с увеличением проницаемости стенок, резкое снижение артериального давления, спазм гладкой мускулатуры бронхов, сопровождающийся одышкой, спазм гладкой мускулатуры кишечника и матки, зуд и отеки.
Нередко наблюдается эрготизм у животных (крупного рогатого скота, лошадей, свиней), что обусловлено потреблением сена, пораженного спорыньей, и проявляется как в гангренозной, так и в конвульсивной формах. У животных при клавицепсотоксикозе также возникают нарушения репродуктивной функции. При экспериментальном скармливании крупному рогатому скоту ячменя, который содержал 0,5% (по массе) спорыньи, у животных наблюдаются признаки гипертермического стресса - повышение ректальной температуры, потеря аппетита и веса тела, депрессия, снижение концентрации пролактина в сыворотке крови. По возвращении животных на нормальную диету указанные симптомы исчезли на протяжении недели.
ЛСД-25, по мнению доктора A. Stoll, является сильнейшим из всех известных психоактивных препаратов. Минимальная доза ЛСД, вызывающая психоз, составляет 0,0005 мг/кг ( 0,035 мг на человека). Оптимальная психотомиметическая доза при пероральном введении LD50 - 0,002 мг/кг, или 0,15 мг на человека (для употребляющих алкоголь, - 0,3-0,5 мг, для неупотребляющих - 0,1-0,2 мг на человека). Смертельная доза ЛСД-25 для человека LD50 составляет 1-5 мг/кг.
Биохимический механизм действия ЛСД сложный и окончательно не выяснен. Диэтиламид лизергиновой кислоты является структурным аналогом серотонина - важного нейротрансмиттера в синапсах головного мозга периферической нервной системы, которая регулирует состояние отдыха, сна и накопления энергии. ЛСД-25 проявляет выразительную антисеротониновую активность и запускает эти процессы, которые, очевидно, и являются причиной галлюцинаций. Считают, что ЛСД-25 - это малоспецифический серотонинолитик. Кроме того, он блокирует фермент моноаминооксидазу (МАО) серотонина и МАО других медиаторов нервной системы, например МАО γ-аминомасляной кислоты, МАО гистамина, МАО норадреналина.
Психотомиметическое действие ЛСД проявляется при введении его всеми возможными путями - перорально, при вдыхании аэрозолей, введении в ткани, внутривенно или непосредственно в ликвор и даже при подкожном применении. Из крови ЛСД очень быстро - через несколько минут- проникает во внутренние органы, в том числе более 70% - в кишечник и только 0,02% - в головной мозг. Тем не менее и этого количества достаточно, чтобы вызвать серьезные расстройства деятельности центральной и периферической нервной системы. Характерно, что местного действия на те органы и ткани, через которые он попадает в организм, ЛСД не проявляет. Не выявлено у ЛСД и кумулятивного действия, хотя после многократных отравлений небольшими дозами наблюдались продолжительные периоды психозов. Привыкание к ЛСД не отмечено.
При отравлении ЛСД наблюдаются разнообразные симптомы - от психических нарушений до вегетативных расстройств. Выделяют три стадии отравления ЛСД: начальную, стадию психоза и завершающую. Начальная стадия характеризуется неприятными субъективными ощущениями. Через 15 минут после попадания ЛСД в организм возникают ощущения сжатия, усталости, тревоги, голода, головокружение и головные боли, неприятные боли в области сердца и тремор рук. Одновременно наблюдаются различные вегетативные нарушения - покраснение или, наоборот, бледность кожи, ощущение жара или холода, потливость, гиперсаливация, слезоточивость, тошнота. Зрачки глаз расширяются, речь становится путанной, пульс ускоряется, дыхание замедляется. Нарушение координации движений приводит к неуверенности при ходьбе. В зависимости от дозы и способа поступления ЛСД в организм начальная стадия длится от 40 минут до 1,5 часов.
Психические нарушения начинаются с изменений эмоционального состояния и поведения, которые зависят от психического состояния человека. У одних возникают настороженность, подавленность, депрессия, у других - эйфория. Постепенно появляется иллюзорное и искаженное восприятие окружающего мира. Люди и предметы видятся в искаженном, деформированном виде и кажутся окрашенными в яркие неестественные цвета. Зрительные галлюцинации в виде ярких образов или картин дополняются слуховыми, обонятельными и тактильными галлюцинациями, которые в свою очередь вызывают зрительные иллюзии. Часто возникают синестезии (смешение восприятий), когда пораженному кажется, что он ощущает запах музыки или прикосновенье запаха, слышит звук цвета. Возникает иллюзия раздвоения личности: пораженный фиксирует все события, происходящие с ним и вокруг него, но считает, что они не имеют никакого отношения к нему. Одновременно теряется ориентация в пространстве и времени, на фоне нарушений мышления и речи обычно снижаются умственные способности. В период психоза настроение может неоднократно изменяться - от эйфории к депрессии и наоборот. У многих пораженных возникает мания преследования, они становятся недоверчивыми и враждебно настроенными. Их агрессивность особенно увеличивается в конце стадии психических расстройств, которая длится 5-8 часов с максимумом через 2-4 часа после приема препарата. Состояние сознания пораженных ЛСД квалифицируется как оглушенность различной степени. Память страдает только при сильных отравлениях, поэтому пораженные после выздоровления могут описать свои ощущения.
В завершающей стадии соматические и вегетативные расстройства постепенно исчезают. Эта стадия длится 16-18 часов, иногда 1,5-2 суток.
В связи с выраженными психотропными свойствами рассматривались перспективы применения ЛСД как боевого химического оружия. Но в связи с тем, что не найдены способы получение ЛСД, приемлемые для крупномасштабного производства, это соединение не было принято на вооружение армиями.
У пациентов препараты спорыньи могут вызывать тошноту, рвоту, диарею, аллергические реакции. Они противопоказаны при гиперчувствительности к составным компонентам препаратов, декомпенсированной недостаточности кровообращения (резистентной к гликозидам наперстянки), митральном стенозе, легочной гипертензии, остром инфаркте миокарда, резистентной к лечению гипертензии, заболеваниях периферических артерий, тяжелых нарушениях функции почек и печени, септических состояниях. Осторожно их следует применять при язвенной болезни желудка, аритмиях. Вызванные алкалоидами спорыньи тонические сокращения мускулатуры матки могут препятствовать нормальному дыханию и приводят к асфиксии новорожденного. Поэтому препараты спорыньи противопоказаны при беременности и во время родов. Опасно применять их непосредственно после рождения ребенка, поскольку спазм мускулатуры может препятствовать отделению плаценты.
При лечении эрготамином в отдельных случаях у пациентов могут возникать тошнота, рвота, диарея; при повышенной возбудимости - бледность лица, похолодание конечностей, парестезии. У лиц с повышенной чувствительностью даже в минимальных дозах возможен синдром Лериша (резкий цианоз и отсутствие пульса в нижних конечностях, боль, нарушение чувствительности по дистальному типу) вследствие нарушения кровообращения в области бифуркации брюшной аорты и ишемии нижних конечностей. Параллельно отмечается снижение пульсации других больших артерий - сонных, аксилярных. Эрготамин не следует применять на протяжении продолжительного времени, поскольку возможно развитие эрготизма. При необходимости длительного лечения после 7 дней делают перерыв на 3-4 дня. Препарат противопоказан при стенокардии и сужении периферических сосудов, выраженном атеросклерозе, в поздних стадиях гипертонической болезни, при приступах мигрени, сопровождаемых очаговыми неврологическими нарушениями, во время беременности, в 1 и 2 периодах родов, при септических состояниях и при нарушениях функции печени и почек.
Метилэргометрин может вызывать угнетение лактации, повышение артериального давления, периферические вазоспастические реакции, головокружение, при применении в высоких дозах - тошноту, рвоту, боль в животе. Описаны одиночные анафилактические реакции на препарат и неврологические осложнения - транзиторные нарушения мозгового кровообращения вследствие повышения артериального давления. Препарат противопоказан во время беременности и в 1 периоде родов, при выраженной артериальной гипертензии, стенокардии, облитерирующих заболеваниях сосудов, острых инфекциях, гиперчувствительности к алкалоидам спорыньи. С осторожностью следует его применять при печеночной и почечной недостаточности, легочном сердце, умеренной гипертензии. Не следует его одновременно применять с бромокриптином в связи с опасностью резкого повышения артериального давления.
При лечении дигидроэрготамином возможны заложенность носа, парестезии конечностей. Препарат противопоказан при коронарной недостаточности, облитерирующих заболеваниях сосудов и резистентной к лечению гипертензии. Противопоказана комбинация препарата с макролидными антибиотиками за исключением спирамицина: при этом замедляется биотрансформация алкалоидов спорыньи в печени и возникает угроза развития эрготизма с развитием некроза конечностей. Не рекомендуется одновременный прием препарата с бромокриптином и метилэргометрином в связи с риском вазоконстрикции и резкого повышения артериального давления. Препарат противопоказан в период беременности и лактации.
Побочными эффектами бромокриптина являются тошнота, иногда рвота, запоры, снижение артериального давления, побледнение пальцев рук и ног при охлаждении. В начале лечения возможны головные боли, отек слизистых оболочек. При применении в правильно подобранных дозах препарат обычно переносится хорошо. Бромокриптин противопоказан при гипотонии, после недавно перенесенного инфаркта миокарда, при выраженных нарушениях сердечного ритма, спазмах периферических сосудов, заболеваниях желудочно-кишечного тракта, психических заболеваниях. Женщины, принимающие препарат, должны находиться под наблюдением гинеколога. При лечении бромокриптином не допускается применение пероральных контрацептивов. Одновременно с бромокриптином нельзя применять антидепрессанты (амитриптилин, мелипрамин, ниаламид и др).
При передозировке препаратов спорыньи наблюдаются тошнота, рвота, спазм сосудов конечностей, угнетение дыхания, возможны судороги, кома. В случае перорального приема рекомендуется промывание желудка, назначение активированного угля. Симптоматическое лечение следует проводить под контролем функции дыхания и сердечно-сосудистой системы. В случае выраженного артериоспазма назначают сильные вазодилятаторы (нитропрусид натрия, фентоламин). При необходимости седативного эффекта можно использовать бензодиазепины.
Is used
Галеновые препараты спорыньи и их основные алкалоиды - эрготамин и эргометрин - имеют большое значение для практической медицины. Они широко применяются в акушерско-гинекологической практике при атонии матки и связанных с нею маточных кровотечениях, неполном аборте. В послеродовом периоде препараты спорыньи ускоряют инволюцию матки. Внутривенное введение эргометрина в послеродовом периоде способствует отделению плаценты, но по сравнению с окситоцином это действие выражено слабее. Галеновые и новогаленовые средства из спорыньи применяют также при меноррагиях (менструальных кровотечениях) и маточных кровотечениях, не связанных с нарушением менструального цикла (при фибромиоме, эндометритах, полипах), дисфункции яичников. В связи с хорошей растворимостью в воде безусловное преимущество имеет эргометрин. Кровоостанавливающее действие эргометрина и эрготамина обусловлено главным образом сужением сосудов при сокращении мускулатуры матки.
Вместе с тем на основе клинического наблюдения за 190 роженицами установлено, что после нормальных родов нет необходимости вводить препараты спорыньи. Полученные данные свидетельствуют, что послеродовой прием препаратов спорыньи не ускоряет сокращение матки. В результате естественного сокращения матки восстановление ее нормального состояния происходило быстрее, чем в случаях назначения препаратов спорыньи.
Эрготамин, кроме окситоциноподобного действия, проявляет обезболивающие, спазмолитические и седативные свойства. В связи с этим его применяют как специфический анальгетик при мигрени. Эрготамин уменьшает экстракраниальное кровообращение и амплитуду пульсации краниальных артерий, что лежит в основе приступов мигрени. Считают, что он угнетает взаимодействие рецепторов окончаний симпатических нервов с норэпинефрином, что обусловливает сосудосуживающий эффект.
Для лечения мигрени эрготамин часто применяется совместно с кофеином. Считают, что кофеин потенцирует действие эрготамина. Возникновение головных болей сосудистого происхождения угнетает полусинтетический аналог эргометрина - метисергид (благодаря способности блокировать серотониновые рецепторы).
Алкалоиды спорыньи проявляют адренолитические свойства, которые более выражены у производимых на основе гидрированных алкалоидов. Они теряют способность избирательно влиять на матку, но приобретают выраженные седативные и гипотензивные свойства. Дигидроэрготамин и дигидроэрготоксин назначают при неврозах, спазмах сосудов, гипертонической болезни. Дигидропроизводные алкалоидов спорыньи входят в состав препарата редергин для лечения нарушений мозгового и периферического кровообращения, гипотензивного препарата бринердин.
Бромокриптин используется в акушерстве для угнетения послеродовой лактации, когда она противопоказана (при тяжелых заболеваниях рожениц, преждевременных родах, гибели новорожденного и др). Его применение предупреждает лактацию и набухание молочных желез, восстанавливает функции яичников. Наряду с прекращением лактации бромокриптин вызывает восстановление менструального цикла и способствует наступлению беременности у женщин с гиперпролактиновой аменореей. Бромокриптин назначают также при галакторее, индуцированной приемом нейролептиков, пероральных контрацептивов и других препаратов. В эндокринологии его используют для лечения акромегалии и болезни Иценко-Кушинга.
Приблизительно в 75% случаев аменореи и галактореи лечение бромокриптином угнетает галакторею полностью или почти полностью и восстанавливает нормальный овуляторно-менструальный цикл. Менструация обычно начинается до полного угнетения галактореи, для этого необходимо в среднем 6-8 недель. Тем не менее у одних пациенток ответ развивается на протяжении нескольких дней, у других - через 8 месяцев. Галакторея может длиться и дольше, что зависит от степени стимуляции ткани молочной железы до начала лечения. Уменьшение секреции, по крайней мере, на 75% обычно наблюдается через 8-12 недель. Но в отдельных случаях эффект не проявляется даже после 12 месяцев лечения.
Бромокриптин существенно снижает повышенный уровень соматотропина в крови пациентов с акромегалией.
В связи со способностью стимулировать центральные D2-дофаминовые рецепторы бромокриптин применяется для лечения болезни Паркинсона, которая характеризуется снижением синтеза дофамина в substantia nigra. Тем не менее антипаркинсонический эффект наблюдается при применении относительно больших доз препарата, которые вызывают побочные действия. Поэтому для лечения паркинсонизма предложено применять бромокриптин в обычных терапевтических дозах (2,5 мг в день - по 1,25 мг утром и 1,25 мг вечером) одновременно с L-дофой и карбидопой.
При применении дигидроэрготоксина в клинике факт улучшения мозгового кровообращения доказан ангиографическим методом. Достигнут успех в коррекции симптомокомплекса, характерного для преждевременного старения, нарушений в эмоциональной сфере. Положительные результаты отмечены при психометрическом тестировании.
В 1932 г. Гартлауб и Тринке ввели Secale cornutum в гомеопатию. В гомеопатической практике спорынью начали использовать для лечения больных с симптомами нарушения центрального и периферического кровообращения: парестезиями в виде онемения, ощущений ползания мурашек, покалывания в ногах, похолодания или зуда конечностей. Secale cornutum в гомеопатии применяют при значительном нарушении кровообращения в артериолах, при атеросклерозе сосудов мозга, облитерирующем эндартериите и гангрене.
Вместе с тем на основе клинического наблюдения за 190 роженицами установлено, что после нормальных родов нет необходимости вводить препараты спорыньи. Полученные данные свидетельствуют, что послеродовой прием препаратов спорыньи не ускоряет сокращение матки. В результате естественного сокращения матки восстановление ее нормального состояния происходило быстрее, чем в случаях назначения препаратов спорыньи.
Эрготамин, кроме окситоциноподобного действия, проявляет обезболивающие, спазмолитические и седативные свойства. В связи с этим его применяют как специфический анальгетик при мигрени. Эрготамин уменьшает экстракраниальное кровообращение и амплитуду пульсации краниальных артерий, что лежит в основе приступов мигрени. Считают, что он угнетает взаимодействие рецепторов окончаний симпатических нервов с норэпинефрином, что обусловливает сосудосуживающий эффект.
Для лечения мигрени эрготамин часто применяется совместно с кофеином. Считают, что кофеин потенцирует действие эрготамина. Возникновение головных болей сосудистого происхождения угнетает полусинтетический аналог эргометрина - метисергид (благодаря способности блокировать серотониновые рецепторы).
Алкалоиды спорыньи проявляют адренолитические свойства, которые более выражены у производимых на основе гидрированных алкалоидов. Они теряют способность избирательно влиять на матку, но приобретают выраженные седативные и гипотензивные свойства. Дигидроэрготамин и дигидроэрготоксин назначают при неврозах, спазмах сосудов, гипертонической болезни. Дигидропроизводные алкалоидов спорыньи входят в состав препарата редергин для лечения нарушений мозгового и периферического кровообращения, гипотензивного препарата бринердин.
Бромокриптин используется в акушерстве для угнетения послеродовой лактации, когда она противопоказана (при тяжелых заболеваниях рожениц, преждевременных родах, гибели новорожденного и др). Его применение предупреждает лактацию и набухание молочных желез, восстанавливает функции яичников. Наряду с прекращением лактации бромокриптин вызывает восстановление менструального цикла и способствует наступлению беременности у женщин с гиперпролактиновой аменореей. Бромокриптин назначают также при галакторее, индуцированной приемом нейролептиков, пероральных контрацептивов и других препаратов. В эндокринологии его используют для лечения акромегалии и болезни Иценко-Кушинга.
Приблизительно в 75% случаев аменореи и галактореи лечение бромокриптином угнетает галакторею полностью или почти полностью и восстанавливает нормальный овуляторно-менструальный цикл. Менструация обычно начинается до полного угнетения галактореи, для этого необходимо в среднем 6-8 недель. Тем не менее у одних пациенток ответ развивается на протяжении нескольких дней, у других - через 8 месяцев. Галакторея может длиться и дольше, что зависит от степени стимуляции ткани молочной железы до начала лечения. Уменьшение секреции, по крайней мере, на 75% обычно наблюдается через 8-12 недель. Но в отдельных случаях эффект не проявляется даже после 12 месяцев лечения.
Бромокриптин существенно снижает повышенный уровень соматотропина в крови пациентов с акромегалией.
В связи со способностью стимулировать центральные D2-дофаминовые рецепторы бромокриптин применяется для лечения болезни Паркинсона, которая характеризуется снижением синтеза дофамина в substantia nigra. Тем не менее антипаркинсонический эффект наблюдается при применении относительно больших доз препарата, которые вызывают побочные действия. Поэтому для лечения паркинсонизма предложено применять бромокриптин в обычных терапевтических дозах (2,5 мг в день - по 1,25 мг утром и 1,25 мг вечером) одновременно с L-дофой и карбидопой.
При применении дигидроэрготоксина в клинике факт улучшения мозгового кровообращения доказан ангиографическим методом. Достигнут успех в коррекции симптомокомплекса, характерного для преждевременного старения, нарушений в эмоциональной сфере. Положительные результаты отмечены при психометрическом тестировании.
В 1932 г. Гартлауб и Тринке ввели Secale cornutum в гомеопатию. В гомеопатической практике спорынью начали использовать для лечения больных с симптомами нарушения центрального и периферического кровообращения: парестезиями в виде онемения, ощущений ползания мурашек, покалывания в ногах, похолодания или зуда конечностей. Secale cornutum в гомеопатии применяют при значительном нарушении кровообращения в артериолах, при атеросклерозе сосудов мозга, облитерирующем эндартериите и гангрене.
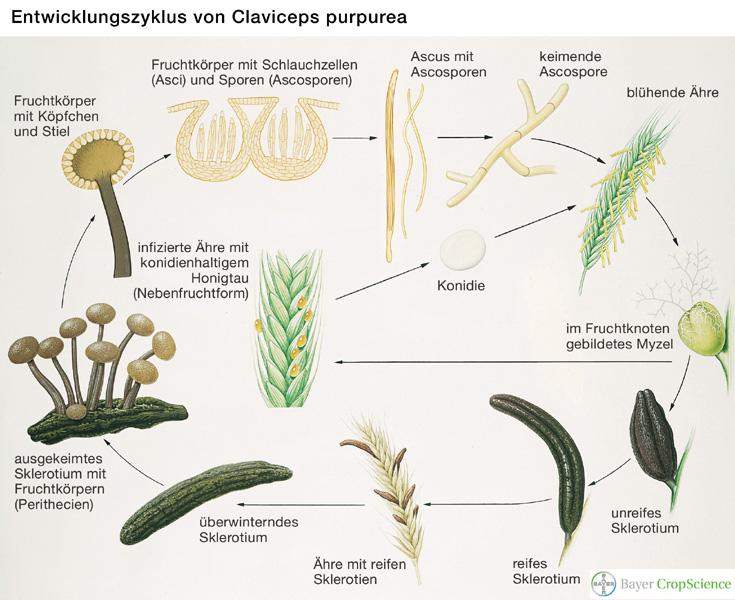
Description of the dosage form
Эрготал (Ergotalum) - сумма алкалоидов спорыньи в виде фосфатов. Выпускается в таблетках, содержащих по 1 мг суммы алкалоидов, и в виде 0,05% раствора для инъекций в ампулах по 1 мл. Применяют при маточных кровотечениях, вызванных атонией матки, для ускорения инволюции матки в послеродовом периоде. Назначают внутрь по 0,5-1 мг 2-3 раза в день или подкожно и внутримышечно по 0,5-1 мл 1-2 раза в день. Хранится по списку Б.
Эрготоксин (Ergotoxine) - смесь трех алкалоидов спорыньи: эргокристина, эргокриптина и эргокорнина. Эргометрина малеат (Ergometrini maleas, Gedeon Richter, Венгрия) - выпускается в таблетках по 0,2 мг и в ампулах по 0,5 и 1 мл 0,02% раствора (0,1 и 0,2 мг). Хранится согласно списку Б.
Применяется в акушерской практике при кровотечениях после ручного отделения плаценты и кесарева сечения, при ранних послеродовых кровотечениях, кровянистых выделениях после аборта, при кровотечениях на фоне миом матки, а также при замедленной инволюции матки в послеродовом периоде и для прерывания беременности.
Назначают внутрь, внутримышечно и внутривенно, в последнем случае наблюдается более быстрое наступление эффекта. Разовая доза при парентеральном введении 0,2 мг, при пероральном - 0,2-0,4 мг. В послеродовом периоде назначают внутрь по 0,2-0,4 мг 2-4 раза в день до исчезновения опасности кровотечения - обычно на протяжении 3 дней, внутримышечно или внутривенно по 0,5-1 мл 0,02% раствора 2-3 раза в день. Наиболее эффективным является внутривенное введение - действие отмечается уже через 0,5-1 мин. и длится 2-4 часа. Парентеральное применение можно совмещать с приемом внутрь.
Побочное действие: препарат обычно хорошо переносится, но не рекомендуется назначать его длительно. В отдельных случаях (у лиц с повышенной чувствительностью) могут возникать явления эрготизма. Препарат противопоказан во время беременности, в 1 и 2 периодах родов, при стенокардии.
В США препарат выпускается под названием Ergotrate Maleate, в Германии - Gynergen, Methergin.
Эрготамина гидротартрат (Ergotamini hydrotartras) - выпускается в ампулах по 1 мл 0,05% раствора, во флаконах по 10 мл 0,1% раствора (20 капель содержат 1 мг) и в виде таблеток (драже) по 1 мг.
Применяется в акушерской практике раннем послеродовом периоде при гипо- и атонических кровотечениях, кровотечениях во время и после кесарева сечения, для ускорения субинволюции матки после родов и аборта, в гинекологии - при сильных дисфункциональных маточных кровотечениях и геморрагиях, связанных с миомами матки, для искусственного прерывания беременности. Эрготамин назначают также при мигрени для ликвидации приступов и их предупреждения; эффективен при применении сразу после первых проявлений приступа мигрени. Есть данные о его эффективности при глаукоме.
При атонии матки и неполном аборте назначают подкожно или внутримышечно по 0,5-1 мл 0,05% раствора, в экстренных случаях вводят медленно внутривенно 0,5 мл. При других показаниях назначают внутрь по 10-15 капель 0,1% раствора или по 1 таблетке (драже) 1-3 раза в день. Для предупреждения приступа мигрени рекомендуют по 15-20 капель или по 1 драже внутрь за несколько часов до ожидаемого приступа. В начале болевой фазы приступа мигрени принимают сублингвально по 1-2 драже через каждые 30 минут (но не более 6 раз), первая доза может составлять 5 мг. Можно применять ректально (3 суппозитория по 2 мг через каждые 45 минут). После употребления препарата рекомендуется спокойно полежать в затемненной комнате. При тяжелом приступе мигрени вводят 0,5-1 мл 0,05% раствора внутримышечно. Максимальные дозы при приеме внутрь: разовая - 2 мг, суточная - 4 мг; подкожно и внутримышечно: разовая - 0,5 мг, суточная - 2 мг.
Побочное действие: в отдельных случаях могут возникать тошнота, рвота, диарея; при повышенной возбудимости - бледность лица, похолодание конечностей, парестезии. У лиц с повышенной чувствительностью даже в минимальных дозах может вызывать синдром Лериша (резкий цианоз и отсутствие пульса на нижних конечностях, боль, нарушение чувствительности по дистальному типу) вследствие нарушения кровообращения в области бифуркации брюшной аорты и ишемии нижних конечностей. Параллельно отмечается снижение пульсации других больших артерий - сонных, аксилярных. Эрготамин не следует применять длительно, поскольку возможно развитие эрготизма. При необходимости длительного лечения после 7 дней делают перерыв на 3-4 дня.
Препарат противопоказан при стенокардии и сужении периферических сосудов, выраженном атеросклерозе, в поздних стадиях гипертонической болезни, при приступах мигрени, сопровождаемых очаговыми неврологическими нарушениями, во время беременности, в 1-м и 2-м периодах родов, при септических состояниях и при нарушениях функции печени и почек.
В США эрготамина гидротартрат выпускается в виде препаратов Ergomar, Ergostat, Medihaler Ergotamine, во Франции - в виде препаратов Gynergene (Sandoz), в Германии - в виде таблеток и суппозиториев Migrexa (Sanorania), капсул Сlavigrenin acut (Hormosan), Еrgo sanol spezial N (Sanol), таблеток Ergo-Kranit mono (Krewel Meuselbach), капель Ergotamin Medihaler (3M Medica), в Австрии - Ergotartrat-Dragees (Rösch & Handel).
Р. В. Куцик, Б. М. Зузук.
Ивано-Франковская государственная медицинская академия.
Эрготоксин (Ergotoxine) - смесь трех алкалоидов спорыньи: эргокристина, эргокриптина и эргокорнина. Эргометрина малеат (Ergometrini maleas, Gedeon Richter, Венгрия) - выпускается в таблетках по 0,2 мг и в ампулах по 0,5 и 1 мл 0,02% раствора (0,1 и 0,2 мг). Хранится согласно списку Б.
Применяется в акушерской практике при кровотечениях после ручного отделения плаценты и кесарева сечения, при ранних послеродовых кровотечениях, кровянистых выделениях после аборта, при кровотечениях на фоне миом матки, а также при замедленной инволюции матки в послеродовом периоде и для прерывания беременности.
Назначают внутрь, внутримышечно и внутривенно, в последнем случае наблюдается более быстрое наступление эффекта. Разовая доза при парентеральном введении 0,2 мг, при пероральном - 0,2-0,4 мг. В послеродовом периоде назначают внутрь по 0,2-0,4 мг 2-4 раза в день до исчезновения опасности кровотечения - обычно на протяжении 3 дней, внутримышечно или внутривенно по 0,5-1 мл 0,02% раствора 2-3 раза в день. Наиболее эффективным является внутривенное введение - действие отмечается уже через 0,5-1 мин. и длится 2-4 часа. Парентеральное применение можно совмещать с приемом внутрь.
Побочное действие: препарат обычно хорошо переносится, но не рекомендуется назначать его длительно. В отдельных случаях (у лиц с повышенной чувствительностью) могут возникать явления эрготизма. Препарат противопоказан во время беременности, в 1 и 2 периодах родов, при стенокардии.
В США препарат выпускается под названием Ergotrate Maleate, в Германии - Gynergen, Methergin.
Эрготамина гидротартрат (Ergotamini hydrotartras) - выпускается в ампулах по 1 мл 0,05% раствора, во флаконах по 10 мл 0,1% раствора (20 капель содержат 1 мг) и в виде таблеток (драже) по 1 мг.
Применяется в акушерской практике раннем послеродовом периоде при гипо- и атонических кровотечениях, кровотечениях во время и после кесарева сечения, для ускорения субинволюции матки после родов и аборта, в гинекологии - при сильных дисфункциональных маточных кровотечениях и геморрагиях, связанных с миомами матки, для искусственного прерывания беременности. Эрготамин назначают также при мигрени для ликвидации приступов и их предупреждения; эффективен при применении сразу после первых проявлений приступа мигрени. Есть данные о его эффективности при глаукоме.
При атонии матки и неполном аборте назначают подкожно или внутримышечно по 0,5-1 мл 0,05% раствора, в экстренных случаях вводят медленно внутривенно 0,5 мл. При других показаниях назначают внутрь по 10-15 капель 0,1% раствора или по 1 таблетке (драже) 1-3 раза в день. Для предупреждения приступа мигрени рекомендуют по 15-20 капель или по 1 драже внутрь за несколько часов до ожидаемого приступа. В начале болевой фазы приступа мигрени принимают сублингвально по 1-2 драже через каждые 30 минут (но не более 6 раз), первая доза может составлять 5 мг. Можно применять ректально (3 суппозитория по 2 мг через каждые 45 минут). После употребления препарата рекомендуется спокойно полежать в затемненной комнате. При тяжелом приступе мигрени вводят 0,5-1 мл 0,05% раствора внутримышечно. Максимальные дозы при приеме внутрь: разовая - 2 мг, суточная - 4 мг; подкожно и внутримышечно: разовая - 0,5 мг, суточная - 2 мг.
Побочное действие: в отдельных случаях могут возникать тошнота, рвота, диарея; при повышенной возбудимости - бледность лица, похолодание конечностей, парестезии. У лиц с повышенной чувствительностью даже в минимальных дозах может вызывать синдром Лериша (резкий цианоз и отсутствие пульса на нижних конечностях, боль, нарушение чувствительности по дистальному типу) вследствие нарушения кровообращения в области бифуркации брюшной аорты и ишемии нижних конечностей. Параллельно отмечается снижение пульсации других больших артерий - сонных, аксилярных. Эрготамин не следует применять длительно, поскольку возможно развитие эрготизма. При необходимости длительного лечения после 7 дней делают перерыв на 3-4 дня.
Препарат противопоказан при стенокардии и сужении периферических сосудов, выраженном атеросклерозе, в поздних стадиях гипертонической болезни, при приступах мигрени, сопровождаемых очаговыми неврологическими нарушениями, во время беременности, в 1-м и 2-м периодах родов, при септических состояниях и при нарушениях функции печени и почек.
В США эрготамина гидротартрат выпускается в виде препаратов Ergomar, Ergostat, Medihaler Ergotamine, во Франции - в виде препаратов Gynergene (Sandoz), в Германии - в виде таблеток и суппозиториев Migrexa (Sanorania), капсул Сlavigrenin acut (Hormosan), Еrgo sanol spezial N (Sanol), таблеток Ergo-Kranit mono (Krewel Meuselbach), капель Ergotamin Medihaler (3M Medica), в Австрии - Ergotartrat-Dragees (Rösch & Handel).
Р. В. Куцик, Б. М. Зузук.
Ивано-Франковская государственная медицинская академия.