Другие названия и синонимы
Interstitial uterine fibroids.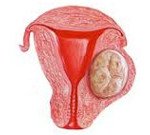
МКБ-10 коды
|
|
Описание
Интерстициальная миома матки. Опухолевидное узловое образование доброкачественной природы, развивающееся из миометрия на фоне его повышенной чувствительности к дисбалансу половых стероидов. Проявлениями интерстициальной миомы матки могут служить тяжесть и боли внизу живота, мено- и метроррагия, анемия, дизурия, запоры, бесплодие, осложнения беременности и родов. Интерстициальную миому матки диагностируют с помощью УЗИ, КТ (МРТ) органов малого таза, доплерографии, гистероскопии, лапароскопии. Для лечения интерстициальной миомы матки предлагаются гормональная терапия, ФУЗ-абляция, ЭМА, лазерная вапоризация, миомэктомия и гистерэктомия.

Дополнительные факты
Интерстициальная миома матки (лейомиома, фибромиома) - гормонально-зависимая доброкачественная опухоль тела или шейки матки, расположенная в толще мышечного слоя. Считается самой распространенной формой миомы (50-61% наблюдений). В 95% случаев поражает тело матки, в 5% диагностируется шеечная миома. Интерстициальная миома матки может локализоваться в границах миометрия (интрамуральная форма), расти внутрь полости матки (интерстициально-субмукозная) или в сторону брюшной полости, выступая наружу (интерстициально-субсерозная). Наиболее часто интерстициальная миома обнаруживается у пациенток детородного возраста (30-45 лет) - в этом возрасте на ее долю приходится около трети всей гинекологической патологии.
Причины
Основная роль в морфологической перестройке миометрия (гиперплазии и гипертрофии гладкомышечных клеток) принадлежит нарушению экскреции и метаболизма эстрогенов и баланса между его фракциями (эстроном, эстрадиолом и эстриолом) в разные фазы цикла. Ткань миомы по сравнению с нормальным миометрием богата рецепторами к эстрадиолу и прогестерону. Половые стероиды реализуют регуляцию роста миомы через комплекс ростовых факторов и индукторов (ИПФР I и II, ТФР-бета, ЭФР, СЭФР-А, ангиогенина, ФРФ-2), контролирующих пролиферацию, апоптоз и ангиогенез в ткани опухоли. Определяющим в развитии миоматозных узлов является избыточный уровень эстрогенов, способствующий ускорению митотической активности и гипертрофии клеток измененного миометрия, увеличению объема межклеточного матрикса.
Провоцировать развитие миомы матки ( , интерстициальной) могут имеющиеся у женщины эндокринные нарушения, травмы органа (частые «агрессивные» оперативные вмешательства - аборты, РДВ) и ожирение. Важным моментом выступает наследственная предрасположенность - наличие миомы у матери или сестры. Зачатки миомы могут формироваться еще в эмбриогенезе вследствие множественных соматических аберраций в нормальных клетках миометрия и после менархе начинать свой рост на фоне высокой активности яичников. Факторами риска миомы являются раннее менархе, бездетность, дисфункция гипофиза и щитовидной железы, этническая принадлежность (самая высокая частота миомы у афро-американских женщин), стрессовые ситуации.
Интерстициальная миома представлена четко отграниченным, плотным округлым узлом из измененных гладкомышечных клеток, соединительнотканных волокон и сосудов, располагающимся в толще мышечной стенки матки; чаще является множественной. Миоматозные узлы имеют разную скорость роста (простые и пролиферирующие) и в связи с этим - разный размер. Величину миоматозных узлов в гинекологии соотносят с размером матки на определенном сроке беременности. При больших объемах миом отмечается сильная деформация тела матки (асимметрия, шаровидность), нарушение ее сократительной способности. Миомы, локализованные на передней и задней стенке матки, считаются более благоприятными в плане наступлении и течения беременности, чем расположенные на шейке, перешейке матки и возле устьев маточных труб.
Провоцировать развитие миомы матки ( , интерстициальной) могут имеющиеся у женщины эндокринные нарушения, травмы органа (частые «агрессивные» оперативные вмешательства - аборты, РДВ) и ожирение. Важным моментом выступает наследственная предрасположенность - наличие миомы у матери или сестры. Зачатки миомы могут формироваться еще в эмбриогенезе вследствие множественных соматических аберраций в нормальных клетках миометрия и после менархе начинать свой рост на фоне высокой активности яичников. Факторами риска миомы являются раннее менархе, бездетность, дисфункция гипофиза и щитовидной железы, этническая принадлежность (самая высокая частота миомы у афро-американских женщин), стрессовые ситуации.
Интерстициальная миома представлена четко отграниченным, плотным округлым узлом из измененных гладкомышечных клеток, соединительнотканных волокон и сосудов, располагающимся в толще мышечной стенки матки; чаще является множественной. Миоматозные узлы имеют разную скорость роста (простые и пролиферирующие) и в связи с этим - разный размер. Величину миоматозных узлов в гинекологии соотносят с размером матки на определенном сроке беременности. При больших объемах миом отмечается сильная деформация тела матки (асимметрия, шаровидность), нарушение ее сократительной способности. Миомы, локализованные на передней и задней стенке матки, считаются более благоприятными в плане наступлении и течения беременности, чем расположенные на шейке, перешейке матки и возле устьев маточных труб.
Диагностика
Диагноз интерстициальной миомы матки устанавливают с помощью УЗИ, КТ (МРТ) органов малого таза, гистероскопии, при необходимости - РДВ, диагностической лапароскопии. При интерстициальной миоме во время гинекологического осмотра можно определить увеличение размеров и деформацию (бугристость поверхности, повышенную плотность) матки.
УЗИ малого таза позволяет визуализировать даже незначительные интерстициальные миоматозные узлы до 0,8-1 оценить гистологическое строение миомы, направление роста (центрифугальное, центрипетальное). Однородность, гиперэхогенность миоматозных узлов указывает на преобладание фиброзной ткани, наличие интранодулярных гипоэхогенных включений - на кистозные полости или некроз, гиперэхогенные элементы с акустическим эффектом поглощения - на процесс кальцинирования. С помощью допплерографии исследуют пери- и интранодулярный кровоток в сосудистой сети миоматозного узла и определяют морфотип опухоли. При простой миоме фиксируется единичный периферический кровоток, при пролиферирующей - усиленный центральный и периферический. Низкая скорость кровотока говорит о некрозе или гиалинозе узла.
Гистероскопия помогает выявить интерстициальные миомы с центрипетальном ростом за счет деформации внутренней поверхности матки, наличие вторичных изменений в миоматозных узлах. Также проводится определение онкомаркеров в крови, РДВ с морфологическим анализом ткани эндометрия. Интерстициальную миому матки необходимо дифференцировать от других видов миомы, опухолей матки, малого таза и брюшной полости (в первую очередь, злокачественных), патологических процессов эндометрия.
УЗИ малого таза позволяет визуализировать даже незначительные интерстициальные миоматозные узлы до 0,8-1 оценить гистологическое строение миомы, направление роста (центрифугальное, центрипетальное). Однородность, гиперэхогенность миоматозных узлов указывает на преобладание фиброзной ткани, наличие интранодулярных гипоэхогенных включений - на кистозные полости или некроз, гиперэхогенные элементы с акустическим эффектом поглощения - на процесс кальцинирования. С помощью допплерографии исследуют пери- и интранодулярный кровоток в сосудистой сети миоматозного узла и определяют морфотип опухоли. При простой миоме фиксируется единичный периферический кровоток, при пролиферирующей - усиленный центральный и периферический. Низкая скорость кровотока говорит о некрозе или гиалинозе узла.
Гистероскопия помогает выявить интерстициальные миомы с центрипетальном ростом за счет деформации внутренней поверхности матки, наличие вторичных изменений в миоматозных узлах. Также проводится определение онкомаркеров в крови, РДВ с морфологическим анализом ткани эндометрия. Интерстициальную миому матки необходимо дифференцировать от других видов миомы, опухолей матки, малого таза и брюшной полости (в первую очередь, злокачественных), патологических процессов эндометрия.
Лечение
Радикальный метод лечения интерстициальной миомы - удаление матки (гистерэктомия, надвлагалищная ампутация матки без придатков) - показан при множественных, крупных размерах (13-14 недель) и быстром росте миоматозных узлов, особенно в постменопаузу, некрозе или шеечном расположении миомы, выраженных кровотечениях, сочетанной патологии. У молодых пациенток репродуктивного возраста предпочтительны малоинвазивные, органосохраняющие способы лечения.
Функциональная хирургия матки с удалением миоматозных узлов (миомэктомия) дает возможность сохранить менструальную и репродуктивную функции, предупредить опущение и нарушение работы тазовых органов. Лапаротомный доступ показан при множественных объемных (7-10 см) интерстициальных миомах, шеечных и перешеечных узлах, особенно задней и боковой локализации. Небольшие интерстициальные узлы удаляют лишь при подготовке к беременности, перед стимуляцией яичников при бесплодии у женщин. Лапароскопический доступ применяется реже и часто не рекомендуется из-за риска разрывов матки во время беременности и родов. Беременность можно планировать через 6 мес. после миомэктомии, родоразрешение предпочтительно методом кесарева сечения.
При небольших интерстициальных миомах матки без заметных симптомов возможно динамическое наблюдение с ежегодным УЗИ контролем, исключением тепловых и солнечные ванн, массажа, физиопроцедур. В качестве консервативной терапии используются КОК, гестагены, иногда андрогены. Возможно применение внутриматочной гормональной системы «Мирена». С целью создания медикаментозной менопаузы применяются антигестагены (мифепристон), аналоги гонадолиберина, в перименопаузу эффективны агонисты ГнРГ. Инновационными препаратами для лечения миомы являются противофибротические и антиангиогенные средства, аналоги соматостатина. Альтернативой оперативному лечению интерстициальной миомы матки выступают ЭМА (эмболизация маточных артерий), неинвазивная ФУЗ-МРТ-абляция, лазерная вапоризация (лапароскопический миолиз).
Прогноз интерстициальной миомы матки считается благоприятным: опухоль доброкачественная, риск малигнизации минимален. Однако в некоторых случаях на фоне миомы может развиться первичное и вторичное бесплодие, при радикальном хирургическом лечении возможна потеря менструальной и репродуктивной функции у молодых пациенток.
Функциональная хирургия матки с удалением миоматозных узлов (миомэктомия) дает возможность сохранить менструальную и репродуктивную функции, предупредить опущение и нарушение работы тазовых органов. Лапаротомный доступ показан при множественных объемных (7-10 см) интерстициальных миомах, шеечных и перешеечных узлах, особенно задней и боковой локализации. Небольшие интерстициальные узлы удаляют лишь при подготовке к беременности, перед стимуляцией яичников при бесплодии у женщин. Лапароскопический доступ применяется реже и часто не рекомендуется из-за риска разрывов матки во время беременности и родов. Беременность можно планировать через 6 мес. после миомэктомии, родоразрешение предпочтительно методом кесарева сечения.
При небольших интерстициальных миомах матки без заметных симптомов возможно динамическое наблюдение с ежегодным УЗИ контролем, исключением тепловых и солнечные ванн, массажа, физиопроцедур. В качестве консервативной терапии используются КОК, гестагены, иногда андрогены. Возможно применение внутриматочной гормональной системы «Мирена». С целью создания медикаментозной менопаузы применяются антигестагены (мифепристон), аналоги гонадолиберина, в перименопаузу эффективны агонисты ГнРГ. Инновационными препаратами для лечения миомы являются противофибротические и антиангиогенные средства, аналоги соматостатина. Альтернативой оперативному лечению интерстициальной миомы матки выступают ЭМА (эмболизация маточных артерий), неинвазивная ФУЗ-МРТ-абляция, лазерная вапоризация (лапароскопический миолиз).
Прогноз интерстициальной миомы матки считается благоприятным: опухоль доброкачественная, риск малигнизации минимален. Однако в некоторых случаях на фоне миомы может развиться первичное и вторичное бесплодие, при радикальном хирургическом лечении возможна потеря менструальной и репродуктивной функции у молодых пациенток.
|
|