Другие названия и синонимы
Depreotide.Фармакологическая группа
Латинское название
Depreotidum ( Depreotidi)[[c.
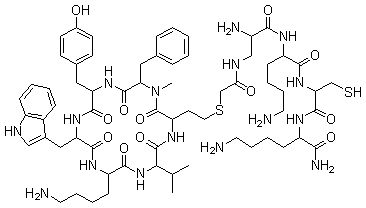
Цикло(L-гомоцистеинил-N-метил-L-фенилаланил-L-тирозил-D-триптофил-L-лизил-L-валила) (1 1 )-тиоэфир с 3-[(меркаптоацетил)амино]-L-аланил-L-лизил-L-цистеинил-L-лизинамидом.
Цикло(L-гомоцистеинил-N-метил-L-фенилаланил-L-тирозил-D-триптофил-L-лизил-L-валила) (1 1 )-тиоэфир с 3-[(меркаптоацетил)амино]-L-аланил-L-лизил-L-цистеинил-L-лизинамидом.
Код CAS
161982-62-3.
Характеристика вещества
Синтетический циклический пептид из 10 аминокислот; аналог соматостатина.[[f.
Реагент для приготовления диагностического раствора 99mTc; с высоким сродством связывается с рецепторами соматостатина подтипов 2, 3 и 5, с высокой плотностью расположенных на мембранах клеток злокачественных опухолей.[[k.
Циркулирует в плазме в основном (90%) в форме комплекса 99mTc-депреотида. Связь с белками плазмы - 12%. После в/в введения быстро выводится из крови, период полураспада - 5 мин. Объем распределения при равновесном состоянии - 1,5-3 л/кг. Наибольшее накопление препарата наблюдается в органах брюшной полости. Выводится преимущественно почками в неизмененном виде (в виде комплекса 99mTc-депреотида). Через 4 ч после инъекции в моче обнаруживается от 1 до 18% радиоактивности от введенной дозы. T1/2 - 20 Общий клиренс - 2-4 мл/мин/кг, почечный клиренс - 0,3 мл/мин/кг.[[p.
Сцинтиграфия легких при подозрении на наличие злокачественных новообразований.[[r.
Гиперчувствительность (в тч к натрия пертехнетату), беременность, период лактации (грудное вскармливание в течение 24 ч после введения препарата), детский возраст до 18 лет.[[m.
Печеночная и/или почечная недостаточность, сахарный диабет (нарушение толерантности к глюкозе и риск гипогликемии), инсулинома.[[i.
В/в, однократно, взрослым - 47 мкг депреотида (1 флакон), меченного 99mTc (активностью 555-740 МБк). Оптимальными сроками для проведения однофотонной эмиссионной компьютерной томографии грудной клетки являются 2 и 4 ч после в/в введения.
Расчетные поглощенные дозы радиации (мГр/МБк): почки - 0,09. селезенка - 0,042. яички - 0,031. щитовидная железа - 0,024. костный мозг - 0,021. печень - 0,021. кожные покровы - 0,015. стенка сердца - 0,014. легкие - 0,014. надпочечники - 0,012. поджелудочная железа - -0,01. мочевой пузырь (при опорожнении мочевого пузыря через 4,8 ч) 0,0089. матка - -.0084, тонкий кишечник - 0,005, восходящая и поперечная ободочная кишка - 0,005, нисходящая ободочная кишка - 0,0038, яичники - 0,0042. Эффективная эквивалентная доза - при введении активности 555-740 МБк - 8,88-11,84 мЭв/70 кг.
Приготовление раствора. Флакон с депреотидом нагревают до 15-30 °C, затем помещают в защищенный контейнер и добавляют натрия пертехнетат-99m с активностью до 1,8 ГБк (при необходимости разводят соответствующим количеством 0,9% NaCl до 1 мл). Для нормализации давления внутри флакона удаляют из него объем газа, равный объему добавленного натрия пертехнетата, и осторожно перемешивают покачиванием в течение 10 сек до полного растворения реагента. Флакон в защитном контейнере помещают в кипящую водяную баню и инкубируют в течение 10 мин. Уровень воды в водяной бане должен быть выше уровня раствора препарата во флаконе. Дают флакону остыть до температуры тела (примерно 15 мин) при комнатной температуре. Не следует охлаждать флакон под струей воды, поскольку это может нарушить процесс связывания с меткой.[[e.
В 0,1-1% случаев - головная боль. тошнота. рвота. диарея. боль в животе. головокружение. «приливы» крови к лицу. усталость.
Лабораторные показатели: лейкоцитоз. базофилия. эозинофилия. моноцитоз. нейтрофилия. повышение активности АСТ. АЛТ. ЛДГ. гипербилирубинемия. увеличение или снижение количества общего белка. эритропения.[[v.
Не следует смешивать с ЛС (взаимодействие не изучено).[[o.
Для уменьшения лучевой нагрузки на мочевой пузырь необходимо проведение соответствующей гидратации для частого опорожнения мочевого пузыря в течение нескольких часов после инъекции.
Работа с препаратом должна проводиться в соответствии с «Основными санитарными правилами обеспечения радиационной безопасности» (ОСПОРБ-99).
Готовый препарат должен быть использован в течение 5 ч после приготовления. [1].
Государственный реестр лекарственных средств. Официальное издание: в 2 т. М. Медицинский совет, 2009. Т.2, 1 - 568 с. 2 - 560 с.
Реагент для приготовления диагностического раствора 99mTc; с высоким сродством связывается с рецепторами соматостатина подтипов 2, 3 и 5, с высокой плотностью расположенных на мембранах клеток злокачественных опухолей.[[k.
Циркулирует в плазме в основном (90%) в форме комплекса 99mTc-депреотида. Связь с белками плазмы - 12%. После в/в введения быстро выводится из крови, период полураспада - 5 мин. Объем распределения при равновесном состоянии - 1,5-3 л/кг. Наибольшее накопление препарата наблюдается в органах брюшной полости. Выводится преимущественно почками в неизмененном виде (в виде комплекса 99mTc-депреотида). Через 4 ч после инъекции в моче обнаруживается от 1 до 18% радиоактивности от введенной дозы. T1/2 - 20 Общий клиренс - 2-4 мл/мин/кг, почечный клиренс - 0,3 мл/мин/кг.[[p.
Сцинтиграфия легких при подозрении на наличие злокачественных новообразований.[[r.
Гиперчувствительность (в тч к натрия пертехнетату), беременность, период лактации (грудное вскармливание в течение 24 ч после введения препарата), детский возраст до 18 лет.[[m.
Печеночная и/или почечная недостаточность, сахарный диабет (нарушение толерантности к глюкозе и риск гипогликемии), инсулинома.[[i.
В/в, однократно, взрослым - 47 мкг депреотида (1 флакон), меченного 99mTc (активностью 555-740 МБк). Оптимальными сроками для проведения однофотонной эмиссионной компьютерной томографии грудной клетки являются 2 и 4 ч после в/в введения.
Расчетные поглощенные дозы радиации (мГр/МБк): почки - 0,09. селезенка - 0,042. яички - 0,031. щитовидная железа - 0,024. костный мозг - 0,021. печень - 0,021. кожные покровы - 0,015. стенка сердца - 0,014. легкие - 0,014. надпочечники - 0,012. поджелудочная железа - -0,01. мочевой пузырь (при опорожнении мочевого пузыря через 4,8 ч) 0,0089. матка - -.0084, тонкий кишечник - 0,005, восходящая и поперечная ободочная кишка - 0,005, нисходящая ободочная кишка - 0,0038, яичники - 0,0042. Эффективная эквивалентная доза - при введении активности 555-740 МБк - 8,88-11,84 мЭв/70 кг.
Приготовление раствора. Флакон с депреотидом нагревают до 15-30 °C, затем помещают в защищенный контейнер и добавляют натрия пертехнетат-99m с активностью до 1,8 ГБк (при необходимости разводят соответствующим количеством 0,9% NaCl до 1 мл). Для нормализации давления внутри флакона удаляют из него объем газа, равный объему добавленного натрия пертехнетата, и осторожно перемешивают покачиванием в течение 10 сек до полного растворения реагента. Флакон в защитном контейнере помещают в кипящую водяную баню и инкубируют в течение 10 мин. Уровень воды в водяной бане должен быть выше уровня раствора препарата во флаконе. Дают флакону остыть до температуры тела (примерно 15 мин) при комнатной температуре. Не следует охлаждать флакон под струей воды, поскольку это может нарушить процесс связывания с меткой.[[e.
В 0,1-1% случаев - головная боль. тошнота. рвота. диарея. боль в животе. головокружение. «приливы» крови к лицу. усталость.
Лабораторные показатели: лейкоцитоз. базофилия. эозинофилия. моноцитоз. нейтрофилия. повышение активности АСТ. АЛТ. ЛДГ. гипербилирубинемия. увеличение или снижение количества общего белка. эритропения.[[v.
Не следует смешивать с ЛС (взаимодействие не изучено).[[o.
Для уменьшения лучевой нагрузки на мочевой пузырь необходимо проведение соответствующей гидратации для частого опорожнения мочевого пузыря в течение нескольких часов после инъекции.
Работа с препаратом должна проводиться в соответствии с «Основными санитарными правилами обеспечения радиационной безопасности» (ОСПОРБ-99).
Готовый препарат должен быть использован в течение 5 ч после приготовления. [1].
Государственный реестр лекарственных средств. Официальное издание: в 2 т. М. Медицинский совет, 2009. Т.2, 1 - 568 с. 2 - 560 с.