МКБ-10 коды
|
|
Вступление
МКБ 10: Q22.4.
Год утверждения (частота пересмотра): 2018 (не реже 1 раза в 3 года).
ID: КР36.
Профессиональные ассоциации.
• Ассоциация сердечно-сосудистых хирургов России.
Год утверждения (частота пересмотра): 2018 (не реже 1 раза в 3 года).
ID: КР36.
Профессиональные ассоциации.
• Ассоциация сердечно-сосудистых хирургов России.
Профессиональные ассоциации
• Ассоциация сердечно-сосудистых хирургов России.

 Список сокращений
Список сокращений
АВ - атриовентрикулярный.
АКГ - ангиокардиография.
АЛА - атрезия легочной артерии.
АЛТ - аланинаминотрансфераза.
АСТ - аспартатаминотрансфераза.
АТК - атрезия трехстворчатого клапана.
АоКл - аортальный клапан.
АЧТВ - активированное частичное тромбопластиновое время.
АСК - ацетилсалициловая кислота.
БДЭП - белково-дефицитная энтеропатия.
ВПВ - верхняя полая вена.
ВПС - врожденный порок сердца.
ДИЛК - дополнительные источники легочного кровотока.
ДКПА - двунаправленный кавопульмональный анастомоз.
ДМЖП - дефект межжелудочковой перегородки.
ДМПП - дефект межпредсердной перегородки.
ЛА - легочная артерия.
ЛЖ - левый желудочек.
ЛП - левое предсердие.
ЛСС - легочное сосудистое сопротивление.
МК - митральный клапан.
МНО - международное нормализованное отношение.
МПС - межпредсердное сообщение.
НК - недостаточность кровообращения.
НПВ - нижняя полая вена.
ОАП - открытый артериальный проток.
ПЖ - правый желудочек.
ПП - правое предсердие.
РКИ - рандомизированное контролируемое исследование.
СЖ - системный желудочек.
СЛА - системно-легочный анастомоз.
СН - сердечная недостаточность.
ТМА - транспозиция магистральных артерий.
ТЭО - тромбоэмболические осложнения.
ЭКГ - электрокардиография.
ЭКК - экстракардиальный кондуит.
ЭхоКГ - эхокардиография.
НПВП- нестероидные противовоспалительные препараты.
АКГ - ангиокардиография.
АЛА - атрезия легочной артерии.
АЛТ - аланинаминотрансфераза.
АСТ - аспартатаминотрансфераза.
АТК - атрезия трехстворчатого клапана.
АоКл - аортальный клапан.
АЧТВ - активированное частичное тромбопластиновое время.
АСК - ацетилсалициловая кислота.
БДЭП - белково-дефицитная энтеропатия.
ВПВ - верхняя полая вена.
ВПС - врожденный порок сердца.
ДИЛК - дополнительные источники легочного кровотока.
ДКПА - двунаправленный кавопульмональный анастомоз.
ДМЖП - дефект межжелудочковой перегородки.
ДМПП - дефект межпредсердной перегородки.
ЛА - легочная артерия.
ЛЖ - левый желудочек.
ЛП - левое предсердие.
ЛСС - легочное сосудистое сопротивление.
МК - митральный клапан.
МНО - международное нормализованное отношение.
МПС - межпредсердное сообщение.
НК - недостаточность кровообращения.
НПВ - нижняя полая вена.
ОАП - открытый артериальный проток.
ПЖ - правый желудочек.
ПП - правое предсердие.
РКИ - рандомизированное контролируемое исследование.
СЖ - системный желудочек.
СЛА - системно-легочный анастомоз.
СН - сердечная недостаточность.
ТМА - транспозиция магистральных артерий.
ТЭО - тромбоэмболические осложнения.
ЭКГ - электрокардиография.
ЭКК - экстракардиальный кондуит.
ЭхоКГ - эхокардиография.
НПВП- нестероидные противовоспалительные препараты.
Термины и определения
Атриовентрикулярная дискордантность. Аномалия развития сердца, предполагающая соединение левого предсердия с правым желудочком, а правого предсердия - с левым желудочком.
Индекс Nakata (синоним. Легочно-артериальный индекс) - отношение суммарной площади поперечного сечения правой и левой легочных артерий к площади поверхности тела.
Индекс McGoon. Отношение суммы диаметров легочных артерий у места их деления к диаметру нисходящей аорты.
Инфундибулярный стеноз. Стеноз выводного отдела правого желудочка.
Процедура Рашкинда. Баллонная атриосептостомия.
Рестриктивный. Создающий препятствие кровотоку.
Транссудация. Состояние, характеризующееся длительным поступлением жидкости из серозный полостей.
Индекс Nakata (синоним. Легочно-артериальный индекс) - отношение суммарной площади поперечного сечения правой и левой легочных артерий к площади поверхности тела.
Индекс McGoon. Отношение суммы диаметров легочных артерий у места их деления к диаметру нисходящей аорты.
Инфундибулярный стеноз. Стеноз выводного отдела правого желудочка.
Процедура Рашкинда. Баллонная атриосептостомия.
Рестриктивный. Создающий препятствие кровотоку.
Транссудация. Состояние, характеризующееся длительным поступлением жидкости из серозный полостей.
Описание
Атрезия трехстворчатого клапана (АТК) - врожденный порок сердца (ВПС), при котором правое предсердие (ПП) не открывается в желудочек через правый атриовентрикулярный (АВ) клапан. При этом имеет место одножелудочковое (синоним: унивентрикулярное) соединение, включающее левосторонний митральный клапан (МК), соединяющий морфологически левое предсердие (ЛП) и левый желудочек (ЛЖ). Другим обязательным компонентом порока, помимо отсутствия прямого сообщения между правыми предсердием и желудочком, является дефект межпредсердной перегородки (ДМПП). Положение предсердий в большинстве случаев нормальное (situs solitus), тогда как правый желудочек (ПЖ) гипоплазирован или отсутствует. Положение дна ПП в большинстве случаев не соответствует приточному отделу ПЖ, а находится над стенкой или другими структурами левого желудочка, что исключает выполнение анатомической (радикальной) коррекции порока. Обычно присутствует дефект межжелудочковой перегородки (ДМЖП), от диаметра которого в прямой зависимости находится размер ПЖ. В случае отсутствия ДМЖП легочный кровоток осуществляется за счет открытого артериального протока (ОАП) или аорто-легочных коллатералей, а клиническая картина соответствует атрезии легочной артерии (АЛА). Вентрикуло-артериальное соединение может быть конкордантным или дискордантным (транспозиция магистральных артерий). Редко при АТК может встречаться обратное (зеркальное) положение предсердий (situs inversus) [1, 2].
Причины
Предрасполагающими факторами формирования АТК, как и прочих ВПС, являются следующие: 1) хромосомные нарушения - 5%; 2) мутация одного гена - 2-3%; 3) факторы среды (алкоголизм родителей, краснуха, лекарственные препараты ) - 1-2%; 4) полигенно-мультифакториальное наследование - 90%.
Основное значение при формировании АТК имеет смещение межжелудочковой перегородки относительно предсердно-желудочкового канала на ранней стадии эмбриогенеза. В результате этого при отсутствии развития синусной части ПЖ межжелудочковая перегородка, передвигаясь вправо, приводит к облитерации правого АВ отверстия [3].
Если во время внутриутробного периода порок существенно не влияет на развитие плода, то вскоре после рождения ребенок может умереть. Это связано с небольшими размерами овального окна или его закрытием (или ОАП при некоторых вариантах порока), что делает невозможным поступление системной венозной крови в малый круг кровообращения. Гемодинамика при всех анатомических вариантах порока имеет общие черты. Венозная кровь, поступающая в ПП по полым венам, через ДМПП направляется в ЛП, где она смешивается с оксигенированной кровью, притекающей из легочных вен. При этом величина ДМПП определяет величину и градиент давления между предсердиями. При небольшом межпредсердном сообщении (МПС) ПП расширяется, стенка его гипертрофируется. В нем повышается систолическое и среднее давление, эти показатели превышают уровень давления в ЛП. Объем крови, изгоняемой ПП через небольшое МПС, мал, в связи с чем в ПП и полых венах повышается давление, что приводит к венозному застою, сердечной недостаточности (СН) и смерти пациентов. При большом МПС градиент давления между предсердиями минимальный, ПП обычных размеров, а левое значительно увеличено. Поскольку в легочном стволе и аорте циркулирует смешанная кровь, то у большинства пациентов определяется артериальная гипоксемия, степень которой зависит от объема легочного кровотока и величины МПС. При большом ДМЖП независимо от типа расположения магистральных артерий давление в желудочках одинаковое, поэтому при отсутствии стеноза легочного ствола у пациента с рождения существует гипертензия в малом круге кровообращения. В связи с увеличенным легочным кровотоком увеличивается объем оксигенированной крови, притекающей в ЛП. Следовательно, в ЛП смешивается большой объем артериальной крови с меньшим объемом венозной крови. У таких пациентов цианоз минимальный. Усиление цианоза связано с уменьшением легочного кровотока в результате развития склеротических изменений в артериальных сосудах легких. Наиболее тяжелым вариантом порока, при котором с рождения ребенка существует легочная гипертензия, является АТК с транспозицией магистральных артерий (ТМА), отсутствием ДМЖП и атрезией устья аорты. Кровообращение в большом круге происходит через ОАП. При отсутствии стеноза ЛА давление в легочном стволе, отходящем непосредственно от желудочка, всегда повышено. У пациентов с АТК и сопутствующим стенозом ЛА, независимо от характера расположения магистральных артерий, наблюдается дефицит легочного кровотока. Это приводит к тому, что в ЛП смешивается относительно небольшой объем крови, поступающей по легочным венам, и большой объем системной венозной крови. У таких пациентов наблюдаются значительная гипоксемия и резко выраженный цианоз. Состояние гемодинамики у пациентов с АТК, отсутствием ДМЖП и АЛА зависит от величины ОАП, а при его отсутствии - от размера системных коллатеральных артерий. При большом ОАП иногда отмечается легочная гипертензия. Однако в большинстве случаев небольшой диаметр протока обусловливает дефицит легочного кровотока [4].
Основное значение при формировании АТК имеет смещение межжелудочковой перегородки относительно предсердно-желудочкового канала на ранней стадии эмбриогенеза. В результате этого при отсутствии развития синусной части ПЖ межжелудочковая перегородка, передвигаясь вправо, приводит к облитерации правого АВ отверстия [3].
Если во время внутриутробного периода порок существенно не влияет на развитие плода, то вскоре после рождения ребенок может умереть. Это связано с небольшими размерами овального окна или его закрытием (или ОАП при некоторых вариантах порока), что делает невозможным поступление системной венозной крови в малый круг кровообращения. Гемодинамика при всех анатомических вариантах порока имеет общие черты. Венозная кровь, поступающая в ПП по полым венам, через ДМПП направляется в ЛП, где она смешивается с оксигенированной кровью, притекающей из легочных вен. При этом величина ДМПП определяет величину и градиент давления между предсердиями. При небольшом межпредсердном сообщении (МПС) ПП расширяется, стенка его гипертрофируется. В нем повышается систолическое и среднее давление, эти показатели превышают уровень давления в ЛП. Объем крови, изгоняемой ПП через небольшое МПС, мал, в связи с чем в ПП и полых венах повышается давление, что приводит к венозному застою, сердечной недостаточности (СН) и смерти пациентов. При большом МПС градиент давления между предсердиями минимальный, ПП обычных размеров, а левое значительно увеличено. Поскольку в легочном стволе и аорте циркулирует смешанная кровь, то у большинства пациентов определяется артериальная гипоксемия, степень которой зависит от объема легочного кровотока и величины МПС. При большом ДМЖП независимо от типа расположения магистральных артерий давление в желудочках одинаковое, поэтому при отсутствии стеноза легочного ствола у пациента с рождения существует гипертензия в малом круге кровообращения. В связи с увеличенным легочным кровотоком увеличивается объем оксигенированной крови, притекающей в ЛП. Следовательно, в ЛП смешивается большой объем артериальной крови с меньшим объемом венозной крови. У таких пациентов цианоз минимальный. Усиление цианоза связано с уменьшением легочного кровотока в результате развития склеротических изменений в артериальных сосудах легких. Наиболее тяжелым вариантом порока, при котором с рождения ребенка существует легочная гипертензия, является АТК с транспозицией магистральных артерий (ТМА), отсутствием ДМЖП и атрезией устья аорты. Кровообращение в большом круге происходит через ОАП. При отсутствии стеноза ЛА давление в легочном стволе, отходящем непосредственно от желудочка, всегда повышено. У пациентов с АТК и сопутствующим стенозом ЛА, независимо от характера расположения магистральных артерий, наблюдается дефицит легочного кровотока. Это приводит к тому, что в ЛП смешивается относительно небольшой объем крови, поступающей по легочным венам, и большой объем системной венозной крови. У таких пациентов наблюдаются значительная гипоксемия и резко выраженный цианоз. Состояние гемодинамики у пациентов с АТК, отсутствием ДМЖП и АЛА зависит от величины ОАП, а при его отсутствии - от размера системных коллатеральных артерий. При большом ОАП иногда отмечается легочная гипертензия. Однако в большинстве случаев небольшой диаметр протока обусловливает дефицит легочного кровотока [4].
|
|
Эпидемиология
АТК встречается в 1,1-3,1% случаев всех ВПС и занимает третье место по распространенности среди пороков «синего» типа [2].
Прогноз естественного течения АТК неблагоприятный: без операции на первом году жизни умирают 55-67%, а к 10 годам - до 90% детей. Тяжесть состояние и ранняя смертность могут быть обусловлены как резко уменьшенным, так и резко увеличенным легочным кровотоком, ввиду чего для пациентов с сопутствующей АЛА или нерестриктивным легочным кровотоком (отсутствие стеноза ЛА) характерен наиболее неблагоприятный прогноз. Продолжительность жизни неоперированных пациентов с относительно сбалансированным легочным кровотоком может достигать 70 лет [2, 5].
Прогноз естественного течения АТК неблагоприятный: без операции на первом году жизни умирают 55-67%, а к 10 годам - до 90% детей. Тяжесть состояние и ранняя смертность могут быть обусловлены как резко уменьшенным, так и резко увеличенным легочным кровотоком, ввиду чего для пациентов с сопутствующей АЛА или нерестриктивным легочным кровотоком (отсутствие стеноза ЛА) характерен наиболее неблагоприятный прогноз. Продолжительность жизни неоперированных пациентов с относительно сбалансированным легочным кровотоком может достигать 70 лет [2, 5].
Классификация
Выделяют следующие формы АТК:
• Мышечная (75% случаев) предполагает отсутствие АВ соединения;
• Мембранозная предполагает наличие неперфорированной мембраны [6, 7].
При мышечной форме дно ПП слепо заканчивается над свободной стенкой ЛЖ, имеет место АВ дискордантность [4]. Мембранозная форма имеет 3 варианта. При первом фиброзная диафрагма блокирует АВ отверстие и остатки клапанного аппарата обнаруживаются под мембраной в ПЖ (АТК с неперфорированной клапанной мембраной) [6-8]. Вторая - это классическая аномалия Эбштейна, но клапан не перфорирован из-за полностью спаянных створок, которые также слиты со стенкой маленького ПЖ [6, 9, 10]. Третий вариант (наиболее редкий) представлен дефектом АВ канала, при котором правосторонний клапан не перфорирован и препятствует сообщению между правыми предсердием и желудочком [11].
Выделяют 2 основных клинико-морфологических типа АТК:
• С нормальным отхождением магистральных артерий (конкордантное вентрикуло-артериальное соединение; 60-70% наблюдений), который обычно ассоциирован с обедненным легочным кровотоком;
• С транспозиционным отхождением магистральных артерий (дискордантное вентрикуло-артериальное соединение; 30-40% случаев), при котором чаще имеет место чрезмерный легочный кровоток [12, 13].
Реже встречается вентрикуло-артериальное соединение типа отхождения аорты и легочной артерии от правого или левого желудочков или типа общего артериального ствола [6]. Существуют и другие, более редкие варианты, однако порядка 80% пациентов имеют 2 основных описанных выше морфологических типа [8, 14].
• Мышечная (75% случаев) предполагает отсутствие АВ соединения;
• Мембранозная предполагает наличие неперфорированной мембраны [6, 7].
При мышечной форме дно ПП слепо заканчивается над свободной стенкой ЛЖ, имеет место АВ дискордантность [4]. Мембранозная форма имеет 3 варианта. При первом фиброзная диафрагма блокирует АВ отверстие и остатки клапанного аппарата обнаруживаются под мембраной в ПЖ (АТК с неперфорированной клапанной мембраной) [6-8]. Вторая - это классическая аномалия Эбштейна, но клапан не перфорирован из-за полностью спаянных створок, которые также слиты со стенкой маленького ПЖ [6, 9, 10]. Третий вариант (наиболее редкий) представлен дефектом АВ канала, при котором правосторонний клапан не перфорирован и препятствует сообщению между правыми предсердием и желудочком [11].
Выделяют 2 основных клинико-морфологических типа АТК:
• С нормальным отхождением магистральных артерий (конкордантное вентрикуло-артериальное соединение; 60-70% наблюдений), который обычно ассоциирован с обедненным легочным кровотоком;
• С транспозиционным отхождением магистральных артерий (дискордантное вентрикуло-артериальное соединение; 30-40% случаев), при котором чаще имеет место чрезмерный легочный кровоток [12, 13].
Реже встречается вентрикуло-артериальное соединение типа отхождения аорты и легочной артерии от правого или левого желудочков или типа общего артериального ствола [6]. Существуют и другие, более редкие варианты, однако порядка 80% пациентов имеют 2 основных описанных выше морфологических типа [8, 14].
Клиническая картина
Клиническая картина АТК зависит в основном от величины ДМПП и состояния кровотока в малом круге кровообращения [2, 4].
В случае обедненного легочного кровотока с рождения или вскоре после него развивается цианоз. Насыщение крови кислородом составляет 70-80%. Цианоз усиливается при нагрузке (движение, плач, кормление), в том числе, - по мере увеличения возраста и роста ребенка. У 10-15% пациентов отмечают одышечно-цианотические приступы; характер их такой же, как при тетраде Фалло (приступы обусловлены спазмом выводного отдела ПЖ или спазмом мышц в области ДМЖП, ограничивающими поступление крови в ЛА). В ряде случаев имеет место прогрессирование инфундибулярного стеноза или закрытие ДМЖП (30-44% случаев), что приводит к прогрессированию цианоза кто ранее были относительно бледны, могут стать синюшными в течение нескольких месяцев. Таким образом, большинство пациентов с АТК находятся в тяжелом состоянии, обусловленного, в первую очередь, хронической артериальной гипоксемией. Избыточный легочный кровоток при АТК встречается значительно реже. Цианоз таких пациентов в раннем детском возрасте часто отсутствует или нерезко выражен. Нарастание цианоза у детей старшего возраста обычно связано с прогрессирующим уменьшением легочного кровотока в результате развития морфологических изменений в артериальных сосудах легких, обусловленных чрезмерным кровотоком.
У большинства пациентов присутствует одышка. В случае обедненного легочного кровотока она имеет место и в покое, также усиливаясь при нагрузке. В случае избыточного легочного кровотока одышка нередко сочетается с признаками СН, выраженной в большей или меньшей степени (от чрезмерной потливости и тахикардии до гепатомегалии, отеков, асцита и/или гидроторакса).
Постепенно происходит изменение дистальных фаланг пальцев рук по типу «барабанных палочек» и «часовых стекол», что обусловлено хронической артериальной гипоксемией. Описанные изменения фаланг пальцев кистей чаще распространены у детей, переживших двухлетний возраст, но иногда могут развиваются уже в 3-4 месяца.
Помимо специфической клинической картины, около 70% пациентов имеют отставание в физическом развитии, а также сколиоз.
При аускультации легких возможно выслушивание застойных хрипов, что характерно для избыточного легочного кровотока и развития СН.
При аускультации сердца у большинства пациентов с конкордантным вентрикуло-артериальным соединением и обедненным легочным кровотоком определяется грубый систолический шум с эпицентром по левому краю грудины. В случае прогрессирующей обструкции легочного кровотока шумы уменьшаются или исчезают. Также может быть слышен непрерывный шум ОАП у пациентов с сопутствующей АЛА и иногда у детей с легочным стенозом. При чрезмерном легочном кровотоке обычно слышен апикальный средне-диастолический шум, а также постоянное расщепление второго тона у основания сердца [1, 3, 5, 15-17].
В случае обедненного легочного кровотока с рождения или вскоре после него развивается цианоз. Насыщение крови кислородом составляет 70-80%. Цианоз усиливается при нагрузке (движение, плач, кормление), в том числе, - по мере увеличения возраста и роста ребенка. У 10-15% пациентов отмечают одышечно-цианотические приступы; характер их такой же, как при тетраде Фалло (приступы обусловлены спазмом выводного отдела ПЖ или спазмом мышц в области ДМЖП, ограничивающими поступление крови в ЛА). В ряде случаев имеет место прогрессирование инфундибулярного стеноза или закрытие ДМЖП (30-44% случаев), что приводит к прогрессированию цианоза кто ранее были относительно бледны, могут стать синюшными в течение нескольких месяцев. Таким образом, большинство пациентов с АТК находятся в тяжелом состоянии, обусловленного, в первую очередь, хронической артериальной гипоксемией. Избыточный легочный кровоток при АТК встречается значительно реже. Цианоз таких пациентов в раннем детском возрасте часто отсутствует или нерезко выражен. Нарастание цианоза у детей старшего возраста обычно связано с прогрессирующим уменьшением легочного кровотока в результате развития морфологических изменений в артериальных сосудах легких, обусловленных чрезмерным кровотоком.
У большинства пациентов присутствует одышка. В случае обедненного легочного кровотока она имеет место и в покое, также усиливаясь при нагрузке. В случае избыточного легочного кровотока одышка нередко сочетается с признаками СН, выраженной в большей или меньшей степени (от чрезмерной потливости и тахикардии до гепатомегалии, отеков, асцита и/или гидроторакса).
Постепенно происходит изменение дистальных фаланг пальцев рук по типу «барабанных палочек» и «часовых стекол», что обусловлено хронической артериальной гипоксемией. Описанные изменения фаланг пальцев кистей чаще распространены у детей, переживших двухлетний возраст, но иногда могут развиваются уже в 3-4 месяца.
Помимо специфической клинической картины, около 70% пациентов имеют отставание в физическом развитии, а также сколиоз.
При аускультации легких возможно выслушивание застойных хрипов, что характерно для избыточного легочного кровотока и развития СН.
При аускультации сердца у большинства пациентов с конкордантным вентрикуло-артериальным соединением и обедненным легочным кровотоком определяется грубый систолический шум с эпицентром по левому краю грудины. В случае прогрессирующей обструкции легочного кровотока шумы уменьшаются или исчезают. Также может быть слышен непрерывный шум ОАП у пациентов с сопутствующей АЛА и иногда у детей с легочным стенозом. При чрезмерном легочном кровотоке обычно слышен апикальный средне-диастолический шум, а также постоянное расщепление второго тона у основания сердца [1, 3, 5, 15-17].
Диагностика
2,1 Жалобы и анамнез.
• При сборе анамнеза и жалоб рекомендуется расспросить пациента (или его родственников) о времени появления цианоза, наличии или отсутствии его прогрессирования, а также о наличии и характере одышки для верификации диагноза и оценке общего состояния [1, 3, 5, 15-17].Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
• При сборе анамнеза и жалоб, для оценки степени выраженности недостаточности кровообращения (НК), рекомендуется расспросить пациента (или его родственников) о наличии и характере потливости [1, 3, 5, 15-18].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
2,2 Физикальное обследование.
• Во время физикального обследования рекомендуется обратить внимание на признаки хронической артериальной гипоксемии у пациента (симптом «барабанных палочек», «часовых стекол») [1, 3, 5, 15-17].Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
• Для косвенной оценки соотношения легочного и системного кровотока, а также тяжести состояния пациента, во время физикального обследования рекомендуется определить уровень системной оксигенации путем пульсоксиметрии (насыщение крови кислородом) [1, 3, 5, 15-17].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
• Во время физикального обследования, для оценки степени выраженности НК и тяжести состояния пациента, рекомендуется обратить внимание на характер и частоту дыхания [1, 3, 5, 15-18].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. При осмотре дыхание пациента может быть физиологическим, с умеренным (втяжением межреберных промежутков) и выраженным (одышка) вовлечением вспомогательной мускулатуры.
• Во время физикального обследования пациента рекомендуется обратить внимание на аускультацию легких для выявления наличия или отсутствия застойных хрипов [1, 3, 5, 15-17].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
• Во время физикального обследования, для определения характера шумов и косвенной оценки состояния легочного кровотока, рекомендуется выполнить аускультацию сердца ( см пункт 1,6) [1, 3, 5, 15-18].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
• Во время физикального обследования пациента рекомендуется обратить внимание на пальпацию живота для выявления наличия или отсутствия гепатомегалии [1, 3, 5, 15-17].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. Тщательно собранный анамнез и данные физикального обследования позволяют точно определить степень выраженности НК и функциональный статус пациента. В детской кардиологической практике для быстрой оценки степени выраженности НК хорошо зарекомендовала себя модифицированная шкала Ross [18].
2,3 Лабораторная диагностика.
• Рекомендуется выполнить общий анализ крови пациенту для определения исходного уровня гемоглобина и тромбоцитов перед оперативным вмешательством [1, 3, 15-17].Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
• Всем пациентам рекомендуется биохимическое исследование крови для оценки функции печени и почек [15].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. Для оценки функции печени целесообразно выполнить анализ уровня общего белка и альбумина, АСТ, АЛТ, билирубина (общий, прямой, непрямой). Для оценки функции почек целесообразно выполнить анализ уровня мочевины, креатинина.
• С целью выявления исходных нарушений системы гемостаза, а также для оценки эффективности послеоперационной тромбопрофилактики, всем пациентам рекомендуется исследование свертывающей системы крови [1, 19].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. На сегодняшний день известным фактом является наличие исходных аномалий свертывающей системы крови у пациентов с одножелудочковой гемодинамикой. Ввиду этого, таким пациентам целесообразно определение показателей локальных (активированное частичное тромбоплатиновое время, фибриноген, международное нормализованное отношение, степень агрегации тромбоцитов) и, при наличии возможности, - глобальных тестов (тромбодинамика 3D) оценки гемостаза.
2,4 Инструментальная диагностика.
• Всем пациентам рекомендуется выполнение ЭКГ для исключения нарушений ритма и проводимости, а также ишемии миокарда [1, 4, 15-17].Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. При АТК с обедненным легочным кровотоком наблюдается отклонение электрической оси сердца влево, признаки гипертрофии ЛЖ и ПП. В случае избыточного легочного кровотока изменения ЭКГ схожи с описанными, однако у таких пациентов чаще регистрируется высокий и расширенный зубец Р в отведениях I, II, aVL, левых грудных, что является признаком гипертрофии ЛП.
• Всем пациентам с АТК рекомендуется выполнение рентгенографии органов грудной полости для оценки степени кардиомегалии и состояния легочного кровотока, а также определения участков гипо- или гипервентиляции легких [1, 4, 15-17].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. В случае обедненного легочного кровотока при рентгеноскопии в передне-задней проекции определяется повышенная прозрачность легочных полей за счет обеднения легочного рисунка. Тень сердца нормальных размеров или слегка увеличена, правый атриовазальный угол смещен вверх, что указывает на увеличение ПП. Левый контур сердца закруглен, верхушка приподнята над диафрагмой, талия сердца подчеркнута. В косых проекциях определяется увеличение ПП и ЛЖ, а также «срезанный» передний контур сердца в проекции ПЖ. При избыточном легочном кровотоке отмечается выраженное усиление легочного рисунка. Тень сердца значительно увеличена, преимущественно за счет левых отделов. При нормальном расположении магистральных артерий по левому контуру сердца определяется выбухание сегмента ЛА.
• Эхокардиографическое исследование рекомендуется всем пациентам с подозрением на АТК как ведущий метод диагностики, позволяющий установить окончательный диагноз [1, 4, 15-17].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. Типичная эхокардиографическая картина включает отсутствие эхо-сигнала от трехстворчатого клапана, локацию небольшой полости ПЖ, перерыв эхо-сигнала в области межпредсердной перегородки и наличие увеличенной полости ЛЖ. При проведении ЭхоКГ необходимо обратить внимание на следующие моменты: 1) положение рудиментарного желудочка; 2) положение магистральных артерий, их размеры, анатомия полулунных клапанов; 3) при дискордантном положении магистральных артерий - размеры ДМЖП и соотношение его с кольцом аортального клапана (АоКл); 4) анатомия левого АВ клапана, степень его недостаточности; 5) размеры МПС, ОАП, направление сброса через них; 6) наличие сопутствующих пороков (коарктация аорты, перерыв дуги аорты); 7) сократительная функция системного желудочка (СЖ).
• Магнитно-резонансная томография рекомендуется пациентам с подозрением на АТК в случаях наличия затруднения в установлении морфологии порока при помощи ЭхоКГ [1, 5, 16, 17, 20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. Методика точно отображает анатомию артериальных и венозных сосудов, клапанного аппарата, субстрат субаортального стеноза, внутрисердечную анатомию, объем желудочков, степень гипертрофии миокарда.
• Рекомендуется проведение АКГ и катетеризации полостей сердца всем пациентам с АТК с целью [1, 4, 16, 17, 20]:
1) уточнения диагноза при недостаточности данных, полученных в ходе ЭхоКГ;
2) оценки размеров легочных артерий;
3) оценки характера обструкции ЛА с возможностью устранения стенозов;
4) оценки размеров МПС и выполнения процедуры Рашкинда при необходимости ( см пункт 3,2);
5) оценки и устранения коллатералей между системными и легочными венами;
6) оценки и устранения аорто-легочных коллатералей (устранение рекомендовано перед операцией Фонтена);
7) у пациентов с системно-легочным анастомозом для оценки его функции;
8) с целью выполнения коронарографии пациентам с клиническими проявлениями стенокардии, ишемическими изменениями на ЭКГ или аномалиями коронарных сосудов.
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. Обследование включает измерение давления и насыщения кислородом в ЛА (наибольшее значение имеет оценка среднего давления), аорте, предсердиях, ЛЖ, определение легочного и системного кровотока, легочного сосудистого сопротивления (ЛСС). ЛСС - показатель, производный от давления в ЛА, оценивающий возможности легочных артерий отвечать на увеличение объема. В большинстве случаев операции, выполняемые с целью коррекции АТК, направлены на увеличение легочного кровотока, поэтому определение давления в ЛА и ЛСС - важные моменты лечебно-диагностического поиска, влияющие на выбор последующей хирургической тактики. Ангиография позволяет оценить анатомию магистральных артерий (особенно ЛА; рассчитывают индексы Nakata и McGoon), гипертрофию миокарда. Для решения вопроса о выборе метода хирургического лечения чрезвычайно важна левая вентрикулография. Она позволяет создать представление о величине ДМЖП, объеме полости гипоплазированного ПЖ, тяжести легочного стеноза, состоятельности левого АВ клапана, характере расположения магистральных артерий. У пациентов с нормальным расположением магистральных артерий из гипоплазированного ПЖ всегда контрастируется ЛА. При ТМА соотношения обратные: из гипоплазированного желудочка контрастируется аорта, а из ЛЖ - легочный ствол, располагающийся сзади и слева от аорты.
|
|
Лечение
3,1 Консервативное лечение.
Консервативные мероприятия направлены на регулирование резистентности легочных или системных сосудов.• У новорожденных с резко обедненным легочным кровотоком рекомендуется применение простагландинов группы Е для поддержания проходимости ОАП [15].
Комментарии. Среди препаратов наиболее распространено применение алпростадила**. Начальная доза составляет 0,02 мкг/кг/мин с возможностью увеличения до 0,05-0,1 мкг/кг/мин, поддерживающая доза - 0,002 мкг/кг/мин.
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
• Рекомендуется применение диуретиков у всех пациентов с СН [15].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарий. Наиболее часто применяются возрастные дозировки фуросемида**; спиронолактона**.
3,2 Хирургическое лечение.
Хирургическая коррекция АТК носит паллиативный (одножелудочковый) характер. Выбор той или иной паллиативной операции зависит в основном от состояния кровотока в малом круге кровообращения.3,2,1 1 этап хирургического лечения.
Основные цели данного этапа. Максимально сбалансировать системный и легочный кровоток, обеспечить беспрепятственное смешивание крови на уровне предсердий, обеспечить необструктивный выход из СЖ [1].• В силу анатомических особенностей, не рекомендуется выполнение двужелудочковой коррекции АТК [1 , 4, 15].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Среди паллиативных операций выделяют следующие:
• Процедура Рашкинда рекомендуется в качестве неотложной меры помощи у новорожденных при наличии рестриктивного МПС [1 , 4, 15].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4 ).
Комментарии. Под рестриктивным МПС понимается наличие сообщения на уровне предсердий, при котором существует разность давлений между правым и левым предсердиями. В этом случае может иметь место сопротивление кровотоку на уровне данного МПС.
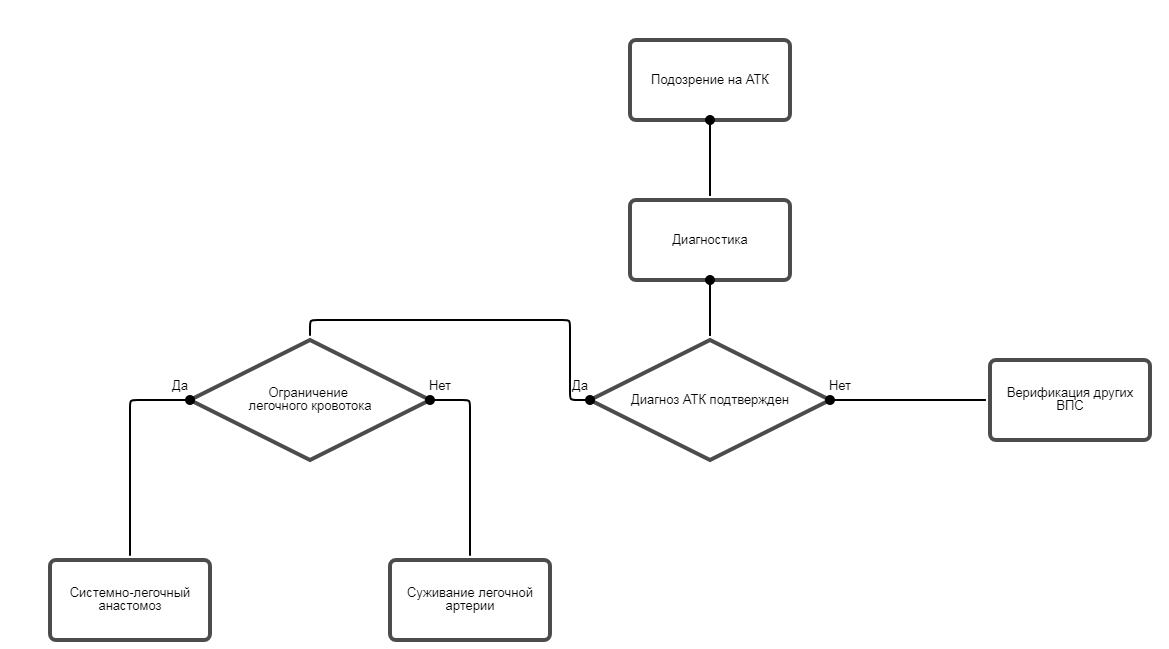
• Суживание ЛА (операция Muller) и перевязка ОАП (при его наличии) рекомендуется в периоде новорожденности при резко увеличенном легочном кровотоке с целью ограничения легочного кровотока и «защиты» малого круга кровообращения от развития склеротических изменений [1, 4, 16, 17, 20-22].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. Избыточный легочный кровоток способствует развитию тяжелой СН и высокой легочной гипертензии.
• Рекомендуется создание системно-легочного анастомоза (СЛА) у пациентов в периоде новорожденности при насыщении крови кислородом менее 70-75% [1, 4, 16, 17, 20-22].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. Выраженная гипоксемия часто характерна для тяжелого стеноза ЛА (нередко при ОАП-зависимом легочном кровотоке). Предпочтительное выполнение СЛА - в возрасте до 3-х месяцев.
• В ранние сроки после СЛА пациентам р екомендуется проведение тромбопрофилактики [23, 24].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. Для целей ранней тромбопрофилактики наиболее часто применяется гепарин натрия**, который, при отсутствии противопоказаний, назначается внутривенно капельно, по мере стабилизации хирургического гемостаза, в большинстве случаев - через 12-24 часа после операции. Разведение: 2 мл гепарина натрия** 48 мл физиологического раствора. Начальная доза - 20 ед/кг/час со скоростью, равной 1/10 веса пациента в кг. До начала инфузии препарата, для повышения его эффективности, целесообразно ввести в/в струйно 50 ед/кг однократно. Запрещено применение у новорожденных, в особенности недоношенных или имеющих низкую массу тела детей.
• Во время тромбопрофилактики гепарином натрия** после СЛА р екомендуется поддержание АЧТВ в пределах 50-85 сек [23, 24].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. Существуют указания на связь гиперкоагуляционных состояний и низких значений АЧТВ (менее 50 сек).
• Рекомендуется контроль уровня тромбоцитов крови у пациентов в случае применения гепарина натрия** свыше 5 суток с целью исключения гепарин-индуцированной тромбоцитопении [23, 24].
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 4).
• В отдаленные сроки после СЛА пациентам рекомендуется проведение долговременной тромбопрофилактики [23, 24].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. Для целей долговременной тромбопрофилактики после СЛА применяется ацетилсалициловая кислота** в дозе 5 мг/кг/сутки (для детей до 18 лет применение вне зарегистрированных показаний). По мере стабилизации состояния пациента и появления возможности приема пищи препарат добавляется к инфузии гепарина натрия**. В течение последующих суток подобной комбинированной тромбопрофилактики поддерживается целевое значение АЧТВ 50-85 сек. Со вторых суток от начала приема ацетилсалициловой кислоты** гепарин натрия** отменяют. Далее продолжается тромбопрофилактика изолированно ацетилсалициловой кислотой**, которая назначается на срок не менее 6 мес или до момента следующего этапа хирургического лечения.
• Рекомендуется контроль степени агрегации тромбоцитов у пациентов после назначения ацетилсалициловой кислоты** с целью долговременной тромбопрофилактики после СЛА [23, 24].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. Контроль показателя проводится через 2-5 дня от начала приема препарата. Критерием эффективности ацетилсалициловой кислоты** считается снижение показателя не менее, чем на 50% от исходного значения. Случаи снижения степени агрегации тромбоцитов менее, чем на 50% от исходного могут быть связаны с недостаточной дозой ацетилсалициловой кислоты**, а также не исключают наличия резистентности пациента к препарату. При наличии резистентности решается вопрос о смене препарата для долговременной тромбопрофилактики (например, на варфарин**).
3,2,2 Гемодинамическая коррекция.
Следующим этапом выполняется так называемая «гемодинамическая» (одножелудочковая) коррекция, заключающаяся в создании тотального кавопульмонального анастомоза (синоним: «полный обход» правого сердца). Цель данного этапа - снижения преднагрузки СЖ и увеличение системной оксигенации [1].• В качестве первого этапа гемодинамической коррекции рекомендуется выполнение двунаправленного кавопульмонального анастомоза (ДКПА; синоним: верхний кавопульмональный анастомоз) [1, 2, 4, 16, 17, 20-22].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
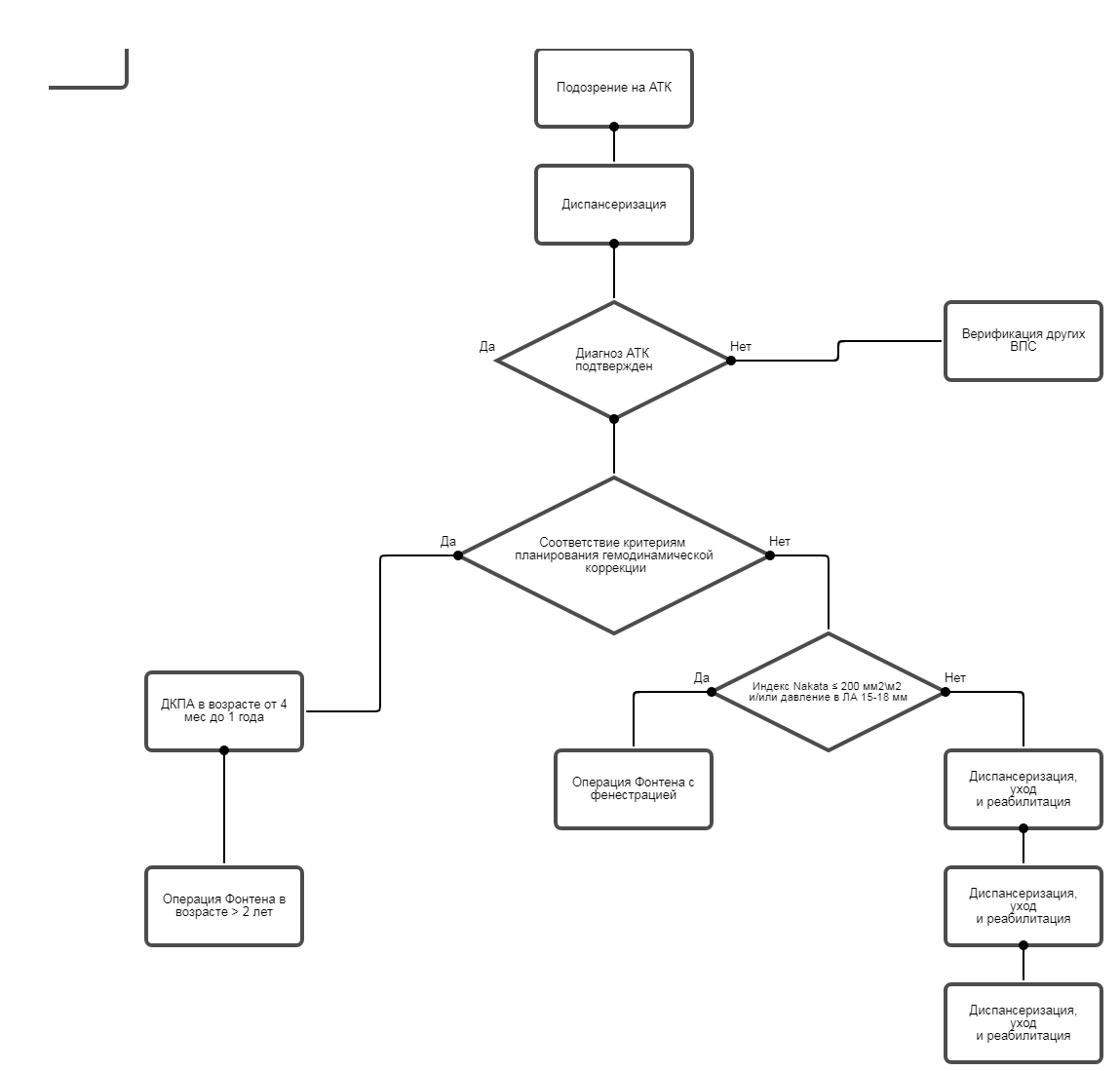
Комментарии. ДКПА заключается в создании анастомоза «конец в бок» между верхней полой веной (ВПВ) и соответствующей главной ветвью ЛА. Предпочтительное выполнение - в возрасте от 4-х мес до 1 года. В большинстве случаев после ДКПА насыщение крови кислородом устанавливается в пределах 80%.
• В качестве второго (заключительного) этапа гемодинамической коррекции рекомендуется выполнение анастомоза между нижней полой веной (НПВ) и легочной артерией (синонимы: операция Фонтена, нижний кавопульмональный анастомоз) [1, 2, 4, 16, 17, 20-22].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. Выполнение одномоментного тотального кавопульмонального анастомоза сопровождалось высокой летальностью, поэтому было предложено разделить операцию на 2 самостоятельных этапа. Данная тактика позволила существенно улучшить результаты гемодинамической коррекции. Наиболее распространенной в настоящее время модификацией операции Фонтена является использование экстракардиального кондуита (ЭКК) из политетрафторэтилена, имплантированного непосредственно между НПВ и ЛА.
• Рекомендуется соблюдение следующих возрастных критериев при планировании гемодинамической коррекции [25-31]:
• для ДКПА - не менее 4 мес.
• для операции Фонтена - предпочтительно не менее 2-х лет.
Уровень убедительности рекомендаций В (уровень достоверности доказательств - 3).
Комментарии. Ранний возраст на сегодняшний день не является фактором, препятствующим выполнению ДКПА, тем не менее до настоящего времени оптимальные сроки операции не определены. Одни авторы рекомендуют ДКПА до 6 месяцев, объясняя это пользой от ранней «разгрузки» СЖ, но не ранее 3 месяцев [25-28], другие считают оптимальным его создание в промежутке от 6 месяцев до 2 лет, что связывают с максимальным приростом насыщения крови кислородом после процедуры в данной возрастной группе [29, 30]. Сомнения, связанные с выполнением операции до 3 месяцев оправданы и связаны с более высоким ЛСС у таких детей, возможным повышением частоты осложнений и летальности, неуверенностью в адекватном росте легочных артерий после операции и риском неблагоприятного влияния процедуры на мозговое кровообращение [25, 27, 28, 31]. Возраст» выполнения операции Фонтена так же оспаривается. Одни авторы склоняются к выполнению данного этапа в более старшем возрасте, объясняя это ограниченным «сроком службы» нефизиологичного одножелудочкового кровообращения и неизбежной его декомпенсацией [32]. При этом основными показаниями к операции выступают такие факторы, как прогрессирование системной гипоксемии и снижение толерантности к физической нагрузке. Другие же, наоборот, стараются перейти к тотальному кавопульмональному анастомозу в более ранние сроки, объясняя подобную тактику пользой от уже упомянутого раннего снижения преднагрузки СЖ [25, 27].
• Рекомендуется выполнение гемодинамической коррекции пациентам с адекватным развитием легочного артериального русла [33-35]:
• индекс Nakata ≥ 200 мм2/м2;
• индекс McGoon ≥ 1,5.
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 3).
Комментарии: Несмотря на вышеуказанные ориентировочные показатели развития легочного артериального русла считается, что небольшие размеры ЛА (индексы Nakata ≤ 100 мм2/м2 и McGoon ≤ 1,2) не оказывают значимого влияния на ранние результаты гемодинамической коррекции [33]. Как известно, размеры ЛА могут зависеть от количества крови, притекающей к ним [34], поэтому абсолютные их значения, возможно, и не самый важный фактор риска [35]. Очевидно, что более важным фактором может являться функциональная способность ЛА отвечать на увеличение кровотока в легкие после операции, выражающаяся в ЛСС ( см пункт 2,4).
• Рекомендуется выполнение гемодинамической коррекции у пациентов с сопоставимыми размерами полых вен и легочных артерий [1, 2, 20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
• При планировании гемодинамической коррекции у пациентов рекомендуется придерживаться следующих значений показателей гемодинамики малого круга кровообращения [1, 2, 20]:
• среднее давление в легочной артерии:
≤ 20 мм ст для ДКПА;
≤ 15 мм для операции Фонтена;
• легочное сосудистое сопротивление:
≤ 5 Ед/м2 для ДКПА;
≤ 4 Ед/м2 для операции Фонтена.
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
• У пациентов с АВ недостаточностью выраженной и более степени рекомендуется ее коррекция на этапах гемодинамической коррекции [1, 2, 20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. Допустимой и не требующей коррекции степенью АВ недостаточности считается умеренная (1-2).
• Пациентам с субаортальной обструкцией, встречающейся при сопутствующем дискордантном (не от тождественного желудочка) отхождении аорты, рекомендуется устранение обструкции на этапах гемодинамической коррекции [1, 2, 20, 36, 37].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии: показания к коррекции субаортальной обструкции определяются наличием градиента систолического давления между СЖ и аортой, рестриктивного ДМЖП (признак рестриктивности ДМЖП - площадь сечения дефекта менее 2 см2/м2), соотношения диаметров ДМЖП и фиброзного кольца АоКл. Хирургическая тактика заключается либо в расширении ДМЖП, либо в выполнении процедуры Damus-Kaye-Stansel одновременно с гемодинамической коррекцией. После расширения ДМЖП нередко отмечены АВ блокады 3 степени, ввиду чего выполнение операции Damus-Kaye-Stansel, при соблюдении показаний, предпочтительно. Одним из ключевых критериев возможности выполнения операции Damus-Kaye-Stansel является сохранение компетентности клапана ЛА.
• Выполнение гемодинамической коррекции рекомендуется при следующих значениях показателей сократительной функции сердца у пациентов [1, 2, 20, 38, 39]:
• фракция выброса better 55%;
• конечно-диастолическое давления ≤ 12 мм.
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии: Косвенным признаком компрометирования сократительной функции СЖ является индекс его конечно-диастолического объема (мл/м2). В ряде работ отмечена связь исходного увеличения конечно-диастолического объема СЖ и угнетения его сократительной функции в послеоперационном периоде.
• При планировании гемодинамической коррекции у пациентов рекомендуется оценка дополнительных источников легочного кровотока (ДИЛК; синоним: гибридный легочный кровоток) [1, 2, 20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. ДИЛК оценивают в ходе ангиокардиографического исследования при выполнении аортографии. При выполнении ДКПА решение о сохранении или устранении ДИЛК в каждом случае носит индивидуальный характер.
• Рекомендуется сохранение ДИЛК на этапе ДКПА при тенденции к снижению насыщения крови кислородом менее 80% и стабильных показателей центральной гемодинамики (среднее давление в ЛА ≤ 15 мм рт., отсутствие прогрессирующей гипотонии, рефрактерной к увеличению доз кардиотонических препаратов) [1, 2, 20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. Оценка показателей проводится в условиях концентрации кислорода во вдыхаемой смеси в пределах 21-30%. При увеличении насыщения крови кислородом свыше 90% выполняется пробное пережатие дополнительных источников, руководствуясь далее уровнем насыщения крови кислородом (целевое значение 80-90%). При сохраняющейся необходимости сохранения гибридного легочного кровотока предпочтение отдается антеградному источнику (легочный ствол). В ряде ситуаций, в основном по причине устьевых стенозов той или иной ветви ЛА, возможно сохранение одновременно двух источников легочного кровотока - антеградного и системно-легочного анастомоза или ОАП дистальнее места стеноза ЛА.
• Рекомендуется сохранение ДИЛК на этапе ДКПА в случаях, когда предполагается повышенный риск последующего выполнения «полного обхода» правых отделов сердца [1, 15-17, 20-22].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. ДКПА с ДИЛК обеспечивает длительное сохранение относительно стабильного насыщения крови кислородом. При необходимости таким пациентам можно создавать дополнительные ДИЛК в отдаленные сроки после ДКПА (СЛА, аксиллярный артериовенозный анастомоз).
• У ряда пациентов со сложными ВПС и высоким риском операции Фонтена, в силу тех или иных анатомо-гемодинамических факторов, рекомендуется выполнение ДКПА с ДИЛК в качестве «окончательного» этапа гемодинамической коррекции или «моста» к пересадке сердца [2, 16, 17, 20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
• Рекомендуется устранение пациентам ДИЛК (при наличии) перед выполнением операции Фонтена [1, 2, 20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. Сохранение ДИЛК на этапе операции Фонтена нередко приводит к венозной гипертензии и развитию НК.
• Рекомендуется оценка состояния венозного оттока у пациентов. В случае обнаружения препятствий на пути последнего хирургическая тактика определяется индивидуально. Причинами обструкции венозного оттока могут быть [1, 2, 20]:
• Аномальный дренаж легочных вен;
• Стенозы устьев легочных вен;
• Рестриктивный ДМПП.
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
• Рекомендуется устранение факторов, способствующих обструкции венозного оттока на этапе ДКПА [1, 20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
• Выполнение первичного ДКПА рекомендуется у пациентов без критического стеноза легочной артерии и ОАП-зависимого легочного кровотока с уровнем системного насыщения better 70-75%, без избыточного легочного кровотока (среднее давление в легочной артерии worse 20 мм ) [1, 20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
• При значимых локальных стенозах ветвей ЛА пациентам рекомендуется коррекция стенозов эндоваскулярными методами или при помощи открытых операций одномоментно с этапами гемодинамической коррекции [2].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
• Рекомендуется выполнить операцию Фонтена с фенестрацией между ЭКК и предсердием при заключительном этапе гемодинамической коррекции пациентам с пограничными размерами ЛА (индекс Nakata ≤ 200 мм2/м2) и повышенном среднем давлении в ЛА (15-18 мм ) [1, 20-22].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
• В ранние сроки после гемодинамической коррекции (ДКПА или операции Фонтена) рекомендуется проведение тромбопрофилактики [19, 23, 24].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. По современным представлениям тромбоэмболические осложнения (ТЭО) занимают одно из ведущих мест в структуре как ранней, так и отдаленной смертности после гемодинамической коррекции. Особенно настораживающим фактом являются случаи тромбозов на фоне проведения лекарственной тромбопрофилактики. С одной стороны, после операций «обхода» правых отделов сердца создаются условия для замедления кровотока, с другой стороны доказанным фактом является наличие исходного, нередко генетически-обусловленного, дефицита факторов свертывания. Совокупность указанных причин повышает вероятность ТЭО после операции. С целью ранней тромбопрофилактики после гемодинамической коррекции, при отсутствии противопоказаний, внутривенно капельно назначается гепарин натрия**. Схема назначения гепарин натрия** после гемодинамической коррекции аналогична схеме после СЛА ( см пункт 3,2,1).
• Во время тромбопрофилактики гепарином натрия** после гемодинамической коррекции пациентам рекомендуется поддержание АЧТВ в пределах 50-85 сек [19, 23, 24].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
• Рекомендуется контроль уровня тромбоцитов крови пациентам в случае применения гепарина натрия** свыше 5 суток [23, 24].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
• В отдаленные сроки после СЛА пациентам рекомендуется проведение долговременной тромбопрофилактики [23, 24].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. Для целей долговременной тромбопрофилактики, при отсутствии противопоказаний, применяется ацетилсалициловой кислота** в дозе 5 мг/кг/сутки (но не более 100 мг/кг/сутки) или варфарин** в возрастной дозировке. Схема назначения ацетилсалициловой кислоты** - см пункт 3,2,1. В случае назначения варфарина**, препарат так же добавляют к инфузии гепарина натрия**, по мере стабилизации состояния пациента и появления возможности приема пищи. В течение последующих суток подобной комбинированной тромбопрофилактики поддерживается целевое значение АЧТВ 50-85 сек. Со вторых суток от начала приема варфарина** гепарин натрия** отменяют. Далее продолжается тромбопрофилактика изолированно варфарином**, которая назначается на срок не менее 6 мес или до момента следующего этапа хирургического лечения. В соответствии с данными литературы, нет значимой разницы эффективности тромбопрофилактики ацетилсалициловой кислотой** и варфарином**, однако настораживающим моментом является сохранение гиперкоагуляционных состояний, несмотря на проведение тромбопрофилактики. Не исключена целесообразность одновременного приема ацетилсалициловой кислоты** и варфарина** для достижения наиболее оптимального состояние свертывающей системы крови.
• Рекомендуется контроль степени агрегации тромбоцитов у пациентов, принимающих ацетилсалициловую кислоту** с целью долговременной тромбопрофилактики после гемодинамической коррекции [23, 24] ( см пункт 3,2,1).
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
• Рекомендуется поддержание целевого МНО (в пределах 2-3) у пациентов, принимающих варфарин**, с целью долговременной тромбопрофилактики после гемодинамической коррекции [19, 23, 24].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. По данным литературы, случаи ТЭО в средне-отдаленные сроки после гемодинамической коррекции, в большей степени, связаны с нарушением приема и/или несвоевременного контроля дозы варфарина** (МНО), выражающиеся в недостижении целевого МНО.
• Не рекомендуется выполнение операции Фонтена пациентам при склеротических изменениях сосудов легких и выраженной дисфункции СЖ [1, 20-22].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. Объективными критериями состояния сосудов легких являются среднее ДЛА и ЛСС, функции системного желудочка - фракция выброса, конечно-диастолическое давление, индекс конечно-дистолического объема.
• Трансплантация сердца рекомендуется пациентам при тяжелой дисфункции СЖ [1, 16, 17, 20, 40-42].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 3).
3,2,3 Послеоперационные осложнения.
Наиболее частыми ранними осложнениями после гемодинамической коррекции являются неврологические нарушения, дыхательная недостаточность, синдром верхней полой вены, повышенная транссудация [28, 30, 43].• Для снижения риска послеоперационных осложнений рекомендуется ранняя (1-е сутки после операции) экстубация пациентов после гемодинамической коррекции [44-49].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 3).
Комментарии. Основные осложнения нередко связывают с повышением венозного давления в кавопульмональном тракте, что в свою очередь может быть обусловлено колебанием ЛСС в раннем послеоперационном периоде и недостаточной компенсацией легочного кровообращения к увеличению кровотока. Искусственная вентиляция легких повышает внутригрудное давление и замедляет венозный возврат по системным венам, что является дополнительным фактором повышения венозного давления.
Среди отдаленных осложнений после гемодинамической коррекции наиболее важными являются венозная гипертензия, нарушения ритма сердца, белково-дефицитная энтеропатия, печеночная дисфункция, тромбоэмболические осложнения [1, 2].
Венозная гипертензия является основной причиной развития и прогрессирования НК (гепатомегалии, асцита, гидроторакса, периферических отеков, цианоза) в средне-отдаленные сроки после операции Фонтена. К факторам, повышающим вероятность развития венозной гипертензии, относятся стенозы ЛА, ДИЛК, недостаточность АВ клапана, стенозы полых вен или экстракардиального кондуита (например, вследствие «перероста» протеза), развитие венозных коллатералей, дисфункция СЖ, белково-дефицитная энтеропатия (БДЭП), ТЭО, печеночной недостаточности [2].
• Рекомендуется устранение локальных стенозов ЛА в случае их развития у пациентов после тех или иных этапов гемодинамической коррекции [2, 16, 17, 20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. В большинстве случаев их устранение возможно путем стентирования.
• Рекомендуется эндоваскулярное устранение ДИЛК в случае их реканализации или развития после ДКПА или операции Фонтена при стойких признаках НК [2, 16, 17, 20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. Аорто-легочные коллатеральные артерии могут быть не диагностированы до операции или же развиваться в ранние или отдаленные сроки после неё. Реканализация ствола ЛА может происходить спустя 1-2 года после операции (положение справедливо для случаев, где легочный ствол был перевязан интраоперационно, и неактуально для пациентов с сопутствующей АЛА).
• При прогрессировании недостаточности АВ клапана более, чем умеренной степени пациентам рекомендуется проведение корригирующей операции [2, 16, 17, 20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. Коррекция недостаточности АВ клапана может быть выполнена как отдельная процедура, так и одновременно с операцией Фонтена. В ряде случаев это осложнение возникает в отдаленном послеоперационном периоде вследствие перенесенного инфекционного эндокардита или дилатации фиброзного кольца клапана в результате прогрессирующей дисфункции СЖ.
• После операции Фонтена в модификации ЭКК пациентам рекомендуется операция по замене сосудистого протеза в случае развития венозной гипертензии вследствие недостаточного размера кондуита относительно роста и развития пациента [2, 16, 17, 20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
• Для увеличения насыщения крови кислородом в случае развития венозных коллатералей после ДКПА пациентам рекомендуется их эмболизация [1, 2, 16, 17, 20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. При отсутствии таких факторов, как выраженная недостаточность АВ клапанов, остаточные стенозы ЛА и повышенное давление в малом круге кровообращения результаты операции ДКПА хорошие. Однако по мере роста пациента происходит постепенно снижение насыщения артериальной крови кислородом, что обусловлено возрастным уменьшением доли венозного возврата по системе ВПВ, а также развитием легочных артериовенозных фистул. Прогрессирующий цианоз в отдаленные сроки после операции ДКПА может быть связан также с развитием коллатеральных сосудов между системами верхней и нижней полых вен, обусловленным разницей давления между ними, приводящей к сбросу крови из ВПВ в НПВ и уменьшению легочного кровотока. Гемодинамическими причинами этого осложнения могут также быть обструкция легочного кровотока на различных уровнях, повышение ЛСС, дисфункция СЖ или АВ клапанов, тромбоз полых вен и другие факторы, приводящие к повышению венозного давления. По данным A. Magee и соавт. венозные коллатеральные сосуды развиваются в 31% случаев после операции ДКПА. Наиболее часто в роли коллатеральных сосудов выступают непарная и полунепарная вены, а также вены перикарда и передней грудной стенки. Эмболизация венозных коллатералей является эффективным методом повышения насыщения крови кислородом в случаях, когда риск выполнения операции Фонтена повышен.
• Рекомендуется трансплантация сердца пациентам при выраженной дисфункции системного желудочка, рефрактерной к консервативной терапии [2].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. Дисфункция СЖ может быть обусловлена как его морфологией, так и исходной тяжестью порока или перенесенными инфекционными заболеваниями (в тч миокардитом) в послеоперационном периоде [50].
• Пациентам рекомендуется немедленная госпитализация в стационар при подозрении на БДЭП [2, 40, 41, 51].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 3).
Комментарии: Под термином «белок-дефицитная энтеропатия» подразумевается состояние, характеризующееся нарушением всасывания белка в тонком кишечнике. Частота этого осложнения составляет в среднем 3,8%. Сроки развития БДЭП составляют от 1 месяца до 16 лет (в среднем 2,7 года), при этом у одной трети пациентов осложнение развивается в сроки свыше 5 лет после операции. Причины развития БДЭП после операции Фонтена до сих пор изучены не полностью. Одним из вероятных механизмов является развитие лимфангиоэктазий в органах брюшной полости, в том числе и в кишечнике, в результате постоянно повышенного венозного и лимфатического давления после операции Фонтена. Клинически БДЭП проявляется гипоальбуминемией, и как следствие этого, отеками, асцитом, плевральной транссудацией или хилотораксом, иммунодефицитом и гипокальциемией. На поздних стадиях развития, большинство проявлений этого осложнения соответствует клинической картине НК. Методом ранней диагностики этого осложнения, разработанным в последние годы, является определение уровня фекального α1-антитрипсина, концентрация которого при БДЭП существенно повышается. Прогноз при этом осложнении, как правило, неблагоприятный. В большинстве работ отмечается высокая летальность среди этих пациентов. Если в течение 5 лет с момента развития осложнения выживаемость составляет около 60%, то через 10 лет остаются в живых менее 20% пациентов.
• Всем пациентам с АТК после СЛА и гемодинамической коррекции, а также при наличии наджелудочковой аритмии, для профилактики ТЭО в отдаленные сроки, рекомендуется пожизненное применение лекарственной тромбопрофилактики [2, 16, 17, 19, 20, 23, 24, 52].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. Детям наиболее часто назначается ацетилсалициловая кислота** или варфарин** ( см пункт 3,2,1, 3,2,2). Взрослым пациентам возможно назначение новых оральных антикоагулянтов, эффективность которых относительно тромбопрофилактики, в ряде наблюдений, превосходит эффективность ацетилсалициловой кислоты** или варфарина**. Имеются данные о высокой частоте гиперкоагуляции на фоне изолированной тромбопрофилактики ацетилсалициловой кислотой** или варфарином** у детей и указания на необходимость комбинации этих препаратов у пациентов данной возрастной группы для достижения оптимального состояния свертывающей системы крови (в силу невозможности применения новых оральных антикоагулянтов).
3,3 Иное лечение.
3,3,1 Обезболивающая терапия у детей.
• Рекомендуется пациентам для премедикации, с целью седации и обеспечения эмоциональной стабильности перед транспортировкой в операционную, применять опиаты и/или бензодиазепины в возрастных дозировках [53-55].Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. Дети до 6 месяцев в премедикации не нуждаются. Дети от 6 месяцев до 3 лет: мидазолам**или диазепам** в/м, либо в/в в возрастных дозировках.
Дети старше 3 лет: тримепередин** и/или мидазолам**, либо диазепам** в/м, в/в в возрастных дозировках.
• Рекомендуется пациентам для индукции в наркоз и поддержания анестезии использовать: фентанил**, пропофол**, бензодиазепины, натрия оксибутират**, фторсодержащие газовые анестетики в возрастных дозировках. Предпочтительным является проведение комбинированной анестезии с применением галогенсодержащих газовых анестетиков на всех этапах хирургического вмешательства, включая искусственное кровообращение [53-55].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. Препараты, используемые для индукции и поддержании анестезии у детей:
Индукция: Дети до 1 месяца: мидазолам**/натрия оксибутират** и фентанил** в/в в возрастных дозировках. Дети старше 1 месяца: мидазолам**/натрия оксибутират**/пропофол** и фентанил** - в/в в возрастных дозировках. Во всех возрастных группах возможно проведение индукции севофлураном** (как моноиндукции, так и в комбинации с в/в введением фентанила**).
Поддержание анестезии: Дети до 1 месяца: мидазолам**/натрия оксибутират** и фентанил** в/в в возрастных дозировках. Дети старше 1 месяца: мидазолам**/натрия оксибутират**/пропофол** и фентанил** в/в в возрастных дозировках. Во всех возрастных группах возможно применение галогенсодержащих газовых анестетиков в комбинации с фентанилом**. При превышении дозировок (применении дозировок, превышающих указанные в инструкции к препарату) необходимо решение врачебной комиссии.
• Рекомендуется пациентам для обезболивания в раннем послеоперационном периоде использовать опиаты и нестероидные противовоспалительные препараты в возрастных дозировках [53-55].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. Препараты, используемые для обезболивания в послеоперационном периоде:
Первые сутки после операции - тримепередин** в/м каждые 6-8 часов, либо в/в инфузия морфина** в возрастных дозировках, далее НПВП. При сохранении выраженного болевого синдрома тримеперидин**/морфин** в возрастных дозировках по показаниям. При превышении дозировок (применении дозировок, превышающих указанные в инструкции к препарату) необходимо решение врачебной комиссии.
При сохранении выраженного болевого синдрома тримеперидин**/морфин** в возрастных дозировках по показаниям.
3,3,2 Обезболивающая терапия у взрослых.
• Рекомендуется пациентам для премедикации с целью седации и обеспечения эмоциональной стабильности вечером накануне операции с целью уменьшения эмоционального стресса назначить транквилизаторы и нейролептики. Для премедикации перед подачей пациента в операционную с целью седации и обеспечения эмоциональной стабильности применяются опиаты и/или бензодиазепины [53-55].Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. Вечером накануне операции - бензодиазепины (Бромдигидрохлорфенилбензодиазепин**, лоразепам), атипичные нейролептики (тиоридазин**, сульпирид**) в индивидуальных дозировках. Перед подачей в операционную в/м тримепередин** и/или диазепам**/мидазолам**.
• Рекомендуется пациентам для индукции в наркоз использовать. Фентанил**, пропофол**, бензодиазепины, для поддержания анестезии - фентанил**, пропофол**, бензодиазепины, фторсодержащие газовые анестетики. Предпочтение необходимо отдавать проведению комбинированной анестезии с применением галогенсодержащих газовых анестетиков на всех этапах хирургического вмешательства, включая искусственное кровообращение [53-55].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. Препараты, используемые для индукции и поддержания анестезии:
Индукция: мидазолам**/диазепам**/пропофол** и фентанил** в/в в расчетных дозировках.
Поддержание анестезии: мидазолам**/диазепам**/пропофол** и фентанил** - в/в в расчетных дозировках. Возможно применение галогенсодержащих газовых анестетиков в комбинации с фентанилом**. При превышении дозировок (применении дозировок, превышающих указанные в инструкции к препарату) необходимо решение врачебной комиссии.
• Рекомендуется пациентам для обезболивания в раннем послеоперационном периоде использовать опиаты и НПВП в возрастных дозировках [53-55].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. Препараты, используемые для обезболивания в послеоперационном периоде:
Первые сутки после операции - тримепередин**, либо морфин** в/м каждые 4-8 часов, далее НПВП. При наличии специальных дозаторов эффективно применение пациент-контролируемой анальгезии фентанилом**. При сохранении выраженного болевого синдрома тримепередин**/морфин**/фентанил** по показаниям.
|
|
Реабилитация и амбулаторное лечение
• В рамках реабилитационного становления, в сроки до 3-х месяцев после хирургического лечения АТК пациентам рекомендуется ограничение по употреблению жидкости, а также по физической нагрузке [56].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Профилактика
• Рекомендуется пожизненное наблюдение кардиолога с обследованием пациентов после различных этапов коррекции АТК в специализированных центрах не реже 1 раза в 6-12 мес [20, 56].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
• Всем женщинам репродуктивного возраста, перенесшим операцию Фонтена, рекомендуется полное обследование с обязательной ЭхоКГ перед планированием беременности [56].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
• В отдаленные сроки после операции Фонтена возможно развитие печеночной дисфукции, поэтому не реже 1 раза в 6-12 мес.пациентам после операции Фонтена рекомендуется контроль биохимического анализа крови (пункт 2,3) [2, 51].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
• Для оценки сократительной функции сердца, компетентности АВ клапана, характера кровотока по СЛА, ДКПА и/или ЭКК, а также с целью исключения гидроторакса/гидроперикарда после различных этапов коррекции АТК всем пациентам рекомендуется проведение ЭхоКГ в течение первого месяца после выписки, далее - не реже 1 раза в 6-12 мес [20, 56].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
• При недостаточных данных, необходимых для оценки характера показателей кровообращения и полученных в ходе ЭхоКГ, пациентам рекомендуется проведение АКГ с зондированием камер сердца [16, 17, 20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
• Всем пациентам с АТК, получающих лекарственную тромбопрофилактику рекомендуется обследование не реже 1 раза в 6 мес для контроля состояния свертывающей системы крови [19, 23, 24].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. Необходимо начать с объективного обследования и обратить внимание на уровень системной оксигенации, признаки НК, их изменение в динамике. Существует мнение о наличии связи микротромбозов с развитием после операции сердечной недостаточности. Среди лабораторных данных важную информацию могут предоставить оценка уровня гемоглобина, тромбоцитов крови, степени агрегации тромбоцитов (для пациентов, получающих ацетилсалициловую кислоту**), МНО (для пациентов, получающих варфарин**), тромбодинамики 3D.
• Рекомендуется применение антибиотикопрофилактики у пациентов с АТК после различных этапов хирургического лечения, в связи с опасностью инфекционного эндокардита [2, 15-17, 20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. Антибиотикопрофилактика назначается в случае необходимости амбулаторных хирургических вмешательств, экстракции зубов и пр.
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
• Всем женщинам репродуктивного возраста, перенесшим операцию Фонтена, рекомендуется полное обследование с обязательной ЭхоКГ перед планированием беременности [56].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
• В отдаленные сроки после операции Фонтена возможно развитие печеночной дисфукции, поэтому не реже 1 раза в 6-12 мес.пациентам после операции Фонтена рекомендуется контроль биохимического анализа крови (пункт 2,3) [2, 51].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
• Для оценки сократительной функции сердца, компетентности АВ клапана, характера кровотока по СЛА, ДКПА и/или ЭКК, а также с целью исключения гидроторакса/гидроперикарда после различных этапов коррекции АТК всем пациентам рекомендуется проведение ЭхоКГ в течение первого месяца после выписки, далее - не реже 1 раза в 6-12 мес [20, 56].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
• При недостаточных данных, необходимых для оценки характера показателей кровообращения и полученных в ходе ЭхоКГ, пациентам рекомендуется проведение АКГ с зондированием камер сердца [16, 17, 20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
• Всем пациентам с АТК, получающих лекарственную тромбопрофилактику рекомендуется обследование не реже 1 раза в 6 мес для контроля состояния свертывающей системы крови [19, 23, 24].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. Необходимо начать с объективного обследования и обратить внимание на уровень системной оксигенации, признаки НК, их изменение в динамике. Существует мнение о наличии связи микротромбозов с развитием после операции сердечной недостаточности. Среди лабораторных данных важную информацию могут предоставить оценка уровня гемоглобина, тромбоцитов крови, степени агрегации тромбоцитов (для пациентов, получающих ацетилсалициловую кислоту**), МНО (для пациентов, получающих варфарин**), тромбодинамики 3D.
• Рекомендуется применение антибиотикопрофилактики у пациентов с АТК после различных этапов хирургического лечения, в связи с опасностью инфекционного эндокардита [2, 15-17, 20].
Уровень убедительности рекомендаций С (уровень достоверности доказательств - 4).
Комментарии. Антибиотикопрофилактика назначается в случае необходимости амбулаторных хирургических вмешательств, экстракции зубов и пр.
Дополнительно
При подозрении на патологию трахео-бронхиального дерева до операции необходимо обследовать пациента у пульмонолога [57].
• Стабильный функциональный статус пациента и отсутствие признаков нарастания недостаточности кровообращения (для оценки использовать приложение Г);
• Стабильное насыщение крови кислородом.
• Плановое хирургическое лечение.
Показания для экстренной госпитализации:
• Ухудшение функционального статуса пациента с прогрессированием признаков недостаточности кровообращения в течение последних 2-4 недель или дней (для оценки использовать приложение Г);
• Прогрессирование снижения насыщение крови кислородом менее 80% в течение последних 2-4 недель или дней;
• Подозрение на развитие у пациента БДЭП.
Показания к выписке пациента из стационара:
• После консервативного лечения:
• Уменьшение клинических проявлений недостаточности кровообращения;
• Увеличение насыщения крови кислородом.
• После этапного хирургического лечения:
• Системно-легочный анастомоз / процедура Рашкинда - увеличение насыщения крови кислородом / устранение рестриктивного межпредсердного сообщения;
• Этапная гемодинамическая коррекция - снижение преднагрузки (уменьшение конечно-диастолического объема) системного желудочка, увеличение насыщения крови кислородом.
7 Организация медицинской помощи.
Показания для плановой госпитализации:• Стабильный функциональный статус пациента и отсутствие признаков нарастания недостаточности кровообращения (для оценки использовать приложение Г);
• Стабильное насыщение крови кислородом.
• Плановое хирургическое лечение.
Показания для экстренной госпитализации:
• Ухудшение функционального статуса пациента с прогрессированием признаков недостаточности кровообращения в течение последних 2-4 недель или дней (для оценки использовать приложение Г);
• Прогрессирование снижения насыщение крови кислородом менее 80% в течение последних 2-4 недель или дней;
• Подозрение на развитие у пациента БДЭП.
Показания к выписке пациента из стационара:
• После консервативного лечения:
• Уменьшение клинических проявлений недостаточности кровообращения;
• Увеличение насыщения крови кислородом.
• После этапного хирургического лечения:
• Системно-легочный анастомоз / процедура Рашкинда - увеличение насыщения крови кислородом / устранение рестриктивного межпредсердного сообщения;
• Этапная гемодинамическая коррекция - снижение преднагрузки (уменьшение конечно-диастолического объема) системного желудочка, увеличение насыщения крови кислородом.
Критерии оценки качества медицинской помощи
| № | Критерий | Уровень убедительности рекомендаций | Уровень достоверности доказательств |
| Этап диагностики | |||
| 1 | При сборе жалоб и анамнеза оценены наличие и характер цианоза кожных покровов, его изменения в динамике | С | 4 |
| 2 | При сборе жалоб и анамнеза оценены наличие и характер одышки, ее изменения в динамике | С | 4 |
| 3 | При сборе жалоб и анамнеза оценены наличие и характер потливости, ее изменения в динамике | С | 4 |
| 4 | При первичном обследовании пациента выполнена оценка насыщения крови кислородом | С | 4 |
| 5 | При первичном обследовании пациента выполнена оценка частоты и характера дыхания | С | 4 |
| 6 | При первичном обследовании пациента выполнена оценка размеров печени | С | 4 |
| 7 | При первичном обследовании пациента выполнена аускультация легких | С | 4 |
| 8 | При первичном обследовании пациента выполнена аускультация сердца | С | 4 |
| 9 | При первичном обследовании пациента выполнен общий анализ крови | С | 4 |
| 10 | При первичном обследовании пациента выполнено биохимическое исследование крови с оценкой общего белка, альбумина, аланинаминотрансферазы, аспартатаминотрансферазы, билирубина, мочевины, креатинина | С | 4 |
| 11 | При первичном обследовании пациента выполнена электрокардиограмма | С | 4 |
| 12 | При первичном обследовании пациента выполнена эхокардиография с оценкой фракции выброса системного желудочка, а также объемов желудочков | С | 4 |
| 13 | При первичном обследовании пациента выполнена ангиокардиография и зондирование полостей сердца с оценкой давления в камерах сердца, индексов развития легочных артерий | С | 4 |
| 14 | Выполнена консультация пульмонолога у пациентов с подозрением на патологию трахео-бронхиального дерева | С | 4 |
| Этап консервативного лечения | |||
| 1 | Назначены простагландины группы Е у новорожденных с резко обедненным легочным кровотоком | С | 4 |
| 2 | Назначены диуретики и ингибиторы ангиотензин-превращающего фермента у пациентов с проявлениями недостаточности кровообращения | С | 4 |
| Этап хирургического лечения (паллиативные операции) | |||
| 1 | Выполнена процедура Рашкинда у новорожденных с рестриктивным межпредсердным сообщением | С | 4 |
| 2 | Выполнена операция Muller) и перевязка открытого артериального протока у новорожденных с резко увеличенным легочным кровотоком | С | 4 |
| 3 | Создан системно-легочный анастомоз у новорожденных (до 3 мес) с системным насыщением менее 70-75% и отсутствием противопоказаний к системно-легочному анастомозу | С | 4 |
| Этап хирургического лечения (гемодинамическая коррекция) | |||
| 1 | Гемодинамическая коррекция выполнена в 2 этапа | С | 4 |
| 2 | Соблюдены критерии отбора пациентов при выполнении двунаправленного кавопульмонального анастомоза | С | 4 |
| 3 | Двунаправленный кавопульмональный анастомоз выполнен в возрасте от 4 мес до 1 года | С | 4 |
| 4 | Выполнено устранение факторов, способствующих обструкции венозного оттока, на этапе ДКПА | С | 4 |
| 5 | Соблюдены критерии отбора пациентов при выполнении операции Фонтена | В | 3 |
| 6 | Операция Фонтена выполнена в возрасте старше 2 лет | В | 3 |
| 7 | Выполнена операция Фонтена с фенестрацией при пограничных размерах и повышенном давлении в легочной артерии | С | 4 |
| 8 | Выполнена коррекция значимых локальных стенозов ветвей легочной артерии в пределах различных этапов гемодинамической коррекции | С | 4 |
| Этап послеоперационного наблюдения | |||
| 1 | Выполнена ранняя (1-е сутки) экстубация пациента после гемодинамической коррекции (при условии отсутствия противопоказаний к экстубации) | С | 3 |
| 2 | С целью ранней тромбопрофилактики через 12-24 часа после системно-легочного анастомоза и гемодинамической коррекции назначено внутривенное капельное введение гепарин натрия (при отсутствии противопоказаний, условии стабильного хирургического гемостаза и значениях активированного частичного тромбопластинового времени, международного нормализованного отношения, в пределах референтных значений) | С | 4 |
| 3 | Во время ранней тромбопрофилактики гепарин натрием после системно-легочного анастомоза и гемодинамической коррекции достигнуто стабильное целевое значение активированного частичного тромбопластинового времени в пределах 50-85 сек. | С | 4 |
| 4 | Выполнен контроль уровня тромбоцитов крови в случае применения гепарин натрия более 5 суток | С | 4 |
| 5 | С целью долговременной тромбопрофилактики после системно-легочного анастомоза, при отсутствии противопоказаний, назначена ацетилсалициловая кислота | С | 4 |
| 6 | С целью долговременной тромбопрофилактики после гемодинамической коррекции, при отсутствии противопоказаний, назначена ацетилсалициловая кислота или варфарин | С | 4 |
| 7 | Через 2-5 суток после назначения АСК для целей долговременной тромбопрофилактики оценена степень агрегации тромбоцитов | С | 4 |
| 8 | Достигнуто стабильное целевое международное нормализованное соотношение (МНО) в пределах 2-3 у пациентов, принимающих варфарин | С | 4 |
| 9 | Осмотр кардиолога выполнен не реже 1 раза в 12 мес. | С | 4 |
| 10 | Выполнена эхокардиография в течение первого месяца после системно-легочного анастомоза или гемодинамической коррекции, далее - не реже 1 раза в 12 мес. | С | 4 |
| 11 | Устранены стенозы легочных артерий при их развитии после двунаправленного кавопульмонального анастомоза или операции Фонтена | С | 4 |
| 12 | Контроль биохимического анализа крови с оценкой общего белка, альбумина, аланинаминотрансферазы, аспартатаминотрансферазы, билирубина, мочевины, креатинина выполнен не менее 1 раза в течение 12 мес после операции Фонтена | С | 4 |
|
|
Список литературы
• Kouchoukos N.T., вlackstone E.H., Hanley F.L., Kirklin J.K. Kirklin/Barratt-Boyes cardiac surgery: morphology, diagnostic criteria, natural history, techniques, results, and indications. 4th ed. Philadelphia: Elsevier; 2013.
• Бокерия Л.А., Зеленикин М.М., Свободов А.А. Пороки с одножелудочковой гемодинамикой. Операции обхода правого сердца. В кн. Бокерия Л.А., Шаталов В. (ред. Детская кардиохирургия. Руководство для врачей. ФГБУ «НЦССХ им. А.Н. Бакулева» МЗ РФ, 2016: 663-683.
• Van Praagh R., Ando M., Dungan W.T. Anatomic types of tricuspid atresia: clinical and development implications. сirculation 1971; 43 and 44: II-115.
• Бураковский В.И., Бухарин В.А., Подзолков В.П., Фальковский Г.Э., Алекси-Месхишвили В.В. Атрезия трехстворчатого клапана. В кн. Бураковский В. И., Бокерия Л. А. (ред. Сердечно-сосудистая хирургия: руководство. М. Медицина; 1996: 251-258.
• вaumgartner H., вonhoeffer P., De Groot N.M., de Haan F., Deanfield J.E., Galie N., Gatzoulis M.A., Gohlke-Baerwolf с., Kaemmerer H., Kilner P., Meijboom F., Mulder в.J., Oechslin E., Oliver J.M., Serraf A., Szatmari A., Thaulow E., Vouhe P.R., Walma E. Task Force on the Management of Grown-up сongenital Heart Disease of the European Society of сardiology (ESC); Association for European Paediatric сardiology (AEPC); ESC сommittee for Practice Guidelines (CPG). ESC Guidelines for the management of grown-up congenital heart disease (new version 2010). Eur. Heart J. 2010; 31 (23): 2915-57. DOI: 10,1093/eurheartj/ehq249.
• Anderson R.H., Wilkins J.L., Gerlis L.M., Smith A., вecker A.E. Atresia of the right atrioventricular orifice. вr. Heart J. 1977; 39: 414. DOI: 10,1136/hrt.39,4,414.
• Scalia D., Russo P., Anderson R.H., Macartney F.J., Hegerty A.S., Ho S.Y., Daliento L., Thiene G. The surgical anatomy of hearts with no direct communication between the right atrium and the ventricular mass - so-called tricuspid atresia. J. Thorac. сardiovasc. Surg. 1984; 87: 743.
• Anderson R.H., Rigby M.L. The morphologic heterogeneity of «tricuspid atresia» (editorial). Int. J. сardiol. 1987; 16: 67. DOI: 10,1016/0167-5273(87)90271-3.
• Rao P.S., Jue K.L., Isabel-Jones J., Ruttenberg H.D. Ebstein’s malformation of the tricuspid valve with atresia. Differentiation from isolated tricuspid atresia. Am. J. сardiol. 1973; 32: 1004. DOI: 10,1016/s0002-9149(73)80173-0.
• Weinberg Anatomy of tricuspid atresia and its relevance to current forms of surgical therapy. Ann. Thorac. Surg. 1980; 29: 306. DOI: 10,1016/s0003-4975(10)61476-2.
• Ottenkamp J., Wenink A.C. Anomalies of the mitral valve and of the left ventricular architecture in tricuspid valve atresia. Am. J. сardiol. 1989; 63: 880. DOI: 10,1016/0002-9149(89)90065-9.
• Annecchino F.P., Fontan F., сhauve A., Quaegebeur J. Palliative reconstruction of the right ventricular outflow tract in tricuspid atresia: a report of 5 patients. Ann. Thorac. Surg. 1980; 29: 317. DOI: 10,1016/s0003-4975(10)61478-6.
• Sittiwangkul R., Azakie A., Van Arsdell G.S., Williams W.G., McCrindle в.W. Outcomes of tricuspid atresia in the Fontan era. Ann. Thorac. Surg. 2004; 77: 889-94. DOI: 10,1016/j.athoracsur.2003,09,027.
• Forrest P., вini R.M., Wilkinson J.L., Arnold R., Wright J.G., McKay R., Hamilton D.I., вargeron L.M. Jr, Pacifico A.D. сongenital absence of the pulmonic valve and tricuspid valve atresia with intact ventricular septum. Am. J. сardiol. 1987; 59: 482. DOI: 10,1016/0002-9149(87)90963-5.
• Шарыкин А.С. Врожденные пороки сердца. Руководство для педиатров, кардиологов, неонатологов. М. Теремок; 2005.
• Клинические рекомендации по ведению взрослых пациентов с врожденными пороками сердца. М. НЦССХ им. А. Н. Бакулева РАМН; 2010.
• Бокерия Л.А. (ред. Клинические рекомендации по ведению детей с врожденными пороками сердца. М. НЦССХ им. А.Н. Бакулева; 2014.
• Ross R.D. The Ross classification for heart failure in children after 25 years: a review and an age-stratified revision. Pediatr. сardiol. 2012; 33 (8): 1295-300. DOI: 10,1007/s00246-012-0306-8.
• Гущин Д., Купряшов А.А., Зеленикин М.М. Оценка эффективности традиционной тромбопрофилактики у пациентов после унивентрикулярной коррекции методом «Тромбодинамика». Новости сердечно-сосудистой хирургии 2018; 1: 16-23.
• Подзолков В.П., Чиаурели М.Р., Зеленикин М.М., Юрлов И.А. Хирургическое лечение врожденных пороков сердца методом гемодинамической коррекции. М. НЦССХ им. А.Н. Бакулева РАМН; 2007.
• Davies R.R., Pizarro с. Decision-making for surgery in the management of patients with univentricular heart. Front. Pediatr. 2015; 3,61. DOI: 10,3389/fped.2015,00061.
• Van Doorn с.A., Tsang V.T., De Leval M.R. Tricuspid atresia and the functionally single ventricle. In: Yuh D.D., Vricella L.A., Yang S.C., Doty J.R. (eds. Johns Hopkins textbook of cardiothoracic surgery, second edition. McGraw-Hill Education; 2014: 1183-1192.
• Monagle P., сhan A.K.C., Goldenberg N.A., Ichord R.N., Journeycake J.M., Nowak-Göttl U., Vesely S.K. Antithrombotic therapy in neonates and children: Antithrombotic Therapy and Prevention of Thrombosis, 9th ed: American сollege of сhest Physicians Evidence-Based сlinical Practice Guidelines. сhest 2012; 141 (2 Suppl): e737S-e801S. DOI: 10,1378/chest.11-2308.
• Dabbous M.K., Sakr F.R., Malaeb D.N. Anticoagulant therapy in pediatrics. J. вasic. сlin. Pharm. 2014; 5 (2): 27-33. DOI: 10,4103/0976-0105,134947.
• сleuziou J., Schreiber с., сornelsen J.K., Horer J., Eicken A., Lange R. вidirectional cavopulmonary connection without additional pulmonary blood flow in patients below the age of 6 months. Eur. J. сardiothorac. Surg. 2008; 34: 556-562. DOI: 10,1016/j.ejcts.2008,05,041.
• Alsoufi в., Manlhiot с., Awan A., Alfadley F., Al-Ahmadi M., Al-Wadei A., McCrindle в.W., Al-Halees Z. сurrent outcomes of the Glenn bidirectional cavopulmonary connection for single ventricle palliation. Eur. J. сardiothorac. Surg. 2012; 42: 42-49. DOI: 10,1093/ejcts/ezr280.
• Friedman K.G., Salvin J.W., Wypij D., Gurmu Y., вacha E.A., вrown D.W., Laussen P.C., Scheurer M.A. Risk factors for failed staged palliation after bidirectional Glenn in infants who have undergone stage one palliation. Eur. J. сardiothorac. Surg. 2011; 40: 1000-1006. DOI: 10,1016/j.ejcts.2011,01,056.
• Gérelli S., вoulitrop с., Van Steenberghe M., Maldonado D., вojana M., Raisky O., Sidi D., Vouhé P.R. вidirectional cavopulmonary shunt with additional pulmonary blood flow: a failed or successful strategy. Eur. J. сardiothorac. Surg. 2012; 42: 513-519. DOI: 10,1093/ejcts/ezs053.
• Tanoue Y., Kado H., вoku N., Tatewaki H., Nakano T., Fukae K., Masuda M., Tominaga R. Three hundred and thirty-three experiences with the bidirectional Glenn procedure in a single institute. Interact. сardioVasc. Thorac. Surg. 2007; 9: 97-101. DOI: 10,1510/icvts.2006,138560.
• сalvaruso D.F., Rubino A., Ocello S., Salviato N., Guardì D., Petruccelli D.F., сipriani A., Fattouch K., Agati S., Mignosa с., Zannini L., Marcelletti с.F. вidirectional Glenn and antegrade pulmonary blood flow: temporary or definitive Palliation. Ann. Thorac. Surg. 2008; 85: 1389-96. DOI: 10,1016/j.athoracsur.2008,01,013.
• Petrucci O., Khoury P.R., Manning P.B., Eghtesady P. Outcomes of the bidirectional Glenn procedure in patients less than 3 months of age. J. Thorac. сadiovasc. Surg. 2010; 139: 562-568. DOI: 10,1016/j.jtcvs.2009,08,025.
• d’Udekem Y., Xu M.Y., Konstantinov I.E. The optimal age at Fontan procedure and the ‘ticking clock’ theory: do we have an answer. Eur. J. сardiothorac. Surg. 2011; 39: 144. DOI: 10,1016/j.ejcts.2010,04,006.
• Lehner A., Schuh A., Herrmann F.E., Riester M., Pallivathukal S., Dalla-Pozza R., Kozlik-Feldmann R., Netz H., Malec E., Januszewska K. Influence of pulmonary artery size on early outcome after the Fontan operation. Ann. Thorac. Surg. 2014; 97 (4): 1387-93. DOI: 10,1016/j.athoracsur.2013,11,068.
• Kansy A., вrzezińska-Rajszys G., Zubrzycka M., Mirkowicz-Małek M., Maruszewski P., Manowska M., Maruszewski в. Pulmonary artery growth in univentricular physiology patients. Kardiol. Pol. 2013; 71 (6): 581-7. DOI: 10,5603/KP.2013,0121.
• Adachi I., Yagihara T., Kagisaki K., Hagino I., Ishizaka T., Kobayashi J., Kitamura S., Uemura H. Preoperative small pulmonary artery did not affect the midterm results of Fontan operation. Eur. J. сardiothorac. Surg. 2007; 32: 156-162. DOI: 10,1016/j.ejcts.2007,03,024.
• Shimada M., Hoashi T., Kagisaki K., Shiraishi I., Yagihara T., Ichikawa H. сlinical outcomes of prophylactic Damus-Kaye-Stansel anastomosis concomitant with bidirectional Glenn procedure. J. Thorac. сardiovasc. Surg. 2012; 143 (1): 137-143. DOI: 10,1016/j.jtcvs.2011,09,009.
• Iwai S., Kawata H., Ozawa H., Yamauchi S., Kishimoto H. Use of the Damus-Kaye-Stansel procedure prevents increased ventricular strain in Fontan candidates. Eur. J. сardiothorac. Surg. 2013; 43 (1): 150-155. DOI: 10,1093/ejcts/ezs142.
• вellsham-Revell H.R., Tibby S.M., вell A.J., Witter T., Simpson J., вeerbaum P., Anderson D., Austin с.B., Greil G.F., Razavi R. Serial magnetic resonance imaging in hypoplastic left heart syndrome gives valuable insight into ventricular and vascular adaptation. J. Am. сoll. сardiol. 2013; 61 (5): 561-70. DOI: 10,1016/j.jacc.2012,11,016.
• Gushchin D.K., Zelenikin M.M., Volkov S.S., Zelenikin M.A. Early results and risk factors of bidirectional cavopulmonary anastomosis in children. In: The 26th Annual Meeting of the Asian Society for сardiovascular and Thoracic Surgery conference proceedings 2018: 220.
• Mertens L., Hagler D.J., Sauer U., Somerville J., Gewillig M. Protein-losing enteropathy after the Fontan operation: an international multicenter study. PLE study group. J. Thorac. сardiovasc. Surg. 1998; 115: 1063-73. DOI: 10,1016/s0022-5223(98)70406-4.
• Freedom R.M., Li J., Yoo S.J. Late complications following the Fontan operation. In: Gatzoulis M.A., Webb G.D., Daubeney P.E. (eds). Diagnosis and Management of Adult сongenital Heart Disease; London: сhurchill Livingston; 2003: 85-91.
• Gamba A., Merlo M., Fiocchi R., Terzi A., Mammana с., Sebastiani R., Ferrazzi P. Heart transplantation in patients with previous Fontan operations. J. Thorac. сardiovasc. Surg. 2004; 127: 555-62. DOI: 10,1016/j.jtcvs.2003,08,016.
• вerdat P.A., вelli E., Lacour-Gayet F., Planché с., Serraf A. Additional pulmonary blood flow has no adverse effect on outcome after bidirectional cavopulmonary anastomosis. Ann. Thorac. Surg. 2005; 79: 29-36. DOI: 10,1016/j.athoracsur.2004,06,002.
• Deshpande S.R., Kirshbom , Maher K.O. Negative pressure ventilation as a therapy for post-operative complications in a patient with single ventricle physiology. Heart Lung сirc. 2011; 20: 763-5. DOI: 10,1016/j.hlc.2011,03,010.
• Mutsuga M., Quiñonez L.G., Mackie A.S., Norris с.M., Marchak в.E., Rutledge J.M., Rebeyka I.M., Ross D.B. Fast-track extubation after modified Fontan procedure. J. Thorac. сardiovasc. Surg. 2012; 144: 547-52. DOI: 10,1016/j.jtcvs.2012,05,047.
• Lofland GK. The enhancement of hemodynamic performance in Fontan circulation using pain free spontaneous ventilation. Eur. J. сardiothorac. Surg. 2001; 20: 114-8; discussion 118-9. DOI: 10,1016/s1010-7940(01)00757-6.
• Türköz A., вalcı S.T., Gönen H., Çınar Ö., Özker E., Türköz R. The effects of different ventilator modes on cerebral tissue oxygen saturation in patients with bidirectional superior cavopulmonary connection. Ann. сard. Anaesth. 2014; 17: 10-5. DOI: 10,4103/0971-9784,124122.
• Harris K.C., Holowachuk S., Pitfield S., Sanatani S., Froese N., Potts J.E., Gandhi S.K. Should early extubation be the goal for children after congenital cardiac surgery. J. Thorac. сardiovasc. Surg. 2014; 148: 2642-7. DOI: 10,1016/j.jtcvs.2014,06,093.
• Гущин Д., Зеленикин М.М., Зеленикин М.А. Двунаправленный кавопульмональный анастомоз у детей раннего возраста: непосредственные результаты и факторы риска. Бюллетень НЦССХ им. А.Н. Бакулева РАМН. Сердечно-сосудистые заболевания 2018; 19 (5): 713-730. DOI: 10,24022/1810-0694-2018-19-5-713-730.
• Piran S., Veldtman G., Siu S., Webb G.D., Liu P.P. Heart failure and ventricular dysfunction in patients with single or systemic right ventricles. сirculation 2002; 105 (10): 1189-94. DOI: 10,1161/hc1002,105182.
• Путято Н.А., Шведунова В.Н., Астраханцева Т.О., Самсонов В.Б., Подзолков В.П. Проблемы отдаленного периода после операции Фонтена. Вестник Российской Академии медицинских наук 2009; 1: 33-36.
• Georgekutty J., Kazerouninia A., Wang Y., Ermis P.R., Parekh D.R., Franklin W.J., Lam W.W. Novel oral anticoagulant use in adult Fontan patients: A single center experience. сongenit. Heart Dis. 2018; 13 (4): 541-547. DOI: 10,1111/chd.12603.
• Рыбка М.М., Хинчагов Д.Я., Мумладзе В., Лобачева Г.В., Ведерникова Л.В. Под ред. Л.А. Бокерия. Протоколы анестезиологического обеспечения кардиохирургических операций, выполняемых у новорожденных и детей. Методические рекомендации. М. НЦССХ им. А.Н. Бакулева РАМН; 2014.
• Рыбка М.М., Хинчагов Д.Я. Под ред. Л.А. Бокерия. Протоколы анестезиологического обеспечения кардиохирургических операций, выполняемых при ишемической болезни сердца, патологии клапанного аппарата, нарушениях ритма, гипертрофической кардиомиопатии, аневризмах восходящего отдела аорты у пациентов различных возрастных групп. Методические рекомендации. М. НЦССХ им. А.Н. Бакулева РАМН; 2015.
• Рыбка М.М., Хинчагов Д.Я., Мумладзе В., Никулкина Е.С. Под ред. Л.А. Бокерия. Протоколы анестезиологического обеспечения рентгенэндоваскулярных и диагностических процедур, выполняемых у кардиохирургических пациентов различных возрастных групп. Методические рекомендации. М. НЦССХ им. А.Н. Бакулева РАМН; 2018.
• Подзолков В.П., Кассирский Г.И. (ред. Реабилитация больных после хирургического лечения врожденных пороков сердца. М. НЦССХ им. А.Н. Бакулева; 2015.
• Kurland G., Deterding R.R., Hagood J.S., Young L.R., вrody A.S., сastile R.G., Dell S., Fan L.L., Hamvas A., Hilman в.C., Langston с., Nogee L.M., Redding G.J. American Thoracic Society сommittee on сhildhood Interstitial Lung Disease (chILD) and the chILD Research Network. An official American Thoracic Society clinical practice guideline: classification, evaluation, and management of childhood interstitial lung disease in infancy. Am. J. Respir. сrit. сare. Med. 2013; 188 (3): 376-94. DOI: 10,1164/rccm.201305-0923ST.
• Фальковский Г.Э., Крупянко С.М. Сердце ребенка: книга для родителей о врожденных пороках сердца. М. Никея, 2011.
• Бокерия Л.А., Зеленикин М.М., Свободов А.А. Пороки с одножелудочковой гемодинамикой. Операции обхода правого сердца. В кн. Бокерия Л.А., Шаталов В. (ред. Детская кардиохирургия. Руководство для врачей. ФГБУ «НЦССХ им. А.Н. Бакулева» МЗ РФ, 2016: 663-683.
• Van Praagh R., Ando M., Dungan W.T. Anatomic types of tricuspid atresia: clinical and development implications. сirculation 1971; 43 and 44: II-115.
• Бураковский В.И., Бухарин В.А., Подзолков В.П., Фальковский Г.Э., Алекси-Месхишвили В.В. Атрезия трехстворчатого клапана. В кн. Бураковский В. И., Бокерия Л. А. (ред. Сердечно-сосудистая хирургия: руководство. М. Медицина; 1996: 251-258.
• вaumgartner H., вonhoeffer P., De Groot N.M., de Haan F., Deanfield J.E., Galie N., Gatzoulis M.A., Gohlke-Baerwolf с., Kaemmerer H., Kilner P., Meijboom F., Mulder в.J., Oechslin E., Oliver J.M., Serraf A., Szatmari A., Thaulow E., Vouhe P.R., Walma E. Task Force on the Management of Grown-up сongenital Heart Disease of the European Society of сardiology (ESC); Association for European Paediatric сardiology (AEPC); ESC сommittee for Practice Guidelines (CPG). ESC Guidelines for the management of grown-up congenital heart disease (new version 2010). Eur. Heart J. 2010; 31 (23): 2915-57. DOI: 10,1093/eurheartj/ehq249.
• Anderson R.H., Wilkins J.L., Gerlis L.M., Smith A., вecker A.E. Atresia of the right atrioventricular orifice. вr. Heart J. 1977; 39: 414. DOI: 10,1136/hrt.39,4,414.
• Scalia D., Russo P., Anderson R.H., Macartney F.J., Hegerty A.S., Ho S.Y., Daliento L., Thiene G. The surgical anatomy of hearts with no direct communication between the right atrium and the ventricular mass - so-called tricuspid atresia. J. Thorac. сardiovasc. Surg. 1984; 87: 743.
• Anderson R.H., Rigby M.L. The morphologic heterogeneity of «tricuspid atresia» (editorial). Int. J. сardiol. 1987; 16: 67. DOI: 10,1016/0167-5273(87)90271-3.
• Rao P.S., Jue K.L., Isabel-Jones J., Ruttenberg H.D. Ebstein’s malformation of the tricuspid valve with atresia. Differentiation from isolated tricuspid atresia. Am. J. сardiol. 1973; 32: 1004. DOI: 10,1016/s0002-9149(73)80173-0.
• Weinberg Anatomy of tricuspid atresia and its relevance to current forms of surgical therapy. Ann. Thorac. Surg. 1980; 29: 306. DOI: 10,1016/s0003-4975(10)61476-2.
• Ottenkamp J., Wenink A.C. Anomalies of the mitral valve and of the left ventricular architecture in tricuspid valve atresia. Am. J. сardiol. 1989; 63: 880. DOI: 10,1016/0002-9149(89)90065-9.
• Annecchino F.P., Fontan F., сhauve A., Quaegebeur J. Palliative reconstruction of the right ventricular outflow tract in tricuspid atresia: a report of 5 patients. Ann. Thorac. Surg. 1980; 29: 317. DOI: 10,1016/s0003-4975(10)61478-6.
• Sittiwangkul R., Azakie A., Van Arsdell G.S., Williams W.G., McCrindle в.W. Outcomes of tricuspid atresia in the Fontan era. Ann. Thorac. Surg. 2004; 77: 889-94. DOI: 10,1016/j.athoracsur.2003,09,027.
• Forrest P., вini R.M., Wilkinson J.L., Arnold R., Wright J.G., McKay R., Hamilton D.I., вargeron L.M. Jr, Pacifico A.D. сongenital absence of the pulmonic valve and tricuspid valve atresia with intact ventricular septum. Am. J. сardiol. 1987; 59: 482. DOI: 10,1016/0002-9149(87)90963-5.
• Шарыкин А.С. Врожденные пороки сердца. Руководство для педиатров, кардиологов, неонатологов. М. Теремок; 2005.
• Клинические рекомендации по ведению взрослых пациентов с врожденными пороками сердца. М. НЦССХ им. А. Н. Бакулева РАМН; 2010.
• Бокерия Л.А. (ред. Клинические рекомендации по ведению детей с врожденными пороками сердца. М. НЦССХ им. А.Н. Бакулева; 2014.
• Ross R.D. The Ross classification for heart failure in children after 25 years: a review and an age-stratified revision. Pediatr. сardiol. 2012; 33 (8): 1295-300. DOI: 10,1007/s00246-012-0306-8.
• Гущин Д., Купряшов А.А., Зеленикин М.М. Оценка эффективности традиционной тромбопрофилактики у пациентов после унивентрикулярной коррекции методом «Тромбодинамика». Новости сердечно-сосудистой хирургии 2018; 1: 16-23.
• Подзолков В.П., Чиаурели М.Р., Зеленикин М.М., Юрлов И.А. Хирургическое лечение врожденных пороков сердца методом гемодинамической коррекции. М. НЦССХ им. А.Н. Бакулева РАМН; 2007.
• Davies R.R., Pizarro с. Decision-making for surgery in the management of patients with univentricular heart. Front. Pediatr. 2015; 3,61. DOI: 10,3389/fped.2015,00061.
• Van Doorn с.A., Tsang V.T., De Leval M.R. Tricuspid atresia and the functionally single ventricle. In: Yuh D.D., Vricella L.A., Yang S.C., Doty J.R. (eds. Johns Hopkins textbook of cardiothoracic surgery, second edition. McGraw-Hill Education; 2014: 1183-1192.
• Monagle P., сhan A.K.C., Goldenberg N.A., Ichord R.N., Journeycake J.M., Nowak-Göttl U., Vesely S.K. Antithrombotic therapy in neonates and children: Antithrombotic Therapy and Prevention of Thrombosis, 9th ed: American сollege of сhest Physicians Evidence-Based сlinical Practice Guidelines. сhest 2012; 141 (2 Suppl): e737S-e801S. DOI: 10,1378/chest.11-2308.
• Dabbous M.K., Sakr F.R., Malaeb D.N. Anticoagulant therapy in pediatrics. J. вasic. сlin. Pharm. 2014; 5 (2): 27-33. DOI: 10,4103/0976-0105,134947.
• сleuziou J., Schreiber с., сornelsen J.K., Horer J., Eicken A., Lange R. вidirectional cavopulmonary connection without additional pulmonary blood flow in patients below the age of 6 months. Eur. J. сardiothorac. Surg. 2008; 34: 556-562. DOI: 10,1016/j.ejcts.2008,05,041.
• Alsoufi в., Manlhiot с., Awan A., Alfadley F., Al-Ahmadi M., Al-Wadei A., McCrindle в.W., Al-Halees Z. сurrent outcomes of the Glenn bidirectional cavopulmonary connection for single ventricle palliation. Eur. J. сardiothorac. Surg. 2012; 42: 42-49. DOI: 10,1093/ejcts/ezr280.
• Friedman K.G., Salvin J.W., Wypij D., Gurmu Y., вacha E.A., вrown D.W., Laussen P.C., Scheurer M.A. Risk factors for failed staged palliation after bidirectional Glenn in infants who have undergone stage one palliation. Eur. J. сardiothorac. Surg. 2011; 40: 1000-1006. DOI: 10,1016/j.ejcts.2011,01,056.
• Gérelli S., вoulitrop с., Van Steenberghe M., Maldonado D., вojana M., Raisky O., Sidi D., Vouhé P.R. вidirectional cavopulmonary shunt with additional pulmonary blood flow: a failed or successful strategy. Eur. J. сardiothorac. Surg. 2012; 42: 513-519. DOI: 10,1093/ejcts/ezs053.
• Tanoue Y., Kado H., вoku N., Tatewaki H., Nakano T., Fukae K., Masuda M., Tominaga R. Three hundred and thirty-three experiences with the bidirectional Glenn procedure in a single institute. Interact. сardioVasc. Thorac. Surg. 2007; 9: 97-101. DOI: 10,1510/icvts.2006,138560.
• сalvaruso D.F., Rubino A., Ocello S., Salviato N., Guardì D., Petruccelli D.F., сipriani A., Fattouch K., Agati S., Mignosa с., Zannini L., Marcelletti с.F. вidirectional Glenn and antegrade pulmonary blood flow: temporary or definitive Palliation. Ann. Thorac. Surg. 2008; 85: 1389-96. DOI: 10,1016/j.athoracsur.2008,01,013.
• Petrucci O., Khoury P.R., Manning P.B., Eghtesady P. Outcomes of the bidirectional Glenn procedure in patients less than 3 months of age. J. Thorac. сadiovasc. Surg. 2010; 139: 562-568. DOI: 10,1016/j.jtcvs.2009,08,025.
• d’Udekem Y., Xu M.Y., Konstantinov I.E. The optimal age at Fontan procedure and the ‘ticking clock’ theory: do we have an answer. Eur. J. сardiothorac. Surg. 2011; 39: 144. DOI: 10,1016/j.ejcts.2010,04,006.
• Lehner A., Schuh A., Herrmann F.E., Riester M., Pallivathukal S., Dalla-Pozza R., Kozlik-Feldmann R., Netz H., Malec E., Januszewska K. Influence of pulmonary artery size on early outcome after the Fontan operation. Ann. Thorac. Surg. 2014; 97 (4): 1387-93. DOI: 10,1016/j.athoracsur.2013,11,068.
• Kansy A., вrzezińska-Rajszys G., Zubrzycka M., Mirkowicz-Małek M., Maruszewski P., Manowska M., Maruszewski в. Pulmonary artery growth in univentricular physiology patients. Kardiol. Pol. 2013; 71 (6): 581-7. DOI: 10,5603/KP.2013,0121.
• Adachi I., Yagihara T., Kagisaki K., Hagino I., Ishizaka T., Kobayashi J., Kitamura S., Uemura H. Preoperative small pulmonary artery did not affect the midterm results of Fontan operation. Eur. J. сardiothorac. Surg. 2007; 32: 156-162. DOI: 10,1016/j.ejcts.2007,03,024.
• Shimada M., Hoashi T., Kagisaki K., Shiraishi I., Yagihara T., Ichikawa H. сlinical outcomes of prophylactic Damus-Kaye-Stansel anastomosis concomitant with bidirectional Glenn procedure. J. Thorac. сardiovasc. Surg. 2012; 143 (1): 137-143. DOI: 10,1016/j.jtcvs.2011,09,009.
• Iwai S., Kawata H., Ozawa H., Yamauchi S., Kishimoto H. Use of the Damus-Kaye-Stansel procedure prevents increased ventricular strain in Fontan candidates. Eur. J. сardiothorac. Surg. 2013; 43 (1): 150-155. DOI: 10,1093/ejcts/ezs142.
• вellsham-Revell H.R., Tibby S.M., вell A.J., Witter T., Simpson J., вeerbaum P., Anderson D., Austin с.B., Greil G.F., Razavi R. Serial magnetic resonance imaging in hypoplastic left heart syndrome gives valuable insight into ventricular and vascular adaptation. J. Am. сoll. сardiol. 2013; 61 (5): 561-70. DOI: 10,1016/j.jacc.2012,11,016.
• Gushchin D.K., Zelenikin M.M., Volkov S.S., Zelenikin M.A. Early results and risk factors of bidirectional cavopulmonary anastomosis in children. In: The 26th Annual Meeting of the Asian Society for сardiovascular and Thoracic Surgery conference proceedings 2018: 220.
• Mertens L., Hagler D.J., Sauer U., Somerville J., Gewillig M. Protein-losing enteropathy after the Fontan operation: an international multicenter study. PLE study group. J. Thorac. сardiovasc. Surg. 1998; 115: 1063-73. DOI: 10,1016/s0022-5223(98)70406-4.
• Freedom R.M., Li J., Yoo S.J. Late complications following the Fontan operation. In: Gatzoulis M.A., Webb G.D., Daubeney P.E. (eds). Diagnosis and Management of Adult сongenital Heart Disease; London: сhurchill Livingston; 2003: 85-91.
• Gamba A., Merlo M., Fiocchi R., Terzi A., Mammana с., Sebastiani R., Ferrazzi P. Heart transplantation in patients with previous Fontan operations. J. Thorac. сardiovasc. Surg. 2004; 127: 555-62. DOI: 10,1016/j.jtcvs.2003,08,016.
• вerdat P.A., вelli E., Lacour-Gayet F., Planché с., Serraf A. Additional pulmonary blood flow has no adverse effect on outcome after bidirectional cavopulmonary anastomosis. Ann. Thorac. Surg. 2005; 79: 29-36. DOI: 10,1016/j.athoracsur.2004,06,002.
• Deshpande S.R., Kirshbom , Maher K.O. Negative pressure ventilation as a therapy for post-operative complications in a patient with single ventricle physiology. Heart Lung сirc. 2011; 20: 763-5. DOI: 10,1016/j.hlc.2011,03,010.
• Mutsuga M., Quiñonez L.G., Mackie A.S., Norris с.M., Marchak в.E., Rutledge J.M., Rebeyka I.M., Ross D.B. Fast-track extubation after modified Fontan procedure. J. Thorac. сardiovasc. Surg. 2012; 144: 547-52. DOI: 10,1016/j.jtcvs.2012,05,047.
• Lofland GK. The enhancement of hemodynamic performance in Fontan circulation using pain free spontaneous ventilation. Eur. J. сardiothorac. Surg. 2001; 20: 114-8; discussion 118-9. DOI: 10,1016/s1010-7940(01)00757-6.
• Türköz A., вalcı S.T., Gönen H., Çınar Ö., Özker E., Türköz R. The effects of different ventilator modes on cerebral tissue oxygen saturation in patients with bidirectional superior cavopulmonary connection. Ann. сard. Anaesth. 2014; 17: 10-5. DOI: 10,4103/0971-9784,124122.
• Harris K.C., Holowachuk S., Pitfield S., Sanatani S., Froese N., Potts J.E., Gandhi S.K. Should early extubation be the goal for children after congenital cardiac surgery. J. Thorac. сardiovasc. Surg. 2014; 148: 2642-7. DOI: 10,1016/j.jtcvs.2014,06,093.
• Гущин Д., Зеленикин М.М., Зеленикин М.А. Двунаправленный кавопульмональный анастомоз у детей раннего возраста: непосредственные результаты и факторы риска. Бюллетень НЦССХ им. А.Н. Бакулева РАМН. Сердечно-сосудистые заболевания 2018; 19 (5): 713-730. DOI: 10,24022/1810-0694-2018-19-5-713-730.
• Piran S., Veldtman G., Siu S., Webb G.D., Liu P.P. Heart failure and ventricular dysfunction in patients with single or systemic right ventricles. сirculation 2002; 105 (10): 1189-94. DOI: 10,1161/hc1002,105182.
• Путято Н.А., Шведунова В.Н., Астраханцева Т.О., Самсонов В.Б., Подзолков В.П. Проблемы отдаленного периода после операции Фонтена. Вестник Российской Академии медицинских наук 2009; 1: 33-36.
• Georgekutty J., Kazerouninia A., Wang Y., Ermis P.R., Parekh D.R., Franklin W.J., Lam W.W. Novel oral anticoagulant use in adult Fontan patients: A single center experience. сongenit. Heart Dis. 2018; 13 (4): 541-547. DOI: 10,1111/chd.12603.
• Рыбка М.М., Хинчагов Д.Я., Мумладзе В., Лобачева Г.В., Ведерникова Л.В. Под ред. Л.А. Бокерия. Протоколы анестезиологического обеспечения кардиохирургических операций, выполняемых у новорожденных и детей. Методические рекомендации. М. НЦССХ им. А.Н. Бакулева РАМН; 2014.
• Рыбка М.М., Хинчагов Д.Я. Под ред. Л.А. Бокерия. Протоколы анестезиологического обеспечения кардиохирургических операций, выполняемых при ишемической болезни сердца, патологии клапанного аппарата, нарушениях ритма, гипертрофической кардиомиопатии, аневризмах восходящего отдела аорты у пациентов различных возрастных групп. Методические рекомендации. М. НЦССХ им. А.Н. Бакулева РАМН; 2015.
• Рыбка М.М., Хинчагов Д.Я., Мумладзе В., Никулкина Е.С. Под ред. Л.А. Бокерия. Протоколы анестезиологического обеспечения рентгенэндоваскулярных и диагностических процедур, выполняемых у кардиохирургических пациентов различных возрастных групп. Методические рекомендации. М. НЦССХ им. А.Н. Бакулева РАМН; 2018.
• Подзолков В.П., Кассирский Г.И. (ред. Реабилитация больных после хирургического лечения врожденных пороков сердца. М. НЦССХ им. А.Н. Бакулева; 2015.
• Kurland G., Deterding R.R., Hagood J.S., Young L.R., вrody A.S., сastile R.G., Dell S., Fan L.L., Hamvas A., Hilman в.C., Langston с., Nogee L.M., Redding G.J. American Thoracic Society сommittee on сhildhood Interstitial Lung Disease (chILD) and the chILD Research Network. An official American Thoracic Society clinical practice guideline: classification, evaluation, and management of childhood interstitial lung disease in infancy. Am. J. Respir. сrit. сare. Med. 2013; 188 (3): 376-94. DOI: 10,1164/rccm.201305-0923ST.
• Фальковский Г.Э., Крупянко С.М. Сердце ребенка: книга для родителей о врожденных пороках сердца. М. Никея, 2011.
|
|
Приложения
Приложение А1.
Состав рабочей группы.• Арнаутова И.В. д.м.н.
• Гущин Д. н.с.
• Горбачевский С.В. д.м.н., профессор.
• Зеленикин М.А. д.м.н., профессор; Ассоциация сердечно-сосудистых хирургов России.
• Зеленикин М.М. д.м.н., профессор; Ассоциация сердечно-сосудистых хирургов России.
• Ким А.И. д.м.н., профессор.
• Кокшенев И.В. д.м.н., професор.
• Купряшов А.А. д.м.н.
• Подзолков В.П. академик РАН.
• Сабиров Б.Н. д.м.н.
• Свободов А.А. д.м.н.
• Шаталов В. д.м.н., профессор.
• Шмальц А.А. д.м.н.
• Юрлов И.А. м.н.
Все члены Рабочей группы подтвердили отсутствие финансовой поддержки/конфликта интересов.
Приложение А2.
Методология разработки клинических рекомендаций.Целевая аудитория данных клинических рекомендаций:
• врач - детский кардиолог;
• врач - кардиолог;
• врач общей практики (семейный врач);
• врач - педиатр;
• врач - педиатр городской (районный);
• врач - педиатр участковый;
• врач по лечебной физкультуре;
• врач по медицинской реабилитации;
• врач по спортивной медицине;
• врач приемного отделения;
• врач - сердечно-сосудистый хирург;
• врач скорой медицинской помощи;
• врач - терапевт;
• врач - терапевт подростковый;
• врач - терапевт участковый.
Таблица П1. Уровни убедительности рекомендаций.
| Уровень убедительности | Основание рекомендации |
| А | Основан на клинических исследованиях хорошего качества, по своей тематике непосредственно применимых к данной специфической рекомендации включающих по меньшей мере одно рандомизированное контролируемое исследование (РКИ) |
| В | Основан на клинических исследованиях хорошего дизайна, но без рандомизации |
| С | Составлен при отсутствии клинических исследований хорошего качества, непосредственно применимых к данной рекомендации |
Таблица П2. Уровни достоверности доказательств.
| Уровень достоверности | Тип данных |
| 1а | Метаанализ РКИ |
| 1б | Хотя бы одно РКИ |
| 2a | Хотя бы одно хорошо выполненное РКИ |
| 2б | Хотя бы одно хорошо выполненное квазиэкспериментальное исследование |
| 3 | Хорошо выполненные неэкспериментальные исследования: сравнительные, корреляционные или «случай-контроль» |
| 4 | Экспертное консенсусное мнение либо клинический опыт признанного авторитета |
Порядок обновления клинических рекомендаций.
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию - не реже чем один раз в три года или при появлении новой информации о тактике ведения пациентов с данным заболеванием. Решение об обновлении принимает МЗ РФ на основе предложений, представленных медицинскими некоммерческими профессиональными организациями. Сформированные предложения должны учитывать результаты комплексной оценки лекарственных препаратов, медицинских изделий, а также результаты клинической апробации.
Приложение А3.
Связанные документы.Нет.
Приложение В.
Информация для пациентов.Термин «атрезия» означает полное отсутствие нормального сообщения между сердечными камерами или между ними и отходящими от них магистральными сосудами (аортой и лёгочным стволом).
В нормально развитом сердце ТК соединяет правое предсердие с правым желудочком. При атрезии этот клапан не развит и на его месте имеется плотная мембрана, через которую поток крови пройти не может. Поскольку при АТК кровь не поступает в ПЖ, то последний резко недоразвит, что имеет место уже внутриутробно. Однако, и плод, и новорожденный какое-то время могут с этим жить, так как кровь смешивается посредством имеющегося ДМПП. То есть: из полых вен, как и в норме, кровь поступает в правое предсердие. Далее единственным возможным оказывается путь крови через ДМПП в левое предсердие. Далее, через нормально развитый митральный клапан, кровь поступает в левый желудочек и затем часть крови идет в аорту, а часть - через ДМЖП в ПЖ и из него - в легочную артерию и легкие. Далее, по легочным венам, кровь из легких возвращается в левые отделы сердца и попадает в левый желудочек. Тут она смешивается с венозной кровью, поступающей посредством ДМПП из полых вен. Путь дальнейшего «распределения» крови зависит от того, куда легче идти основному ее потоку: в аорту или (через ДМЖП) в легочную артерию и легкие. В большинстве случаев больший объем крови проходит в аорту и меньший - в легкие. Нормально развитый левый желудочек обеспечивает кровообращение как малого (легкие), так и большого (прочие органы и ткани) кругов. Так как в левом желудочке смешиваются потоки венозной (обедненной кислородом) крови из полых вен и артериальной (насыщенной кислородом) из легких, то значительная часть крови остается недонасыщенной кислородом. Органы и ткани (в тч кожные покровы) получают такую кровь, что выражается в ее цианозе (синюшность).
Качество и продолжительность жизни детей с АТК зависит от величины кровотока в легких и размерами ДМЖП и ДМПП. Со временем, по мере роста ребенка, положение ухудшается, нарастает цианоз и около 90% детей не доживут до года, если им не оказать хирургическую помощь. Оставшиеся 10% имеют достаточно большой дефект в перегородке и легочный кровоток у них нормальный, а в ряде случаев - усиленный. Они чувствует себя относительно неплохо, почти не синюшны и могут прожить более 10-15 лет, но, учитывая значительную нагрузку на левый желудочек, обеспечивающим в одиночку потребности организма, постепенно будут развиваться признаки сердечной недостаточности (одышка, отеки, увеличение печени) и нарастать цианоз.
Каковы методы помощй Следует понять, что если у ребенка изначально не было одного из четырех клапанов и правый желудочек в значительной степени недоразвит, то исправить это нельзя. Поэтому процесс хирургического лечения носит так называемый «паллиативный» характер, то есть направлен на облегчение состояния путем этапного улучшения кровообращения с уменьшением выраженности цианоза, что улучшает качество жизни таких пациентов. Детям с выраженным цианозом в течение первых месяцев жизни выполняется так называемый «системно-легочный анастомоз», соединение крупной артерии организма (наиболее часто подключичной артерии) с легочной артерией. В результате этой операции в легочную артерию поступает дополнительный объем насыщенной кислородом крови. После операции уменьшается выраженность цианоза, дети начинают развиваться и вести себя соответственно возрасту. Но это - только первый этап хирургического лечения. Если не выполнять последующих этапов, то по мере роста ребенка будут нарастать проявления цианоза, так как ранее созданный системно-легочный анастомоз будет не в состоянии обеспечить возрастающие потребности организма в кислороде. В последующем, между первым и вторым годами жизни, выполняется следующий этап - так называемый «двунаправленный кавопульмональный анастомоз», заключающийся в соединении верхней полой вены напрямую с легочной артерией. После операции кровь от верхней половины тела идет в легочную артерию, сразу в оба легких (от сюда и название - двунаправленный). Цели данного этапа: 1) так как кровь от верхней половины тела поступает в легкие, минуя сердце, то осуществляется «разгрузка» левого желудочка, что предохраняет его от возможного развития сердечной недостаточности в будущем; 2) одновременно происходит увеличение легочного кровотока и повышение насыщения крови кислородом, уменьшается цианоз. Вышесказанное способствует еще в большей степени улучшению качества жизни и функционального состояния ребенка. ДКПА можно выполнить не только в возрасте 1-2 лет. В ряде ситуаций эта операция выпоняется первично (без предшествующего системно-легочного анастомоза) в возрасте до года (но не ранее 4 мес.), что определяется кардиологом и кардиохирургом, постоянно наблюдающих ребенка.
Следующим этапом соединяют нижнюю полую вену, несущую кровь от нижней половины тела в сердце, с легочной артерией, при этом используется синтетический сосудистый протез. Данный этап называется «операция Фонтена в модификации экстракардиального кондуита». Обычно данная операция выполняется в возрасте старше 2-х лет. Таким образом, теперь вся венозная кровь от всего организма идет в легкие, а насыщенная кислородом в полном объеме - в левые отделы. И если ранее потоки венозной и артериальной крови смешивались, что обуславливало ту или иную степень цианоза, то теперь эти потоки разделены. Ребенок розовеет.
Но, напомним, что описанный принцип хирургического лечения не излечивает порок, он облегчает состояние пациента путем оптимизации кровообращения в условиях резкого недоразвития правого желудочка. После операции такие пациенты живут и развиваются, их состояние в большинстве случаев соответствует I-II функциональному классу, то есть почти как здоровые дети или имеющие минимальные ограничения по функциональному состоянию [58].
После выписки из специализированного центра необходимо строго соблюдать предписания, указанные в выписных документах (выписной эпикриз). Наблюдение у кардиолога по месту жительства - не реже 1 раза в 6 мес, строго соблюдая его предписания и назначения. Наблюдение кардиолога в специализированном центре - не реже 1 раза в 12 мес. При любых инвазивных манипуляциях (стоматологические, косметологические, прочие процедуры, предполагающие или несущие риск нарушения целостности кожных покровов и слизистых) обязательно проводить антибактериальное прикрытие для профилактики возникновения инфекционного эндокардита. Случаи предполагаемых инвазивных манипуляций обязательно согласуются с кардиологом, ведущим наблюдение за пациентом по месту жительства. Изменение доз и схем тех или иных лекарственных препаратов, а также назначение дополнительных или альтернативных лекарственных препаратов осуществляет только лечащий врач. При возникновении побочных эффектов от приема лекарственных препаратов необходимо в максимально быстрые сроки обсудить это с лечащим врачом. Следует избегать чрезмерных физических нагрузок. При возникновении или резком прогрессировании следующих симптомов в максимально короткие сроки необходима внеочередная консультация кардиолога: утомляемость, одышка, цианоз, отеки, увеличение объема живота, аритмии, потери сознания, неврологический дефицит (потеря зрения, слуха, речи, онемение конечности, парезы и параличи, в тч кратковременные), острые респираторные заболевания, лихорадка неясного генеза.
Приложение Г.
Модифицированная шкала оценки выраженности недостаточности кровообращения и функционального состояния пациента по Ross R.D.
Потливость в анамнезе:□ 0 баллов: нет/только голова.
□ 1 балл: голова и тело при нагрузке.
□ 2 балла: голова голова и тело в покое.
Тахипноэ в анамнезе:
□ 0 баллов: редко.
□ 1 балл: периодически.
□ 2 балла: часто.
Объективное обследование.
Дыхание:
□ 0 баллов: физиологическое.
□ 1 балл: втяжение межреберных промежутков.
□ 2 балла: одышка.
Частота дыхания в 1 мин в покое:
0-1 год.
□ 0 баллов: worse 50.
□ 1 балл: 50-60.
□ 2 балла: >60.
1-6 лет.
□ 0 баллов: <35.
□ 1 балл: 35-40.
□ 2 балла: >45.
7-10 лет.
□ 0 баллов: <25.
□ 1 балл: 25-35.
□ 2 балла: >35.
11-14 лет.
□ 0 баллов: <18.
□ 1 балл: 18-28.
□ 2 балла: >28.
Частота сердечных сокращений в 1 мин:
0-1 год.
□ 0 баллов: <160.
□ 1 балл: 160-170.
□ 2 балла: >170.
1-6 лет.
□ 0 баллов: <105.
□ 1 балл: 105-115.
□ 2 балла: >115.
7-10 лет.
□ 0 баллов: <90.
□ 1 балл: 90-100.
□ 2 балла: >100.
11-14 лет.
□ 0 баллов: <80.
□ 1 бал: 80-90.
□ 2 балла: >90.
Гепатомегалия, см:
□ 0 баллов: <2.
□ 1 балл: 2-3.
□ 2 балла: >3.
Оценка:
Сумма баллов ____.
□ 0-2 балла: НК 0 (I ФК).
□ 3-6 баллов: умеренная НК (II ФК).
□ 7-9 баллов: выраженная НК (III ФК).
□ 10-12 баллов: тяжелая НК (IV ФК).
|
|
Год актуализации информации
2018.