
МКБ-10 коды
|
|
Вступление
Кодирование по Международной статистической классификации болезней и проблем, связанных со здоровьем: Q20.4.
Год утверждения (частота пересмотра): 2022.
Возрастная категория: Взрослые , Дети.
Пересмотр не позднее: 2024.
ID: 44.
Разработчик клинической рекомендации.
• Ассоциация сердечно-сосудистых хирургов России.
Одобрено Научно-практическим Советом Минздрава РФ.
Год утверждения (частота пересмотра): 2022.
Возрастная категория: Взрослые , Дети.
Пересмотр не позднее: 2024.
ID: 44.
Разработчик клинической рекомендации.
• Ассоциация сердечно-сосудистых хирургов России.
Одобрено Научно-практическим Советом Минздрава РФ.
|
|
 Список сокращений
Список сокращений
АВ - атриовентрикулярный.
АКГ - ангиокардиография (чрезвенозная катетеризация сердца, зондирование камер сердца).
Ао - аорта.
АЧТВ - активированное частичное тромбопластиновое время.
БВО - бульбо-вентрикулярное отверстие.
БДЭП - белково-дефицитная энтеропатия.
ВПВ - верхняя полая вена.
ВПС - врожденный порок сердца.
ДИЛК - дополнительный источник легочного кровотока.
ДКПА - двунаправленный кавопульмональный анастомоз.
ДМЖП - дефект межжелудочковой перегородки.
ЕЖ - единственный желудочек.
ЛА - легочная артерия.
ЛСС - легочное сосудистое сопротивление.
ЛЖ - левый желудочек.
МНО - международное нормализованное отношение.
МПС - межпредсердное сообщение.
НК - недостаточность кровообращения.
НПВ - нижняя полая вена.
НПВП - нестероидные противовоспалительные препараты.
ОАП - открытый артериальный проток.
ПЖ - правый желудочек.
РКИ - рандомизированное контролируемое исследование.
СЖ - системный желудочек.
СЛА - системно-легочный анастомоз.
СН - сердечная недостаточность.
ТМА - транспозиция магистральных артерий.
ТЭО - тромбоэмболические осложнения.
ЭКГ - электрокардиография.
ЭКК - экстракардиальный кондуит (протез кровеносных сосудов синтетический).
ЭхоКГ - эхокардиография.
АКГ - ангиокардиография (чрезвенозная катетеризация сердца, зондирование камер сердца).
Ао - аорта.
АЧТВ - активированное частичное тромбопластиновое время.
БВО - бульбо-вентрикулярное отверстие.
БДЭП - белково-дефицитная энтеропатия.
ВПВ - верхняя полая вена.
ВПС - врожденный порок сердца.
ДИЛК - дополнительный источник легочного кровотока.
ДКПА - двунаправленный кавопульмональный анастомоз.
ДМЖП - дефект межжелудочковой перегородки.
ЕЖ - единственный желудочек.
ЛА - легочная артерия.
ЛСС - легочное сосудистое сопротивление.
ЛЖ - левый желудочек.
МНО - международное нормализованное отношение.
МПС - межпредсердное сообщение.
НК - недостаточность кровообращения.
НПВ - нижняя полая вена.
НПВП - нестероидные противовоспалительные препараты.
ОАП - открытый артериальный проток.
ПЖ - правый желудочек.
РКИ - рандомизированное контролируемое исследование.
СЖ - системный желудочек.
СЛА - системно-легочный анастомоз.
СН - сердечная недостаточность.
ТМА - транспозиция магистральных артерий.
ТЭО - тромбоэмболические осложнения.
ЭКГ - электрокардиография.
ЭКК - экстракардиальный кондуит (протез кровеносных сосудов синтетический).
ЭхоКГ - эхокардиография.
Термины и определения
Индекс Nakata (синоним. Легочно-артериальный индекс) - отношение суммарной площади поперечного сечения правой и левой легочных артерий к площади поверхности тела.
Индекс McGoon. Отношение суммы диаметров легочных артерий у места их деления к диаметру нисходящей аорты.
«Критические» врожденные пороки сердца. Состояния, характеризующиеся острым дефицитом сердечного выброса, быстрым прогрессированием сердечной недостаточности, кислородным голоданием тканей с развитием декомпенсированного метаболического ацидоза и нарушением функции жизненно важных органов [1].
Процедура Рашкинда (синоним. Баллонная атриосептостомия) - эндоваскулярная операция, заключающаяся в проведении катетера с расширительным баллоном в овальное окно межпредсердной перегородки и последующей дилатации межпредсердного сообщения.
Рестриктивный. Создающий препятствие кровотоку.
Транссудация. Состояние, характеризующееся длительным поступлением жидкости из серозный полостей.
Индекс McGoon. Отношение суммы диаметров легочных артерий у места их деления к диаметру нисходящей аорты.
«Критические» врожденные пороки сердца. Состояния, характеризующиеся острым дефицитом сердечного выброса, быстрым прогрессированием сердечной недостаточности, кислородным голоданием тканей с развитием декомпенсированного метаболического ацидоза и нарушением функции жизненно важных органов [1].
Процедура Рашкинда (синоним. Баллонная атриосептостомия) - эндоваскулярная операция, заключающаяся в проведении катетера с расширительным баллоном в овальное окно межпредсердной перегородки и последующей дилатации межпредсердного сообщения.
Рестриктивный. Создающий препятствие кровотоку.
Транссудация. Состояние, характеризующееся длительным поступлением жидкости из серозный полостей.
Описание
Единственный желудочек сердца (ЕЖ) - врожденный порок сердца (ВПС), характеризующийся нарушением предсердно-желудочковой связи, когда полости предсердий через митральный и трехстворчатый клапаны соединяются лишь с одним, хорошо развитым доминирующим желудочком. При этом кровообращение в малом и большом кругах осуществляется параллельно, а не последовательно, как в норме [1-3].
Причины
Предрасполагающими факторами формирования ЕЖ, как и прочих ВПС, являются следующие: 1) хромосомные нарушения - 5%; 2) мутация одного гена - 2-3%; 3) факторы среды (алкоголизм родителей, краснуха, лекарственные препараты ) - 1-2%; 4) полигенно-мультифакториальное наследование - 90%.
Считалось, что указанные причины приводят к агенезии межжелудочковой перегородки, с которой связывали возникновение ЕЖ. Однако исследования, проведенные R. Van Praagh [4], показали, что данный механизм не является универсальным, так как представляет лишь один из вариантов возникновения ЕЖ, а с точки зрения эмбриологического развития и анатомии этот порок чаще возникает тогда, когда происходит задержка развития одного или обоих желудочков сердца. Для понимания механизмов развития различных анатомических вариантов ЕЖ следует вспомнить некоторые аспекты нормального эмбриогенеза сердца. В ранней стадии развития сердца оба предсердия сообщаются с первичным желудочком, который в свою очередь сообщается с артериальным бульбусом, дающим начало артериальному стволу. Из первичного желудочка образуется левый желудочек (ЛЖ), из синусной части артериального бульбуса - приточный и основной отделы правого желудочка (ПЖ), а из конусной части - выходные тракты обоих желудочков. Следовательно, задержка развития синусной части артериального бульбуса приведет к отсутствию ПЖ, а единственная желудочковая камера приобретает строение левого желудочка. В таких случаях от ПЖ остается только выходная (инфундибулярная) камера - «выпускник», от которого, как правило, отходит тот сосуд, который должен отходить от ПЖ: при нормальном расположении магистральных сосудов - легочная артерия (ЛА), а при транспозиции магистральных артерий (ТМА) - аорта (Ао). При задержке развития первичного желудочка единственная желудочковая камера имеет строение ПЖ, а магистральные сосуды независимо от типа их взаимоотношения отходят от выходной камеры. При задержке развития первичного желудочка, синусной части артериального бульбуса и агенезии межжелудочковой перегородки единственная желудочковая полость аналогична по своему внутреннему строению выходному отделу ПЖ [1].
Особенности гемодинамических нарушений при ЕЖ определяются смешиванием потоков оксигенированной крови из легочных вен (насыщение кислородом - 95-100%) и неоксигенированной крови из системных вен (насыщение кислородом - 55-60%) в одной камере, что приводит к той или иной степени артериальной гипоксемии. При равном легочном и системном кровотоке результирующая оксигенация составит 75-80%. При возрастании легочного кровотока возрастает и системное насыщение. В свою очередь, объем кровотока через малый и большой круги кровообращения (при отсутствии анатомических сужений) определяется относительной резистентностью соответствующих сосудов. При постоянно интенсивном легочном кровотоке быстро развивается объемная перегрузка ЕЖ, обеспечивающего как системное, так и легочное кровообращение. В результате развивается застойная сердечная недостаточность (СН), желудочек теряет способность изгонять кровь против высокого системного сопротивления, и все бо́льшая часть крови рециркулирует через легочные сосуды. Длительное существование усиленного легочного кровотока приводит к изменениям в легочных сосудах вплоть до склеротических и повышению легочного сосудистого сопротивления (легочная гипертензия). В случае сопутствующего стеноза ЛА наблюдается снижение соотношения легочного и системного кровотока ниже 1,0, что приводит к значительному снижению системного насыщения, однако СН менее выражена.
При отхождении аорты от рудиментарной желудочковой камеры на пути кровотока из системного желудочка в аорту имеется так называемое бульбовентрикулярное отверстие, представляющее собой по сути дефект межжелудочковой перегородки (ДМЖП). Со временем происходит нарастание обструкции на уровне БВО (субаортальный стеноз), что затрудняет системный кровоток. В ряде наблюдений имеются одновременно препятствия на пути и системного и легочного кровотока.
В поддержании адекватной гемодинамики как малого, так и большого кругов кровообращения важную роль может играть открытый артериальный проток (дуктус-зависимые состояния) [3].
Считалось, что указанные причины приводят к агенезии межжелудочковой перегородки, с которой связывали возникновение ЕЖ. Однако исследования, проведенные R. Van Praagh [4], показали, что данный механизм не является универсальным, так как представляет лишь один из вариантов возникновения ЕЖ, а с точки зрения эмбриологического развития и анатомии этот порок чаще возникает тогда, когда происходит задержка развития одного или обоих желудочков сердца. Для понимания механизмов развития различных анатомических вариантов ЕЖ следует вспомнить некоторые аспекты нормального эмбриогенеза сердца. В ранней стадии развития сердца оба предсердия сообщаются с первичным желудочком, который в свою очередь сообщается с артериальным бульбусом, дающим начало артериальному стволу. Из первичного желудочка образуется левый желудочек (ЛЖ), из синусной части артериального бульбуса - приточный и основной отделы правого желудочка (ПЖ), а из конусной части - выходные тракты обоих желудочков. Следовательно, задержка развития синусной части артериального бульбуса приведет к отсутствию ПЖ, а единственная желудочковая камера приобретает строение левого желудочка. В таких случаях от ПЖ остается только выходная (инфундибулярная) камера - «выпускник», от которого, как правило, отходит тот сосуд, который должен отходить от ПЖ: при нормальном расположении магистральных сосудов - легочная артерия (ЛА), а при транспозиции магистральных артерий (ТМА) - аорта (Ао). При задержке развития первичного желудочка единственная желудочковая камера имеет строение ПЖ, а магистральные сосуды независимо от типа их взаимоотношения отходят от выходной камеры. При задержке развития первичного желудочка, синусной части артериального бульбуса и агенезии межжелудочковой перегородки единственная желудочковая полость аналогична по своему внутреннему строению выходному отделу ПЖ [1].
Особенности гемодинамических нарушений при ЕЖ определяются смешиванием потоков оксигенированной крови из легочных вен (насыщение кислородом - 95-100%) и неоксигенированной крови из системных вен (насыщение кислородом - 55-60%) в одной камере, что приводит к той или иной степени артериальной гипоксемии. При равном легочном и системном кровотоке результирующая оксигенация составит 75-80%. При возрастании легочного кровотока возрастает и системное насыщение. В свою очередь, объем кровотока через малый и большой круги кровообращения (при отсутствии анатомических сужений) определяется относительной резистентностью соответствующих сосудов. При постоянно интенсивном легочном кровотоке быстро развивается объемная перегрузка ЕЖ, обеспечивающего как системное, так и легочное кровообращение. В результате развивается застойная сердечная недостаточность (СН), желудочек теряет способность изгонять кровь против высокого системного сопротивления, и все бо́льшая часть крови рециркулирует через легочные сосуды. Длительное существование усиленного легочного кровотока приводит к изменениям в легочных сосудах вплоть до склеротических и повышению легочного сосудистого сопротивления (легочная гипертензия). В случае сопутствующего стеноза ЛА наблюдается снижение соотношения легочного и системного кровотока ниже 1,0, что приводит к значительному снижению системного насыщения, однако СН менее выражена.
При отхождении аорты от рудиментарной желудочковой камеры на пути кровотока из системного желудочка в аорту имеется так называемое бульбовентрикулярное отверстие, представляющее собой по сути дефект межжелудочковой перегородки (ДМЖП). Со временем происходит нарастание обструкции на уровне БВО (субаортальный стеноз), что затрудняет системный кровоток. В ряде наблюдений имеются одновременно препятствия на пути и системного и легочного кровотока.
В поддержании адекватной гемодинамики как малого, так и большого кругов кровообращения важную роль может играть открытый артериальный проток (дуктус-зависимые состояния) [3].
|
|
Эпидемиология
Частота ЕЖ составляет около 0,13/1000 новорожденных, среди всех ВПС - 2,5%, среди «критических» ВПС - 5,5%, в течение первого года жизни без лечения смертность составляет 75% [1, 5]. Наиболее частый вариант - двуприточный ЛЖ с ТМА [1].
Прогноз естественного течения ЕЖ неблагоприятный: без операции на первом году жизни умирают 55-67%, а к 10 годам - до 90% детей [2].
Q20,4 - Удвоение входного отверстия желудочка (Общий желудочек. Трехкамерное сердце. Единственный желудочек).
Прогноз естественного течения ЕЖ неблагоприятный: без операции на первом году жизни умирают 55-67%, а к 10 годам - до 90% детей [2].
1,4 Особенности кодирования заболевания или состояния (группы заболеваний или состояний) по Международной статистической классификации болезней и проблем, связанных со здоровьем.
В соответствии с Международной классификацией болезней 10-го пересмотра -Врожденные аномалии (пороки развития) сердечных камер и соединений (Q20):Q20,4 - Удвоение входного отверстия желудочка (Общий желудочек. Трехкамерное сердце. Единственный желудочек).
Классификация
1,5 Классификация заболевания или состояния (группы заболеваний или состояний).
ЕЖ характеризуют при помощи классификации Van Praagh и соавт. (1964), за основу которой принято анатомическое строение желудочковой камеры и расположение магистральных сосудов [4] либо системы, предложенной R.H. Anderson и соавт. (1975) и характеризующей последовательность расположения камер сердца [6]. Согласно мнению Van Praagh, внутренняя архитектоника ЕЖ может иметь строение:• левого желудочка;
• правого желудочка;
• левого и правого желудочков;
• выходного отдела правого желудочка, или неопределенное строение.
В один или общий желудочек открываются трехстворчатый и митральный клапаны, или общий атриовентрикулярный клапан.
При каждом анатомическом варианте расположение магистральных сосудов может быть:
• нормальным (I тип);
• аорта может быть расположена справа по отношению к легочному стволу (II тип);
• аорта может быть расположена слева по отношению к легочному стволу (III тип);
• обратное нормальному положение магистральных сосудов (IV тип).
Указанные варианты могут встречаться в условиях нормального, обратного и неопределенного расположения внутренних органов. Недостатком классификации Van Praagh является исключение из нее атрезии митрального и трехстворчатого клапанов. Система R.H. Anderson аналогично подчеркивает характер соединений предсердий и желудочков, утверждая, что объединяющим критерием одножелудочкового сердца является то, что соединение предсердий происходит только с одним желудочком, тогда как второй желудочек, если он присутствует, будет резко недоразвит [6, 7]. При этом факт отсутствия одного атрио-вентрикулярного соединения позволяет рассматривать сердце с атрезией трехстворчатого клапана как одножелудочковое [6, 7].
По данным Базы данных ВПС и Европейской Ассоциации Кардиоторакальной хирургии ЕЖ включает [5]:
• двуприточный левый желудочек;
• двуприточный правый желудочек;
• сердце с отсутствием одного атриовентрикулярного соединения (атрезия митрального клапана, атрезия трехстворчатого клапана);
• сердце с общим атриовентрикулярным клапаном и только одним полностью развитым желудочком (несбалансированный общий атриовентрикулярный канал);
• сердце только с одним полностью развитым желудочком и синдромом гетеротаксии;
• другие редкие формы одножелудочковых сердец, которые не входят в одну из указанных категорий.
Клиническая картина
Клиническая симптоматика определяется объемной перегрузкой сердца и легочной гипертензией у пациентов без сопутствующего стеноза ЛА и выраженной гипоксемией - у пациентов со стенозом ЛА.
В случае обедненного легочного кровотока с момента рождения или вскоре после него развивается цианоз. Насыщение крови кислородом составляет 70-80%. Цианоз усиливается при нагрузке (движение, плач, кормление), в том числе, по мере увеличения возраста и роста ребенка. У 10-15% пациентов отмечают одышечно-цианотические приступы; характер их такой же, как при тетраде Фалло (приступы обусловлены спазмом выводного отдела ПЖ, ограничивающими поступление крови в ЛА). Таким образом, большинство пациентов с ЕЖ находятся в тяжелом состоянии, обусловленном, в первую очередь, хронической артериальной гипоксемией. Избыточный легочный кровоток при ЕЖ встречается значительно реже. Цианоз у таких пациентов в раннем детском возрасте часто отсутствует или нерезко выражен. Нарастание цианоза у пациентов старшего детского возраста обычно связано с прогрессирующим уменьшением легочного кровотока в результате развития морфологических изменений в артериальных сосудах легких, обусловленных чрезмерным кровотоком.
У большинства пациентов присутствует одышка. В случае обедненного легочного кровотока она имеет место и в покое, также усиливаясь при нагрузке. В случае избыточного легочного кровотока одышка нередко сочетается с признаками СН, выраженной в большей или меньшей степени (от чрезмерной потливости и тахикардии до гепатомегалии, отеков, асцита и/или гидроторакса).
Постепенно происходит изменение дистальных фаланг пальцев рук по типу «барабанных палочек» и «часовых стекол», что обусловлено хронической артериальной гипоксемией. Описанные изменения фаланг пальцев кистей чаще распространены у детей, переживших двухлетний возраст, но иногда могут развиваются уже в 3-4 месяца.
В случае сопутствующих субаортального стеноза, гипоплазии дуги аорты или коарктации аорты быстро могут развиваться и прогрессировать симптомы недостаточной перфузии органов и тканей, вплоть до шока. Пациенты с одновременной обструкцией системного и легочного кровотока, как правило, нежизнеспособны.
Помимо специфической клинической картины, около 70% пациентов имеют отставание в физическом развитии, а также сколиоз.
При аускультации легких возможно выслушивание застойных хрипов, что характерно для избыточного легочного кровотока и развития СН. Картина аускультации сердца определяется, в первую очередь, наличием и степенью выраженности обструкции на уровне БВО и/или легочного ствола. Над областью сердца выслушивается систолический шум, причем у пациентов без стеноза ЛА он максимально выражен в 3-4 межреберьи. Происхождение систолического шума может быть обусловлено либо прохождением крови из системного желудочка (СЖ) через БВО в камеру-выпускник и далее - в аорту. При стенозе ЛА шум носит грубый характер и максимально выражен над основанием сердца, соответственно уровню стеноза. Систолический шум на верхушке соответствует недостаточности атриовентрикулярного клапана. Следует помнить, что ЕЖ часто сочетается с аномалиями положения сердца, которые меняют локализацию шумов [1-3, 8-11].
В случае обедненного легочного кровотока с момента рождения или вскоре после него развивается цианоз. Насыщение крови кислородом составляет 70-80%. Цианоз усиливается при нагрузке (движение, плач, кормление), в том числе, по мере увеличения возраста и роста ребенка. У 10-15% пациентов отмечают одышечно-цианотические приступы; характер их такой же, как при тетраде Фалло (приступы обусловлены спазмом выводного отдела ПЖ, ограничивающими поступление крови в ЛА). Таким образом, большинство пациентов с ЕЖ находятся в тяжелом состоянии, обусловленном, в первую очередь, хронической артериальной гипоксемией. Избыточный легочный кровоток при ЕЖ встречается значительно реже. Цианоз у таких пациентов в раннем детском возрасте часто отсутствует или нерезко выражен. Нарастание цианоза у пациентов старшего детского возраста обычно связано с прогрессирующим уменьшением легочного кровотока в результате развития морфологических изменений в артериальных сосудах легких, обусловленных чрезмерным кровотоком.
У большинства пациентов присутствует одышка. В случае обедненного легочного кровотока она имеет место и в покое, также усиливаясь при нагрузке. В случае избыточного легочного кровотока одышка нередко сочетается с признаками СН, выраженной в большей или меньшей степени (от чрезмерной потливости и тахикардии до гепатомегалии, отеков, асцита и/или гидроторакса).
Постепенно происходит изменение дистальных фаланг пальцев рук по типу «барабанных палочек» и «часовых стекол», что обусловлено хронической артериальной гипоксемией. Описанные изменения фаланг пальцев кистей чаще распространены у детей, переживших двухлетний возраст, но иногда могут развиваются уже в 3-4 месяца.
В случае сопутствующих субаортального стеноза, гипоплазии дуги аорты или коарктации аорты быстро могут развиваться и прогрессировать симптомы недостаточной перфузии органов и тканей, вплоть до шока. Пациенты с одновременной обструкцией системного и легочного кровотока, как правило, нежизнеспособны.
Помимо специфической клинической картины, около 70% пациентов имеют отставание в физическом развитии, а также сколиоз.
При аускультации легких возможно выслушивание застойных хрипов, что характерно для избыточного легочного кровотока и развития СН. Картина аускультации сердца определяется, в первую очередь, наличием и степенью выраженности обструкции на уровне БВО и/или легочного ствола. Над областью сердца выслушивается систолический шум, причем у пациентов без стеноза ЛА он максимально выражен в 3-4 межреберьи. Происхождение систолического шума может быть обусловлено либо прохождением крови из системного желудочка (СЖ) через БВО в камеру-выпускник и далее - в аорту. При стенозе ЛА шум носит грубый характер и максимально выражен над основанием сердца, соответственно уровню стеноза. Систолический шум на верхушке соответствует недостаточности атриовентрикулярного клапана. Следует помнить, что ЕЖ часто сочетается с аномалиями положения сердца, которые меняют локализацию шумов [1-3, 8-11].
Диагностика
Критерии установления диагноза:
- Данные объективного исследования: цианоз, признаки недостаточности кровообращения;- Данные эхокардиографии / ангиокардиографии: отсутствие межжелудочковой перегородки, наличие атрио-вентрикулярных клапанов, открывающихся в ЕЖ, наличие камеры-выпускника (рудиментарного желудочка) и отходящим от нее магистральным сосудом.
2,1 Жалобы и анамнез.
• При расспросе пациента (или их родственников в случае маленьких детей) с подозрением на ВПС рекомендуется определить время появления цианоза, наличия или отсутствия его прогрессирования, а также расспросить о наличии и характере одышки для верификации диагноза и оценке общего состояния [1-3, 8-11].(УУР С, УДД 5).
• При сборе анамнеза и жалоб у пациентов с подозрением на ВПС, для оценки степени выраженности недостаточности кровообращения (НК), рекомендуется оценить у пациента (или его родственников) наличие и характер потливости [1-3, 8-12].
(УУР С, УДД 5).
2,2 Физикальное обследование.
• Во время физикального обследования у пациентов с подозрением на ВПС рекомендуется оценить признаки хронической артериальной гипоксемии (симптом «барабанных палочек», «часовых стекол») [1-3, 8-11].(УУР С, УДД 5).
• Для косвенной оценки соотношения легочного и системного кровотока, а также тяжести состояния пациента, во время физикального обследования у пациентов с подозрением на ВПС, рекомендуется определить уровень системной оксигенации (насыщение крови кислородом) путем пульсоксиметрии [1-3, 8-11].
(УУР С, УДД 5).
• Во время физикального обследования у пациентов с подозрением на ВПС, для оценки степени выраженности НК и тяжести состояния пациента, рекомендуется оценить характер и частоту дыхания [1-3, 8-12].
(УУР С, УДД 5).
Комментарии. При осмотре дыхание пациента может быть физиологическим, с умеренным (втяжение межреберных промежутков) и выраженным (одышка) вовлечением вспомогательной мускулатуры.
• Во время физикального обследования у пациентов с подозрением на ВПС, рекомендуется аускультация легких для выявления наличия или отсутствия застойных хрипов [1-3, 8-11].
(УУР С, УДД 5).
• Во время физикального обследования у пациентов с подозрением на ВПС, для определения характера шумов и косвенной оценки состояния легочного кровотока, рекомендуется выполнить аускультацию сердца ( см пункт 1,6) [1-3, 8-12].
(УУР С, УДД 5).
• Во время физикального обследования у пациентов с подозрением на ВПС, рекомендуется пальпация живота для выявления наличия или отсутствия гепатомегалии [1-3, 8-11].
(УУР С, УДД 5).
Комментарии. Тщательно собранный анамнез и данные физикального обследования позволяют точно определить степень выраженности НК и функциональный статус пациента. В детской кардиологической практике для быстрой оценки степени выраженности НК хорошо зарекомендовала себя модифицированная шкала Ross [12] (приложение Г).
2,3 Лабораторные диагностические исследования.
• На этапе обследования, в тч перед оперативным вмешательством, всем пациентам рекомендуется выполнить общий (клинический) анализ крови для определения исходного уровня гемоглобина и тромбоцитов [1-3, 8-11].(УУР С, УДД 5).
• На этапе обследования, в тч перед оперативным вмешательством, всем пациентам рекомендуется анализ крови биохимический общетерапевтический для оценки функции печени и почек [3, 13-16].
(УУР С, УДД 4).
Комментарии. Для оценки функции печени целесообразно выполнить исследование уровня общего белка и альбумина, АСТ, АЛТ, билирубина (общий, прямой, непрямой). Для оценки функции почек целесообразно выполнить исследование уровня мочевины, креатинина.
• На этапе обследования, в тч перед оперативным вмешательством, всем пациентам рекомендуется исследование коагулограммы (ориентировочное исследование системы гемостаза) с целью выявления исходных нарушений системы гемостаза, а также для оценки эффективности последующей (послеоперационной) тромбопрофилактики [8, 17-20].
(УУР В, УДД 3).
Комментарии. На сегодняшний день известным фактом является наличие исходных аномалий свертывающей системы крови у пациентов с одножелудочковой гемодинамикой. Ввиду этого, таким пациентам целесообразно определение показателей локальных (активированное частичное тромбоплатиновое время (АЧТВ), фибриноген, международное нормализованное отношение (МНО), степень агрегации тромбоцитов) и, при наличии возможности, - глобальных тестов (тромбоэластография) оценки гемостаза.
2,4 Инструментальные диагностические исследования.
• На этапе обследования, в тч перед оперативным вмешательством, всем пациентам рекомендуется регистрация электрокардиограммы (ЭКГ) для исключения нарушений ритма и проводимости, а также ишемии миокарда [1-3, 8-11, 21].(УУР С, УДД 4).
Комментарии. Наиболее закономерным является отклонение электрической оси сердца вправо (у более 70% пациентов) с признаками гипертрофии ПЖ (у более 94% пациентов). У 50% пациентов отмечаются также признаки гипертрофии ЛЖ. Характерными для ЕЖ являются высоковольтная ЭКГ в грудных отведениях, за исключением V1, преобладание зубцов S над зубцами R или равнозначные комплексы RS. У пациентов с ТМА может отмечаться отсутствие зубцов Q в левых и наличие их в правых грудных отведениях. Для пациентов с ЕЖ в значительной степени характерны нарушения проводимости и ритма различного характера.
• На этапе обследования, в тч перед оперативным вмешательством, всем пациентам с ЕЖ рекомендуется выполнение рентгенографии органов грудной клетки для оценки степени кардиомегалии и состояния легочного кровотока, а также определения участков гипо- или гипервентиляции легких [1-3, 8-11].
(УУР С, УДД 5).
Комментарии. У всех пациентов с ЕЖ, независимо от расположения магистральных артерий, наблюдается расширение тени сердца в поперечнике. В большей степени оно выражено у пациентов с увеличенным легочным кровотоком. Нередко имеют место признаки увеличения ПЖ, реже - левого. У всех пациентов имеет место увеличение правого предсердия. У пациентов с необструктивным легочным кровотоком наблюдается усиление легочного рисунка и расширение корней легких. В периферических отделах легочный рисунок представлен узкими артериальными сосудами, также отмечается симптом «ампутации» крупных артериальных ветвей (картина высокой легочной гипертензии). У пациентов с нормальным расположением магистральных артерий или расположении их, как при полной транспозиции со стенозом ЛА, в передне-задней проекции, в области второй дуги, отмечается западение, аналогичное тому, которое обычно имеет место при тетраде Фалло. При корригированной ТМА левый контур сердца не дифференцируется на первую и вторую дуги и представлен непрерывной, слегка выпуклой или прямой тенью, что связано с левосторонним расположением восходящей Ао. При этом у пациентов со стенозом ЛА по левому контуру сердца определяется выбухание третьей дуги, обусловленное расположением в этой области корня Ао и камеры-выпускника.
• Эхокардиография (ЭхоКГ) рекомендуется всем пациентам с подозрением на ЕЖ как ведущий метод диагностики, позволяющий установить окончательный диагноз [1-3, 8-11].
(УУР С, УДД 5).
Комментарии. Регистрируется отсутствие межжелудочковой перегородки и наличие атрио-вентрикулярных клапанов, открывающихся в ЕЖ. Удается определить камеру-выпускник и отходящий от нее магистральный сосуд. При нормальном расположении магистральных артерий определяется митрально-аортальное соединение, при ТМА - митрально-легочное. При проведении ЭхоКГ необходимо обратить внимание на следующие моменты: 1) оценка морфологии ЕЖ (левая или правая), его объема и сократительной функции, положение рудиментарного желудочка; 2) положение магистральных артерий, их размеры, анатомия полулунных клапанов; 3) при дискордантном положении магистральных артерий - размеры БВО и соотношение его с кольцом аортального клапана; 4) анатомия АВ клапанов, степень их недостаточности; 5) размеры межпредсердного сообщения (МПС), открытого артериального протока (ОАП), направление сброса через них; 6) наличие сопутствующих пороков (коарктация Ао, перерыв дуги Ао).
• Компьютерная / Магнитно-резонансная томография сердца с контрастированием (МРТ) рекомендуется пациентам с подозрением на ЕЖ в случаях наличия затруднения в установлении морфологии порока при помощи ЭхоКГ [8-11, 14].
(УУР С, УДД 5).
Комментарии. Методика точно отображает анатомию артериальных и венозных сосудов, клапанного аппарата, субстрат субаортального стеноза, внутрисердечную анатомию, объем желудочка, степень гипертрофии миокарда.
• Рекомендуется проведение ангиокардиографии (АКГ) (чрезвенозной катетеризации сердца, зондирования камер сердца) всем пациентам с ЕЖ с целью [1, 8, 10, 11, 22]:
1) уточнения диагноза при недостаточности данных, полученных в ходе ЭхоКГ;
2) оценки морфологии желудочка;
3) оценки размеров легочных артерий;
3) оценки наличия камеры-выпускника и типа вентрикуло-артериального соединения;
4) оценки характера обструкции ЛА с возможностью устранения стенозов ( см пункт 3,2);
5) оценки размеров МПС и выполнения процедуры Рашкинда при необходимости ( см пункт 3,2);
6) оценки и устранения коллатералей между системными и легочными венами;
7) оценки и устранения аорто-легочных коллатералей (устранение рекомендовано перед операцией Фонтена);
8) у пациентов с системно-легочным анастомозом для оценки его функции;
9) с целью выполнения коронарографии пациентам с клиническими проявлениями стенокардии, ишемическими изменениями на ЭКГ или аномалиями коронарных сосудов.
(УУР С, УДД 5).
Комментарии: Обследование включает измерение давления и насыщения кислородом в ЛА (наибольшее значение имеет оценка среднего давления), Ао, предсердиях, СЖ, определение легочного и системного кровотока, легочного сосудистого сопротивления (ЛСС). ЛСС - показатель, производный от давления в ЛА, оценивающий возможности легочных артерий отвечать на увеличение объема. В большинстве случаев операции, выполняемые с целью коррекции ЕЖ, направлены на увеличение легочного кровотока, поэтому определение давления в ЛА и ЛСС - важные моменты лечебно-диагностического поиска, влияющие на выбор последующей хирургической тактики. Ангиография позволяет оценить анатомию магистральных артерий (особенно ЛА; рассчитывают индексы Nakata, McGoon, нижнедолевой индекс), гипертрофию миокарда. Для решения вопроса о выборе метода хирургического лечения чрезвычайно важна вентрикулография. Она позволяет создать представление о величине БВО, объеме полости гипоплазированного желудочка, тяжести легочного стеноза, состоятельности АВ клапанов, характере расположения магистральных артерий. При введении контраста в ЕЖ, независимо от наличия или отсутствия стеноза ЛА, определяется большая полость желудочка, занимающая практически всю область сердечной тени как в передне-задней, так и в боковой проекции. Значительно чаще в ЕЖ обнаруживаются гладкие внутренние контуры, что соответствует архитектонике левого желудочка, реже - грубая трабекулярность, свойственная правому желудочку. В соответствии с номенклатурой медицинских услуг исследование включает: ангиографию грудной аорты ретроградную, ангиографию легочной артерии избирательную, ангиографию легочной артерии и ее ветвей, зондирование камер сердца, флебографию верхней полой вены, флебографию нижней полой вены, вентрикулографию сердца.
2,5 Иные диагностические исследования.
• Перед выпиской из стационара всем пациентам с целью контроля после выполненного оперативного вмешательства рекомендуется выполнить электрокардиографию [23, 24].(УУР С, УДД 5).
• Перед выпиской из стационара всем пациентам с целью контроля после выполненного оперативного вмешательства рекомендуется выполнить эхокардиографию [23, 24].
(УУР С, УДД 5).
|
|
Лечение
3,1 Консервативное лечение.
Консервативные мероприятия направлены на регулирование резистентности легочных или системных сосудов.• У новорожденных с резко обедненным легочным кровотоком рекомендуется применение простагландинов для поддержания проходимости ОАП [3, 25, 26].
(УУР С, УДД 5).
Комментарии. Среди препаратов наиболее распространено применение алпростадила** (применение у детей вне зарегистрированной инструкции). Препарат вводится внутривенно, как правило, в условиях отделения реанимации. Начальная доза составляет 0,02 мкг/кг/мин с возможностью увеличения до 0,05-0,1 мкг/кг/мин, поддерживающая доза - 0,002 мкг/кг/мин [25]. Срок терапии определяется индивидуально.
• Рекомендуется применение диуретиков, с целью лечения СН, осложняющей течение ЕЖ, в том числе, - при отсутствии отечного синдрома [3, 27-30].
(УУР С, УДД 5).
Комментарий. Наиболее часто применяются возрастные дозировки фуросемида** (противопоказано применение таблетированной лекарственной формы у детей до 3-х лет), доза у детей - внутривенно 0,5-2 мг/кг или per os 1-2 мг/кг каждые 6-12 часов [28, 30]; спиронолактона**, доза у детей - 1-4 мг/кг/сутки [29, 30].
• В ранние сроки после системно-легочного анастомоза (СЛА), а также после гемодинамической коррекции (двунаправленный кавопульмональный анастомоз (ДКПА) или операции Фонтена) ( см пункт 3,2,1) пациентам рекомендуется проведение тромбопрофилактики [20, 31-36].
(УУР С, УДД 5).
Комментарии. По современным представлениям тромбоэмболические осложнения (ТЭО) занимают одно из ведущих мест в структуре как ранней, так и отдаленной смертности после гемодинамической коррекции. Особенно настораживающим фактом являются случаи тромбозов на фоне проведения лекарственной тромбопрофилактики. С одной стороны, после операций «обхода» правых отделов сердца создаются условия для замедления кровотока, с другой стороны доказанным фактом является наличие исходного, нередко генетически-обусловленного, дефицита факторов свертывания. Совокупность указанных причин повышает вероятность ТЭО после операции. Для целей ранней тромбопрофилактики наиболее часто применяется гепарин натрия**, который, при отсутствии противопоказаний, назначается внутривенно капельно, по мере стабилизации хирургического гемостаза, в большинстве случаев - через 12-24 часа после операции. Начальная доза у детей - 28 ед/кг/час у детей первого года жизни и 20 ед/кг/час у детей старше года. До начала инфузии препарата целесообразно определить АЧТВ, при его значении менее 50 сек - ввести в/в струйно гепарин натрия** в дозе 50 ед/кг. Далее - в соответствии с рекомендациями ( см приложение А3) [36]. Запрещено применение у новорожденных, в особенности недоношенных или имеющих низкую массу тела детей.
• Для профилактики гиперкоагуляционных состояний во время тромбопрофилактики гепарином натрия** после СЛА, а также после гемодинамической коррекции рекомендуется поддержание АЧТВ в пределах 60-85 сек [20, 34-36].
(УУР С, УДД 5).
Комментарии. Существуют указания на связь гиперкоагуляционных состояний и низких значений АЧТВ (менее 50 сек).
• Рекомендуется контроль уровня тромбоцитов крови у пациентов в случае применения гепарина натрия** свыше 5 суток с целью исключения гепарин-индуцированной тромбоцитопении [34-36].
(УУР С, УДД 5).
• В отдаленные сроки после СЛА, а также после гемодинамической коррекции пациентам рекомендуется проведение долговременной тромбопрофилактики [20, 31, 34-37].
(УУР С, УДД 5).
Комментарии. Для целей долговременной тромбопрофилактики после СЛА применяется ацетилсалициловая кислота** в дозе 1-5 мг/кг/сутки (для пациентов до 18 лет - применение вне зарегистрированной инструкции); после гемодинамической коррекции применяется ацетилсалициловой кислота** у детей в дозе 1-5 мг/кг/сутки (нередко 50 мг/сутки при весе до 10 кг и 5 мг/кг/сутки при весе более 10 кг, но не более 100 мг/кг/сутки) [20, 31, 36], у взрослых - 50-200 мг/сутки или варфарин** в возрастной дозировке. тромбопрофилактика ацетилсалициловой кислотой** продолжается, не менее 6 мес или до момента следующего этапа хирургического лечения. В случае тромбопрофилактики варфарином** назначается на срок не менее 6 мес или до момента следующего этапа хирургического лечения [20]. В соответствии с данными литературы, нет значимой разницы эффективности тромбопрофилактики ацетилсалициловой кислотой** и варфарином**, однако настораживающим моментом является сохранение гиперкоагуляционных состояний, несмотря на проведение тромбопрофилактики. Не исключена целесообразность одновременного приема ацетилсалициловой кислоты** и варфарина** для достижения наиболее оптимального состояния свертывающей системы крови [20, 37].Рекомендуется исследование агрегации тромбоцитов у пациентов после назначения ацетилсалициловой кислоты** с целью долговременной тромбопрофилактики после СЛА или гемодинамической коррекции [34, 35].
(УУР С, УДД 5).
Комментарии. Контроль показателя проводится через 2-5 дня от начала приема препарата. Критерием эффективности ацетилсалициловой кислоты** считается снижение показателя не менее, чем на 50% от исходного значения. Случаи снижения степени агрегации тромбоцитов менее, чем на 50% от исходного могут быть связаны с недостаточной дозой ацетилсалициловой кислоты**, а также не исключают наличия резистентности пациента к препарату. При наличии резистентности решается вопрос о смене препарата для долговременной тромбопрофилактики (например, на варфарин**).
• Рекомендуется поддержание целевого МНО (в пределах 2-3) у пациентов, принимающих варфарин**, с целью долговременной тромбопрофилактики после гемодинамической коррекции [20, 34, 35].
(УУР С, УДД 5).
Комментарии. По данным литературы, случаи ТЭО в средне-отдаленные сроки после гемодинамической коррекции, в большей степени, связаны с нарушением приема и/или несвоевременного контроля дозы варфарина** (МНО), выражающиеся в недостижении целевого МНО.
• Всем пациентам с ЕЖ после СЛА и гемодинамической коррекции, а также при наличии наджелудочковой аритмии, для профилактики ТЭО в отдаленные сроки, рекомендуется пожизненное применение лекарственной тромбопрофилактики [2, 10, 11, 20, 22, 34, 35, 38, 39].
(УУР С, УДД 4).
Комментарии. Детям наиболее часто назначается ацетилсалициловая кислота** или варфарин** в указанных ранее дозах [20, 31, 36]. Имеются данные о высокой частоте гиперкоагуляции на фоне изолированной тромбопрофилактики ацетилсалициловой кислотой** или варфарином** у детей и указания на необходимость комбинации этих препаратов у пациентов данной возрастной группы для достижения оптимального состояния свертывающей системы крови (в силу ограниченного опыта применения новых оральных антикоагулянтов).
3,2 Хирургическое лечение.
Хирургическая коррекция ЕЖ носит паллиативный (одножелудочковый) характер. Выбор той или иной паллиативной операции зависит в основном от состояния кровотока в малом круге кровообращения.Этап хирургического лечения.
Основные цели данного этапа. Максимально сбалансировать системный и легочный кровоток, обеспечить беспрепятственное смешивание крови на уровне предсердий, обеспечить необструктивный выход из СЖ [1].
• Ввиду высокой вероятности неблагоприятного исхода двужелудочковой коррекции, не рекомендуется ее выполнение пациентам с ЕЖ [1-3, 8].
(УУР С, УДД 5.
Среди паллиативных операций выделяют следующие:
• Процедура Рашкинда рекомендуется в качестве неотложной меры помощи у новорожденных при наличии рестриктивного МПС у пациентов [1-3, 8].
(УУР С, УДД 5).
Комментарии. Под рестриктивным МПС понимается наличие сообщения на уровне предсердий, при котором существует разность давлений между правым и левым предсердиями. В этом случае может иметь место сопротивление кровотоку на уровне данного МПС.
• Суживание ЛА (операция Muller) и перевязка ОАП (при его наличии) рекомендуется в периоде новорожденности при резко увеличенном легочном кровотоке с целью ограничения легочного кровотока и «защиты» малого круга кровообращения от развития склеротических изменений [1, 2, 8, 10, 11, 22, 32, 34].
(УУР С, УДД 5).
Комментарии. Избыточный легочный кровоток способствует развитию тяжелой СН и высокой легочной гипертензии.
• Рекомендуется создание СЛА у пациентов в периоде новорожденности при насыщении крови кислородом менее 70-75% [1, 2, 8, 10, 11, 22, 32, 34].
(УУР С, УДД 5).
Комментарии. Выраженная гипоксемия часто характерна для тяжелого стеноза ЛА (нередко при ОАП-зависимом легочном кровотоке). Предпочтительное выполнение СЛА - в возрасте до 3-х месяцев.
Гемодинамическая коррекция.
Следующим этапом выполняется так называемая «гемодинамическая» (одножелудочковая) коррекция, заключающаяся в создании тотального кавопульмонального анастомоза (синоним: «полный обход» правого сердца). Цель данного этапа - снижения преднагрузки СЖ и увеличение системной оксигенации [2, 8].
• В качестве первого этапа гемодинамической коррекции у детей рекомендуется выполнение ДКПА (синоним: верхний кавопульмональный анастомоз) [1, 2, 8, 10, 11, 22].
(УУР С, УДД 5).
Комментарии. ДКПА заключается в создании анастомоза «конец в бок» между верхней полой веной (ВПВ) и соответствующей главной ветвью ЛА. Предпочтительное выполнение - в возрасте от 4-х мес до 1 года. В большинстве случаев после ДКПА насыщение крови кислородом устанавливается в пределах 80%.
• В качестве второго (заключительного) этапа гемодинамической коррекции у детей рекомендуется выполнение анастомоза между нижней полой веной (НПВ) и ЛА (синонимы: операция Фонтена, нижний кавопульмональный анастомоз) [1, 2, 8, 10, 11, 22,].
(УУР С, УДД 5).
Комментарии. Выполнение одномоментного тотального кавопульмонального анастомоза сопровождалось высокой летальностью, поэтому было предложено разделить операцию на 2 самостоятельных этапа. Данная тактика позволила существенно улучшить результаты гемодинамической коррекции. Наиболее распространенной в настоящее время модификацией операции Фонтена является использование сосудистого протеза (протез кровеносных сосудов синтетический), имплантированного непосредственно между НПВ и ЛА.
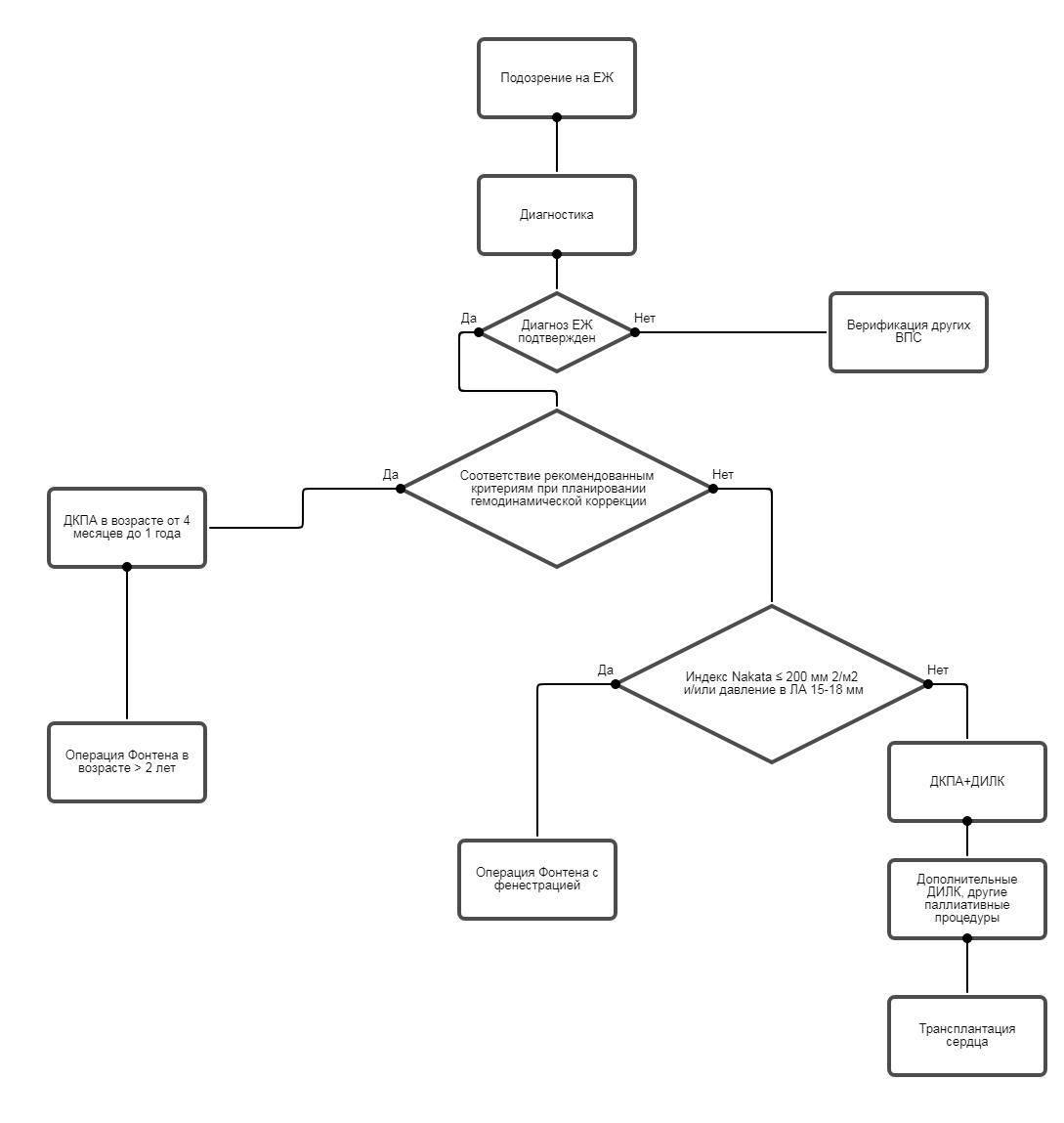
• Рекомендуется соблюдение следующих возрастных критериев при планировании гемодинамической коррекции [40-46]:
- для ДКПА - не менее 4 мес.
- для операции Фонтена - предпочтительно не менее 2-х лет.
(УУР с, УДД 4).
Комментарии. Ранний возраст на сегодняшний день не является фактором, препятствующим выполнению ДКПА, тем не менее до настоящего времени оптимальные сроки операции не определены. Одни авторы рекомендуют ДКПА до 6 месяцев, объясняя это пользой от ранней «разгрузки» СЖ, но не ранее 3 месяцев [19-22], другие считают оптимальным его создание в промежутке от 6 месяцев до 2 лет, что связывают с максимальным приростом насыщения крови кислородом после процедуры в данной возрастной группе [24, 25]. Сомнения, связанные с выполнением операции до 3 месяцев, оправданны и связаны с более высоким ЛСС у таких детей, возможным повышением частоты осложнений и летальности, неуверенностью в адекватном росте легочных артерий после операции и риском неблагоприятного влияния процедуры на мозговое кровообращение [40, 42, 44, 46]. Возраст» выполнения операции Фонтена так же оспаривается. Одни авторы склоняются к выполнению данного этапа в более старшем возрасте, объясняя это ограниченным «сроком службы» нефизиологичного одножелудочкового кровообращения и неизбежной его декомпенсацией. При этом основными показаниями к операции выступают такие факторы, как прогрессирование системной гипоксемии и снижение толерантности к физической нагрузке. Другие же, наоборот, стараются перейти к тотальному кавопульмональному анастомозу в более ранние сроки, объясняя подобную тактику пользой от уже упомянутого раннего снижения преднагрузки СЖ [40, 42].
• Рекомендуется соблюдение критериев адекватного развития легочного артериального русла у пациентов при планировании гемодинамической коррекции [47-49]:
- индекс Nakata ≥ 200 мм2/м2;
- индекс McGoon ≥ 1,5.
(УУР с, УДД 4).
Комментарии. Несмотря на вышеуказанные ориентировочные показатели развития легочного артериального русла считается, что небольшие размеры ЛА (индексы Nakata ≤ 100 мм2/м2 и McGoon ≤ 1,2) не оказывают значимого влияния на ранние результаты гемодинамической коррекции [47]. Как известно, размеры ЛА могут зависеть от количества крови, притекающей к ним [48], поэтому абсолютные их значения, возможно, и не самый важный фактор риска [49]. Очевидно, что более важным фактором может являться функциональная способность ЛА отвечать на увеличение кровотока в легкие после операции, выражающаяся в ЛСС ( см пункт 2,4).
• Для достижения наиболее оптимальных результатов операции рекомендуется выполнение гемодинамической коррекции у пациентов с сопоставимыми размерами полых вен и легочных артерий [2, 8, 22].
(УУР С, УДД 5).
• При планировании гемодинамической коррекции у пациентов рекомендуется придерживаться следующих значений показателей гемодинамики малого круга кровообращения [2, 8, 22]:
- среднее давление в ЛА:
≤ 20 мм ст для ДКПА;
≤ 15 мм для операции Фонтена;
- легочное сосудистое сопротивление:
≤ 5 Ед/м2 для ДКПА;
≤ 4 Ед/м2 для операции Фонтена.
(УУР С, УДД 5).
• У пациентов с АВ недостаточностью выраженной и более степени рекомендуется ее коррекция на этапах гемодинамической коррекции [2, 8, 22].
(УУР С, УДД 5).
Комментарии. Допустимой и не требующей коррекции степенью АВ недостаточности считается умеренная (1-2).
• Пациентам с субаортальной обструкцией, встречающейся при сопутствующем дискордантном (не от тождественного желудочка) отхождении Ао, рекомендуется устранение обструкции на этапах гемодинамической коррекции [2, 8, 22, 50, 51].
(УУР с, УДД 4).
Комментарии. Показания к коррекции субаортальной обструкции определяются наличием градиента систолического давления между СЖ и Ао, рестриктивного ДМЖП (признак рестриктивности ДМЖП - площадь сечения дефекта менее 2 см2/м2), соотношения диаметров ДМЖП и фиброзного кольца аортального клапана. Хирургическая тактика заключается либо в расширении ДМЖП, либо в выполнении процедуры Damus-Kaye-Stansel одновременно с гемодинамической коррекцией. После расширения ДМЖП нередко отмечены АВ блокады 3 степени, ввиду чего выполнение операции Damus-Kaye-Stansel, при соблюдении показаний, предпочтительно. Одним из ключевых критериев возможности выполнения операции Damus-Kaye-Stansel является сохранение компетентности клапана ЛА.
• Выполнение гемодинамической коррекции рекомендуется при следующих значениях показателей сократительной функции сердца у пациентов [2, 8, 22, 52]:
- фракция выброса better 55%;
- конечно-диастолическое давления ≤ 12 мм.
(УУР с, УДД 5).
Комментарии. Косвенным признаком компрометирования сократительной функции СЖ является индекс его конечно-диастолического объема (мл/м2). В ряде работ отмечена связь исходного увеличения конечно-диастолического объема СЖ и угнетения его сократительной функции в послеоперационном периоде.
• При планировании гемодинамической коррекции у пациентов рекомендуется оценка дополнительных источников легочного кровотока (ДИЛК; синоним: гибридный легочный кровоток) [2, 8, 22].
(УУР С, УДД 5).
Комментарии. ДИЛК оценивают в ходе ангиокардиографического исследования при выполнении аортографии. При выполнении ДКПА решение о сохранении или устранении ДИЛК в каждом случае носит индивидуальный характер.
• Рекомендуется сохранение ДИЛК на этапе ДКПА при тенденции к снижению насыщения крови кислородом менее 80% и стабильных показателей центральной гемодинамики (среднее давление в ЛА ≤ 15 мм рт. , отсутствие прогрессирующей гипотонии) [2, 8, 22].
(УУР С, УДД 5).
Комментарии. Оценка показателей проводится непосредственно после ДКПА, в условиях концентрации кислорода во вдыхаемой смеси в пределах 21-30%. При увеличении насыщения крови кислородом свыше 90% выполняется пробное пережатие дополнительных источников, руководствуясь далее уровнем насыщения крови кислородом (целевое значение 80-90%). При сохраняющейся необходимости сохранения гибридного легочного кровотока предпочтение отдается антеградному источнику (легочный ствол). В ряде ситуаций, в основном по причине устьевых стенозов той или иной ветви ЛА, возможно сохранение одновременно двух источников легочного кровотока - антеградного и СЛА или ОАП дистальнее места стеноза ЛА.
• Рекомендуется сохранение ДИЛК на этапе ДКПА в случаях, когда предполагается повышенный риск последующего выполнения «полного обхода» правых отделов сердца [3, 8, 10, 11, 22].
(УУР С, УДД 5).
Комментарии. ДКПА с ДИЛК обеспечивает длительное сохранение относительно стабильного насыщения крови кислородом. При необходимости таким пациентам можно создавать дополнительные ДИЛК в отдаленные сроки после ДКПА (СЛА, аксиллярный артериовенозный анастомоз).
• У ряда пациентов со сложными ВПС и высоким риском операции Фонтена, в силу тех или иных анатомо-гемодинамических факторов, рекомендуется выполнение ДКПА с ДИЛК в качестве «окончательного» этапа гемодинамической коррекции или «моста» к пересадке сердца [2, 10, 11, 22].
(УУР С, УДД 5).
• Сохранение ДИЛК на этапе операции Фонтена нередко приводит к венозной гипертензии и развитию НК, поэтому рекомендуется устранение ДИЛК (при наличии) пациентам перед выполнением операции Фонтена [2, 8, 22].
(УУР С, УДД 5).
• Для достижения наиболее оптимальных результатов операции при планировании гемодинамической коррекции рекомендуется оценка состояния венозного оттока у пациентов [2, 8, 22]:
(УУР С, УДД 5).
Комментарии. В случае обнаружения препятствий на пути венозного оттока хирургическая тактика определяется индивидуально. Наиболее частыми причинами обструкции венозного оттока являются аномальный дренаж легочных вен, стенозы устьев легочных вен, рестриктивное МПС.
• Для достижения наиболее оптимальных результатов гемодинамической коррекции рекомендуется устранение факторов, способствующих обструкции венозного оттока на этапе ДКПА [2, 8, 22].
(УУР С, УДД 5).
• Выполнение первичного ДКПА рекомендуется у пациентов без критического стеноза ЛА и ОАП-зависимого легочного кровотока с уровнем системного насыщения better 70-75%, без избыточного легочного кровотока (среднее давление в легочной артерии worse 20 мм ) [2, 8, 22].
(УУР С, УДД 5).
• При значимых локальных стенозах ветвей ЛА пациентам рекомендуется коррекция стенозов эндоваскулярными методами или при помощи открытых операций одномоментно с этапами гемодинамической коррекции [2].
(УУР С, УДД 5).
• При планировании заключительного этапа гемодинамической коррекции пациентам с пограничными размерами ЛА (индекс Nakata ≤ 200 мм2/м2) и повышенном среднем давлении в ЛА (15-18 мм ) рекомендуется выполнение операции Фонтена с фенестрацией между ЭКК и предсердием [2, 8, 22].
(УУР С, УДД 5).
• Не рекомендуется выполнение операции Фонтена пациентам при склеротических изменениях сосудов легких и выраженной дисфункции СЖ [1, 41-43].
(УУР с, УДД 5).
Комментарии. Объективными критериями состояния сосудов легких являются среднее ДЛА и ЛСС, функции системного желудочка - фракция выброса, конечно-диастолическое давление, индекс конечно-дистолического объема.
• Трансплантация сердца рекомендуется пациентам при тяжелой дисфункции СЖ [8, 22, 32, 34, 53-55].
(УУР С, УДД 4).
Послеоперационные осложнения.
Наиболее частыми ранними осложнениями после гемодинамической коррекции являются неврологические нарушения, дыхательная недостаточность, синдром верхней полой вены, повышенная транссудация [43, 45, 56].
• Для снижения риска послеоперационных осложнений рекомендуется ранняя (1-е сутки после операции) экстубация пациентов после гемодинамической коррекции [57-62].
(УУР с, УДД 4).
Комментарии. Основные осложнения нередко связывают с повышением венозного давления в кавопульмональном тракте, что в свою очередь может быть обусловлено колебанием ЛСС в раннем послеоперационном периоде и недостаточной компенсацией легочного кровообращения к увеличению кровотока. Искусственная вентиляция легких повышает внутригрудное давление и замедляет венозный возврат по системным венам, что является дополнительным фактором повышения венозного давления.
Среди отдаленных осложнений после гемодинамической коррекции наиболее важными являются венозная гипертензия, нарушения ритма сердца, белково-дефицитная энтеропатия, печеночная дисфункция, тромбоэмболические осложнения [2, 8].
Венозная гипертензия является основной причиной развития и прогрессирования НК (гепатомегалии, асцита, гидроторакса, периферических отеков, цианоза) в средне-отдаленные сроки после операции Фонтена. К факторам, повышающим вероятность развития венозной гипертензии, относятся стенозы ЛА, ДИЛК, недостаточность АВ клапана, стенозы полых вен или сосудистого протеза между НПВ и ЛА (например, вследствие «перероста» протеза), развитие венозных коллатералей, дисфункция СЖ, белково-дефицитная энтеропатия (БДЭП), ТЭО, печеночной недостаточности [2].
• Рекомендуется устранение локальных стенозов ЛА в случае их развития у пациентов после тех или иных этапов гемодинамической коррекции [2, 10, 11, 22].
(УУР С, УДД 5).
Комментарии. В большинстве случаев их устранение возможно эндоваскулярным способом.
• Рекомендуется эндоваскулярное устранение ДИЛК в случае их реканализации или развития после ДКПА или операции Фонтена при стойких признаках НК [2, 10, 11, 22].
(УУР С, УДД 5).
Комментарии. Аорто-легочные коллатеральные артерии могут быть не диагностированы до операции или же развиваться в ранние или отдаленные сроки после неё. Реканализация ствола ЛА может происходить спустя 1-2 года после операции (положение справедливо для случаев, где легочный ствол был перевязан интраоперационно, и неактуально для пациентов с сопутствующей атрезией легочной артерии).
• При прогрессировании недостаточности АВ клапана более, чем умеренной степени пациентам рекомендуется проведение корригирующей операции [2, 10, 11, 22].
(УУР С, УДД 5).
Комментарии. Коррекция недостаточности АВ клапана может быть выполнена как отдельная процедура, так и одновременно с операцией Фонтена. В ряде случаев это осложнение возникает в отдаленном послеоперационном периоде вследствие перенесенного инфекционного эндокардита или дилатации фиброзного кольца клапана в результате прогрессирующей дисфункции СЖ.
• После операции Фонтена в модификации ЭКК пациентам рекомендуется операция по замене сосудистого протеза в случае развития венозной гипертензии вследствие недостаточного размера кондуита относительно роста и развития пациента [2, 10, 11, 22].
(УУР С, УДД 5).
• Для увеличения насыщения крови кислородом в случае развития венозных коллатералей после ДКПА пациентам рекомендуется их эмболизация [2, 10, 11, 22].
(УУР С, УДД 5).
Комментарии. При отсутствии таких факторов, как выраженная недостаточность АВ клапанов, остаточные стенозы ЛА и повышенное давление в малом круге кровообращения результаты операции ДКПА хорошие. Однако по мере роста пациента происходит постепенно снижение насыщения артериальной крови кислородом, что обусловлено возрастным уменьшением доли венозного возврата по системе ВПВ, а также развитием легочных артериовенозных фистул. Прогрессирующий цианоз в отдаленные сроки после операции ДКПА может быть связан также с развитием коллатеральных сосудов между системами верхней и нижней полых вен, обусловленным разницей давления между ними, приводящей к сбросу крови из ВПВ в НПВ и уменьшению легочного кровотока. Гемодинамическими причинами этого осложнения также могут быть обструкция легочного кровотока на различных уровнях, повышение ЛСС, дисфункция СЖ или АВ клапанов, тромбоз полых вен и другие факторы, приводящие к повышению венозного давления. По данным A. Magee и соавт. венозные коллатеральные сосуды развиваются в 31% случаев после операции ДКПА. Наиболее часто в роли коллатеральных сосудов выступают непарная и полунепарная вены, а также вены перикарда и передней грудной стенки. Эмболизация венозных коллатералей является эффективным методом повышения насыщения крови кислородом в случаях, когда риск выполнения операции Фонтена повышен.
• Рекомендуется трансплантация сердца пациентам при выраженной дисфункции СЖ, рефрактерной к консервативной терапии [2].
(УУР С, УДД 5).
Комментарии. Дисфункция СЖ может быть обусловлена как его морфологией, так и исходной тяжестью порока или перенесенными инфекционными заболеваниями (в тч миокардитом) в послеоперационном периоде [6].
• Пациентам рекомендуется немедленная госпитализация в стационар при подозрении на БДЭП [2, 53, 54].
(УУР С, УДД 3).
Комментарии. Под термином «белок-дефицитная энтеропатия» подразумевается состояние, характеризующееся нарушением всасывания белка в тонком кишечнике. Частота этого осложнения составляет в среднем 3,8%. Сроки развития БДЭП составляют от 1 месяца до 16 лет (в среднем 2,7 года), при этом у одной трети пациентов осложнение развивается в сроки свыше 5 лет после операции. Причины развития БДЭП после операции Фонтена до сих пор изучены не полностью. Одним из вероятных механизмов является развитие лимфангиоэктазий в органах брюшной полости, в том числе и в кишечнике в результате постоянно повышенного венозного и лимфатического давления после операции Фонтена. Клинически БДЭП проявляется гипоальбуминемией, и как следствие этого, отеками, асцитом, плевральной транссудацией или хилотораксом, иммунодефицитом и гипокальциемией. На поздних стадиях развития большинство проявлений этого осложнения соответствует клинической картине НК. Методом ранней диагностики БДЭП является определение уровня фекального α1-антитрипсина, концентрация которого при БДЭП существенно повышается. Прогноз в случае развития БДЭП, как правило, неблагоприятный. В большинстве работ отмечается высокая летальность среди этих пациентов. Если в течение 5 лет с момента развития осложнения выживаемость составляет около 60%, то через 10 лет остаются в живых менее 20% пациентов.
|
|
Реабилитация и амбулаторное лечение
• В рамках реабилитационного становления, в сроки до 3-х месяцев после хирургического лечения ЕЖ пациентам рекомендуется ограничение по употреблению жидкости, а также по физической нагрузке [64].
(УУР С, УДД 5).
Комментарии. Употребление жидкость (особенно в течение первого месяца после операции) регламентируется как 60-80% от суточного потребления. В течение указанного периода целесообразно избегать чрезмерных физических нагрузок (импульсивные, силовые игры, быстрый бег, поднятие тяжестей), особенно следует избегать избыточной нагрузки на пояс верхних конечностей (способствует правильному срастанию грудины).
(УУР С, УДД 5).
Комментарии. Употребление жидкость (особенно в течение первого месяца после операции) регламентируется как 60-80% от суточного потребления. В течение указанного периода целесообразно избегать чрезмерных физических нагрузок (импульсивные, силовые игры, быстрый бег, поднятие тяжестей), особенно следует избегать избыточной нагрузки на пояс верхних конечностей (способствует правильному срастанию грудины).
Профилактика
• Рекомендуется пожизненное наблюдение врача-кардиолога с обследованием пациентов после различных этапов коррекции ЕЖ в специализированных центрах не реже 1 раза в 6-12 мес [22, 64].
(УУР С, УДД 5).
• Всем женщинам репродуктивного возраста, перенесшим операцию Фонтена, рекомендуется полное обследование с обязательной ЭхоКГ перед планированием беременности [64].
(УУР С, УДД 5).
• В отдаленные сроки после операции Фонтена возможно развитие печеночной дисфункции, поэтому не реже 1 раза в 6-12 мес.пациентам после операции Фонтена рекомендуется контроль таких биохимических показателей крови как общего белка, альбумина, АСТ, АЛТ, билирубина (общего, прямого, непрямого) [2, 65].
(УУР С, УДД 5).
• Для оценки сократительной функции сердца, компетентности АВ клапанов, характера кровотока по СЛА, ДКПА и/или ЭКК, а также с целью исключения гидроторакса/гидроперикарда всем пациентам после различных этапов коррекции ЕЖ рекомендуется проведение ЭхоКГ в течение первого месяца после выписки, далее - не реже 1 раза в 6-12 мес [22, 64].
(УУР С, УДД 5).
• При недостаточных данных, необходимых для оценки характера показателей кровообращения и полученных в ходе ЭхоКГ после СЛА или этапной гемодинамической коррекции (в тч при планировании следующего этапа) пациентам рекомендуется проведение АКГ с зондированием камер сердца, сроки которого определяются индивидуально [10, 11, 22].
(УУР С, УДД 5).
Комментарии. После СЛА исследование проводится в сроки от 6 до 12 мес, после ДКПА - не менее, чем через 12 мес. Основные цели АКГ в указанные сроки - оценка возможности выполнения следующего этапа хирургического лечения, в случае его невозможности - оценка функции СЛА и/или ДКПА, степени развития легочного артериального русла. После операции Фонтена необходимость АКГ обусловлена, в первую очередь, необходимостью тех или иных эндоваскулярных вмешательств (диллатации или стентирования легочных артерий при их стенозировании, устранения ДИЛК, закрытия фенестрации между ЭКК и предсердием), при этом сроки АКГ четко не регламентированы.
• Всем пациентам с ЕЖ, получающим лекарственную тромбопрофилактику, рекомендуется не реже 1 раза в 6 мес выполнение коагулограммы (ориентировочное исследование системы гемостаза) [20, 34, 35].
(УУР С, УДД 5).
Комментарии. Необходимо начать с объективного обследования и обратить внимание на уровень системной оксигенации, признаки НК, их изменение в динамике. Существует мнение о наличии связи микротромбозов с развитием после операции сердечной недостаточности. Среди лабораторных данных важную информацию могут предоставить оценка общего (клинического) анализа крови (гемоглобин, тромбоциты), исследование агрегации тромбоцитов (для пациентов, получающих ацетилсалициловую кислоту**), МНО (для пациентов, получающих варфарин**), тромбоэластографии.
• Рекомендуется применение антибактериальных препаратов системного действия (пенициллины широкого спектра действия, другие бета-лактамные антибактериальные препараты) у пациентов с ЕЖ после различных этапов хирургического лечения, в связи с опасностью инфекционного эндокардита [2, 3, 10, 11, 22].
(УУР С, УДД 5).
Комментарии. Антибиотикопрофилактика назначается в случае необходимости амбулаторных хирургических вмешательств, экстракции зубов и пр.
(УУР С, УДД 5).
• Всем женщинам репродуктивного возраста, перенесшим операцию Фонтена, рекомендуется полное обследование с обязательной ЭхоКГ перед планированием беременности [64].
(УУР С, УДД 5).
• В отдаленные сроки после операции Фонтена возможно развитие печеночной дисфункции, поэтому не реже 1 раза в 6-12 мес.пациентам после операции Фонтена рекомендуется контроль таких биохимических показателей крови как общего белка, альбумина, АСТ, АЛТ, билирубина (общего, прямого, непрямого) [2, 65].
(УУР С, УДД 5).
• Для оценки сократительной функции сердца, компетентности АВ клапанов, характера кровотока по СЛА, ДКПА и/или ЭКК, а также с целью исключения гидроторакса/гидроперикарда всем пациентам после различных этапов коррекции ЕЖ рекомендуется проведение ЭхоКГ в течение первого месяца после выписки, далее - не реже 1 раза в 6-12 мес [22, 64].
(УУР С, УДД 5).
• При недостаточных данных, необходимых для оценки характера показателей кровообращения и полученных в ходе ЭхоКГ после СЛА или этапной гемодинамической коррекции (в тч при планировании следующего этапа) пациентам рекомендуется проведение АКГ с зондированием камер сердца, сроки которого определяются индивидуально [10, 11, 22].
(УУР С, УДД 5).
Комментарии. После СЛА исследование проводится в сроки от 6 до 12 мес, после ДКПА - не менее, чем через 12 мес. Основные цели АКГ в указанные сроки - оценка возможности выполнения следующего этапа хирургического лечения, в случае его невозможности - оценка функции СЛА и/или ДКПА, степени развития легочного артериального русла. После операции Фонтена необходимость АКГ обусловлена, в первую очередь, необходимостью тех или иных эндоваскулярных вмешательств (диллатации или стентирования легочных артерий при их стенозировании, устранения ДИЛК, закрытия фенестрации между ЭКК и предсердием), при этом сроки АКГ четко не регламентированы.
• Всем пациентам с ЕЖ, получающим лекарственную тромбопрофилактику, рекомендуется не реже 1 раза в 6 мес выполнение коагулограммы (ориентировочное исследование системы гемостаза) [20, 34, 35].
(УУР С, УДД 5).
Комментарии. Необходимо начать с объективного обследования и обратить внимание на уровень системной оксигенации, признаки НК, их изменение в динамике. Существует мнение о наличии связи микротромбозов с развитием после операции сердечной недостаточности. Среди лабораторных данных важную информацию могут предоставить оценка общего (клинического) анализа крови (гемоглобин, тромбоциты), исследование агрегации тромбоцитов (для пациентов, получающих ацетилсалициловую кислоту**), МНО (для пациентов, получающих варфарин**), тромбоэластографии.
• Рекомендуется применение антибактериальных препаратов системного действия (пенициллины широкого спектра действия, другие бета-лактамные антибактериальные препараты) у пациентов с ЕЖ после различных этапов хирургического лечения, в связи с опасностью инфекционного эндокардита [2, 3, 10, 11, 22].
(УУР С, УДД 5).
Комментарии. Антибиотикопрофилактика назначается в случае необходимости амбулаторных хирургических вмешательств, экстракции зубов и пр.
Организация оказания медицинской помощи
Показания для плановой госпитализации:
1. Отсутствие признаков нарастания НК и стабильный функциональный статус пациента (I-II функциональный класс) без тенденции к ухудшению в течение 6-12 мес после СЛА, в течение не менее 12 мес - после этапной гемодинамической коррекции (для оценки у взрослых пациентов применяется классификация сердечной недостаточности Нью-Иоркской ассоциации сердца (NYHA), для оценки у детей - классификация Ross (приложение Г);
2. Стабильное насыщение крови кислородом без тенденции к снижению.
3. Плановое хирургическое лечение.
Показания для экстренной госпитализации:
1. Ухудшение функционального статуса пациента с прогрессированием признаков НК в течение последних 2-4 недель или дней (для оценки у взрослых пациентов применяется классификация сердечной недостаточности Нью-Иоркской ассоциации сердца (NYHA), для оценки у детей - классификация Ross (приложение Г));
2. Прогрессирование снижения насыщение крови кислородом менее 80% в течение последних 2-4 недель или дней;
3. Подозрение на развитие у пациента БДЭП.
Показания к выписке пациента из стационара:
1. После консервативного лечения:
· Уменьшение клинических проявлений НК;
· Увеличение насыщения крови кислородом.
2. После этапного хирургического лечения:
· Системно-легочный анастомоз / процедура Рашкинда - увеличение насыщения крови кислородом / устранение рестриктивного МПС;
· Этапная гемодинамическая коррекция - снижение преднагрузки (уменьшение конечно-диастолического объема) СЖ, увеличение насыщения крови кислородом.
1. Отсутствие признаков нарастания НК и стабильный функциональный статус пациента (I-II функциональный класс) без тенденции к ухудшению в течение 6-12 мес после СЛА, в течение не менее 12 мес - после этапной гемодинамической коррекции (для оценки у взрослых пациентов применяется классификация сердечной недостаточности Нью-Иоркской ассоциации сердца (NYHA), для оценки у детей - классификация Ross (приложение Г);
2. Стабильное насыщение крови кислородом без тенденции к снижению.
3. Плановое хирургическое лечение.
Показания для экстренной госпитализации:
1. Ухудшение функционального статуса пациента с прогрессированием признаков НК в течение последних 2-4 недель или дней (для оценки у взрослых пациентов применяется классификация сердечной недостаточности Нью-Иоркской ассоциации сердца (NYHA), для оценки у детей - классификация Ross (приложение Г));
2. Прогрессирование снижения насыщение крови кислородом менее 80% в течение последних 2-4 недель или дней;
3. Подозрение на развитие у пациента БДЭП.
Показания к выписке пациента из стационара:
1. После консервативного лечения:
· Уменьшение клинических проявлений НК;
· Увеличение насыщения крови кислородом.
2. После этапного хирургического лечения:
· Системно-легочный анастомоз / процедура Рашкинда - увеличение насыщения крови кислородом / устранение рестриктивного МПС;
· Этапная гемодинамическая коррекция - снижение преднагрузки (уменьшение конечно-диастолического объема) СЖ, увеличение насыщения крови кислородом.
Дополнительно
При подозрении на патологию трахео-бронхиального дерева до операции необходимо обследовать пациента у врача-пульмонолога [66].
Критерии оценки качества медицинской помощи
| Этап диагностики | |||
| 1 | Проведен сбор жалоб и анамнеза пациенту с подозрением на врожденный порок сердца | С | 5 |
| 2 | Проведено физикальное обследование пациенту с подозрением на врожденный порок сердца | С | 5 |
| 4 | При первичном обследовании пациента выполнена оценка насыщения крови кислородом | С | 5 |
| 5 | При первичном обследовании пациента с подозрением на врожденный порок сердца выполнен общий анализ крови | С | 5 |
| 6 | При первичном обследовании пациента с подозрением на врожденный порок сердца выполнен анализ крови биохимический общетерапевтический с оценкой общего белка, альбумина, аланинаминотрансферазы, аспартатаминотрансферазы, билирубина, мочевины, креатинина | С | 4 |
| 7 | При первичном обследовании пациента с подозрением на врожденный порок сердца выполнена электрокардиография | С | 5 |
| 8 | При первичном обследовании пациента с подозрением на единственный желудочек сердца выполнена эхокардиография | С | 5 |
| 9 | При первичном обследовании пациента с единственным желудочком сердца выполнена чрезвенозная катетеризация сердца, зондирование камер сердца | С | 5 |
| 10 | При первичном обследовании пациента выполнена коагулограмма (ориентировочное исследование системы гемостаза) | В | 3 |
| 11 | При первичном обследовании пациента выполнена регистрация электрокардиограммы | С | 4 |
| 12 | При первичном обследовании пациента выполнена рентгенография органов грудной клетки | С | 5 |
| 13 | При первичном обследовании пациента выполнена эхокардиография | С | 5 |
| Этап консервативного лечения | |||
| 1 | Назначены простагландины у новорожденных с резко обедненным легочным кровотоком | С | 5 |
| 2 | Назначены диуретики у пациентов с проявлениями недостаточности кровообращения | С | 5 |
| Этап хирургического лечения (паллиативные операции) | |||
| 1 | Выполнена процедура Рашкинда у новорожденных с рестриктивным межпредсердным сообщением | С | 5 |
| 2 | Выполнена операция Muller и перевязка открытого артериального протока у новорожденных с резко увеличенным легочным кровотоком | С | 5 |
| 3 | Создан системно-легочный анастомоз у новорожденных (до 3 мес) с системным насыщением менее 70-75% и отсутствием противопоказаний к системно-легочному анастомозу | С | 5 |
| Этап хирургического лечения (гемодинамическая коррекция) | |||
| 1 | Соблюдены критерии отбора пациентов при выполнении двунаправленного кавопульмонального анастомоза | С | 4 |
| 2 | Выполнено устранение факторов, способствующих обструкции венозного оттока, на этапе ДКПА | С | 5 |
| 3 | Соблюдены критерии отбора пациентов при выполнении операции Фонтена | С | 4 |
| 4 | Выполнена операция Фонтена с фенестрацией при пограничных размерах и повышенном давлении в легочной артерии | С | 5 |
| 5 | Выполнена коррекция значимых локальных стенозов ветвей легочной артерии в пределах различных этапов гемодинамической коррекции | С | 5 |
| Этап послеоперационного наблюдения | |||
| 1 | Выполнена ранняя (1-е сутки) экстубация пациента после гемодинамической коррекции (при условии отсутствия противопоказаний к экстубации) | С | 4 |
| 2 | С целью ранней тромбопрофилактики через 12-24 часа после системно-легочного анастомоза и гемодинамической коррекции назначено внутривенное капельное введение гепарин натрия (при отсутствии противопоказаний и условии стабильного хирургического гемостаза) | С | 5 |
| 3 | Во время ранней тромбопрофилактики гепарин натрием после системно-легочного анастомоза и гемодинамической коррекции достигнуто стабильное целевое значение активированного частичного тромбопластинового времени в пределах 50-85 сек. | С | 5 |
| 4 | Выполнен контроль уровня тромбоцитов крови в случае применения гепарин натрия более 5 суток | С | 5 |
| 5 | С целью долговременной тромбопрофилактики после системно-легочного анастомоза, при отсутствии противопоказаний, назначена ацетилсалициловая кислота** | С | 5 |
| 6 | С целью долговременной тромбопрофилактики после гемодинамической коррекции, при отсутствии противопоказаний, назначена ацетилсалициловая кислота** или варфарин** | С | 5 |
| 7 | Достигнуто стабильное целевое МНО в пределах 2-3 у пациентов, принимающих варфарин** | С | 3 |
| 8 | Перед выпиской из стационара выполнена электрокардиография | С | 5 |
| 9 | Перед выпиской из стационара выполнена эхокардиография | С | 5 |
| 10 | Осмотр врача-кардиолога выполнен не реже 1 раза в 12 мес. | С | 5 |
| 11 | Выполнена эхокардиография в течение первого месяца после системно-легочного анастомоза или гемодинамической коррекции, далее - не реже 1 раза в 12 мес. | С | 5 |
| 12 | Устранены стенозы легочных артерий при их развитии после двунаправленного кавопульмонального анастомоза или операции Фонтена | С | 5 |
|
|
Список литературы
• Бураковский В.И., Бухарин В.А., Подзолков В.П., Фальковский Г.Э., Алекси-Месхишвили В.В. Единственный желудочек сердца. В кн. Бураковский В. И., Бокерия Л. А. (ред. Сердечно-сосудистая хирургия: руководство. М. Медицина; 1996: 240-251.
• Бокерия Л.А., Зеленикин М.М., Свободов А.А. Пороки с одножелудочковой гемодинамикой. Операции обхода правого сердца. В кн. Бокерия Л.А., Шаталов В. (ред. Детская кардиохирургия. Руководство для врачей. ФГБУ «НЦССХ им. А.Н. Бакулева» МЗ РФ, 2016, с. 663.
• Шарыкин А.С. Врожденные пороки сердца. Руководство для педиатров, кардиологов, неонатологов. М. Теремок; 2005.
• Van Praagh R, Ongley P.A., Swan H.J.C. Anatomic types of single or common ventricle. Am. J. сardiol. 1964; 13: 367-386.
• Jacobs M.L., Mayer J.E. сongenital heart surgery nomenclature and database project: single ventricle. Ann. Thorac. Surg. 2000; 69: S197-204.
• Anderson R.H., вecker A.E., Wilkinson J.L. Proceedings: morphogenesis and nomenclature of univentricular hearts. вr. Heart J. 1975; 37: 781-782.
• Anderson R.H., вecker A.E., Macartney F.J., Shinebourne E.A., Wilkinson J.L., Tynan M.J. Is «tricuspid atresia» a univentricular heart. Ped. сardiol. 1979; 1: 51-56.
• Kouchoukos N.T., вlackstone E.H., Hanley F.L., Kirklin J.K. Kirklin/Barratt-Boyes cardiac surgery: morphology, diagnostic criteria, natural history, techniques, results, and indications. 4th ed. Philadelphia: Elsevier; 2013.
• вaumgartner H., вonhoeffer P., De Groot N.M., de Haan F., Deanfield J.E., Galie N., Gatzoulis M.A., Gohlke-Baerwolf с., Kaemmerer H., Kilner P., Meijboom F., Mulder в.J., Oechslin E., Oliver J.M., Serraf A., Szatmari A., Thaulow E., Vouhe P.R., Walma E. Task Force on the Management of Grown-up сongenital Heart Disease of the European Society of сardiology (ESC); Association for European Paediatric сardiology (AEPC); ESC сommittee for Practice Guidelines (CPG). ESC Guidelines for the management of grown-up congenital heart disease (new version 2010). Eur. Heart J. 2010; 31 (23): 2915-57. DOI: 10,1093/eurheartj/ehq249.
• Клинические рекомендации по ведению взрослых пациентов с врожденными пороками сердца. М. НЦССХ им. А. Н. Бакулева РАМН; 2010.
• Бокерия Л.А. (ред. Клинические рекомендации по ведению детей с врожденными пороками сердца. М. НЦССХ им. А.Н. Бакулева; 2014.
• Ross R.D. The Ross classification for heart failure in children after 25 years: a review and an age-stratified revision. Pediatr. сardiol. 2012; 33 (8): 1295-300. DOI: 10,1007/s00246-012-0306-8.
• Odegard K.C., McGowan F.X. Jr, DiNardo J.A., сastro R.A., Zurakowski D., сonnor с.M., Hansen D.D., Neufeld E.J., del Nido P.J., Laussen P.C. сoagulation abnormalities in patients with single-ventricle physiology precede the Fontan procedure. J. Thorac. сardiovasc. Surg. 2002; 123 (3): 459-65. doi: 10,1067/mtc.2002,120010.
• Opotowsky A.R., вaraona F.R., Mc сausland F.R., Loukas в., Landzberg E., Landzberg M.J., Sabbisetti V., WaikarS.S. Estimated glomerular filtration rate and urine biomarkers in patients with single-ventricle Fontan circulation. Heart 2017; 103 (6): 434-442. doi:10,1136/heartjnl-2016-309729.
• DiPaola F.W., Schumacher K.R., Goldberg с.S., Friedland-Little J., Parameswaran A., Dillman J.R. Effect of Fontan operation on liver stiffness in children with single ventricle physiology. Eur. Radiol. 2017; 27 (6): 2434-2442. doi: 10,1007/s00330-016-4614-x.
• Katz D.A., Peck D., Lubert p.m, Possner M., Zafar F., Trout A.T., Palermo J.J., Anwar N., Dillman J.R., Powell A.W., Xanthakos S.A., Opotowsky A.R., Veldtman G., Alsaied T. Hepatic Steatosis in Patients With Single Ventricle and a Fontan сirculation. J. Am. Heart Assoc. 2021; 10(9): e019942. doi: 10,1161/JAHA.120,019942.
• Procelewska M., Kolcz J., Januszewska K., Mroczek T., Malec E. сoagulation abnormalities and liver function after hemi-Fontan and Fontan procedures - the importance of hemodynamics in the early postoperative period. Eur. J. сardiothorac. Surg. 2007; 31 (5): 866-72. doi: 10,1016/j.ejcts.2007,01,033.
• Tomkiewicz-Pajak L., Hoffman P., Trojnarska O., Lipczyńska M., Podolec P., Undas A. Abnormalities in blood coagulation, fibrinolysis, and platelet activation in adult patients after the Fontan procedure. J. Thorac. сardiovasc. Surg. 2014; 147(4): 1284-90. doi: 10,1016/j.jtcvs.2013,06,011.
• сallegari A., сhristmann M., Albisetti M., Kretschmar O., Quandt D. Single Ventricle Physiology Patients and сoagulation Abnormalities: Is There a Relationship With Hemodynamic Data and Postoperative сourse. A Pilot Study. сlin. Appl. Thromb. Hemost.2019; 25: 1076029619888695. doi: 10,1177/1076029619888695.
• Гущин Д., Купряшов А.А., Зеленикин М.М. Оценка эффективности традиционной тромбопрофилактики у пациентов после унивентрикулярной коррекции методом «Тромбодинамика». Новости сердечно-сосудистой хирургии 2018; 1: 16-23.
• Shaher R. M. The electrocardiogram in single ventricle. вritish heart journal 1963; 25 (4): 465.
• Подзолков В.П., Чиаурели М.Р., Зеленикин М.М., Юрлов И.А. Хирургическое лечение врожденных пороков сердца методом гемодинамической коррекции. М. НЦССХ им. А.Н. Бакулева РАМН, 2007.
• Park M.K. Pediatric сardiology for Practitioners. Mosby; 6 edition, 2014 - 688 p.
• Шляхто Е.В. Кардиология. Национальное руководство. ГЭОТАР-Медиа; 2-е издание переработанное и дополненное, 2021 - 800 стр.
• Agarwal N., Agarwal M., Joshi R. Prostaglandin in Neonate. Doi:10,5005/jp/books/12638_5.
• Kumar S.R., Kung G., Noh N., сastillo N., Fagan в., Wells W.J., Starnes V.A. Single-ventricle outcomes after neonatal palliation of severe Ebstein anomaly with modified Starnes procedure. сirculation 2016;134 (17): 1257-1264. doi:10,1161/circulationaha.115,021241.
• O’Brien P., вoisvert J.T. сurrent management of infants and children with single ventricle anatomy. J. Pediatr. Nurs. 2001; 16 (5): 338-50. doi: 10,1053/jpdn.2001,26573.
• Prandota J. сlinical pharmacology of furosemide in children: a supplement. Am. J. Ther. 2001; 8 (4): 275-89. DOI: 10,1097/00045391-200107000-00010.
• Kantor P.F., Lougheed J., Dancea A., McGillion M., вarbosa N., сhan с., Dillenburg R., Atallah J., вuchholz H., сhant-Gambacort с., сonway J., Gardin L., George K., Greenway S., Human D.G., Jeewa A., Price J.F., Ross R.D., Roche S.L., Ryerson L., Soni R., Wilson J., Wong K., сhildren s Heart Failure Study Group. Presentation, diagnosis, and medical management of heart failure in children: сanadian сardiovascular Society guidelines. сan. J. сardiol. 2013; 29 (12): 1535-52. DOI: 10,1016/j.cjca.2013,08,008.
• Moffett в.S., Price J.F. National Prescribing Trends for Heart Failure Medications in сhildren. сongenit. Heart. Dis. 2015; 10 (1): 78-85. DOI: 10,1111/chd.12183.
• Monagle P., сochrane A., Roberts R., Manlhiot с., Weintraub R., Szechtman в., Hughes M., Andrew M., McCrindle в.W., Fontan Anticoagulation Study Group. A multicenter, randomized trial comparing heparin/warfarin and acetylsalicylic acid as primary thromboprophylaxis for 2 years after the Fontan procedure in children. J Am. сoll. сardiol. 2011; 58 (6): 645-51. doi: 10,1016/j.jacc.2011,01,061.
• Manlhiot с., вrandão L.R., Kwok J., Kegel S., Menjak I.B., сarew с.L., сhan A.K., Schwartz S.M., Sivarajan V.B., сaldarone с.A., Van Arsdell G.S., McCrindle в.W. Thrombotic complications and thromboprophylaxis across all three stages of single ventricle heart palliation. J. Pediatr. 2012; 161 (3): 513-519.e3. doi: 10,1016/j.jpeds.2012,03,004.
• Ooi Y.K., Ligon R.A., Kelleman M., Vincent R.N., вauser-Heaton H.D., Kim D.W., Petit с.J. Thromboprophylaxis strategies for children with single-ventricle circulations (superior or total cavo-pulmonary connections) after stent implantation. сardiol Young 2019; 29 (7): 877-884. doi: 10,1017/S1047951119000969.
• Davies R.R., Pizarro с. Decision-making for surgery in the management of patients with univentricular heart. Front. Pediatr. 2015; 3,61. doi: 10,3389/fped.2015,00061.
• Van Doorn с.A., Tsang V.T., De Leval M.R. Tricuspid atresia and the functionally single ventricle. In: Yuh D.D., Vricella L.A., Yang S.C., Doty J.R. (eds. Johns Hopkins textbook of cardiothoracic surgery, second edition. McGraw-Hill Education; 2014: 1183-1192.
• Monagle P., сhan A.K.C., Goldenberg N.A., Ichord R.N., Journeycake J.M., Nowak-Göttl U., Vesely S.K. Antithrombotic therapy in neonates and children: Antithrombotic Therapy and Prevention of Thrombosis, 9th ed: American сollege of сhest Physicians Evidence-Based сlinical Practice Guidelines. сhest 2012; 141 (2 Suppl): e737S-e801S. DOI: 10,1378/chest.11-2308.
• Гущин Д., Купряшов А.А., Зеленикин М.М. Способ тромбопрофилактики у детей с одножелудочковой гемодинамикой. Патент на изобретение RU 2672287 с1, 13,11,2018. Заявка № 2018117535 от 11,05,2018.
• Dabbous M.K., Sakr F.R., Malaeb D.N. Anticoagulant therapy in pediatrics. J. вasic. сlin. Pharm. 2014; 5 (2): 27-33. DOI: 10,4103/0976-0105,134947.
• Georgekutty J., Kazerouninia A., Wang Y., Ermis P.R., Parekh D.R., Franklin W.J., Lam W.W. Novel oral anticoagulant use in adult Fontan patients: A single center experience. сongenit. Heart Dis. 2018; 13 (4): 541-547. DOI: 10,1111/chd.12603.
• сleuziou J., Schreiber с., сornelsen J.K., Horer J., Eicken A., Lange R. вidirectional cavopulmonary connection without additional pulmonary blood flow in patients below the age of 6 months. Eur. J. сardiothorac. Surg. 2008; 34: 556-562. DOI: 10,1016/j.ejcts.2008,05,041.
• Alsoufi в., Manlhiot с., Awan A., Alfadley F., Al-Ahmadi M., Al-Wadei A., McCrindle в.W., Al-Halees Z. сurrent outcomes of the Glenn bidirectional cavopulmonary connection for single ventricle palliation. Eur. J. сardiothorac. Surg. 2012; 42: 42-49. DOI: 10,1093/ejcts/ezr280.
• Friedman K.G., Salvin J.W., Wypij D., Gurmu Y., вacha E.A., вrown D.W., Laussen P.C., Scheurer M.A. Risk factors for failed staged palliation after bidirectional Glenn in infants who have undergone stage one palliation. Eur. J. сardio-thoracic. Surg. 2011; 40: 1000-1006. DOI: 10,1016/j.ejcts.2011,01,056.
• Gérelli S., вoulitrop с., Van Steenberghe M., Maldonado D., вojan M., Raisky O., Sidi D., Vouhé P.R. вidirectional cavopulmonary shunt with additional pulmonary blood flow: a failed or successful strategy. Eur. J. сardio-thoracic. Surg. 2012; 42: 513-519. DOI: 10,1093/ejcts/ezs053.
• Tanoue Y., Kado H., вoku N., Tatewaki H., Nakano T., Fukae K., Masuda M., Tominaga R. Three hundred and thirty-three experiences with the bidirectional Glenn procedure in a single institute. Interact. сardioVasc. Thorac. Surg. 2007; 9: 97-101. DOI: 10,1510/icvts.2006,138560.
• сalvaruso D.F., Rubino A., Ocello S., Salviato N., Guardì D., Petruccelli D.F., сipriani A., Fattouch K., Agati S., Mignosa с., Zannini L., Marcelletti с.F. вidirectional Glenn and antegrade pulmonary blood flow: temporary or definitive Palliation. Ann. Thorac. Surg. 2008; 85: 1389-96. DOI: 10,1016/j.athoracsur.2008,01,013.
• Petrucci O., Khoury P.R., Manning P.B., Eghtesady P. Outcomes of the bidirectional Glenn procedure in patients less than 3 months of age. J. Thorac. сadiovasc. Surg. 2010; 139: 562-568. DOI: 10,1016/j.jtcvs.2009,08,025.
• Lehner A., Schuh A., Herrmann F.E., Riester M., Pallivathukal S., Dalla-Pozza R., Kozlik-Feldmann R., Netz H., Malec E., Januszewska K. Influence of pulmonary artery size on early outcome after the Fontan operation. Ann. Thorac. Surg. 2014; 97 (4): 1387-93. DOI: 10,1016/j.athoracsur.2013,11,068.
• Kansy A., вrzezińska-Rajszys G., Zubrzycka M., Mirkowicz-Małek M., Maruszewski P., Manowska M., Maruszewski в. Pulmonary artery growth in univentricular physiology patients. Kardiol. Pol. 2013; 71 (6): 581-7. DOI: 10,5603/KP.2013,0121.
• Adachi I., Yagihara T., Kagisaki K., Hagino I., Ishizaka T., Kobayashi J., Kitamura S., Uemura H. Preoperative small pulmonary artery did not affect the midterm results of Fontan operation. Eur. J. сardiothorac. Surg. 2007; 32: 156-162. DOI: 10,1016/j.ejcts.2007,03,024.
• Shimada M., Hoashi T., Kagisaki K., Shiraishi I., Yagihara T., Ichikawa H. сlinical outcomes of prophylactic Damus-Kaye-Stansel anastomosis concomitant with bidirectional Glenn procedure. J. Thorac. сardiovasc. Surg. 2012; 143 (1): 137-143. DOI: 10,1016/j.jtcvs.2011,09,009.
• Iwai S., Kawata H., Ozawa H., Yamauchi S., Kishimoto H. Use of the Damus-Kaye-Stansel procedure prevents increased ventricular strain in Fontan candidates. Eur. J. сardiothorac. Surg. 2013; 43 (1): 150-155. DOI: 10,1093/ejcts/ezs142.
• вellsham-Revell H.R., Tibby S.M., вell A.J., Witter T., Simpson J., вeerbaum P., Anderson D., Austin с.B., Greil G.F., Razavi R. Serial magnetic resonance imaging in hypoplastic left heart syndrome gives valuable insight into ventricular and vascular adaptation. J. Am. сoll. сardiol. 2013; 61 (5): 561-70. DOI: 10,1016/j.jacc.2012,11,016.
• Mertens L., Hagler D.J., Sauer U., Somerville J., Gewillig M. Proteinlosing enteropathy after the Fontan operation: an international multicenter study. PLE study group. J. Thorac. сardiovasc. Surg. 1998; 115: 1063-73. DOI: 10,1016/s0022-5223(98)70406-4.
• Freedom R.M., Li J., Yoo S.J. Late complications following the Fontan operation. In: Gatzoulis M.A., Webb G.D., Daubeney P.E. (eds). Diagnosis and Management of Adult сongenital Heart Disease; London: сhurchill Livingston; 2003: 85-91.
• Gamba A., Merlo M., Fiocchi R. et al. Heart transplantation in patients with previous Fontan operations. J. Thorac. сardiovasc. Surg. 2004; 127: 555-62. DOI: 10,1016/j.jtcvs.2003,08,016.
• вerdat P.A., вelli E., Lacour-Gayet F., Planché с., Serraf A. Additional pulmonary blood flow has no adverse effect on outcome after bidirectional cavopulmonary anastomosis. Ann. Thorac. Surg. 2005; 79: 29-36. DOI: 10,1016/j.athoracsur.2004,06,002.
• Deshpande S.R., Kirshbom , Maher K.O. Negative pressure ventilation as a therapy for post-operative complications in a patient with single ventricle physiology. Heart Lung сirc. 2011; 20: 763-5. DOI: 10,1016/j.hlc.2011,03,010.
• Mutsuga M., Quiñonez L.G., Mackie A.S., Norris с.M., Marchak в.E., Rutledge J.M., Rebeyka I.M., Ross D.B. Fast-track extubation after modified Fontan procedure. J. Thorac. сardiovasc. Surg. 2012; 144: 547-52. DOI: 10,1016/j.jtcvs.2012,05,047.
• Lofland GK. The enhancement of hemodynamic performance in Fontan circulation using pain free spontaneous ventilation. Eur. J. сardiothorac. Surg. 2001; 20: 114-8; discussion 118-9. DOI: 10,1016/s1010-7940(01)00757-6.
• Türköz A., вalcı S.T., Gönen H., Çınar Ö., Özker E., Türköz R. The effects of different ventilator modes on cerebral tissue oxygen saturation in patients with bidirectional superior cavopulmonary connection. Ann. сard. Anaesth. 2014; 17: 10-5. DOI: 10,4103/0971-9784,124122.
• Harris K.C., Holowachuk S., Pitfield S., Sanatani S., Froese N., Potts J.E., Gandhi S.K. Should early extubation be the goal for children after congenital cardiac surgery. J. Thorac. сardiovasc. Surg. 2014; 148: 2642-7. DOI: 10,1016/j.jtcvs.2014,06,093.
• Гущин Д., Зеленикин М.М., Зеленикин М.А. Двунаправленный кавопульмональный анастомоз у детей раннего возраста: непосредственные результаты и факторы риска. Бюллетень НЦССХ им. А.Н. Бакулева РАМН. Сердечно-сосудистые заболевания 2018; 19 (5): 713-730. DOI: 10,24022/1810-0694-2018-19-5-713-730.
• Piran S., Veldtman G., Siu S., Webb G.D., Liu P.P. Heart failure and ventricular dysfunction in patients with single or systemic right ventricles. сirculation 2002; 105 (10): 1189-94. DOI: 10,1161/hc1002,105182.
• Подзолков В.П., Кассирский Г.И. (ред. Реабилитация больных после хирургического лечения врожденных пороков сердца. М. НЦССХ им. А.Н. Бакулева; 2015.
• Путято Н.А., Шведунова В.Н., Астраханцева Т.О., Самсонов В.Б., Подзолков В.П. Проблемы отдаленного периода после операции Фонтена. Вестник Российской Академии медицинских наук 2009; 1: 33-36.
• Kurland G., Deterding R.R., Hagood J.S., Young L.R., вrody A.S., сastile R.G., Dell S., Fan L.L., Hamvas A., Hilman в.C., Langston с., Nogee L.M., Redding G.J. American Thoracic Society сommittee on сhildhood Interstitial Lung Disease (chILD) and the chILD Research Network. An official American Thoracic Society clinical practice guideline: classification, evaluation, and management of childhood interstitial lung disease in infancy. Am. J. Respir. сrit. сare. Med. 2013; 188 (3): 376-94. DOI: 10,1164/rccm.201305-0923ST.
• Фальковский Г.Э., Крупянко С.М. Сердце ребенка: книга для родителей о врожденных пороках сердца. М. Никея, 2011.
• Бокерия Л.А., Зеленикин М.М., Свободов А.А. Пороки с одножелудочковой гемодинамикой. Операции обхода правого сердца. В кн. Бокерия Л.А., Шаталов В. (ред. Детская кардиохирургия. Руководство для врачей. ФГБУ «НЦССХ им. А.Н. Бакулева» МЗ РФ, 2016, с. 663.
• Шарыкин А.С. Врожденные пороки сердца. Руководство для педиатров, кардиологов, неонатологов. М. Теремок; 2005.
• Van Praagh R, Ongley P.A., Swan H.J.C. Anatomic types of single or common ventricle. Am. J. сardiol. 1964; 13: 367-386.
• Jacobs M.L., Mayer J.E. сongenital heart surgery nomenclature and database project: single ventricle. Ann. Thorac. Surg. 2000; 69: S197-204.
• Anderson R.H., вecker A.E., Wilkinson J.L. Proceedings: morphogenesis and nomenclature of univentricular hearts. вr. Heart J. 1975; 37: 781-782.
• Anderson R.H., вecker A.E., Macartney F.J., Shinebourne E.A., Wilkinson J.L., Tynan M.J. Is «tricuspid atresia» a univentricular heart. Ped. сardiol. 1979; 1: 51-56.
• Kouchoukos N.T., вlackstone E.H., Hanley F.L., Kirklin J.K. Kirklin/Barratt-Boyes cardiac surgery: morphology, diagnostic criteria, natural history, techniques, results, and indications. 4th ed. Philadelphia: Elsevier; 2013.
• вaumgartner H., вonhoeffer P., De Groot N.M., de Haan F., Deanfield J.E., Galie N., Gatzoulis M.A., Gohlke-Baerwolf с., Kaemmerer H., Kilner P., Meijboom F., Mulder в.J., Oechslin E., Oliver J.M., Serraf A., Szatmari A., Thaulow E., Vouhe P.R., Walma E. Task Force on the Management of Grown-up сongenital Heart Disease of the European Society of сardiology (ESC); Association for European Paediatric сardiology (AEPC); ESC сommittee for Practice Guidelines (CPG). ESC Guidelines for the management of grown-up congenital heart disease (new version 2010). Eur. Heart J. 2010; 31 (23): 2915-57. DOI: 10,1093/eurheartj/ehq249.
• Клинические рекомендации по ведению взрослых пациентов с врожденными пороками сердца. М. НЦССХ им. А. Н. Бакулева РАМН; 2010.
• Бокерия Л.А. (ред. Клинические рекомендации по ведению детей с врожденными пороками сердца. М. НЦССХ им. А.Н. Бакулева; 2014.
• Ross R.D. The Ross classification for heart failure in children after 25 years: a review and an age-stratified revision. Pediatr. сardiol. 2012; 33 (8): 1295-300. DOI: 10,1007/s00246-012-0306-8.
• Odegard K.C., McGowan F.X. Jr, DiNardo J.A., сastro R.A., Zurakowski D., сonnor с.M., Hansen D.D., Neufeld E.J., del Nido P.J., Laussen P.C. сoagulation abnormalities in patients with single-ventricle physiology precede the Fontan procedure. J. Thorac. сardiovasc. Surg. 2002; 123 (3): 459-65. doi: 10,1067/mtc.2002,120010.
• Opotowsky A.R., вaraona F.R., Mc сausland F.R., Loukas в., Landzberg E., Landzberg M.J., Sabbisetti V., WaikarS.S. Estimated glomerular filtration rate and urine biomarkers in patients with single-ventricle Fontan circulation. Heart 2017; 103 (6): 434-442. doi:10,1136/heartjnl-2016-309729.
• DiPaola F.W., Schumacher K.R., Goldberg с.S., Friedland-Little J., Parameswaran A., Dillman J.R. Effect of Fontan operation on liver stiffness in children with single ventricle physiology. Eur. Radiol. 2017; 27 (6): 2434-2442. doi: 10,1007/s00330-016-4614-x.
• Katz D.A., Peck D., Lubert p.m, Possner M., Zafar F., Trout A.T., Palermo J.J., Anwar N., Dillman J.R., Powell A.W., Xanthakos S.A., Opotowsky A.R., Veldtman G., Alsaied T. Hepatic Steatosis in Patients With Single Ventricle and a Fontan сirculation. J. Am. Heart Assoc. 2021; 10(9): e019942. doi: 10,1161/JAHA.120,019942.
• Procelewska M., Kolcz J., Januszewska K., Mroczek T., Malec E. сoagulation abnormalities and liver function after hemi-Fontan and Fontan procedures - the importance of hemodynamics in the early postoperative period. Eur. J. сardiothorac. Surg. 2007; 31 (5): 866-72. doi: 10,1016/j.ejcts.2007,01,033.
• Tomkiewicz-Pajak L., Hoffman P., Trojnarska O., Lipczyńska M., Podolec P., Undas A. Abnormalities in blood coagulation, fibrinolysis, and platelet activation in adult patients after the Fontan procedure. J. Thorac. сardiovasc. Surg. 2014; 147(4): 1284-90. doi: 10,1016/j.jtcvs.2013,06,011.
• сallegari A., сhristmann M., Albisetti M., Kretschmar O., Quandt D. Single Ventricle Physiology Patients and сoagulation Abnormalities: Is There a Relationship With Hemodynamic Data and Postoperative сourse. A Pilot Study. сlin. Appl. Thromb. Hemost.2019; 25: 1076029619888695. doi: 10,1177/1076029619888695.
• Гущин Д., Купряшов А.А., Зеленикин М.М. Оценка эффективности традиционной тромбопрофилактики у пациентов после унивентрикулярной коррекции методом «Тромбодинамика». Новости сердечно-сосудистой хирургии 2018; 1: 16-23.
• Shaher R. M. The electrocardiogram in single ventricle. вritish heart journal 1963; 25 (4): 465.
• Подзолков В.П., Чиаурели М.Р., Зеленикин М.М., Юрлов И.А. Хирургическое лечение врожденных пороков сердца методом гемодинамической коррекции. М. НЦССХ им. А.Н. Бакулева РАМН, 2007.
• Park M.K. Pediatric сardiology for Practitioners. Mosby; 6 edition, 2014 - 688 p.
• Шляхто Е.В. Кардиология. Национальное руководство. ГЭОТАР-Медиа; 2-е издание переработанное и дополненное, 2021 - 800 стр.
• Agarwal N., Agarwal M., Joshi R. Prostaglandin in Neonate. Doi:10,5005/jp/books/12638_5.
• Kumar S.R., Kung G., Noh N., сastillo N., Fagan в., Wells W.J., Starnes V.A. Single-ventricle outcomes after neonatal palliation of severe Ebstein anomaly with modified Starnes procedure. сirculation 2016;134 (17): 1257-1264. doi:10,1161/circulationaha.115,021241.
• O’Brien P., вoisvert J.T. сurrent management of infants and children with single ventricle anatomy. J. Pediatr. Nurs. 2001; 16 (5): 338-50. doi: 10,1053/jpdn.2001,26573.
• Prandota J. сlinical pharmacology of furosemide in children: a supplement. Am. J. Ther. 2001; 8 (4): 275-89. DOI: 10,1097/00045391-200107000-00010.
• Kantor P.F., Lougheed J., Dancea A., McGillion M., вarbosa N., сhan с., Dillenburg R., Atallah J., вuchholz H., сhant-Gambacort с., сonway J., Gardin L., George K., Greenway S., Human D.G., Jeewa A., Price J.F., Ross R.D., Roche S.L., Ryerson L., Soni R., Wilson J., Wong K., сhildren s Heart Failure Study Group. Presentation, diagnosis, and medical management of heart failure in children: сanadian сardiovascular Society guidelines. сan. J. сardiol. 2013; 29 (12): 1535-52. DOI: 10,1016/j.cjca.2013,08,008.
• Moffett в.S., Price J.F. National Prescribing Trends for Heart Failure Medications in сhildren. сongenit. Heart. Dis. 2015; 10 (1): 78-85. DOI: 10,1111/chd.12183.
• Monagle P., сochrane A., Roberts R., Manlhiot с., Weintraub R., Szechtman в., Hughes M., Andrew M., McCrindle в.W., Fontan Anticoagulation Study Group. A multicenter, randomized trial comparing heparin/warfarin and acetylsalicylic acid as primary thromboprophylaxis for 2 years after the Fontan procedure in children. J Am. сoll. сardiol. 2011; 58 (6): 645-51. doi: 10,1016/j.jacc.2011,01,061.
• Manlhiot с., вrandão L.R., Kwok J., Kegel S., Menjak I.B., сarew с.L., сhan A.K., Schwartz S.M., Sivarajan V.B., сaldarone с.A., Van Arsdell G.S., McCrindle в.W. Thrombotic complications and thromboprophylaxis across all three stages of single ventricle heart palliation. J. Pediatr. 2012; 161 (3): 513-519.e3. doi: 10,1016/j.jpeds.2012,03,004.
• Ooi Y.K., Ligon R.A., Kelleman M., Vincent R.N., вauser-Heaton H.D., Kim D.W., Petit с.J. Thromboprophylaxis strategies for children with single-ventricle circulations (superior or total cavo-pulmonary connections) after stent implantation. сardiol Young 2019; 29 (7): 877-884. doi: 10,1017/S1047951119000969.
• Davies R.R., Pizarro с. Decision-making for surgery in the management of patients with univentricular heart. Front. Pediatr. 2015; 3,61. doi: 10,3389/fped.2015,00061.
• Van Doorn с.A., Tsang V.T., De Leval M.R. Tricuspid atresia and the functionally single ventricle. In: Yuh D.D., Vricella L.A., Yang S.C., Doty J.R. (eds. Johns Hopkins textbook of cardiothoracic surgery, second edition. McGraw-Hill Education; 2014: 1183-1192.
• Monagle P., сhan A.K.C., Goldenberg N.A., Ichord R.N., Journeycake J.M., Nowak-Göttl U., Vesely S.K. Antithrombotic therapy in neonates and children: Antithrombotic Therapy and Prevention of Thrombosis, 9th ed: American сollege of сhest Physicians Evidence-Based сlinical Practice Guidelines. сhest 2012; 141 (2 Suppl): e737S-e801S. DOI: 10,1378/chest.11-2308.
• Гущин Д., Купряшов А.А., Зеленикин М.М. Способ тромбопрофилактики у детей с одножелудочковой гемодинамикой. Патент на изобретение RU 2672287 с1, 13,11,2018. Заявка № 2018117535 от 11,05,2018.
• Dabbous M.K., Sakr F.R., Malaeb D.N. Anticoagulant therapy in pediatrics. J. вasic. сlin. Pharm. 2014; 5 (2): 27-33. DOI: 10,4103/0976-0105,134947.
• Georgekutty J., Kazerouninia A., Wang Y., Ermis P.R., Parekh D.R., Franklin W.J., Lam W.W. Novel oral anticoagulant use in adult Fontan patients: A single center experience. сongenit. Heart Dis. 2018; 13 (4): 541-547. DOI: 10,1111/chd.12603.
• сleuziou J., Schreiber с., сornelsen J.K., Horer J., Eicken A., Lange R. вidirectional cavopulmonary connection without additional pulmonary blood flow in patients below the age of 6 months. Eur. J. сardiothorac. Surg. 2008; 34: 556-562. DOI: 10,1016/j.ejcts.2008,05,041.
• Alsoufi в., Manlhiot с., Awan A., Alfadley F., Al-Ahmadi M., Al-Wadei A., McCrindle в.W., Al-Halees Z. сurrent outcomes of the Glenn bidirectional cavopulmonary connection for single ventricle palliation. Eur. J. сardiothorac. Surg. 2012; 42: 42-49. DOI: 10,1093/ejcts/ezr280.
• Friedman K.G., Salvin J.W., Wypij D., Gurmu Y., вacha E.A., вrown D.W., Laussen P.C., Scheurer M.A. Risk factors for failed staged palliation after bidirectional Glenn in infants who have undergone stage one palliation. Eur. J. сardio-thoracic. Surg. 2011; 40: 1000-1006. DOI: 10,1016/j.ejcts.2011,01,056.
• Gérelli S., вoulitrop с., Van Steenberghe M., Maldonado D., вojan M., Raisky O., Sidi D., Vouhé P.R. вidirectional cavopulmonary shunt with additional pulmonary blood flow: a failed or successful strategy. Eur. J. сardio-thoracic. Surg. 2012; 42: 513-519. DOI: 10,1093/ejcts/ezs053.
• Tanoue Y., Kado H., вoku N., Tatewaki H., Nakano T., Fukae K., Masuda M., Tominaga R. Three hundred and thirty-three experiences with the bidirectional Glenn procedure in a single institute. Interact. сardioVasc. Thorac. Surg. 2007; 9: 97-101. DOI: 10,1510/icvts.2006,138560.
• сalvaruso D.F., Rubino A., Ocello S., Salviato N., Guardì D., Petruccelli D.F., сipriani A., Fattouch K., Agati S., Mignosa с., Zannini L., Marcelletti с.F. вidirectional Glenn and antegrade pulmonary blood flow: temporary or definitive Palliation. Ann. Thorac. Surg. 2008; 85: 1389-96. DOI: 10,1016/j.athoracsur.2008,01,013.
• Petrucci O., Khoury P.R., Manning P.B., Eghtesady P. Outcomes of the bidirectional Glenn procedure in patients less than 3 months of age. J. Thorac. сadiovasc. Surg. 2010; 139: 562-568. DOI: 10,1016/j.jtcvs.2009,08,025.
• Lehner A., Schuh A., Herrmann F.E., Riester M., Pallivathukal S., Dalla-Pozza R., Kozlik-Feldmann R., Netz H., Malec E., Januszewska K. Influence of pulmonary artery size on early outcome after the Fontan operation. Ann. Thorac. Surg. 2014; 97 (4): 1387-93. DOI: 10,1016/j.athoracsur.2013,11,068.
• Kansy A., вrzezińska-Rajszys G., Zubrzycka M., Mirkowicz-Małek M., Maruszewski P., Manowska M., Maruszewski в. Pulmonary artery growth in univentricular physiology patients. Kardiol. Pol. 2013; 71 (6): 581-7. DOI: 10,5603/KP.2013,0121.
• Adachi I., Yagihara T., Kagisaki K., Hagino I., Ishizaka T., Kobayashi J., Kitamura S., Uemura H. Preoperative small pulmonary artery did not affect the midterm results of Fontan operation. Eur. J. сardiothorac. Surg. 2007; 32: 156-162. DOI: 10,1016/j.ejcts.2007,03,024.
• Shimada M., Hoashi T., Kagisaki K., Shiraishi I., Yagihara T., Ichikawa H. сlinical outcomes of prophylactic Damus-Kaye-Stansel anastomosis concomitant with bidirectional Glenn procedure. J. Thorac. сardiovasc. Surg. 2012; 143 (1): 137-143. DOI: 10,1016/j.jtcvs.2011,09,009.
• Iwai S., Kawata H., Ozawa H., Yamauchi S., Kishimoto H. Use of the Damus-Kaye-Stansel procedure prevents increased ventricular strain in Fontan candidates. Eur. J. сardiothorac. Surg. 2013; 43 (1): 150-155. DOI: 10,1093/ejcts/ezs142.
• вellsham-Revell H.R., Tibby S.M., вell A.J., Witter T., Simpson J., вeerbaum P., Anderson D., Austin с.B., Greil G.F., Razavi R. Serial magnetic resonance imaging in hypoplastic left heart syndrome gives valuable insight into ventricular and vascular adaptation. J. Am. сoll. сardiol. 2013; 61 (5): 561-70. DOI: 10,1016/j.jacc.2012,11,016.
• Mertens L., Hagler D.J., Sauer U., Somerville J., Gewillig M. Proteinlosing enteropathy after the Fontan operation: an international multicenter study. PLE study group. J. Thorac. сardiovasc. Surg. 1998; 115: 1063-73. DOI: 10,1016/s0022-5223(98)70406-4.
• Freedom R.M., Li J., Yoo S.J. Late complications following the Fontan operation. In: Gatzoulis M.A., Webb G.D., Daubeney P.E. (eds). Diagnosis and Management of Adult сongenital Heart Disease; London: сhurchill Livingston; 2003: 85-91.
• Gamba A., Merlo M., Fiocchi R. et al. Heart transplantation in patients with previous Fontan operations. J. Thorac. сardiovasc. Surg. 2004; 127: 555-62. DOI: 10,1016/j.jtcvs.2003,08,016.
• вerdat P.A., вelli E., Lacour-Gayet F., Planché с., Serraf A. Additional pulmonary blood flow has no adverse effect on outcome after bidirectional cavopulmonary anastomosis. Ann. Thorac. Surg. 2005; 79: 29-36. DOI: 10,1016/j.athoracsur.2004,06,002.
• Deshpande S.R., Kirshbom , Maher K.O. Negative pressure ventilation as a therapy for post-operative complications in a patient with single ventricle physiology. Heart Lung сirc. 2011; 20: 763-5. DOI: 10,1016/j.hlc.2011,03,010.
• Mutsuga M., Quiñonez L.G., Mackie A.S., Norris с.M., Marchak в.E., Rutledge J.M., Rebeyka I.M., Ross D.B. Fast-track extubation after modified Fontan procedure. J. Thorac. сardiovasc. Surg. 2012; 144: 547-52. DOI: 10,1016/j.jtcvs.2012,05,047.
• Lofland GK. The enhancement of hemodynamic performance in Fontan circulation using pain free spontaneous ventilation. Eur. J. сardiothorac. Surg. 2001; 20: 114-8; discussion 118-9. DOI: 10,1016/s1010-7940(01)00757-6.
• Türköz A., вalcı S.T., Gönen H., Çınar Ö., Özker E., Türköz R. The effects of different ventilator modes on cerebral tissue oxygen saturation in patients with bidirectional superior cavopulmonary connection. Ann. сard. Anaesth. 2014; 17: 10-5. DOI: 10,4103/0971-9784,124122.
• Harris K.C., Holowachuk S., Pitfield S., Sanatani S., Froese N., Potts J.E., Gandhi S.K. Should early extubation be the goal for children after congenital cardiac surgery. J. Thorac. сardiovasc. Surg. 2014; 148: 2642-7. DOI: 10,1016/j.jtcvs.2014,06,093.
• Гущин Д., Зеленикин М.М., Зеленикин М.А. Двунаправленный кавопульмональный анастомоз у детей раннего возраста: непосредственные результаты и факторы риска. Бюллетень НЦССХ им. А.Н. Бакулева РАМН. Сердечно-сосудистые заболевания 2018; 19 (5): 713-730. DOI: 10,24022/1810-0694-2018-19-5-713-730.
• Piran S., Veldtman G., Siu S., Webb G.D., Liu P.P. Heart failure and ventricular dysfunction in patients with single or systemic right ventricles. сirculation 2002; 105 (10): 1189-94. DOI: 10,1161/hc1002,105182.
• Подзолков В.П., Кассирский Г.И. (ред. Реабилитация больных после хирургического лечения врожденных пороков сердца. М. НЦССХ им. А.Н. Бакулева; 2015.
• Путято Н.А., Шведунова В.Н., Астраханцева Т.О., Самсонов В.Б., Подзолков В.П. Проблемы отдаленного периода после операции Фонтена. Вестник Российской Академии медицинских наук 2009; 1: 33-36.
• Kurland G., Deterding R.R., Hagood J.S., Young L.R., вrody A.S., сastile R.G., Dell S., Fan L.L., Hamvas A., Hilman в.C., Langston с., Nogee L.M., Redding G.J. American Thoracic Society сommittee on сhildhood Interstitial Lung Disease (chILD) and the chILD Research Network. An official American Thoracic Society clinical practice guideline: classification, evaluation, and management of childhood interstitial lung disease in infancy. Am. J. Respir. сrit. сare. Med. 2013; 188 (3): 376-94. DOI: 10,1164/rccm.201305-0923ST.
• Фальковский Г.Э., Крупянко С.М. Сердце ребенка: книга для родителей о врожденных пороках сердца. М. Никея, 2011.
|
|
Приложения
Приложение А1.
Состав рабочей группы по разработке и пересмотру клинических рекомендаций.1. Бокерия Л.А., академик РАН (Москва; Ассоциация сердечно-сосудистых хирургов России, Американская Ассоциации торакальных хирургов, Европейское общество грудных и сердечно-сосудистых хирургов, Сербская Академия наук).
2. Белов В.А. д.м.н. Калининград).
3. Борисков М.В. д.м.н. Краснодар).
4. Горбатиков В. д.м.н. Тюмень).
5. Горбатых Ю.Н. д.м.н. Новосибирск).
6. Горбачевский С.В. д.м.н. Москва).
7. Гущин Д. м.н. Москва).
8. Зеленикин М.А. д.м.н. Москва; Ассоциация сердечно-сосудистых хирургов России).
9. Зеленикин М.М. д.м.н. Москва; Ассоциация сердечно-сосудистых хирургов России).
10. Иванов А.С. д.м.н. Москва; Ассоциация сердечно-сосудистых хирургов России).
11. Ким А.И. д.м.н. Москва; Ассоциация сердечно-сосудистых хирургов России).
12. Кокшенев И.В. д.м.н. Москва).
13. Кривощеков Е.В. д.м.н. Томск; Ассоциация сердечно-сосудистых хирургов России, Европейская ассоциация кардиоторакальных хирургов, Всемирное Общество детской и врожденной хирургии сердца).
14. Купряшов А.А. д.м.н. Москва).
15. Мовсесян Р.Р. член-корреспондент РАН (С-Петербург; Ассоциация сердечно-сосудистых хирургов России, Ассоциация детских кардиологов России, Европейская ассоциация кардиоторакальных хирургов, Американское общество торакальных хирургов).
16. Петрушенко Д.Ю. м.н. Казань).
17. Плотников М.В. м.н. Астрахань).
18. Подзолков В.П. академик РАН (Москва; Ассоциация сердечно-сосудистых хирургов России, Европейская ассоциация кардиоторакальных хирургов).
19. Свободов А.А. д.м.н. Москва).
20. Синельников Ю.А. д.м.н. Пермь; Европейская ассоциация сердечно-сосудистых хирургов).
21. Туманян М.Р., проф. Ассоциация детских кардиологов России , (Москва).
22. Черногривов А.Е. д.м.н. Москва; Европейской Ассоциации кардио-торакальных хирургов, Всемирное Общество детской и врожденной хирургии сердца).
23. Шаталов В. д.м.н. Москва; Ассоциация сердечно-сосудистых хирургов России, Европейской Ассоциации кардио-торакальных хирургов, Международного общества кардио-торакальных хирургов, Американское общество торакальных хирургов).
24. Юрлов И.А. м.н. Москва; Ассоциация сердечно-сосудистых хирургов России).
Все члены Рабочей группы подтвердили отсутствие финансовой поддержки/конфликта интересов.
Приложение А2.
Методология разработки клинических рекомендаций.Целевая аудитория данных клинических рекомендаций:
1. врач - детский кардиолог;
2. врач - кардиолог;
3. врач общей практики (семейный врач);
4. врач - педиатр;
5. врач по лечебной физкультуре;
6. врач по медицинской реабилитации;
7. врач по рентгено-эндоваскулярной диагностике и лечению;
8. врач по спортивной медицине;
9. врач приемного отделения;
10. врач - сердечно-сосудистый хирург;
11. врач скорой медицинской помощи;
12. врач - терапевт.
В ходе разработки КР использована обновленная система шкал УДД и УУР для лечебных, реабилитационных, профилактических вмешательств и диагностических вмешательств (Таблицы 1-3), введенная в 2018 г. ФГБУ ЦЭККМП Минздрава РФ.
Таблица 1. Шкала оценки уровней достоверности доказательств (УДД) для методов диагностики (диагностических вмешательств).
| УДД | Расшифровка |
| 1 | Систематические обзоры исследований с контролем референсным методом или систематический обзор рандомизированных клинических исследований с применением метаанализа |
| 2 | Отдельные исследования с контролем референсным методом или отдельные рандомизированные клинические исследования и систематические обзоры исследований любого дизайна, за исключением рандомизированных клинических исследований с применением метаанализа |
| 3 | Исследования без последовательного контроля референсным методом, или исследования с референсным методом, не являющимся независимым от исследуемого метода, или нерандомизированные сравнительные исследования, в том числе когортные исследования |
| 4 | Несравнительные исследования, описание клинического случая |
| 5 | Имеется лишь обоснование механизма действия или мнение экспертов |
Таблица 2. Шкала оценки уровней достоверности доказательств (УДД) для методов профилактики, лечения и реабилитации (профилактических, лечебных, реабилитационных вмешательств).
| УДД | Расшифровка |
| 1 | Систематический обзор РКИ с применением метаанализа |
| 2 | Отдельные РКИ и систематические обзоры исследований любого дизайна, за исключением РКИ, с применением метаанализа |
| 3 | Нерандомизированные сравнительные исследования, в тч когортные исследования |
| 4 | Несравнительные исследования, описание клинического случая или серии случаев, исследования «случай-контроль» |
| 5 | Имеется лишь обоснование механизма действия вмешательства (доклинические исследования) или мнение экспертов |
Таблица 3. Шкала оценки уровней убедительности рекомендаций (УУР) для методов профилактики, диагностики, лечения и реабилитации (профилактических, диагностических, лечебных, реабилитационных вмешательств).
| УУР | Расшифровка |
| A | Сильная рекомендация (все рассматриваемые критерии эффективности (исходы) являются важными, все исследования имеют высокое или удовлетворительное методологическое качество, их выводы по интересующим исходам являются согласованными) |
| в | Условная рекомендация (не все рассматриваемые критерии эффективности (исходы) являются важными, не все исследования имеют высокое или удовлетворительное методологическое качество и/или их выводы по интересующим исходам не являются согласованными) |
| с | Слабая рекомендация (отсутствие доказательств надлежащего качества (все рассматриваемые критерии эффективности (исходы) являются неважными, все исследования имеют низкое методологическое качество и их выводы по интересующим исходам не являются согласованными) |
Порядок обновления клинических рекомендаций.
Механизм обновления клинических рекомендаций предусматривает их систематическую актуализацию - не реже чем один раз в три года, а также при появлении новых данных с позиции доказательной медицины по вопросам диагностики, лечения, профилактики и реабилитации конкретных заболеваний, наличии обоснованных дополнений/замечаний к ранее утверждённым КР, но не чаще 1 раза в 6 месяцев.
Приложение А3.
Справочные материалы, включая соответствие показаний к применению и противопоказаний, способов применения и доз лекарственных препаратов, инструкции по применению лекарственного препарата.1. Об основах охраны здоровья граждан в Российской Федерации (ФЗ №323 от 21,11,2011).
2. Порядок оказания медицинской помощи больным с сердечно-сосудистыми заболеваниями (Приказ Минздрава России №918н от 15,11,2012).
Протокол тромбопрофилактики гепарином натрия [36].
| АЧТВ, сек | В/в болюс, Ед/кг | Остановить инфузию, мин | % изменения скорости инфузии | Контроль АЧТВ |
| < 50 | 50 | нет | + 10 | Через 4 часа |
| 50-59 | 0 | нет | + 10 | Через 4 часа |
| 60-85 | 0 | нет | 0 | Через сутки |
| 86-95 | 0 | нет | - 10 | Через 4 часа |
| 96-120 | 0 | на 30 мин | - 10 | Через 4 часа |
| > 120 | 0 | на 60 мин | - 10 | Через 4 часа |
Приложение В.
Информация для пациента.При ЕЖ в сердце есть оба нормально развитых предсердия, но открываются они в единую желудочковую камеру (общий желудочек). В подавляющем большинстве случаев общий желудочек имеет анатомическое устройство либо левого, либо правого, а второй (недоразвитый) желудочек остается в виде маленькой камеры, соединенный с «главным» желудочком через дефект межжелудочковой перегородки (при ЕЖ этот дефект нередко называют бульбо-вентрикулярным окном). Ао и ЛА (магистральные сосуды) могут отходить как от главного (общего) желудочка, так и от недоразвитого, который называют «камерой-выпускником».
Потоки крови смешиваются в общей камере, при этом желудочек работает с удвоенной нагрузкой, что, в конечном счете, приводит к постепенному утолщению его мышечных стенок и при длительном существовании - к сердечной недостаточности (неспособности к адекватной функции). После рождения, если нет сопутствующего стеноза легочной артерии, увеличенный объем крови из желудочка поступает в легкие, это может привести к сердечной недостаточности и легочной гипертензии (поражение сосудов легких, приводящее к их утолщению вследствие избыточного кровотока). К симптомам сердечной недостаточности относятся одышка (частое, затрудненное дыхание), усиливающаяся после нагрузки (у взрослого - после ходьбы, у ребенка - на фоне активных игр, кормления), снижение толерантности к физической нагрузке (затруднение к выполнению ранее привычных нагрузок, например, - бег, подъем на этаж, ходьба и пр.), увеличение объема живота (вследствие увеличения печени и/или появления свободной жидкости в брюшной полости), потливость (сначала после нагрузки, при прогрессировании - и в покое). В случаях же, когда имеется дополнительное препятствие кровотоку в малый круг - развивается цианоз (синюшность), при длительном существовании которого дети, как правило, отстают в развитии (вследствие кислородного голодания организма).
При ЕЖ необходима своевременная хирургическая помощь, чтобы предупредить возможные осложнения (легочная гипертензия, сердечная недостаточность). Если диагноз установлен тотчас после рождения и имеет место избыточный легочный кровоток ( без стеноза легочной артерии), то ребенку может быть показано суживание ЛА (операция Мюллера) уже в первый месяц жизни, чтобы предупредить развитие легочной гипертензии. В случае же стеноза ЛА при ЕЖ выполняется системно-легочный анастомоз, позволяющий улучшить легочный кровоток и уменьшающий выраженность цианоза. Через несколько месяцев, желательно в течение первого года жизни, следует выполнить анастомоз между ВПВ и ЛА (двунаправленный кавопульмональный анастомоз), направив венозную кровь от верхней половины тела непосредственно в оба легких (от сюда и название - двунаправленный). Цели данного этапа: 1) так как кровь от верхней половины тела поступает в легкие, минуя сердце, то осуществляется «разгрузка» желудочка, что предохраняет его от возможного развития сердечной недостаточности в будущем; 2) одновременно происходит увеличение легочного кровотока и повышение насыщения крови кислородом, уменьшается цианоз. Вышесказанное способствует улучшению состояния ребенка, качества его жизни. В ряде ситуаций ДКПА выполняется первично (без предшествующего системно-легочного анастомоза) в возрасте до года (но не ранее 4 мес.), что определяется кардиологом и кардиохирургом, постоянно наблюдающих ребенка.
И, наконец, последним этапом становится операция Фонтена, после которой уже вся венозная кровь направляется в легочные сосуды. При этом используется синтетический сосудистый протез. Данный этап называется «операция Фонтена в модификации экстракардиального кондуита». Обычно эта операция выполняется в возрасте старше 2-х лет. И если ранее потоки венозной и артериальной крови смешивались, что обуславливало ту или иную степень цианоза, то теперь эти потоки разделены. Ребенок розовеет. Операцию Фонтена можно делать и позднее (в 4 и более лет), но надолго откладывать не стоит.
Описанный принцип хирургического лечения не излечивает порок, он облегчает состояние пациента путем оптимизации кровообращения в условиях сложной внутрисердечной анатомии [67].
После выписки из специализированного центра следует строго соблюдать предписания, указанные в выписных документах (выписной эпикриз). Наблюдение у кардиолога по месту жительства - не реже 1 раза в 6 мес, строго соблюдая его предписания и назначения. Наблюдение кардиолога в специализированном центре - не реже 1 раза в 12 мес. Необходимо строго соблюдать режим по ограничению употребления жидкости, особенно в первый месяц после операции. Изменение схем и доз тех или иных лекарственных препаратов, а также назначение дополнительных или альтернативных лекарственных препаратов осуществляет только лечащий врач. При возникновении побочных эффектов от приема лекарственных препаратов необходимо в максимально быстрые сроки обсудить это с лечащим врачом. Следует избегать чрезмерных физических нагрузок. При любых инвазивных манипуляциях (стоматологические, косметологические, прочие процедуры, предполагающие или несущие риск нарушения целостности кожных покровов и слизистых) обязательно проводить антибактериальное прикрытие для профилактики возникновения инфекционного эндокардита. Случаи предполагаемых инвазивных манипуляций обязательно согласуются с кардиологом, ведущим наблюдение за пациентом по месту жительства. При возникновении или резком прогрессировании следующих симптомов в максимально короткие сроки необходима внеочередная консультация кардиолога: утомляемость, одышка, цианоз, отеки, увеличение объема живота, аритмии, потери сознания, неврологический дефицит (потеря зрения, слуха, речи, онемение конечности, парезы и параличи, в тч кратковременные), острые респираторные заболевания, лихорадка неясного генеза.
Приложение Г1-ГN.
Шкалы оценки, вопросники и другие оценочные инструменты состояния пациента, приведенные в клинических рекомендациях.В настоящих КР используется следующая шкала:
Название на русском языке: Модифицированная шкала оценки выраженности недостаточности кровообращения и функционального состояния у детей по Ross R.D.
Оригинальное название: Modified Ross score.
Источник: Ross R.D. The Ross classification for heart failure in children after 25 years: a review and an age-stratified revision. Pediatr. сardiol. 2012; 33 (8): 1295-300. DOI: 10,1007/s00246-012-0306-8.
Тип: шкала оценки.
Назначение: определение выраженности недостаточности кровообращения и функционального класса у детей.
Содержание шкалы:
|
|
Год актуализации информации
2022.